一种顺式构型的2,2-二氟-4-苯基丁-3-烯酸乙酯类化合物及其制备方法
1.本发明涉及一种顺式烯烃类化合物及其合成方法,应用于有机合成、药物化学技术领域。
背景技术:
2.作为常见的结构,顺式烯烃因其相较于反式烯烃的热力学不稳定性而在合成上具有挑战性。在有机氟化学领域,向有机分子中引入偕二氟亚甲基也已成为近期研究的热点,而到目前为止,获取这些特定骨架的方法还局限于在一定条件下,过渡金属参与发生的氢化反应和交叉偶联反应。本质上,所有这些策略都依赖于动力学控制和使用特定的催化剂。另一方面,各种利用光催化的氧化还原反应在过去的20年里已经成为一种绿色、高效的方法,在碳碳键偶联中做出了许多贡献。而本专利旨在利用更加绿色、高效的光催化完成此反应
3.以brcf2co2et为氟源,在室温下1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯(hantzsch ester)与蓝光led(465nm)共同作用,将末端芳基炔烃还原为顺式烯烃的偕二氟亚甲基化反应。这一过程提供了一种高效的合成方法,合成了顺式构型的2,2-二氟-4-苯基丁-3-烯酸乙酯,并有着良好的产率和z/e比。
[0004][0005]
近年来,已有不少光催化在偕二氟亚甲基化中的应用方法,相关的合成方法主要有以下几种:
[0006]
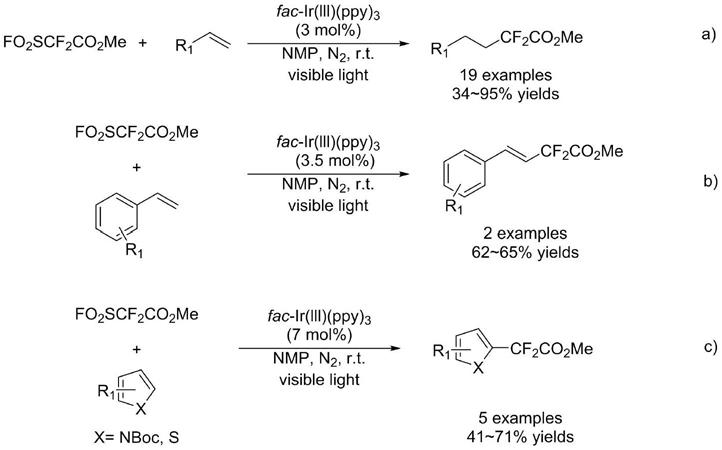
2007年,barigelletti课题组报道了未活化烯烃和苯乙烯中c(sp2)的二氟烷基化反应,利用金属铱催化剂和可见光作用形成偕二氟亚甲基自由基,最终生成相应的产物,可以发现底物拓展中,含有芳基的共轭结构中并不能使得双键反应,而脂肪族底物则会将双键氧化,产率良好,为光催化在偕二氟亚甲基化中的应用提供了良好的例子(l.flamigni,a.barbieri,c.sabatini,b.ventura,f.barigelletti,top.curr.chem.2007,281,143.)。
[0007][0008]
2014年,cho课题组报道了利用二氟溴乙酸乙酯这种简单易得的偕二氟亚甲基化试剂作为氟源,用于未活化烯烃的二氟烷基化反应。碱和溶剂的选择对于指导二氟烷基化烷烃和烯烃的化学选择性合成至关重要。该反应通过光催化剂和碱的作用,反应在室温下即可取得良好的产率。实现了一种利用不同的碱从而生成完全还原的烷烃产物和非还原状态的烯烃产物,此方法十分有利于选择性还原有机分子中的烯烃,产率从良好至优秀(c.yu,n.iqbal,s.park,e.j.cho,chem.commun.2014,50,12884.)。
[0009][0010]
2016年,liu课题组报道了一种用碘二氟乙酸乙酯烷基化试剂对不饱和羧酸进行脱羧偕二氟亚甲基化的反应方法,此方法采用了双催化体系,即光催化与铜催化的融合,成功实现了对不饱和羧酸进行脱羧功能化,并且反应条件温和,底物适应性良好,立体选择性效果以反式产物居多(h.-r.zhang,d.-q.chen,y.-p.han,y.-f.qiu,d.-p.jin,x.-y.liu,chem.commun.2016,52,11827.)。
[0011][0012]
2017年,课题组用溴二氟乙酸乙酯作为碘二氟乙酸乙酯的替代品对不饱和羧酸进行脱羧功能化。该方法对于间取代和对取代的基团以及含电子中性的不饱和羧酸等底物均可以发生反应,芳香环和杂环取代基(吡啶和噻吩)上的给电子、吸电子取代基对二氟烷基苯乙烯均无较大影响,并且反应具有良好的立体选择性(x.-j.wei,w.boom,v.hessel,t.acs catal.2017,7,7136.)。
[0013][0014]
2017年,kishikawa课题组报道了一篇在可见光引发下,在作为氢源的1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯存在下,还原烯烃的加氢二氟烷基化反应。该反应也同样适用于炔烃的加氢二氟烷基化反应,虽然该反应成功构建了c(sp2)-cf2和c(sp3)-cf2的骨架,但是反应会产生含有br的副产物,不过此反应产率良好,官能团耐受性较强,充分利用了1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯的还原特性以及光照对电子转移的作用(s.sumino,m.uno,t.fukuyama,i.ryu,m.matsuura,a.yamamoto,y.kishikawa,j.org.chem.2017,82,5469.)。
[0015]
技术实现要素:
[0016]
为了解决现有技术问题,本发明的目的在于克服已有技术存在的不足,提供一种顺式构型的2,2-二氟-4-苯基丁-3-烯酸乙酯类化合物及其制备方法,在不使用任何光催化剂的前提下,以1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯作为氢源和催化剂、丙酮作为
溶剂,蓝光led作为光源,发生反应,原料简单易得,操作简单,条件温和,反应环保,产率高。本发明通过应用该方法合成顺式构型的2,2-二氟-4-苯基丁-3-烯酸乙酯类化合物,在有机合成、药物化学中具有潜在的应用价值,在工业生产中有较好的应用前景。
[0017]
为达到上述目的,本发明采用如下技术方案:
[0018]
一种顺式构型的2,2-二氟-4-苯基丁-3-烯酸乙酯类化合物,其结构式为:
[0019][0020]
其中,r1为甲基或乙基,x为o或nh。
[0021]
一种本发明顺式构型的2,2-二氟-4-苯基丁-3-烯酸乙酯类化合物的制备方法,包括如下步骤:
[0022]
(1)将苯乙炔衍生物和二氟溴乙酸乙酯衍生物以摩尔比为1:1~1:5的投料比例进行混合,作为反应原料,并加入丙酮为溶剂,形成反应物体系,在反应体系中加入0.5倍当量~2倍当量的k2co3和0.5倍当量~2倍当量的1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯,在18~45w的蓝光led灯照射下,反应18~30小时,然后置换氮气,在20-30℃下搅拌至反应原料消失;
[0023]
(2)在反应结束后,将反应产物液冷至室温,用乙酸乙酯萃取产物后,使用饱和食盐水洗涤,干燥后去除溶剂,得粗产物;
[0024]
(3)将粗产物经用柱层析分离提纯,得到顺式构型的2,2-二氟-4-苯基丁-3-烯酸乙酯类化合物。
[0025]
优选地,在所述步骤(3)中,采用正己烷和乙酸乙酯的体积比为5:1~30:1的混合溶剂,进行柱层析分离提纯。
[0026]
优选地,在所述步骤(1)中,将苯乙炔衍生物和二氟溴乙酸乙酯衍生物以摩尔比为1:2~1:5的投料比例进行混合。
[0027]
优选地,在所述步骤(1)中,在反应体系中加入1倍当量~2倍当量的k2co3和1倍当量~2倍当量的1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯。
[0028]
本发明原理:
[0029]
发明采用了如下的技术方案:
[0030][0031]
其中,r1为甲基或乙基,x为o或nh。
[0032]
本发明方法采用的反应机理为:1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯与[
·
c(ar)=ch-cf2co2et]中间体发生作用时的空间位阻导致的,由此可以发现,1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯在此反应中不但充当了单电子转移(set)的引发剂,也充当了氢源的作用。而值得注意的是,此反应只将炔烃还原为了烯烃,而没有进行完全还原至烷烃,事实上,当尝试将炔烃完全还原为烷烃时,反应并不能进行,这证明了在此条件下,苯炔并不能完全还原,即实现一种将苯基炔烃还原为大量顺式烯烃的方法,参见图1。
[0033]
本发明与现有技术相比较,具有如下显而易见的突出实质性特点和显著优点:
[0034]
1.本发明在不使用任何光催化剂的前提下,以1,4-二氢-2,6-二甲基-3,5吡啶二
甲酸二乙酯作为氢源和催化剂、丙酮作为溶剂,蓝光led作为光源,发生反应,原料简单易得,操作简单,条件温和,反应环保,产率高;
[0035]
2.本发明能根据不同的产物需求,通过选择投料比来调控产率,满足不同烯酸乙酯类化合物制备的需要;
[0036]
3.本发明通过应用该方法合成顺式构型的2,2-二氟-4-苯基丁-3-烯酸乙酯类化合物,在有机合成、药物化学中具有潜在的应用价值,在工业生产中有较好的应用前景。
附图说明
[0037]
图1为本发明顺式构型的2,2-二氟-4-苯基丁-3-烯酸乙酯类化合物的制备方法的原理图。
具体实施方式
[0038]
以下结合具体的实施例子对上述方案做进一步说明,本发明的优选实施例详述如下:
[0039]
实施例一:z-2,2-二氟-4-苯基丁-3-烯酸乙酯
[0040]
z-2,2-二氟-4-苯基丁-3-烯酸乙酯化合物采用下述步骤:
[0041]
①
在10ml反应管中依次加入51mg苯乙炔(0.50mmol)和406mg二氟溴乙酸乙酯(2.0mmol),69mg的k2co3,253mg的1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯,然后加入2ml丙酮作为溶剂,在室温环境下,抽换氮气后在30w蓝光led灯下进行反应。用薄层层析方法监测反应,至反应原料消失;
[0042]
②
反应结束后,反应液冷至室温。用乙酸乙酯萃取产物,用饱和食盐水洗涤,干燥后用旋转蒸发仪去除溶剂,得粗产物;
[0043]
③
粗产物用柱层析(正己烷/乙酸乙酯=5:1~30:1)纯化,得到101.6mgz-2,2-二氟-4-苯基丁-3-烯酸乙酯化合物,其主要结构式为:产率为90%。
[0044]
在本实施例中,通过选择投料比来调控产率,满足不同烯酸乙酯类化合物制备的需要。
[0045]
投料比例:苯乙炔:二氟溴乙酸乙酯=1:1时,其他投料量不变,产率为54%;投料比例:苯乙炔:二氟溴乙酸乙酯=1:2时,其他投料量不变,产率为61%;投料比例:苯乙炔:二氟溴乙酸乙酯=1:5时,其他投料量不变,产率为88%;投料比例:1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯投料量为1当量时,其他投料量不变,产率为49%;投料比例:k2co3投料量为2当量时,其他投料量不变,产率为72%。
[0046]
cas:915791-21-8.
[0047]1h nmr(500mhz,cdcl3)δppm{e:7.44-7.50(m),z:7.30-7.38(m),5h},{e:7.08(dt,j=16.2,2.5hz),z:6.95(dt,j=12.8,1.6hz),1h},{e:6.31(dt,j=16.2,11.2hz),z:5.88(dt,j=12.8,12.8hz),1h},{e:4.36(q,j=7.2hz),z:4.03(q,j=7.2hz),2h},{e:1.37(t,j=7.2hz),z:1.13(t,j=7.2hz),3h}.
[0048]
19
f nmr(471mhz,cdcl3)δppm{z:-93.93(d,j=12.8hz),e:-103.24(dd,j=11.2,2.5hz),cf2}.
[0049]
13
c nmr for the z-product(125mhz,cdcl3)δppm 163.52(t,j=33.6hz),138.86(t,j=8.8hz),134.39,129.04(t,j=2.6hz),128.84,128.33,122.06(t,j=28.0hz),112.39(t,j=244.3hz),63.04,13.71.
[0050]
实施例二:z-乙基-4-(4-甲基苯基)-2,2-二氟丁-3-烯酸酯
[0051]
z-乙基-4-(4-甲基苯基)-2,2-二氟丁-3-烯酸酯化合物采用下述步骤:
[0052]
①
在10ml反应管中依次加入58mg对甲基苯乙炔(0.50mmol)和406mg二氟溴乙酸乙酯(2.0mmol),69mg的k2co3,253mg的1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯,然后加入2ml丙酮作为溶剂,在室温环境下,抽换氮气后在30w蓝光led灯下进行反应。用薄层层析方法监测反应,至反应原料消失;
[0053]
②
反应结束后,反应液冷至室温。用乙酸乙酯萃取产物,用饱和食盐水洗涤,干燥后用旋转蒸发仪去除溶剂,得粗产物;
[0054]
③
粗产物用柱层析(正己烷/乙酸乙酯=5:1~30:1)纯化,得到88.0mgz-乙基-4-(4-甲基苯基)-2,2-二氟丁-3-烯酸酯化合物,其主要结构式为:产率为74%。
[0055]
在本实施例中,通过选择投料比来调控产率,满足不同烯酸乙酯类化合物制备的需要。投料比例:4-甲基苯乙炔:二氟溴乙酸乙酯=1:1时,其他投料量不变,产率为51%;投料比例:4-甲基苯乙炔:二氟溴乙酸乙酯=1:2时,其他投料量不变,产率为56%;投料比例:4-甲基苯乙炔:二氟溴乙酸乙酯=1:5时,其他投料量不变,产率为68%;投料比例:1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯投料量为1当量时,其他投料量不变,产率为35%;投料比例:k2co3投料量为2当量时,其他投料量不变,产率为70%。
[0056]
cas:1854980-98-5.
[0057]1h nmr(500mhz,cdcl3)δppm{e:7.33-7.36(m),7.17-7.20(m),z:7.23-7.27(m),7.13-7.17(m),4h},{e:7.05(dt,j=16.1,2.3hz),z:6.90(dt,j=13.0,1.9hz),1h},{e:6.25(dt,j=16.1,11.7hz),z:5.82(dt,j=13.0,13.3hz),1h},{e:4.35(q,j=7.2hz),z:4.06(q,j=7.2hz),2h},{e:2.37(s),z:2.35(s),3h},{e:1.36(t,j=7.2hz),z:1.14(t,j=7.2hz),3h}.
[0058]
19
f nmr(471mhz,cdcl3)δppm{z:-94.01(d,j=13.2hz),e:-103.00(dd,j=12.7,2.3hz),cf2}.
[0059]
13
c nmr for the z-product(125mhz,cdcl3)δppm 163.63(t,j=34.0hz),138.95,138.88(t,j=9.2hz),131.52,129.11(t,j=2.5hz),129.04,121.15(t,j=28.0hz),112.52(t,j=245.7hz),63.01,21.38,13.72.
[0060]
实施例三:z-乙基-4-(4-乙基苯基)-2,2-二氟丁-3-烯酸酯
[0061]
z-乙基-4-(4-乙基苯基)-2,2-二氟丁-3-烯酸酯化合物采用下述步骤:
[0062]
①
在10ml反应管中依次加入65mg对乙基苯乙炔(0.50mmol)和406mg二氟溴乙酸乙酯(2.0mmol),69mg的k2co3,253mg的1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯,然后加入2ml丙酮作为溶剂,在室温环境下,抽换氮气后在30w蓝光led灯下进行反应。用薄层层析方法监测反应,至反应原料消失;
[0063]
②
反应结束后,反应液冷至室温。用乙酸乙酯萃取产物,用饱和食盐水洗涤,干燥后用旋转蒸发仪去除溶剂,得粗产物;
[0064]
③
粗产物用柱层析(正己烷/乙酸乙酯=5:1~30:1)纯化,得到109.1mg z-乙基-4-(4-乙基苯基)-2,2-二氟丁-3-烯酸酯化合物,其主要结构式为:产率为86%。
[0065]
在本实施例中,通过选择投料比来调控产率,满足不同烯酸乙酯类化合物制备的需要。投料比例:4-乙基苯乙炔:二氟溴乙酸乙酯=1:1时,其他投料量不变,产率为44%;投料比例:4-乙基苯乙炔:二氟溴乙酸乙酯=1:2时,其他投料量不变,产率为51%;投料比例:4-乙基苯乙炔:二氟溴乙酸乙酯=1:5时,其他投料量不变,产率为78%;投料比例:1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯投料量为1当量时,其他投料量不变,产率为43%;投料比例:k2co3投料量为2当量时,其他投料量不变,产率为79%。
[0066]
cas:1854981-01-3.
[0067]1h nmr(500mhz,cdcl3)δppm{e:7.36-7.39(m),7.19-7.23(m),z:7.26-7.30(m),7.16-7.19(m),4h},{e:7.06(dt,j=16.2,2.9hz),z:6.91(dt,j=12.9,1.8hz),1h},{e:6.26(dt,j=16.2,11.4hz),z:5.82(dt,j=12.9,12.9hz),1h},{e:4.35(q,j=7.2hz),z:4.04(q,j=7.2hz),2h},2.64(q,j=7.6hz,2h),1.23(t,j=7.6hz,3h),{e:1.36(t,j=7.2hz),z:1.12(t,j=7.2hz),3h}.
[0068]
19
f nmr(471mhz,cdcl3)δppm{z:-93.85(d,j=12.9hz),e:-103.04(dd,j=11.4,2.9hz),cf2}.
[0069]
13
c nmr for the z-product(125mhz,cdcl3)δppm 163.61(t,j=33.6hz),145.28,138.86(t,j=8.7hz),131.75,129.20(t,j=2.6hz),127.85,121.17(t,j=27.6hz),112.51(t,j=244.1hz),62.99,28.76,15.53,13.69.
[0070]
实施例四:z-乙基-4-(4-异丙基苯基)-2,2-二氟丁-3-烯酸酯
[0071]
z-乙基-4-(4-异丙基苯基)-2,2-二氟丁-3-烯酸酯化合物采用下述步骤:
[0072]
①
在10ml反应管中依次加入72mg对异丙基苯乙炔(0.50mmol)和406mg二氟溴乙酸乙酯(2.0mmol),69mg的k2co3,253mg的1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯,然后加入2ml丙酮作为溶剂,在室温环境下,抽换氮气后在30w蓝光led灯下进行反应。用薄层层析方法监测反应,至反应原料消失;
[0073]
②
反应结束后,反应液冷至室温。用乙酸乙酯萃取产物,用饱和食盐水洗涤,干燥后用旋转蒸发仪去除溶剂,得粗产物;
[0074]
③
粗产物用柱层析(正己烷/乙酸乙酯=5:1~30:1)纯化,得到119.4mgz-乙基-4-(4-异丙基苯基)-2,2-二氟丁-3-烯酸酯化合物,其主要结构式为:产率为89%。
[0075]
在本实施例中,通过选择投料比来调控产率,满足不同烯酸乙酯类化合物制备的需要。投料比例:4-异丙基苯乙炔:二氟溴乙酸乙酯=1:1时,其他投料量不变,产率为45%;
投料比例:4-异丙基苯乙炔:二氟溴乙酸乙酯=1:2时,其他投料量不变,产率为53%;投料比例:4-异丙基苯乙炔:二氟溴乙酸乙酯=1:5时,其他投料量不变,产率为83%;投料比例:1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯投料量为1当量时,其他投料量不变,产率为56%;投料比例:k2co3投料量为2当量时,其他投料量不变,产率为81%。
[0076]
cas:2131740-85-5.
[0077]1h nmr(500mhz,cdcl3)δppm{e:7.37-7.40(m),7.22-7.25(m),z:7.27-7.31(m),7.18-7.22(m),4h},{e:7.05(dt,j=16.3,2.8hz),z:6.91(dt,j=12.9,1.8hz),1h},{e:6.25(dt,j=16.3,11.7hz),z:5.82(dt,j=12.9,12.7hz),1h},{e:4.34(q,j=7.2hz),z:4.03(q,j=7.2hz),2h},2.9(m,1h),{e:1.25(d,j=7.0hz),z:1.24(d,j=7.0hz),6h},{e:1.36(t,j=7.2hz),z:1.10(t,j=7.2hz),3h}.
[0078]
19
f nmr(471mhz,cdcl3)δppm{z:-93.71(d,j=12.7hz),e:-103.08(dd,j=11.7,2.8hz),cf2}.
[0079]
13
c nmr for the z-product(125mhz,cdcl3)δppm 163.61(t,j=33.7hz),149.89,138.83(t,j=8.9hz),131.89,129.23(t,j=2.6hz),127.06,126.43,121.19(t,j=28.1hz),112.51(t,j=243.9hz),62.99,34.04,23.93,13.67.
[0080]
实施例五:z-乙基-4-(4-甲氧基苯基)-2,2-二氟丁-3-烯酸酯
[0081]
z-乙基-4-(4-甲氧基苯基)-2,2-二氟丁-3-烯酸酯化合物采用下述步骤:
[0082]
①
在10ml反应管中依次加入66mg对甲氧基苯乙炔(0.50mmol)和406mg二氟溴乙酸乙酯(2.0mmol),69mg的k2co3,253mg的1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯,然后加入2ml丙酮作为溶剂,在室温环境下,抽换氮气后在30w蓝光led灯下进行反应。用薄层层析方法监测反应,至反应原料消失;
[0083]
②
反应结束后,反应液冷至室温。用乙酸乙酯萃取产物,用饱和食盐水洗涤,干燥后用旋转蒸发仪去除溶剂,得粗产物;
[0084]
③
粗产物用柱层析(正己烷/乙酸乙酯=5:1~30:1)纯化,得到99.4mgz-乙基-4-(4-甲氧基苯基)-2,2-二氟丁-3-烯酸酯化合物,其主要结构式为:产率为78%。
[0085]
在本实施例中,通过选择投料比来调控产率,满足不同烯酸乙酯类化合物制备的需要。投料比例:4-甲氧基苯乙炔:二氟溴乙酸乙酯=1:1时,其他投料量不变,产率为34%;投料比例:4-甲氧基苯乙炔:二氟溴乙酸乙酯=1:2时,其他投料量不变,产率为46%;投料比例:4-甲氧基苯乙炔:二氟溴乙酸乙酯=1:5时,其他投料量不变,产率为72%;投料比例:1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯投料量为1当量时,其他投料量不变,产率为41%;投料比例:k2co3投料量为2当量时,其他投料量不变,产率为74%。
[0086]
cas:1627895-88-8.
[0087]1h nmr(500mhz,cdcl3)δppm{e:7.37-7.41(m),6.87-6.91(m),z:7.31-7.35(m),6.85-6.88(m),4h},{e:7.01(dt,j=16.1,2.8hz),z:6.87(dt,j=13.1,1.9hz),1h},{e:6.16(dt,j=16.1,11.8hz),z:5.8(dt,j=13.1,13.3hz),1h},{e:4.35(q,j=7.2hz),z:4.11(q,j=7.2hz),2h},{e:3.83(s),z:3.81(s),3h},{e:1.36(t,j=7.2hz),z:1.16(t,j
=7.2hz),3h}.
[0088]
19
f nmr(471mhz,cdcl3)δppm{z:-95.04(d,j=13.3hz),e:-103.36(dd,j=11.8,2.8hz),cf2}.
[0089]
13
c nmr for the z-product(125mhz,cdcl3)δppm 163.50(t,j=34.0hz),159.94,138.26(t,j=8.3hz),130.67(t,j=2.8hz),126.61,119.66(t,j=27.5hz),113.51,112.41(t,j=244.1hz),62.81,55.13,13.53.
[0090]
实施例六:z-乙基-4-(4-三氟甲基苯基)-2,2-二氟丁-3-烯酸酯
[0091]
z-乙基-4-(4-三氟甲基苯基)-2,2-二氟丁-3-烯酸酯化合物采用下述步骤:
[0092]
①
在10ml反应管中依次加入85mg对三氟甲基苯乙炔(0.50mmol)和406mg二氟溴乙酸乙酯(2.0mmol),69mg的k2co3,253mg的1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯,然后加入2ml丙酮作为溶剂,在室温环境下,抽换氮气后在30w蓝光led灯下进行反应。用薄层层析方法监测反应,至反应原料消失;
[0093]
②
反应结束后,反应液冷至室温。用乙酸乙酯萃取产物,用饱和食盐水洗涤,干燥后用旋转蒸发仪去除溶剂,得粗产物;
[0094]
③
粗产物用柱层析(正己烷/乙酸乙酯=5:1~30:1)纯化,得到94.2mg z-乙基-4-(4-三氟甲基苯基)-2,2-二氟丁-3-烯酸酯化合物,其主要结构式为:产率为64%。
[0095]
在本实施例中,通过选择投料比来调控产率,满足不同烯酸乙酯类化合物制备的需要。投料比例:4-三氟甲基苯乙炔:二氟溴乙酸乙酯=1:1时,其他投料量不变,产率为27%;投料比例:4-三氟甲基苯乙炔:二氟溴乙酸乙酯=1:2时,其他投料量不变,产率为32%;投料比例:4-三氟甲基苯乙炔:二氟溴乙酸乙酯=1:5时,其他投料量不变,产率为60%;投料比例:1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯投料量为1当量时,其他投料量不变,产率为39%;投料比例:k2co3投料量为2当量时,其他投料量不变,产率为59%。
[0096]
cas:1854981-12-6.
[0097]1h nmr(500mhz,cdcl3)δppm{e:7.62-7.65(m),7.54-7.58(m),z:7.58-7.62(m),7.44-7.49(m),4h},{e:7.12(dt,j=16.2,2.8hz),z:6.96(dt,j=13.1,1.9hz),1h},{e:6.40(dt,j=16.2,12.7hz),z:5.97(dt,j=13.1,13.5hz),1h},{e:4.36(q,j=7.2hz),z:4.12(q,j=7.2hz),2h},{e:1.37(t,j=7.2hz),z:1.19(t,j=7.2hz),3h}.
[0098]
19
f nmr(471mhz,cdcl3)δppm-62.83(3f),{z:-95.55(d,j=13.6hz),e:-103.74(dd,j=12.7,2.8hz),cf2}.
[0099]
13
c nmr for the z-product(125mhz,cdcl3)δppm 163.42(t,j=34.0hz),137.33(t,j=8.1hz),130.67(q,j=32.6hz),129.33(t,j=2.8hz),125.97(q,j=3.7hz),125.24(q,j=3.7hz),124.06(q,j=270.4hz),123.83(t,j=27.3hz),112.16(t,j=246.0hz),63.32,13.76.
[0100]
实施例七:z-乙基-4-(4-氟苯基)-2,2-二氟丁-3-烯酸酯
[0101]
z-乙基-4-(4-氟苯基)-2,2-二氟丁-3-烯酸酯化合物采用下述步骤:
[0102]
①
在10ml反应管中依次加入60mg对氟苯乙炔(0.50mmol)和406mg二氟溴乙酸乙酯
(2.0mmol),69mg的k2co3,253mg的1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯,然后加入2ml丙酮作为溶剂,在室温环境下,抽换氮气后在30w蓝光led灯下进行反应。用薄层层析方法监测反应,至反应原料消失;
[0103]
②
反应结束后,反应液冷至室温。用乙酸乙酯萃取产物,用饱和食盐水洗涤,干燥后用旋转蒸发仪去除溶剂,得粗产物;
[0104]
③
粗产物用柱层析(正己烷/乙酸乙酯=5:1~30:1)纯化,得到101.6mg z-乙基-4-(4-氟苯基)-2,2-二氟丁-3-烯酸酯化合物,其主要结构式为:产率为83%。
[0105]
在本实施例中,通过选择投料比来调控产率,满足不同烯酸乙酯类化合物制备的需要。投料比例:4-氟苯乙炔:二氟溴乙酸乙酯=1:1时,其他投料量不变,产率为33%;投料比例:4-氟苯乙炔:二氟溴乙酸乙酯=1:2时,其他投料量不变,产率为44%;投料比例:4-氟苯乙炔:二氟溴乙酸乙酯=1:5时,其他投料量不变,产率为76%;投料比例:1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯投料量为1当量时,其他投料量不变,产率为41%;投料比例:k2co3投料量为2当量时,其他投料量不变,产率为79%。
[0106]
cas:1627895-84-4.
[0107]1h nmr(500mhz,cdcl3)δppm 7.32-7.38(m,2h),7.00-7.06(m,2h),z:6.88(dt,j=13.0,2.5hz,1h),{e:6.41(dt,j=16.4,12.1hz),z:5.85(dt,j=13.0,13.6hz),1h},{e:4.35(q,j=7.2hz),z:4.11(q,j=7.2hz),2h},{e:1.36(t,j=7.2hz),z:1.18(t,j=7.2hz),3h}.
[0108]
19
f nmr(471mhz,cdcl3)δppm{z:-94.75(d,j=13.6hz),e:-103.20(dd,j=12.1,2.5hz),cf2},-112.13(m,1f).
[0109]
13
c nmr for the z-product(125mhz,cdcl3)δppm 163.53(t,j=33.6hz),162.97(d,j=247.7hz),137.73(t,j=8.4hz),131.12(dt,j=8.6,3.7hz),121.86(t,j=27.6hz),115.35(d,j=21.6hz),112.35(t,j=245.1hz),63.16,13.77.
[0110]
实施例八:z-乙基-4-(4-氯苯基)-2,2-二氟丁-3-烯酸酯
[0111]
z-乙基-4-(4-氯苯基)-2,2-二氟丁-3-烯酸酯化合物采用下述步骤:
[0112]
①
在10ml反应管中依次加入68mg对氯苯乙炔(0.50mmol)和406mg二氟溴乙酸乙酯(2.0mmol),69mg的k2co3,253mg的1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯,然后加入2ml丙酮作为溶剂,在室温环境下,抽换氮气后在30w蓝光led灯下进行反应。用薄层层析方法监测反应,至反应原料消失;
[0113]
②
反应结束后,反应液冷至室温。用乙酸乙酯萃取产物,用饱和食盐水洗涤,干燥后用旋转蒸发仪去除溶剂,得粗产物;
[0114]
③
粗产物用柱层析(正己烷/乙酸乙酯=5:1~30:1)纯化,得到106.8mgz-乙基-4-(4-氯苯基)-2,2-二氟丁-3-烯酸酯化合物,其主要结构式为:产率为82%。
[0115]
在本实施例中,通过选择投料比来调控产率,满足不同烯酸乙酯类化合物制备的
需要。投料比例:4-氯苯乙炔:二氟溴乙酸乙酯=1:1时,其他投料量不变,产率为47%;投料比例:4-氯苯乙炔:二氟溴乙酸乙酯=1:2时,其他投料量不变,产率为52%;投料比例:4-氯苯乙炔:二氟溴乙酸乙酯=1:5时,其他投料量不变,产率为77%;投料比例:1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯投料量为1当量时,其他投料量不变,产率为53%;投料比例:k2co3投料量为2当量时,其他投料量不变,产率为78%。
[0116]
cas:2010149-21-8.
[0117]1h nmr(500mhz,cdcl3)δppm{e:7.34-7.40(m),z:7.28-7.32(m),4h},{e:7.03(dt,j=15.6,2.6hz),z:6.87(dt,j=13.1,2.5hz),1h},{e:6.23(dt,j=15.6,12.0hz),z:5.88(dt,j=12.6,12.6hz),1h},{e:4.35(q,j=7.2hz),z:4.12(q,j=7.2hz),2h},{e:1.37(t,j=7.2hz),z:1.20(t,j=7.2hz),3h}.
[0118]
19
f nmr(471mhz,cdcl3)δppm{z:-95.03(d,j=12.6hz),e:-103.36(dd,j=12.0,2.6hz),cf2}.
[0119]
13
c nmr for the z-product(125mhz,cdcl3)δppm 163.25(t,j=34.0hz),137.35(t,j=8.3hz),134.66,132.52,130.23(t,j=2.8hz),128.31,122.23(t,j=27.5hz),112.03(t,j=245.6hz),62.98,13.57.
[0120]
实施例九:z-乙基-4-(4-溴苯基)-2,2-二氟丁-3-烯酸酯
[0121]
z-乙基-4-(4-溴苯基)-2,2-二氟丁-3-烯酸酯化合物采用下述步骤:
[0122]
①
在10ml反应管中依次加入91mg对溴苯乙炔(0.50mmol)和406mg二氟溴乙酸乙酯(2.0mmol),69mg的k2co3,253mg的1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯,然后加入2ml丙酮作为溶剂,在室温环境下,抽换氮气后在30w蓝光led灯下进行反应。用薄层层析方法监测反应,至反应原料消失;
[0123]
②
反应结束后,反应液冷至室温。用乙酸乙酯萃取产物,用饱和食盐水洗涤,干燥后用旋转蒸发仪去除溶剂,得粗产物;
[0124]
③
粗产物用柱层析(正己烷/乙酸乙酯=5:1~30:1)纯化,得到105.6mg z-乙基-4-(4-溴苯基)-2,2-二氟丁-3-烯酸酯化合物,其主要结构式为:产率为69%。
[0125]
在本实施例中,通过选择投料比来调控产率,满足不同烯酸乙酯类化合物制备的需要。投料比例:4-溴苯乙炔:二氟溴乙酸乙酯=1:1时,其他投料量不变,产率为35%;投料比例:4-溴苯乙炔:二氟溴乙酸乙酯=1:2时,其他投料量不变,产率为41%;投料比例:4-溴苯乙炔:二氟溴乙酸乙酯=1:5时,其他投料量不变,产率为69%;投料比例:1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯投料量为1当量时,其他投料量不变,产率为36%;投料比例:k2co3投料量为2当量时,其他投料量不变,产率为60%。
[0126]
cas:1627895-86-6.
[0127]1h nmr(500mhz,cdcl3)δppm{e:7.49-7.52(m),7.30-7.33(m),z:7.45-7.49(m),7.21-7.25(m),4h},{e:7.02(dt,j=16.2,2.5hz),z:6.85(dt,j=13.0,1.9hz),1h},{e:6.30(dt,j=16.2,11.7hz),z:5.89(dt,j=13.0,13.6hz),1h},{e:4.35(q,j=7.2hz),z:4.12(q,j=7.2hz),2h},{e:1.37(t,j=7.2hz),z:1.19(t,j=7.2hz),3h}.
[0128]
19
f nmr(471mhz,cdcl3)δppm{z:-95.08(d,j=13.6hz),e:-103.41(dd,j=11.7,
2.4hz),cf2}.
[0129]
13
c nmr for the z-product(125mhz,cdcl3)δppm 163.45(t,j=33.6hz),137.62(t,j=8.3hz),133.21,131.49,130.70(t,j=2.7hz),123.12,122.52(t,j=27.4hz),112.26(t,j=245.3hz),63.23,13.79.
[0130]
实施例十:z-乙基-4-(4-苯基苯基)-2,2-二氟丁-3-烯酸酯
[0131]
z-乙基-4-(4-苯基苯基)-2,2-二氟丁-3-烯酸酯化合物采用下述步骤:
[0132]
①
在10ml反应管中依次加入89mg对苯基苯乙炔(0.50mmol)和406mg二氟溴乙酸乙酯(2.0mmol),69mg的k2co3,253mg的1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯,然后加入2ml丙酮作为溶剂,在室温环境下,抽换氮气后在30w蓝光led灯下进行反应。用薄层层析方法监测反应,至反应原料消失;
[0133]
②
反应结束后,反应液冷至室温。用乙酸乙酯萃取产物,用饱和食盐水洗涤,干燥后用旋转蒸发仪去除溶剂,得粗产物;
[0134]
③
粗产物用柱层析(正己烷/乙酸乙酯=5:1~30:1)纯化,得到92.1mgz-乙基-4-(4-苯基苯基)-2,2-二氟丁-3-烯酸酯化合物,其主要结构式为:产率为61%。
[0135]
在本实施例中,通过选择投料比来调控产率,满足不同烯酸乙酯类化合物制备的需要。投料比例:4-苯基苯乙炔:二氟溴乙酸乙酯=1:1时,其他投料量不变,产率为29%;投料比例:4-苯基苯乙炔:二氟溴乙酸乙酯=1:2时,其他投料量不变,产率为34%;投料比例:4-苯基苯乙炔:二氟溴乙酸乙酯=1:5时,其他投料量不变,产率为59%;投料比例:1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯投料量为1当量时,其他投料量不变,产率为30%;投料比例:k2co3投料量为2当量时,其他投料量不变,产率为58%。
[0136]
cas:1854981-16-0.
[0137]1h nmr(500mhz,cdcl3)δppm{e:7.42-7.65(m),9h z:7.58-7.62(m),4h,z:7.43-7.48(m),4h},z:7.35-7.40(m),1h,{e:7.13(dt,j=16.2,2.7hz),z:6.97(dt,j=13.1,1.8hz),1h},{e:6.35(dt,j=16.2,11.4hz),z:5.90(dt,j=13.1,13.4hz),1h},{e:4.37(q,j=7.2hz),z:4.01(q,j=7.2hz),2h},{e:1.38(t,j=7.2hz),z:1.16(t,j=7.2hz),3h}.
[0138]
19
f nmr(471mhz,cdcl3)δppm{z:-94.22(d,j=13.5hz),e:-103.11(dd,j=11.5,2.7hz),cf2}.
[0139]
13
c nmr for the z-product(125mhz,cdcl3)δppm 163.61(t,j=33.7hz),141.63,140.40,138.46(t,j=8.6hz),133.31,129.70,128.99,127.80,127.15,126.97,121.86(t,j=27.8hz),112.47(t,j=244.5hz),63.13,13.77.
[0140]
实施例十一:z-2,2-二氟-4-苯基丁-3-烯酸甲酯
[0141]
z-2,2-二氟-4-苯基丁-3-烯酸甲酯化合物采用下述步骤:
[0142]
①
在10ml反应管中依次加入89mg对苯基苯乙炔(0.50mmol)和378mg二氟溴乙酸甲酯(2.0mmol),69mg的k2co3,253mg的1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯,然后加
入2ml丙酮作为溶剂,在室温环境下,抽换氮气后在30w蓝光led灯下进行反应。用薄层层析方法监测反应,至反应原料消失;
[0143]
②
反应结束后,反应液冷至室温。用乙酸乙酯萃取产物,用饱和食盐水洗涤,干燥后用旋转蒸发仪去除溶剂,得粗产物;
[0144]
③
粗产物用柱层析(正己烷/乙酸乙酯=5:1~30:1)纯化,得到69mg z-2,2-二氟-4-苯基丁-3-烯酸甲酯化合物,其主要结构式为:产率为65%。
[0145]
在本实施例中,通过选择投料比来调控产率,满足不同烯酸乙酯类化合物制备的需要。投料比例:4-苯基苯乙炔:二氟溴乙酸甲酯=1:1时,其他投料量不变,产率为31%;投料比例:4-苯基苯乙炔:二氟溴乙酸甲酯=1:2时,其他投料量不变,产率为39%;投料比例:4-苯基苯乙炔:二氟溴乙酸甲酯=1:5时,其他投料量不变,产率为61%;投料比例:1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯投料量为1当量时,其他投料量不变,产率为33%;投料比例:k2co3投料量为2当量时,其他投料量不变,产率为59%。
[0146]
cas:109872-94-8.
[0147]1h nmr(500mhz,cdcl3)δppm{e:7.44-7.50(m),z:7.30-7.38(m),5h},{e:7.08(dt,j=16.2,2.5hz),z:6.95(dt,j=12.8,1.6hz),1h},{e:6.31(dt,j=16.2,11.2hz),z:5.88(dt,j=12.8,12.8hz),1h},{e:4.02(s,3h),z:3.61(s,3h)}.
[0148]
19
f nmr(471mhz,cdcl3)δppm{z:-95.08(d,j=13.6hz),e:-103.41(dd,j=11.7,2.4hz),cf2}.
[0149]
13
c nmr for the z-product(125mhz,cdcl3)δppm 163.91(t,j=34hz),138.92(t,j=8.8hz),134.18,128.86(t,j=3.3hz),128.23,127.48,121.88(t,j=27.7hz),112.25(t,j=247hz),53.28.
[0150]
实施例十二:z-乙基-4-(4-甲酯基苯基)-2,2-二氟丁-3-烯酸酯
[0151]
z-乙基-4-(4-甲酯基苯基)-2,2-二氟丁-3-烯酸酯化合物采用下述步骤:
[0152]
①
在10ml反应管中依次加入80mg 4-乙炔基苯甲酸甲酯(0.50mmol)和406mg二氟溴乙酸乙酯(2.0mmol),69mg的k2co3,253mg的1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯,然后加入2ml丙酮作为溶剂,在室温环境下,抽换氮气后在30w蓝光led灯下进行反应。用薄层层析方法监测反应,至反应原料消失;
[0153]
②
反应结束后,反应液冷至室温。用乙酸乙酯萃取产物,用饱和食盐水洗涤,干燥后用旋转蒸发仪去除溶剂,得粗产物;
[0154]
③
粗产物用柱层析(正己烷/乙酸乙酯=5:1~30:1)纯化,得到109.4mg z-乙基-4-(4-甲酯基苯基)-2,2-二氟丁-3-烯酸酯化合物,其主要结构式为:产率为77%。
[0155]
在本实施例中,通过选择投料比来调控产率,满足不同烯酸乙酯类化合物制备的需要。投料比例:4-乙炔基苯甲酸甲酯:二氟溴乙酸乙酯=1:1时,其他投料量不变,产率为41%;投料比例:4-乙炔基苯甲酸甲酯:二氟溴乙酸乙酯=1:2时,其他投料量不变,产率为
58%;投料比例:4-乙炔基苯甲酸甲酯:二氟溴乙酸乙酯=1:5时,其他投料量不变,产率为75%;投料比例:1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯投料量为1当量时,其他投料量不变,产率为36%;投料比例:k2co3投料量为2当量时,其他投料量不变,产率为59%。
[0156]
cas:1796567-66-2.
[0157]1h nmr(500mhz,cdcl3)δppm{e:8.02-8.06(m),7.49-7.53(m),z:7.99-8.02(m),7.38-7.43(m),4h}{e:7.11(dt,j=16.2,2.7hz),z:6.96(dt,j=12.8,1.7hz),1h},{e:6.40(dt,j=16.2,11.7hz),z:5.95(dt,j=12.8,13.4hz),1h},{e:4.36(q,j=7.2hz),z:4.09(q,j=7.1hz),2h},{e:3.93(s),z:3.92(s),3h},{e:1.37(t,j=7.2hz),z:1.17(t,j=7.1hz),3h}.
[0158]
19
f nmr(471mhz,cdcl3)δppm{z:-95.14(d,j=13.4hz),e:-103.62(dd,j=11.7,2.7hz),cf2}.
[0159]
13
c nmr for the z-product(125mhz,cdcl3)δppm 166.64,163.31(t,j=34.0hz),138.86,137.72(t,j=8.3hz),130.18,129.48,128,97(t,j=2.7hz),123.52(t,j=27.4hz),112.13(t,j=246.0hz),63.19,52.28,13.75.
[0160]
实施例十三:z-乙基-4-(4-丙基苯基)-2,2-二氟丁-3-烯酸酯
[0161]
z-乙基-4-(4-丙基苯基)-2,2-二氟丁-3-烯酸酯化合物采用下述步骤:
[0162]
①
在10ml反应管中依次加入72mg对丙基苯乙炔(0.50mmol)和406mg二氟溴乙酸乙酯(2.0mmol),69mg的k2co3,253mg的1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯,然后加入2ml丙酮作为溶剂,在室温环境下,抽换氮气后在30w蓝光led灯下进行反应。用薄层层析方法监测反应,至反应原料消失;
[0163]
②
反应结束后,反应液冷至室温。用乙酸乙酯萃取产物,用饱和食盐水洗涤,干燥后用旋转蒸发仪去除溶剂,得粗产物;
[0164]
③
粗产物用柱层析(正己烷/乙酸乙酯=5:1~30:1)纯化,得到101.7mg z-乙基-4-(4-丙基苯基)-2,2-二氟丁-3-烯酸酯化合物,其主要结构式为:产率为76%。
[0165]
在本实施例中,通过选择投料比来调控产率,满足不同烯酸乙酯类化合物制备的需要。投料比例:对丙基苯乙炔:二氟溴乙酸乙酯=1:1时,其他投料量不变,产率为40%;投料比例:对丙基苯乙炔:二氟溴乙酸乙酯=1:2时,其他投料量不变,产率为57%;投料比例:对丙基苯乙炔:二氟溴乙酸乙酯=1:5时,其他投料量不变,产率为74%;投料比例:1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯投料量为1当量时,其他投料量不变,产率为35%;投料比例:k2co3投料量为2当量时,其他投料量不变,产率为58%。
[0166]
cas:1854981-03-5.
[0167]1h nmr(500mhz,cdcl3)δppm{e:7.35-7.38(m),7.17-7.20(m),z:7.25-7.29(m),7.13-7.17(m),4h}{e:7.36(dt,j=16.1,2.8hz),z:6.91(dt,j=12.9,1.8hz),1h},{e:6.25(dt,j=16.1,11.4hz),z:5.82(dt,j=12.9,13.2hz),1h},{e:4.35(q,j=7.2hz),z:4.03(q,j=7.2hz),2h},2.58(t,j=7.4hz,2h),1.63(m,2h),{e:1.36(t,j=7.2hz),z:1.12(t,j=7.2hz),3h},{e:0.94(t,j=7.4hz),z:0.93(t,j=7.4hz),3h}.
[0168]
19
f nmr(471mhz,cdcl3)δppm{z:-93.73(d,j=13.2hz),e:-103.04(dd,j=11.4,
2.8hz),cf2}.
[0169]
13
c nmr for the z-product(125mhz,cdcl3)δppm 163.60(t,j=33.8hz),143.74,138.88(t,j=9.1hz),131.76,129.12(t,j=2.7hz),128.46,121.17(t,j=28.0hz),112.51(t,j=244.1hz),62.98,37.89,24.51,13.86,13.70.
[0170]
实施例十四:z-乙基-4-(4-丁基苯基)-2,2-二氟丁-3-烯酸酯
[0171]
z-乙基-4-(4-丁基苯基)-2,2-二氟丁-3-烯酸酯化合物采用下述步骤:
[0172]
①
在10ml反应管中依次加入79mg对丁基苯乙炔(0.50mmol)和406mg二氟溴乙酸乙酯(2.0mmol),69mg的k2co3,253mg的1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯,然后加入2ml丙酮作为溶剂,在室温环境下,抽换氮气后在30w蓝光led灯下进行反应。用薄层层析方法监测反应,至反应原料消失;
[0173]
②
反应结束后,反应液冷至室温。用乙酸乙酯萃取产物,用饱和食盐水洗涤,干燥后用旋转蒸发仪去除溶剂,得粗产物;
[0174]
③
粗产物用柱层析(正己烷/乙酸乙酯=5:1~30:1)纯化,得到109.5mg z-乙基-4-(4-丁基苯基)-2,2-二氟丁-3-烯酸酯化合物,其主要结构式为:产率为78%。
[0175]
在本实施例中,通过选择投料比来调控产率,满足不同烯酸乙酯类化合物制备的需要。投料比例:对丁基苯乙炔:二氟溴乙酸乙酯=1:1时,其他投料量不变,产率为42%;投料比例:对丁基苯乙炔:二氟溴乙酸乙酯=1:2时,其他投料量不变,产率为59%;投料比例:对丁基苯乙炔:二氟溴乙酸乙酯=1:5时,其他投料量不变,产率为76%;投料比例:1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯投料量为1当量时,其他投料量不变,产率为37%;投料比例:k2co3投料量为2当量时,其他投料量不变,产率为60%。)
[0176]
cas:2410381-18-7.
[0177]1h nmr(500mhz,cdcl3)δppm{e:7.35-7.38(m),7.17-7.20(m),z:7.25-7.28(m),7.13-7.17(m),4h},{e:7.05(dt,j=16.2,2.7hz),z:6.90(dt,j=12.9,1.9hz),1h},{e:6.25(dt,j=16.2,11.9hz),z:5.82(dt,j=12.9,13.0hz),1h},{e:4.35(q,j=7.1hz),z:4.03(q,j=7.1hz),2h},2.60(t,j=7.6hz,2h),1.54-1.62(m,2h),1.30-1.40(m,2h),{e:1.36(t,j=7.1hz),z:1.12(t,j=7.1hz),3h},{e:0.93(t,j=7.6hz),z:0.92(t,j=7.6hz),3h}.
[0178]
19
f nmr(471mhz,cdcl3)δppm{z:-93.72(d,j=13.0hz),e:-103.05(dd,j=11.9,2.7hz),cf2}.
[0179]
13
c nmr for the z-product(125mhz,cdcl3)δppm 163.60(t,j=33.8hz),143.98,138.88(t,j=8.9hz),131.71,129.13(t,j=2.6hz),128.42,121.15(t,j=27.7hz),112.51(t,j=244.1hz),62.99,35.52,33.57,22.42,14.03,13.70.
[0180]
实施例十五:z-2,2-二氟-4-(噻吩-2-基)丁-3-烯酸乙酯
[0181]
z-2,2-二氟-4-(噻吩-2-基)丁-3-烯酸乙酯化合物采用下述步骤:
[0182]
①
在10ml反应管中依次加入54mg 2-乙炔基噻吩(0.50mmol)和406mg二氟溴乙酸乙酯(2.0mmol),69mg的k2co3,253mg的1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯,然后
加入2ml丙酮作为溶剂,在室温环境下,抽换氮气后在30w蓝光led灯下进行反应。用薄层层析方法监测反应,至反应原料消失;
[0183]
②
反应结束后,反应液冷至室温。用乙酸乙酯萃取产物,用饱和食盐水洗涤,干燥后用旋转蒸发仪去除溶剂,得粗产物;
[0184]
③
粗产物用柱层析(正己烷/乙酸乙酯=5:1~30:1)纯化,得到102.9mg z-2,2-二氟-4-(噻吩-2-基)丁-3-烯酸乙酯化合物,其主要结构式为:产率为89%。
[0185]
在本实施例中,通过选择投料比来调控产率,满足不同烯酸乙酯类化合物制备的需要。投料比例:对丁基苯乙炔:二氟溴乙酸乙酯=1:1时,其他投料量不变,产率为53%;投料比例:对丁基苯乙炔:二氟溴乙酸乙酯=1:2时,其他投料量不变,产率为70%;投料比例:对丁基苯乙炔:二氟溴乙酸乙酯=1:5时,其他投料量不变,产率为87%;投料比例:1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯投料量为1当量时,其他投料量不变,产率为48%;投料比例:k2co3投料量为2当量时,其他投料量不变,产率为71%。
[0186]
cas:2010149-38-7.
[0187]1h nmr(500mhz,cdcl3)δppm 7.39-7.21(m,3h),{e:7.09-7.07(m),z:6.94(d,j=12.0hz),1h}{e:7.19(dt,j=16.4,3.1hz),z:6.88(dt,j=12.9,1.8hz),1h},{e:6.11(dt,j=16.4,11.6hz),z:5.71(dt,j=12.9,14.1hz),1h},{e:4.35(q,j=7.2hz),z:4.22(q,j=7.2hz,2h),{e:1.36(t,j=7.2hz),z:1.23(t,j=7.2hz),3h}.
[0188]
19
f nmr(471mhz,cdcl3)δppm{z:-96.35(d,j=14.2hz),e:-102.99(dd,j=11.7,3.1hz),cf2}.
[0189]
13
c nmr for the z-product(125mhz,cdcl3)δppm 163.45(t,j=33.8hz),136.39,131.21(t,j=3.6hz),130.27(t,j=8.3hz),129.03,127.74,118.67(t,j=27.9hz),112.43(t,j=245.2hz),63.21,13.87.
[0190]
实施例十六:z-2,2-二氟-n-甲基-4-苯基丁-3-烯酰胺
[0191]
z-2,2-二氟-n-甲基-4-苯基丁-3-烯酰胺化合物采用下述步骤:
[0192]
①
在10ml反应管中依次加入51mg苯乙炔(0.50mmol)和374mg2-溴-2,2-二氟-n-甲基乙酰胺(2.0mmol),69mg的k2co3,253mg的1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯,然后加入2ml丙酮作为溶剂,在室温环境下,抽换氮气后在30w蓝光led灯下进行反应。用薄层层析方法监测反应,至反应原料消失;
[0193]
②
反应结束后,反应液冷至室温。用乙酸乙酯萃取产物,用饱和食盐水洗涤,干燥后用旋转蒸发仪去除溶剂,得粗产物;
[0194]
③
粗产物用柱层析(正己烷/乙酸乙酯=5:1~30:1)纯化,得到83.9mg z-2,2-二氟-n-甲基-4-苯基丁-3-烯酰胺化合物,其主要结构式为:产率为85%。
[0195]
在本实施例中,通过选择投料比来调控产率,满足不同烯酸乙酯类化合物制备的需要。投料比例:苯乙炔:2-溴-2,2-二氟-n-甲基乙酰胺=1:1时,其他投料量不变,产率为
56%;投料比例:苯乙炔:2-溴-2,2-二氟-n-甲基乙酰胺=1:2时,其他投料量不变,产率为72%;投料比例:苯乙炔:2-溴-2,2-二氟-n-甲基乙酰胺=1:5时,其他投料量不变,产率为82%;投料比例:1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯投料量为1当量时,其他投料量不变,产率为49%;投料比例:k2co3投料量为2当量时,其他投料量不变,产率为81%。
[0196]1h nmr(500mhz,cdcl3)δppm 7.33-7.60(m,5h),7.50(s,1h),{e:6.98(dt,j=16.4,3.1hz),z:6.84(dt,j=12.9,1.8hz),1h},{e:6.27(dt,j=16.4,3.1hz),z:5.84(dt,j=12.9,1.8hz),1h},{e:2.80(s),z:2.65(s),3h}.
[0197]
19
f nmr(471mhz,cdcl3)δppm{z:-95.30(d,j=14.2hz),e:-103.72(dd,j=11.7,3.1hz),cf2}.
[0198]
13
c nmr for the z-product(125mhz,cdcl3)δppm 171.20(t,j=33.8hz),136.40,131.21(t,j=3.6hz),130.27(t,j=8.3hz),129.43,127.74,121.50,118.37(t,j=27.9hz),112.43(t,j=245.2hz),110.50,26.30.
[0199]
上述实施例在不使用任何光催化剂的前提下,以1,4-二氢-2,6-二甲基-3,5吡啶二甲酸二乙酯作为氢源和催化剂、丙酮作为溶剂,蓝光led作为光源,发生反应,原料简单易得、操作简单、条件温和、反应环保、产率一般到优秀可调。通过应用该方法合成顺式构型的2,2-二氟-4-苯基丁-3-烯酸乙酯类化合物,在有机合成、药物化学中具有潜在的应用价值,在工业生产中有较好的应用前景。
[0200]
上面结合附图对本发明实施例进行了说明,但本发明不限于上述实施例,还可以根据本发明的发明创造的目的做出多种变化,凡依据本发明技术方案的精神实质和原理下做的改变、修饰、替代、组合或简化,均应为等效的置换方式,只要符合本发明的发明目的,只要不背离本发明的技术原理和发明构思,都属于本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1