对苯二甲酸及其制备方法和回收高聚合度聚对苯二甲酸乙二醇酯的方法与流程
1.本发明涉及对苯二甲酸的制备技术领域,具体而言,涉及对苯二甲酸及其制备方法和回收高聚合度聚对苯二甲酸乙二醇酯的方法。
背景技术:
2.若要实现聚对苯二甲酸乙二醇酯(以下简称“pet”)的化学回收利用,需要利用乙二醇(以下简称“eg”)溶剂,在高温高压环境下断开分子链,完成解聚;或在酸、碱性环境下,在醇类等极性溶剂中进行水解等断开分子链的过程。
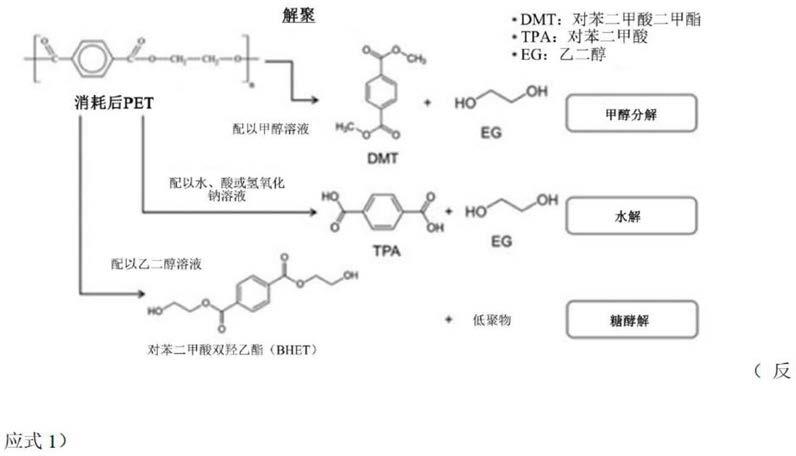
3.此时,若pet小于聚合度不高时,主要使用以下(反应式1)三种方法。
4.方法一:如(反应式1)的(a)所示,利用甲醇分解作用,在甲醇溶剂下进行分解,制备对苯二甲酸二甲酯的方法(dmt)。混合一定量的有机溶剂,如二甲基亚砜(dmso)、二氯甲烷(dichloromethane)等,促进pet的溶胀,以便在较弱的条件下完成反应。
[0005][0006]
第二种方法:如[反应式1]的(b)所示,在极性有机溶剂中,利用naoh等碱性物质进行水解,相对容易地分解为对苯二酸双钠盐(tra-na2)和乙二醇(eg),tpa-na2则很容易在酸的作用下转换为对苯二酸(tpa)。这一工艺目前已广泛应用于聚对苯二甲酸乙二醇酯纤维垃圾的回收利用、pet布料减量加工等领域。有观点认为,有时添加分子链溶胀用有机溶剂(例:dmso),通过碱性物质溶于醇时产生的热量就能完成大量的水解。此时在pet聚合度较低的纤维或包装材料等情况下,即使不能完全水解,也可以水解一部分,但是在pet瓶等高聚合度,因为dmso的溶胀效果差,所以水解程度微乎其微。
[0007]
第三种方法:如(反应式1)的(c)所示,将乙二醇(eg)作为溶剂,在高温高压环境下糖醇解pet,分解为对苯二甲酸双羟乙酯(bhet)和低聚物状态,这是pet制备企业从很久以前开始就最广为使用的pet废料重复使用方法。这些反应产物可再次混合送入聚合工艺中,
用于pet聚合。这种情况下,主要使用pet生产中污染少的pet废料重复使用方法。这是因为聚合pet时,若原料的纯度不高,聚合物就会下降,所以要使用高纯度原材料,但在使用pet瓶等再生pet时,很难将粘在pet上的污染物质清理干净,获得的低聚物也就很难提炼出高纯度。
[0008]
所以,上述方法都是以有机溶剂作为反应溶剂,而后进行分解反应的方法,可适用于聚合度低、分子链状态相对松散的pet,但很难适用于pet瓶等因固相聚合和热定型(heatsetting)处理等大于iv=0.75dl/g的聚合度高且分子链紧密封装的产品。实际上,将pet瓶粉碎物质(矿泉水瓶、饮料瓶等混合粉碎物)按重量比进行混合,使固态物质占30%左右,用醇类溶剂在高压反应管中进行碱水解时,在3-5bar的反应压力和醇沸腾温度下进行回流并大力搅拌。即使如此进行一周的水解反应,仍有20%的pet残留物。尤其是饮料用耐热pet瓶等,其生产工艺中包含了比普通矿泉水瓶一次吹制强很多的热定型工艺,即二次吹制工艺,分子量高,加上到结晶化所需的分子链的紧密程度更高,所以比普通矿泉水瓶更难进行碱水解。这些物质还很难溶于测定petiv时使用的六氟异丙醇(hfip)和三氟乙酸(tfa)等强效溶剂,甚至会残留相当数量的未溶解物质,所以进行普通水解时,将产生更多的未分解残留物。这些残留物的表面被溶剂溶胀后,向糕一样凝聚在一起,粘在反应器的内壁和搅拌机上,结果可导致反应器无法工作,或堵住反应器的出料口,很难进行正常的出料。用作普通水解溶剂的醇类,如甲醇、乙醇等,即使有溶剂极性的差异,水解结果也类似,以单位%的水平添加溶胀用有机溶剂(dmso、ch2cl2)等,结果也并没有明显改善。
[0009]
可见,用已知方法水解高聚合度pet时,虽然部分表面开始水解,但由于聚合度高,无法进一步向内部分解,只在表面发生溶胀现象。表面变得向凝胶一样具有黏性以后,即使大力搅拌,pet碎片也会粘在一起,随着时间的推移会粘在反应器内壁和搅拌器等上,甚至连反应产物也会粘在上面,形成糕状硬块。其结果是酸、碱物质无法继续进一步渗透内部,分解反应速度大幅下降,无法进行正常反应。有一种最大限度减少这种现象的方法,那就是将pet尽量粉碎,但由于pet非结晶性高,常温下很难进行物理粉碎。尤其是pet瓶,很难粉碎成粉末状,所以尽量将其切成小碎片使用。一般来讲,用液氮超低温粉碎机或球磨机粉碎塑料制品,虽然结晶性高分子或硬度高的高分子的粉碎效果不错,但由于pet非结晶性程度高,所以很难粉碎。再加上对于高聚合pet来说,难度更大,从经济性角度来讲,这种粉碎方法毫无意义。
[0010]
由于上述理由,到目前为止,聚合度高的pet几乎无法实现经济实惠的化学性回收利用,目前主要的回收方式为清洗烘干后,通过单纯地熔融纺纱,做成填充棉或人造短纤维等低级的纤维。
[0011]
综上,聚合度高的pet的化学分解存在以下诸多问题:
[0012]
(1)传统方法中使用有毒且易燃的低沸点有机溶剂作为反应溶剂,为实现快速反应,还要进行加热加压反应。最普遍用于碱水解的溶剂有乙醇、甲醇等醇类,虽然程度不同,但对皮肤和眼睛均有毒性,且沸点低、挥发性强、易燃、蒸汽毒性强、有爆炸的危险。
[0013]
(2)eg解聚时,会产生对人体有害的环状低聚物、bht等物质,再次聚合成用于矿泉水、食品容器的pet时,可能会对健康造成威胁。具体地,添加dmso、ch2cl2等溶胀用有机溶剂进行水解时,反应后需要重新将这些物质分离,还因为副产物导致很难获得高纯度的单体产物。若要获得高纯度产品,需要高水平的提纯设备。另外,往往分解的最终产物不是tpa,
而是对苯二甲酸二甲酯(dmt),此时,将会生成包括tpa在内各种单体、低聚物等杂质。这种情况下几乎不可能提纯,更不能用作需要超高纯度的pet聚合原料。
[0014]
(3)更加关键的问题在于,iv=0.75dl/g以上的高聚合度pet很难发生(反应式1)的(a)、(b)、(c)的分解。iv=0.75dl/g以上的高聚合度pet中,最具代表性的产品就是pet矿泉水瓶;饮料用pet耐热瓶因结晶化程度更高,更难分解;对于需要更强机械性能的pet轮胎圈等高强力丝更是达到iv=1.0~1.2dl/g。
[0015]
鉴于此,特提出本发明。
技术实现要素:
[0016]
本发明的目的在于提供对苯二甲酸及其制备方法和回收高聚合度聚对苯二甲酸乙二醇酯的方法。本发明实施例提供的制备方法能够在不使用有机溶剂作为反应溶剂的基础上,能水解高聚合度的对苯二甲酸乙二醇酯,提高对苯二甲酸的产出率。特别是能够改善pet的经济性水解反应中,有关上述有机溶剂存在的安全性和低反应率的问题,尤其是要解决pet瓶等本身很难发生反应的高聚合度pet的低反应率等问题。
[0017]
本发明是这样实现的:
[0018]
第一方面,本发明提供一种对苯二甲酸的制备方法,包括:将熔融的高聚合度聚对苯二甲酸乙二醇酯、含有碱金属的强碱、所述碱金属的弱酸盐以及乙二醇混合进行无溶剂反应,所述乙二醇的用量低于所述高聚合度聚对苯二甲酸乙二醇酯的质量的10%。
[0019]
在可选的实施方式中,包括:将高聚合度聚对苯二甲酸乙二醇酯和含有碱金属的第一强碱混合熔融形成第一熔融液,而后将所述第一熔融液、含有碱金属的第二强碱、弱酸盐和乙二醇混合,接着,进行多阶段加热;
[0020]
其中,所述第一强碱的用量与所述高聚合度聚对苯二甲酸乙二醇酯的重量的5-10%所述第二强碱的用量为所述高聚合度聚对苯二甲酸乙二醇酯的2-2.5倍当量;所述弱酸盐的用量为所述高聚合度聚对苯二甲酸乙二醇酯的0.1-0.5倍当量;所述乙二醇的用量为所述高聚合度聚对苯二甲酸乙二醇酯的0.1-0.3倍当量。
[0021]
在可选的实施方式中,包括:将所述高聚合度聚对苯二甲酸乙二醇酯和所述第一强碱同时加入连续式挤出机内进行熔融形成所述第一熔融液,而后将所述第二强碱、所述弱酸盐和所述乙二醇的混合物加入所述第一熔融液所在的所述连续式挤出机的内部位置,接着,在所述连续式挤出机不同的反应区进行多阶段加热。
[0022]
在可选的实施方式中,形成第一熔融液的温度为100-180℃,加入所述混合物的温度为150-230℃;此时的温度并不是指混合物自身的温度,而是指加入所述混合物时,所述第一熔融液所在所述连续式挤出机的内部位置的温度为150-230℃;
[0023]
优选地,多阶段加热包括:在180-230℃的条件下进行加热后再在180-200℃的条件下进行加热,最后,在150-180℃的条件下进行加热;
[0024]
优选地,制备所述对苯二甲酸的整个过程中,压力不高于3个标准大气压,优选为2.5-3个标准大气压。
[0025]
在可选的实施方式中,包括:对无溶剂反应形成的碱金属对苯二酸盐进行后处理;
[0026]
优选地,后处理包括:将所述碱金属对苯二酸盐与水混合后过滤和离心,接着,加入酸。
[0027]
在可选的实施方式中,所述高聚合度聚对苯二甲酸乙二醇酯的聚合物大于在可选的实施方式中,所述高聚合度聚对苯二甲酸乙二醇酯的聚合物大于优选地,大于
[0028]
优选地,所述高聚合度聚对苯二甲酸乙二醇酯的聚合物选自均聚物或共聚物。
[0029]
在可选的实施方式中,所述碱金属选自锂、钠和钾中的任意一种。
[0030]
在可选的实施方式中,所述弱酸盐包括碳酸盐、碳酸氢盐、磷酸盐、磷酸氢盐、磷酸二氢盐、醋酸盐和甲酸盐中的任意一种。
[0031]
第二方面,本发明提供一种对苯二甲酸,其通过前述实施方式任一项所述的对苯二甲酸的制备方法制备得到。
[0032]
第三方面,本发明提供一种回收高聚合度聚对苯二甲酸乙二醇酯的方法,包括前述实施方式任一项所述的对苯二甲酸的制备方法。
[0033]
本发明具有以下有益效果:本发明无需使用有毒有机溶剂作为反应溶剂的情况下,通过无溶剂反应快速水解传统方法很难水解的以上的高聚合度pet,继而高产率和安全性地制备出高纯度的对苯二甲酸。
附图说明
[0034]
为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
[0035]
图1为本发明实施例提供的无溶剂反应的工艺原理图;
[0036]
图2为本发明实施例提供的挤出机的螺杆的形态截面图;
[0037]
图3为本发明实施例中使用的高聚合度pet的拉曼光谱仪光谱;
[0038]
图4为本发明实施例提供的对苯二甲酸钠盐的标准物质的拉曼光谱仪光谱;
[0039]
图5为本发明实施例提供的对苯二甲酸的标准物质的拉曼光谱仪光谱;
[0040]
图6为本发明实施例提供的实施例1中制备得到的对苯二甲酸钠盐的拉曼光谱仪光谱;
[0041]
图7为本发明实施例提供的实施例1中制备得到的对苯二甲酸的拉曼光谱仪光谱;
[0042]
图8为本发明实施例提供的比较例1中制备得到的对苯二甲酸钠盐的拉曼光谱仪光谱;
[0043]
图9为本发明实施例提供的比较例2中制备得到的对苯二甲酸钠盐的拉曼光谱仪光谱;
[0044]
图10为本发明实施例提供的比较例3中制备得到的对苯二甲酸钠盐的拉曼光谱仪光谱;
[0045]
图11为本发明实施例提供的比较例4中制备得到的对苯二甲酸钠盐的拉曼光谱仪光谱;
[0046]
图12为本发明实施例提供的比较例5中制备得到的对苯二甲酸的拉曼光谱仪光谱;
[0047]
图13为本发明实施例提供的比较例6中制备得到的对苯二甲酸钠盐的拉曼光谱仪
光谱;
[0048]
图14为本发明实施例提供的比较例7中制备得到的对苯二甲酸钠盐的拉曼光谱仪光谱;
[0049]
图15为本发明实施例提供的比较例8中制备得到的对苯二甲酸的拉曼光谱仪光谱;
[0050]
图16为本发明实施例提供的实施例2中制备得到的对苯二甲酸钾盐的拉曼光谱仪光谱;
[0051]
图17为本发明实施例提供的实施例2中制备得到的对苯二甲酸的拉曼光谱仪光谱;
[0052]
图18为本发明实施例提供的验证例2中500倍nasem-eds分布图;
[0053]
图19为本发明实施例提供的验证例1中500倍nasem-eds分布图;
[0054]
图20为本发明实施例提供的eg的温度和蒸气压相关关系的曲线图。
具体实施方式
[0055]
为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
[0056]
本发明实施例提供一种对苯二甲酸的制备方法,包括:将熔融的高聚合度聚对苯二甲酸乙二醇酯、含有碱金属的强碱、所述碱金属的弱酸盐以及乙二醇混合进行无溶剂反应,其中,乙二醇的用量低于所述高聚合度聚对苯二甲酸乙二醇酯的质量的10%。
[0057]
具体地,传统分解反应是向反应器中倒入乙醇或甲醇等有机溶剂等作为反应溶剂进行的分解反应,但是其存在诸多问题。本发明实施例将pet熔融,熔融的pet本身既是反应物质,又起到类似溶剂作用,而并未实际添加有机溶剂作为反应溶剂,继而进行无溶剂连续式分解反应。在使用熔融pet的基础上加入催化剂水平的乙二醇、含有碱金属的强碱、所述碱金属的弱酸盐。以naoh作为含有碱金属的强碱的例子,倒入naoh及其弱酸(碳酸)的盐(碳酸钠)。按照[反应式2]进行反应,pet水解后,生成对苯二酸双钠盐(tpa-na2)和乙二醇,同时na
+
的浓度逐渐降低,水解反应速度也逐渐减慢。但是,此时如果有na
+
的弱酸盐na2co3,它将会溶入eg内,产生更多的na
+
,加上naoh释放的na
+
浓度,na
+
的浓度会进一步提高,生成更多的nao-c2h
4-ona。借此防止pet水解反应导致的na
+
浓度降低,确保反应速度保持在较快水平。
[0058]
同时可知,本发明实施例中虽然添加有乙二醇,但是其并不是作为反应溶剂,若其最初便是作为反应溶剂,那么其用量应该达到高聚合度聚对苯二甲酸乙二醇酯的200%,在本发明实施例中上述添加量的乙二醇的功能不是溶解反应物质,而是一种催化剂。即,最初加入的eg与碱金属生成碱金属盐(例如,羟基乙酸钠),催化反应,使反应更加均匀且快速。另外,eg是pet分解反应产生的反应产物,其作用相当于降低未反应熔融pet黏度的稀释溶液,也并不是反应溶剂,因为这不是为了促进反应而从外部添加eg。若最初加入大量eg(即作为反应溶剂),反而因副反应出现酵解现象,反而会影响主反应。
[0059]
反应式2:
[0060]
na2co3→
2na+co
3-2
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(1)
[0061]
2naoh+ho-c2h
4-oh
→
nao-c2h4ona+2h2o
ꢀꢀ
(2)
[0062]
pet+naoc2h
4-ona
→
na-tpana+ho-c2h4oh
ꢀꢀ
(3)。
[0063]
本发明实施例采用的分解反应中并未使用易燃且对人体有害的有机溶剂作为反应溶剂,而是通过熔融的pet和含有碱金属的碱(如koh、naoh等),加上相当于催化剂的碱金属盐和乙二醇进行无溶剂反应。无溶剂反应的优点在于,没有那些与反应无关、只作为溶剂存在的有害化合物,在安全性、反应率和速度方面都有非常好的效果。
[0064]
从反应率方面来讲,没有反应溶剂导致的浓度稀释,反应物质之间直接发生反应(即,反应浓度为100%),所以反应速度比使用溶剂时要快,副反应少,杂质明显减少。但是会出现的问题是,进行此类无溶剂反应时,pet的熔融黏度远高于普通有机溶剂反应,所以很难在间歇反应器中混合反应物质。解决上述问题的一个非常有效的方法就是使用像挤出机这样的混合装置作为反应器。还有一点非常重要,那就是用挤出机进行反应时,可以通过降低反应温度和熔融黏度来提高反应率。
[0065]
具体地,本发明实施例中采用连续式挤出机进行熔融以及无溶剂反应等。该挤出机是最常见的连续反应器。挤出机可将其使用的螺杆组合成其他螺旋形式的东西。即,可按反应区的温度、压力等反应条件设定设备特性,而且由于是连续式,可以以小装置获得高产量。当然,使用高效率的双螺杆挤出机时,由于其更高的混合效率,可以比单螺杆挤出机更快反应,产率更高。
[0066]
进一步地,参见图1,该连续式挤出机具有5个反应区,在5个不同反应区添加不同物料和进行不同反应。首先,将高聚合度聚对苯二甲酸乙二醇酯送入挤出机形式的连续反应器中,即加入反应区1,然后进行加热加压,制备流动性聚对苯二甲酸乙二醇酯,即熔融高聚合度聚对苯二甲酸乙二醇酯。
[0067]
优选地,在加入高聚合度聚对苯二甲酸乙二醇酯的同时,加入含有碱金属的第一强碱,其中,第一强碱的用量与所述高聚合度聚对苯二甲酸乙二醇酯的重量的5-10%,高聚合度聚对苯二甲酸乙二醇酯的聚合物大于优选地,大于所述高聚合度聚对苯二甲酸乙二醇酯的聚合物选自均聚物或共聚物。
[0068]
此时,挤出机的螺杆并未采用整体相同的螺杆结构,而是如图2所示,采用符合各反应区特性的结构。采用符合反应区1(pet入料)-》反应区2(naoh混合)-》反应区3(1次反应)-》反应区4(2次反应)-》反应区5(出料)反应目的的结构。
[0069]
而后,将含有碱金属的第二强碱、弱酸盐和乙二醇的混合物加入所述第一熔融液所在的所述连续式挤出机的内部位置,即反应区2,继而在挤出机内使得熔融的聚对苯二甲酸乙二醇酯与上述混合物在所述连续式挤出机不同的反应区进行多阶段加热,以进行无溶剂反应,制备碱金属对苯二酸盐。
[0070]
为保持较低的反应温度,提高混合效果,本发明实施例采用分两次倒入碱的方法。首先,在将pet首次送入连续反应器(挤出机)时,混入少量的碱(例:naoh),就会发生1次水解反应,使得pet的平均分子量减少,熔融温度下降。同时与少量产生的eg混合,黏度进一步下降,使得反应条件更加温和,控制分解反应变得更加容易。然后,进行正式的分解反应,将包括碱金属的碱、上述碱金属的弱酸盐及乙二醇的混合物足量送入2次反应温度更低的连续反应器的混合区(反应区2)。即使送料量过多,但由于1次水解后pet黏度下降,混合也将
变得更加容易。即第二强碱、第一强碱和含有碱金属的强碱均为同一种强碱。只是将含有碱金属的强碱分两次,本发明实施例为了区分添加的时间,故而命名为第二强碱和第一强碱。
[0071]
进一步地,所述第二强碱的用量为所述高聚合度聚对苯二甲酸乙二醇酯的2-2.5倍当量;所述弱酸盐的用量为所述高聚合度聚对苯二甲酸乙二醇酯的0.1-0.5倍当量;所述乙二醇的用量为所述高聚合度聚对苯二甲酸乙二醇酯的0.1-0.3倍当量。碱金属选自锂、钠和钾中的任意一种。弱酸盐可以是碱金属和碳酸形成的碳酸盐或碳酸氢盐;可以是碱金属与磷酸形成的磷酸盐、磷酸氢盐或磷酸二氢盐;可以是碱金属与醋酸形成的醋酸盐,也可以是碱金属与甲酸形成的甲酸盐中的任意一种。强碱中的碱金属和弱酸盐中的碱金属为同一种碱金属。
[0072]
进一步地,设定挤出机内各反应区温度时,最需要考虑的是pet的热学特性,即玻璃化温度点(tg:70℃左右)、熔点(tm:普通250-260℃左右)、eg的沸点(b.p:197℃,1个标准大气压)等,如果产生了压力,这些温度自然与常温有所不同。
[0073]
各反应区详情如下:
[0074]
第一个反应区是pet入料区,输送过来的pet固体碎片在螺杆和块的热量和压力下转换成流动性物体,被向前推移。此时,如果仅送入pet,若要实现pet的流动化需要将温度提升至熔融温度,此时熔融黏度过高。为确保供应和流动化,在送入的pet中混入重量比为5-10%的碱在送入pet的同时进行1次水解反应,这样能降低熔点和黏度,使入料变得更容易。
[0075]
另外,挤出机螺杆的形式也很重要。一般来讲,投入原料的粒径越大,就用螺距更大的螺杆。为确保pet瓶碎片可顺利入料,使用普通pet碎片时,螺杆将采用更大的螺距。此时,pet供应区,即反应区1的起始温度保持在pet的玻璃化温度点(tg)和熔点(tm)之间,通常为100-180℃,使得pet在进行1次分解时熔融。这样才能确保在第二个混合区,即反应区2中可以和2次入料的碱充分混合。
[0076]
第二个反应区2是混合区。在这里,应设计为螺杆可以混合从入料区推过来的流动性pet和碱,并提高混合效率。首先,混合少量eg和略微大于当量比的碱(例:naoh、koh)及碱金属的弱酸盐(例:na2co3、k2co3等),制备混合物。这样一来,如以下(反应式3)所示,eg和碱moh(m:碱金属)发生反应,生成金属乙醇酸盐。另外,金属盐m2co3的一部分解离成m
+
离子和co
3-2
离子,这些离子全部处于混合状态。此时,m
+
离子的量比当量比多10-20%左右。
[0077]
反应式3:
[0078]
ho-ch2ch
2-oh+2m
+
+20h
‑→
mo-ch2ch
2-om+h2o
[0079][0080]
用齿轮泵或第2送料挤出机将所述混合物定量推入主挤出机的混合区,与流动性pet充分混合。在反应区2中,温度开始低于pettm,然后越来越低,到了反应区2的末端附近,使温度达到200℃左右。随着流动pet通过反应区1的末端流入反应区2时,pet的tm因1次水解而降低。这种温度因素和1次水解导致分子量减少,从而使得黏度下降,通过合理调节反应区2的温度,保持混合的切力,使得pet和混合物充分混合。在反应区2,两个反应物质混合,进一步发生了部分反应,但反应的完结将在第三个反应区3和第四个反应区4中完成,并采用可提高混合效率的螺杆结构。
na,进一步促进水解反应。
[0091]
图20是表示eg温度和蒸气压相关关系的曲线图,根据图20可知,若要使eg在特定温度下保持液态,需要比蒸气压更高的压力。例如,在1个标准大气压下eg的沸点是197℃,此时的蒸气压为760mmhg。在pet的熔融温度260℃下,蒸气压约为4000mmhg(约5.3个标准大气压),在这个温度下要使eg保持液态,则反应压力应保持在高于5.3个标准大气压的水平。
[0092]
而在实际工艺中,pet分解开始生成eg时,pet的分子量急剧减少,即使反应温度比260℃低20-30℃,pet也能保持熔融状态。但此时的eg蒸气压小于2000mmhg,故压力不用保持5.3个大气压以上的高压,只需保持2.5-3个标准大气压的反应压力,eg也能保持液态,从而保持快速的水解反应速度。因此,制备所述对苯二甲酸的整个过程中,压力不高于3个标准大气压,优选为2.5-3个标准大气压。
[0093]
无溶剂反应结束后,将形成的碱金属对苯二酸盐与水混合后过滤和离心,接着,加入酸进行反应,形成高纯度的对苯二酸。
[0094]
本发明实施例利用拉曼光谱仪确认此反应各过程的产物。拉曼光谱仪无需预处理过程就能直接测定固态样品的分子结构,从而直接确认本发明实施例各产物的反应程度。除此之外,用iv测定了pet的分子量变化,用sem-edx确定了碱金属(例如钠)的分布程度,以确认挤出机的混合性能。
[0095]
首先,测定了各阶段化合物的拉曼参照光谱。
[0096]
本发明实施例提供的反应经历pet
→
tpa-na
→
tpa的过程,最大分子结构变化的特点如下。
[0097]
pet最具代表性结构为苯环和酯羧基(estercarbonyl)c=o,如(图3)所示,在1601cm-1
处出现苯环峰值,在1714cm-1
处出现酯的大峰值。随着pet的酯键转换成tpa-na时,此峰值变小,由此可以判断pet的分解量。
[0098]
对苯二甲酸钠(tpa-na)由于酯结构分解,成为了羟酸钠c-o-na,如此转换以后,如(图4)所示,苯环峰值处在相同位置,但1714cm-1
处的酯峰值逐渐消失,1123cm-1
处的羟酸钠峰值逐渐增大。
[0099]
tpa出现如下特征:通过向tpa-na中倒入酸,h离子替换了na离子,最终成为羟酸-cooh。其结果如(图5)所示,1123cm-1
处的羟酸钠峰值消失,在823cm-1
处生成新的羟酸钠峰值,苯环峰值也略微位移,出现在1617cm-1
处。
[0100]
在这种基本拉曼光谱的基础上,对试验过程中得到的化合物进行比较确认。
[0101]
第二方面,本发明提供一种对苯二甲酸,其通过前述实施方式任一项所述的对苯二甲酸的制备方法制备得到。
[0102]
第三方面,本发明提供一种回收高聚合度聚对苯二甲酸乙二醇酯的方法,包括前述实施方式任一项所述的对苯二甲酸的制备方法。
[0103]
以下结合实施例对本发明的特征和性能作进一步的详细描述。
[0104]
实施例1
[0105]
本发明实施例提供一种对苯二甲酸的制备方法,包括:
[0106]
首先,制备对苯二甲酸钠盐:
[0107]
利用具有5个反应区(温度调节区)的双螺杆挤出机,充分混合大于iv=0.83dl/g的pet瓶碎片和重量比为5%的naoh,并将其送料,之后用第二阶挤出机将30%的naoh(相对
pet的质量)、5%的na2co3(相对pet的质量)与10%的eg(相对pet的质量)混合后制备混合物,将其送入挤出机反应区2,制备对苯二甲酸钠盐。
[0108]
双螺杆挤出机用电加热和水冷的方式调节温度,也可以通过真空清除产生的气体。螺杆的长度:直径之比为40:1。
[0109]
此时,反应区1、反应区2、反应区3、反应区4和反应区5的温度各设定为160℃、180℃、220℃、200℃和170℃。整个压力为3个标准大气压以下。调整螺杆的转数,使pet在挤出机内的停留时间为10分钟左右。
[0110]
将完成反应的对苯二甲酸钠进行冷却。对其进行检测,检测结果参见图6,根据图6可知,在1123cm-1
处出现大峰值,在1714cm-1
处的酯峰值大幅变小,只能看到痕迹。
[0111]
其次,制备对苯二甲酸;
[0112]
将上述制备得到的100g对苯二甲酸钠盐溶于1l的纯净水,通过搅拌使其完全溶解。约10分钟后,用滤纸过滤水溶液。将经滤纸过滤后的固体再次放入1l纯净水内,通过搅拌使其完全溶解。10分钟后再次用滤纸过滤,将未溶解部分的固体烘干后称重的结果为2g,这说明本实施例pet
→
tpa-na2的转换反应率为98%左右。将1l的2次过滤液和1l的1次过滤液合并在一起。在2l过滤液中混入少量盐酸,充分搅拌后测定酸度(ph值)。持续放入盐酸,直至溶液酸度呈弱酸性(ph=4.5左右)。然后会出现白色沉淀物,用滤纸过滤这些沉淀物,再用纯净水清洗2次后烘干,制备得到对苯二甲酸。
[0113]
对制备得到的对苯二甲酸进行检测,检测结果参见图7,与图5的标准物质tpa的拉曼光谱仪光谱进行比较,从结果可以看出烘干的白色沉淀物即为tpa。
[0114]
实施例2
[0115]
本发明实施例提供一种对苯二甲酸的制备方法,包括:
[0116]
首先,制备对苯二甲酸钾盐:
[0117]
利用双螺杆挤出机,充分混合大于iv=0.83dl/g的pet瓶碎片和重量比为5%的koh,将其第1次送料,之后使用第二阶挤出机,除了第2次送入的35%的koh(相对pet的质量)、5%的k2co3(相对pet的质量)与10%的eg(相对pet的质量)混合物外,采用与实施例1相同的方式制备对苯二甲酸钾盐。
[0118]
制备的对苯二甲酸钾盐的拉曼光谱仪光谱如图16所示。图16虽然和对苯二甲酸钠盐的拉曼光谱仪光谱几乎一样,但在峰值强度比等方面有一定差异。
[0119]
其次,制备对苯二甲酸;
[0120]
将上述制备得到的100g对苯二甲酸钾盐溶于1l的纯净水,通过搅拌使其完全溶解。约10分钟后,用滤纸过滤水溶液。将经滤纸过滤后的固体再次放入1l纯净水内,通过搅拌使其完全溶解。10分钟后再次用滤纸过滤,将未溶解部分的固体烘干后称重的结果为4g,这说明pet
→
tpa-k2的转换反应率为96%左右。将1l的2次过滤液和1l的1次过滤液合并在一起。在2l过滤液中混入少量盐酸,充分搅拌后测定酸度(ph值)。持续放入盐酸,直至溶液酸度呈弱酸性(ph=4.5左右)。然后会出现白色沉淀物,用滤纸过滤这些沉淀物,再用纯净水清洗2次后烘干,制备得到对苯二甲酸。
[0121]
制备得到的对苯二甲酸的拉曼光谱仪光谱如图17所示,与图5的标准物质tpa的拉曼光谱仪光谱进行比较,从结果可以看出烘干的白色沉淀物即为tpa。
[0122]
比较例1
[0123]
制备对苯二甲酸钠盐
[0124]
利用具有5个反应区(温度调节区)的双螺杆挤出机使iv=0.83dl/g的pet瓶碎片和naoh发生反应,制备对苯二甲酸钠盐(tpa-na2)。双螺杆挤出机用电加热和水冷的方式调节温度,也可以通过真空清除产生的气体。螺杆的长度:直径之比为40:1。
[0125]
将naoh以5%的重量比与pet碎片均匀混合,送入挤出机。此时,反应区1、反应区2、反应区3、反应区4和反应区5的温度各设定为160℃、180℃、220℃、200℃和170℃。调整螺杆的转数,使pet在挤出机内的停留时间为10分钟左右。
[0126]
将完成反应的对苯二甲酸钠进行冷却。制备的对苯二甲酸钠盐的iv测定结果为0.51dl/g,拉曼光谱仪光谱如图8所示。iv从0.83dl/g降至0.51dl/g,说明分解反应达到了一定的程度。另外,从图8的拉曼光谱仪光谱可以看出,1123cm-1
处出现了小峰值,这是因为pet部分分解,生成了对苯二甲酸钠盐(tpa-na2)。
[0127]
比较例2
[0128]
制备对苯二甲酸钠盐
[0129]
除了将混有iv=0.83dl/g的pet瓶碎片和重量比为15%的naoh的混合物送入双螺杆挤出机以外,采用与实施例1相同的方式制备对苯二甲酸钠盐。完成反应的对苯二甲酸钠盐的拉曼光谱仪光谱如图9所示。从图9可以看出,在1123cm-1
处出现了非常大的峰值,在1714cm-1
处的pet酯峰值几乎缩小至一半,小于1123cm-1
;两个峰值的强度(intensity)约为代表对苯二甲酸钠(tpa-na2)量的1123cm-1
处峰值的1.2倍。
[0130]
比较例3
[0131]
制备对苯二甲酸钠盐
[0132]
除了将混有iv=0.83dl/g的pet瓶碎片和重量比为30%的naoh的混合物送入双螺杆挤出机以外,采用与比较例1相同的方式制备对苯二甲酸钠盐。完成反应的对苯二甲酸钠盐的拉曼光谱仪光谱如图10所示。从图10可以看出,在1123cm-1
处出现了非常大的峰值,在1714cm-1
处的pet酯峰值大幅缩小,强度缩小为1123cm-1
处峰值的约1/16。
[0133]
比较例4
[0134]
制备对苯二甲酸钠盐
[0135]
利用双螺杆挤出机,充分混合大于iv=0.83dl/g的pet瓶碎片和重量比为5%的naoh,将其第1次送料,之后使用第二阶挤出机,除了第2次送入的30%的naoh与15%的eg混合物外,采用与实施例1相同的方式制备对苯二甲酸钠盐。完成反应的对苯二甲酸钠盐的拉曼光谱仪光谱如图11所示。从图11可以看出,在1123cm-1
处出现了非常大的峰值,在1714cm-1
处pet酯峰值大幅缩小,强度缩小为1123cm-1
处峰值的约1/18,但仍有未分解的pet。
[0136]
比较例5
[0137]
制备对苯二甲酸
[0138]
将比较例4中获得的100g对苯二甲酸钠盐溶于1l的纯净水,通过搅拌使其完全溶解。约10分钟后,用滤纸过滤水溶液。将经滤纸过滤后的固体再次放入1l纯净水内,通过搅拌使其完全溶解。10分钟后再次用滤纸过滤,将未溶解部分的固体烘干后称重的结果为13g,这说明pet
→
tpa-na的转换反应率为87%左右。将1l的2次过滤液和1l的1次过滤液合并在一起。在2l过滤液中混入少量盐酸,充分搅拌后测定酸度(ph值)。持续放入盐酸,直至溶液酸度呈弱酸性(ph=4.5左右)。然后会出现白色沉淀物,用滤纸过滤这些沉淀物,再用
纯净水清洗2次后烘干,制备得到对苯二甲酸。
[0139]
制备得到的对苯二甲酸的拉曼光谱仪光谱测定结果如图12所示。与图5的标准物质tpa的拉曼光谱仪光谱进行比较,从结果可以看出制备的白色固体物质即为tpa。
[0140]
比较例6
[0141]
用乙醇溶剂制备对苯二甲酸钠盐
[0142]
在1升的四口圆底烧杯上安装搅拌机、温度计、回流冷却器,并安装到加热罩上。加入iv=0.83dl/g的100克pet瓶碎片、30毫升乙二醇钠盐、40克氢氧化钠、600ml乙醇。将加热罩的温度升高,直至乙醇沸腾,启动搅拌机进行回流,进行约10小时的反应。反应后,用100目的筛子将反应液进行过滤,将未反应残留的pet瓶碎片过滤出来后,用纯净的100ml乙醇擦拭。将烘干未反应的物质后进行称重,结果为23g。这说明高聚合度pet分解反应率仅为77%左右。
[0143]
将已去除未反应pet碎片的含有白色沉淀物的乳白色反应液用滤纸过滤,获得白色沉淀物。将白色沉淀物用甲醇清洗3次后进行烘干,制备对苯二甲酸钠盐。
[0144]
将获得的对苯二甲酸钠盐溶于水,用拉曼光谱仪测定的光谱结果如图13所示。将其与图4的标准物质对苯二甲酸钠盐的拉曼光谱仪光谱进行比较,确认成分即为对苯二甲酸钠盐。
[0145]
比较例7
[0146]
用乙醇溶剂制备对苯二甲酸钠盐
[0147]
在1升的四口圆底烧杯上安装搅拌机、温度计、回流冷却器,并安装到加热罩上。加入iv=0.55dl/g的切细的100克光亮pet布碎片、30毫升乙二醇钠盐、40克氢氧化钠、600ml乙醇。将加热罩的温度升高,直至乙醇沸腾,启动搅拌机进行回流,进行约1小时的反应。反应后,用100目的筛子将反应液进行过滤,将未反应残留的pet瓶碎片过滤出来后,用纯净的100ml乙醇擦拭。完全没有过滤出未反应物质。这说明中低聚合度pet的分解反应率几乎为100%。
[0148]
将已去除未反应物的含有白色沉淀物的乳白色反应液用滤纸过滤,获得白色沉淀。将白色沉淀物用甲醇清洗3次后进行烘干,制备对苯二甲酸钠盐。
[0149]
将获得的对苯二甲酸钠盐溶于水,用拉曼光谱仪测定的光谱结果如图14所示。将其与图4的标准物质对苯二甲酸钠盐的拉曼光谱仪光谱进行比较,确认成分即为对苯二甲酸钠盐。
[0150]
比较例8
[0151]
制备对苯二甲酸
[0152]
将在比较例7中获得的100g对苯二甲酸钠倒入2升的烧杯中,倒入1.5升蒸馏水,进行搅拌使其完全溶解。然后,一点点加入盐酸并充分搅拌,直至溶液呈弱酸性(ph=4.5左右)。然后会出现白色沉淀。用滤纸过滤这些沉淀物后烘干,制备对苯二甲酸。
[0153]
制备的对苯二甲酸的拉曼光谱仪光谱如图15所示,与图5的标准物质的拉曼光谱仪光谱进行比较,确认成分是对苯二甲酸。
[0154]
验证例1
[0155]
使用nacl确认碱粉末混合程度的确认试验
[0156]
在与实施例1相同的试验条件下,将重量比为10%的nacl粉末与pet混合。将排出
物进行常温冷却,凝固后,在500倍时测定的sem-eds结果如图19所示,图片上na(天蓝色)和来自pet的c(红色)元素充分混合,无大结块,这说明nacl的粉末均匀分布。这表明,在pet送料时,第1次先少量混合投入总量naoh中的一部分,再进行第2次送料,即渐进式水解反应,可使pet黏度缓慢下降,混合更加均匀。这说明了为什么将naoh分两次添加比一次性添加的反应更均匀、更好。
[0157]
验证例2
[0158]
使用nacl确认碱粉末混合程度的确认实验
[0159]
与比较例3相同的反应条件下,将重量比为10%的nacl粉末与pet混合。将排出物冷却至常温,在500倍时测量sem-eds的结果如图18所示。来自nacl的na(绿色)和来自pet的c(红色)元素并未充分混合,有很多块状物。这是因为一次投入过多naoh导致水解反应过于剧烈,各位置pet黏度差大,变化不均匀,这说明nacl的粉末分布不均匀。这说明,在实验中使用的双螺杆挤出机运行条件下,一次性送入naoh时,在混合过程中的混合并不充分。
[0160]
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1