一类抗细菌多肽及其应用
1.本发明公开一类抗细菌多肽及其应用,属于医药技术应用领域。
背景技术:
2.抗生素的滥用引起了较为严重的细菌耐药现象,新药的研制却远远赶不上细菌产生耐药的速度。如今,抗菌肽(amps)被发现为一种具有独特抗菌活性,并且不易产生耐药性的理想抗生素替代物。然而抗菌肽在生理环境中不易保持稳定,容易被降解,并且大部分抗菌肽存在着一定的细胞毒性。这些都限制了抗菌肽的应用。
3.目前对amps的抗菌机理有多种看法,其中最被大家认可的一种是其可对细菌细胞膜进行破坏、裂解,以致细菌最终的死亡。amps通常有很高的碱性氨基酸残基(如赖氨酸、精氨酸)含量,因此在生理环境下通常显正电性(但由于其也含疏水链段,整体呈两亲性)﹔而细菌的表面由于磷壁酸或脂多糖等分子的存在而呈负电。因此amps可以通过静电作用与细菌结合,并与细胞膜发生作用,提高细胞膜的通透性,使胞内物质流失以致细菌最终死亡。
技术实现要素:
4.本发明主要目的在于发明一种安全、高效的抗细菌多肽。
5.本发明针对革兰氏阴性菌和革兰氏阳性菌均有着抗菌活性,该类多肽对于革兰氏阴性菌有着更好的抗菌活性。
6.本发明的目的通过如下技术实现:
7.本发明经过一些设计步骤:(1)设计序列为cin(ikki)min,m为2~3,n为0~1;(2)对其亲水部分赖氨酸k进行移动变换,k总数量不变为6个不变;(3)在序列前端半胱氨酸后或尾c-端增加亲油的异亮氨酸i,0~1个;(4)c-端采用酰胺化修饰,n-端采用半胱氨酸修饰。
8.经筛选,本抗细菌多肽为如下氨基酸序列:m4:ckki(ikki)2i-nh2;m5:c(ikki)3i-nh2;m6:ci(ikki)
3-nh2;m7:ci(ikki)3i-nh2。
9.本发明提供的多肽序列编码也在本发明的保护范围。
10.相较于现有技术,本发明的抗细菌多肽有如下优点:该cin(ikki)min系列抗细菌多肽对革兰氏阴性菌和革兰氏阳性菌,所述为大肠杆菌以及金黄色葡萄球菌均具有抑制和杀灭效果,尤其对大肠杆菌更为显著,具有良好的应用前景。且2个(ikki)序列和3个(ikki)序列对革兰氏阴性菌并无太大抗菌效果差异。半胱氨酸(cys)后或c端增加一个亲油异亮氨酸(i)能增强多肽的抗菌效果,只在c端增加一个i比在cys后增加i拥有更好的抗菌效果。
11.本发明的多肽可以用做制备抗菌药物(抗细菌的抑制剂,例如抗革兰氏阴性菌的抑制剂或抗革兰氏阳性菌的抑制剂),更具体的是制备大肠杆菌和金黄色葡萄球菌的抑制剂。
附图说明
12.下面结合附图与具体实施方式对本发明作进一步详细的说明。以m4为例:
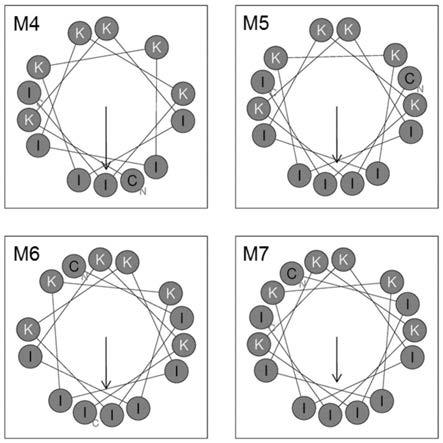
13.图1为本发明抗菌肽m4、m5、m6和m7的氨基酸分布图;
14.图2为本发明抗菌肽m4、m5、m6和m7的液相色谱图;
15.图3为本发明抗菌肽m4、m5、m6和m7的质谱图;
16.图4为本发明抗菌肽m4、m5、m6和m7对大肠杆菌(atcc 25922)的抗菌活性;
17.图5为本发明抗菌肽m4、m5、m6和m7对金黄色葡萄球菌(atcc 25923)的抗菌活性;
18.图6为本发明抗菌肽m4的溶血活性。
具体实施方式
19.本发明不局限于下列具体实施方式,本领域一般技术人员根据本发明公开的内容,可以采用其他多种具体实施方式实施本发明的,或者凡是采用本发明的设计结构和思路,做简单变化或更改的,都落入本发明的保护范围。需要说明的是,在不冲突的情况下,本发明中的实施例及实施例中的特征可以相互组合。
20.下面结合具体实施例对本发明做进一步详细的说明。
21.本发明所用实验药品均可通过商业渠道购买得到,下面对本发明所用部分实验仪器的型号及规格进行说明;
22.分析天平;细菌培养摇床;细菌培养箱;冷冻离心机;多功能酶标仪;本发明设计中用到的的抗菌肽由上海生工制备合成,采用fmoc固相合成法。其通过在rink酰胺mbha树脂上合成,纯度在96%以上。大肠杆菌atcc 25922和金黄色葡萄球菌atcc 25923由常州第二人民医院馈赠。
23.实施方式1
24.抗细菌多肽的设计:
25.一类抗菌肽的设计步骤:(1)设计基础序列为cin(ikki)min,m为2~3,n为0~1;(2)亲水区赖氨酸k总数量不变,为6个;(3)在半胱氨酸后或c-端增加亲油的异亮氨酸i,0~1个;(4)c-端采用酰胺化修饰,n-端采用半胱氨酸修饰。
26.表1氨基酸序列
[0027][0028][0029]
抗菌肽m4的电荷数为+6,疏水性为0.492;m5的电荷数为+6,疏水性为0.586;m6的电荷数为+6,疏水性为0.586;m7的电荷数为+6,疏水性为0.667。
[0030]
图2为抗菌肽m4、m5、m6、m7的液相色谱图。肽m4的纯度为96.43%,肽m5的纯度为98.9%,肽m6的纯度为98.64%,肽m7的纯度为98.64%。
[0031]
图3为抗菌肽m4、m5、m6、m7的质谱图。
[0032]
实施方式2
[0033]
抗细菌多肽最低抑菌浓度(mic)的测定:
[0034]
最低抑菌浓度(mic)的测定参照clsi的标准方法进行。将菌株的单菌落用接种棒挑至lb液体培养基中,放置在37℃,160rpm的恒温振荡培养箱中过夜培养,然后将其制备104cfu/ml的菌液。在96孔板中加入100μl菌液,将抗菌肽通过2倍倍比稀释法对抗菌肽进行稀释,在每孔中加入100μl的抗菌肽,使其终浓度分别为50、25、12.5、6.2、3.1和1.6μmol,阴性对照组将100μl的抗菌肽溶液替换成等量的lb液体培养基,空白对照组为无菌的lb液体培养基。每个处理三个平行样。将96孔板放置在37℃,160rpm的恒温振荡培养箱中培养24h,直到阴性对照孔中有肉眼可见的浑浊液出现。能够完全抑制细菌生长的抗菌肽浓度(孔为澄清)即为抗菌肽对该菌的mic值。
[0035]
图4中可以看出,抗菌肽m4对大肠杆菌的mic值为3.1μm,抗菌肽m5对大肠杆菌的mic值为1.6μm,抗菌肽m6对大肠杆菌的mic值为3.1μm,抗菌肽m7对大肠杆菌的mic值为3.1μm。抗菌肽m4、m5、m6、m7对大肠杆菌有显著的抑制效果。
[0036]
图5中可以看出,抗菌肽m4对金黄色葡萄球菌的mic值为50μm,抗菌肽m5对金黄色葡萄球菌的mic值为25μm,抗菌肽m6对金黄色葡萄球菌的mic值为50μm,抗菌肽m7对金黄色葡萄球菌的mic值为25μm。抗菌肽m4、m5、m6、m7对金黄色葡萄球菌有较好的抑制效果。
[0037]
该类抗菌肽对于革兰氏阴性菌有着更好的抗菌活性。
[0038]
实验方式3
[0039]
抗细菌多肽的溶血活性测定:
[0040]
一般用对红细胞的溶血活性来评价抗菌剂对正常哺乳动物细胞的杀伤作用。采集志愿者的新鲜血液中加入抗凝剂。将血液转移至离心管中,在4℃下,3000rpm,3min的离心条件弃去上层血清,留下红细胞沉淀。用等量的pbs溶液对红细胞进行离心清洗三次,除去残留的血清。将离心清洗后的红细胞用pbs溶液进行稀释至8%(v/v)。取100μl红细胞溶液至离心管中,再加入一系列2倍稀释梯度的aunr@c-at5溶液。用100μl的pbs作为实验的阴性对照,用100μl 0.1%triton x-100溶液作为实验的阳性对照。将离心管放置在37℃,160rpm的恒温摇床中进行孵育1h。在反应结束后,在4℃下,3000rpm,离心3min,使得红细胞沉淀。吸取离心管中上层清液至96孔板中,酶标仪检测540nm处的吸光度,溶血率按下列公式计算:
[0041]
溶血率(%)=(abs
肽-abs
pbs
)/(abs
0.1%triton x-100-abs
aunr@c-at5
)
×
100%。
[0042]
结果如图6所示,抗菌肽m4在浓度为50μm时溶血活性在3.65%,当溶血率大于5%时则视为溶血。但是m4在e.coli与s.aureus抗菌试验中分别在3.1μm和50μm时就已经做到抑菌,此时并未出现溶血现象。表明m4可在较低浓度下进行抗菌试验,说明本抗菌肽具有较好的生物相容性。
[0043]
以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,根据本发明的技术方案及其构思加以等同替换或改变,都应涵盖在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1