一种烯基硼酸酯化合物的合成方法
1.本发明涉及一种烯基硼酸酯化合物的合成方法,通过对苯乙炔类化合物进行选择性的 c-h键的硼化来合成反式烯烃硼酸酯化合物,属于有机合成领域。
背景技术:
2.烯基硼酸酯是有机合成中高度通用的构建单元,因为它们在构建c-c键和c-杂原子键方面具有广泛的应用,常见于药物设计、合成生物活性分子和功能材料中。
3.炔烃的硼氢化是合成这些硼酸酯化合物的直接方法。但是,由铜催化炔烃与二硼酸频哪醇或其他过程反应,通常会产生β-乙烯基(频哪醇)硼。其他类型的乙烯基硼酸酯的制备方法,如β-乙烯基(新戊基乙醇酸根)硼的制备方法相对有限,一般需要多步转化。由于缺乏β乙烯基(新戊基乙醇酸根)硼的制备方法,很少对其进行研究。因此,本研究开发的通过低负载钯催化从炔烃直接制备烯基硼酸酯的方法具有重要意义。
4.参考文献:
5.[1]miyaura,n.;suzuki,a.chem.rev.1995,95,2457.
[0006]
[2]meng,f.;mcgrath,k.p.;hoveyda,a.h.nature 2014,513,367.
[0007]
[3]molander,g.a.;ellis,n.m.acc.chem.res.2007,40,275.
[0008]
[4]d.g.hall(ed.),2nd ed.,wiley-vch,weinheim,germany,2011.
[0009]
[5]h.c.brown and s.k.gupta,j.am.chem.soc.1972,94,4370.
[0010]
[6]h.jang,a.r.zhugralin,y.lee,a.h.hoveyda,j.am.chem.soc.2011,133,7859
–
7871.
[0011]
[7]d.p.ojha,k.r.prabhu.org.lett.2016,18,432-435.
[0012]
[8]m.magre,b.maity,a.falconnet,l.cavallo,m.angew.chem.int.ed.2019,58,1
–7[0013]
[9]j.v.obligacion,j.m.neely,a.n.yazdani,i.pappas,p.j.j.am.chem.soc.2015,137, 5855-5858.
[0014]
[10]liu x.-w.,echavarren j.,zarate c.,martin r.j.am.chem.soc.2015,137(39), 12470
–
12473.
[0015]
[11]tobisu m.,shimasaki t.,chatani.angew.chem.int.ed.2008,47(26),4866
–
4869.
技术实现要素:
[0016]
本发明针对现有合成路线的缺点,提供了一种烯基硼酸酯化合物的合成方法,使用低负载的钯含量即可催化炔烃的硼氢化反应,且不需要高温环境,具有原料易得、工艺简单、条件温和、产率比较高、底物范围广、副产物比较少等优点。
[0017]
本发明烯基硼酸酯化合物的合成方法,是以苯乙炔类化合物为原料,在催化剂、碱以及硼试剂的存在下进行反应,分离提纯后得到烯基硼酸酯化合物。
[0018]
具体是将苯乙炔类化合物在75℃、氩气保护条件下溶于溶剂中,在催化剂、碱以及硼试剂的存在下进行反应,反应结束后分离提纯得到目标产物。
[0019]
所述苯乙炔类化合物的结构式为:
[0020][0021]
其中:r为cl、ph、f、噻吩基团或萘基团。
[0022]
本发明合成方法的反应温度为60-150℃,优选为75℃,反应时间为2-10h。
[0023]
所述催化剂为氯钯酸钠、双(二亚苄基丙酮)钯、四(三苯基膦)钯、(1,3-双二苯基磷丙烷)钯、二(乙酰丙酮)钯、氯化钯、三氟乙酸钯、双三苯基膦二氯化钯、醋酸钯、二氯二(三环己基磷)钯、[1,1
’‑
双(二苯基磷基)二茂铁]二氯化钯中的至少一种,催化剂的添加量为100ppm-1倍当量(以苯乙炔烃计)。
[0024]
所述碱为叔丁基醇钾、叔丁基醇锂、叔丁基醇钠、乙酸钾、氢氧化钠、1,8-二氮杂二环十一碳-7-烯、吡啶、甲醇锂、甲醇钠、碳酸铯、碳酸钾中的至少一种,添加量为1-3倍当量(以苯乙炔烃计)。
[0025]
所述硼试剂为联硼酸频那醇酯、频那醇硼烷、双联邻苯二酚硼酸酯、双(新戊基乙二醇) 二硼中的至少一种,硼试剂的添加量为1-4倍当量(以苯乙炔烃计)。
[0026]
所述溶剂为乙腈、二氯甲烷、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺、1,4-二氧六环、甲醇、甲苯、丙酮、二甲亚砜、二乙二醇二甲醚、乙酸乙酯或四氢呋喃。
[0027]
所述分离提纯是向反应液中加入水,用乙酸乙酯萃取,无水硫酸钠干燥,最后利用旋蒸除去溶剂,通过柱层析分离纯化,柱层析分离纯化时的洗脱液为石油醚:乙酸乙酯=20:1~100:1,v/v,即可得到目标产物。
[0028]
本发明反应过程如下:
[0029][0030]
本发明的有益效果体现在:
[0031]
1、本发明的合成方法条件温和反应时间比较短,操作简便安全,有害金属含量低。
[0032]
2、本发明的合成方法底物适用性广,产率比较高,副产物比较少,能兼容多种官能团,适用于多种取代基的烯基硼酸酯。
具体实施方式
[0033]
为进一步阐述本发明的特征和优点,下面结合具体的实施例对本发明的技术方案进行描述。但下列实施例仅为了进一步说明本发明,而不是限制本发明。
[0034]
实施例1:
[0035][0036]
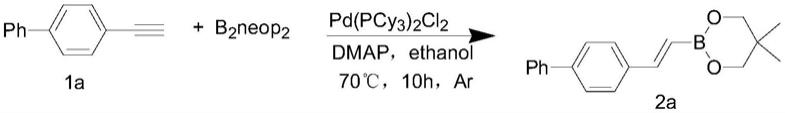
向将联硼酸新戊二醇酯(0.30mmol,1.5equiv)、4-二甲氨基吡啶(0.60mmol,
3.0equiv) 放入装有搅拌子的透明schlenk管中,管子抽真空,然后鼓入氩气,重复3-4次。在氩气氛围下添加联苯乙炔(1a)(0.20mmol,1.0equiv)、pd(pcy3)2cl2(400ppm)和溶剂(乙醇,3ml),将反应混合物在70℃下搅拌10小时;反应结束后冷却至室温,用水淬灭并用乙酸乙酯萃取,合并有机层,经硫酸钠干燥,然后真空浓缩,产物通过硅胶快速柱色谱法纯化(石油醚/乙酸乙酯=20:1)得无色油(2a)(44mg,75%)。该化合物的核磁数据为:1h nmr(600mhz,cdcl3) δ7.59(d,j=8.1hz,2h),7.56(d,j=2.6hz,3h),7.43(t,j=7.7hz,2h),7.37(d,j=18.3hz, 1h),7.33(t,j=7.4hz,1h),6.14(d,j=18.3hz,1h),3.71(s,4h),1.01(s,6h).
13
c nmr(151 mhz,cdcl3)δ146.69,141.33,140.76,136.91,128.86,127.53,127.46,127.31,127.06,72.40, 31.88,21.83.
11
b nmr(193mhz,cdcl3)δ25.31.
[0037]
实施例2:
[0038][0039]
表1低浓度金属催化的炔烃氢化硼化
[0040][0041][0042]
针对上述反应,我们以4-乙炔基-1,1'-联苯(1)和联硼酸新戊二醇酯(2)为模型底物,邻二甲苯为溶剂,醋酸钾为碱,通过筛选适宜的400ppm浓度的金属催化剂来实现炔烃的氢化硼化反应。开始进行廉价金属的尝试,400ppm(0.04mol%)的氯化镍,或者其与多种膦配体组合(pph3,pcy3,xantphos)也能提供较低产率的目标产物,但副产物较多。400ppm(0.04 mol%)的氯化亚铜与菲罗啉配体(1,10-ph,nc)组合不能提供目标产物,400ppm(0.04mol%) 的氯化亚铜与膦配体组合(pph3,pcy3,sphos,xphos,5mol%)能提供较低产率的目标产物,但反应比较杂。令人兴奋的是,400ppm的pd(pcy3)2cl2可以提供60%的目标产物,并且副产物少。与前几种转化相比,此种转化ppm浓度廉价金属也可以催化,但与钯催化
剂相比副反应较多。
[0043]
实施例3:
[0044][0045]
表2炔烃氢化硼化的碱的优化
[0046]
entrybaseyield(%)b1ch3cook602ch3coona503na2co3254k2co3305cs2co3156kbf4trace7koh338naohtrace9dmap6510dabco1011tea2212dbu55
[0047]
筛选出适宜的催化剂后,对碱进行了筛选。三个当量的醋酸钠可以提供的50%的目标产物。碳酸钠、碳酸钾、碳酸铯能提供较低产率的目标产物(25%,30%,15%),氢氧化钾可以提供33%的目标产物,氢氧化钠也不能提供目标产物。有机碱也进行了考察,三乙胺能提供22%的目标产物,1,8-二氮杂双环[5.4.0]十一碳-7-烯可以提供的55%的目标产物。三乙烯二胺可以提供10%的目标产物,4-二甲氨基吡啶的效果最好,可以提供65%的目标产物。
[0048]
实施例4:
[0049][0050]
表3炔烃氢化硼化的溶剂优化
[0051]
entrysloventyield(%)b1o-xylene652toluene603cyclohexane254dce05mecn18
6ea57etoh(95%)75
[0052]
筛选出适宜的催化剂、碱,接着对溶剂也进行了筛选。邻二甲苯和甲苯可以分别提供65%和60%的目标产物,环己烷,乙腈和乙酸乙酯可以提供较低产率的目标产物(25%,18%,5%),1,2-二氯乙烷不能提供目标产物,乙醇是此反应的最佳溶剂,在最优条件下可以提供75%的目标产物。
[0053]
实施例5:
[0054][0055]
表4低浓度钯催化的炔烃氢化硼化
[0056]
entrycatalyst(400ppm)yield(%)b1pd(oac)2242pdcl2203pd2(dba)3414pd(pph3)4235pd(dppf)cl2156pd(oac)2/pph3407pd(oac)2/xantphos108pd(oac)2/binap309pd(oac)2/dave-phos3610pd(oac)2/
t
buxphos3011pd(oac)2/ruphos3512pd(oac)2/pcy35213pd(pcy3)2cl275
[0057]
在上文研究基础上,我们又进一步考察了多种商品化的钯,在这种低浓度金属催化反应上的表现。400ppm的醋酸钯,氯化钯,三二亚苄基丙酮二钯可以提供较低产率的目标产物 (24%,20%,41%)。四(三苯基膦)钯可以提供23%的目标产物,1,1'-双二苯基膦二茂铁二氯化钯能提供15%的目标产物。在400ppm的醋酸钯为前催化剂的条件下,多种膦配体的作用也进行了考察(5mol%的配体),pph3可以提供40%的目标产物,dave-phos可以提供36%的目标产物,ruphos,pcy3可以分别提供35%和52%的目标产物。xantphos,binap, t
buxphos能提供较低产率目标产物(10%,30%,30%)。pd(oac)2/pcy3能提供52%的目标产物,经过筛选pd(pcy3)2cl2的效果最好,75%的目标产物。
[0058]
实施例6:
[0059]
[0060]
用苯乙炔(1b)代替联苯乙炔(1a),其他同实施例1。产物通过硅胶快速柱色谱法纯化(石油醚/乙酸乙酯=20:1)得无色油(2b)(26mg,60%)。该化合物的核磁数据为:1h nmr (600mhz,cdcl3)δ7.49(d,j=7.0hz,2h),7.34(d,j=7.5hz,1h),7.33
–
7.31(m,2h),7.27(d, j=7.3hz,1h),6.11(d,j=18.3hz,1h),3.70(s,4h),1.00(s,6h).
13
c nmr(151mhz,cdcl3)δ 147.22(s),137.89(s),128.60(s),127.08(s),111.81(s),72.16(s),31.94(s),21.96(s).
11
b nmr (193mhz,cdcl3)δ25.43(s).
[0061]
实施例7:
[0062][0063]
用3-甲基苯乙炔(1c)代替联苯乙炔(1a),其他同实施例1。产物通过硅胶快速柱色谱法纯化(石油醚/乙酸乙酯=20:1)得无色油(2c)(28mg,61%)该化合物的核磁数据为:1h nmr(600mhz,cd3cocd3)δ7.32(s,1h),7.29(d,j=7.7hz,1h),7.24(d,j=18.3hz,1h), 7.21(t,j=7.6hz,1h),7.09(d,j=7.5hz,1h),6.04(d,j=18.2hz,1h),3.66(s,4h),2.30(s, 3h),0.95(s,2h).
13
c nmr(151mhz,cd3cocd3)δ147.01,138.05,137.90,129.30,128.52, 127.53,124.10,71.68,31.54,21.07,20.51.
11
b nmr(128mhz,cd3cocd3)δ25.31
[0064]
实施例8:
[0065][0066]
用4-氨基苯乙炔(1d)代替联苯乙炔(1a),其他同实施例1。产物通过硅胶快速柱色谱法纯化(石油醚/乙酸乙酯=20:1)得无色油(2d)(21mg,45%)。该化合物的核磁数据为:1h nmr(600mhz,cd3cocd3)δ7.22(d,j=8.4hz,2h),7.15(d,j=18.2hz,1h),6.61(d,j=8.5hz,2h),5.72(d,j=18.2hz,1h),4.83(s,2h),3.63(s,4h),0.94(s,6h).
13
c nmr(151mhz, cd3cocd3)δ149.42,147.53,128.24,126.82,114.13,71.62,31.54,21.11.
11
b nmr(193mhz, cd3cocd3)δ25.48.
[0067]
实施例9:
[0068][0069]
用4-氟苯乙炔(1e)代替联苯乙炔(1a),其他同实施例1。产物通过硅胶快速柱色谱法纯化(石油醚/乙酸乙酯=20:1)得无色油(2e)(30.5mg,65%)。该化合物的核磁数据为:1h nmr(400mhz,cd3cocd3)δ7.55(m,2h),7.25(d,j=18.3hz,1h),7.09(m,2h),5.99(d, j=18.3hz,1h),3.67(s,4h),0.95(s,6h).
13
c nmr(101mhz,cd3cocd3)δ169.38,166.93, 150.64,139.66,134.06,120.48,76.89,36.75,26.25.
11
b nmr(128mhz,cd3cocd3)δ30.48.
[0070]
实施例10:
[0071][0072]
用4-甲氧羰基基苯乙炔(1f)代替联苯乙炔(1a),其他同实施例1。产物通过硅胶快速柱色谱法纯化(石油醚/乙酸乙酯=20:1)得无色油(2f)(27.5mg,50%)。该化合物的核磁数据为:1h nmr(600mhz,cd3cocd3)δ7.96(d,j=8.4hz,2h),7.63(d,j=8.3hz,2h),7.31(d, j=18.3hz,1h),6.21(d,j=18.3hz,1h),3.85(s,3h),3.68(s,4h),0.96(s,6h).
13
c nmr(151 mhz,cd3cocd3)δ166.08,145.48,142.23,130.02,129.72,126.92,71.73,51.48,31.54, 21.02.
11
b nmr(193mhz,cd3cocd3)δ25.23.
[0073]
实施例11:
[0074][0075]
用4-氰基苯乙炔(1g)代替联苯乙炔(1a),其他同实施例1。产物通过硅胶快速柱色谱法纯化(石油醚/乙酸乙酯=20:1)得无色油(2g)(30.5mg,63%)。该化合物的核磁数据为:1h nmr(400mhz,cd3cocd3)δ7.74
–
7.67(m,4h),7.28(d,j=18.2hz,1h),6.25(d,j=18.3hz,1h),3.67(s,4h),0.95(s,6h).
13
c nmr(101mhz,cd3cocd3)δ132.49,132.01, 129.10,128.41,127.56,118.53,71.77,31.58,21.06.
11
b nmr(128mhz,cd3cocd3)δ25.02.
[0076]
实施例12:
[0077][0078]
用4-硝基苯乙炔(1h)代替联苯乙炔(1a),其他同实施例1。产物通过硅胶快速柱色谱法纯化(石油醚/乙酸乙酯=20:1)得无色油(2h)(18.5mg,35%)。该化合物的核磁数据为:1h nmr(400mhz,cd3cocd3)δ7.84
–
7.61(m,4h),7.29(d,j=18.3hz,1h),6.24(d,j=18.3hz),3.69(s,4h),0.96(s,6h).
13
c nmr(101mhz,cd3cocd3)δ144.85,142.18,132.54, 127.60,118.48,111.66,71.70,31.55,20.97.
11
b nmr(128mhz,cd3cocd3)δ25.12。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1