冠状病毒抗体
冠状病毒抗体
1.本发明涉及抗体,并且特别地涉及在冠状病毒感染的诊断和治疗中所用的抗体。本发明延伸到包含抗体的组合物,包括药物组合物、诊断组合物和试剂盒。本发明也延伸到例如,在冠状病毒感染的诊断和治疗中制备和使用抗体的方法。
2.引起新型冠状病毒ncov或冠状病毒covid疾病的严重急性呼吸综合征冠状病毒(sars-cov-2)是属于致病病原体的冠状病毒(cov)组的病毒,该组的病毒包括严重急性呼吸综合征冠状病毒(sars)和中东呼吸综合征相关冠状病毒(mers)。冠状病毒通常限于其野生宿主(例如,蝙蝠)。然而,sars和mers,以及最近的sars-cov-2均已转移到人类,并且这分别地引起sars和mers爆发。
3.最近已在大量新出现的病原体优先级列表,即,ukvn、who蓝图和cepi中鉴定了冠状病毒家族,强调了提高我们对冠状病毒免疫应答的理解的迫切需要,以控制当前问题,并为新出现的威胁做好准备。大量的基因上不同的冠状病毒和cov的人类群体与动物贮主之间增加的界面表明,存在新的cov人畜共患感染的显著风险。实际上,sars-cov-2的爆发已经证明是这种情况。冠状病毒倾向于靶向呼吸系统,因此,由于这些周期的爆发,迫切地需要有效地靶向冠状病毒的治疗。此外,还需要改进的加强的检测方法。
4.对于人cov感染,无可用的特异性治疗。然而,越来越多地引入单克隆抗体(mab)作为抗癌症和病毒感染的免疫疗法的治疗。虽然它们可以具有免疫调节能力,但是在病毒感染(例如,hiv、hbv、hbc以及埃博拉(ebola))中,由于它们以高特异性结合病毒进入宿主细胞所需的病毒表面抗原的能力,它们主要用作中和剂。抗病毒的mab可以直接地减弱病毒繁殖,并且在一些情况下,接合宿主的免疫系统,导致持久的保护性疫苗样作用。然而,由于cov的高度多样化性质,从患者分离的大多数人mab是毒株特异性的,并且迄今为止尚未鉴定到广泛地中和抗体。
5.因此,用于高致病性cov的基于cov-mab的免疫疗法的研发将致力于解决立即未满足的医学需要,并且可以证明快速诊断和治疗,不仅用于当前的sars-cov-2,而且还用于未来新出现的大流行性cov。
6.因此,在本发明的第一方面,提供了结合严重急性呼吸综合征冠状病毒(sars-cov)、中东呼吸综合征相关冠状病毒(mers-cov)和/或严重急性呼吸综合征冠状病毒2(sars-cov-2)的刺突蛋白s2结构域的抗体或其抗原结合片段。
7.实施例中所描述的数据表明:本发明的抗体通过结合刺突蛋白的s2结构域,展示了与多种冠状病毒株的令人惊讶地加强的交叉反应性。此外,令人惊讶地,这些抗体展示抗每种病毒株的中和活性。本发明人认为他们是第一个研发对sars-cov-2、mers-cov和sars-cov s有利地展示交叉反应性的抗体的,从而提供可以用于检测和治疗所有已知冠状病毒病原体的泛的或“通用的”冠状病毒抗体,并且可能提供用于检测和治疗未来冠状病毒感染毒株的手段。
8.技术人员将理解,sars-cov-2还可称为sarscov2、冠状病毒病(covid-)或新型冠状病毒(ncov)。
9.优选地,抗体或其抗原结合片段与sars-cov、mers-cov和sars cov2交叉反应。优
选地,抗体或其抗原结合片段中和sars-cov、mers-cov和sars cov2。
10.优选地,抗体或其抗原结合片段结合sars-cov和mers-cov的刺突蛋白s2结构域。优选地,抗体或其抗原结合片段结合sars-cov和sars cov2的刺突蛋白s2结构域。优选地,抗体或其抗原结合片段结合mers-cov和sars cov2的刺突蛋白s2结构域。
11.优选地,抗体或其抗原结合片段结合类似于sars-cov的蝙蝠冠状病毒变体的刺突蛋白s2结构域。蝙蝠冠状病毒变体可以是wiv16变体或ratg13变体。优选地,抗体或其抗原结合片段结合sars-cov-2貂突变体的刺突蛋白s2结构域。优选地,抗体或其抗原结合片段结合sars-cov-2b1.1.7变体(“kent变体”)或sars-cov-2b.1.351变体(“南非变体”)的刺突蛋白s2结构域。
12.然而,最优选地,抗体或其抗原结合片段结合sars-cov、mers-cov和sars cov2的刺突蛋白s2结构域。现在将在此描述这些s2结构域中的每个。
13.sars-cov
14.在一个实施方式中,sars-cov刺突蛋白可由genbank id no:aar07630.1表示,其在此作为seq id no:1提供如下:
15.mfifllfltltsgsdldrcttfddvqapnytqhtssmrgvyypdeifrsdtlyltqdlflpfysnvtgfhtinhtfgnpvipfkdgiyfaateksnvvrgwvfgstmnnksqsviiinnstnvviracnfelcdnpffavskpmgtqthtmifdnafnctfeyisdafsldvseksgnfkhlrefvfknkdgflyvykgyqpidvvrdlpsgfntlkpifklplginitnfrailtafspaqdiwgtsaaayfvgylkpttfmlkydengtitdavdcsqnplaelkcsvksfeidkgiyqtsnfrvvpsgdvvrfpnitnlcpfgevfnatkfpsvyawerkkisncvadysvlynstffstfkcygvsatklndlcfsnvyadsfvvkgddvrqiapgqtgviadynyklpddfmgcvlawntrnidatstgnynykyrylrhgklrpferdisnvpfspdgkpctppalncywplndygfytttgigyqpyrvvvlsfellnapatvcgpklstdliknqcvnfnfngltgtgvltpsskrfqpfqqfgrdvsdftdsvrdpktseildispcsfggvsvitpgtnassevavlyqdvnctdvstaihadqltpawriystgnnvfqtqagcligaehvdtsyecdipigagicasyhtvsllrstsqksivaytmslgadssiaysnntiaiptnfsisittevmpvsmaktsvdcnmyicgdstecanlllqygsfctqlnralsgiaaeqdrntrevfaqvkqmyktptlkyfggfnfsqilpdplkptkrsfiedllfnkvtladagfmkqygeclgdinardlicaqkfngltvlpplltddmiaaytaalvsgtatagwtfgagaalqipfamqmayrfngigvtqnvlyenqkqianqfnkaisqiqesltttstalgklqdvvnqnaqalntlvkqlssnfgaissvlndilsrldkveaevqidrlitgrlqslqtyvtqqliraaeirasanlaatkmsecvlgqskrvdfcgkgyhlmsfpqaaphgvvflhvtyvpsqernfttapaichegkayfpregvfvfngtswfitqrnffspqiittdntfvsgncdvvigiinntvydplqpeldsfkeeldkyfknhtspdvdlgdisginasvvniqkeidrlnevaknlneslidlqelgkyeqyikwpwyvwlgfiagliaivmvtillccmtsccsclkgacscgscckfdeddsepvlkgvklhyt
16.[seq id no:1]
[0017]
抗体或其抗原结合片段可以结合基本上如seq id no:1中所示的sars-cov刺突蛋白的氨基酸位置700与900、750与900、800与900、700与850、750与850、800与850、700与800或750与800之间的区域。
[0018]
抗体或其抗原结合片段可以结合基本上如seq id no:1中所示的sars-cov刺突蛋白的氨基酸位置770与790、780与800、790与810或800与820之间的区域。
[0019]
抗体或其抗原结合片段可以结合基本上如seq id no:1中所示的sars-cov刺突蛋白的氨基酸位置774与790、774与800、774与810、774与819、780与819、790与819、800与819
或810与819之间的区域。
[0020]
然而,优选地,抗体或其抗原结合片段可以结合基本上如seq id no:1中所示的sars-cov刺突蛋白的氨基酸位置774与819之间的区域。
[0021]
在一个实施方式中,sars-cov刺突蛋白s2结构域可由genbank id no:aat74874.1表示,其在此作为seq id no:2提供如下:
[0022]
asyhtvsllrstsqksivaytmslgadssiaysnntiaiptnfsisittevmpvsmaktsvdcnmyicgdstecanlllqygsfctqlnralsgiaaeqdrntrevfaqvkqmyktptlkyfggfnfsqilpdplkptkrsfiedllfnkvtladagfmkqygeclgdinardlicaqkfngltvlpplltddmiaaytaalvsgtatagwtfgagaalqipfamqmayrfngigvtqnvlyenqkqianqfnkaisqiqesltttstalgklqdvvnqnaqalntlvkqlssnfgaissvlndilsrldkveaevqidrlitgrlqslqtyvtqqliraaeirasanlaatkmsecvlgqskrvdfcgkgyhlmsfpqaaphgvvflhvtyvpsqernfttapaichegkayfpregvfvfngtswfitqrnffspqiittdntfvsgncdvvigiinntvydplqpeldsfkeeldkyfknhtspdvdlgdisginasvvniqkeidrlnevaknlneslidlqelgkyeqyikwpwyvwlgfiagliaivmvtillccmtsccsclkgacscgscckfdeddsepvlkgvkl
[0023]
[seq id no:2]
[0024]
优选地,抗体或其抗原结合片段结合序列,该序列包含基本上如seq id no:2中所示的序列或者其片段或变体,或者该序列由基本上如seq id no:2中所示的序列或者其片段或变体组成。
[0025]
优选地,抗体或其抗原结合片段结合seq id no:2中的一个或多个氨基酸,或者其片段或变体。
[0026]
优选地,抗体或其抗原结合片段结合seq id no:2中存在的任何5、10、15、20、25、30、35、40或45个氨基酸,或者其变体或片段。
[0027]
优选地,抗体或其抗原结合片段可以结合sars-cov刺突蛋白的氨基酸位置774与819之间的一个或多个氨基酸,其在此作为seq id no:3提供如下:
[0028]
ptlkyfggfnfsqilpdplkptkrsfiedllfnkvtladaagfmkqy
[0029]
[seq id no:3]
[0030]
因此,优选地,抗体或其抗原结合片段结合序列,该序列包含基本上如seq id no:3中所示的序列或者其片段或变体,或者该序列由基本上如seq id no:3中所示的序列或者其片段或变体组成。
[0031]
优选地,抗体或其抗原结合片段结合seq id no:3中的一个或多个氨基酸,或者其片段或变体。
[0032]
优选地,抗体或其抗原结合片段结合seq id no:3中存在的任何5、10、15、20、25、30、35、40或45个氨基酸序列,或者其变体或片段。
[0033]
如实施例中所描述,并且如图14c-e中所示,发明人发现根据本发明的抗体或其抗原结合片段结合sars-cov、mers-cov和/或sars-cov-2每个中的刺突蛋白s2结构域中的一个或多个表位(在此表示为p1和p2)。因此,下文描述了sars-cov的p1和p2表位。
[0034]
因此,在优选的实施方式中,抗体或其抗原结合片段可以结合基本上如seq id no:1中所示的sars-cov刺突蛋白的氨基酸位置690与950之间的区域。抗体或其抗原结合片段可以结合基本上如seq id no:1中所示的sars-cov刺突蛋白的氨基酸位置710与910之间的区域。抗体或其抗原结合片段可以结合基本上如seq id no:1中所示的sars-cov刺突蛋
白的氨基酸位置690与750、700与740或711与730之间的区域。这个表位表示为p1,如图14d和14e中所示。抗体或其抗原结合片段可以结合基本上如seq id no:1中所示的sars-cov刺突蛋白的氨基酸位置705与735、710与730、711与740、711与730、700与728、710与728、或711与728之间的区域。优选地,抗体或其抗原结合片段可以结合基本上如seq id no:1中所示的sars-cov刺突蛋白的氨基酸位置711与728之间的区域。
[0035]
抗体或其抗原结合片段可以结合基本上如seq id no:1中所示的sars-cov刺突蛋白的氨基酸位置840与930、850与920、860与910或870与900之间的区域。这个表位表示为p2,如图14d和14e中所示。抗体或其抗原结合片段可以结合基本上如seq id no:1中所示的sars-cov刺突蛋白的氨基酸位置865与898、870与898、878与910、878与905或878与900之间的区域。优选地,抗体或其抗原结合片段可以结合基本上如seq id no:1中所示的sars-cov刺突蛋白的氨基酸位置878与898之间的区域。
[0036]
因此,在一个实施方式中,抗体或其抗原结合片段可以结合基本上如seq id no:1中所示的sars-cov刺突蛋白的氨基酸位置711与728之间和/或878与898之间的区域。
[0037]
优选地,抗体或其抗原结合片段可以结合sars-cov刺突蛋白的氨基酸位置711与728之间的一个或多个氨基酸(即p1表位),其在此作为seq id no:80提供如下:
[0038]
vsmaktsvdcnyicgds
[0039]
[seq id no:80]
[0040]
因此,优选地,抗体或其抗原结合片段结合序列,该序列包含基本上如seq id no:80中所示的序列或者其变体或片段,或者该序列由基本上如seq id no:80中所示的序列或者其变体或片段组成。
[0041]
优选地,抗体或其抗原结合片段结合seq id no:80中的一个或多个氨基酸,或者其片段或变体。
[0042]
优选地,抗体或其抗原结合片段结合seq id no:80中存在的任何5、10、15或20个氨基酸序列,或者其变体或片段。
[0043]
优选地,抗体或其抗原结合片段可以结合sars-cov刺突蛋白的氨基酸位置878与898之间的一个或多个氨基酸(即,p2表位),其在此作为seq id no:76提供如下:
[0044]
ipfamqmayrfngigvtqnvl
[0045]
[seq id no:76]
[0046]
因此,优选地,抗体或其抗原结合片段结合序列,该序列包含基本上如seq id no:76中所示的序列或者其变体或片段,或者该序列由基本上如seq id no:76中所示的序列或者其变体或片段组成。
[0047]
优选地,抗体或其抗原结合片段结合seq id no:76中的一个或多个氨基酸,或者其片段或变体。
[0048]
优选地,抗体或其抗原结合片段结合seq id no:76中存在的任何5、10、15或20个氨基酸序列,或者其变体或片段。
[0049]
mers-cov
[0050]
在一个实施方式中,mers-cov刺突蛋白可由genbank id no:ahx71946.1表示,其在此作为seq id no:4提供如下:
[0051]
mihsvfllmflltptesyvdvgpdsvksacievdiqqtffdktwprpidvskadgiiypqgrtysniti
tyqglfpyqgdhgdmyvysaghatgttpqklfvanysqdvkqfangfvvrigaaanstgtviispstsatirkiypafmlgssvgnfsdgkmgrffnhtlvllpdgcgtllrafycileprsgnhcpagnshtsfatyhtpatdcsdgnynrnaslnsfkeyfnlrnctfmytynitedeilewfgitqtaqgvhlfssryvdlyggnmfqfatlpvydtikyysiiphsirsiqsdrkawaafyvyklqpltflldfsvdgyirraidcgfndlsqlhcsyesfdvesgvysvssfeakpsgsvveqaegvecdfspllsgtppqvynfkrlvftncnynltkllslfsvndftcsqispaaiasncysslildyfsyplsmksdlsvssagpisqfnykqsfsnptclilatvphnlttitkplkysyinkcsrllsddrtevpqlvnanqyspcvsivpstvwedgdyyrkqlsplegggwlvasgstvamteqlqmgfgitvqygtdtnsvcpklefandtkiasqlgncveyslygvsgrgvfqnctavgvrqqrfvydayqnlvgyysddgnyyclracvsvpvsviydketkthatlfgsvacehisstmsqysrstrsmlkrrdstygplqtpvgcvlglvnsslfvedcklplgqslcalpdtpstltprsvrsvpgemrlasiafnhpiqvdqlnssyfklsiptnfsfgvtqeyiqttiqkvtvdckqyvcngfqkceqllreygqfcskinqalhganlrqddsvrnlfasvkssqsspiipgfggdfnltllepvsistgsrsarsaiedllfdkvtiadpgymqgyddcmqqgpasardlicaqyvagykvlpplmdvnmeaaytssllgsiagvgwtaglssfaaipfaqsifyrlngvgitqqvlsenqkliankfnqalgamqtgftttneafrkvqdavnnnaqalsklaselsntfgaisasigdiiqrldvleqdaqidrlingrlttlnafvaqqlvrsesaalsaqlakdkvnecvkaqskrsgfcgqgthivsfvvnapnglyfmhvgyypsnhievvsayglcdaanptnciapvngyfiktnntrivdewsytgssfyapepitslntkyvapqvtyqnistnlpppllgnstgidfqdeldeffknvstsipnfgsltqinttlldltyemlslqqvvkalnesyidlkelgnytyynkwpwyiwlgfiaglvalalcvffilcctgcgtncmgklkcnrccdryeeydlephkvhvh
[0052]
[seq id no:4]
[0053]
抗体或其抗原结合片段可以结合基本上如seq id no:4中所示的mers-cov刺突蛋白的氨基酸位置800与1000、800与950、800与900、850与1000、850与950、850与900或900与950之间的区域。
[0054]
抗体或其抗原结合片段可以结合基本上如seq id no:4中所示的mers-cov刺突蛋白的氨基酸位置850与870、860与880、870与890或880与900或890与910之间的区域。
[0055]
抗体或其抗原结合片段可以结合基本上如seq id no:4中所示的mers-cov刺突蛋白的氨基酸位置860与880、860与890、860与900、860与910、870与910、880与910、890与910或900与910之间的区域。
[0056]
优选地,抗体或其抗原结合片段可以结合基本上如seq id no:4中所示的mers-cov刺突蛋白的氨基酸位置860与910之间的区域。
[0057]
在一个实施方式中,mers-cov刺突蛋白s2结构域可由genbank id no:ala49836.1表示,其在此作为seq id no:5提供如下:
[0058]
vdqlnssyfklsiptnfsfgvtqeyiqttiqkvtvdckqyvcngfqkceqllreygqfcskinqalhganlrqddsvrnlfasvkssqsspiipgfggdfnltllepvsistgsrsarsaiedllfdkvtiadpgymqgyddcmqqgpasardlicaqyvagykvlpplmdvnmeaaytssllgsiagvgwtaglssfaaipfaqsifyrlngvgitqqvlsenqkliankfnqalgamqtgftttneafrkvqdavnnnaqalsklaselsntfgaisasigdiiqrldvleqdaqidrlingrlttlnafvaqqlvrsesaalsaqlakdkvnecvkaqskrsgfcgqgthivsfvvnapnglyfmhvgyypsnhievvsayglcdaanptnciapvngyfiktnntrivdewsytgssfyapepitslntkyvapqvtyqnistnlpppllgnstgidfqdeldeffknvstsipnfgsltqinttlldltyemlslqqvvkalnesyidlkelgnytyynkwpwyiwlgfiaglvalalcvffilcctgcgtncmgklkcnrccdryeeydlephkvh
[0059]
[seq id no:5]
[0060]
优选地,抗体或其抗原结合片段结合序列,该序列包含基本上如seq id no:5中所示的序列或者其片段或变体,或者该序列由基本上如seq id no:5中所示的序列或者其片段或变体组成。
[0061]
优选地,抗体或其抗原结合片段结合seq id no:5中的一个或多个氨基酸,或者其片段或变体。
[0062]
优选地,抗体或其抗原结合片段结合seq id no:5中存在的任何5、10、15、20、25、30、35、40或45个氨基酸序列,或者其变体或片段。
[0063]
抗体或其抗原结合片段可以结合mers-cov刺突蛋白的氨基酸位置860与910之间的一个或多个氨基酸,其在此作为seq id no:6提供如下:
[0064]
piipgfggdfnltllepvsistgsrsarsaiedllfdkvtiadpgymqgy
[0065]
[seq id no:6]
[0066]
因此,优选地,抗体或其抗原结合片段结合序列,该序列包含基本上如seq id no:6中所示的序列或者其片段或变体,或者该序列由基本上如seq id no:6中所示的序列或者其片段或变体组成。
[0067]
优选地,抗体或其抗原结合片段结合seq id no:6中的一个或多个氨基酸,或者其片段或变体。
[0068]
优选地,抗体或其抗原结合片段结合seq id no:6中存在的任何5、10、15、20、25、30、35、40或45个氨基酸序列,或者其变体或片段。
[0069]
参考图14c-e,发明人发现根据本发明的抗体或其抗原结合片段结合mers-cov中的刺突蛋白s2结构域中的一个或多个表位(在此表示为p1和p2),如下。
[0070]
优选地,抗体或其抗原结合片段可以结合基本上如seq id no:4中所示的mers-cov刺突蛋白的氨基酸位置760与1150、770与1100、780与1000或790与1000之间的区域。抗体或其抗原结合片段可以结合基本上如seq id no:4中所示的mers-cov刺突蛋白的氨基酸位置760与850、770与840、780与830、790与820或795与815之间的区域。这个表位表示为p1,如图14d和14e中所示。优选地,抗体或其抗原结合片段可以结合基本上如seq id no:4中所示的mers-cov刺突蛋白的氨基酸位置797与814之间的区域。
[0071]
抗体或其抗原结合片段可以结合基本上如seq id no:4中所示的mers-cov刺突蛋白的氨基酸位置940与1020、950与1010、960与1000或970与995之间的区域。这个表位表示为p2,如图14d和14e中所示。优选地,抗体或其抗原结合片段可以结合基本上如seq id no:4中所示的mers-cov刺突蛋白的氨基酸位置970与990之间的区域。
[0072]
因此,在一个实施方式中,抗体或其抗原结合片段可以结合基本上如seq id no:4中所示的mers-cov刺突蛋白的氨基酸位置797与814之间和/或970与990之间的区域。
[0073]
抗体或其抗原结合片段可以结合mers-cov刺突蛋白的氨基酸位置797与814之间的一个或多个氨基酸(即p1表位),其在此作为seq id no:81提供如下:
[0074]
ttiqkvtvdckqyvcngf
[0075]
[seq id no:81]
[0076]
因此,优选地,抗体或其抗原结合片段结合序列,该序列包含基本上如seq id no:81中所示的序列或者其片段或变体,或者该序列由基本上如seq id no:81中所示的序列或者其片段或变体组成。
[0077]
优选地,抗体或其抗原结合片段结合seq id no:81中的一个或多个氨基酸,或者其片段或变体。
[0078]
优选地,抗体或其抗原结合片段结合seq id no:81中存在的任何5、10、15或20个氨基酸序列,或者其变体或片段。
[0079]
抗体或其抗原结合片段可以结合mers-cov刺突蛋白的氨基酸位置970-990之间的一个或多个氨基酸(即,p2表位),其在此作为seq id no:77提供如下:
[0080]
ipfaqsifyrlngvgitqqvl
[0081]
[seq id no:77]
[0082]
因此,优选地,抗体或其抗原结合片段结合序列,该序列包含基本上如seq id no:77中所示的序列或者其片段或变体,或者该序列由基本上如seq id no:77中所示的序列或者其片段或变体组成。
[0083]
优选地,抗体或其抗原结合片段结合seq id no:77中的一个或多个氨基酸,或者其片段或变体。
[0084]
优选地,抗体或其抗原结合片段结合seq id no:77中存在的任何5、10、15或20个氨基酸序列,或者其变体或片段。
[0085]
sars-cov-2(covid-19)
[0086]
在一个实施方式中,sars-cov2刺突蛋白可由genbank id no:yp009724390.1表示,其在此作为seq id no:7提供如下:
[0087]
mfvflvllplvssqcvnlttrtqlppaytnsftrgvyypdkvfrssvlhstqdlflpffsnvtwfhaihvsgtngtkrfdnpvlpfndgvyfasteksniirgwifgttldsktqsllivnnatnvvikvcefqfcndpflgvyyhknnkswmesefrvyssannctfeyvsqpflmdlegkqgnfknlrefvfknidgyfkiyskhtpinlvrdlpqgfsaleplvdlpiginitrfqtllalhrsyltpgdsssgwtagaaayyvgylqprtfllkynengtitdavdcaldplsetkctlksftvekgiyqtsnfrvqptesivrfpnitnlcpfgevfnatrfasvyawnrkrisncvadysvlynsasfstfkcygvsptklndlcftnvyadsfvirgdevrqiapgqtgkiadynyklpddftgcviawnsnnldskvggnynylyrlfrksnlkpferdisteiyqagstpcngvegfncyfplqsygfqptngvgyqpyrvvvlsfellhapatvcgpkkstnlvknkcvnfnfngltgtgvltesnkkflpfqqfgrdiadttdavrdpqtleilditpcsfggvsvitpgtntsnqvavlyqdvnctevpvaihadqltptwrvystgsnvfqtragcligaehvnnsyecdipigagicasyqtqtnsprrarsvasqsiiaytmslgaensvaysnnsiaiptnftisvtteilpvsmtktsvdctmyicgdstecsnlllqygsfctqlnraltgiaveqdkntqevfaqvkqiyktppikdfggfnfsqilpdpskpskrsfiedllfnkvtladagfikqygdclgdiaardlicaqkfngltvlpplltdemiaqytsallagtitsgwtfgagaalqipfamqmayrfngigvtqnvlyenqklianqfnsaigkiqdslsstasalgklqdvvnqnaqalntlvkqlssnfgaissvlndilsrldkveaevqidrlitgrlqslqtyvtqqliraaeirasanlaatkmsecvlgqskrvdfcgkgyhlmsfpqsaphgvvflhvtyvpaqeknfttapaichdgkahfpregvfvsngthwfvtqrnfyepqiittdntfvsgncdvvigivnntvydplqpeldsfkeeldkyfknhtspdvdlgdisginasvvniqkeidrlnevaknlneslidlqelgkyeqyikwpwyiwlgfiagliaivmvtimlccmtsccsclkgccscgscckfdeddsepvlkgvklhyt
[0088]
[seq id no:7]
[0089]
抗体或其抗原结合片段可以结合基本上如seq id no:7中所示的sars-cov2刺突蛋白的氨基酸位置700与900、750与900、800与900、700与850、750与850、800与850、700与800或750与800之间的区域。
cov2刺突蛋白的氨基酸位置700与950、800与950、850与950、700与900、700与850或700与800之间的区域。
[0107]
抗体或其抗原结合片段可以结合基本上如seq id no:7中所示的sars-cov2刺突蛋白的氨基酸位置690与780、700与770、710与760或720与750之间的区域。这个表位表示为p1,如图14d和14e中所示。抗体或其抗原结合片段可以结合基本上如seq id no:7中所示的sars-cov2刺突蛋白的氨基酸位置729与770、729与760、729与750、700与746、710与746、720与746或725与746之间的区域。优选地,抗体或其抗原结合片段可以结合基本上如seq id no:7中所示的sars-cov2刺突蛋白的氨基酸位置729与746之间的区域。
[0108]
抗体或其抗原结合片段可以结合到基本上如seq id no:7中所示的sars-cov2刺突蛋白的氨基酸位置870与930、880与925、890与920、896与930、896与925、896与920、880与916、885与916或890与916之间的区域。这个表位表示为p2,如图14d和14e中所示。优选地,抗体或其抗原结合片段可以结合基本上如seq id no:7中所示的sars-cov2刺突蛋白的氨基酸位置896与916之间的区域。
[0109]
因此,在一个实施方式中,抗体或其抗原结合片段可以结合基本上如seq id no:7中所示的sars-cov2刺突蛋白的氨基酸位置729与746之间和/或896与916之间的区域。
[0110]
因此,抗体或其抗原结合片段可以结合sars-cov2刺突蛋白的氨基酸位置729与746之间的一个或多个氨基酸(即,p1表位),其在此作为seq id no:82提供如下:
[0111]
vsmtktsvdctmyicgds
[0112]
[seq id no:82]
[0113]
因此,优选地,抗体或其抗原结合片段结合序列,该序列包含基本上如seq id no:82中所示的序列或者其片段或变体,或者该序列由基本上如seq id no:82中所示的序列或者其片段或变体组成。
[0114]
优选地,抗体或其抗原结合片段结合seq id no:82中的一个或多个氨基酸,或者其片段或变体。
[0115]
优选地,抗体或其抗原结合片段结合seq id no:82中存在的任何5、10、15和20个氨基酸序列,或者其变体或片段。
[0116]
抗体或其抗原结合片段可以结合sars-cov2刺突蛋白的氨基酸位置896与916之间的一个或多个氨基酸(即,p2表位),其此作为seq id no:78提供如下:
[0117]
ipfamqmayrfngigvtqnvl
[0118]
[seq id no:78]
[0119]
因此,优选地,抗体或其抗原结合片段结合序列,该序列包含基本上如seq id no:78中所示的序列或者其片段或变体,或者该序列由基本上如seq id no:78中所示的序列或者其片段或变体组成。
[0120]
优选地,抗体或其抗原结合片段结合seq id no:78中的一个或多个氨基酸,或者其片段或变体。
[0121]
优选地,抗体或其抗原结合片段结合seq id no:9中存在的任何5、10、15和20个氨基酸序列,或者其变体或片段。
[0122]
共有序列
[0123]
如图12中所示,基于发明人在sars-cov、mer-cov和sars-cov2的刺突蛋白的s2结
构域中共享表位区域的鉴定,发明人已经能够产生用于交叉反应的抗体结合的共有表位序列,其在此作为seq id no:10提供如下:
[0124]
px1x2x3x4fggx3fnx5x6x7x8x9px
10
x
11
x
12
x
13
x
14
x
15
x
16
x
17
x
18
x
19
rsx
20
iedllfx
21
kvtx
22
adx
23
gx
24
x
25
x
26
x
27y[0125]
[seq id no:10]
[0126]
因此,优选地,抗体或其抗原结合片段结合序列,该序列包含基本上如seq id no:10中所示的序列或者其片段或变体,或者该序列由基本上如seq id no:10中所示的序列或者其片段或变体组成,其中x1至x
27
可以是任何氨基酸或无氨基酸。优选地,x1至x4、x6至x
11
以及x
14
至x
27
可以是任何氨基酸,并且x5、x
11
至x
13
可以无氨基酸。
[0127]
x1至x
27
可以是存在于seq id no:6的mers-cov序列、seq id no:3的sars-cov序列或seq id no:9的sars-cov-2序列中的相应氨基位置中的氨基酸。
[0128]
然而,在优选的实施方式中,并且基于发明人对sars-cov、mer-cov和sars-cov2的刺突蛋白的s2结构域中的共享表位区域(即,p1表位)的鉴定,如图14d中所示,发明人已经能够产生用于交叉反应的抗体结合的共有表位序列,其在此作为seq id no:83提供如下:
[0129]
x1x2x3x4ktsvdcx5x6yx7cx8x9x
10
[0130]
[seq id no:83]
[0131]
因此,优选地,抗体或其抗原结合片段结合序列,该序列包含基本上如seq id no:83中所示的序列或者其片段或变体,或者该序列由基本上如seq id no:83中所示的序列或者其片段或变体组成,其中x1至x
10
可以是任何氨基酸。
[0132]
x1至x
10
可以是存在于seq id no:6的mers-cov序列、seq id no:3的sars-cov序列或seq id no:9的sars-cov-2序列中的相应氨基位置中的氨基酸。
[0133]
发明人已经鉴定了另外的共享表位区域(即,p2表位),如图14d中所示,并且发明人已经能够产生用于交叉反应的抗体结合的另外的共有表位序列,其在此作为seq id no:79提供如下:
[0134]
ipfax1x2x3x4yrx5ngigx6tqx7vl
[0135]
[seq id no:79]
[0136]
因此,优选地,抗体或其抗原结合片段结合序列,该序列包含基本上如seq id no:79中所示的序列或者其片段或变体,或者该序列由基本上如seq id no:79中所示的序列或者其片段或变体组成,其中x1至x7可以是任何氨基酸。
[0137]
x1至x7可以是存在于seq id no:77的mers-cov序列、seq id no:76的sars-cov序列或seq id no:78的sars-cov-2序列中的相应氨基位置中的氨基酸。
[0138]
优选地,本发明的抗体或其抗原结合片段能够中和和/或诱导sars-cov、mers-cov和/或sars cov2的抗体依赖细胞的细胞毒性(adcc)。
[0139]
技术人员将理解,“中和”意指降低或中和病毒的生物效应。优选地,抗体能够阻断刺突蛋白结合宿主细胞中的细胞膜上存在的血管紧张肽转化酶2(ace2)。
[0140]
优选地,本发明的抗体或其抗原结合片段能够引发抗sars-cov、mers-cov和/或sars cov2的免疫应答。
[0141]
优选地,抗体或其抗原结合片段刺激在宿主中产生中和抗体和/或两种cd4+和cd8+t细胞应答。
[0142]
本发明延伸到对sars-cov、mers-cov和/或sars cov2的s2结构域具有免疫特异性的全抗体(即,免疫球蛋白),以及相应的全长抗体的抗原结合片段或区域。
[0143]
抗体或其抗原结合片段可以是单价、二价或多价的。单价抗体是二聚体(hl),其包含通过二硫桥键与轻链(l)缔合的重链(h)。二价抗体是四聚体(h2l2),其包含通过至少一个二硫桥键缔合的两个二聚体。例如,通过连接多个二聚体,也可以产生多价抗体。抗体分子的基本结构由两条相同的轻链和两条相同的重链组成,它们非共价地缔合,并且可以通过二硫键连接。每条重链和轻链含有约110个氨基酸的氨基末端可变区,以及链的剩余部分中的恒定序列。可变区包括几个高变区或互补决定区(cdr),其形成抗体分子的抗原结合位点,并且决定其对抗原,即,sars-cov、mers-cov和/或sars cov2的s2结构域或者其变体或片段(例如,表位)的特异性。在重链和轻链的cdr的每侧上是框架区,锚定和定向cdr的相对保守的氨基酸序列。抗体片段可以包括双特异性抗体(bsab)或嵌合抗原受体(car)。
[0144]
重链恒定区典型地包含三个结构域c
h1
、c
h2
和c
h3
。每条轻链典型地包含轻链可变区(v
l
)和轻链恒定区。轻链恒定区典型地包含一个结构域,缩写为c
l
。
[0145]
每条重链和轻链通常包括按以下顺序(从n端至c端)布置的三个cdr和四个fr:fr
1-cdr
1-fr
2-cdr
2-fr
3-cdr
3-fr4。cdr涉及抗原结合,并且赋予抗体的抗原特异性和结合亲和力。参见kabat等,具有免疫学意义的蛋白质序列(sequences of proteins of immunological interest)5th ed.(1991)public health service,national institutes of health,bethesda,md,以引用方式全文并入本文。
[0146]
来自任何脊椎动物物种的重链可分为五种不同类别(或同种型)之一:iga、igd、ige、igg和igm。这些类别还分别地被指定为α、δ、ε、γ和μ。igg和iga类别基于序列和功能的差异进一步分成亚类。人类表达以下亚类:igg1、igg2、igg3、igg4、iga1以及iga2。
[0147]
基于恒定结构域的序列,可以将来自任何脊椎动物物种的轻链指定为两种类型,称为κ和λ之一。
[0148]
恒定区由五个重链序列(μ、γ、ζ、α或ε)中的一个和两个轻链序列(κ或λ)中的一个组成。重链恒定区序列决定抗体的同种型和分子的效应子功能。
[0149]
优选地,分离或纯化抗体或其抗原结合片段。
[0150]
在一个优选实施方式中,抗体或其抗原结合片段包括多克隆抗体或其抗原结合片段。可以在兔、小鼠或大鼠中产生抗体或其抗原结合片段。
[0151]
优选地,通过用sars-cov、mers-cov和/或sars cov2的s2结构域或者其变体或片段免疫宿主动物,然后收集抗体或其抗原结合片段而获得抗体或其抗原结合片段。宿主动物最优选地是兔。
[0152]
在另一个优选的实施方式中,抗体或其抗原结合片段包括单克隆抗体或其抗原结合片段。优选地,本发明的抗体是人抗体。如此所用的术语“人抗体”可以意指抗体,如单克隆抗体,其包含与在特定人抗体中所发现的基本上相同的重链和轻链cdr氨基酸序列,或者其变体或片段,该特定人抗体对sars-cov、mers-cov和/或sars cov2的s2结构域表现出免疫特异性。当与参考序列相比较时,与重链或轻链cdr基本上相同的氨基酸序列表现出相当大量的序列同一性。这种同一性明确已知或可识别为代表特定人抗体的氨基酸序列。基本上相同的重链和轻链cdr氨基酸序列可以具有例如,氨基酸的微小修饰或保守取代。这种人抗体维持其选择性结合sars-cov、mers-cov和/或sars cov2的s2结构域或者其变体或片段
的功能。
[0153]
术语“人单克隆抗体”可以包括一种具有基本上或完全人cdr氨基酸序列的单克隆抗体,例如,通过重组方法,如通过噬菌体文库、淋巴细胞或杂交瘤细胞的产生来产生该单克隆抗体。
[0154]
术语“单克隆抗体”是指来自基本上同质抗体群体的抗体。基本上同质抗体的群体包括基本上相似的和结合相同表位的抗体,除了在单克隆抗体产生期间可能正常出现的变体之外。这种变体通常仅以少量存在。典型地,通过包括从多种抗体中选择单一抗体的方法来获得单克隆抗体。例如,选择方法可以是从多个克隆,如杂交瘤克隆、噬菌体克隆、酵母克隆、细菌克隆或其他重组dna克隆的库中选择唯一的克隆。可以进一步改变所选择的抗体,例如,以改善对靶的亲和力(“亲和力成熟”)、使抗体人源化、改善其在细胞培养物中的产生、和/或降低其在受试者中的免疫原性。
[0155]
术语“人源化抗体”可以意指来自非人物种(例如,小鼠或兔)的抗体,其蛋白质序列已经被修饰,以增加它们与在人类中天然产生的抗体的相似性。
[0156]
抗体可以是重组抗体。术语“重组人抗体”可以包括使用重组dna技术产生的人抗体。
[0157]
术语“抗原结合区”可以意指对其靶抗原具有特异性结合亲和力的抗体的区域,例如sars-cov、mers-cov和/或sars cov2的s2结构域,或者其变体或片段。优选地,片段是表位。抗原结合区可以是高变cdr或其功能部分。术语cdr的“功能部分”可以意指cdr内的序列,该序列显示对靶抗原的特异性亲和力。cdr的功能部分可以包含特异性地结合sars-cov、mers-cov和/或sars cov2的s2结构域或其片段的配体。
[0158]
术语“cdr”可以意指在重和轻可变链中的高变区。在抗体的重链和轻链的每条链中可以存在一个、两个、三个或更多个cdr。正常地,每条链上存在至少三个cdr,当配置在一起时,它们形成抗原结合位点,即,抗原与其结合或特异性地反应的三维结合位点。然而,已经假定在一些抗体的重链中可以存在四个cdr。
[0159]
cdr的定义还包括当彼此比较时氨基酸残基的重叠或子集。包含特定cdr或其功能部分的确切的残基编号将取决于cdr的序列和大小而变化。在给定抗体的可变氨基酸序列的情况下,本领域技术人员可以常规地确定哪些残基包含特定的cdr。
[0160]
通过使用多种已知编号方案中的任一种,可以确定cdr的氨基酸序列边界,包括由kabat等人,见上文所述的那些(“kabat”编号方案);al-lazikani等人,1997,j.mol.biol.,273:927-948(“chothia”编号方案);maccallum等人,1996,j.mol.biol.262:732-745(“contact”编号方案);lefranc等人,dev.comp.immunol.,2003,27:55-77(“imgt”编号方案);以及honegge和pl
ü
ckthun,j.mol.biol.,2001,309:657-70(“aho”编号方案)。
[0161]
术语抗体的“功能性片段”可以意指保留功能性活性的抗体的一部分。功能性活性可以是例如,抗原结合活性或特异性。功能性活性还可以是例如,由抗体恒定区提供的效应子功能。术语“功能性片段”还旨在包括,例如,通过本领域技术人员已知的蛋白酶消化或人类单克隆抗体的还原,以及重组dna方法产生的片段。人单克隆抗体功能性片段包括,例如,单独的重链或轻链及其片段,如vl、vh和fd;单价片段,如fv、fab和fab';二价片段如f(ab')2;单链fv(scfv);和fc片段。
[0162]
术语“vl片段”可以意指人单克隆抗体的轻链的片段,其包括轻链可变区的全部或
部分,包括cdr。vl片段可以进一步包括轻链恒定区序列。
[0163]
术语“vh片段”可以意指人单克隆抗体的重链的片段,其包括重链可变区的全部或部分,包括cdr。
[0164]
术语“fd片段
””
可以意指连接至第一重链恒定区的重链可变区,即vh和ch-1。“fd片段”不包括轻链,或重链的第二和第三恒定区。
[0165]
术语“fv片段”可以意指人单克隆抗体的单价抗原结合片段,包括重链和轻链的可变区的全部或部分,并且重链和轻链的恒定区不存在。重链和轻链的可变区包括例如,cdr。例如,fv片段包括重链和轻链两者的约110个氨基酸的氨基末端可变区的全部或部分。
[0166]
术语“fab片段”可以意指大于fv片段的人单克隆抗体的单价抗原结合片段。例如,fab片段包括可变区以及重链和轻链的第一恒定区的全部或部分。因此,fab片段另外包括重链和轻链的例如,从约110至约220的氨基酸残基。
[0167]
术语“fab'片段”可以意指大于fab片段的人单克隆抗体的单价抗原结合片段。例如,fab'片段包括所有轻链、重链的所有可变区、以及重链的第一和第二恒定区的全部或部分。例如,fab'片段可以另外包括重链的氨基酸残基220至330中的一些或全部。
[0168]
术语“f(ab')2片段”可以意指人单克隆抗体的二价抗原结合片段。f(ab')2片段包括例如,两条重链和两条轻链的可变区的全部或部分,并且可以进一步包括两条重链和两条轻链的第一恒定结构域的全部或部分。
[0169]
术语“单链fv(scfv)”可以意指与短接头肽连接的重链(vh)和轻链(vl)的可变区的融合。
[0170]
术语“双特异性抗体(bsab)”可以意指包括通过较短连接的肽彼此连接的两个scfv的双特异性抗体。
[0171]
本领域技术人员知道,抗体片段的确切边界并不重要,只要该片段保持功能性活性即可。使用熟知的重组方法,本领域技术人员可以通过基因工程改造多核苷酸序列,以表达功能性片段,该功能性片段具有所期望的用于特定应用的任何端点。抗体的功能性片段可以包含具有与人抗体基本上相同的重链和轻链可变区的片段或由该片段组成。
[0172]
优选地,对于本发明的第一方面,其抗原结合片段对sars-cov、mers-cov和/或sars cov2的s2结构域内的表位是免疫特异性的。其抗原结合片段可以包含选自由vh、vl、fd、fv、fab、fab'、scfv、f(ab')2和fc片段组成的组的任何片段或由该片段组成。
[0173]
其抗原结合片段可以包含人抗体的vl的抗原结合区序列中的任一个、vh的抗原结合区序列中的任一个或vl和vh抗原结合区的组合,或者由它们组成。取决于所希望的亲和力和特异性以及抗原结合片段的预期用途,本领域技术人员可以确定vh和vl抗原结合区序列的适当数量和组合。使用本领域技术人员熟知的方法可以容易地产生和分离抗体的功能性片段或抗原结合片段。此类方法包括例如,蛋白酶解方法、重组方法和化学合成。用于分离功能性片段的蛋白酶解方法包括使用人抗体作为起始材料。适于人免疫球蛋白的蛋白酶解的酶可以包括例如木瓜蛋白酶和胃蛋白酶。本领域技术人员可以容易地选择适当的酶,取决于例如,是否需要单价或二价片段。例如,木瓜蛋白酶切割产生结合抗原的两个单价fab'片段和fc片段。例如,胃蛋白酶切割产生二价f(ab')片段。例如,使用dtt或2-巯基乙醇,可以进一步还原本发明的f(ab')2片段,以产生两个单价fab'片段。
[0174]
通过亲和柱层析程序可以纯化通过蛋白酶解产生的抗体的功能性片段或抗原结
合片段。例如,通过结合蛋白a可以移除未消化的抗体和fc片段。此外,功能性片段可以利用它们的电荷和大小,例如使用离子交换和凝胶过滤层析来纯化。本领域技术人员熟知此类方法。
[0175]
通过重组方法可以产生抗体或其抗原结合片段。优选地,人们最初分离编码抗体重链和轻链的所期望的区域的多核苷酸。此类区域可以包括例如,重链和轻链的可变区的全部或部分。优选地,此类区域可以特别地包括重链和轻链的抗原结合区,优选地抗原结合位点,最优选地cdr。
[0176]
编码根据本发明的抗体或其抗原结合片段的多核苷酸可以使用本领域技术人员已知的方法来产生。通过本领域已知的寡核苷酸合成的方法,编码抗体或其抗原结合片段的多核苷酸可以直接地被合成。可替代地,使用本领域已知的重组方法可以合成和连接更小的片段,以形成更大的功能性片段。
[0177]
如此所用的术语“免疫特异性”可以意指抗体或其抗原结合片段的结合区能够通过与sars-cov、mers-cov和/或sars cov2的s2结构域或者其变体或片段特异性结合而与其免疫反应。抗体或其抗原结合片段可以与抗原(sars-cov、mers-cov和/或sars cov2的s2结构域)以约10-5
至10-13
m-1
,优选地10-6
至10-9
m-1
,甚至更优选地10-10
至10-12
m-1
的亲和常数,选择性地相互作用。
[0178]
术语“免疫反应”可以意指结合区在与sars-cov、mers-cov和/或sars cov2的s2结构域或其表位结合时能够引发免疫应答。
[0179]
术语“表位”可以意指能够引发抗体或其抗原结合片段的结合区,并且与其结合的抗原的任何区域。表位可以是线性或构象表位。优选地,表位是线性的。这可以意指抗体与抗原的多个连续氨基酸相互作用,并且因此表位可以由这些限定的氨基酸组成。优选地,表位是构象的,即非线性的或不连续的。这可以意指抗体与来自抗原的一级氨基酸序列的多个不同的区段相互作用。表位可以包含在此定义的表示为p1的表位和/或表示为p2的表位。
[0180]
因此,抗体或其抗原结合片段可以包含重链。重链可以选自由以下各项组成的组:iga、igd、ige、igg以及igm。优选地,重链是igg。优选地,重链是iga。
[0181]
重链可以是igg1。重链可以是igg2。重链可以是igg3。重链可以是igg4。重链可以是iga1。重链可以是iga2。
[0182]
如实施例中所描述和如图18中所示的,发明人分离了16种对sars-cov高度免疫特异性的抗体,15种对mers-cov免疫特异性的抗体和9种对sars cov2免疫特异性的抗体。发明人还有利地鉴定了四种单克隆抗体,其令人惊奇地展示出与sars-cov、mers-cov和sars cov2的高交叉反应性。这些抗体在此被鉴定为ic001、ic008、ic006和ic004,并且它们的重链和轻链的cdr和框架序列总结在图11中,并且如以下详细讨论。
[0183]
ic001
[0184]
在一个实施方式中,抗体或其抗原结合片段在此被称为ic001(参见图11a和b中所示的表的第1行)。抗体或其抗原结合片段可以包含seq id no:11的cdr-h1结构域,其在此提供如下:
[0185]
gytftsya
[0186]
[seq id no:11]
[0187]
因此,优选地,抗体或其抗原结合片段包含cdr-h1结构域,该结构域包含基本上如
seq id no:11中所示的序列或者其变体或片段,或者由其组成。
[0188]
抗体或其抗原结合片段可以包含seq id no:12的cdr-h2结构域,其在此提供如下:
[0189]
inagngnt[seq id no:12]
[0190]
因此,优选地,抗体或其抗原结合片段包含cdr-h2结构域,该结构域包含基本上如seq id no:12中所示的序列或者或其变体或片段,或者由其组成。
[0191]
抗体或其抗原结合片段可以包含seq id no:13的cdr-h3结构域,其在此提供如下:
[0192]
ardrhmvvpaavfdy
[0193]
[seq id no:13]
[0194]
因此,优选地,抗体或其抗原结合片段包含cdr-h3结构域,该结构域包含基本上如seq id no:13中所示的序列或者其变体或片段,或者由其组成。
[0195]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:11组成的cdr-h1结构域、包含或由seq id no:12组成的cdr-h2结构域和/或包含或由seq id no:13组成的cdr-h3结构域。然而,优选地,抗体或其抗原结合片段包含:包含或由seq id no:11组成的cdr-h1结构域、包含或由seq id no:12组成的cdr-h2结构域以及包含或由seq id no:13组成的cdr-h3结构域。
[0196]
抗体或其抗原结合片段可以包含seq id no:14的fr-h1结构域,其在此提供如下:
[0197]
qvqlvqsgaevkkpgasvkvsckas
[0198]
[seq id no:14]
[0199]
因此,优选地,抗体或其抗原结合片段包含fr-h1结构域,该结构域包含基本上如seq id no:14中所示的序列或者其变体或片段,或者由其组成。
[0200]
抗体或其抗原结合片段可以包含seq id no:15的fr-h2结构域,其在此提供如下:
[0201]
mhwvrqapgqrlewmgw
[0202]
[seq id no:15]
[0203]
因此,优选地,抗体或其抗原结合片段包含cdr-fr-h2结构域,该结构域包含基本上如seq id no:15中所示的序列或者其变体或片段,或者由其组成。
[0204]
抗体或其抗原结合片段可以包含seq id no:16的fr-h3结构域,其在此提供如下:
[0205]
kysqkfqgrvtitrdtsastaymelsslrsedtavyyc
[0206]
[seq id no:16]
[0207]
因此,优选地,抗体或其抗原结合片段包含cdr-fr-h3结构域,该结构域包含基本上如seq id no:16中所示的序列或者其变体或片段,或者由其组成。
[0208]
抗体或其抗原结合片段可以包含seq id no:17的fr-h4结构域,其在此提供如下:
[0209]
wgqgtlvtvss
[0210]
[seq id no:17]
[0211]
因此,优选地,抗体或其抗原结合片段包含fr-h4结构域,该结构域包含基本上如seq id no:17中所示的序列或者其变体或片段,或者由其组成。
[0212]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:14组成的fr-h1结构域、包含或由seq id no:15组成的fr-h2结构域、包含或由seq id no:16组成的fr-h3结构
域和/或包含或由seq id no:17组成的fr-h4结构域。然而,优选地,抗体或其抗原结合片段包含:包含或由seq id no:14组成的fr-h1结构域、包含或由seq id no:15组成的fr-h2结构域、包含或由seq id no:16组成的fr-h3结构域以及包含或由seq id no:17组成的fr-h4结构域。
[0213]
抗体或其抗原结合片段可以包含seq id no:18中所示的重链序列,其在此提供如下:
[0214]
qvqlvqsgaevkkpgasvkvsckasgytftsyamhwvrqapgqrlewmgwinagngntkysqkfqgrvtitrdtsastaymelsslrsedtavyycardrhmvvpaavfdywgqgtlvtvss
[0215]
[seq id no:18]
[0216]
优选地,抗体或其抗原结合片段包含重链可变区,该重链可变区包含基本上如seq id no:18中所示的序列或者其变体或片段,或者由其组成。
[0217]
抗体或其抗原结合片段可以包含seq id no:19的轻链cdr-l1结构域,其在此提供如下:
[0218]
qsissw
[0219]
[seq id no:19]
[0220]
因此,优选地,抗体或其抗原结合片段包含cdr-l1结构域,该结构域包含基本上如seq id no:19中所示的序列或者其变体或片段,或者由其组成。
[0221]
抗体或其抗原结合片段可以包含seq id no:20的cdr-l2结构域,其在此提供如下:
[0222]
kas
[0223]
[seq id no:20]
[0224]
因此,优选地,抗体或其抗原结合片段包含cdr-l2结构域,该结构域包含基本上如seq id no:20中所示的序列或者其变体或片段,或者由其组成。
[0225]
抗体或其抗原结合片段可以包含seq id no:21的cdr-l3结构域,其在此提供如下:
[0226]
qqygt
[0227]
[seq id no:21]
[0228]
因此,优选地,抗体或其抗原结合片段包含cdr-l3结构域,该结构域包含基本上如seq id no:21中所示的序列或者其变体或片段,或者由其组成。
[0229]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:19组成的cdr-l1结构域、包含或由seq id no:20组成的cdr-l2结构域和/或包含或由seq id no:21组成的cdr-l3结构域。然而,优选地,抗体或其抗原结合片段包含:包含或由seq id no:19组成的cdr-l1结构域、包含或由seq id no:20组成的cdr-l2结构域以及包含或由seq id no:21组成的cdr-l3结构域。
[0230]
抗体或其抗原结合片段可以包含seq id no:22的fr-l1结构域,其在此提供如下:
[0231]
aiqltqsspstlsasvgdrvtitcras
[0232]
[seq id no:22]
[0233]
因此,优选地,抗体或其抗原结合片段包含fr-l1结构域,该结构域包含基本上如seq id no:22中所示的序列或者其变体或片段,或者由其组成。
[0234]
抗体或其抗原结合片段可以包含seq id no:23的fr-l2结构域,其在此提供如下:
[0235]
lawyqqkpgkapklliy
[0236]
[seq id no:23]
[0237]
因此,优选地,抗体或其抗原结合片段包含cdr-fr-l2结构域,该结构域包含基本上如seq id no:23中所示的序列或者其变体或片段,或者由其组成。
[0238]
抗体或其抗原结合片段可以包含seq id no:24的fr-l3结构域,其在此提供如下:
[0239]
slesgvpsrfsgsgsgteftltisslqpddfatyyc
[0240]
[seq id no:24]
[0241]
因此,优选地,抗体或其抗原结合片段包含cdr-fr-l3结构域,该结构域包含基本上如seq id no:24中所示的序列或者其变体或片段,或者由其组成。
[0242]
抗体或其抗原结合片段可以包含seq id no:25的fr-l4结构域,其在此提供如下:
[0243]
fgqgtkwisn
[0244]
[seq id no:25]
[0245]
因此,优选地,抗体或其抗原结合片段包含fr-l4结构域,该结构域包含基本上如seq id no:25中所示的序列或者其变体或片段,或者由其组成。
[0246]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:22组成的fr-l1结构域、包含或由seq id no:23组成的fr-l2结构域、包含或由seq id no:24组成的fr-l3结构域和/或包含或由seq id no:25组成的fr-l4结构域。然而,优选地,抗体或其抗原结合片段包含:包含或由seq id no:22组成的fr-l1结构域、包含或由seq id no:23组成的fr-l2结构域、包含或由seq id no:24组成的fr-l3结构域以及包含或由seq id no:25组成的fr-l4结构域。
[0247]
抗体或其抗原结合片段可以包含如seq id no:26中所示的轻链序列,其在此提供如下:
[0248]
aiqltqsspstlsasvgdrvtitcrasqsisswlawyqqkpgkapklliykasslesgvpsrfsgsgsgteftltisslqpddfatyycqqygtfgqgtkwisn
[0249]
[seq id no:26]
[0250]
优选地,抗体或其抗原结合片段包含轻链可变区,该轻链可变区包含基本上如seq id no:26中所示的序列或者其变体或片段,或者由其组成。
[0251]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:11组成的cdr-h1结构域、包含或由seq id no:12组成的cdr-h2结构域、包含或由seq id no:13组成的cdr-h3结构域、包含或由seq id no:14组成的fr-h1结构域、包含或由seq id no:15组成的fr-h2结构域、包含或由seq id no:16组成的fr-h3结构域以及包含或由seq id no:17组成的fr-h4结构域。
[0252]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:19组成的cdr-l1结构域、包含或由seq id no:20组成的cdr-l2结构域、包含或由seq id no:21组成的cdr-l3结构域、包含或由seq id no:22组成的fr-l1结构域、包含或由seq id no:23组成的fr-l2结构域、包含或由seq id no:24组成的fr-l3结构域以及包含或由seq id no:25组成的fr-l4结构域。
[0253]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:11组成的cdr-h1结构
域、包含或由seq id no:12组成的cdr-h2结构域、包含或由seq id no:13组成的cdr-h3结构域、包含或由seq id no:19组成的cdr-l1结构域、包含或由seq id no:20组成的cdr-l2结构域和/或包含或由seq id no:21组成的cdr-l3结构域。
[0254]
优选地,抗体或其抗原结合片段包含至少一个、至少两个、至少三个、至少四个、至少五个或至少六个cdr。优选地,抗体或其抗原结合片段至少包含cdr-h3。
[0255]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:11组成的cdr-h1结构域、包含或由seq id no:12组成的cdr-h2结构域;包含或由seq id no:13组成的cdr-h3结构域、包含或由seq id no:19组成的cdr-l1结构域、包含或由seq id no:20组成的cdr-l2结构域以及包含或由seq id no:21组成的cdr-l3结构域。
[0256]
优选地,抗体或其抗原结合片段包含重链可变区和轻链可变区,该重链可变区包含或由seq id no:18组成,并且该轻链可变区包含或由seq id no:26组成。
[0257]
ic008
[0258]
在一个实施方式中,抗体或其抗原结合片段在此被称为ic008(参见图11a和b中所示的表的第2行)。抗体或其抗原结合片段可以包含seq id no:27的cdr-h1结构域,其在此提供如下:
[0259]
ggsisssrhy
[0260]
[seq id no:27]
[0261]
因此,优选地,抗体或其抗原结合片段包含cdr-h1结构域,该结构域包含基本上如seq id no:27中所示的序列或者其变体或片段,或者由其组成。
[0262]
抗体或其抗原结合片段可以包含seq id no:28的cdr-h2结构域,其在此提供如下:
[0263]
idysggt
[0264]
[seq id no:28]
[0265]
因此,优选地,抗体或其抗原结合片段包含cdr-h2结构域,该结构域包含基本上如seq id no:28中所示的序列或者其变体或片段,或者由其组成。
[0266]
抗体或其抗原结合片段可以包含seq id no:29的cdr-h3结构域,其在此提供如下:
[0267]
arqvghsgrghnwfdp
[0268]
[seq id no:29]
[0269]
因此,优选地,抗体或其抗原结合片段包含cdr-h3结构域,该结构域包含基本上如seq id no:29中所示的序列或者其变体或片段,或者由其组成。
[0270]
抗体或其抗原结合片段包含:包含或由seq id no:27组成的cdr-h1结构域、包含或由seq id no:28组成的cdr-h2结构域;和/或包含或由seq id no:29组成的cdr-h3结构域。
[0271]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:27组成的cdr-h1结构域、包含或由seq id no:28组成的cdr-h2结构域以及包含或由seq id no:29组成的cdr-h3结构域。
[0272]
抗体或其抗原结合片段可以包含seq id no:30的fr-h1结构域,其在此提供如下:
[0273]
lvqlqesgprltpsetlsltctvs
[0274]
[seq id no:30]
[0275]
因此,优选地,抗体或其抗原结合片段包含fr-h1结构域,该结构域包含基本上如seq id no:30中所示的序列或者其变体或片段,或者由其组成。
[0276]
抗体或其抗原结合片段可以包含seq id no:31的fr-h2结构域,其在此提供如下:
[0277]
wgwirqppgmglewigs
[0278]
[seq id no:31]
[0279]
因此,优选地,抗体或其抗原结合片段包含fr-h2结构域,该结构域包含基本上如seq id no:31中所示的序列或者其变体或片段,或者由其组成。
[0280]
抗体或其抗原结合片段可以包含seq id no:32的fr-h3结构域,其在此提供如下:
[0281]
ycnpslksrvtisedtsknqfslkvnsvtaadtavyyc
[0282]
[seq id no:32]
[0283]
因此,优选地,抗体或其抗原结合片段包含fr-h3结构域,该结构域包含基本上如seq id no:32中所示的序列或者其变体或片段,或者由其组成。
[0284]
抗体或其抗原结合片段可以包含seq id no:33的fr-h4结构域,其在此提供如下:
[0285]
wgqgtlvtvss
[0286]
[seq id no:33]
[0287]
因此,优选地,抗体或其抗原结合片段包含fr-h4结构域,该结构域包含基本上如seq id no:33中所示的序列或者其变体或片段,或者由其组成。
[0288]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:30组成的fr-h1结构域、包含或由seq id no:31组成的fr-h2结构域、包含或由seq id no:32组成的fr-h3结构域和/或包含或由seq id no:33组成的fr-h4结构域。
[0289]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:30组成的fr-h1结构域、包含或由seq id no:31组成的fr-h2结构域、包含或由seq id no:32组成的fr-h3结构域以及包含或由seq id no:33组成的fr-h4结构域。
[0290]
抗体或其抗原结合片段可以包含如seq id no:34中所示的重链序列,其在此如提供如下:
[0291]
lvqlqesgprltpsetlsltctvsggsisssrhywgwirqppgmglewigsidysggtycnpslksrvtisedtsknqfslkvnsvtaadtavyycarqvghsgrghnwfdpwgqgtlvtvss
[0292]
[seq id no:34]
[0293]
优选地,抗体或其抗原结合片段包含重链可变区,该重链可变区包含基本上如seq id no:34中所示的序列或者其变体或片段,或者由其组成。
[0294]
抗体或其抗原结合片段可以包含seq id no:35的轻链cdr-l1结构域,其在此提供如下:
[0295]
qsiyny
[0296]
[seq id no:35]
[0297]
因此,优选地,抗体或其抗原结合片段包含cdr-l1结构域,该结构域包含基本上如seq id no:35中所示的序列或者其变体或片段,或者由其组成。
[0298]
抗体或其抗原结合片段可以包含seq id no:36的cdr-l2结构域,其在此提供如下:
[0299]
aas
[0300]
[seq id no:36]
[0301]
因此,优选地,抗体或其抗原结合片段包含cdr-l2结构域,该结构域包含基本上如seq id no:36中所示的序列或者其变体或片段,或者由其组成。
[0302]
抗体或其抗原结合片段可以包含seq id no:37的cdr-l3结构域,其在此提供如下:
[0303]
qqsysssvt
[0304]
[seq id no:37]
[0305]
因此,优选地,抗体或其抗原结合片段包含cdr-l3结构域,该结构域包含基本上如seq id no:37中所示的序列或者其变体或片段,或者由其组成。
[0306]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:35组成的cdr-l1结构域、包含或由seq id no:36组成的cdr-l2结构域和/或包含或由seq id no:37组成的cdr-l3结构域。
[0307]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:35组成的cdr-l1结构域、包含或由seq id no:36组成的cdr-l2结构域以及包含或由seq id no:37组成的cdr-l3结构域。
[0308]
抗体或其抗原结合片段可以包含seq id no:38的fr-l1结构域,其在此提供如下:
[0309]
diqmtqspsslsasvgdrvtitcras
[0310]
[seq id no:38]
[0311]
因此,优选地,抗体或其抗原结合片段包含fr-l1结构域,该结构域包含基本上如seq id no:38中所示的序列或者其变体或片段,或者由其组成。
[0312]
抗体或其抗原结合片段可以包含seq id no:39的fr-l2结构域,其在此提供如下:
[0313]
lnwyqqkpgkapkfliy
[0314]
[seq id no:39]
[0315]
因此,优选地,抗体或其抗原结合片段包含fr-l2结构域,该结构域包含基本上如seq id no:39中所示的序列或者其变体或片段,或者由其组成。
[0316]
抗体或其抗原结合片段可以包含seq id no:40的fr-l3结构域,其在此提供如下:
[0317]
tlqtgvpsrfsgsgsgtdftltisslqpedfatyyc
[0318]
[seq id no:40]
[0319]
因此,优选地,抗体或其抗原结合片段包含fr-l3结构域,该结构域包含基本上如seq id no:40中所示的序列或者其变体或片段,或者由其组成。
[0320]
抗体或其抗原结合片段可以包含seq id no:41的fr-l4结构域,其在此提供如下:
[0321]
fgqgtrleik
[0322]
[seq id no:41]
[0323]
因此,优选地,抗体或其抗原结合片段包含fr-l4结构域,该结构域包含基本上如seq id no:41中所示的序列或者其变体或片段,或者由其组成。
[0324]
优选地,抗体或其抗原结合片段包含:含有或由seq id no:38组成的fr-l1结构域、包含或由seq id no:39组成的fr-l2结构域、包含或由seq id no:40组成的fr-l3结构域和/或包含或由seq id no:41组成的fr-l4结构域。
[0325]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:38组成的fr-l1结构域、包含或由seq id no:39组成的fr-l2结构域、包含或由seq id no:40组成的fr-l3结构域以及包含或由seq id no:41组成的fr-l4结构域。
[0326]
抗体或其抗原结合片段可以包含如seq id no:42中所示的轻链序列,其在此提供如下:
[0327]
diqmtqspsslsasvgdrvtitcrasqsiynylnwyqqkpgkapkfliyaastlqtgvpsrfsgsgsgtdftltisslqpedfatyycqqsysssvtfgqgtrleik
[0328]
[seq id no:42]
[0329]
优选地,抗体或其抗原结合片段包含轻链可变区,该轻链可变区包含如seq id no:42中所示的序列或者其变体或片段,或者由其组成。
[0330]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:27组成的cdr-h1结构域、包含或由seq id no:28组成的cdr-h2结构域、包含或由seq id no:29组成的cdr-h3结构域;包含或由seq id no:30组成的fr-h1结构域,包含或由seq id no:31组成的fr-h2结构域,包含或由seq id no:32组成的fr-h3结构域以及包含或由seq id no:33组成的fr-h4结构域。
[0331]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:35组成的cdr-l1结构域、包含或由seq id no:36组成的cdr-l2结构域、包含或由seq id no:37组成的cdr-l3结构域、包含或由seq id no:38组成的fr-l1结构域、包含或由seq id no:39组成的fr-l2结构域、包含或由seq id no:40组成的fr-l3结构域以及包含或由seq id no:41组成的fr-l4结构域。
[0332]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:27组成的cdr-h1结构域、包含或由seq id no:28组成的cdr-h2结构域、包含或由seq id no:29组成的cdr-h3结构域、包含或由seq id no:35组成的cdr-l1结构域、包含或由seq id no:36组成的cdr-l2结构域和/或包含或由seq id no:37组成的cdr-l3结构域。
[0333]
优选地,抗体或其抗原结合片段包含至少一个、至少两个、至少三个、至少四个、至少五个或至少六个cdr。优选地,抗体或其抗原结合片段至少包含cdr-h3。
[0334]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:27组成的cdr-h1结构域、包含或由seq id no:28组成的cdr-h2结构域、包含或由seq id no:29组成的cdr-h3结构域、包含或由seq id no:35组成的cdr-l1结构域、包含或由seq id no:36组成的cdr-l2结构域以及包含或由seq id no:37组成的cdr-l3结构域。
[0335]
优选地,抗体或其抗原结合片段包含重链可变区和轻链可变区,该重链可变区包含或由seq id no:34组成,并且该轻链可变区包含或由seq id no:42组成。
[0336]
ic006
[0337]
在一个实施方式中,抗体或其抗原结合片段在此被称为ic006(参见图11a和b中所示的表的第3行)。抗体或其抗原结合片段可以包含seq id no:43的cdr-h1结构域,其在此提供如下:
[0338]
gftfssya
[0339]
[seq id no:43]
[0340]
因此,优选地,抗体或其抗原结合片段包含cdr-h1结构域,该结构域包含基本上如
seq id no:43中所示的序列或者其变体或片段,或者由其组成。
[0341]
抗体或其抗原结合片段可以包含seq id no:44的cdr-h2结构域,其在此提供如下:
[0342]
isgsggst
[0343]
[seq id no:44]
[0344]
因此,优选地,抗体或其抗原结合片段包含cdr-h2结构域,该结构域包含基本上如seq id no:44中所示的序列或者其变体或片段,或者由其组成。
[0345]
抗体或其抗原结合片段可以包含seq id no:45的cdr-h3结构域,其在此提供如下:
[0346]
akagnsklrffdwlltm
[0347]
[seq id no:45]
[0348]
因此,优选地,抗体或其抗原结合片段包含cdr-h3结构域,该结构域包含基本上如seq id no:45中所示的序列或者其变体或片段,或者由其组成。
[0349]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:43组成的cdr-h1结构域、包含或由seq id no:44组成的cdr-h2结构域和/或包含或由seq id no:45组成的cdr-h3结构域。
[0350]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:43组成的cdr-h1结构域、包含或由seq id no:44组成的cdr-h2结构域以及包含或由seq id no:45其组成的cdr-h3结构域。
[0351]
抗体或其抗原结合片段可以包含seq id no:46的fr-h1结构域,其在此提供如下:
[0352]
qvqlvqsggglvqpggslrlscaas
[0353]
[seq id no:46]
[0354]
因此,优选地,抗体或其抗原结合片段包含fr-h1结构域,该结构域包含基本上如seq id no:46中所示的序列或者其变体或片段,或者由其组成。
[0355]
抗体或其抗原结合片段可以包含seq id no:47的fr-h2结构域,其在此提供如下:
[0356]
mswvrqtpgkglewvsa
[0357]
[seq id no:47]
[0358]
因此,优选地,抗体或其抗原结合片段包含fr-h2结构域,该结构域包含基本上如seq id no:47中所示的序列或者其变体或片段,或者由其组成。
[0359]
抗体或其抗原结合片段可以包含seq id no:48的fr-h3结构域,其在此提供如下:
[0360]
yyadsvkgrftisrdnskntlylqmnslraadtavyyc
[0361]
[seq id no:48]
[0362]
因此,优选地,抗体或其抗原结合片段包含fr-h3结构域,该结构域包含基本上如seq id no:48中所示的序列或者其变体或片段,或者由其组成。
[0363]
抗体或其抗原结合片段可以包含seq id no:49的fr-h4结构域,其在此提供如下:
[0364]
wgqgtlvtvss
[0365]
[seq id no:49]
[0366]
因此,优选地,抗体或其抗原结合片段包含fr-h4结构域,该结构域包含基本上如seq id no:49中所示的序列或者其变体或片段,或者由其组成。
[0367]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:46组成的fr-h1结构域、包含或由seq id no:47组成的fr-h2结构域、包含或由seq id no:48组成的fr-h3结构域和/或包含或由seq id no:49组成的fr-h4结构域。
[0368]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:46组成的fr-h1结构域、包含或由seq id no:47组成的fr-h2结构域、包含或由seq id no:48组成的fr-h3结构域以及包含或由seq id no:49组成的fr-h4结构域。
[0369]
抗体或其抗原结合片段可以包含seq id no:50中所示的重链序列,其在此提供如下:
[0370]
qvqlvqsggglvqpggslrlscaasgftfssyamswvrqtpgkglewvsaisgsggstyyadsvkgrftisrdnskntlylqmnslraadtavyycakagnsklrffdwlltmwgqgtlvtvss
[0371]
[seq id no:50]
[0372]
优选地,抗体或其抗原结合片段包含重链可变区,该重链可变区包含基本上如seq id no:50中所示的序列或者其变体或片段,或者由其组成。
[0373]
抗体或其抗原结合片段可以包含seq id no:51的轻链cdr-l1结构域,其在此提供如下:
[0374]
qsvlyssnnkny
[0375]
[seq id no:51]
[0376]
因此,优选地,抗体或其抗原结合片段包含cdr-l1结构域,该结构域包含基本上如seq id no:51中所示的序列或者其变体或片段,或者由其组成。
[0377]
抗体或其抗原结合片段可以包含seq id no:52的cdr-l2结构域,其在此提供如下:
[0378]
was
[0379]
[seq id no:52]
[0380]
因此,优选地,抗体或其抗原结合片段包含cdr-l2结构域,该结构域包含基本上如seq id no:52中所示的序列或者其变体或片段,或者由其组成。
[0381]
抗体或其抗原结合片段可以包含seq id no:53的cdr-l3结构域,其在此提供如下:
[0382]
qqsysssvt
[0383]
[seq id no:53]
[0384]
因此,优选地,抗体或其抗原结合片段包含cdr-l3结构域,该结构域包含基本上如seq id no:53中所示的序列或者其变体或片段,或者由其组成。
[0385]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:51组成的cdr-l1结构域、包含或由seq id no:52组成的cdr-l2结构域和/或包含或由seq id no:53组成的cdr-l3结构域。
[0386]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:51组成的cdr-l1结构域、包含或由seq id no:52组成的cdr-l2结构域以及包含或由seq id no:53组成的cdr-l3结构域。
[0387]
抗体或其抗原结合片段可以包含seq id no:54的fr-l1结构域,其在此提供如下:
[0388]
diqltqspdslavslgeratinckss
[0389]
[seq id no:54]
[0390]
因此,优选地,抗体或其抗原结合片段包含fr-l1结构域,该结构域包含基本上如seq id no:54中所示的序列或者其变体或片段,或者由其组成。
[0391]
抗体或其抗原结合片段可以包含seq id no:55的fr-l2结构域,其在此提供如下:
[0392]
lawyqqkpgqppklliy
[0393]
[seq id no:55]
[0394]
因此,优选地,抗体或其抗原结合片段包含fr-l2结构域,该结构域包含基本上如seq id no:55中所示的序列或者其变体或片段,或者由其组成。
[0395]
抗体或其抗原结合片段可以包含seq id no:56的fr-l3结构域,其在此提供如下:
[0396]
tresgvpdrfsgsgsgtdftltisslqaedvavyyc
[0397]
[seq id no:56]
[0398]
因此,优选地,抗体或其抗原结合片段包含fr-l3结构域,该结构域包含基本上如seq id no:56中所示的序列或者其变体或片段,或者由其组成。
[0399]
抗体或其抗原结合片段可以包含seq id no:57的fr-l4结构域,其在此提供如下:
[0400]
fgpgtkveik
[0401]
[seq id no:57]
[0402]
因此,优选地,抗体或其抗原结合片段包含fr-l4结构域,该结构域包含基本上如seq id no:57中所示的序列或者其变体或片段,或者由其组成。
[0403]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:54组成的fr-l1结构域、包含或由seq id no:55组成的fr-l2结构域、包含或由seq id no:56组成的fr-l3结构域和/或包含或由seq id no:57组成的fr-l4结构域。
[0404]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:54组成的fr-l1结构域、包含或由seq id no:55组成的fr-l2结构域、包含或由seq id no:56组成的fr-l3结构域以及包含或由seq id no:57组成的fr-l4结构域。
[0405]
抗体或其抗原结合片段可以包含如seq id no:58中所示的轻链序列,其在此提供如下:
[0406]
diqltqspdslavslgeratinckssdiqltqspdslavslgeratincksslawyqqkpgqppklliywastresgvpdrfsgsgsgtdftltisslqaedvavyycqqyystpatfgpgtkveik
[0407]
[seq id no:58]
[0408]
优选地,抗体或其抗原结合片段包含轻链可变区,该轻链可变区包含基本上如seq id no:58中所示的序列或者其变体或片段,或者由其组成。
[0409]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:43组成的cdr-h1结构域、包含或由seq id no:44组成的cdr-h2结构域和/或包含或由seq id no:45组成的cdr-h3结构域、包含或由seq id no:46组成的fr-h1结构域、包含或由seq id no:47组成的fr-h2结构域、包含或由seq id no:48组成的fr-h3结构域以及包含或由seq id no:49组成的fr-h4结构域。
[0410]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:51组成的cdr-l1结构域、包含或由seq id no:52组成的cdr-l2结构域以及包含或由seq id no:53组成的cdr-l3结构域、包含或由seq id no:54组成的fr-l1结构域、包含或由seq id no:55组成的fr-l2
结构域、包含或由seq id no:56组成的fr-l3结构域以及包含或由seq id no:57组成的fr-l4结构域。
[0411]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:43组成的cdr-h1结构域、包含或由seq id no:44组成的cdr-h2结构域、包含或由seq id no:45组成的cdr-h3结构域、包含或由seq id no:51组成的cdr-l1结构域、包含或由seq id no:52组成的cdr-l2结构域和/或包含或由seq id no:53组成的cdr-l3结构域。
[0412]
优选地,抗体或其抗原结合片段包含至少一个、至少两个、至少三个、至少四个、至少五个或至少六个cdr。优选地,抗体或其抗原结合片段至少包含cdr-h3。
[0413]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:43组成的cdr-h1结构域、包含或由seq id no:44组成的cdr-h2结构域、包含或由seq id no:45组成的cdr-h3结构域、包含或由seq id no:51组成的cdr-l1结构域、包含或由seq id no:52组成的cdr-l2结构域以及包含或由seq id no:53组成的cdr-l3结构域。
[0414]
优选地,抗体或其抗原结合片段包含重链可变区和轻链可变区,该链可变区包含或由seq id no:50组成,并且该轻链可变区包含或由seq id no:58组成。
[0415]
ic004
[0416]
在一个实施方式中,抗体或其抗原结合片段在此被称为ic004(参见图11a和b中所示的表的第4行)。抗体或其抗原结合片段可以包含seq id no:59的cdr-h1结构域,其在此提供如下:
[0417]
gftfssyd
[0418]
[seq id no:59]
[0419]
因此,优选地,抗体或其抗原结合片段包含cdr-h1结构域,该结构域包含基本上如seq id no:59中所示的序列或者其变体或片段,或者由其组成。
[0420]
抗体或其抗原结合片段可以包含seq id no:60的cdr-h2结构域,其在此提供如下:
[0421]
igtagdt
[0422]
[seq id no:60]
[0423]
因此,优选地,抗体或其抗原结合片段包含cdr-h2结构域,该结构域包含基本上如seq id no:60中所示的序列或者其变体或片段,或者由其组成。
[0424]
抗体或其抗原结合片段可以包含seq id no:61的cdr-h3结构域,其在此提供如下:
[0425]
ggpsvwlllllrygr
[0426]
[seq id no:61]
[0427]
因此,优选地,抗体或其抗原结合片段包含cdr-h3结构域,该结构域包含基本上如seq id no:61中所示的序列或者其变体或片段,或者由其组成。
[0428]
本发明人令人惊奇地发现,编码ic004的抗体的cdr-h3结构域的核苷酸序列(seq id no:61)在编码色氨酸(w)和亮氨酸(l)的序列之间包含终止密码子,并且如图11a的表中由*所示。尽管在开放阅读框中存在终止密码子,发明人非常惊讶地能够产生全长抗体,该全长抗体包含如seq id no:61中所示的全长cdr-h3序列。鉴于cdh-h3提供抗原结合的多样性的巨大潜力,这是特别显著的,并且在赋予结合活性和特异性方面是重要的。
[0429]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:59组成的cdr-h1结构域、包含或由seq id no:60组成的cdr-h2结构域和/或包含或由seq id no:61组成的cdr-h3结构域。
[0430]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:59组成的cdr-h1结构域、包含或由seq id no:60组成的cdr-h2结构域以及包含或由seq id no:61组成的cdr-h3结构域。
[0431]
抗体或其抗原结合片段可以包含seq id no:62的fr-h1结构域,其在此提供如下:
[0432]
vqlvesggglvqpggslrlscaas
[0433]
[seq id no:62]
[0434]
因此,优选地,抗体或其抗原结合片段包含fr-h1结构域,该结构域包含基本上如seq id no:62中所示的序列或者其变体或片段,或者由其组成。
[0435]
抗体或其抗原结合片段可以包含seq id no:63的fr-h2结构域,其在此提供如下:
[0436]
mhwvrqatgkglewvsa
[0437]
[seq id no:63]
[0438]
因此,优选地,抗体或其抗原结合片段包含fr-h2结构域,该结构域包含基本上如seq id no:63中所示的序列或者其变体或片段,或者由其组成。
[0439]
抗体或其抗原结合片段可以包含seq id no:64的fr-h3结构域,其在此提供如下:
[0440]
yypgsvkgrftisrenaknslylqmnslragdtavyyf
[0441]
[seq id no:64]
[0442]
因此,优选地,抗体或其抗原结合片段包含fr-h3结构域,该结构域包含基本上如seq id no:64中所示的序列或者其变体或片段,或者由其组成。
[0443]
抗体或其抗原结合片段可以包含seq id no:65的fr-h4结构域,其在此提供如下:
[0444]
lgprdhghrll
[0445]
[seq id no:65]
[0446]
因此,优选地,抗体或其抗原结合片段包含fr-h4结构域,该结构域包含基本上如seq id no:65中所示的序列或者其变体或片段,或者由其组成。
[0447]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:62组成的fr-h1结构域、包含或由seq id no:63组成的fr-h2结构域、包含或由seq id no:64组成的fr-h3结构域和/或包含或由seq id no:65组成的fr-h4结构域。
[0448]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:62组成的fr-h1结构域、包含或由seq id no:63组成的fr-h2结构域、包含或由seq id no:64组成的fr-h3结构域以及包含或由seq id no:65组成的fr-h4结构域。
[0449]
抗体或其抗原结合片段可以包含seq id no:66中所示的重链序列,其在此提供如下:
[0450]
evqlvesggglvqpggslrlscaasgftfssydmhwvrqatgkglewvsaigtagdtyypgsvkgrftisrenaknsslylqmnslragdtavyyfggpsvwllllllrygr
[0451]
[seq id no:66]
[0452]
优选地,抗体或其抗原结合片段包含重链可变区,该重链可变区包含基本上如seq id no:66中所示的序列或者其变体或片段,或者由其组成。
[0453]
抗体或其抗原结合片段可以包含seq id no:67的轻链cdr-l1结构域,其在此提供如下:
[0454]
ssnigagyd
[0455]
[seq id no:67]
[0456]
因此,优选地,抗体或其抗原结合片段包含cdr-l1结构域,该结构域包含基本上如seq id no:67中所示的序列或者其变体或片段,或者由其组成。
[0457]
抗体或其抗原结合片段可以包含seq id no:68的cdr-l2结构域,其在此提供如下:
[0458]
gns
[0459]
[seq id no:68]
[0460]
因此,优选地,抗体或其抗原结合片段包含cdr-l2结构域,该结构域包含基本上如seq id no:68中所示的序列或者其变体或片段,或者由其组成。
[0461]
抗体或其抗原结合片段可以包含seq id no:69的cdr-l3结构域,其在此提供如下:
[0462]
qsydsslsgsv
[0463]
[seq id no:69]
[0464]
因此,优选地,抗体或其抗原结合片段包含cdr-l3结构域,该结构域包含基本上如seq id no:69中所示的序列或者其变体或片段,或者由其组成。
[0465]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:67组成的cdr-l1结构域、包含或由seq id no:68组成的cdr-l2结构域和/或包含或由seq id no:69组成的cdr-l3结构域。
[0466]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:67组成的cdr-l1结构域、包含或由seq id no:68组成的cdr-l2结构域以及包含或由seq id no:69组成的cdr-l3结构域。
[0467]
抗体或其抗原结合片段可以包含seq id no:70的fr-l1结构域,其在此提供如下:
[0468]
qsvltqppsvsgaapgqrvtisctgs
[0469]
[seq id no:70]
[0470]
因此,优选地,抗体或其抗原结合片段包含fr-l1结构域,该结构域包含基本上如seq id no:70中所示的序列或者其变体或片段,或者由其组成。
[0471]
抗体或其抗原结合片段可以包含seq id no:71的fr-l2结构域,其在此提供如下:
[0472]
vhwyqqlpgtapklliy
[0473]
[seq id no:71]
[0474]
因此,优选地,抗体或其抗原结合片段包含fr-l2结构域,该结构域包含基本上如seq id no:71中所示的序列或者其变体或片段,或者由其组成。
[0475]
抗体或其抗原结合片段可以包含seq id no:72的fr-l3结构域,其在此提供如下:
[0476]
nrpsgvpdrfsgsksgtsaslaitglqaedeadyyc
[0477]
[seq id no:72]
[0478]
因此,优选地,抗体或其抗原结合片段包含fr-l3结构域,该结构域包含基本上如seq id no:72中所示的序列或者其变体或片段,或者由其组成。
[0479]
抗体或其抗原结合片段可以包含seq id no:73的fr-l4结构域,其在此提供如下:
[0480]
fgggtkltvl
[0481]
[seq id no:73]
[0482]
因此,优选地,抗体或其抗原结合片段包含fr-l4结构域,该结构域包含基本上如seq id no:73中所示的序列或者其变体或片段,或者由其组成。
[0483]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:70组成的fr-l1结构域、包含或由seq id no:71组成的fr-l2结构域、包含或由seq id no:72组成的fr-l3结构域和/或包含或由seq id no:73组成的fr-l4结构域。
[0484]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:70组成的fr-l1结构域、包含或由seq id no:71组成的fr-l2结构域、包含或由seq id no:72组成的fr-l3结构域以及包含或由seq id no:73组成的fr-l4结构域。
[0485]
抗体或其抗原结合片段可以包含seq id no:74中所示的轻链序列,其在此提供如下:
[0486]
qsvltqppsvsgaapgqrvtisctgsssnigagydvhwyqqlpgtapklliygnsnrpsgvpdrfsgsksgtsaslaitglqaedeadyycqsydsslsgsvgggtkltvl
[0487]
[seq id no:74]
[0488]
优选地,抗体或其抗原结合片段包含轻链可变区,该轻链可变区包含基本上如seq id no:74中所示的序列或者其变体或片段,或者由其组成。
[0489]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:59组成的cdr-h1结构域、包含或由seq id no:60组成的cdr-h2结构域和包含或由seq id no:61组成的cdr-h3结构域、包含或由seq id no:62组成的fr-h1结构域、包含或由seq id no:63组成的fr-h2结构域、包含或由seq id no:64组成的fr-h3结构域以及包含或由seq id no:65组成的fr-h4结构域。
[0490]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:67组成的cdr-l1结构域、包含或由seq id no:68组成的cdr-l2结构域和包含或由seq id no:69组成的cdr-l3结构域、包含或由seq id no:70组成的fr-l1结构域、包含或由seq id no:71组成的fr-l2结构域、包含或由seq id no:72组成的fr-l3结构域以及包含或由seq id no:73组成的fr-l4结构域。
[0491]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:59组成的cdr-h1结构域、包含或由seq id no:60组成的cdr-h2结构域、包含或由seq id no:61组成的cdr-h3结构域、包含或由seq id no:67组成的cdr-l1结构域、包含或由seq id no:68组成的cdr-l2结构域和/或包含或由seq id no:69组成的cdr-l3结构域。
[0492]
优选地,抗体或其抗原结合片段包含至少一个、至少两个、至少三个、至少四个、至少五个或至少六个cdr。优选地,抗体或其抗原结合片段至少包含cdr-h3。
[0493]
优选地,抗体或其抗原结合片段包含:包含或由seq id no:59组成的cdr-h1结构域、包含或由seq id no:60组成的cdr-h2结构域、包含或由seq id no:61组成的cdr-h3结构域、包含或由seq id no:67组成的cdr-l1结构域、包含或由seq id no:68组成的cdr-l2结构域以及包含或由seq id no:69组成的cdr-l3结构域。
[0494]
优选地,抗体或其抗原结合片段包含重链可变区和轻链可变区,该重链可变区包
含seq id no:66或由其组成,并且该轻链可变区包含seq id no:74或由其组成。
[0495]
优选地,抗体或其抗原结合片段可以包含在此披露的cdr和/或fr序列的任何组合。
[0496]
此外,如isaacs等人(1998);j.immun.;161:3862-3869(“therapy with monoclonal antibodies
–
the contribution of the fc gamma receptor binding and the influence of ch1and ch3 domains on in vivo effector function(用单克隆抗体治疗-fcγ受体结合的贡献以及ch1和ch3结构域对体内效应子功能的影响)”)中所描述的,本发明的抗体或抗原结合片段可以在对fcγr结合关键的基序内包含一个或多个突变。例如,突变可以包括谷氨酸233至脯氨酸、亮氨酸/苯丙氨酸234至缬氨酸、和/或亮氨酸235至丙氨酸取代。
[0497]
有利地,根据本发明的第一方面的抗体或其抗原结合片段以其本身作为治疗剂具有实用性,并且可以用于冠状病毒感染的治疗、改善或预防中。
[0498]
因此,在本发明的第二方面,提供了根据第一方面的抗体或其抗原结合片段在治疗中的用途。
[0499]
在本发明的第三方面,提供了根据第一方面的抗体或其抗原结合片段在治疗、预防或改善冠状病毒感染中的用途。
[0500]
根据本发明的第四方面,提供了一种治疗、预防或改善受试者中的冠状病毒感染的方法,该方法包括向需要这种治疗的患者施用或已经施用治疗有效量的根据第一方面的抗体或其抗原结合片段。
[0501]
优选地,冠状病毒感染是如第一方面中定义的冠状病毒的感染。
[0502]
在次所描述的抗体或抗原结合片段可以提供给受试者接种抗冠状病毒感染的有效手段。
[0503]
因此,在本发明的第五方面,提供了包含根据第一方面的抗体或其抗原结合片段的疫苗。
[0504]
优选地,疫苗包含合适的佐剂。佐剂可以是编码的分子佐剂或作为被掺入到递送制剂中的佐剂。
[0505]
掺入到递送制剂中的佐剂可以选自由以下各项组成的组:细菌脂肽、脂蛋白和脂磷壁酸;分支杆菌脂聚糖;酵母的酵母聚糖、(膜)孔蛋白、脂多糖、脂质a、单磷酰脂质a(mpl)、鞭毛蛋白、cpg dna、疟原虫色素、皂(角)苷(quil-a、qs-21、番茄碱糖苷、iscom、iscomatrixtm)、基于角鲨烯的乳液、聚合物如pei、卡波普、脂质纳米颗粒和细菌毒素(ct、lt)。
[0506]
在本发明的第六方面,提供了根据第一方面的抗体或其抗原结合片段或根据第五方面的疫苗在受试者中刺激免疫应答的用途。
[0507]
可以刺激免疫应答抗冠状病毒,优选地sars-cov、mers-cov和/或sars cov2感染。
[0508]
应当理解的是,根据本发明的抗体、其片段或疫苗(在此统称为“试剂”)可以用于单一疗法中(例如,单独使用抗体或其抗原结合片段),用于治疗、改善或预防冠状病毒感染。可替代地,根据本发明的试剂可以用作用于治疗、改善或预防冠状病毒感染的已知疗法的辅助或与已知疗法组合。
[0509]
根据本发明的试剂可以组合在具有多种不同形式的组合物中,特别地取决于组合
物待使用的方式。因此,例如,组合物可以是以下形式:粉末、片剂、胶囊、液体、软膏、乳膏、凝胶、水凝胶、气溶胶、喷雾、胶束溶液、透皮贴剂、脂质体悬浮液或可以施用给需要治疗的人或动物的任何其他适合的形式。应当理解,根据本发明的药物的载体应该是施用它的受试者良好耐受的载体。
[0510]
可以通过多种方式使用包含本发明的试剂的药物。例如,可以需要口服施用,在这种情况下,试剂可以被包含在组合物中,该组合物可以例如,以片剂、胶囊或液体的形式被口服摄取。包含本发明的试剂和药物的组合物可以通过吸入(例如,鼻内)施用。还可以配制组合物用于局部使用。例如,乳膏或软膏可以施用于皮肤。
[0511]
根据本发明的试剂和药物还可以结合在缓释或延迟释放装置中。这样的装置可以例如被插入在皮肤上或皮下,并且药物可以被释放数周或甚至数月。至少邻近治疗部位可以定位装置。当需要用根据本发明使用的试剂长期治疗时,并且正常地需要频繁施用(例如,至少每天注射),这样的装置可以是特别地有利的。
[0512]
在优选的实施方式中,根据本发明的试剂和药物可以通过注射到血流中或直接注射到需要治疗的部位来施用给受试者。注射可以是静脉内(推注或输注)或皮下(推注或输注)或皮内(推注或输注)。
[0513]
应当理解,所需的抗体和片段(即,试剂)的量由其生物活性和生物利用度决定,这接着取决于施用模式,试剂的生理化学性质以及其是用作单一疗法还是用于联合疗法。施用的频率还将受正在治疗的受试者体内的试剂的半衰期影响。待施用的最佳剂量可以由本领域技术人员确定,并且将随使用的特定试剂、药物组合物的强度、施用模式和冠状病毒感染的进展而变化。取决于所治疗的特定受试者的另外的因素将导致需要调整剂量,包括受试者年龄、体重、性别、饮食、以及施用时间。
[0514]
通常,取决于哪种试剂,根据本发明的试剂在0.001μg/kg体重与10mg/kg体重之间的每日剂量可以用于治疗、改善或预防冠状病毒感染。更优选地,试剂的每日剂量是在0.01μg/kg体重与1mg/kg体重之间,更优选地在0.1μg/kg与100μg/kg体重之间,并且最优选地在约0.1μg/kg与10μg/kg体重之间。
[0515]
可以在冠状病毒感染发作之前、期间或之后施用试剂。可以作为单次施用(例如,每日单次注射)给出每日剂量。可替代地,在一天期间可以需要试剂施用两次或更多次。作为实施例,试剂可以作为0.07μg与700mg(即,假定体重为70kg)之间的两次(或更多次,取决于正在治疗的冠状病毒感染的严重性)每日剂量施用。接受治疗的患者在醒来时可以服用第一剂量,并且然后在晚上,或在此之后以3小时或4小时的间隔,服用第二剂量(如果涉及两次剂量方案)。可替代地,可以使用缓释装置来向患者提供根据本发明的试剂的最佳剂量,而无需施用重复剂量。已知的程序,例如制药工业常规采用的那些(例如,体内实验、临床试验等),可以用于形成根据本发明的试剂的特定制剂以及精确的治疗方案(例如,试剂的每日剂量以及施用的频率)。
[0516]
在本发明的第七方面,提供了一种药物组合物,该药物组合物包含根据第一方面的抗体或其抗原结合片段,或根据第五方面的疫苗,以及可选地药物学上可接受的载体。
[0517]
药物组合物优选地为抗冠状病毒组合物,即,用于治疗性改善、预防或治疗受试者中的冠状病毒感染(如sars-cov、mers-cov和/或sars cov2感染)的药物制剂。
[0518]
本发明在第八方面中还提供了用于制备根据第四方面的药物组合物的方法,该方
法包括将治疗有效量的如第一方面中定义的抗体或其抗原结合片段,或根据第五方面的疫苗与药物学上可接受的载体组合。
[0519]
抗体或其抗原结合片段可以是如相对于第一方面所定义的。
[0520]“受试者”可以是脊椎动物、哺乳动物或家畜。因此,根据本发明的药物可以用于治疗任何哺乳动物,例如家畜(例如马)、宠物,或可以用于其他兽医应用中。最优选地,受试者是人类。
[0521]
抗体或其抗原结合片段的“治疗有效量”是任何量,该任何量是当给受试者施用时,治疗冠状病毒感染或产生期望效果所需的试剂的量。
[0522]
例如,所使用的抗体或其片段的治疗有效量可以是从约0.001ng至约1mg,并且优选地从约0.01ng至约100ng。抗体或片段的量优选地为约0.1ng至约10ng,并且最优选地约0.5ng至约5ng的量。
[0523]
如在此提及的“药物学上可接受的载体”是本领域技术人员已知的在配制药物组合物中有用的任何已知的化合物或已知化合物的组合。
[0524]
在一个实施方式中,药物学上可接受的载体可以是固体,并且组合物可以是粉末或片剂的形式。固体药物学上可接受的载体可以包括一种或多种物质,该一种或多种物质还可以充当调味剂、润滑剂、增溶剂、悬浮剂、染料、填充剂、助流剂、压缩助剂、惰性粘合剂、甜味剂、防腐剂、染料、包衣或片剂崩解剂。载体还可以是封装材料。在粉末中,载体是与根据本发明的精细分散的活性剂混合的精细分散的固体。在片剂中,活性剂可以与具有必要压缩特性的载体以合适的比例混合,并且以所期望的形状和尺寸被压实。粉末和片剂优选地包含高达99%的活性剂。合适的固体载体包括例如,磷酸钙、硬脂酸镁、滑石、糖、乳糖、糊精、淀粉、明胶、纤维素、聚乙烯吡咯烷、低熔点蜡和离子交换树脂。在另一个实施方式中,药物载体可以是凝胶,并且组合物可以是乳膏等的形式。
[0525]
然而,药物载体可以是液体,并且药物组合物是溶液的形式。液体载体用于制备溶液、悬浮液、乳液、糖浆、酏剂以及加压组合物。根据本发明的活性剂可以溶解或悬浮在药物学上可接受的液体载体中,例如水、有机溶剂、二者的混合物或药物学上可接受的油或脂肪。液体载体可以包含其他合适的药物添加剂,如增溶剂、乳化剂、缓冲剂、防腐剂、甜味剂、调味剂、悬浮剂、增稠剂、着色剂、粘度调节剂、稳定剂或渗透调节剂。用于口服和胃肠外施用的液体载体的合适实施例包括水(部分包含上述添加剂,例如纤维素衍生物,优选羧甲基纤维素钠溶液)、醇(包括一元醇和多元醇,例如乙二醇)及其衍生物和油(例如,分馏的椰子油和花生油)。对于肠胃外施用,载体还可以是油酯,如油酸乙酯和豆蔻酸异丙酯。无菌液体载体在用于肠胃外施用的无菌液体形式组合物中是有用的。用于加压组合物的液体载体可以是卤代烃或其他药物学上可接受的推进剂。
[0526]
液体药物组合物是无菌溶液或悬浮液,可以通过例如肌内、鞘内、硬膜外、腹膜内、静脉内,并且特别地皮下注射来利用。试剂可制备为无菌固体组合物,其可在施用时使用无菌水、盐水或其他合适的无菌注射介质溶解或悬浮。
[0527]
本发明的试剂和组合物可以按无菌溶液或悬浮液的形式口服施用,该无菌溶液或悬浮液含有其他溶质或悬浮剂(例如,足以使溶液等渗的盐水或葡萄糖)、胆汁盐、阿拉伯胶、明胶、脱水山梨醇单油酸酯、聚山梨醇酯80(山梨醇的油酸酯及其与环氧乙烷共聚的酸酐)等。根据本发明使用的试剂还可以以液体或固体组合物形式口服施用。适合于口服施用
的组合物包括固体形式,如丸剂、胶囊、颗粒、片剂、以及粉末,以及液体形式,如溶液、糖浆、酏剂以及悬浮液。可用于肠胃外施用的形式包括无菌溶液、乳液和悬浮液。
[0528]
如在此所讨论的,本发明的抗体能够结合sars-cov、mers-cov和sars cov2的刺突蛋白s2结构域,该结构域充当表位。这个发现表明,抗体或其抗原结合片段可以用作用于检测冠状病毒感染的加强的诊断工具。
[0529]
因此,根据第九方面,提供了用于诊断受试者中的冠状病毒感染,或预后受试者的状况的方法,该方法包括检测获自受试者的样品中冠状病毒的存在,其中使用根据第一方面的抗体或抗原结合片段实现检测。
[0530]
根据第十方面,提供了根据第一方面的抗体或抗体结合片段在诊断或预后中的用途。
[0531]
根据本发明的第十一方面,提供了根据第一方面的抗体或抗体结合片段在诊断或预后冠状病毒感染中的用途。
[0532]
根据本发明的第十二方面,提供了用于诊断患有冠状病毒感染的受试者,或用于提供受试者状况的预后的试剂盒,该试剂盒包括根据第一方面的用于检测来自测试受试者的样品中的冠状病毒的抗体或其抗原结合片段。
[0533]
优选地,与第九至第十二方面中任一项有关的冠状病毒如第一方面中所定义。
[0534]
预后可以涉及确定已经被诊断患有冠状病毒感染的受试者中的治疗结果。预后可涉及预测受试者中冠状病毒感染的进展或改善的速率和/或持续时间、存活的概率和/或各种治疗方案的功效。因此,不良预后可以指示冠状病毒感染进展、低存活概率和治疗方案降低的功效。有利的预后可以指示冠状病毒感染消退、高存活概率和治疗方案增加的功效。
[0535]
优选地,样品包括生物样品。样品可以是从受试者可获得的任何材料,从该材料可获得蛋白质。
[0536]
生物样品可以是组织或生物流体。生物样品可以是从受试者可获得的任何材料,从该材料可获得单核细胞。此外,样品可以是血液、血浆、血清、脊髓液、尿液、汗液、唾液、泪液、胸腔抽吸物、母乳、前列腺液、精液、阴道液、粪便、子宫颈刮屑、细胞、羊水、眼内液、粘液、呼吸中的水分、动物组织、细胞裂解物、肿瘤组织、毛发、皮肤、口腔刮屑、淋巴液、间质液、指甲、骨髓、软骨、朊病毒、骨粉、盯聍、淋巴液、肉芽肿、癌症活组织检查或其组合。
[0537]
样品可以是液体抽吸物。例如,样品可以是支气管肺泡灌洗(bal)、腹水、胸膜灌洗或心包灌洗。
[0538]
样品可以包括血液、尿液、组织等。在一个优选的实施方式中,生物样品包括血液样品。血液可以是静脉或动脉血液。可以立即测定血液样品。可替代地,在进行方法之前,血液样品可以在低温下储存,例如冰箱中或甚至冷冻。可替代地,在进行方法之前,血液样品可以储存在室温下,例如18摄氏度至22摄氏度之间。血液样品可以包括血清。血液样品可以包括血浆。然而,优选地,对全血进行检测,最优选地,血液样品是外周血。
[0539]
可以在执行第一方面的使用之前进一步处理血液。例如,可以添加抗凝剂,如柠檬酸盐(如柠檬酸钠)、水蛭素、肝素、ppack或氟化钠。因此,样品采集容器可以包含抗凝剂,以防止血液样品凝结。
[0540]
本发明还延伸到以上鉴定的冠状病毒的表位作为抗原用于生产本发明的抗体或抗体片段的用途。
[0541]
因此,在本发明的第十三方面,提供了如第一方面中所定义的刺突蛋白s2结构域或刺突蛋白结构域的区域作为抗原的用途。
[0542]
优选地,抗原充当抗体结合的表位。
[0543]
优选地,抗原包含基本上如seq id no:6中所示的序列或者其变体或片段,或者由其组成。
[0544]
在第十四方面,提供了通过以下方法获得的抗体或其抗原结合片段,该方法包括:
[0545]
(i)用如第一方面中所定义的刺突蛋白s2结构域或刺突蛋白结构域的区域免疫宿主生物体;以及
[0546]
(ii)从宿主收集抗体或其抗原结合片段。
[0547]
宿主可以是哺乳动物,并且可以是人、兔或小鼠。
[0548]
优选地,方法包括使宿主动物出血,并且然后优选地从血液,最优选地血清中收集抗体或其抗原结合片段。优选地,使血清通过具有共价结合的肽载体的重力柱。洗涤之后,优选地,在缓冲液中洗脱抗体或其抗原结合片段,缓冲液优选地是酸性缓冲液,并且然后可以中和溶液。方法可以进一步包括凭借适合的缓冲液(例如,pbs)进行渗析,和可选地冻干。
[0549]
在本发明的第十五方面中,提供了编码如第一方面中所定义的抗体或其抗原结合片段的多核苷酸序列。
[0550]
在本发明的第十六方面,提供了包含根据第十五方面的多核苷酸序列的表达盒。
[0551]
编码本发明的抗体或其抗原结合片段的多核苷酸序列优选地被携带在重组载体中,例如用于递送到目的宿主细胞中的重组载体,以使得能够产生抗体或其抗原结合片段。
[0552]
因此,在本发明的第十七方面,提供了包含根据第十六方面的表达盒的重组载体。
[0553]
编码第一方面的抗体或其抗原结合片段的载体可以是例如,质粒、粘粒或噬菌体和/或病毒载体。此类重组载体在用于使用核苷酸序列转化细胞的本发明的递送系统中是高度有用的。核苷酸序列可以优选地是dna序列,并且这个dna序列编码抗体或其抗原结合片段序列,形成第二方面的抗体或其抗原结合片段。
[0554]
编码第一方面的抗体或其抗原结合片段的重组载体还可以包括其他功能元件。例如,它们可进一步包含多种其他功能元件,包括用于在将载体引入宿主细胞中时启动转基因表达的合适启动子。例如,载体优选地能够在宿主细胞的细胞核中自主复制。在这种情况下,在重组载体中可能需要诱导或调节dna复制的元件。可替代地,可以设计重组载体使得它整合到宿主细胞的基因组中。在这种情况下,设想有利于靶向整合(例如,通过同源重组)的dna序列。适合的启动子可以包括sv40启动子、cmv、ef1a、pgk、病毒长末端重复序列,连同诱导型启动子,例如四环素诱导型系统,作为实例。盒或载体还可以包含终止子,例如β球蛋白、sv40聚腺苷酸化序列或合成的聚腺苷酸化序列。重组载体还可以包含启动子或调节子或增强子,以根据需要控制核酸的表达。
[0555]
载体还可以包含编码基因的dna,所述基因可以用作克隆过程中的选择标记,即,使得能够选择已经转染或转化的细胞,并且使得能够选择携带载体的细胞,该载体掺入了异源dna。例如,设想氨苄青霉素、新霉素、嘌呤霉素或氯霉素的抗性。可替代地,选择标记基因可以在与含有转基因的载体同时使用的不同载体中。盒或载体还可以包含dna,该dna涉及调节核苷酸序列的表达,或用于将表达的多肽靶向宿主细胞的某个部分。
[0556]
纯化的载体可以通过合适的方法直接插入到宿主细胞中,例如,直接胞吞摄取。通
过转染、感染、电穿孔、显微注射、细胞融合、原生质体融合、磷酸钙、基于阳离子脂质的脂质转染、基于聚合物或树枝状聚合物的方法或弹道轰击,可以将载体直接地引入到宿主细胞(例如,真核或原核细胞)中。可替代地,可以使用粒子枪将本发明的载体直接地引入到宿主细胞中。
[0557]
可替代地,递送系统可向宿主细胞提供多核苷酸,而不将其掺入载体中。例如,核酸分子可以掺入在脂质体或病毒颗粒内。可替代地,“裸”多核苷酸可以通过适合的手段,例如直接胞吞摄取,插入到宿主细胞中。
[0558]
在本发明的第十八方面,提供了包含根据第十五方面的多核苷酸序列,根据第十六方面的表达盒或根据十七方面的载体的宿主细胞。
[0559]
宿主细胞可以是真核或原核宿主细胞。优选地,宿主细胞是真核宿主细胞。更优选地,宿主细胞是哺乳动物宿主细胞,如nso鼠骨髓瘤细胞、人细胞、人胚肾293细胞或中国仓鼠卵巢(cho)细胞。最优选地,宿主细胞是cho细胞。
[0560]
在第十九方面,提供了制备根据第一方面的抗体或抗原结合片段的方法,该方法包括:
[0561]
a)将第十七方面的载体引入到宿主细胞中;以及
[0562]
b)在导致根据第一方面的抗体或抗原结合片段的产生的条件下,培养宿主细胞。
[0563]
步骤a)的宿主细胞可以是真核或原核宿主细胞。优选地,宿主细胞是真核宿主细胞。更优选地,宿主细胞是哺乳动物宿主细胞,如nso鼠骨髓瘤细胞、人细胞、人胚肾293细胞或中国仓鼠卵巢(cho)细胞。最优选地,宿主细胞是cho细胞。
[0564]
方法可以进一步包括(c)收获、离心和/或过滤细胞培养基,以获得包含抗体或其抗原结合片段的细胞培养物上清液。
[0565]
方法可以进一步包括(d)从细胞培养物上清液,分离和纯化抗体或其抗原结合片段。优选地,通过至少一个层析步骤,进行纯化。
[0566]
合适的层析步骤包括亲和层析和/或离子交换层析。优选地,亲和层析是蛋白a层析。离子交换层析可以是阴离子交换层析和/或阳离子交换层析。
[0567]
优选地,步骤(d)包括通过以下方式,从细胞培养物上清液,分离和纯化抗体或其抗原结合片段:
[0568]
i)蛋白a层析;
[0569]
ii)阴离子交换层析;和/或
[0570]
iii)阳离子交换层析。
[0571]
方法可以进一步包括(e)过滤自步骤(d)产生的纯化的抗体或其抗原结合片段。优选地,步骤(e)包括病毒过滤。因此,优选地,使用病毒过滤膜,过滤从步骤(d)产生的纯化的抗体或其抗原结合片段。合适的膜是本领域技术人员已知的。
[0572]
应当理解,本发明延伸至任何核酸或肽或其变体、衍生物或类似物,其基本上包含在此提及的任何序列的氨基酸或核酸序列,包括其变体或片段。术语“基本上氨基酸/核苷酸/肽序列”、“变体”和“片段”可以是与在此提及的任何一种序列的氨基酸/核苷酸/肽序列具有至少40%序列同一性的序列,例如与被鉴定为seq id no:1-89的序列具有40%同一性的序列,等等。
[0573]
还设想了与所提及的任何序列具有大于65%、更优选地大于70%、甚至更优选地
大于75%、并且还更优选地大于80%序列同一性的序列同一性的氨基酸/多核苷酸/多肽序列。优选地,氨基酸/多核苷酸/多肽序列与在此提及的任何序列具有至少85%同一性,更优选地至少90%同一性,甚至更优选地至少92%同一性,甚至更优选地至少95%同一性,甚至更优选地至少97%同一性,甚至更优选地至少98%同一性,并且最优选地至少99%同一性。
[0574]
技术人员将理解如何计算两个氨基酸/多核苷酸/多肽序列之间的百分比同一性。为了计算两个氨基酸/多核苷酸/多肽序列之间的百分比同一性,必须首先准备两个序列的比对,随后计算序列同一性值。两个序列的百分比同一性可以取不同的值,这取决于:(i)用于比对序列的方法,例如clustalw、blast、fasta、smith-waterman(在不同的程序中实施),或来自3d比较的结构比对;和(ii)比对方法使用的参数,例如,局部比对对整体比对,使用的对记分矩阵(例如,blosum62、pam250、gonnet等),以及空位罚分,例如,函数形式和常数。
[0575]
在进行比对后,存在计算两个序列之间的百分比同一性的许多不同方式。例如,可以将同一性的数除以:(i)最短序列的长度;(ii)比对的长度;(iii)序列的平均长度;(iv)非空位位置的数;或(v)排除突出端的等效位置的数。此外,应当理解,百分比同一性也强烈依赖于长度。因此,一对序列越短,可以预期偶然发生的序列同一性越高。
[0576]
因此,应当理解,蛋白质或dna序列的准确比对是复杂的过程。流行的多重比对程序clustalw(thompson等人,1994,nucleic acids research,22,4673-4680;thompson等人,1997,nucleic acids research,24,4876-4882)是用于产生根据本发明的蛋白质或dna的多重比对的优选方式。clustalw的适合的参数可以如下:对于dna比对:空位开放罚分=15.0,空位延伸罚分=6.66,并且矩阵=同一性。对于蛋白质比对:空位开放罚分=10.0,空位延伸罚分=0.2,并且矩阵=gonnet。对于dna和蛋白质比对:endgap=-1,并且gapdist=4。本领域技术人员将意识到,可能需要改变这些和其他参数,以用于最佳序列比对。
[0577]
优选地,两个氨基酸/多核苷酸/多肽序列之间的百分比同一性的计算然后可以从如(n/t)*100的比对来计算,其中n是序列共享相同残基的位置的数,并且t是比较的位置的总数,包括空位,并且包括或排除突出端。优选地,在计算中包括突出端。因此,用于计算两个序列之间的百分比同一性的最优选的方法包括:(i)使用clustalw程序,使用合适的参数集合,准备序列比对,例如,如上所述;以及(ii)将n和t的值插入下式:序列同一性=(n/t)*100。
[0578]
用于鉴定类似序列的替代方法是本领域技术人员已知的。例如,基本上相似的核苷酸序列将由在严格条件下与dna序列或其互补序列杂交的序列编码。通过严格条件,发明人意指在约45℃下在3x氯化钠/柠檬酸钠(ssc)中与过滤结合的dna或rna杂交,随后在约20-65℃下在0.2xssc/0.1% sds中进行至少一次洗涤的核苷酸。可替代地,基本上相似的多肽可以与例如,seq id no:1至89的那些(它们是氨基酸序列)中示出的序列相差至少1、但少于5、10、20、50或100个氨基酸。
[0579]
由于遗传密码的简并性,清楚的是在此所描述的任何核酸序列可以变化或改变而基本上不影响由其编码的蛋白质的序列,以提供其功能变体。合适的核苷酸变体是具有通过编码序列内的相同氨基酸的不同密码子的取代而改变的序列,从而产生沉默(同义)变化的那些。其他合适的变体是具有同源核苷酸序列,但包含全部或部分序列的变体,所述序列通过编码氨基酸的不同密码子的取代而改变,所述氨基酸具有与其取代的氨基酸类似的生物物理特性的侧链,以产生保守改变。例如,小的非极性疏水性氨基酸包括甘氨酸、丙氨酸、
亮氨酸、异亮氨酸、缬氨酸、脯氨酸和甲硫氨酸。大的非极性疏水性氨基酸包括苯丙氨酸、色氨酸和酪氨酸。极性中性氨基酸包括丝氨酸、苏氨酸、半胱氨酸、天冬酰胺和谷氨酰胺。带正电荷的(碱性)氨基酸包括赖氨酸、精氨酸和组氨酸。带负电荷的(酸性)氨基酸包括天冬氨酸和谷氨酸。因此,应当理解,哪些氨基酸可以被具有相似生物物理特性的氨基酸替换,并且本领域技术人员将知道编码这些氨基酸的核苷酸序列。
[0580]
在此所描述的所有特征(包括任何所附权利要求、摘要和附图)和/或如此公开的任何方法或过程的所有步骤可以通过任何组合方式与任何上述方面组合,除了这样的特征和/或步骤中的至少一些相互排斥的组合之外。
[0581]
为了更好地理解本发明,并且示出可以如何实施本发明的实施方式,现在将通过实施例的方式参照附图,在附图中:
[0582]
图1显示了在sars恢复期血清中与sars特异性igg比较时mers特异性igg的elisa结果。来自sars恢复期群组的血清通过elisa显示与sars-cov对mers-cov的刺突蛋白结合,表明两种病毒之间的血清学交叉反应性。
[0583]
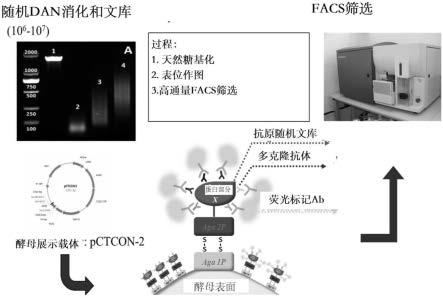
图2显示了用于血清抗体谱的酵母表面展示抗原文库(ysdl)平台。
[0584]
图3显示了sars-刺突酵母文库和mers-刺突酵母文库。来自sars和mers的刺突蛋白的ysdl用于筛选sars恢复期血清,并且鉴定了s蛋白的s2结构域中的交叉反应性抗体表位。
[0585]
图4显示了本发明人使用ysdl的高通量人mab克隆策略。
[0586]
图5显示了新的单克隆抗体克隆方法,其表明相比于2个月的标准方案,在图4中总结的策略在所需的时间方面更有效,将发展时间减少至2周。
[0587]
图6显示了顶部4cov-bnmab对293t细胞中表达的sars-cov-2的s蛋白的膜形式的结合特异性。
[0588]
图7显示了交叉反应性抗mers cov s mab结合酵母刺突2。
[0589]
图8显示了本发明的单克隆抗体中和假型mers-cov。
[0590]
图9显示了先前公布的数据,其显示sars-cov和mers-cov融合至靶细胞的膜。
[0591]
图10a和10b显示了sars-cov、mers-cov和sars-cov2刺突蛋白之间的序列比对。
[0592]
图11a和11b显示了发明人发现抗sars-cov、mers-cov和sars-cov2的令人惊奇地交叉反应性的四种抗体的重链和轻链序列。
[0593]
图12显示了mers-cov、sars-cov和sars-cov-2中s2区的交叉反应性结构域的序列。
[0594]
图13显示了发明人研发的单克隆抗体结合和中和sars-cov、mers-cov和sars-cov-2。a)热图总结通过elisa以1μg/ml结合sars-cov、mers-cov和sars-cov-2的第十七种mab。b)描述结合所有三种冠状病毒的mab的数的饼图。n=9。c)通过elisa,mab与sars-cov、mers-cov和sars-cov-2刺突蛋白的剂量依赖性结合。实验重复三次。计算平均值和sd。d)mab对假病毒sars-cov、mers-cov和sars-cov-2的中和效力。绘制假病毒抑制的百分比。数据代表两次独立研究。虚线表示病毒感染性的50%减少(ic50)。通过非线性回归计算ic50。e)通过具有真实sars-cov、mers-cov和sars-cov-2的细胞病变效应(cpe)的mab的中和效力。用病毒感染vero细胞,并且通过与未感染的对照比较对保护进行记分。显示了用和不用mab处理的感染细胞的代表性图。f)以100μg/ml下,mab抗sars-cov、mers-cov和sars-cov-2
介导的细胞融合的抑制活性。显示了与具有ace2/dpp4表达的huh7细胞的刺突转染的293t细胞共温育的mab的代表性图。
[0595]
图14显示了抗体的结合亲和力和mab的表位作图。a)使用纯化的mab对荧光标记的sars-cov、mers-cov和sars-cov刺突三聚体的微量热泳(mst)-结合曲线。使用nanotemper分析1.2.101计算标准化的荧光,并且将其作为mab浓度的函数作图。通过在prism 8.4.3中的hill方程的非线性回归计算有效的一半最大结合(ec50),n=3。b)通过结合的交叉抑制来定义抗体表位。将cr3022用作指导mab以区分抗rbd抗体。将流感和埃博拉抗体用作非抑制对照。如以下方法中所述,使用从患者克隆的mab通过elisa来测试彼此的抑制作用。红色表示生物素化的抗体对竞争抗体的抑制,而绿色表示没有抑制,n=3。c)对覆盖sars-cov-2刺突的重叠肽文库筛选所选择的mab。d)所识别的肽表示在sars-cov刺突单体的结构上,pdb:6vxx。e)显示了sars-cov、mers-cov和sars-cov中每一者中的刺突蛋白s2结构域中的p1和p2表位的实施方式。
[0596]
图15显示了总结抗体的中和潜能的表。
[0597]
图16显示了ace2与作为参照的刺突的结合亲和力。
[0598]
图17显示了mab与刺突的s1和s2区的结合。如所预期的,所有mab识别sars-cov-2的s2区,但不识别s1区。
[0599]
图18显示了抗体ic001、ic005、ic009、ic010、ic013、ic008、ic004、ic03和ic006抗各种突变体或变体的冠状病毒的中和百分比,包括(i)类似于sars-cov的两种蝙蝠冠状病毒变体,即wiv116和ratg13;(ii)sars-cov-2貂突变体;(iii)sars-cov-2b1.1.7变体(kent突变体);和(iv)sars-cov-2b.1.351变体(南非变体)。
实施例
[0600]
本发明人最初提出了产生具有冠状病毒sars-cov与mers-cov之间的交叉反应性的抗体。由于新的高度致病性冠状病毒(由who在2020年2月11日重命名为sars-cov-2)爆发,发明人延伸了他们的工作以产生与多种冠状病毒毒株(包括sars-cov、mers-cov和sars-cov-2)交叉反应的抗体。序列比对发现,与mers-cov(35%)相比,sars-cov-2的s蛋白(抗体应答的主要靶)与sars-cov(77%)共享更高的同源性。
[0601]
发明人假设,由sars患者产生的一些cov单克隆抗体,除了mers-cov和sars-cov外,还可以与sars-cov-2交叉反应,本发明人获得的数据显示cov单克隆抗体可以特异性地结合293t细胞表面上表达的sars-cov-2s蛋白,以及mers-cov和sars-cov s蛋白。因此,本发明人认为,他们第一个研发了对sars-cov-2、mers-cov和sars-cov s显示交叉反应性的抗体,提供可以用于检测和治疗所有已知和未来的冠状病毒感染的泛冠状病毒抗体。
[0602]
材料和方法
[0603]
构建sars-cov、mers-cov和sars cov2的ysd刺突文库。
[0604]
使用扩展高保真pcr系统(expand high fidelity pcr system)(目录号11732650001,roche),通过pcr,扩增编码sars-cov、mers-cov和sars cov2刺突的dna序列。然后将pcr产物纯化、消化和连接至pctcon2载体。将连接产物转化到感受态tg1细胞中。测序后,制备具有100%同源性的重组质粒,并且相应地称为pctcon2-sars-cov、mers-cov和sars cov2。然后,使用gene pμlser xcell
tm
完全系统(目录编号165
–
2660,bio-rad),经由
ep 0.1mm基因脉冲发生器比色杯(目录号165-2089,bio-rad),用pctcon2
–
sars-cov、mers-cov和sars cov2转化感受态eby100细胞,使用的ep参数为1.2kv、25uf和电阻200ω。然后,在30℃,培养酵母细胞1h,随后在sdcaa板上铺展,并且在30℃,培养48h。从选择性平板挑取单个菌落,并且在sdcaa培养基中培养,随后在sgcaa培养基中诱导表面片段表达。通过用流式细胞术,分析c-myc标记的表面表达来验证sars-cov、mers-cov和sars cov2刺突片段的表面表达。对于表位作图,在4℃,在sgcaa培养基中培养30h之后,通过流式细胞术,用不同稀释度的sars患者的血清分析表达片段的酵母细胞。
[0605]
通过ysd文库进行的血清谱分析(facs分选和酵母测序)
[0606]
如前所描述的,基于酵母表面展示(ysd)文库进行血清谱分析(zuo et al.2011;guo etal.2015)。简而言之,构建sars-cov、mers-cov和sars-cov-2刺突的组合片段文库,并分别地展示在酵母表面上,用于抗体染色和荧光激活细胞分选(facs)。具体而言,消化全长的刺突基因,并且将其pcr重组成100bp-1000bp的片段的范围,将重组的片段凝胶纯化,并且克隆到酵母表面展示载体中。然后,使用电穿孔,将克隆的产物转化到感受态酵母细胞系eby100中。
[0607]
诱导酵母文库,并且与单独的或混合的sars血清温育,使用aria iii(bd,usa),通过facs阳性分选。展示相应的抗原片段的分选的阳性酵母克隆被收获,并且编码相应片段的质粒被提取,并且对质粒进行测序和序列分析。
[0608]
通过酵母克隆和mab产生,分离单记忆b细胞
[0609]
从被酵母刺突结合的单个b细胞,分离单克隆抗体。将来自sars患者的pbmc用冷的胎儿牛血清在4℃解冻,并且然后与bv421标记的mers刺突酵母以1:2的比率共培养。然后洗涤pbmc mers刺突酵母混合物,并且将cd19
+
bv421
+
细胞单细胞分选到含有10μl rna酶抑制rt-pcr捕获缓冲液(5ml无rna酶的水、50μl 1m tris ph 8以及125μl rnasin(promega)的96孔板中。将板立即密封,并且在干冰上冷冻和在-80℃下储存。通过添加15μl rt-pcr反应混合物,在原始分选板中合成单细胞cdna。rt-pcr反应混合物包含1μl正向引物混合物(1.2μm)、1μl反向引物混合物(1.2μm)、1μl dntps(200μm)、5μl 10*缓冲液、0.5μl pcr酶混合物和6.5μl h2o。使用hotstartaq pcr试剂盒,在第二轮pcr反应中扩增单独的igh和igl(k或λ)基因。在连接到igh/igl表达载体的可变基因克隆位点中之前,用agei/sali或agei/xhoi分别地消化igh和igλ基因。表达载体包括鼠免疫球蛋白信号肽下游的适当的人恒定区和氨苄青霉素抗性基因。对igk产物进行测序,并且根据其基因家族通过另一轮pcr进行扩增。然后,将它们用agei/bsiwi消化,然后连接到igk表达载体中。将含有igh和igl链的质粒与pei(聚氮丙啶)混合,并且转染到人胚肾成纤维细胞293t细胞中。转染后24小时,用dmem/pbs洗涤细胞,然后在无蛋白培养基中培养。转染后5-6天收集上清液。
[0610]
抗体纯化
[0611]
在收集上清液之前,将用vh和vl质粒转染的293t细胞在pf ultradoma(lonza)中培养5天,过滤(0.2μm),并且用mnase(2.5u/ml)处理120分钟。然后,将上清液加载到填充有蛋白a珠的柱中,并且在用甘氨酸ph 2.7洗脱和用tris-hcl ph8中和之前,用pbs洗涤三次。随后用pbs缓冲液交换纯化的抗体,并储存在-80℃中。
[0612]
elisa结合
[0613]
用1.5μg/ml的抗his(abcam)抗体涂覆nunc elisa板,在4℃过夜。然后用pbst洗涤
板,并在室温,用3%bsa(sigma)封闭1小时。将sars-cov、mers-cov和sars-cov2刺突三聚体以与抗his抗体相同的浓度添加到板中。然后,将mab或患者血清以各种稀释度添加至板。在添加抗人igg碱性磷酸酶(sigma)之前,将板洗涤两次。pbst洗涤后,使用pnpp(对硝基苯磷酸)溶液(sigma)来产生用于od读数的颜色。
[0614]
体外中和测定
[0615]
在微量中和(mn)测定中,分析mab抗sars cov、mers cov和sars cov2毒株的中和活性。将vero-e6细胞以3x10^4细胞/孔接种在10x 96孔板上的dmem+10% fbs+1% p/s中。将单克隆抗体在96孔u-底板中的一式四份柱中系列稀释(三个用于cpe记分,一个用于无病毒对照nvc/细胞毒性对照)。将60μl纯dmem添加至行b至h,并且将60μl稀释的抗体添加至行a和b。通过将60μl混合抗体从行b至c向下转移至行h,用多通道移液管将mab系列稀释。
[0616]
将60μl稀释的病毒添加至稀释抗体的三列,并且将60μl纯dmem添加至nvc柱中,在37℃孵育一小时。然后将100μl的抗体-病毒混合物转移至具有vero-e6细胞的培养板中,从行h至行a。每个孔包含浓度起始于10、5、2.5、1.25、0.625、0.313、0.156和0.078μg/ml的100tcid50病毒和抗体。将vero细胞、mab和病毒混合物在5% co2、37℃温育箱中温育72小时。对记录表中的细胞病变效应(cpe)进行记分,并且确定抗100x tcid 50病毒的中和抗体浓度。参照无病毒对照(nvc),100x tcid50病毒接种物报告为对cpe起因的完全保护的中和滴度。
[0617]
体外中和测定
[0618]
基于酵母表面展示(ysd)文库进行mab的表位作图。构建sars-cov、mers-cov和sars cov2刺突的组合片段文库,并在酵母表面展示,用于抗体染色和荧光激活细胞分选(facs)。具体而言,消化全长的刺突基因,并且将其pcr重组成100bp-900bp片段的范围,将重组的片段进行凝胶纯化,并且克隆到酵母表面展示载体中。然后,使用电穿孔,将克隆的产物转化到感受态酵母细胞系eby100中。诱导酵母文库,并且与每种抗mers/sarscov/sarscov2 mab温育,使用aria 11i(bd,usa),通过facs阳性分选。展示相应抗原片段的分选阳性酵母克隆被收获,并且编码相应片段的质粒被提取和对该质粒进行测序和序列分析。
[0619]
蛋白质表达和纯化
[0620]
sars-cov和mers-covs胞外域蛋白由g.gao*友好地惠赠。为了表达covid19 s胞外域,合成了编码covid19刺突的残基1-1208的基因(基因库:yp009724390.1)、c-末端t4纤维蛋白三聚化基序、hrv3c蛋白酶切割位点、streptag,并且克隆到昆虫表达载体pfbdm中。使用tn7转座方法,将表达载体转化到bacmids中。用sf9细胞进行转染和病毒扩增,并且使用hi5细胞(invitrogen)来产生重组蛋白。通过streptrap hp 5ml柱(ge healthcare)从细胞上清液捕获可溶性s蛋白。将洗脱产物混合,并且通过凝胶过滤层析法,用superose 6 10/300gl(ge healthcare)柱进一步纯化,该柱用含有20mm tris
–
hcl(ph 8.0)、150mm nacl和1mm edta的缓冲液平衡。
[0621]
结果与讨论
[0622]
参考图1,显示了来自sars恢复期群组的血清,通过elisa显示与sars-cov对mers-cov的刺突蛋白结合,表明两种病毒之间存在血清学交叉反应性。
[0623]
发明人使用酵母表面展示抗原文库(ysdl)平台用于血清抗体谱,如图2所示。使用来自sars和mers的刺突蛋白的ysdl,本发明人能够筛选sars恢复期血清,以鉴定交叉反应
性抗体表位。特别地,鉴定了s蛋白的s2结构域,如图3所示。发明人利用高通量单克隆抗体(mab)筛选策略,如图4所示,使用ysdl。该策略被证明在产生抗体所需的时间方面更有效,将时间减少至2周,与基于标准方案的2个月相比(图5)。
[0624]
然后,本发明人试验了四种令人惊奇地有效的cov-bnmab对293t细胞中表达的sars-cov-2的s蛋白的膜形式的结合特异性。图11a和图11b中提供了四种抗体序列。如图6中所示,抗体能够结合s蛋白。发明人还证实了交叉反应性抗mers cov s mab结合酵母刺突2蛋白的能力,如图7所示。
[0625]
发明人使用它们的系统克隆了总共270个mab,这些mab展示出独特的vdj序列。它们通过酶联免疫吸附测定(elisa)筛选抗sars-cov、sars-cov-2和mers-cov刺突的mab(图13a),其中9个与所有三个刺突结合。
[0626]
结合曲线以微摩尔至纳摩尔的亲和力展示了mab与sars-cov、mers-cov刺突和sars-cov-2刺突的可比的抗体亲抗原性(图13c)。特别地,ic001是特别地有效,并且与sars-cov和mers-cov以纳摩尔亲和力结合。然后发明人试验了抗sars-cov、mers-cov和sars-cov-2假病毒的mab的中和。与公开的结果相反,发明人发现抗s2 mab还中和sars-cov-2假病毒(ic50:2.2μg/ml至8.1μg/ml)(图18d)。mab在三种冠状病毒中显示出抗sars-cov的最佳中和效果(ic50:1.8μg/ml至4.7μg/ml)。ic001在mab中显示出对sars-cov(1.8μg/ml)和mers-cov(2.9μg/ml)两者的最强中和能力,这与其对三种冠状病毒的刺突蛋白的高结合的抗体亲抗原性相关(图13c)。
[0627]
此外,ic001还显示出抗突变体sars-cov-2假病毒(包括sars-cov-2貂突变体、sars-cov-2b1.1.7(kent突变体))以及类似于sars-cov的两种蝙蝠冠状病毒(即,ratg13和wiv16)的中和。有趣的是,ic006显示对sars-cov-2、b1.1.17和b.1.351(南非)突变体的中和,但对蝙蝠冠状病毒没有中和,这可能表明表位在蝙蝠冠状病毒中不是保守的(图18)。
[0628]
为了评估抗真实活病毒的抗体中和,本发明人用mab对活sars-cov、mers-cov和sars-cov-2进行细胞病变效应(cpe)抑制测定。ic001显示出抗所有三种冠状病毒的完全中和(sars-cov和mers-cov为5μg/ml,sars-cov-2为10μg/ml)。ic006在10μg/ml下显示出抗sars-cov和sars-cov-2的完全中和(图13e)。ic001和ic006的中和潜能与它们对三种冠状病毒刺突的结合的抗体亲抗原性相关(图15)。为了进一步研究mab的中和机制,发明人试验了这些mab的融合抑制能力。ic001显示出分别地抗sars-cov-2和mers-cov的60%和80%融合抑制,与其中和能力一致。另一方面,ic008显示出抗sars-cov-2而不是抗mers-cov的强的融合抑制,进一步证实了它的中和效力(图13f)。
[0629]
通过微量热泳(mst)测定来测量mab与三种冠状病毒刺突蛋白之间的特异性相互作用。mst数据显示ic001分别地以520nm和586nm的类似亲和力与sars-cov和sars-cov-2刺突相互作用。它以857nm的亲和力结合mers-cov刺突(图14a)。相反,ic006以类似的亲和力(分别地为1.4μm和1.5μm)结合sars-cov和mers-cov刺突,但比sars-cov-2(2.1μm)弱得多。发明人还测量了ace2与作为参照的刺突的结合亲和力(83nm)(图16)。尽管ic001的结合亲和力是ace2约7倍弱,但ic001的中和能力仍与具有比ace2高10倍的亲和力的mab相当。然后,发明人尝试用三种测定来定义mab的表位。首先,它们测量mab与刺突的s1和s2区的结合。如所预期的,所有mab识别sars-cov-2的s2区,但不识别s1(图17)。其次,发明人测量mab彼此的结合的竞争性抑制。他们发现ic001和ic008共享相似的表位,而ic006、ic003、ic007
和ic013共享相似的表位(图14b)。第三,发明人量化mab与覆盖s2区的重叠肽的结合。ic001与hr1区强力地结合,而ic006与fp区结合(图14c)。发明人已经能够基于这些数据在s2区中鉴定两个共享的表位区,在图14d中突出为p1和p2。
[0630]
结论
[0631]
最近已在大量新出现的病原体优先级列表,即,ukvn、who蓝图和cepi中鉴定了冠状病毒家族,强调了提高我们对冠状病毒免疫应答的理解的迫切需要,以控制当前问题,并为新出现的威胁做好准备。大量的基因上不同的cov以及cov的人类群体与动物贮主之间增加的界面表明,在人类中存在新的cov人畜共患感染的显著风险。实际上,sars-cov爆发、mers-cov爆发以及最近的sars-cov-2爆发已经证明是这种情况。目前,在人类中没有可用于cov感染的有效治疗或疫苗,这主要是由于野生动物中cov家族的多样性以及从动物宿主到人类的周期性人畜共患的传染。
[0632]
发明人已经证明了酵母展示系统所鉴定的三个β冠状病毒的s2区上的新表位。据他们所知,他们首先产生识别,并且结合sars-cov、sars-cov-2和mers-cov的刺突的mab。这些mab有利地中和所有三种β冠状病毒,并且能够进行泛冠状病毒中和。
[0633]
因此,用于高致病性cov,基于人cov广泛中和性mab(cov-bnmab)的免疫疗法的发明人的研发将致力于解决立即未满足的医学需要,并且可以证明不仅对于目前已知的人cov,而且对于未来未知的新出现大流行性cov的快速治疗。
[0634]
此外,考虑到与大流行性人cov感染(特别地在老年人中)相关的高死亡率,开发有效的广谱抗体(例如,在此所描述的抗体)仍然是非常重要的事情。这些抗体不仅用于治疗受感染患者,而且用于诊断感染,并且还用于处于风险中的一线卫生保健人员的预防性保护,以及可以被储存抗未来的爆发。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1