靶向BCMA的嵌合抗原受体及其用途的制作方法
靶向bcma的嵌合抗原受体及其用途
技术领域
1.本发明涉及靶向bcma的嵌合抗原受体及其用途,更详细地,涉及靶向bcma的抗体、包含上述抗体的嵌合抗原受体、表达上述嵌合抗原受体的嵌合抗原受体-t细胞(car-t)。
背景技术:
2.嵌合抗原受体(car)t细胞是为了生成显出特定抗癌活性的嵌合蛋白,使对目标抗原的基于抗体的特异性与t细胞受体激活胞内结构域组合的分子。通常,嵌合抗原受体包含细胞外抗原结合结构域、跨膜结构域及细胞内信号转导结构域。细胞外抗原结合结构域可以包含已确认的肿瘤抗原为靶向的单链可变片段(single-chain variable fragment;scfv)。
3.嵌合抗原受体可以利用基因转染技术在作为免疫效应细胞(immune effector cell)的t细胞的表面上表达。当在t细胞表面表达的嵌合抗原受体与靶向肿瘤抗原结合时,嵌合抗原受体能够激活t细胞来以抗原依赖的方式着手特定的抗肿瘤反应。
4.另一方面,已知为cd269或tnfrsf17的b细胞成熟抗原(b-cell maturation antigen:bcma)为肿瘤坏死因子(tumor necrosis factor)受体家族的成员。据报告,bcma可以与b细胞激活因子受体(b-cell activating factor receptor:baff)及b细胞增殖诱导配体(b-cell proliferation-inducing ligand:april)结合来在不同的发育阶段促进b细胞的存活。非正常的信号转导引起b细胞的非正常增殖,从而可能引起多发性骨髓瘤等自身免疫疾病(autoimmune diseases)及肿瘤发生(tumorigenesis)(rickert,et al.,immunological reviews,2011,vol.244:115-133)。
5.多发性骨髓瘤为因浆细胞的非正常分化及增殖而引起的血液癌的一种,该疾病生成肿瘤并因溶解骨质而诱发疼痛。不仅如此,多发性骨髓瘤还侵犯骨髓,减少白细胞、红细胞、血小板的数值,从而增加贫血、感染、出血的风险。进而,骨髓瘤细胞还生成作为非正常免疫蛋白的m蛋白(m protein),这使血液的浓度增加,引起血液高黏滞综合征或损伤肾脏。
6.多发性骨髓瘤的部分治疗方法与其他癌症的治疗方法相似,例如,化学治疗方法或放射线治疗方法、干细胞移植或骨髓移植、靶向化的治疗方法或生物学治疗方法。基于抗体的细胞免疫疗法对血液学的恶性肿瘤,尤其是对患有b细胞非霍奇金淋巴瘤的患者的实际上的临床有益性已得到了确认,但大部分患者出现复发或二次排斥的问题,因此需要用于治疗多发性骨髓瘤的免疫治疗激动剂,为此,正在研究利用嵌合抗原受体-t细胞的治疗方法(ellebrecht et al.,science 353:179-184,2016;carpenter et al.,clin cancer res,19(8):2048-2060,2013;wo2016-014789;wo 2016/014565;wo 2013/154760)。
技术实现要素:
7.技术问题
8.在本发明中,为开发多发性骨髓瘤等与b细胞相关疾病的治疗剂而多番努力的结果,筛选了靶向bcma的抗体,通过使上述筛选的抗bcma抗体人类化(humanized antibody)
来最终制备了靶向bcma的嵌合抗原受体及嵌合抗原受体-t细胞。确认到上述制备的bcma靶向嵌合抗原受体-t细胞与bcma结合,确认到有效杀灭表达bcma的肿瘤细胞。
9.因此,本发明的目的在于,提供靶向bcma的抗体及包含上述抗体的嵌合抗原受体。
10.本发明的再一目的在于,提供编码靶向bcma的嵌合抗原受体的多核苷酸、包含其的载体以及表达包含上述多核苷酸或载体的嵌合抗原受体的免疫效应细胞。
11.本发明的还有一目的在于,提供一种用于预防或治疗与bcma的表达相关的疾病的药物组合物,包含上述表达靶向bcma的嵌合抗原受体的免疫效应细胞。
12.技术方案
13.为了实现上述目的,本发明提供一种与bcma(b-cell maturation antigen)特异性结合的抗体或其片段,包含:重链可变区,包含由序列1的氨基酸序列表示的cdr1区域、由序列2的氨基酸序列表示的cdr2区域及由序列3的氨基酸序列表示的cdr3区域;以及轻链可变区,包含由序列4的氨基酸序列表示的cdr1区域、由序列5的氨基酸序列表示的cdr2区域及由序列6的氨基酸序列表示的cdr3区域。
14.在本发明的一优选实施例中,上述抗体可以为由序列7的氨基酸序列所表示的重链可变区及序列8的氨基酸序列所表示的轻链可变区构成的抗体或者由序列13的氨基酸序列所表示的重链可变区及序列14的氨基酸序列所表示的轻链可变区构成的抗体。
15.并且,本发明提供一种嵌合抗原受体(chimeric antigen receptor:car),上述嵌合抗原受体包含bcma-结合结构域、跨膜结构域(transmembrane domain)、共刺激结构域(costimulatory domain)以及细胞内信号转导结构域(intracellular signal transduction domain),上述bcma-结合结构域包含能够与bcma特异性结合的抗体或其片段,上述抗体包含:重链可变区,包含由序列1的氨基酸序列表示的cdr1区域、由序列2的氨基酸序列表示的cdr2区域及由序列3的氨基酸序列表示的cdr3区域;以及轻链可变区,包含由序列4的氨基酸序列表示的cdr1区域、由序列5的氨基酸序列表示的cdr2区域及由序列6的氨基酸序列表示的cdr3区域。
16.在本发明的一优选实施例中,上述跨膜结构域可以源自选自由cd8α、cd4、cd28、cd137、cd80、cd86、cd152及pd1组成的组中的蛋白质。
17.在本发明的再一优选实施例中,上述共刺激结构域可以源自选自由cd28、4-1bb、ox-40及icos组成的组中的蛋白质,上述信号转导结构域可以源自cd3ζ。
18.在本发明的另一优选实施例中,还可以包含位于上述bcma-结合结构域的c末端与跨膜结构域的n末端之间的铰链区(hinge region),上述铰链区可以源自cd8α。
19.为了实现再一目的,本发明提供编码上述嵌合抗原受体的多核苷酸。
20.并且,本发明提供包含编码嵌合抗原受体的多核苷酸的载体。
21.在本发明的一优选实施例中,上述载体可以为质粒(plasmid)、逆转录病毒(retroviral)载体或慢病毒(lentiviral)载体。
22.并且,本发明提供包含编码上述嵌合抗原受体的多核苷酸或包含编码嵌合抗原受体多核苷酸的载体且表达上述嵌合抗原受体的免疫效应细胞。
23.在本发明的一优选实施例中,上述免疫效应细胞可以为t细胞。
24.为了实现另一目的,本发明提供一种用于预防或治疗与bcma的表达相关的疾病的药物组合物,包含表达靶向bcma的嵌合抗原受体的免疫效应细胞或与bcma特异性结合的抗
体或其片段。
25.在本发明的一优选实施例中,上述与bcma的表达相关的疾病可以为多发性骨髓瘤(multiple myeloma)、血液癌、非霍奇金淋巴瘤(non-hodgkin's lymphoma)、自身抗体依赖性自身免疫性疾病(autoantibody-dependent autoimmune disease)、系统性红斑狼疮(systemic lupus erythematosus,sle)或类风湿关节炎(rheumatoid arthritis)。
26.发明的效果
27.确认到本发明中制备的靶向bcma的嵌合抗原受体及嵌合抗原受体-t细胞与作为抗原的bcma特异性结合,实现与bcma结合的嵌合抗原受体-t细胞的激活。
28.并且,确认到本发明的嵌合抗原受体-t细胞有效杀灭表达bcma的细胞,因此,本发明的靶向bcma的嵌合抗原受体及嵌合抗原受体-t细胞能够有用地用作用于预防或治疗与b细胞或bcma的表达相关的疾病的组合物。
附图说明
29.图1为确认人类化的抗bcma单克隆抗体(3g4v2)的bcma结合能力的数据。
30.图2示出表达靶向bcma的嵌合抗原受体(hbcma-car)慢病毒载体及在t细胞中表达的嵌合抗原受体的示意图。
31.图3为示出利用表达hbcma-car的慢病毒制备hbcma-嵌合抗原受体-t细胞的方法的示意图。
32.图4为确认hbcma-嵌合抗原受体-t细胞的bcma结合能力的数据。
33.图5是为了确认hbcma-嵌合抗原受体-t细胞的激活,在靶向细胞存在的条件下确认通过3g4v2-嵌合抗原受体t细胞表达ifnγ及cd107a的程度的数据。
34.图6为确认通过hbcma-嵌合抗原受体-t细胞杀灭靶向细胞的效果的数据。
具体实施方式
35.以下,详细说明本发明。
36.靶向bcma的抗体
37.本发明的一实施方式涉及一种与bcma特异性结合的抗体或其片段,包含:重链可变区,包含由序列1的氨基酸序列表示的cdr1区域、由序列2的氨基酸序列表示的cdr2区域及由序列3的氨基酸序列表示的cdr3区域;以及轻链可变区,包含由序列4的氨基酸序列表示的cdr1区域、由序列5的氨基酸序列表示的cdr2区域及由序列6的氨基酸序列表示的cdr3区域。
38.在本发明中,上述抗体可以为单克隆抗体(monoclonal antibody)。在本发明中,术语“单克隆抗体”称为monoclonal antibody或单克隆抗体,作为由单抗体形成细胞生成的抗体,具有一级结构(氨基酸排列)均匀的特征。只识别一个抗原决定基,通常通过培养融合癌细胞与抗体生成细胞的杂交瘤细胞(hybridoma cell)来生产,但也可以通过利用获得的抗体基因序列来利用其它重组蛋白表达宿主细胞来生产。
39.在本发明中,术语“抗体”不仅可以使用具有两个全长的轻链及两个全长的重链的完整形态,还可以使用抗体分子的片段。抗体分子的片段是指至少保有肽标签(表位)结合功能的片段,包括scfv、fab、f(ab')、f(ab')2、单结构域(single domain)等。
40.在抗体片段中,fab为具有轻链、重链的可变区、轻链的恒定区以及重链的第一个恒定区(ch1)的结构,具有一个抗原结合部位。fab'在重链ch1结构域的c末端具有包含一个以上的半胱氨酸残基的铰链区(hinge region),从这一点来说,是与fab不同的。f(ab')2抗体是通过fab'的铰链区的半胱氨酸残基形成二硫键来生成的。fv为只具有重链可变区及轻链可变区的最小的抗体片段,国际公开专利第wo 88/10649号、第wo 88/106630号、第wo 88/07085号、第wo 88/07086号及wo 88/09344号中公开了生产fv片段的技术。双重链fv(dsfv)通过二硫键连接重链可变区与轻链可变区,单链fv(scfv)通常通过肽接头以共价键连接重链的可变区与轻链的可变区。这样的抗体片段可以利用蛋白水解酶来获得(例如,可以使用木瓜蛋白酶有限切割整个抗体来获得fab,使用胃蛋白酶切割可以获得f(ab')2片段),优选地,可以通过基因重组技术来制备。
41.本发明的与bcma特异性结合的单克隆抗体可以利用上述bcma蛋白的全部或部分肽作为免疫原(或抗原)来制备。更详细地,根据需要将上述bcma、包含上述bcma蛋白的融合蛋白或包含上述bcma蛋白质的载体(carrier)作为优选免疫原与作为免疫增强剂的佐剂(adjuvant)(例如,弗氏佐剂(freund adjuvant))一同向除人类以外的哺乳动物的皮下、肌肉、静脉、足凸肉或腹腔内注射一次以上来免疫致敏(immunization)。优选地,上述除人类以外的哺乳动物为小鼠、大鼠、仓鼠、豚鼠、鸡、兔、猫、狗、猪、山羊、绵羊、驴、马或牛(包括用来生产人类抗体的转化(transgenic)小鼠等以生产其他动物源性抗体为目的制备的转化(transgenic)动物),更优选地,为小鼠、大鼠、仓鼠、豚鼠、鸡或兔。从第一次免疫开始,约每1天~21天实施1次~4次免疫,在最终免疫约1天~10天后,可以从免疫致敏的哺乳动物中获得生产抗体的细胞。可以根据所使用的免疫原的特征等来适当变更免疫致敏的次数及时间间隔。
42.可以根据凯拉及米尔斯坦等的方法(nature,1975,vol.256,p.495-497)及以此为准的方法制备分泌单克隆抗体的杂交瘤细胞。可以通过将选自由从上述免疫致敏的除人类以外的动物中采取的脾脏、淋巴结、骨髓或扁桃体组成的组中的任一种,优选地,将脾脏中所包含的生产抗体的细胞与没有产生自身抗体的能力的源自哺乳动物的骨髓瘤细胞(myeloma cells)融合为细胞来制备杂交瘤细胞(hybridoma)
43.细胞融合可以利用例如通过聚乙二醇或仙台病毒等融合促进剂或者通过电脉冲的方法,例如,在含有融合促进剂的培养基中使抗体生产细胞与能够无限增殖的源自哺乳动物的细胞以约1∶1至1∶10的比例悬浮,在此状态下以约30℃至40℃的温度培养约1分钟至5分钟。融合培养基使用例如mem培养基、rpmi1640培养基及iscove改良的杜氏伊戈尔培养基(iscove's modified dulbecco's medium)等通常的普通培养基即可,优选地,排除牛血清等血清类。
44.筛选生产上述单克隆抗体的杂交瘤细胞克隆的方法,首先,将如上所述获得的融合细胞移到hat培养基等筛选用培养基,以约30℃至40℃的温度培养3天至3周来杀灭除杂交瘤细胞以外的细胞。接着,在微量滴定板(microtiter plate)等中培养杂交瘤细胞后,可以通过放射免疫法(ria,radioactive substance-marked immuno antibody)或酶联免疫吸附测定(elisa,enzyme-linked immunosorbent assay)等免疫分析方法寻找增加与上述除人类以外的动物的免疫反应中所使用的免疫原及上清液的反应性的部分。然后,在上述内容中找到的生产单克隆抗体的克隆显出对上述免疫原的特异性的结合力。
45.本发明的单克隆抗体可以通过在生物体内外培养上述杂交瘤细胞来获得。上述培养利用用于培养哺乳动物来源的细胞的通常的方法,为了从培养物等中采取单克隆抗体,利用本发明所属技术领域中通常用于纯化抗体的方法。各种方法可以为例如盐析、透析、过滤、浓缩、离心分离、分别沉淀、凝胶过滤层析、离子交换层析、亲和层析、高效液相色谱、凝胶电泳及等电点电泳等,可以根据需要组合来应用。然后,浓缩、干燥纯化的单克隆抗体来根据用途制备为液体或固体。
46.并且,本发明的单克隆抗体可以通过如下方法获得,即,通过聚合酶链式反应(pcr)方法或化学合成分别合成编码重链及轻链可变区的脱氧核糖核酸(dna)、分别与编码重链及轻链的正常区域的基础脱氧核糖核酸(例如,参照日本第2007-252372号公报)分别连接的基因后,移植到能够表达上述基因的公知的载体等来制备转化体后,通过在cho细胞或大肠杆菌等宿主中表达来生产抗体,从这些培养液中利用蛋白a或g(protein a或g)柱等纯化抗体来获得。
47.在本发明的一具体实施例中,制备并筛选与bcma特异性结合的小鼠抗体来确立新型的抗体,将其命名为3g4。
48.确认到上述3g4抗体包含:重链可变区,包含由序列1的氨基酸序列(gytftsyv)表示的cdr1区域、由序列2的氨基酸序列(iipyndgt)表示的cdr2区域及由序列3的氨基酸序列(arwnwdgyfdv)表示的cdr3区域;以及轻链可变区,包含由序列4的氨基酸序列(ksllhsngity)表示的cdr1区域、由序列5的氨基酸序列(qms)表示的cdr2区域及由序列6的氨基酸序列(tqnlelpft)表示的cdr3区域。
49.优选地,上述3g4抗体由序列7的氨基酸序列所表示的重链可变区及序列8的氨基酸序列所表示的轻链可变区构成,并且,3g4抗体的重链可变区可以由序列9的碱基序列编码,3g4抗体的轻链可变区可以由序列10的碱基序列编码。在上述3g4抗体以scfv形态存在的情况下,能够以轻链可变区-接头-重链可变区的方式连接,优选地,可以由序列11的氨基酸序列表示,或由序列12的碱基序列编码。
50.在本发明的再一具体实施例中,将作为抗bcma抗体的3g4制备为变更为与人类相对应的结构的人类化的抗体(humanized antibody),将其命名为3g4v2。
51.上述3g4v2的重链可变区cdr和轻链可变区cdr与3g4相同,使除cdr部分以外的剩余部分人类化。优选地,3g4v2由序列13的氨基酸序列所表示的重链可变区及序列14的氨基酸序列所表示的轻链可变区构成,并且,3g4v2抗体的重链可变区可以由序列15的碱基序列编码,3g4v2抗体的轻链可变区可以由序列16的碱基序列编码。在上述3g4抗体以scfv形态存在的情况下,能够以轻链可变区-接头-重链可变区的方式连接,优选地,可以由序列17的氨基酸序列表示,或由序列18的碱基序列编码。
52.在本发明的还有一具体实施例中,确认作为人类化的抗bcma抗体的3g4v2是否与bcma特异性结合的结果,如图1所示,在不表达hbcma的a549细胞中未确认到与3g4v2的结合,但确认到增加了3g4v2与表达hbcma的a549细胞的结合能力。
53.因此,在本发明中,利用作为人类化的抗bcma抗体的3g4v2制备靶向bcma的嵌合抗原受体
54.在本发明中,术语“人类化抗体”是指拥有与通过人类生产的抗体相应的氨基酸序列和/或利用本技术中公开的用于制备人类抗体的技术中心的一种来制备的抗体。人类化
抗体的定义特定排除包含非人类抗原结合残基的人类化抗体。
55.并且,应该来理解的是,本发明包含的蛋白质、多肽和/或氨基酸序列包括至少具有与蛋白质或多肽相同或相似功能的功能性变异体(functional variants)或同源体。
56.在本发明中,功能性变异体可以为在上述蛋白质和/或多肽的氨基酸序列中取代、缺失或添加一个以上氨基酸来获得的蛋白质或多肽。功能性变异体实质上可以保留未变形的蛋白质或多肽(取代、缺失、添加)的生物学特性。例如,功能性变异体可以保留原蛋白质或多肽的生物学活性(如抗原结合能力)的至少60%、70%、80%、90%或100%。
57.在本发明中,同源体可以为与上述蛋白质和/或多肽具有与85%以上(例如,约85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或以上)的氨基酸序列同源性的蛋白质或多肽(例如能够与bcma或其片段特异性结合的抗体)。
58.在本发明中,同源性通常是指两个以上序列之间的相似性或相关性。
59.靶向bcma的嵌合抗原受体(chimeric antigen receptor)
60.本发明的再一实施方式涉及一种嵌合抗原受体,包含bcma-结合结构域、跨膜结构域、共刺激结构域以及细胞内信号转导结构域,其特征在于,上述bcma-结合结构域包含能够与bcma特异性结合的抗体或其片段,上述抗体包含:重链可变区,包含由序列1的氨基酸序列表示的cdr1区域、由序列2的氨基酸序列表示的cdr2区域及由序列3的氨基酸序列表示的cdr3区域;以及轻链可变区,包含由序列4的氨基酸序列表示的cdr1区域、由序列5的氨基酸序列表示的cdr2区域及由序列6的氨基酸序列表示的cdr3区域。
61.在本发明中,术语“嵌合抗原受体”通常是指含有抗原及具有与一个以上的细胞内结构域结合的能力的细胞外结构域的融合蛋白。嵌合抗原受体为嵌合抗原受体t细胞(car-t)的核心部分,可以包含抗原结合结构域、跨膜结构域、共刺激域及细胞内信号转导结构域。嵌合抗原受体可以基于抗体的抗原(例如bcma)特异性来与t细胞受体-激活细胞内结构域组合。基因被变形的car-表达t细胞可以识别并清除靶向抗原-表达恶性细胞。
62.在本发明中,术语“bcma(b-cell maturation antigen)”是指b细胞成熟抗原。bcma(也公知为tnfrsf17、bcm或cd269)为肿瘤坏死受体(tnfr)家族的成员,在最终分化b细胞中,例如在记忆b细胞及浆细胞上优势地表达。bcma在肿瘤细胞(例如多发性骨髓瘤细胞)中表达或位于肿瘤细胞表面。本发明的“bcma”可以包括包含全长的野生型bcma的突变,例如点突变、片段、插入、缺失以及剪接变异体的蛋白质。
63.在本发明中,术语“bcma-结合结构域(bcma-binding domain)”通常是指能够与bcma蛋白特异性结合的结构域。例如,bcma-结合结构域可以含有与b细胞中表达的人类bcma多肽或其片段特异性结合的抗bcma抗体或其片段。
64.在本发明中,术语“结合结构域(binding domain)”可以与“胞外结构域(extracellular domain)”、“细胞外结合结构域(extracellular binding domain)”、“抗原-特异性结合结构域(antigenspecific binding domain)”及“细胞外抗原-特异性结合结构域(extracellular antigen-specific biding domain)”相互交换来使用,是指具有能够与目标抗原(例如bcma)特异性结合的能力的嵌合抗原受体结构域或片段。
65.在本发明中,上述抗bcma抗体或其片段作为上述抗bcma抗体,为单克隆抗体,优选地,为scfv(单链可变片段(single chain variable fragment)),在本发明中,使用作为人类化的抗bcma抗体的3g4v2。
66.在本发明中,术语“跨膜结构域”通常是指通过细胞膜与细胞内信号转导结构域连接来起到信号传递作用的嵌合抗原受体的结构域。上述跨膜结构域可以源自选自由cd8α、cd4、cd2、cd137、cd80、cd86、cd152及pd1组成的组中的蛋白质,优选地,可以由序列29的氨基酸序列表示。
67.在本发明中,“共刺激域”通常是指能够提供作为对淋巴细胞的抗原有效反应所需的细胞表面分子的免疫刺激分子的细胞内结构域。上述记载的共刺激域可以包括cd28的共刺激域,可以包括ox40及4-1bb的共刺激域等tnf受体家族的共刺激域,优选地,可以为由序列30的氨基酸序列表示的4-1bb。
68.在本发明中,“细胞内信号转导结构域”通常是指位于细胞内的能够传递信号的结构域。在本发明中,细胞内信号转导结构域为嵌合抗原受体的细胞内信号转导结构域。例如,细胞内信号转导结构域可以选自cd3ζ细胞内结构域、cd28细胞内结构域、cd28细胞内结构域、4-1bb细胞内结构域及ox40细胞内结构域中,优选地,可以为由序列31的氨基酸序列表示的cd3ζ。
69.在本发明中,还可以包含位于bcma-结合结构域的c末端及跨膜结构域的n末端之间的铰链区,上述铰链区源自cd8α,优选地,可以由序列28的氨基酸序列表示。上述“铰链区”通常是指抗原-结合区域与免疫细胞fc受体(fcr)-结合区域之间的连接区域。
70.在本发明中,还可以在bcma-结合结构域的n末端包含信号肽(signal peptide),上述“信号肽”通常是指用于引导蛋白质传递的肽链。信号肽可以为具有5个至30个氨基酸长度的短的肽,优选地,本发明中使用序列27的氨基酸序列。
71.编码嵌合抗原受体的多核苷酸及表达嵌合抗原受体的载体本发明的另一实施方式涉及编码上述嵌合抗原受体的多核苷酸。
72.在本发明中,上述编码嵌合抗原受体的多核苷酸可以包含bcma-结合结构域的多核苷酸、编码跨膜结构域的多核苷酸、编码共刺激结构域的多核苷酸以及编码细胞内信号转导结构域的多核苷酸。
73.优选地,上述编码bcma-结合结构域的多核苷酸可以为编码3g4抗体或3g4v2抗体的多核苷酸,具体的碱基序列如上所述。
74.优选地,本发明的编码嵌合抗原受体的多核苷酸包含:由序列21的碱基序列表示的信号肽;由序列18的碱基序列表示的作为抗bcma抗体的3g4v2;由序列23的碱基序列表示的跨膜结构域;由序列24的碱基序列表示的4-1bb(共刺激结构域);以及由序列25的碱基序列表示的cd3ζ(细胞内信号转导结构域)。
75.并且,还可以在编码bcma-结合结构域的多核苷酸与跨膜结构域之间包含编码铰链区的多核苷酸,优选地,可以为由序列22的碱基序列表示的cd8铰链区。
76.在本发明中,术语“多核苷酸”通常是指分离为任意长度的核酸分子(nucleic acid molecule)、脱氧核糖核苷酸、核糖核苷酸或它们的相似体。在一部分实例中,本发明的多核苷酸可以通过如下方式制备:(1)聚合酶链式反应扩增等体外(in-vitro)扩增;(2)克隆及重组;(3)切割(digestion)及凝胶电泳分离等纯化;以及(4)化学合成等合成,优选地,可以通过重组脱氧核糖核酸技术制备分离的多核苷酸。在本发明中,可以采用包括合成寡核苷酸的限制片段操作(restriction fragment operation)或重叠延伸聚合酶链式反应(soe pcr)在内的方法来制备用于编码抗体或其抗原结合片段的核酸,但不限定于此,可
以使用本发明所属技术领域中公知的多种方法来制备。
77.本发明的又一实施方式涉及包含上述编码嵌合抗原受体的多核苷酸的载体。
78.在本发明中,术语“载体(expression vector)”是以能够在适当的宿主细胞内表达目标基因的方式包含启动子等必需的调节要素的基因制备物。载体可以选自质粒、反转录病毒载体及慢病毒载体中的一种以上。当转化到适当的宿主时,载体可以与宿主基因组无关地进行复制并起到相应的功能,或者在部分情况下,可以与基因组本身整合。
79.并且,载体可以包含能够使编码区域在适当的宿主中正确表达的表达控制要素。这样的调节要素是相关从业人员所熟知的,例如,可以包括启动子、核糖体结合位点(ribosome-binding site)、增强子(enhancer)以及用于调节基因转录(transcription)或信使核糖核酸(mrna)翻译的其他调节要素。表达调节序列的特定结构可以根据物种或细胞类型的功能的不同而不同,通常包含tata框(box)、加帽(capped)序列、caat序列等参与转录开始及翻译开始的5'非转录序列以及5'或3'非翻译序列。例如,5'非转录表达调节序列可以包含启动子区域,上述启动子区域可以包含用于转录及调节功能性连接的核酸的启动子序列。
80.在本发明的具体实例中,上述载体为重组病毒载体,优选地,为慢病毒载体,包含:可操作地连接的ef1α启动子;编码信号肽的多核苷酸;编码bcma-结合结构域的多核苷酸;编码跨膜结构域的多核苷酸;以及编码细胞内信号转导结构域的多核苷酸。为了增加蛋白质表达,还可以包含wpre(woodchuck hepatitis virus post-transcriptional regulatory element(土拨鼠肝炎病毒转录后调控元件))(图2)。
81.上述ef1α启动子可以由序列19的碱基序列表示,可以根据需要与上述序列19的碱基序列具有90%以上、93%以上、95%以上、96%以上、97%以上、98%以上或99%以上相同的序列。
82.并且,可操作地连接上述启动子来诱导作为bcma-结合结构域的抗hbcma抗体(scfv)的表达,其中,“可操作地连接(operably linked)”是指通过功能性地连接核酸表达调节序列与编码目标蛋白质的核酸序列来执行一般功能。与重组载体的可操作连接可以利用本发明所属技术领域中众所周知的基因重组技术来制备,表位-特异性脱氧核糖核酸(dna)切割及连接使用本发明所属技术领域中通常的酶等。
83.向细胞内导入基因并表达的方法是相关技术领域中公知的。与表达载体相关地,可以通过相关技术领域的任意方法轻易地向宿主细胞内导入载体。例如,可以通过物理、化学或生物学手段将表达载体移到宿主细胞内。
84.向宿主细胞内导入多核苷酸的物理方法包括磷酸钙沉淀、脂质体转染、粒子冲击、微注射、电穿孔等。生产载体和/或包含外因性核酸的细胞的方法在相关技术领域中是公知的。例如,参照文献[sambrook et al,2012,molecular cloning:a laboratory manual,volumes 1
ꢀ‑
4,cold spring harbor press,ny]。优选地,用于向宿主细胞内导入多核苷酸的方法为磷酸钙转染。
[0085]
用于向宿主细胞内导入多核苷酸的生物学方法包括脱氧核糖核酸及核糖核酸(rna)载体的使用。病毒载体,尤其是反转录病毒载体已成为将基因插入哺乳动物,例如将基因插入人类细胞内的最广泛使用的方法。其他病毒载体可以源自慢病毒、痘病毒、单纯疱疹病毒、腺病毒及腺相关病毒等。
[0086]
向宿主细胞内导入多核苷酸的化学方法有胶体分散液系统,例如,包括大分子复合物、纳米胶囊、微球体、磁珠及水中油乳液、胶束、混合的胶束以及脂质体等基于脂质的系统。用于在试验管内及生物体内用作递送载体的例示性的胶体系统为脂质体(例如人造膜囊泡)。可以使用核酸的最新技术的靶向递送,例如,可以利用使用靶向化的纳米粒子或其他适当的不足千分尺大小的递送系统的用于递送多核苷酸的其他方法。
[0087]
在利用非病毒传递系统的情况下,例示性的递送载体为脂质体。为了向宿主细胞内导入核酸(试验管内、生物体外或生物体内),可以考虑脂质制剂的使用。另一方面,核酸可以与脂质关联。与脂质关联的核酸在脂质体的水性内部胶囊化,或者散布于脂质体的脂质双层内,或者通过与脂质体及寡核苷酸两者关联的连接分子附着于脂质体,或者被捕获在脂质体内,或者与脂质体形成复合物,或者分散在含有脂质的溶液中,或者与脂质混合,或者与脂质组合,或者以悬浮液的形式包含于脂质内,或者与胶束一同含有或被复合物化,或者可以与脂质有别的关联。脂质、脂质/脱氧核糖核酸或脂质/表达载体关联组合物不受溶液中任意特定结构的限制。
[0088]
嵌合抗原受体表达免疫效应细胞
[0089]
本发明的还有一实施方式涉及包含编码上述嵌合抗原受体的多核苷酸或包含编码嵌合抗原受体的多核苷酸的载体且表达上述嵌合抗原受体的免疫效应细胞。
[0090]
在本发明中,上述免疫效应细胞可以为哺乳动物来源细胞,优选地,可以为t细胞或自然杀伤(nk)细胞。
[0091]
在本发明中,上述表达嵌合抗原受体的免疫效应细胞可以通过将本发明的嵌合抗原受体载体导入免疫效应细胞,例如,导入t细胞或自然杀伤细胞内来制备。
[0092]
具体地,嵌合抗原受体载体可以通过电穿孔法、lipofectamine(lipofectamine 2000,invitrogen公司)等本发明所属技术领域中公知的方法来向细胞内导入。例如,免疫效应细胞可以通过慢病毒载体转染使运输嵌合抗原受体分子的病毒基因组与宿主基因组整合来保证目标基因的长期且稳定的表达。再举一例,可以在向靶细胞内导入嵌合抗原受体运输质粒(transposon)及转移酶运输质粒的过程中利用转位子(transposon)。再举一例,嵌合抗原受体分子可以通过基因编辑方法(例如crispr/cas9)添加到基因组中。
[0093]
在本发明的具体的一实施例中,如图2所示,制备插入编码hbcma-car的多核苷酸的慢病毒载体,通过将制备的载体转化到t细胞来制备hbcma-嵌合抗原受体-t细胞。在制备的hbcma-嵌合抗原受体-t细胞中表达本发明的靶向bcma的嵌合抗原受体。
[0094]
可以从对象中获得用于制备表达嵌合抗原受体的免疫效应细胞的免疫效应细胞,上述“对象”包括能够导出免疫反应的活的有机体(例如哺乳动物)。对象的例包括人类、狗、猫、小鼠、大鼠及其转基因种。t细胞可以从外周血单核细胞、骨髓、淋巴结组织、脐带血、胸腺组织、感染部位的组织、腹水、胸膜渗出液,脾脏组织及肿瘤等多种供应源中获得。
[0095]
上述t细胞可以使用本发明所属技术领域的普通技术人员公知的任意多种技术,例如,使用ficoll
tm
分离从对象收集的血液单位中获得。通过分离单采术从血液中获得细胞,典型的分离单采术产物含有t细胞、单核细胞、粒细胞、b细胞等淋巴细胞、其他有核血细胞、红细胞及血小板。
[0096]
通过分离单采术收集的细胞在去除血浆分馏物后,为了后续的处理步骤以及为了保管在适当的缓冲剂或培养基中,可以洗涤细胞。溶解红细胞后,例如通过percoll
tm
梯度的
离心分离或逆流离心分离耗尽单核细胞后,从外周血淋巴细胞中分离出t细胞。
[0097]
在本发明的一具体实例中,如图3所示,从外周血单个核细胞(peripheral blood mononuclear cell,pbmc)中分离激活的t细胞后,向t细胞转导hbcma-car慢病毒来制备hbcma-嵌合抗原受体-t细胞。确认制备的hbcma-嵌合抗原受体-t细胞的hbcma肽结合能力的结果如图4所示,确认到随着hbcma肽的增加,与hbcma结合的表达cd4或cd8的hbcma-嵌合抗原受体-t细胞也增加。这表示本发明中制备的hbcma-嵌合抗原受体-t细胞有效地与bcma结合。
[0098]
在本发明的再一具体实例中,为了确认hbcma-嵌合抗原受体-t细胞的激活,在靶向细胞的存在下确认了通过3g4v2-嵌合抗原受体-t细胞的ifnγ及cd107a表达程度。结果如图5所示,在未表达bcma的k562细胞中,t细胞未被激活,与之相反,在表达bcma的h929细胞的存在下,确认到t细胞被激活而增加了ifnγ的表达。
[0099]
在本发明的还有一具体实例中,确认通过hbcma-嵌合抗原受体-t细胞的靶细胞的杀灭效果的结果如图6所示,确认到hbcma-嵌合抗原受体-t细胞显出对表达bcma的rpmi8226细胞及h929细胞特异性地杀灭效果。
[0100]
即,本发明的靶向bcma的嵌合抗原受体及嵌合抗原受体-t细胞可以有用地用作用于预防或治疗与b细胞或与bcma的表达相关的疾病的组合物。
[0101]
用于预防或治疗与bcma的表达相关的疾病的组合物
[0102]
本发明的还有一实施方式涉及一种用于预防或治疗与bcma的表达相关的疾病的药物组合物,包含表达靶向bcma的嵌合抗原受体的免疫效应细胞。
[0103]
本发明还有一实施方式涉及一种用于预防或治疗与b细胞相关的疾病的药物组合物,包含靶向bcma的抗体。
[0104]
与b细胞相关的疾病或与bcma(野生型或突变体bcma)的表达相关的疾病可以为癌症、恶性肿瘤或自身免疫疾病。优选地,可以为多发性骨髓瘤、血液癌、非霍奇金淋巴瘤、自身抗体依赖性自身免疫性疾病、系统性红斑狼疮或类风湿关节炎。
[0105]
上述药物组合物还可以包含药学上可接受的载体。口服给药时可以使用结合剂、悬浮剂、崩解剂、赋形剂、可溶剂、分散剂、稳定剂、悬浮化剂、色素、香料等,在注射剂的情况下,可以混合缓冲剂、保存剂、无痛化剂、可溶剂、等渗剂、稳定剂等来使用,在局部给药时,可以使用基剂、赋形剂、润滑剂、保存剂等。
[0106]
上述药物组合物的剂型可以与上述药剂学上可接受的载体混合来多种多样地制备。例如,口服给药时可以制备为片剂、糖衣片、胶囊、药水、缓释剂、糖浆、圆片等形态,在注射剂的情况下,可以制备为单位给药安倍瓶或多次给药的形态。
[0107]
并且,上述药物组合物可以包含能够提高膜透过性的表面活性剂。上述表面活性剂可以为从类固醇中诱导的或n-[1-(2,3-二醇油)丙基-n,n,n-三甲基氯化铵(dotma)等阳离子脂质,或者胆固醇琥珀酸单酯、磷脂酰甘油等各种混合物,但不限定于此。
[0108]
并且,本发明提供预防或治疗癌症的方法,包括向个体给药本发明的药物组合物的步骤。为了预防或治疗与b细胞相关的疾病,可以给药药学上有效的量的上述包含hbcma-嵌合抗原受体-t细胞或抗hbcma抗体的药物组合物。可以根据疾病的种类、患者的年龄、体重、症状的特性及程度、现在的治疗方法的种类、治疗的次数、给药形态及途径等多种因素的不同而不同,可以通过相关领域的专家轻松决定。
[0109]
上述药物组合物可以与上述药理学或生理学成分一同给药或依次给药,并且,可以与追加的现有治疗剂联合给药,可以与先有的治疗剂依次或同时给药。这样的给药可以是单次给药或多次给药。重要的在于,在考虑到上述所有因素后以无副作用的最小的量获得最大的效果的量来给药,这可以通过相关领域的普通技术人员轻松地决定。
[0110]
本说明书中使用的术语“个体”是指处于可以通过给药上述药物组合物来减轻、抑制或治疗的状态或具有患有疾病的风险的哺乳动物,优选地,是指人类。
[0111]
本发明中使用的术语“给药”是指以任意适当的方法向个体提供本发明的药物组合物。本发明的药物组合物可以通过研究人员、兽医、医生或其他临床方式以在能够想象到的组织系统、动物或人类中诱导生物学或医学反应的有效成分或药物组合物的量,即,以作为诱导所要治疗的疾病或障碍的症状的缓解的量的治疗上有效的量来给药。本发明所属技术领域的普通技术人员应该自明的是,有关本发明的药物组合物的治疗上有效的给药量及给药次数根据所希望的效果而变化。因此,给药的最佳给药量可以通过相关从业者轻易决定,可以根据疾病的种类、疾病的严重程度、组合物中含有的有效成分及其他成分的含量、剂型的种类、患者的年龄、体重、一般健康状态、性别及饮食、给药时间、给药途径及组合物的分泌率、治疗期间、同时使用的药物等多种因素来调节。本发明的药物组合物能够以1mg/kg/天~10000mg/kg/天的量给药,可以一天给药一次,也可以分为数次给药。
[0112]
以下,通过优选实施例来帮助理解本发明。但下述实施例仅为更易于理解本发明而提供,本发明的内容不限定于下述实施例。
[0113]
实施例1:制备和筛选靶向bcma的抗体
[0114]
为了筛选对bcma肽具有特异性的抗体,通过制备生产与bcma结合的抗体的杂交瘤细胞来筛选抗体。
[0115]
首先,通过本发明所属技术领域公知的方法利用bcma肽(序列19;acrobiosystems inc.公司,cat#bca-h522y)使小鼠免疫后,摘出脾脏细胞后通过细胞融合与小鼠骨髓瘤细胞融合来制备杂交瘤细胞。
[0116]
由于用于细胞融合的小鼠骨髓瘤细胞不具有次黄嘌呤-鸟嘌呤磷酸核糖转移酶(hgprt,hypoxanthineguanidine-phosphoribosyl-transferase),因此不能在hat培养基中存活,但杂交瘤细胞可以通过与脾脏细胞融合来在hat培养基中存活。若利用这种方式,可以只使杂交瘤细胞增殖,因此一直在hat培养基中使其增殖直至确立普通杂交瘤细胞。
[0117]
为了在杂交瘤细胞中生产与bcma结合的抗体,使用了有限稀释法。首先,每96孔成为一个细胞以下,筛选从一个细胞增殖的克隆。重复上述过程3次来筛选生产与bcma结合的抗体的杂交瘤瘤细胞。
[0118]
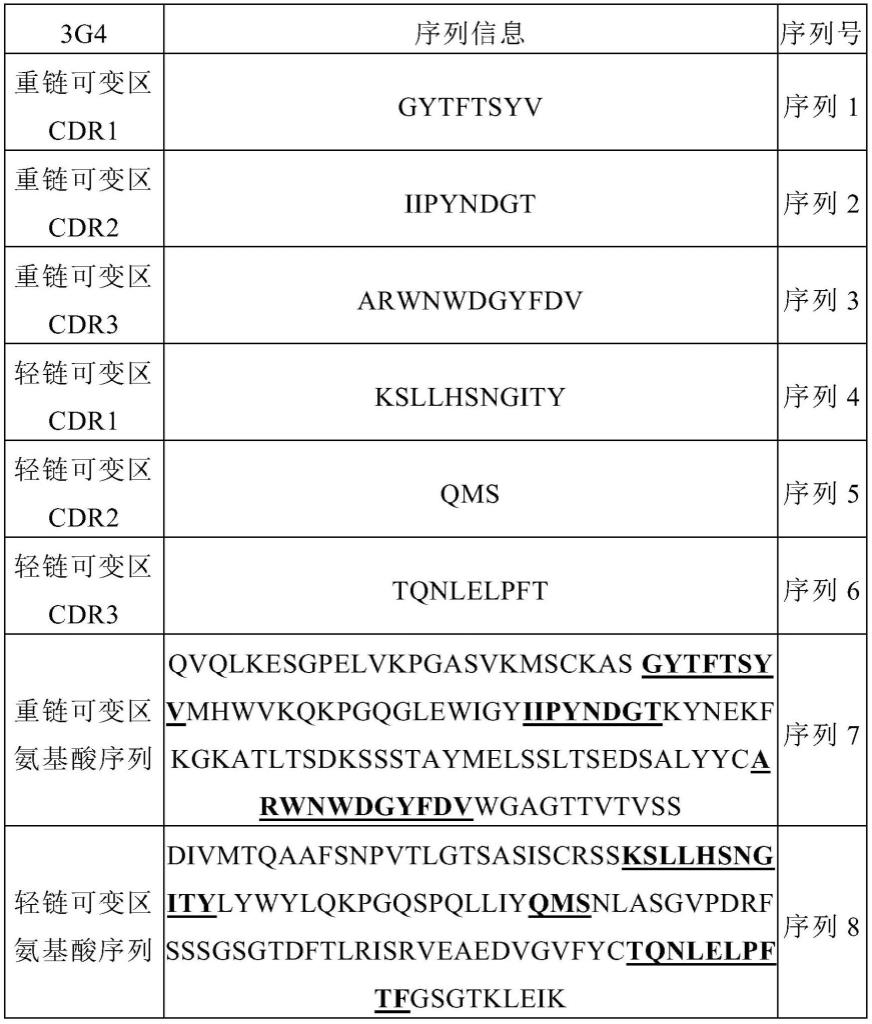
将在杂交瘤细胞中筛选的抗体命名为3g4抗体(抗hbcma单克隆抗体(anti-hbcma monoclonal antibody)),分析了氨基酸序列。根据序列分析结果的有关抗体的重链可变区及轻链可变区的序列信息如下述表1所示,下述表1中有下划线的部分表示互补决定区(complementarity determining region;cdr)。
[0119]
表1. 3g4抗体的序列信息
[0120]
[0121][0122]
如表1所示,确认到3g4抗体包含:重链可变区,包含由序列1的氨基酸序列(gytftsyv)表示的cdr1区域、由序列2的氨基酸序列(iipyndgt)表示的cdr2区域及由序列3的氨基酸序列(arwnwdgyfdv)表示的cdr3区域;以及轻链可变区,包含由序列4的氨基酸序列(ksllhsngity)表示的cdr1区域、由序列5的氨基酸序列(qms)表示的cdr2区域及由序列6的氨基酸序列(tqnlelpft)表示的cdr3区域。
[0123]
具体地,上述3g4抗体由序列7的氨基酸序列所表示的重链可变区及序列8的氨基酸序列所表示的轻链可变区构成,并且,3g4抗体的重链可变区可以由序列9的碱基序列编码,3g4抗体的轻链可变区可以由序列10的碱基序列编码。
[0124]
实施例2:制备基于3g4抗体的人类化抗体
[0125]
将上述实施例1中筛选的3g4抗体制备为变更为与人类相对应的结构的人类化的抗体。
[0126]
具体地,以人类抗体的生殖系列碱基序列(germline sequence)为框架(frame),通过将与bcma结合的小鼠抗体的cdr替换为人类抗体的cdr的cdr-移植(cdr grafting)方法将3g4抗体制备为人类化的抗体。人类化的抗体命名为3g4v2,分析氨基酸序列。根据序列分析结果的有关抗体重链可变区及轻链可变区的序列信息如下述表2所示,下述表2中有下划线的部分表示互补决定区。
[0127]
表2. 3g4v2抗体的序列信息
[0128]
[0129]
[0130][0131]
如表2所示,确认到3g4v2抗体由序列13的氨基酸序列所表示的重链可变区及序列14的氨基酸序列所表示的轻链可变区构成,并且,3g4v2抗体的重链可变区由序列15的碱基序列编码,3g4v2抗体的轻链可变区由序列16的碱基序列编码。
[0132]
实施例3:确认抗bcma抗体的bcma结合能力
[0133]
在本发明中,确认了上述实施例2中制备的作为人类化的抗bcma抗体的3g4v2能否特异性地靶向化bcma。
[0134]
首先,为了生产3g4v2抗体,在人类抗体igg1的重链抗体表达载体中克隆由序列15的碱基序列表示的重链可变区,在人类抗体卡帕(kappa)轻链抗体表达载体中克隆由序列16的碱基序列表示的轻链可变区,向cho细胞共转染(co-transfection)各表达载体来生产抗体。使用蛋白a(protein a)柱(thermo fisher公司,cat#20356)纯化生产的抗体。
[0135]
然后,使用1mg的上述纯化的抗体分别处理a549细胞和表达hbcma的a549细胞并反应后,处理对人类igg fc部分具有特异性的二抗(biolegend公司,cat#409304)。与抗体反应后,通过流式细胞分析(flow cytometry)方法测定二抗的pe荧光。
[0136]
结果如图1所示,在不表达hbcma的a549细胞中未确认到与3g4v2的结合,但确认到表达hbcma的a549细胞与3g4v2的结合能力增加为60.1%。
[0137]
实施例4:制备靶向bcma的嵌合抗原受体表达载体
[0138]
在本发明中,制备了表达包含上述实施例2中制备的作为人类化的抗bcma抗体的3g4v2的靶向bcma的嵌合抗原受体的慢病毒载体(hbcma-car慢病毒)。
[0139]
如图3的示意图所示,在生物体外合成由ef1α启动子(序列20)、编码信号肽的多核苷酸(序列21)、编码bcma-结合结构域的多核苷酸(序列18)、编码cd8铰链区的多核苷酸(序列22)、编码跨膜结构域的多核苷酸(序列23)、编码4-1bb(共刺激结构域)的多核苷酸(序列24)、编码cd3ζ(细胞内信号转导结构域)的多核苷酸(序列25)以及编码wpre的多核苷酸(序列26)构成的嵌合抗原受体脱氧核糖核酸(car dna)(序列32)来插入第三代慢病毒载体中。
[0140]
慢病毒载体为使用将lenti-x 293t细胞共转染(co-transfection)pmdlg/prre
(addgene公司,cat##12251)、pmd2.g(addgene公司,cat##12259)、prsv-rev(addgene公司,cat##12253)这三种载体后,生产hbcma-car慢病毒。为了共转染,使用lipofectamine 3000转染试剂盒(transfection kit)(invitrogen公司,cat#l3000-015)和opti-mem+glutamax(gibco公司,cat#51985-034)培养基(media)培养三种载体与lenti-x 293t细胞6小时。
[0141]
实施例5:制备hbcma-嵌合抗原受体-t细胞
[0142]
在本发明中,通过将上述实施例4中制备的hbcma-car慢病毒载体转化到t细胞来制备hbcma-嵌合抗原受体-t细胞(或3g4v2-嵌合抗原受体-t细胞)。
[0143]
具体地,如图3所示,在血液中分离外周血单个核细胞(peripheral blood mononuclear cell,pbmc)后,使用t细胞激活珠(t cell activation bead;miltenyl biotec公司,cat#130-091-441)激活t细胞。向激活的t细胞转导上述实施例4中制备的hbcma-car慢病毒来制备hbcma-嵌合抗原受体-t细胞,使用lenti-boost-p来增加转导的效率。
[0144]
通过流式细胞分析方法确认hbcma-嵌合抗原受体-t细胞的hbcma肽结合能力。使上述制备的hbcma-嵌合抗原受体-t细胞与fitc-hbcma蛋白、anti-cd3、anti-cd4、anti-cd8抗体反应后,利用流式细胞荧光分选技术(facs)仪器测量荧光强度。在分析过程中,以表达cd3的细胞为t细胞,确认t细胞中fitc的表达程度。
[0145]
结果如图4所示,确认到随着hbcma肽的增加,与hbcma结合的表达cd4或cd8的hbcma-嵌合抗原受体-t细胞也增加。这表示本发明中制备的hbcma-嵌合抗原受体-t细胞有效地与bcma结合。
[0146]
实施例6:确认通过hbcma肽激活hbcma-嵌合抗原受体-t细胞
[0147]
在本发明中,为了确认是否通过bcma肽激活上述实施例5中制备的hbcma-嵌合抗原受体-t细胞,在靶向细胞存在的情况下确认通过hbcma-嵌合抗原受体-t细胞的ifnγ及cd107a的表达程度。
[0148]
靶向细胞使用不表达bcma的k562细胞(atcc公司,cat#ccl-243)及表达bcma的h929细胞(atcc公司,cat#crl-9068),分别以2∶1、1∶1、0.5∶1、0:1的比例使hbcma-嵌合抗原受体-t细胞与靶向细胞反应规定时间后,使用表面和内部抗体(surface&intra antibody)染色并通过流式细胞荧光分选技术进行测量(bcma蛋白(protein)、inf-r、cd107a、cd3、cd4、cd8染色)。以0∶1(只有嵌合抗原受体t细胞(car-t only))为基准确认与靶细胞反应的hbcma-car-t的ifnγ及cd107a的表达程度。
[0149]
结果如图5所示,确认到在不表达bcma的k562细胞中未激活t细胞,相反,在表达bcma的h929细胞存在下,t细胞被激活而增加了ifnγ的表达。
[0150]
实施例7:确认hbcma-嵌合抗原受体-t细胞对bcma表达细胞的杀灭效果
[0151]
在本发明中,确认了hbcma-嵌合抗原受体-t细胞对靶向细胞的杀灭效果。
[0152]
利用不表达bcma的k562细胞与表达bcma的rpmi8226细胞及h929细胞作为靶向细胞,分别以1∶4、1∶2、1∶1、1∶0.5及1∶0.25的比例与hbcma-嵌合抗原受体-t细胞混合后,测量发光(cytotox-glo细胞毒性测定(cytotox-glo cytotoxicity assay),promega公司,cat#g9291)。以测量的值利用下述数学式1计算细胞杀灭效果。
[0153]
数学式1
[0154]
%细胞毒性(cytotoxicity)=[(experimental-effector spontaneous-
target spontaneous)/(target maximum-target spontaneous)]
×
100
[0155]
experimental:从复合培养靶细胞及嵌合抗原受体-t细胞的培养基中导出的发光(luminescence)值
[0156]
effector spontaneous:从只有嵌合抗原受体-t细胞的培养基中导出的发光值
[0157]
target spontaneous:从只有靶细胞的培养基中导出的发光值
[0158]
target maximum:从靶细胞的100%裂解(利用裂解试剂(lysis reagent))的发光值
[0159]
结果如图6所示,确认到hbcma-嵌合抗原受体-t细胞显出特异性地杀灭表达bcma的rpmi8226细胞及h929细胞的效果。
[0160]
即,本发明的靶向bcma的嵌合抗原受体及嵌合抗原受体-t细胞可以有用地用作用于预防或治疗与b细胞相关或与bcma的表达相关的疾病。
[0161]
产业上的可利用性
[0162]
在本发明中,确认到筛选抗体特异性地识别表达bcma的细胞,利用上述确立的抗体确认到靶向bcma的嵌合抗原受体及嵌合抗原受体-t细胞不仅与bcma有效结合,而且实现与bcma结合的嵌合抗原受体-t细胞的激活。
[0163]
并且,确认到本发明的嵌合抗原受体-t细胞有效杀灭表达bcma的细胞,因此,本发明的bcma特异性抗体、靶向bcma的嵌合抗原受体及嵌合抗原受体-t细胞可以有用地用作用于预防或治疗与bcma的表达相关的疾病的组合物。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1