经修饰的抗病毒结合剂的制作方法
本发明涉及通过向有需要的受试者递送结合剂来治疗病毒感染(诸如冠状病毒感染)的方法,其中所述结合剂包含(i)至少一个结合病毒表面上表达的病毒蛋白的结合结构域,和(ii)经修饰的fc结构域,与野生型fc结构域相比,所述经修饰的fc结构域表现出(a)与fc激活受体的结合减少或(b)与fc抑制性受体的结合增加。结合剂可以作为多核苷酸(例如,mrna)或蛋白质递送,并且可以包含在用于递送的媒介物诸如病毒或非病毒载体中。本公开还涉及多核苷酸、蛋白质和媒介物(例如,病毒和非病毒载体)以及它们的组合物,包括在所述方法中使用的多核苷酸、蛋白质和媒介物以及它们的组合物。
背景技术:
1、冠状病毒(cov)是一组系统发育多样的包膜病毒,其编码最大的正链rna基因组并在大多数哺乳动物中有效复制。人cov感染通常导致轻度至重度上呼吸道和下呼吸道疾病。严重急性呼吸综合征冠状病毒(sars-cov)在2002-2003年出现,引起急性呼吸窘迫综合征(ards),总死亡率为10%,并且老年人死亡率高达50%。中东呼吸综合征。冠状病毒(mers-cov)于2012年4月在中东出现,表现为严重肺炎、急性呼吸窘迫综合征(ards)和急性肾衰竭。最近,冠状病毒株的sars-cov-2已作为人的感染性毒株出现。
2、用于治疗或预防冠状病毒感染(包括sars-cov-2感染)的疗法有限。许多正在研究的药物最初是为其他病原体设计的,并且迅速重新用于当前的covid-19试验,包括瑞德西韦(remdesivir)、羟氯喹(hydroxychloroquine)和法匹拉韦(favipiravir)。在一些方面,没有足够的证据表明任何现有的抗病毒药物可以有效地治疗冠状病毒感染。仍然需要用于治疗病毒感染(包括冠状病毒感染,包括与sars-cov-2相关的那些)的改进疗法。
技术实现思路
1、本文提供了用于减轻受试者中响应于病毒感染的炎症的结合剂、多核苷酸、载体以及它们的递送方法。本文还提供了用于调节免疫复合物功能(诸如抑制激活免疫复合物和促进抑制性免疫复合物功能)的结合剂、多核苷酸、载体以及它们的递送方法。在一些方面,所述方法还包括治疗病毒感染。
2、本文提供了一种结合剂,其包含:(i)至少一个结合暴露于病毒表面的病毒蛋白的结合结构域,和(ii)经修饰的fc结构域,其中所述结合剂能够中和所述病毒并且与未经修饰的fc结构域相比表现出降低的促炎活性。本文还提供了一种结合剂,其包含:(i)至少一个结合暴露于病毒表面的病毒蛋白的结合结构域,和(ii)与igg1 fc结构域相比具有降低的促炎活性的fc结构域,其中所述结合剂能够中和所述病毒。
3、在任何提供的实施方案中的一些中,fc结构域是igg2或igg4 fc结构域。在任何提供的实施方案中的一些中,经修饰的fc表现出与fc激活受体的结合减少。在任何提供的实施方案中的一些中,与野生型fc结构域相比,所述经修饰的fc表现出与fc抑制性受体的结合增加。
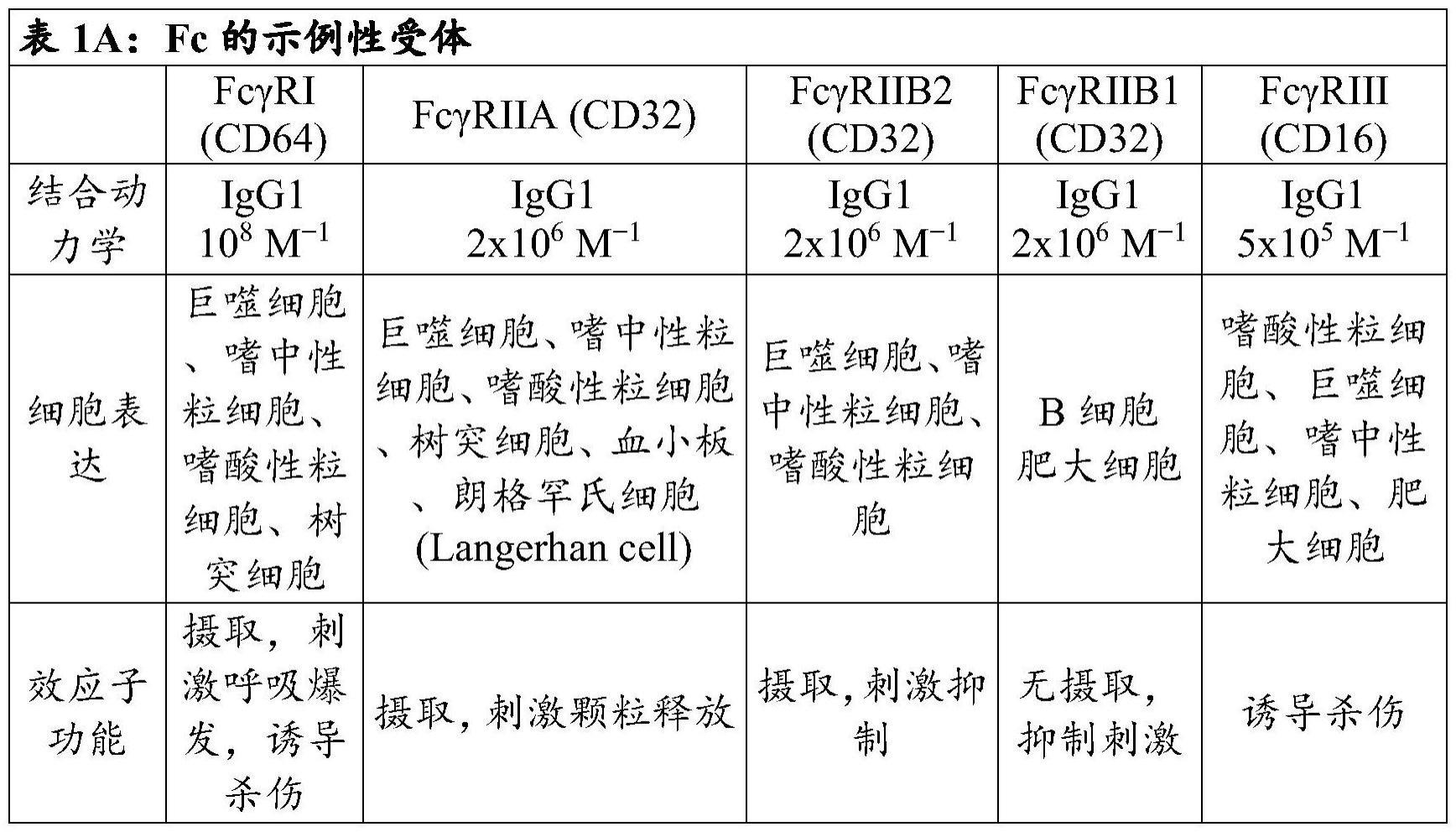
4、本文还提供了结合剂,其包含(i)至少一个结合表面暴露的病毒蛋白的结合结构域,和(ii)经修饰的fc结构域,其中与野生型fc结构域相比,所述经修饰的fc结构域与至少一个fc激活受体家族成员的结合减少。在任何提供的实施方案中的一些中,fc激活受体是fcγ受体i(fcγri)、fcγ受体iia(fcγriia)或fcγ受体iii(fcγriii)。
5、在任何提供的实施方案中的一些中,结合剂能够形成与由包含至少一个结合结构域和野生型fc结构域的结合剂形成的免疫复合物相比具有降低的促炎活性的免疫复合物。
6、在任何提供的实施方案中的一些中,经修饰的fc结构域包含选自以下的各自基于eu编号的氨基酸取代:ser228pro、glu233pro、leu234ala、leu234glu、leu235ala、leu235glu、leu235phe、gly236arg、gly237ala、pro238ser、asp265ala、his268ala、his268gln、ser288pro、asn297ala、asn297gly、asn297gln、val309leu、gly318ala、leu328arg、pro329gly、ala330ser和pro331ser,或者前述任一者的组合。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的leu235glu取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的leu234ala取代和基于eu编号的leu235ala取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的ser288pro取代和基于eu编号的leu235glu取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的leu234ala取代、基于eu编号的leu235ala取代和基于eu编号的pro329gly取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的pro331ser取代、基于eu编号的leu234glu取代和基于eu编号的leu235phe取代。
7、在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的asp265ala取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的gly237ala取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的gly318ala取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的glu233pro取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的gly236arg取代、基于eu编号的leu328arg取代和基于eu编号的pro329gly取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的his268gln取代、基于eu编号的val309leu取代和基于eu编号的ala330ser取代和/或基于eu编号的pro331ser取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的leu234ala取代、基于eu编号的leu235ala取代、基于eu编号的gly237ala取代、基于eu编号的pro238ser取代、基于eu编号的his268ala取代、基于eu编号的ala330ser取代和基于eu编号的pro331ser取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的asn297ala取代、基于eu编号的asn297gly取代或基于eu编号的asn297gln取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的ser228pro取代、基于eu编号的phe234ala取代和基于eu编号的leu235ala取代。
8、本文还提供了一种结合剂,其包含(i)至少一个结合暴露于病毒表面的病毒蛋白的结合结构域,和(ii)经修饰的fc结构域,其中与野生型fc结构域相比,所述经修饰的fc结构域与抑制性fc受体的结合增加。
9、在任何提供的实施方案中的一些中,抑制性fc受体是fcγriib,任选地其中fcriib是fcγriib1或fcγriib2。在任何提供的实施方案中的一些中,结合剂能够形成与由包含至少一个结合结构域和野生型fc结构域的结合剂形成的免疫复合物相比具有增加的抗炎活性的免疫复合物。在任何提供的实施方案中的一些中,结合剂能够形成与由包含至少一个结合结构域和野生型fc结构域的结合剂形成的免疫复合物相比具有降低的炎性活性的免疫复合物。在任何提供的实施方案中的一些中,经修饰的fc结构域包含选自以下的各自基于eu编号的氨基酸取代:phe241ala、ser267glu、his268phe、leu328phe、ser324thr、pro238asp、leu328glu、ser239asp、ile332glu、gly236ala,或者前述任一者的组合。
10、在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的ser267glu取代和基于eu编号的his268phe取代,以及基于eu编号的ser324thr取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的ser267glu取代和基于eu编号的leu328phe取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的pro238asp取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的leu328glu取代。
11、在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的ser239asp取代和基于eu编号的ile332glu取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的ser239asp取代和基于eu编号的ile332glu取代,以及基于eu编号的gly236ala取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的ser267glu取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的e233d取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的g237d取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的h268d取代。
12、在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的p271g取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的a330r取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的e233d取代和基于eu编号的a330r取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的e233d取代、基于eu编号的p271g取代和基于eu编号的a330r取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的g237d取代、基于eu编号的h268d取代和基于eu编号的p271g取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的g237d取代、基于eu编号的p271g取代和基于eu编号的a330r取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的e233d取代、基于eu编号的h268d取代、基于eu编号的p271g取代和基于eu编号的a330r取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的g237d取代、基于eu编号的h268d取代、基于eu编号的p271g取代和基于eu编号的a330r取代。在任何提供的实施方案中的一些中,经修饰的fc结构域包含基于eu编号的e233d取代、基于eu编号的g237d取代、基于eu编号的h268d取代、基于eu编号的p271g取代和基于eu编号的a330r取代。
13、在任何提供的实施方案中的一些中,所述经修饰的fc结构域与野生型fc结构域相比包含一个或多个氨基酸取代。在任何提供的实施方案中的一些中,野生型fc结构域是野生型igg1。在任何提供的实施方案中的一些中,野生型fc结构域包含seq id no 1中所示的氨基酸序列。在任何提供的实施方案中的一些中,经修饰的fc结构域包含与seq id no 1表现出至少85%、至少90%、至少92%、至少95%、至少97%序列同一性的氨基酸序列。
14、在任何提供的实施方案中的一些中,野生型fc结构域是野生型igg2。在任何提供的实施方案中的一些中,野生型fc结构域包含seq id no 2中所示的氨基酸序列。在任何提供的实施方案中的一些中,经修饰的fc结构域包含与seq id no 2表现出至少85%、至少90%、至少92%、至少95%、至少97%序列同一性的氨基酸序列。
15、在任何提供的实施方案中的一些中,野生型fc结构域是野生型igg4。在任何提供的实施方案中的一些中,野生型fc结构域包含seq id no 3中所示的氨基酸序列。在任何提供的实施方案中的一些中,经修饰的fc结构域包含与seq id no 3表现出至少85%、至少90%、至少92%、至少95%、至少97%序列同一性的氨基酸序列。在任何提供的实施方案中的一些中,经修饰的fc结构域包含与seq id no 1-3中的任一个表现出少85%序列同一性的氨基酸序列。
16、在任何提供的实施方案中的一些中,至少一个结合结构域和经修饰的fc结构域直接连接。在任何提供的实施方案中的一些中,至少一个结合结构域和经修饰的fc结构域通过接头间接连接。在任何提供的实施方案中的一些中,接头是肽接头。在任何提供的实施方案中的一些中,肽接头是(gms)n(seq id no:4),其中m和n各自为1至4之间的整数,包括端点值。
17、在任何提供的实施方案中的一些中,至少一个结合结构域是至少两个结合结构域。在任何提供的实施方案中的一些中,至少两个结合结构域结合病毒蛋白的至少两个不同表位。在任何提供的实施方案中的一些中,至少两个结合结构域直接连接。在任何提供的实施方案中的一些中,至少两个结合结构域通过接头间接连接。在任何提供的实施方案中的一些中,接头是肽接头。在任何提供的实施方案中的一些中,肽接头是(gms)n(seq idno:4),其中m和n各自为1至4之间的整数,包括端点值。
18、在任何提供的实施方案中的一些中,病毒蛋白是病毒受体。在任何提供的实施方案中的一些中,病毒是rna病毒。在任何提供的实施方案中的一些中,病毒是正粘病毒,任选地其中所述病毒是流感病毒。在任何提供的实施方案中的一些中,病毒是副粘病毒(paramyxovirus)。在任何提供的实施方案中的一些中,病毒是呼吸道合胞病毒(rsv)。在任何提供的实施方案中的一些中,病毒是麻疹病毒(measles morbillivirus)(mev)。在任何提供的实施方案中的一些中,病毒是冠状病毒。在任何提供的实施方案中的一些中,病毒是严重急性呼吸综合征(sars)cov-2。在任何提供的实施方案中的一些中,病毒是sars cov-2的变体。在任何提供的实施方案中的一些中,病毒是感兴趣的sars cov-2变体(voi)、关注的变体(variant of concern;voc)和/或有严重后果的变体(variant of highconsequence;vohc)。在任何提供的实施方案中的一些中,sars cov-2变体选自包括以下的组:α(即b.1.1.7)、β(即b.1.351、b.1.351.2、b.1.351.3)、δ(即b.1.617.2、ay.1、ay.2、ay.3)和γ(即p.1、p.1.1、p.1.2)。在任何提供的实施方案中的一些中,病毒是sars cov-1。在任何提供的实施方案中的一些中,病毒是中东呼吸综合征病毒(mers-v)。
19、在任何提供的实施方案中的一些中,结合剂是二聚体。在任何提供的实施方案中的一些中,结合剂能够中和病毒。在任何提供的实施方案中的一些中,结合剂减少或防止病毒附着至宿主细胞。在任何提供的实施方案中的一些中,至少一个结合结构域包含特异性结合病毒蛋白的抗体的抗原结合片段。
20、在任何提供的实施方案中的一些中,至少一个结合结构域特异性结合sars病毒的s(刺突)糖蛋白。
21、在任何提供的实施方案中的一些中,抗原结合片段包含可变重链(vh)和可变轻链(vl)。在任何提供的实施方案中的一些中,抗原结合片段选自fab片段、f(ab’)2片段、fab’片段、fv片段。在任何提供的实施方案中的一些中,至少一个结合结构域特异性结合sars病毒的s(刺突)糖蛋白。在任何提供的实施方案中的一些中,至少一个结合结构域是选自sti-1499、sti-4398、regn10933、regn10987、r egn-cov2和js016的抗体的抗原结合片段。在任何提供的实施方案中的一些中,至少一个结合结构域是选自是选自以下的抗体的抗原结合片段:sti-1499、sti-4398、sti-2020、regn10933、regn10987、regn-cov2、js016、ly-cov555、ly-3819253、tb181-8、t b181-28、tb181-36、bgb-dxp593、ty027、ct-p59、brii-196、b rii-198、scta01、mw33、azd8895、azd1061、hlx70、15g11、18f4、1e5、1g3、21c3、22d(、23d11、26e2、29f7、3b3、3f2、d59047-11955、d70678-12637-s1、d70678-12799-s1、d70678-13531-s1、d70678-13576-s1、d70678-14004-s2、d70678-14027-s2、d70678-2155-s1、d70678-2743-s1或d70678-5521-s2。
22、在任何提供的实施方案中的一些中,至少一个结合结构域是单结构域抗体(sdab)。在任何提供的实施方案中的一些中,至少一个结合结构域是选自tb201-1、tb202-3、tb202-63的单结构域抗体。
23、在任何提供的实施方案中的一些中,至少一个结合结构域是抗体模拟物,任选地选自经设计的锚蛋白重复蛋白(darpin)、adnectins或抗原结合纤连蛋白iii型(fn3)支架。
24、本文提供了一种颗粒,其包含(i)如权利要求1至88中任一项所述的结合剂和(ii)能够由结合剂的至少一个结合结构域结合的病毒蛋白。
25、在任何提供的实施方案中的一些中,病毒蛋白是纯化的病毒蛋白。在任何提供的实施方案中的一些中,病毒蛋白是重组病毒蛋白。在任何提供的实施方案中的一些中,病毒蛋白是sars病毒的s(刺突)糖蛋白。在任何提供的实施方案中的一些中,病毒蛋白是sars冠状病毒1(sars cov-1)的s糖蛋白。在任何提供的实施方案中的一些中,病毒蛋白是sars冠状病毒2(sars cov-2)的s糖蛋白。在任何提供的实施方案中的一些中,病毒蛋白是sarscov-2变体的s糖蛋白。在任何提供的实施方案中的一些中,病毒蛋白是感兴趣的sars cov-2变体(voi)、关注的变体(voc)和/或有严重后果的变体(vohc)的s糖蛋白。在任何提供的实施方案中的一些中,病毒蛋白是选自包括以下的组的sars cov-2变体的s糖蛋白:α(即b.1.1.7)、β(即b.1.351、b.1.351.2、b.1.351.3)、δ(即b.1.617.2、ay.1、ay.2、ay.3)和γ(即p.1、p.1.1、p.1.2)。
26、本文提供了一种核酸分子,其编码本文提供的任何结合剂。在任何提供的实施方案中的一些中,结合剂的至少一个结合结构域包含可变重链(vh)和可变轻链(vl),其中核酸包含编码vh链和经修饰的fc的第一序列和编码vl链的第二序列,并且其中第一序列和第二序列被多顺反子元件分开。在任何提供的实施方案中的一些中,多顺反子元件包含编码核糖体跳跃元件的序列,所述核糖体跳跃元件选自t2a、p2a、e2a或f2a或内部核糖体进入位点(ires)。在任何提供的实施方案中的一些中,第一序列和第二序列可操作地连接到同一启动子。在任何提供的实施方案中的一些中,核酸分子是mrna。
27、本文提供了一种细胞,诸如包含所提供核酸中的任一种的细胞。
28、本文还提供一种载体,诸如包含本文提供的核酸分子中的任一种的载体。在任何提供的实施方案中的一些中,载体是病毒载体或病毒样颗粒。在任何提供的实施方案中的一些中,载体源自腺病毒。在任何提供的实施方案中的一些中,病毒载体源自腺相关病毒(aav)。在任何提供的实施方案中的一些中,aav属于血清型1、2、5、6、8或9。在任何提供的实施方案中的一些中,aav属于血清型8。在任何提供的实施方案中的一些中,aav属于血清型6。在任何提供的实施方案中的一些中,aav属于血清型6.2。在任何提供的实施方案中的一些中,病毒载体源自慢病毒。在任何提供的实施方案中的一些中,慢病毒是人免疫缺陷病毒-1(hiv-1)。
29、在任何提供的实施方案中的一些中,病毒载体或病毒样颗粒包含融合剂(fusogen)。在任何提供的实施方案中的一些中,载体是脂质颗粒,其中脂质颗粒包含(i)包围内腔的脂质双层,和(ii)融合剂,其中所述融合剂包埋在脂质双层中。在任何提供的实施方案中的一些中,脂质双层源自用于产生病毒或病毒样颗粒的宿主细胞膜。在任何提供的实施方案中的一些中,脂质双层源自用于产生病毒样颗粒的宿主细胞膜,其中所述病毒样颗粒是复制缺陷型的。在任何提供的实施方案中的一些中,融合剂是选自i类病毒膜融合蛋白、ii类病毒膜蛋白、ii类病毒膜融合蛋白、病毒膜糖蛋白或病毒包膜蛋白的病毒融合剂。
30、在任何提供的实施方案中的一些中,融合剂是水疱性口炎病毒包膜糖蛋白(vsv-g)。在任何提供的实施方案中的一些中,融合剂是狒狒内源性病毒(baev)包膜糖蛋白。在任何提供的实施方案中的一些中,融合剂是合胞体蛋白。在任何提供的实施方案中的一些中,融合剂来自冠状病毒。在任何提供的实施方案中的一些中,融合剂是严重急性呼吸综合征(sars)冠状病毒1(sars cov-1)刺突糖蛋白。在任何提供的实施方案中的一些中,融合剂是严重急性呼吸综合征(sars)冠状病毒2(sars cov-2)刺突糖蛋白。在任何提供的实施方案中的一些中,融合剂是α冠状病毒cd13蛋白。
31、在任何提供的实施方案中的一些中,融合剂包含来自副粘病毒的f蛋白分子或其生物活性部分和/或来自副粘病毒的糖蛋白g(g蛋白)或其生物活性部分。在任何提供的实施方案中的一些中,融合剂源自来自副粘病毒的f蛋白分子或其生物活性部分和/或来自副粘病毒的糖蛋白g(g蛋白)或其生物活性部分。在任何提供的实施方案中的一些中,副粘病毒是亨尼帕病毒(henipavirus)。在任何提供的实施方案中的一些中,副粘病毒是尼帕病毒(nipah virus)。在任何提供的实施方案中的一些中,副粘病毒是亨德拉病毒(hendravirus)。
32、在任何提供的实施方案中的一些中,融合剂是包含结合靶细胞上的分子的靶向部分的再靶向融合剂。在任何提供的实施方案中的一些中,靶向部分是经设计的锚蛋白重复蛋白(darpin)、单结构域抗体(sdab)、单链可变片段(scfv)或抗原结合纤连蛋白iii型(fn3)支架。
33、在任何提供的实施方案中的一些中,靶细胞已知或怀疑被冠状病毒感染。在任何提供的实施方案中的一些中,靶向部分结合冠状病毒的受体。在任何提供的实施方案中的一些中,靶向部分结合血管紧张素转化酶2(ace2)。在任何提供的实施方案中的一些中,靶细胞是b淋巴细胞。在任何提供的实施方案中的一些中,靶向部分结合人cd20。
34、在任何提供的实施方案中的一些中,融合剂被修饰以降低其天然结合向性。在任何提供的实施方案中的一些中,g蛋白或其生物活性部分是突变体niv-g蛋白,其表现出与肝配蛋白(ephrin)b2或肝配蛋白b3的结合减少。
35、在任何提供的实施方案中的一些中,突变体niv-g蛋白包含一个或多个氨基酸取代,所述氨基酸取代对应于选自由参考seq id no:5中所示的编号的e501a、w504a、q530a和e533a组成的组的氨基酸取代。在任何提供的实施方案中的一些中,突变体niv-g蛋白具有seq id no:34中所示的氨基酸序列或与seq id no:34具有为或约80%、至少或约81%、至少或约82%、至少或约83%、为或约84%、至少或约85%、至少或约86%、或至少或约87%、至少或约88%、或至少或约89%、至少或约90%、至少或约91%、至少或约92%、至少或约93%、至少或约94%、至少或约95%、为或约96%、至少或约97%、至少或约98%或至少或约99%序列同一性的氨基酸序列。在任何提供的实施方案中的一些中,突变体niv-g蛋白具有seq id no:35中所示的氨基酸序列或与seq id no:35具有为或约80%、至少或约81%、至少或约82%、至少或约83%、为或约84%、至少或约85%、至少或约86%、或至少或约87%、至少或约88%、或至少或约89%、至少或约90%、至少或约91%、至少或约92%、至少或约93%、至少或约94%、至少或约95%、为或约96%、至少或约97%、至少或约98%或至少或约99%序列同一性的氨基酸序列。在任何提供的实施方案中的一些中,niv-f蛋白是其生物活性部分,其在野生型niv-f蛋白(seq id no:19)的c末端或其附近具有20个氨基酸截短。在任何提供的实施方案中的一些中,niv-f蛋白具有seq id no:32中所示的氨基酸序列或与seq id no:32具有为或约80%、至少或约81%、至少或约82%、至少或约83%、为或约84%、至少或约85%、至少或约86%、或至少或约87%、至少或约88%、或至少或约89%、至少或约90%、至少或约91%、至少或约92%、至少或约93%、至少或约94%、至少或约95%、为或约96%、至少或约97%、至少或约98%或至少或约99%序列同一性的氨基酸序列。在任何提供的实施方案中的一些中,niv-f蛋白是其生物活性部分,其在野生型niv-f蛋白(seq id no:37)的c末端或其附近具有22个氨基酸截短。在任何提供的实施方案中的一些中,niv-f蛋白具有seq id no:36中所示的氨基酸序列或与seq id no:36具有为或约80%、至少或约81%、至少或约82%、至少或约83%、为或约84%、至少或约85%、至少或约86%、或至少或约87%、至少或约88%、或至少或约89%、至少或约90%、至少或约91%、至少或约92%、至少或约93%、至少或约94%、至少或约95%、为或约96%、至少或约97%、至少或约98%或至少或约99%序列同一性的序列。在任何提供的实施方案中的一些中,niv-f蛋白具有seq idno:38中所示的氨基酸序列或与seq id no:38具有为或约80%、至少或约81%、至少或约82%、至少或约83%、为或约84%、至少或约85%、至少或约86%、或至少或约87%、至少或约88%、或至少或约89%、至少或约90%、至少或约91%、至少或约92%、至少或约93%、至少或约94%、至少或约95%、为或约96%、至少或约97%、至少或约98%或至少或约99%序列同一性的序列。
36、在任何提供的实施方案中的一些中,niv-f蛋白包含n-连接糖基化位点上的点突变。在任何提供的实施方案中的一些中,niv-f蛋白是其生物活性部分,其包含:i)在野生型niv-f蛋白(seq id no:36)的c末端或其附近的20个氨基酸截短;和ii)n-连接糖基化位点上的点突变。
37、本文提供了一种产生结合剂的方法,所述方法包括在细胞中表达结合剂的条件下,将如权利要求93至98中任一项所述的核酸分子或如权利要求99至144中任一项所述的载体引入宿主细胞中。在任何提供的实施方案中的一些中,方法还包括从细胞中分离或纯化结合剂。
38、本文还提供了一种形成免疫复合物的方法,所述方法包括向已知或怀疑患有病毒感染的受试者施用所提供的任一者的一种或多种结合剂,其中在受试者中形成包含所施用的一种或多种结合剂的免疫复合物。
39、在任何提供的实施方案中的一些中,免疫复合物还包含至少一种针对暴露于病毒表面的病毒蛋白的内源性抗体。在任何提供的实施方案中的一些中,一种或多种结合剂和至少一种内源性抗体结合相同的病毒蛋白。在任何提供的实施方案中的一些中,一种或多种结合剂和至少一种内源性剂结合病毒蛋白的相同表位。在任何提供的实施方案中的一些中,一种或多种结合剂和至少一种内源性剂结合病毒蛋白的不同表位。在任何提供的实施方案中的一些中,一种或多种结合剂和至少一种内源性剂结合病毒蛋白的重叠表位。
40、本文提供了一种组合物,其包含免疫复合物,所述免疫复合物包含:(i)所提供结合剂中的任一种和(ii)由结合剂的至少一个结合结构域结合的表面暴露的病毒蛋白。
41、在任何提供的实施方案中的一些中,免疫复合物包含两种或更多种结合剂。在任何提供的实施方案中的一些中,至少两个结合结构域结合病毒蛋白的不同表位。在任何提供的实施方案中的一些中,免疫复合物还包含任选地来自一种和/或多种内源性抗体的内源性结合结构域。在任何提供的实施方案中的一些中,至少两个结合结构域和内源性结合结构域结合病毒蛋白的相同表位。在任何提供的实施方案中的一些中,至少两个结合结构域和内源性结合结构域结合病毒蛋白的不同表位。在任何提供的实施方案中的一些中,至少两个结合结构域和内源性结合结构域结合病毒蛋白的重叠表位。
42、本文提供了一种药物组合物,其包含所提供结合剂中的任一种、所提供核酸中的任一种、所提供细胞、所提供载体和/或所提供颗粒中的任一种。
43、本文还提供了一种药物组合物,其包含(i)如权利要求1至88中任一项所述的结合剂和(ii)能够由结合剂的至少一个结合结构域结合的重组病毒蛋白。
44、在任何提供的实施方案中的一些中,药物组合物包含药学上可接受的赋形剂。在任何提供的实施方案中的一些中,药物组合物是无菌的。
45、本文提供了一种减轻受试者中响应于病毒感染的炎症的方法,所述方法包括向已知或怀疑患有病毒感染的受试者施用治疗有效量的所提供结合剂中的任一种、所提供颗粒中的任一种、所提供核酸中的任一种、所提供细胞中的任一种或所提供载体中的任一种。
46、本文提供了一种减轻受试者中响应于病毒感染的炎症的方法,所述方法包括向已知或怀疑患有病毒感染的受试者施用治疗有效量的所提供药物组合物中的任一种。
47、本文还提供了一种减轻受试者中响应于病毒感染的炎症的方法,所述方法包括向已知或怀疑患有病毒感染的受试者施用(i)治疗有效量的所提供药物组合物中的任一种,(ii)能够由结合剂的至少一个结合结构域结合的重组病毒蛋白。
48、在任何提供的实施方案中的一些中,炎症包括肺中的淋巴细胞积聚、肺中的淋巴细胞增殖、外周血淋巴细胞减少、促炎性细胞因子产生或前述任一者的组合。在任何提供的实施方案中的一些中,促炎性细胞因子选自由以下组成的组:mcp-1、il-8、il-1β、ifn-γ、ip-10、il-4、il-10、il-2、il-7、gcsf、mip-1a和tnf-α。
49、在任何提供的实施方案中的一些中,同时施用药物组合物和重组病毒蛋白。在任何提供的实施方案中的一些中,依序施用药物组合物和重组病毒蛋白,任选地其中首先施用重组病毒蛋白。在任何提供的实施方案中的一些中,依序施用药物组合物和重组病毒蛋白,任选其中首先施用药物组合物。
50、本文提供了一种促进抑制性免疫复合物功能的方法,其包括施用治疗有效量的所提供药物组合物中的任一种。
51、本文还提供了一种促进抑制性免疫复合物功能的方法,其包括施用治疗有效量的所提供结合剂中的任一种、所提供颗粒中的任一种、所提供核酸中的任一种、所提供细胞中的任一种、所提供载体中的任一种。
52、在任何提供的实施方案中的一些中,抑制性免疫复合物功能包括减少的抗原摄取、减少的抗原呈递、减少的细胞激活、减少的抗体分泌、抗炎细胞因子的产生或前述任一者的组合。
53、本文提供了一种降低激活免疫复合物功能的方法,其包括施用治疗有效量的所提供药物组合物中的任一种。
54、本文还提供了一种降低激活免疫复合物功能的方法,其包括施用治疗有效量的所提供结合剂中的任一种、所提供颗粒中的任一种、所提供核酸中的任一种、所提供细胞中的任一种、所提供载体中的任一种。
55、在任何提供的实施方案中的一些中,激活免疫复合物功能包括抗体依赖性细胞介导的细胞毒性(adcc)、抗体依赖性增强(ade)、炎性介质的释放、前细胞因子的产生、吞噬作用或前述任一者的组合。
56、在任何提供的实施方案中的一些中,方法还包括治疗受试者的病毒感染。在任何提供的实施方案中的一些中,病毒感染是由具有被结合剂的至少一个结合结构域识别的表面暴露的病毒蛋白的病毒引起的感染。在任何提供的实施方案中的一些中,病毒是rna病毒。在任何提供的实施方案中的一些中,病毒选自sars-cov-1、sars-cov-2、mers、rsv、流感病毒和麻疹病毒。
57、本文还提供了本文提供的结合剂、颗粒、核酸、细胞、载体或药物组合物中的任一种,其用于减轻受试者中响应于病毒感染的炎症的方法中。本文还提供了本文提供的结合剂、颗粒、核酸、细胞、载体或药物组合物中的任一种在制造用于减轻受试者中响应于病毒感染的炎症的药物中的用途。在任何上述实施方案中的一些中,减轻受试者中响应于病毒感染的炎症的方法还包括使用能够由结合剂的至少一个结合结构域结合的重组病毒蛋白。
58、官能化含氟化合物(例如芳基氟化物)常常被用作医药剂。在一些实施方案中,这些产品具有有利的药理学特性,例如理想的代谢稳定性。
59、本文提供了本文提供的结合剂、颗粒、核酸、细胞、载体或药物组合物中的任一种,其用于促进抑制剂免疫复合物功能的方法中。本文还提供了本文提供的结合剂、颗粒、核酸、细胞、载体或药物组合物中的任一种在制备用于降低激活免疫复合物功能的药物中的用途。
- 还没有人留言评论。精彩留言会获得点赞!