靶向SOX2抗原的免疫治疗的制作方法
靶向sox2抗原的免疫治疗
1.关于序列表的陈述
2.与本技术相关的序列表以text格式提供以替代纸质副本,并通过引用结合于本文说明书中。包含序列表的text文件的名称是360056_47701wo_sequence_listing.txt。该text文件为158kb,创建于2021年9月23日,并通过efs-web以电子方式提交。
背景技术:
3.各种恶性肿瘤(包括多发性骨髓瘤)的临床结果差,遵循标准护理治疗后的复发性疾病与极差的预后相关。标准治疗方案包括外科手术、放射疗法和/或化学疗法;然而,这些方法并不是对所有患者都有效,并且可能伴有毒性。因此,需要针对难以治疗的癌症制定新的策略。本公开解决了这种需求,并进一步提供了其他相关优势。
附图说明
4.图1提供了示出在高尔基抑制剂(golgi plug)和高尔基阻断剂(golgi block)存在的情况下,用1μg/ml sox2肽、培养基或细胞刺激剂(cell stimulation cocktail)刺激4小时后,在(上)具有sox2反应性的示例性cd8
+
t细胞系和(下)没有sox2反应性的示例性cd8
+
t细胞系中产生ifn-γ的t细胞的百分比的流式细胞术图。数据来自3轮刺激后的第10-14天。
5.图2提供了示出sox2反应性和hla-a*02:01限制性的示例性cd8
+
t细胞系中产生ifn-γ的t细胞的百分比的流式细胞术图。数据来自3轮刺激后的第10-14天,在高尔基抑制剂和高尔基阻断剂存在的情况下,用1μg/ml sox2肽、培养基或预先加载有sox2肽或培养基的t2细胞刺激持续4小时。
6.图3提供了示出对六种不同的sox2肽(如图所示)做出反应的cd8
+
t细胞系中产生ifn-γ的t细胞的百分比的流式细胞术图。
7.图4提供了示出经修饰以表达标准蛋白酶体(293e-sp)或免疫蛋白酶体(293e-ip)的293e靶细胞表达sox2的数据。
8.图5提供了示出如示例中所述的使用标记的sox2
+
293e靶细胞进行杀伤试验(incucyte)的实验设置的图解。
9.图6提供了示出sox2(277-287)和sox2(58-66)表位由标准蛋白酶体(sp)处理的incucyte杀伤试验的数据。在incucyte s3系统中在两天的时间内对孔进行成像,并对rapidred
+
caspase 3/7green
+
靶细胞的量进行量化。
10.图7提供了示出sox2(277-287)和sox2(58-66)表位由免疫蛋白(ip)处理的incucyte杀伤试验的数据。在incucyte s3系统中在两天的时间内对孔进行成像,并对rapidred
+
caspase 3/7green
+
靶细胞的量进行量化。
11.图8提供了示出sox2(277-287)特异性t细胞杀伤sox2
+
浆细胞白血病细胞的incucyte杀伤试验的数据。在incucyte s3系统中在两天的时间内对孔进行成像,并对rapidred
+
caspase 3/7green
+
靶细胞的量进行量化。
12.图9提供了示出sox2(277-287)特异性t细胞杀伤sox2
+
卵巢癌细胞的incucyte杀
伤试验的数据。在incucyte s3系统中在两天的时间内对孔进行成像,并对rapidred
+
caspase 3/7green
+
靶细胞的量进行量化。
13.图10示出了用于分选sox2特异性cd8
+
t细胞的肽:hla四聚体门控试验的数据。
14.图11a-11m提供了与根据本公开的示例性sox2特异性t细胞及其用途相关的附加数据和实验设计。图11a示出了(上)评估cd8
+
t细胞系对sox2肽库反应产生ifn-γ的实验方案,以及(下)代表性数据。图11b示出了评估cd8
+
t细胞系在一定浓度范围内对sox2肽反应产生ifn-γ的实验方案。图11c和11d示出了使用图11b所示的实验方案的某些t细胞系的数据。图11e示出了评估cd8
+
t细胞系对用sox2肽脉冲的t2细胞反应产生ifn-γ的实验方案。图11f示出了使用图11e所示的实验方案的某些t细胞系的数据。图11g示出了评估在sox2肽存在下扩增的cd8
+
t细胞中cd137表达(作为激活的测量)的实验方案。图11h示出了使用图11g所示的实验方案的t细胞系的数据。图11i示出了在杀伤试验中使用标记的l363靶细胞评估在sox2肽存在下扩增的cd8
+
t细胞系杀伤活性的实验方案。图11j示出了使用图11i所示的实验方案的某些t细胞系的数据。图11k示出了将l363细胞注射到人源化小鼠模型的实验方案。图11l示出了接受一种或另一种剂量的l363细胞或不接受l363细胞的人源化小鼠随时间的存活情况。图11m示出了体内(3只小鼠)或体外l363细胞中稳定的sox2表达。
15.图12示出了某些sox2 277-287特异性tcr的功能亲合力(肽抗原logec
50
)。“tcr2”包含seq id no.:30的vα氨基酸序列和seq id no.:25的vβ氨基酸序列。“tcr4”包含seq id no.:42的vα氨基酸序列和seq id no.:37的vβ氨基酸序列。“tcr5”包含seq id no.:54的vα氨基酸序列和seq id no.:49的vβ氨基酸序列。“tcr6”包含seq id no.:66的vα氨基酸序列和seq id no.:61的vβ氨基酸序列。“tcr9”包含seq id no.:90的vα氨基酸序列和seq id no.:85的vβ氨基酸序列。“tcr10”包含seq id no.:102的vα氨基酸序列和seq id no.:97的vβ氨基酸序列。“tcr11”包含seq id no.:114的vα氨基酸序列和seq id no.:109的vβ氨基酸序列。“tcr13”包含seq id no.:126的vα氨基酸序列和seq id no.:121的vβ氨基酸序列。
16.图13示出了隔夜t细胞:肿瘤细胞共培养物的设置图,测试t细胞对内源性处理和呈递的sox2表位的识别。
17.图14和14a-14d示出了响应sox2
+
肿瘤细胞系,用tcr5或tcr10转导的t细胞的识别(表达cd137的t细胞百分比)。图14a-14d示出了图14部分的增强视图。
具体实施方式
18.本公开一般涉及sox2抗原和sox2抗原特异性的结合蛋白和免疫细胞(例如t细胞)。作为背景,免疫治疗可以对某些癌症有效。例如,t细胞免疫治疗可以对血液系统恶性肿瘤非常有效,临床试验评估了靶向cd19的嵌合抗原受体(car)基因修饰的治疗性t细胞治疗急性淋巴细胞白血病(all)的令人印象深刻的结果就是例证。然而,包含来自抗体(例如scfv、fab)的结合结构域的一些car仅限于靶向细胞表面表达的分子,并且识别具有疾病特异性表达模式(即,在健康细胞和组织上均不表达)的靶细胞表面抗原可能是一个挑战。替代的免疫治疗策略包括给予或诱导天然表达或经修饰表达t细胞受体(tcr,包括工程化tcr)的t细胞,该t细胞受体对源自内源性细胞蛋白的肽抗原具有特异性,并与hla分子缔合存在于细胞表面。
19.选择合适的抗原靶点对于有效的免疫治疗非常重要。细胞表面抗原(例如,多发性骨髓瘤中的cd19、bcma或cd138)在治疗后表达频繁减少,可能导致抗原低或抗原阴性细胞的过度生长和疾病复发。因此,免疫治疗的成功抗原靶点包括那些在肿瘤上选择性表达的抗原,由在疾病人群中高度流行的广泛表达的hla等位基因呈现,并涉及恶性表型的诱导或维持。
20.本公开说明sox2是一种用于癌症免疫治疗的候选抗原靶点。本发明部分提供了来自sox2的抗原肽,其能够引发免疫细胞反应并在某些癌症中表达,包括例如多发性骨髓瘤、浆细胞白血病、卵巢癌、胶质瘤、肺癌、颈癌和宫颈癌。
21.在某些实施例中,抗原肽意外且有利地通过标准蛋白酶体(sp)处理途径进行处理,该标准蛋白酶体处理途径由某些非造血恶性肿瘤中的癌症细胞使用;以及通过免疫蛋白酶体(ip)处理途径进行处理,该免疫蛋白酶体处理途径由某些血液肿瘤中的癌症细胞使用,但在某些情况下较少使用或不被实体肿瘤细胞使用。
22.因此,在一些实施例中,抗原肽可用于靶向一系列恶性肿瘤,无论恶性细胞是否利用sp处理、ip处理或两种处理。
23.本公开还提供能够结合sox2抗原的结合蛋白(例如,在肽:hla复合物的上下文中)。结合蛋白能够(例如,当由宿主细胞如免疫细胞(例如t细胞)表达时)结合并促进呈递这种抗原的细胞的杀伤(例如,与hla分子(如hla-a*02:01)复合)。在一些实施例中,结合包括如本文所公开的特异性结合。本公开还提供了宿主细胞(例如,免疫细胞,例如t细胞),其编码并能够表达sox2特异性结合蛋白,所述sox2特异结合蛋白能够与含有sox2抗原的肽结合,并且能够与编码结合蛋白的分离的多核苷酸结合。在某些实施例中,提供了包含编码结合蛋白的多核苷酸的修饰的免疫细胞,该结合蛋白能够结合到含有本公开sox2抗原的肽,以及本公开组合物用于治疗疾病(例如,癌症)、引发免疫应答或识别抗原反应性细胞等的用途。
24.目前公开的结合蛋白、多核苷酸、载体、宿主细胞、组合物和方法可用于治疗实体瘤、血液恶性肿瘤或两者。在某些实施例中,本公开的结合蛋白、多核苷酸、载体、宿主细胞、组合物和方法可用于治疗其中癌症细胞表达sox2并表达标准蛋白酶体的癌症,或其中癌症细胞表达sox2和免疫蛋白酶体的癌症,或其中癌症细胞表达sox2和标准蛋白酶体及免疫蛋白酶体的癌症。
25.在更详细地阐述本公开之前,提供本文中使用的某些术语的定义可能有助于理解本公开。在整个本公开中阐述了其他的定义。
26.在本说明书中,除非另有说明,否则任何浓度范围、百分比范围、比率范围或整数范围应理解为包括所述范围内的任何整数的值,并且在适当时包括其分数(例如整数的十分之一和百分之一)。此外,除非另有说明,否则本文所述的与任何物理特征(例如聚合物亚基、尺寸或厚度)相关的任何数量范围应理解为包括所述范围内的任何整数。除非另有说明,否则如本文所用的术语“约”是指所示范围、数值或结构的
±
20%。应当理解,如本文所用的术语“一(a)”和“一个(an)”指的是所列举的组分中的“一个或多个”。替代方案(如“或”)的使用应理解为替代方案中的任一个、两者或其任何组合。如本文所用,术语“包括(include)”、“具有(have)”和“包括(comprise)”是同义词,这些术语及其变体旨在被解释为非限制性的。
27.此外,应当理解,本技术公开了衍生自本文所述结构和取代基的各种组合的单个化合物或化合物组,其公开程度与单独阐述每个化合物或化合物组的程度相同。因此,特定结构或特定取代基的选择在本公开的范围内。
28.术语“基本上由
……
组成”并不等同于“包括”,而是指权利要求的特定材料或步骤,或指不实质上影响所要求保护的主题的基本特征的那些材料或步骤。例如,蛋白质结构域、区或模块(例如,结合结构域、铰链区、接头模块)或蛋白质(其可能具有一个或多个结构域、区或模块)“基本上由”特定氨基酸序列组成,当结构域、区、模块或蛋白质的氨基酸序列包括延伸、缺失、突变、或它们的组合(例如,在氨基或羧基末端或结构域之间的氨基酸)时,它们的组合占结构域、区、模块的长度至多20%(例如,至多15%、10%、8%、6%、5%、4%、3%、2%或1%),并且基本上不影响(即,不将活性降低超过50%,例如不超过40%、30%、25%、20%、15%、10%、5%或1%)结构域、区、模块或蛋白质的活性(例如,结合蛋白的靶结合亲和力)。
29.如本文所用,“蛋白质”或“多肽”是指氨基酸残基的聚合物。蛋白质适用于天然存在的氨基酸聚合物,以及其中一个或多个氨基酸残基是相应的天然存在氨基酸的人工化学模拟物的氨基酸聚合物和非天然存在的氨基酸聚合物。
[0030]“免疫球蛋白超家族结合蛋白”或“igsf结合蛋白”是指细胞表面或可溶性蛋白,其涉及识别、结合和/或粘附靶点(例如细胞、抗原、可溶性因子),并包含一个或多个免疫球蛋白结构域和/或免疫球蛋白折叠。本公开的igsf结合蛋白包含抗原识别结构域,例如可变结构域或可变区,如在抗体或其抗原结合片段(任何同种型)中发现的,或在t细胞受体或其抗原结合片段(例如igv区)中发现的。igsf蛋白可以具有靶点的天然结合特异性,或者可以被工程化以具有或增强靶点的结合特异性和/或亲和力。用于本公开的其他igsf蛋白包括,例如,包含igc1结构域、igc2结构域和/或igi结构域的蛋白;杀伤细胞免疫球蛋白样受体(kir);白细胞免疫球蛋白样受体(lilr);细胞粘附分子(cam);以及这些的组合。
[0031]
如本文所用,术语“免疫系统细胞”或“免疫细胞”是指源自骨髓中造血干细胞的免疫系统的任何细胞,其产生两个主要的谱系,即髓系祖细胞(其产生髓样细胞,如单核细胞、巨噬细胞、树突状细胞、巨核细胞和粒细胞)和淋巴祖细胞(其产生淋巴细胞,如t细胞、b细胞和自然杀伤(nk)细胞)。示例性免疫系统细胞包括cd4
+
t细胞、cd8
+
t细胞、cd4-cd8-双阴性t细胞、γδt细胞、调节性t细胞、干细胞记忆t细胞、自然杀伤细胞、自然杀伤t细胞和树突状细胞。巨噬细胞和树突状细胞可以被称为“抗原呈递细胞”或“apc”,它们是专门的细胞,当肽复合的apc表面上的主要组织相容性复合物(mhc)受体与t细胞表面的tcr相互作用时,可以激活t细胞。
[0032]“t细胞”或“t淋巴细胞”是在胸腺中成熟并产生t细胞受体(tcr)的免疫系统细胞。t细胞可以是幼稚的(“tn”;不暴露于抗原;与tcm相比,cd62l、ccr7、cd28、cd3、cd127和cd45ra的表达增加,而cd45ro的表达减少或不表达(本文所述))、记忆t细胞(tm)(经历过抗原且长期存活),包括干细胞记忆t细胞和效应细胞(经历过抗原,细胞毒性)。tm可进一步分为中央记忆t细胞(tcm,表达cd62l、ccr7、cd28、cd95、cd45ro和cd127)和效应记忆t细胞(tem,表达cd45ro,而cd62l、ccr7、cd28和cd45ra表达减少)的亚群。效应t细胞(te)是指表达cd45ra的经历过cd8
+
细胞毒性t淋巴细胞,与tcm相比,其cd62l、ccr7和cd28的表达降低,并且对颗粒酶和穿孔素呈阳性。辅助t细胞(th)是通过释放细胞因子影响其他免疫细胞活
性的cd4
+
细胞。cd4
+
t细胞可以激活和抑制适应性免疫应答,这两种功能中的哪一种被诱导将取决于其他细胞和信号的存在。可以使用已知技术收集t细胞,并且可以通过已知技术(例如通过与抗体的亲和结合、流式细胞术或免疫磁性选择)富集或耗尽其各种亚群或其组合。其他示例性t细胞包括调节性t细胞,例如cd4
+
cd25
+
(foxp3
+
)调节性t细胞和treg17细胞,以及tr1、th3、cd8
+
cd28-和qa-1限制性t细胞。
[0033]
术语“t细胞受体”(tcr)是指免疫球蛋白超家族成员(具有可变结合结构域、恒定结构域、跨膜区和短细胞质尾;参见,例如,janeway et al.,immunobiology:the immune system in health and disease,3rd ed.,current biology publications,p.433,1997),其能够与结合到mhc受体的抗原肽特异性结合。tcr可以在细胞表面或以可溶形式存在,通常由具有α和β多肽(分别称为tcrα和tcrβ)或γ和δ多肽(分别也称为tcrγ和tcrδ)的异二聚体组成。
[0034]
与其他免疫球蛋白(例如,抗体)一样,tcr多肽(例如,α-多肽、β-多肽)的胞外部分包含两个免疫球蛋白结构域,即位于n-末端的可变结构域(例如,α-多肽可变结构域或vα多肽或vβ多肽;通常是基于kabat编号的氨基酸1-116)(kabat et al.,"sequences of proteins ofimmunological interest,us dept.health and human services,public health service national institutes of health,1991,5th ed.)和与细胞膜相邻的恒定结构域(例如,α链恒定结构域或cα,通常是基于kabat的5个氨基酸117至259,β链恒定结构或cβ,通常是基于kabat氨基酸117至295)。同样,与抗体一样,可变结构域包含由框架区(fr)分隔的互补决定区(cdr)(参见,例如,jores et al.,proc.nat'l acad.sci.usa87:9138,1990;chothia et al.,embo j.7:3745,1988;see also lefranc et al.,dev.comp.immunol.27:55,2003)。本公开中使用的tcr的来源可以来自各种动物物种中的任何一种,例如人、小鼠、大鼠、兔子或其他哺乳动物。
[0035]
术语“可变区”或“可变结构域”是指免疫球蛋白超家族结合蛋白(例如tcrα多肽或β多肽(或γδtcr的γ多肽和δ多肽))的结构域,其涉及免疫球蛋白超家族结合蛋白(如tcr、抗体)与抗原的结合。天然tcr的α多肽和β多肽的可变结构域(分别为vα和vβ)通常具有相似的结构,每个结构域包括四个保守的框架区(fr)和三个cdr。vα结构域由两个单独的dna片段编码,即可变基因片段和连接基因片段(v-j);vβ结构域由三个单独的dna片段编码,即可变基因片段、多样性基因片段和连接基因片段(v-d-j)。单个vα或vβ结构域可能足以赋予抗原结合特异性。此外,可以使用来自结合抗原的tcr中的vα或vβ结构域来分离结合特定抗原的tcr,以分别筛选互补的vα或vβ结构域的库。
[0036]
术语“互补决定区”和“cdr”与“高变区”或“hvr”同义,并且在本领域中已知是指免疫球蛋白(例如tcr)可变区内的氨基酸序列,其赋予抗原特异性和/或结合亲和力,并通过框架区彼此分离。一般而言,每个tcrα-多肽可变区有三个cdr(αcdr1、αcdr2、αcdr3),每个tcr-β-多肽可变区有三个cdr(βcdr1、βcdr2、βcdr3)。在抗体(仅重链抗体除外)的情况下,存在重链和轻链可变区,并且这些可变区中的每一个都包含三个cdr(cdrh1、cdrh2、cdrh3、cdrl1、cdrl2、cdrl3)。
[0037]
在tcr中,cdr3被认为是负责识别加工抗原的主要cdr。通常,cdr1和cdr2主要与mhc相互作用。
[0038]
cdr1和cdr2编码于tcr可变区编码序列的可变基因片段内,而cdr3由跨越vα的可
变和连接片段的区域,或跨越vβ的可变、多样性和连接片段的区域编码。因此,如果已知vα或vβ的可变基因片段的同一性,则可以推断出其相应cdr1和cdr2的序列。与cdr1和cdr2相比,由于重组过程中核苷酸的添加和丢失,cdr3通常更加显著多样化。tcr中的cdr3β和抗体中的cdrh3是典型的情况。
[0039]
tcr和抗体可变结构域序列可以与编号方案(例如,kabat,chothia,enhanced chothia,eu,imgt和aho)相一致,从而允许注释等效的残基位置并使用例如anarci软件工具比较不同的分子(2016,bioinformatics 15:298-300)。编号方案提供了tcr可变结构域中框架区和cdr的标准化描绘。在某些实施例中,可变结构域序列根据imgt编号方案(参见lefranc et al.,dev.comp.immunol.27:55,2003and imgt.org)。在一些实施例中,tcr的cdr序列(氨基酸或编码核苷酸)包括或在v和j等位基因的连接处编码、或在v和d等位基因的连接处编码、或在d和j等位基因连接处编码的序列(氨基酸或编码核苷酸)。imgt连接是本领域普通技术人员所认识的。例如,在seq id no.:25:dvkvtqssrylvkrtgekvflecvqdmdhenmfwyrqdpglglrliyfsydvkm kekgdipegysvsrekkerfslilesastnqtsmylcasslilagrntgelffgegsr ltvle中所述的tcr vβ序列中,imgt cdr3氨基酸序列是asslilagrntgelf(seq id no.:28),包括连接氨基酸的imgt cdr3氨基酸序列是casslilagrntgelff(seq id no.:29)。本文公开的某些cdr序列包含连接氨基酸。
[0040]
在某些实施例中,tcr存在于t细胞(或t淋巴细胞)表面并与cd3复合物相关。“cd3”是六个多肽的多蛋白复合物(参见abbas and lichtman,2003;janeway et al.,p.172and 178,1999),其与t细胞中的抗原信号传导相关。在哺乳动物中,复合物包括一条cd3γ链、一个cd3δ多肽、两个cd3ε多肽和一个cd3ζ多肽的同二聚体。cd3γ、cd3β和cd3ε多肽是含有单个免疫球蛋白结构域的免疫球蛋白超家族的相关细胞表面蛋白。cd3γ、cd3β和cd3ε多肽的跨膜区带负电荷,据信这允许这些多肽与带正电荷的t细胞受体多肽结合。cd3γ、cd3β和cd3ε多肽的细胞内尾部各含有一个保守基序,称为免疫受体酪氨酸激活基序或itam,而每个cd3ζ链有三个itam。不希望被理论束缚,据信itam对于tcr复合物的信号传递能力很重要。本公开中使用的cd3可以来自各种动物物种,包括人类、小鼠、大鼠或其他哺乳动物。
[0041]
如本文所用,术语“tcr复合物”是指通过cd3与tcr缔合形成的复合物。例如,tcr复合物可以由cd3γ多肽、cd3β多肽、两个cd3ε多肽、cd3ζ多肽的同二聚体、tcrα多肽和tcrβ多肽组成。或者,tcr复合物可以由cd3γ链、cd3β链、两个cd3ε链、cd3ζ链的同二聚体、tcrγ链和tcrβ链组成。
[0042]
如本文所用,“tcr复合物的组分”是指tcr链(即tcrα、tcrβ、tcrγ或tcrδ)、cd3链(即cd3γ、cd3δ、cd3ε或cd3ζ)、或由两个或多个tcr多肽或cd3多肽形成的复合物(例如,tcrα和tcrβ的复合物、tcrγ和tcrδ的复合物、cd3ε和cd3δ的复合物、cd3γ和cd3ε的复合物、或tcrα、tcrβ、cd3γ、cd3δ和两个cd3ε多肽的亚tcr复合物)。
[0043]“嵌合抗原受体”(car)是指融合蛋白,该融合蛋白经工程改造以包含两个或多个天然存在的氨基酸序列,这些氨基酸序列以非天然存在或非天然存在于宿主细胞中的方式连接在一起,当存在于细胞表面时,融合蛋白可以作为受体发挥作用。car可以包括细胞外部分,该细胞外部分包含与跨膜结构域和一个或多个细胞内信号传导结构域(可选地包含共刺激结构域)连接的抗原结合结构域(例如,从免疫球蛋白或免疫球蛋白样分子获得或衍生,例如从癌症抗原特异性tcr获得或衍生的tcr结合结构域、从抗体衍生或获得的scfv、或
从来自nk细胞的杀伤免疫受体衍生或获得的抗原结合结构域)(参见,sadelain et al.,cancer discov.,3(4):388(2013);也参见harris and kranz,trends pharmacol.sci.,37(3):220(2016),stone et al.,cancer immunol.immunother.,63(11):1163(2014),and walseng et al.,scientific reports 7:10713(2017),其中car构建体及其制造方法通过引用并入本文)。在一些实施例中,与抗原特异性结合的本公开car(例如,在肽:hla复合物的情况下)包括tcr vα结构域和vβ结构域。
[0044]
如本文所用,“融合蛋白”或“融合多肽”是指在单链中具有至少两个不同的结构域、序列、基序的蛋白质,其中该结构域、序列或基序并非天然地(例如,以特定的排列、顺序或数量、或所有都有)一起存在于蛋白质中。在某些实施例中,融合蛋白包含至少两个不同的结构域或基序,它们不是天然地一起存在于单个肽或多肽中。编码融合蛋白的多核苷酸可以使用pcr、重组工程等构建,或者可以合成这样的融合蛋白。
[0045]
如本文所用,“抗原”或“ag”是指激发免疫应答的免疫原性分子。这种免疫应答可能涉及抗体的产生、特定免疫活性细胞(例如t细胞)的激活或两者都有。抗原(免疫原性分子)可以是例如肽、糖肽、多肽、糖多肽、多核苷酸、多糖、脂质等。很明显,抗原可以合成、重组产生或衍生自生物样品。可包含一种或多种抗原的示例性生物样品包括组织样品、肿瘤样品、细胞、生物流体或其组合。抗原可由经修饰或基因工程化以表达抗原的细胞产生,或由内源性(例如,未经人为干预的修饰或基因工程)表达免疫原性的突变或多态性的细胞产生。
[0046]
术语“表位”或“抗原表位”包括被同源结合分子识别并特异性结合的任何分子、结构、氨基酸序列或蛋白质决定簇,如免疫球蛋白、t细胞受体(tcr)、嵌合抗原受体或其他结合分子、结构域或蛋白质。表位决定簇通常包含分子的化学活性表面基团,如氨基酸或糖侧链,并且可以具有特定的三维结构特征以及特定的电荷特征。
[0047]“sox2”在本领域也称为“sry-2”和“性别决定区y”,其是涉及未分化胚胎干细胞的自我更新、胚胎干细胞和神经干细胞的维持以及某些癌症的恶性表型的转录因子。sox2是转录因子sox家族的成员之一,其共有约80个氨基酸的高迁移率组(hmg)盒结构域。人sox2的氨基酸序列在seq id no:1中提供。
[0048]
如本文所用,术语“sox2抗原”是指sox2蛋白的天然或合成产生的肽部分,其长度范围为约7个氨基酸至约25个氨基酸或更多。在一些实施例中,sox2抗原的长度包括约9个氨基酸、约10个氨基酸、约11个氨基酸、约12个氨基酸、约13个氨基酸、约14个氨基酸、约15个氨基酸、约16个氨基酸、约17个氨基酸、约18个氨基酸、约19个氨基酸、约20个氨基酸、约21个氨基酸、约22个氨基酸、约23个氨基酸、约24个氨基酸、约25个氨基酸、约30个氨基酸、约35个氨基酸或更多。在一些实施例中,sox2抗原的长度包括9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24或25个氨基酸。在某些实施例中,“sox2抗原”与“sox2肽”或“sox2抗原肽”或“sox2肽抗原”可互换使用。在一些实施例中,sox2抗原包括或由seq id no:2、3、4、5、6或7中所述的氨基酸序列组成。还考虑参考sox2抗原的抗原性氨基酸序列变体,其包括或由seq id no:2、3、4、5、6或7中所述的氨基酸序列组成。变体通常具有与参考sox2抗原相同的长度,但与参考sox2抗原相比,变体可包括一个或多个氨基酸变化和/或翻译后修饰的差异,同时保留参考sox2抗原的抗原性、hla相容性以及一般结构和电荷特性。
[0049]
抗原呈递细胞(apc)(例如树突状细胞、巨噬细胞、淋巴细胞或其他细胞类型)处理
抗原以及apc将抗原呈递给t细胞的原理,包括免疫相容(例如共享至少一种与抗原呈递相关的mhc基因的等位基因形式)apc和t细胞之间的主要组织相容性复合物(mhc)限制性呈递,均已确立(参见,例如,murphy,janeway’s immunobiology(8th ed.)2011garland science,ny;chapters 6,9and 16)。例如,源自胞质溶胶(例如肿瘤抗原、细胞内病原体)的经处理的抗原肽的长度通常为约7个氨基酸至约11个氨基酸,并与i类mhc(hla)分子缔合,而在囊泡系统(例如细菌、病毒)中处理的肽的长度从约10个氨基酸到约25个氨基酸不等,并与ii类mhc(hla)分子缔合。
[0050]“主要组织相容性复合物”(mhc)是指将肽抗原递送到所有有核细胞的细胞表面的糖蛋白。mhc i类分子是具有跨膜α多肽(具有三个α结构域)和非共价结合的β2微球蛋白的异二聚体。mhc ii类分子由两种跨膜糖蛋白α和β组成,它们都跨越膜。每个多肽有两个结构域。mhc i类分子将源自胞质溶胶的肽递送至细胞表面,其中肽:mhc复合物被cd8
+
t细胞所识别。mhc ii类分子将源自囊泡系统的肽递送至细胞表面,其中它们被cd4
+
t细胞所识别。人类mhc被称为人类白细胞抗原(hla)。对应于“i类”mhc的hla从细胞内部呈现肽,包括例如hla-a、hla-b和hla-c。等位基因包括,例如,hla-a*02:01;hla-a*03:01;hla-a*11:01;hla-b*40:01;hla-b*44:02;或hla-b*44:03。对应于“ii类”mhc的hla从细胞外部呈现肽,包括例如hla-dp、hla-dm、hla-doa、hla-dob、hla-dq和hla-dr。
[0051]
如本文所用,术语“cd8共受体”或“cd8”是指细胞表面糖蛋白cd8,作为α-α同二聚体或α-β异二聚体。cd8共受体有助于细胞毒性t细胞(cd8
+
)的功能,并通过其胞质酪氨酸磷酸化途径通过信号传导发挥作用(gao and jakobsen,immunol.today 21:630-636,2000;cole and gao,cell.mol.immunol.1:81-88,2004)。有五(5)种已知的cd8β多肽同种型(参见uniprotkb标识符p10966)和一种已知的cd8α多肽(参见uniprotkb标识符p01732)。
[0052]“cd4”是一种免疫球蛋白共受体糖蛋白,其帮助tcr与抗原呈递细胞进行交流(参见campbell&reece,biology 909(benjamin cummings,sixth ed.,2002))。cd4存在于免疫细胞(如t辅助细胞、单核细胞、巨噬细胞和树突状细胞)的表面,并包括在细胞表面表达的四个免疫球蛋白结构域(d1至d4)。在抗原呈递过程中,cd4与tcr复合物一起被募集,以结合到mhcii分子的不同区域(cd4与mhciiβ2结合,而tcr复合物结合mhciiα1/β1)。不希望受到理论的束缚,据信紧紧靠近tcr复合物允许cd4相关激酶分子磷酸化存在于cd3胞质结构域上的免疫受体酪氨酸激活基序(itam)。这种活动被认为会放大由激活的tcr产生的信号,以产生各种类型的t辅助细胞。
[0053]
抗体技术领域的技术人员所理解的术语均被赋予本领域所获得的含义,除非本文中明确定义不同。例如,术语“抗体”是指完整的抗体,其包括通过二硫键相互连接的至少两条重(h)链和两条轻(l)链,以及完整抗体的任何抗原结合部分或片段,其具有或保持与完整抗体识别的抗原靶分子结合的能力,例如scfv、fab或fab'2片段。因此,本文中的术语“抗体”在最广泛的意义上使用,包括多克隆和单克隆抗体,包括完整抗体及其功能(抗原结合)抗体片段,包括片段抗原结合(fab)片段、f(ab')2片段、fab’片段、fv片段、重组igg(rigg)片段、单链抗体片段,包括单链可变片段(scfv)和单域抗体(例如sdab、sdfv、纳米体)片段。该术语包括免疫球蛋白的基因工程和/或其他修饰形式,例如内抗体、肽体、嵌合抗体、全人抗体、人源化抗体和异源偶联抗体、多特异性抗体,例如双特异性抗体、双抗体、三抗体、四抗体、串联双scfv和串联三scfv。除非另有说明,术语“抗体”应理解为包含其功能抗体片
段。该术语还包括完整或全长抗体,包括任何类别或亚类的抗体,包括igg及其亚类(igg1、igg2、igg3、igg4)、igm、ige、iga和igd。
[0054]
术语“v
l”或“vl”和“v
h”或“vh”分别指抗体轻链和抗体重链的可变结合区或结构域。在某些实施例中,vl是kappa(κ)类(此处也称为“vk”)。在某些实施例中,vl是lambda(λ)类。与tcr可变结构域一样,抗体的可变结构域包括cdr和框架区(fr)。每个抗体可变结构域中有三个cdr(hcdr1、hcdr2、hcdr3;lcdr1、lcdr2、lcdr3;也分别称为cdrh和cdrl)。在某些实施例中,抗体vh包含如下四个fr和三个cdr:fr1-hcdr1-fr2-hcdr2-fr3-hcdr3-fr4;并且抗体vl包含如下的四个fr和三个cdr:fr1-lcdr1-fr2-lcd2-fr3-lcdr3-fr4。通常,vh和vl通过各自的cdr一起形成抗原结合位点。
[0055]
tcr模拟抗体是能够与肽:mhc复合物结合(即,识别肽:mhc复合物并与其结合)的抗体(具有任何同种型的抗体,例如igg(1、2、3、4)、ige、igd、iga、igm)。在一些实施例中,tcr模拟抗体具有与t细胞受体相似的抗原特异性、主要组织相容性复合物相容性或限制性。例如,tcr模拟抗体可以通过如kohler et al.,nature256:495(1975)所述的杂交瘤方法制备,或者可以在细菌、真核动物或植物细胞中使用重组dna方法制备(参见,例如美国专利号4,816,567)。tcr模拟抗体也可以使用clackson et al.,nature,352:624-628(1991)和marks et al.,j.mol.biol.,222:581-597(1991)以及noy et al.expert rev.anticancer ther.5(3):523-536(2005)中所述的技术从噬菌体抗体库中分离,这些技术全部并入本文。tcr模拟抗体也可以使用pct申请wo 2004/076677a2中所公开的方法获得。还可以考虑tcr模拟抗体的抗原结合片段(例如cdr、vh、vl、fab、fd等)。
[0056]
改变的结构域或改变的蛋白质或衍生物可以包括基于相同氨基酸的所有可能密码子选择的那些和基于保守氨基酸取代的密码子选择。例如,以下六组每组都包含彼此保守取代的氨基酸:1)丙氨酸(ala;a)、丝氨酸(ser;s)、苏氨酸(thr;t);2)天冬氨酸(asp;d)、谷氨酸(glu;e);3)天冬酰胺(asn;n)、谷氨酰胺(gln;q);4)精氨酸(arg;r)、赖氨酸(lys;k);5)异亮氨酸(ile;i)、亮氨酸(l)、甲硫氨酸(met;m)、缬氨酸(val;v);和6)苯丙氨酸(phe;f)、酪氨酸(tyr;y)、色氨酸(trp;w)。(也参见wo97/09433第10页;lehninger,biochemistry,2nd edition,worth publishers,inc.,ny,ny,pp.71-77,1975;lewin genes iv,oxford university press,ny and cell press,cambridge,ma,p.8,1990;creighton,proteins,w.h.freeman and company 1984)。此外,改变、添加或删除编码序列中的单个氨基酸或一小部分氨基酸的个别取代、缺失或添加也是“保守取代”。
[0057]
如本文所用,“核酸”或“核酸分子”或“多核苷酸”是指脱氧核糖核酸(dna)、核糖核酸(rna)、寡核苷酸、多核苷酸、例如通过聚合酶链反应(pcr)或通过体外翻译产生的其片段中任一个,并且也指由任何连接、断裂、核酸内切酶作用或核酸外切酶作用产生的片段。在某些实施例中,本公开的核酸通过pcr产生。核酸可由单体组成,这些单体是天然存在的核苷酸(如脱氧核糖核苷酸和核糖核苷酸)、天然存在的核苷酸的类似物(例如,天然核苷酸的α-对映体形式)或两者的组合。修饰的核苷酸可以对糖部分或嘧啶或嘌呤碱基部分进行修饰或取代。核酸单体可通过磷酸二酯键或此类键的类似物连接。磷酸二酯键的类似物包括硫代磷酸酯、二硫代磷酸酯、硒代磷酸酯、二硒代磷酸酯、苯胺硫代磷酸酯、苯胺磷酸酯、氨基磷酸酯等。核酸分子可以是单链或双链的。
[0058]
术语“分离”是指材料从其原始环境中移除(例如,自然环境,如果是天然存在)。例
如,活体动物中的天然存在的核酸或多肽不是分离的,但是,从天然系统中的一些或全部共存物质中分离出来的相同核酸或多肽是分离的。这样的核酸可以是载体的一部分和/或这样的核酸或多肽可以是组合物(例如,细胞裂解物)的一部分,并且仍然是分离的,因为这样的载体或组合物不是核酸或多肽的自然环境的一部分。术语“基因”是指涉及产生多肽链的dna片段;它包括编码区之前和之后的区域(“前导和尾部”)以及各个编码片段(外显子)之间的插入序列(内含子)。
[0059]
如本文所用,术语“重组的”、“工程化的”和“修饰的”是指通过引入外源核酸分子而修饰的细胞、微生物、核酸分子、多肽、蛋白质、质粒或载体,或指通过人为干预进行基因工程改造的细胞或微生物,即通过引入异源核酸分子进行修饰,或指已被改变使得内源核酸分子或基因的表达受到控制、解除调节或组成性的细胞或微生物,可以通过基因工程引入此类改变或修饰。人类产生的遗传改变可以包括,例如,引入编码一种或多种蛋白质或酶的核酸分子(可能包括表达控制元素,例如启动子)的修饰,或细胞遗传物质的其他核酸分子添加、缺失、取代或其他功能破坏或添加。示例性修饰包括来自参考或亲本分子的异源或同源多肽的编码区或其功能片段中的那些。
[0060]
如本文所用,“突变”是指分别与参照或野生型核酸分子或多肽分子相比,核酸分子或多肽分子的序列发生变化。突变可导致多种不同类型的序列变化,包括核苷酸或氨基酸的取代、插入或缺失。在某些实施例中,突变是1个或3个密码子或氨基酸的取代、1到约5个密码子或氨基酸的缺失、或其组合。
[0061]
在本领域中,“保守取代”被认为是一种氨基酸被另一种具有相似特性的氨基酸置换。示例性保守取代是本领域众所周知的(参见,例如,wo 97/09433第10页;lehninger,biochemistry,2nd edition;worth publishers,inc.ny,ny,pp.71-77,1975;lewin,genes iv,oxford university press,ny and cell press,cambridge,ma,p.8,1990)。
[0062]
术语“构建体”是指包含重组核酸分子的任何多核苷酸。“转基因”或“转基因构建体”是指包含以自然界中未发现的排列可操作地连接的两个或更多个基因的构建体。术语“可操作地连接”(或本文中的“可操作连接”)是指两个或更多个核酸分子在单个核酸片段上的缔合,使得一个的功能受另一个的影响。例如,当启动子可以影响编码序列的表达时,启动子与编码序列可操作地连接(即,编码序列在启动子的转录控制之下)。“未连接”是指相关的遗传元件彼此之间没有密切联系,一个的功能不影响另一个。在一些实施例中,转基因中存在的基因与表达控制序列(例如,启动子)可操作地连接。
[0063]
构建体(例如,转基因)可以存在于载体(例如,细菌载体、病毒载体)中或可以整合到基因组中。“载体”是能够运输另一种核酸分子的核酸分子。例如,载体可以是可以包括染色体、非染色体、半合成或合成核酸分子的质粒、粘粒、病毒、rna载体或线性或环状dna或rna分子。示例性载体是能够自主复制(附加型载体(episomal vector))或表达与其连接的核酸分子(表达载体)的那些。可用于本公开的组合物和方法的载体在本文中进一步描述。
[0064]
如本文所用,术语“表达”是指基于核酸分子(例如基因)的编码序列产生多肽的过程。该过程可以包括转录、转录后控制、转录后修饰、翻译、翻译后控制、翻译后修饰、或其任何组合。
[0065]
在将核酸分子插入细胞的情况下,术语“引入”是指“转染”或“转化”或“转导”,并且术语包括提及将核酸分子掺入真核或原核细胞,其中核酸分子可以掺入细胞的基因组
(例如,染色体、质粒、质体或线粒体dna),转化为自主复制子,或瞬时表达(例如,转染的mrna)。
[0066]
如本文所用,“异源”或“外源”核酸分子、构建体或序列是指对宿主细胞是非天然的核酸分子或核酸分子的一部分,但可以与来自宿主细胞的核酸分子或核酸分子的一部分同源。异源或外源核酸分子、构建体或序列的来源可以来自不同的属或种。在某些实施例中,通过例如缀合、转化、转染、转导、电穿孔等将异源或外源核酸分子添加(即,非内源性或天然的)到宿主细胞或宿主基因组中,其中添加的分子可以整合到宿主基因组中或可以作为染色体外遗传物质存在(例如,作为质粒或其他形式的自我复制载体),并且可以存在于多个拷贝中。此外,“异源”是指由引入宿主细胞的外源核酸分子编码的非天然酶、蛋白质或其他活性,即使宿主细胞编码同源蛋白质或活性。应当理解,在包含异源多核苷酸的宿主细胞的情况下,该多核苷酸对于宿主细胞的后代是“异源的”,无论后代自身是否被操纵(例如,转导)以包含该多核苷酸。这样的后代可以被称为“修饰的”宿主细胞,无论受试者宿主细胞本身是否被修饰为包含多核苷酸,或者受试者寄主细胞的祖细胞是否被修饰为包含多核苷酸序列。
[0067]
如本文所述,可以将超过一个异源或外源核酸分子作为单独的核酸分子、作为多个单独控制的基因、作为多顺反子核酸分子、作为编码融合蛋白的单个核酸分子、或其任何组合引入宿主细胞。当两个或多个外源核酸分子被引入宿主细胞时,应理解,两个或多个外源核酸分子可以作为单个核酸分子(例如,在单个载体上)在单独的载体上引入、在单个位点或多个位点整合到宿主染色体中、或其任何组合。提及的异源核酸分子或蛋白质活性的数量是指编码核酸分子的数量或蛋白质活性的数量,而不是被引入宿主细胞的单独的核酸分子的数量。
[0068]
如本文所用,术语“内源的”或“天然的”是指通常存在于宿主细胞中的基因、蛋白质或活性。而且,与亲代基因、蛋白质或活性相比,发生突变、过表达、改组(shuffled)、复制或以其他方式改变的基因、蛋白质或活性仍被认为对该特定宿主细胞是内源性的或天然的。例如,来自第一基因(例如,启动子、翻译衰减序列)的内源性控制序列可用于改变或调节第二天然基因或核酸分子的表达,其中第二天然基因或核酸分子的表达或调控不同于亲代细胞中的正常表达或调控。
[0069]
术语“同源”或“同源物”是指在宿主细胞、物种或菌株中发现的或衍生自宿主细胞、物种或菌株的分子或活性。例如,异源或外源核酸分子可以与天然宿主细胞基因同源,并且可以任选地具有改变的表达水平、不同的序列、改变的活性、或其任何组合。
[0070]
如本文所用,“序列同一性”是指在比对序列并引入缺口(如有必要)以实现最大百分比的序列同一性后,一个序列中的氨基酸残基与另一参考多肽序列中的氨基酸残基相同的百分比,并且不考虑任何保守取代作为序列同一性的一部分。可以使用altschul et al.(1997),nucl.acids res.25:3389-3402中所定义的ncbi blast 2.0软件生成百分比序列同一性值,其中参数设置为默认值。
[0071]
免疫原性组合物
[0072]
在某些方面,本公开提供了包含或由本文所公开的一种或多种sox2肽抗原组成的免疫原性组合物。在某些实施例中,免疫原性组合物包含分离的肽或多肽,所述肽或多肽包含或由seq id nos:2-7中任一项中所述的氨基酸序列组成。目前公开的免疫原性组合物能
够引发针对以sox2表达(在某些实施例中包括过表达)和/或活性为特征或以其他方式与之相关的疾病或病症(如多发性骨髓瘤)的免疫应答(例如,抗原特异性t细胞、抗体、细胞因子等的产生)。在某些实施例中,组合物包含seq id nos:2-7中所述的氨基酸序列中的任何1个、2个、3个、4个、5个或6个;例如,在融合多肽和/或分离的多肽中,每个多肽独立地为长度不超过约250、不超过约200、不超过约150、不超过约100、不超过约50、不超过约25、不超过约20或不超过约15个氨基酸。示例性免疫原性融合多肽可以以任何顺序包括seq id nos:2-7中所述的氨基酸序列中的两个或多个,并且可以包括两个或多个拷贝的seq id nos:2-7中所述的氨基酸序列中的任何一个或多个。在一些实施例中,将自切割肽(例如p2a、t2a、e2a、f2a)置于融合物的两个sox2肽之间。在某些实施例中,免疫原性组合物进一步包含药学上可接受的佐剂(adjuvant)。佐剂旨在提高(或改善、增强)对免疫原性肽和包含该肽的融合多肽的免疫应答(即,与不施用佐剂时的特异性免疫应答水平相比,以统计学、生物学或临床上显著的方式增加对免疫原性肽或融合多肽的特异性免疫应答水平)。
[0073]
对于人类给药,药学上可接受的佐剂是指已被相关监管机构批准或可批准用于人类给药的佐剂。所需佐剂增强对免疫原性肽或融合多肽的应答,而不会引起可能对定性免疫应答产生不利影响的免疫原的构象变化。合适的佐剂包括铝盐,如明矾(硫酸铝钾),或其他含铝佐剂,如氢氧化铝、磷酸铝或硫酸铝。其他药学上合适的佐剂包括无毒的脂质a相关佐剂,例如,通过非限制性示例,无毒的单磷酸脂质a(参见,例如,persing et al.,trends microbiol.25 10:s32-s37(2002)),例如,3-脱-o-酰化单磷酰脂a(mpl)(参见,例如,英国专利申请号gb 2220211)。其他有用的佐剂包括qs21和quila,其包含从南美洲发现的皂树(quillaja saponaria molina)的树皮中分离的三萜糖苷或皂苷(参见,例如,kensil et al.,in vaccine design:the subunit and adjuvant approach(eds.powell and 30newman,plenum press,ny,1995);美国专利号5,057,540)。其他合适的佐剂包括水包油乳剂,其任选地与免疫刺激物如单磷酰脂质a组合(参见,例如,stoute et al.,n.engl.j.med.336,86-91(1997))。其他合适的佐剂包括聚合物或单体氨基酸,如聚谷氨酸或聚赖氨酸、脂质体和cpg(参见,例如klinman,35int.rev.immunol.25(3-4):135-54(2006);美国专利号7,402,572;欧洲专利号772 619)。还提供了包含异源多核苷酸的宿主细胞,其编码本文所提供的免疫原性sox2肽或融合多肽。在某些实施例中,宿主细胞包括免疫细胞,例如人类免疫细胞。在某些实施例中,宿主细胞包括树突状细胞或t细胞。在某些实施例中,将免疫原性组合物或宿主细胞施用于hla-a:02*01
+
的受试者。
[0074]
在一些实施例中,免疫原性组合物包含:(i)包含或由seq id no:2的氨基酸序列组成的分离的肽或多肽;(ii)包含或由seq id no:3的氨基酸序列组成的分离的肽或多肽;(iii)包含或由seq id no:4的氨基酸序列组成的分离的肽或多肽;(iv)包含或由seq id no:5的氨基酸序列组成的分离的肽或多肽;(v)包含或由seq id no:6的氨基酸序列组成的分离的肽或多肽;(vi)包含或由seq id no:7的氨基酸序列组成的分离的肽或多肽;和/或(vii)与seq id no:2、3、4、5、6或7相比具有1个、2个或3个氨基酸差异的(i)至(vi)中任一项的分离的肽或多肽的变体,其中(i)至(vii)中任一项的分离的肽或多肽不包含分离的全长人sox2。在某些实施例中,(a)(i)至(vii)中任一项的一个或多个拷贝和/或(b)(
ⅰ
)至(vii)中任一项的一种或多种存在于融合多肽中,其中所述融合多肽任选地进一步包含自切割肽的氨基酸序列。
[0075]
在某些实施例中,免疫原性组合物能够在受试者中引发针对癌症细胞的免疫应答,其中,任选地,该癌症细胞包括多发性骨髓瘤细胞、胶质瘤细胞、颈癌细胞、肺癌细胞、浆细胞白血病细胞和/或卵巢癌细胞。
[0076]
在某些实施例中,所述免疫原性组合物进一步包含佐剂。
[0077]
还提供了分离的多核苷酸,其编码:(i)包含或由seq id no:2的氨基酸序列组成的肽或多肽;(ii)包含或由seq id no:3的氨基酸序列组成的肽或多肽;(iii)包含或由seq id no:4的氨基酸序列组成的肽或多肽;(iv)包含或由seq id no:5的氨基酸序列组成的肽或多肽;(v)包含或由seq id no:6的氨基酸序列组成的肽或多肽;(vi)包含或由seq id no:7的氨基酸序列组成的肽或多肽;和/或(vii)与seq id no:2、3、4、5、6或7相比具有1个、2个或3个氨基酸差异的(i)至(vii)中任一项的肽或多肽的变体,其中所述多核苷酸任选地包含在载体中和/或(i)至(vii)中任一项的肽或多肽不包含全长人sox2。在某些实施例中,所述多核苷酸经过密码子优化用于在宿主细胞中表达,其中所述宿主细胞任选地是树突状细胞或t细胞。还提供了包含多核苷酸的宿主细胞,其中多核苷酸与宿主细胞异源,并且其中宿主细胞任选地是免疫细胞,并且进一步任选地是专职性抗原呈递细胞。在一些实施例中,宿主细胞是树突状细胞或t细胞。
[0078]
还提供了一种在受试者中引发针对与sox2表达或活性相关的疾病或病症的免疫应答的方法,该方法包括向受试者施用本公开的结合蛋白、编码结合蛋白的多核苷酸、载体、编码/表达结合蛋白的宿主细胞、组合物、免疫原性组合物、编码肽的多核苷酸和/或编码肽的宿主细胞。
[0079]
还提供了一种扩增t细胞群的方法,所述t细胞群与选自以下各项的肽(例如,包含在肽:hla复合物中的肽)结合:(i)包含或由seq id no:2的氨基酸序列组成的肽;(ii)包含或由seq id no:3的氨基酸序列组成的肽;(iii)包含或由seq id no:4的氨基酸序列组成的肽;(iv)包含或由seq id no:5的氨基酸序列组成的肽;(v)包含或由seq id no:6的氨基酸序列组成的肽;和/或(vi)包含或由seq id no:7的氨基酸序列组成的肽,所述方法包括将包含与所述肽结合的一个或多个t细胞的样品与免疫原性组合物、编码肽的多核苷酸、编码肽的宿主细胞和/或抗原呈递细胞接触,所述抗原呈递细胞已与包含或由seq id nos:2-7中任一项所述的氨基酸序列组成的肽或多肽接触。
[0080]
还提供了一种产生和/或分离t细胞的方法,该方法包括将包含t细胞的样品(其中所述样品任选包含外周血细胞)与公开的免疫原性组合物、编码肽的多核苷酸、编码肽的宿主细胞和/或抗原呈递细胞(apc)接触,所述抗原呈递细胞表达或已与sox2抗原接触,所述sox2抗原包含或由seq id nos:2-7中任一项所述的氨基酸序列组成,并且任选地从样品中的其他细胞分选t细胞,从而分离和/或产生t细胞。还提供了通过该方法分离和/或产生的t细胞。
[0081]
结合蛋白与宿主细胞
[0082]
在某些方面,本公开提供了能够与sox2抗原结合(例如,特异性结合)的结合蛋白,例如在肽:hla复合物的情况下。在一些实施例中,hla包含hla-a*02:01和/或sox2抗原包含或由seq id nos:2-7中任一项所述的氨基酸序列组成。还提供了编码结合蛋白的多核苷酸,以及包含这种多核苷酸并能够表达所编码的结合蛋白的宿主细胞。
[0083]
如本文所用,术语“sox2特异性结合蛋白”是指能够结合(例如在细胞表面上的)
sox2肽抗原:hlahla复合物的蛋白质或多肽(例如,如tcr或抗原结合结构域或其片段,或car的抗原结合结构域,或tcr模拟抗体或抗原结合结构域或其片段)。在一些实施例中,sox2特异性结合蛋白不结合不包含sox2肽抗原的蛋白质或多肽和/或不结合包含这样的肽的hla复合物。编码和/或表达本公开的sox2特异性结合蛋白(即,异源或其他)的宿主细胞(例如,如免疫细胞)在某些情况下被称为“sox2特异”细胞。
[0084]
本公开的结合蛋白,例如tcr、sctv、sctcr、car和tcr模拟抗体及其抗原结合片段,将包含能够与sox2抗原结合的结合结构域,例如在sox2抗原:hla复合物中。如本文所用,“结合结构域”(也称为“结合区”或“结合部分”)是指具有与靶标特异性且非共价缔合、结合或组合的能力(例如抗原肽或肽:mhc复合物)的分子或其部分(例如肽、寡肽、多肽、蛋白质)。结合结构域包括生物分子、分子复合物(即包含两个或多个生物分子的复合物)或其他感兴趣靶标的任何天然存在的、合成的、半合成的或重组产生的结合伴侣(binding partner)。某些结合结构域包括免疫球蛋白可变区或包含其的单链构建体(例如,单链tcr(sctcr)、sctv、scfv)。
[0085]
在某些实施例中,结合蛋白包含来自免疫球蛋白超家族结合蛋白的一个或多个可变结构域。在一些实施例中,结合蛋白包含t细胞受体(tcr)α链可变结构域(vα)和/或tcrβ链可变结构域(vβ)。在一些实施例中,结合蛋白包含来自tcr模拟抗体的一个或多个可变结构域(参见,例如,kurosawa et al.,sci reports 9:9827(2019);trenevska et al.front.immunol.(2017)doi.org/10.3389/fimmu.2017.01001;dahan&reiter,expert rec.mol.med.14e6(2012)doi.org/10.1017/erm.2012.2;chang et al.exper opin biol ther 16:979-987(2016)doi.org/10.1080/14712598.2016.1176138);noy et al.,expert rev.anticancer ther.5(3):523-236(2005))。
[0086]
在一些实施例中,结合蛋白包括t细胞受体(tcr)α-多肽可变结构域(vα)和tcrβ-多肽可变结构域(vβ),其中所述结合蛋白能够与含有sox2抗原:hla复合物的肽结合,其中sox2抗原包含或由seq id nos:2-7中任一项所述的氨基酸序列组成。
[0087]
在本文公开的任何实施例中,hla包括hla-a*02:01。
[0088]
在一些实施例中,与sox2肽抗原:hla复合物的结合包括特异性结合。如本文所用,在结合相互作用的情况下,“特异性结合”或“特异于”是指结合蛋白(如tcr受体、sctv、sctcr、car、tcr模拟抗体)或结合结构域(或其融合蛋白)与靶分子的缔合或结合,其亲和力或ka(即特定结合相互作用的平衡缔合常数,单位为1/m)等于或大于105m-1
(这等于该缔合反应的缔合速率[k
on
]与解离速率[k
off
]的比率),而不与样品中的任何其他分子或组分显著缔合或结合。结合蛋白或结合结构域(或其融合蛋白)可分类为“高亲和力”结合蛋白或其结合结构域(或其融合蛋白),或分类为“低亲和力”结合蛋白或结合结构结构域(或其融合蛋白)。“高亲和力”结合蛋白或结合结构域是指ka为至少107m-1
、至少108m-1
、至少109m-1
、至少10
10
m-1
、至少10
11
m-1
、至少10
12
m-1
或至少10
13
m-1
的那些结合蛋白或结合结构域。“低亲和力”结合蛋白或结合结构域是指ka高达107m-1
、高达106m-1
、高达105m-1
的那些结合蛋白或结合结构域。或者,亲和力可以定义为以m为单位(例如,10-5
m至10-13
m)的特定结合相互作用的平衡解离常数(kd)。
[0089]
在某些实施例中,本公开的结合蛋白与含有sox2的肽(或sox2肽:hla复合物)结合,其kd为小于约10-8
m、小于约10-9
m、小于约10-10
m、小于约10-11
m、小于约10-12
m或小于约10-13
m,或具有与本文提供的示例性结合蛋白(例如本文提供的任何示例性sox2特异性tcr)所显示的亲和力大致相同、至少大致相同、或大于或大约为所显示的亲和力,例如,通过相同的试验来测量。在某些实施例中,sox2结合蛋白包括sox2特异性免疫球蛋白超家族结合蛋白或其结合部分。
[0090]
在某些实施例中,受体或结合结构域可以具有“增强的亲和力”,其指的是与野生型(或亲代)结合结构域相比,对靶抗原具有更强结合的选定或工程化受体或结合结构域。例如,增强的亲和力可能是由于靶抗原的ka(缔合常数)高于野生型结合结构域的ka,由于靶抗原的kd(解离常数)低于野生型结合域的kd,由于靶抗原的解离速率(k
off
)低于野生型结合结构域的k
off
,或其组合。
[0091]
已知多种试验用于鉴定本公开的特异性结合特定靶标的结合结构域,以及确定结合结构域或结合蛋白亲和力,例如多聚体/四聚体染色(例如肽:mhc四聚体)、蛋白质印迹、elisa、分析超速离心、光谱和表面等离子共振分析(参见,例如,dolton et al.,immunology 146:11-22,2015;scatchard et al.,ann.ny acad.sci.51:660,1949;wilson,science 20295:2103,2002;wolff et al.,cancer res.53:2560,1993;和美国专利号5,283,173、5,468,614,或等效物;均通过引用并入本文)。结合结构域也可以通过筛选例如t细胞、b细胞、浆细胞、pbmc或杂交瘤对本文提供的sox2肽抗原或sox2肽抗原:hla复合物的反应性/结合来鉴定。例如,这些细胞或它们的上清液可以暴露于表达感兴趣抗原或已经用感兴趣抗原脉冲的抗原呈递细胞。结合蛋白也可以通过将感兴趣抗原引入抗原外源的合适宿主,如小鼠、兔子、骆驼、非人灵长类动物或鲨鱼,然后从宿主中分离t细胞、nk-t细胞、nk细胞、b细胞、脾细胞、浆细胞等,并确定分离的细胞是否表达抗原特异性的结合蛋白来产生。
[0092]
在某些实施例中,本公开的结合蛋白或融合蛋白(例如,tcr、sctcr、car、sctv、tcr模拟抗体或抗原结合片段)由宿主细胞(例如,由异源表达结合蛋白的t细胞、nk细胞或nk-t细胞)表达,优选在结合蛋白能够在细胞表面起受体作用时在细胞表面表达。这种宿主细胞对sox2肽抗原或sox2肽-抗原:hla复合物的亲和力可以通过例如将宿主细胞暴露于肽,或暴露于肽:hla复合物(例如,组织为四聚体),或暴露于抗原呈递细胞(apc)来确定,所述抗原呈递细胞将肽呈递给宿主细胞,任选地以肽:hla复合物的形式,然后测量宿主细胞的活性,例如,如细胞因子(例如ifn-γ;tnfα)的产生或分泌;宿主细胞信号传导或激活成分(例如cd137(4-1bb))的表达增加;宿主细胞的增殖;或杀伤apc(例如使用标记的铬释放试验或caspase-3/7试验)。tcr模拟抗体的活性可以使用标准抗体试验(例如,如elisa、bli、spr)、效应器功能试验(例如使用靶细胞和免疫效应器细胞)(例如表达fcγr驱动细胞激活报告元件的表达)等来评估。
[0093]
术语“功能亲合力”是指体外免疫细胞(如t细胞、nk细胞、nk-t细胞)对给定浓度的配体(如抗原)的应答的生物学测量或激活阈值,其中生物学测量可以包括细胞因子产生(如ifnγ产生、il-2产生等)、细胞毒性活性、激活和增殖。例如,通过产生细胞因子、具有细胞毒性、表达激活标记或增殖而在体外对低抗原剂量产生生物学(免疫)应答的t细胞被认为具有高功能亲合力,而具有较低功能亲合力的t细胞在引发类似于高亲合力t细胞所获得的免疫应答前需要更高量的抗原。应当理解,功能亲合力不同于亲和力(affinity)和亲合力(avidity)。亲和力是指结合蛋白与其抗原/配体之间任何给定键的强度。一些结合蛋白
是多价的,可以与多种抗原结合——在这种情况下,整体连接的强度是亲合力。
[0094]
功能亲合力和免疫应答的有效性之间存在许多相关性。一些体外研究表明,不同的t细胞功能(例如增殖、细胞因子产生(例如使用如elisa、luminex(例如luminex)等所测量或检测的)可以在不同的阈值下触发(参见,例如betts et al.,j.immunol.172:6407,2004;langenkamp et al.,eur.j.immunol.32:2046,2002)。可以影响功能亲合力的因素包括(a)tcr对pmhc复合物的亲和力,即tcr和pmhc之间相互作用的强度(cawthon et al.,j.immunol.167:2577,2001),(b)tcr和cd4或cd8共受体的表达水平,以及(c)信号分子的分布和组成(viola and lanzavecchia,science 273:104,1996),以及减弱t细胞功能和tcr信号传导的分子的表达水平。
[0095]
在指定的暴露时间后,在基线和最大反应之间诱导半最大反应所需的抗原浓度被称为“半最大有效浓度”或“ec
50”。ec
50
值通常表示为摩尔(摩尔/升)量,但通常会转换为对数值,如下所示——log10(ec
50
)。例如,如果ec
50
等于1μm(10-6
m),则log
10
(ec
50
)值为-6。使用的另一个值是pec
50
,它被定义为ec
50
的负对数(-log
10
(ec
50
))。例如,见图12。在上述示例中,等于1μm的ec
50
的pec
50
值为6。在某些实施例中,本公开的结合蛋白的功能亲合力是其促进免疫细胞(例如,t细胞、nk-t细胞、nk细胞)产生ifnγ的能力的测量,其可以使用本领域已知和/或本文所述的试验来测量。“高功能亲合力”tcr或其结合结构域是指具有至少10-4
m、至少约10-5
m或至少约10-6
m的ec
50
的那些tcr或其结合结构域。
[0096]
还考虑了融合蛋白,其包含与抗体(例如igg(1、2、3、4)、ige、igd、iga、igm、及其变体)的恒定结构域或其片段(例如,在一些实施例中,保留与一种或多种fc受体、c1q、蛋白a、蛋白g、或其任何组合结合的片段)连接的根据本公开的tcr或sctcr或sctv可变结构域,并且包括免疫球蛋白重链单体和多聚体,例如fc二聚体;参见,例如,wong et al.,j.immunol.198:1supp.(2017)。包含增强、减少或消除与例如fcrn或其他fc受体结合或通过其结合的突变的变体fc多肽是已知的,并且在本公开中被考虑。
[0097]“改变的结构域”或“改变的蛋白质”是指与野生型基序、区、结构域、肽、多肽或蛋白质(例如,野生型tcrα多肽、tcrβ多肽、tcrα恒定结构域、tcrβ恒定结构域)具有至少85%(例如,86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%、99.1%、99.2%、99.3%、99.4%、99.5%、99.6%、99.7%、99.8%、99.9%)的不同序列同一性的基序、区、结构域、或肽、多肽或蛋白质。
[0098]
在某些实施例中,与参考序列或野生型序列相比,根据本公开的结合蛋白包含变体序列(例如,与本文所述的t细胞的tcr的亲代或野生型tcr cdr3β相比的变体tcr cdr3β)。如本文所用,“变体”氨基酸序列、肽或多肽是指与参考或野生型氨基酸序列相比具有一个或两个氨基酸取代、缺失或插入的氨基酸序列(或肽或多肽)。在某些实施例中,变体氨基酸序列、肽或多肽保留与参考或野生型分子基本相同的功能(例如,对肽:hla复合物的结合特异性和亲和力);例如,与亲代或野生型tcr cdr3β相比,本文公开的变体tcr cdr3β保留了约50%、约60%、约70%、约80%、约90%、约95%、约99%或100%的抗原结合特异性或亲和力。
[0099]
在某些情况下,tcr可变结构域框架区的工程化已被证明可以改善蛋白质表达,而不会降低或实质性降低结合功能(thomas et al.,nature communications 10:4451(2019);doi.org/10.1038/s41467-019-12441-w;其中框架突变通过引用并入本文)。这种
突变可以任选地与tcr恒定区中的半胱氨酸突变(例如t48c(cα)和s79c或s57c(cβ))组合使用,以潜在地改善表达和功能。
[0100]
与工程tcr的“优势”(相对于内源性tcr)表达相关的氨基酸包括:
[0101]
·
vα:
[0102]
o在框架区1中,在imgt位置5处的t、imgt位置8处的q、imgt位置19处的v、imgt位置20处的t和/或在imgt位置24处的t;
[0103]
o在框架区2中,在imgt位置39处的l、imgt位置50处的m和/或imgt位置55处的r;和
[0104]
o在框架区3中,在imgt位置66处的a、imgt位置86处的s,以及imgt位置96处的l。
[0105]
·
vβ:
[0106]
o在框架区1中,在imgt位置9处的的r和/或imgt位置10处的y;和
[0107]
o在框架区2中,在imgt位置43处的q。
[0108]
因此,将上述氨基酸中的一种或多种引入所指示位置的tcr v区(如果尚未存在于天然氨基酸序列中)可以产生具有潜在改善的表达和任选功能的变体。
[0109]
在一些实施例中,提供了能够与sox2肽:hla复合物结合的分离的结合蛋白,其中sox2肽包含或由seq id no.:5、2、3、4、6或7中所述的氨基酸序列组成,并且其中,任选地,所述结合包括特异性结合。在某些实施例中,hla包括hla-a*02:01。
[0110]
在一些实施例中,结合蛋白包括免疫球蛋白超家族可变结构域。在一些实施例中,结合蛋白包含tcrα链可变结构域(vα)和/或tcrβ链可变结构域(vβ)。在一些实施例中,结合蛋白包含tcr模拟抗体的重链可变结构域(vh)和/或轻链可变结构域(vl)。
[0111]
在某些变体中,结合蛋白包含:(i)seq id nos.:52、53、100、101、16、17、28、29、40、41、64、65、76、77、88、89、112、113、124、125、136、137、148和149中任一项中所述的氨基酸序列,或其包含一个、两个或三个氨基酸取代的变体,其中所述氨基酸序列任选为cdr3β;(ii)seq id nos.:51、99、15、27、39、63、75、87、111、123、135和147中任一项所述的氨基酸序列,或其包含一个、两个或三个氨基酸取代的变体,其中所述氨基酸序列任选为cdr2β;(iii)seq id nos.:50、98、14、26、38、62、74、86、110、122、134和146中任一项所述的氨基酸序列,或其包含一个、两个或三个氨基酸取代的变体,其中所述氨基酸序列任选为cdr1β;(iv)seq id nos.:57、58、105、106、21、22、33、34、45、46、69、70、81、82、93、94、117、118、129、130、141、142、153和154中任一项所述的氨基酸序列,或其包含一个、两个或三个氨基酸取代的变体,其中所述氨基酸序列任选为cdr3α;(v)seq id nos.:56、104、20、32、44、68、80、92、116、128、140和152中任一项中所述的氨基酸序列,或其包含一个、两个或三个氨基酸取代的变体,其中所述氨基酸序列任选为cdr2α;和/或(vi)seq id nos.:55、103、19、31、43、67、79、91、115、127、139和151中任一项所述的氨基酸序列,或其包含一个、两个或三个氨基酸取代的变体,其中所述氨基酸序列任选为cdr1α。
[0112]
在一些实施例中,结合蛋白包含(1)包含cdr1α、cdr2α和cdr3α的tcr vα;和(2)包含cdr1β、cdr2β和cdr3β的tcr vβ,其中所述cdr1α、cdr2α、cdr3α、cdr1β、cdr2β和cdr3β为如下各项序列所述:(i)分别为seq id nos.:55、56、57或58、50、51、和52或53;(ii)分别为seq id nos.:103、104、105或106、98、99、和100或101;(iii)分别为seq id nos.:19、20、21或22、14、15、和16或17;(iv)分别为seq id nos.:31、32、33或34、26、27、和28或29;(v)分别为seq id nos.:43、44、45或46、38、39、和40或41;(vi)分别为seq id nos.:67、68、69或70、
62、63、和64或65;(vii)分别为seq id nos.:79、80、81或82、74、75、和76或77;(viii)分别为seq id nos.:91、92、93或94、86、87、和88或89;(ix)分别为seq id nos.:115、116、117或118、110、111、和112或113;(x)分别为seq id nos.:127、128、129或130、122、123、和124或125;(xi)分别为seq id nos.:分别为139、140、141或142、134、135、和136或137;或(xii)分别为seq id nos.:151、152、153或154、146、147、和148或149。
[0113]
在一些实施例中,vα包含或由与seq id nos.:54、102、18、30、42、66、78、90、114、126、138和150中任一项所述的氨基酸序列具有至少80%、至少85%、至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%或至少99%同一性的氨基酸序列组成。在一些实施例中,vβ包含或由与seq id nos.:49、97、13、25、37、61、73、85、109、121、133和145中任一项所述的氨基酸序列具有至少80%、至少85%、至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%或至少99%同一性的氨基酸序列组成。
[0114]
在某些实施例中,结合蛋白包含vα和vβ,所述vα和vβ包含或由与下述氨基酸序列具有至少80%、至少85%、至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%或至少99%同一性的氨基酸序列组成:(i)分别为seq id nos.:54和49;(ii)分别为seq id nos.:102和97;(iii)分别为seq id nos.:18和13;(iv)分别为seq id nos.:30和25;(v)分别为seq id nos.:42和37;(vi)分别为seq id nos.:66和61;(vii)分别为seq id nos.:78和73;(viii)分别为seq id nos.:90和85;(ix)分别为seq id nos.:114和109;(x)分别为seq id nos.:126和121;(xi)分别为seq id nos.:138和133;或(xii)分别为seq id nos.:150和145。
[0115]
在一些实施例中,提供了包含vα和vβ的结合蛋白,所述vα和vβ包含或由根据以下各项的氨基酸序列组成:(i)分别为seq id nos.:54和49;(ii)分别为seq id nos.:102和97;(iii)分别为seq id nos.:18和13;(iv)分别为seq id nos.:30和25;(v)分别为seq id nos.:42和37;(vi)分别为seq id nos.:66和61;(vii)分别为seq id nos.:78和73;(viii)分别为seq id nos.:90和85;(ix)分别为seq id nos.:114和109;(x)分别为seq id nos.:126和121;(xi)分别为seq id nos.:138和133;或(xii)分别为seq id nos.:150和145。
[0116]
在一些实施例中,结合蛋白包含在以下各项中:与seq id nos.:48、96、12、24、36、60、72、84、108、120、132和144中任一项所述的氨基酸序列具有至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%或至少99%同一性的氨基酸序列、或包含或由seq id nos.:48、96、12、24、36、60、72、84、108、120、132和144中任一项所述的氨基酸序列组成的氨基酸序列。
[0117]
在某些实施例中,结合蛋白包含tcr vα结构域和tcr vβ结构域,其包括:(i)根据t细胞的tcr的cdr3β,所述t细胞来自:供体1系1、供体1系3、供体2系8、供体2系1、供体2系13、供体2系11或供体2系19;(ii)根据t细胞的tcr的cdr3α,所述t细胞来自:供体1系1、供体1系3、供体2系8、供体2系1、供体2系13、供体2系11或供体2系19;(iii)与t细胞的tcr的vα结构域具有至少90%(90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更多)的氨基酸同一性的vα结构域,所述t细胞来自:供体1系1、供体1系3、供体2系8、供体2系1、供体2系13、供体2系11或供体2系19;或(iv)与t细胞的tcr的vβ结构域具有至少90%(90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更多)的氨基酸同一性的vβ结构域,所述t
细胞来自:供体1系1、供体1系3、供体2系8、供体2系1、供体2系13、供体2系11或供体2系19,条件是(a)至少三个或四个cdr没有突变;(b)具有突变的cdr仅具有至多两个氨基酸取代、至多连续的五个氨基酸缺失、或其组合;和(c)编码的结合蛋白保留其与包含sox2:hla复合物的肽(例如,与hla-a*02:01分子复合的根据seq id no:2、3、4、5、6或7的sox2肽)结合的能力。
[0118]
在进一步的实施例中,所述结合蛋白进一步包括根据t细胞的tcr的cdr1β、cdr2β、cdr1α和/或cdr2α,所述t细胞来自供体1系1、供体1系3、供体2系8、供体2系1、供体2系13、供体2系11或供体2系19。
[0119]
本公开的sox2特异性t细胞系的tcr和t细胞克隆是可识别的,并且具有使用已知方法可确定的序列。例如,参见bleakley et al.,blood 115:4923-4933,2010;warren et al.,blood 91(6):2197-2207(1998);walter et al.,n.engl.j.med.333(16):1038-1044;pct申请no.wo 2018/058002(示例1),该方法和相关试剂通过引用并入本文。例如,可以使用5
′
第一链互补dna(cdna)扩增和使用smarter race cdna扩增试剂盒(clontech laboratories)的cdna末端聚合酶链式反应(race-pcr)的快速扩增来鉴定完整的tcr区域。简言之,cdna是使用5
′
cds引物a、smarter iia寡聚物和smartscribe逆转录酶由rna合成的。然后使用cdna进行race-pcr反应,该反应使用phusion高保真dna聚合酶和tcrα(htcr_calpha-r 5
′‑
cagccgcagcgtcatgagcagatta-3
′
(seq id no:8))或tcrβ链(htcr_cb1-r 5
′‑
ccacttccagggctgccttcagaaatc-3
′
(seq id no:9)和htcr_cb2-r 5
′‑
tgggatggttttggagctagcctctgg-3
′
(seq id no:10))的基因特异性引物。对race-pcr产物进行纯化和测序,以鉴定tcrα和β多肽。可以使用imgt/v-quest软件定义tcr变量、多样性和连接区域。
[0120]
可以通过将编码每个sox2/hla-a*02:01-特异性t细胞克隆中的优势多肽的tra和trb序列配对来构建tcr。tra和trb序列通过pcr确认,使用来自适当v区的5’末端的正向引物和来自tra或trb恒定区的反向引物,然后进行sanger测序。
[0121]
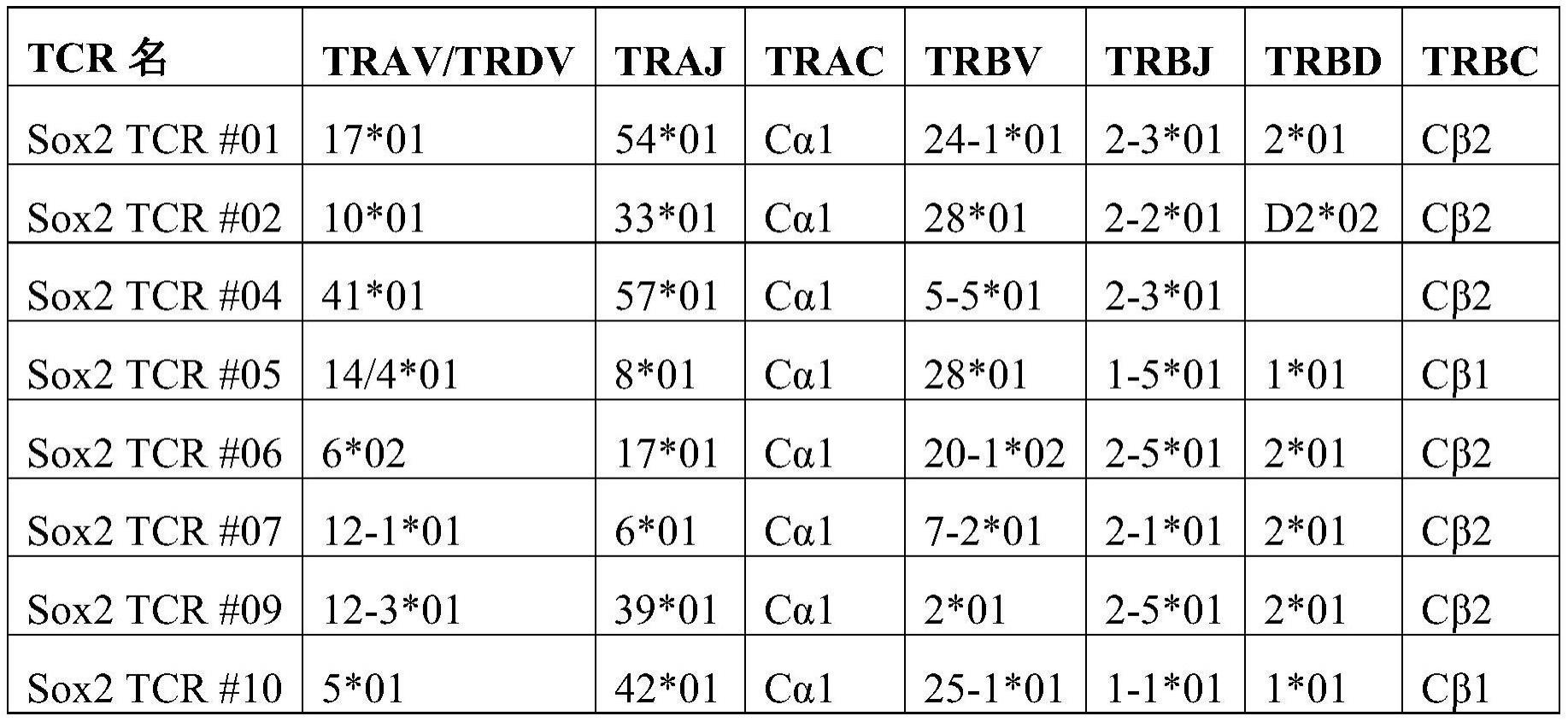
在本文公开的任何实施例中,结合蛋白包含tcr、单链tcr(sctcr)、sctcr、sctv、嵌合抗原受体(car)、或其任何组合。本公开的tcr的示例包括tcr1、tcr2、tcr1、tcp2、tcr4、tcr5、tcr6、tcr7、tcr9、tcr10、tcr11、tcr13、tcr15,和tcr16(或者分别称为sox2 tcr#01、sox2 tcr#02、sox2 tcr#04、sox2tcr#05、sox2 tcr#06、sox2 tcr#07、sox2 tcr#09、sox2 tcr#10、sox2tcr#11、sox2 tcr#13、sox2 tcr#15和sox2 tcr#16)。本文提供了这些tcr的氨基酸序列。
[0122]
生产工程化tcr的方法在例如bowerman et al.,mol.immunol.,46(15):3000(2009)中进行了描述,其技术通过引用并入本文。制造car的方法是已知的,并且例如在美国专利号6,410,319;美国专利号7,446,191;美国专利公开号2010/065818;美国专利号8,822,647;pct公开号wo 2014/031687;美国专利号7,514,537;和brentjens et al.,2007,clin.cancer res.13:5426中进行了描述,其技术通过引用并入本文中。
[0123]
在某些实施例中,单独的sox2特异性结合结构域(即,没有结合蛋白的任何其他部分)可以是可溶性的,并且可以与kd小于约10-8
m、小于约10-9
m、小于约10-10
m、小于约10-11
m、小于约10-12
m或小于约10-13
m的抗原或抗原:hla复合物结合。在特定实施例中,sox2特异性结合结构域包括抗原特异性sctcr(例如单链αβtcr蛋白,如vα-l-vβ、vβ-l-vα、vα-cα-l-vα
或vα-l-vβ-cβ,其中vα和vβ分别是tcrα和β的可变结构域,cα和cβ分别是tcrα和β的恒定结构域,以及l是接头)。
[0124]
在某些实施例中,结合蛋白进一步包含tcrβ多肽恒定结构域(cβ)、tcrα多肽恒定结构区(cα)、或两者。vβ和cβ一起包含tcrβ多肽或链。vα和cα一起包含tcrα多肽或链。在一些实施例中,cβ包含或由以下各项组成:与seq id no.:156或157中所述的氨基酸序列具有至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%或至少99%同一性的氨基酸序列、或包含或由seq id no.:156或157中所述的氨基酸序列组成的氨基酸序列,和/或cα包含或由以下各项组成:与seq id no.:155中所述氨基酸序列具有至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%或至少99%同一性的氨基酸序列、或包含或由seq id no.:155中所述氨基酸序列组成的氨基酸序列。
[0125]
在某些实施例中,cβ和/或cα包含一个或多个非天然氨基酸,其位置使得当cβ和cα缔合形成二聚体时,在cβ和cα之间形成非天然二硫键,其中,任选地,非天然氨基酸包含cβ中的半胱氨酸和/或cα中的半胱氨酸。在一些实施例中,结合蛋白包含tcr cβ和tcr cα,其中tcr cβ包含在氨基酸位置57处取代天然丝氨酸的半胱氨酸氨基酸(例如,gv(s
→
c)td),并且tcr cα包含在氨基酸位置48处取代天然苏氨酸的半胱氨酸氨基酸(例如,gv(s
→
c)vl;参见,例如cohen et al.,cancer res.67(8):3898-3903(2007))。
[0126]
在某些实施例中,结合蛋白包括两种组分,例如α多肽和β多肽,它们可以在细胞表面缔合以形成功能性结合蛋白。这两种缔合的组分可以包括成熟的蛋白质。在某些实施例中,tcr的抗原结合片段包含单链tcr(sctcr),其包含tcr vα和tcr vβ结构域,但仅包含单个tcr恒定结构域(cα或cβ)。
[0127]
在进一步的实施例中,tcr或嵌合抗原受体的抗原结合片段是嵌合的(例如,包含来自超过一个供体或物种的氨基酸残基或基序)、人源化的(例如,包含来自被改变或被取代以降低人类免疫原性风险的非人生物体的残基)、或人类的。
[0128]
本公开的结合蛋白可以由宿主细胞表达,例如,无论是作为细胞表面分子(例如tcr、sctcr、car)还是可溶性分子(例如,tcr模拟抗体、sctv)(参见例如novoty et al.pnas 88(19):8646-8650(1991))。
[0129]
本公开的宿主细胞(例如免疫细胞)可以包括编码本文所述的结合蛋白的单个多核苷酸,或者该结合蛋白可以由超过一个的多核苷酸编码。换句话说,结合蛋白的组分或部分可以由两个或多个多核苷酸编码,其可以包含在单个核酸分子上,也可以包含在两个或多个核酸分子上。
[0130]
在某些实施例中,编码本公开的结合蛋白的两个或多个组分或部分的多核苷酸包括在单个开放阅读框中可操作地缔合的两个或多个编码序列。这样的排列可以有利地允许所需基因产物的协同表达,例如,如tcr的α和β多肽的同时表达,使得它们以约1:1的比例产生。在某些实施例中,本公开的结合蛋白(例如tcr(例如,α链和β链)或tcr模拟抗体(例如,重链和轻链))的两个或多个取代基因产物表达为分离的分子并在翻译后缔合。在进一步的实施例中,本公开的结合蛋白的两个或多个取代基因产物表达为单个肽,其具有由可裂解或可移除的片段分离的部分。例如,可用于表达由单个多核苷酸或载体编码的可分离多肽的自切割肽是本领域已知的,并且包括例如猪捷申病毒2a(porcine teschovirus-1 2a,
p2a)肽、thoseaasigna病毒2a(t2a)肽、马鼻炎a病毒(equine rhinitis avirus,erav)2a(e2a)肽和口蹄疫病毒2a(foot-and-mouth disease virus 2a,f2a)肽。
[0131]
在某些实施例中,本公开的结合蛋白包含一个或多个连接氨基酸。“连接氨基酸”或“连接氨基酸残基”是指多肽的两个相邻基序、区域或结构域之间的一个或多个(例如,2至约10个)氨基酸残基,例如在结合结构域和相邻恒定结构域之间或在tcr链和相邻自切割肽之间。连接氨基酸可以源自编码融合蛋白的构建体的设计(例如,在编码融合蛋白核酸分子的构建过程中使用限制性酶位点产生的氨基酸残基),或者源自例如与本公开的编码结合蛋白的一个或多个结构域相邻的自切割肽的切割(例如,位于tcrα-多肽和tcrβ-多肽之间的p2a肽,其自切割可在α-多肽、tcrβ多肽或两者中留下一个或多个连接氨基酸)。
[0132]
在本文所述的任何实施例中,本公开的编码多肽可以包括“信号肽”(也称为前导序列、前导肽或转运肽)。信号肽将新合成的多肽靶向细胞内外的适当位置。在定位或分泌完成期间或一旦完成定位或分泌,可以从多肽中去除信号肽。具有信号肽的多肽在本文中称为“前蛋白”,并且已去除其信号肽的多肽在本文中被称为“成熟”蛋白质或多肽。
[0133]
在本文公开的任何实施例中,编码结合蛋白(以及任选的一种或多种辅助蛋白)的多核苷酸可以经过密码子优化用于在宿主细胞中表达。一旦已知或鉴定了编码序列,就可以使用已知的技术和工具进行密码子优化,例如使用optimiumgene
tm
工具;另外参见scholten et al.,clin.immunol.119:135,2006。密码子优化的序列包括部分密码子优化(即,优化了一个或多个密码子用于在宿主细胞中的表达)的序列和完全密码子优化的序列。
[0134]
任何合适的宿主细胞都可以编码本公开的结合蛋白,或者被工程化为包括编码本公开结合蛋白的异源多核苷酸。在一些实施例中,优选为免疫细胞(例如,t细胞、nk细胞、nk-t细胞、b细胞或浆细胞)。在一些实施例中,免疫细胞包括cd4
+
t细胞、cd8
+
t细胞、或两者。用所需核酸转染/转导t细胞的方法(例如,美国专利申请公开号us 2004/0087025)已经被描述为使用具有所需靶特异性的t细胞的过继转移程序(例如,schmitt et al.,hum.gen.20:1240,2009;till et al.,blood 112:2261,2008;wang et al.,hum.gene ther.18:712,2007;kuball et al.,blood 109:2331,2007;us 2011/0243972;us 2011/0189141;leen et al.,ann.rev.immunol.25:243,2007),使得基于本文的教导,考虑将这些方法适应于本公开的实施例。
[0135]
在某些实施例中,可以对编码本公开的结合蛋白(例如tcr)的多核苷酸进行密码子优化以增强特定宿主细胞(例如免疫系统的细胞、造血干细胞、t细胞、原代t细胞、t细胞系、nk细胞或自然杀伤t细胞)中的表达。示例性t细胞包括cd4
+
t细胞、cd8
+
t细胞及其相关亚群(例如,幼稚、中枢记忆、效应记忆、干细胞记忆)。
[0136]
任何合适的方法都可以用于转染或转导细胞(例如t细胞),或用于施用本方法的多核苷酸或组合物。将多核苷酸递送到宿主细胞的已知方法包括,例如,使用阳离子聚合物、类脂分子和某些商业产品(例如,in-vivo-jet pei)。其他方法包括离体转导、注射、电穿孔、deae-葡聚糖、超声加载、脂质体介导的转染、受体介导的转导、微粒轰击、转座子介导的转移等。转染或转导宿主细胞的进一步方法采用了本文进一步详细描述的载体。将编码结合蛋白的多核苷酸引入宿主细胞或宿主细胞基因组的其他方法包括基因工程策略,例如crispr/cas系统。
[0137]
在本文公开的任何实施例中,免疫细胞包括t细胞、nk细胞、nk-t细胞、或其任何组合。在某些实施例中,免疫细胞包括cd8
+
t细胞、cd4
+
t细胞、或两者。在某些实施例中,在根据seq id nos:2-7中任一个或多个的sox2肽抗原存在时,宿主细胞(例如免疫细胞,例如表达本公开的sox2特异性结合蛋白的t细胞(例如cd8
+
t细胞))能够产生细胞因子。在某些实施例中,细胞因子是或包含ifn-γ。在某些实施例中,当sox2肽抗原以约1ng/ml、约10ng/ml、约100ng/ml、或约1000ng/ml存在时,宿主细胞产生细胞因子。在一些实施例中,进一步存在能够处理和呈递肽:hla复合物中的sox2肽抗原的靶细胞或抗原呈递细胞的细胞。
[0138]
在某些实施例中,在根据seq id nos:2-7中任一个或多个的sox2肽抗原(和任选的抗原呈递细胞,例如树突状细胞或t2细胞)存在时表达本公开的sox2特异性结合蛋白的宿主细胞(例如免疫细胞,例如t细胞)能够扩增,并且任选地进一步在细胞因子存在时扩增。在某些实施例中,细胞因子是或包含ifn-γ。在某些实施例中,sox2肽抗原以约1ng/ml、约10ng/ml、约100ng/ml、或约1000ng/ml存在。
[0139]
在某些实施例中,当与多发性骨髓瘤细胞共培养(例如,在12小时的细胞培养中)时,表达本公开的sox2特异性结合蛋白的宿主细胞(例如免疫细胞,例如t细胞)具有增加的cd137表达。在某些实施例中,多发性骨髓瘤细胞是l363细胞(dsmz no.acc 49)。在某些实施例中,多发性骨髓瘤细胞是患者来源的。
[0140]
在某些实施例中,表达本公开的sox2特异性结合蛋白的宿主细胞(例如免疫细胞,例如t细胞)能够特异性杀伤多发性骨髓瘤细胞(例如,体外、离体或体内)。在某些实施例中,多发性骨髓瘤细胞是l363细胞(dsmz no.acc 49)。在某些实施例中,多发性骨髓瘤细胞是患者来源的。
[0141]
在一些实施例中,当存在sox2抗原:hla复合物时,宿主细胞产生ifn-γ,其中,任选地,sox2抗原:hla复合物在靶细胞的表面上表达。在某些实施例中,结合蛋白能够与ylpgaevpepa(seq id no.:5):hla复合物结合,ifnγ产生pec
50
在6.0至9.0之间(即包括6.0、9.0及其之间的任何值)、在6.0至8.5之间、在6.0至8.0之间、在6.0至7.5之间、在6.0至7.0之间、在6.0至6.5之间、在6.5至9.0之间、在6.5至8.5之间、在6.5至8.0之间、在6.5至7.5之间、在6.5至7.0之间、在7.0至9.0之间、在7.0至8.5之间、在7.0至8.0之间、在7.0至7.5之间、在7.5至9.0之间、在7.5至8.5之间、在7.5至8.0之间、在8.0至9.0之间、在8.0至8.5之间、或在8.2至9.0之间。
[0142]
在宿主细胞的一些实施例中,结合蛋白能够与ylpgaevpepa(seq id no.:5):hla复合物结合,ifnγ产生pec
50
为约6.0、约6.1、约6.2、约6.3、约6.4、约6.5、约6.6、约6.7、约6.8、约6.9、约7.0、约7.1、约7.2、约7.3、约7.4、约7.5、约7.6、约7.7、约7.8、约7.9、约8.0、约8.1、约8.2、约8.3、约8.4、约8.5、约8.6、约8.7、约8.8、约8.9、或约9.0。
[0143]
在宿主细胞的一些实施例中,结合蛋白能够与ylpgaevpepa(seq id no.:5):hla复合物结合,ifnγ产生pec
50
为6.0或更高。在宿主细胞的一些实施例中,结合蛋白能够与ylpgaevpepa(seq id no.:5):hla复合物结合,ifnγ产生pec
50
为6.5或更高。在宿主细胞的一些实施例中,结合蛋白能够与ylpgaevpepa(seq id no.:5):hla复合物结合,ifnγ产生pec
50
为7.0或更高。在宿主细胞的一些实施例中,结合蛋白能够与ylpgaevpepa(seq id no.:5):hla复合物结合,ifnγ产生pec
50
为7.5或更高。在宿主细胞的一些实施例中,结合蛋白能够与ylpgaevpepa(seq id no.:5):hla复合物结合,ifnγ产生pec
50
为8.0或更高。在一
些实施例中,当在以下肿瘤细胞系中的任一种或多种的细胞存在时:cfpac1、h441、panc08.13、sw620、sw527、l363、表达hla-a2的mm1r和表达hla-a2的ina6,宿主细胞表达cd137,其中,任选地,在宿主细胞与一种或多种肿瘤细胞系的一个或多个细胞孵育后,通过宿主细胞的流式细胞术评估cd137的表达。在一些实施例中,在样品中存在的多个宿主细胞,在与以下肿瘤细胞系中的任一种或多种孵育后:cfpac1、h441、panc08.13、sw620、sw527、l363、表达hla-a2的mm1r、表达hla-a2的ina6,5%或更多、10%或更多、15%或更多、20%或更多、25%或更多、30%或更多、35%或更多、40%或更多、45%或更多、50%或更多、55%或更多、60%或更多、65%或更多、70%或更多、75%或更多、或80%或更多的所述多个宿主细胞对cd137的表达呈阳性。在一些实施例中,孵育包括约16小时至约18小时的持续时间,任选地,其中孵育包括16至18小时之间的持续时间。在某些进一步的实施例中,在孵育之前,将在肿瘤细胞系的细胞中增加hla-a2表达的试剂施用于肿瘤细胞系的细胞,其中,任选地,该试剂包括ifn-γ。
[0144]
在任何前述实施例中,宿主细胞(例如免疫细胞,如t细胞、nk-t细胞或nk细胞)可以被修饰以减少或消除编码参与免疫信号传导或其他相关活性的多肽的一种或多种内源基因的表达。基因敲除的例子包括编码pd-1、lag-3、ctla4、tim3、hla分子、tcr组分等的基因敲除。不希望被理论束缚,某些内源性表达的免疫细胞蛋白可能被接受修饰的免疫细胞的同种异体(allogeneic)宿主识别为外来的,这可能导致经修饰的免疫细胞(例如hla等位基因)的消除,或可能下调经修饰的免疫细胞(例如pd-1、lag-3、ctla4)的免疫活性,或可能干扰本公开的异源表达的结合蛋白的结合活性(例如,结合非sox2抗原并由此干扰经修饰的t细胞结合表达sox2抗原的细胞或启动t细胞对sox2抗原应答,或有助于或导致t细胞耗尽的经修饰的t细胞的内源性tcr)。
[0145]
因此,减少或消除这种内源基因或蛋白质的表达或活性可以提高宿主细胞在自体或同种异体宿主环境中的活性、耐受性或持久性,并且可以允许细胞的普遍给药(例如,对任何受体,无论hla类型如何)。在某些实施例中,宿主细胞是供体细胞(例如,同种异体)或自体细胞。在某些实施例中,本公开的宿主细胞包括编码pd-1、lag-3、ctla4、tim3、tigit、hla组分(例如,编码α1巨球蛋白、α2巨球蛋白、α3巨球蛋白,β1微球蛋白或β2微球蛋白的基因)或tcr组分(例如,编码tcr可变区或tcr恒定区的基因)的基因中的一种或多种的染色体基因敲除(参见,例如,torikai et al.,nature sci.rep.6:21757(2016);torikai et al.,blood 119(24):5697(2012);和torikai et al.,blood 122(8):1341(2013),其基因编辑技术、组合物和过继细胞疗法通过引用整体并入本文)。
[0146]
如本文所用,术语“染色体基因敲除”是指宿主细胞中的基因改变或引入的抑制物,其阻止(例如,减少、延迟、抑制或消除)宿主细胞产生功能活性内源性多肽产物。导致染色体基因敲除的改变可以包括,例如,引入的无义突变(包括过早终止密码子的形成)、错义突变、基因缺失和链断裂,以及抑制宿主细胞中内源基因表达的抑制性核酸分子的异源表达。
[0147]
在某些实施例中,染色体基因敲除或基因敲入是通过宿主细胞的染色体编辑而进行的。可以使用例如核酸内切酶进行染色体编辑。如本文所用,“核酸内切酶”是指能够催化多核苷酸链内磷酸二酯键断裂的酶。在某些实施例中,核酸内切酶能够切割靶向基因,从而使靶向基因失活或“敲除”。核酸内切酶可以是天然存在的、重组的、基因修饰的、或融合的
核酸内切酶。由核酸内切酶引起的核酸链断裂通常通过同源重组或非同源末端连接(nhej)的不同机制进行修复。在同源重组过程中,供体核酸分子可用于供体基因“敲入”、用于靶基因“敲除”,以及任选地通过供体基因敲入或靶基因敲除事件使靶基因失活。nhej是一种容易出错的修复过程,通常会导致切割位点的dna序列发生变化,例如至少一个核苷酸的取代、缺失或添加。nhej可用于“敲除”靶基因。核酸内切酶的示例包括锌指核酸酶、tale-核酸酶、crispr-cas核酸酶、大范围核酸酶和megatal。
[0148]
如本文所用,“锌指核酸酶”(zfn)是指包含与非特异性dna切割结构域融合的锌指dna结合结构域的融合蛋白,例如fokl核酸内切酶。每个约30个氨基酸的锌指基序与dna的约3个碱基对结合,并且可以改变某些残基处的氨基酸以改变三联体序列特异性(参见,例如,desjarlais et al.,proc.natl.acad.sci.90:2256-2260,1993;wolfe et al.,j.mol.biol.285:1917-1934,1999)。多个锌指基序可以串联连接,以产生对所需dna序列的结合特异性,例如长度范围为约9至约18个碱基对的区域。作为背景,zfn通过催化基因组中的位点特异性dna双链断裂(dsb)的形成来介导基因组编辑,并且通过同源定向修复促进了转基因的靶向整合,该转基因包括与在dsb位点的基因组同源的侧翼序列。或者,通过zfn产生的dsb可以通过非同源末端连接(nhej)修复导致靶基因敲除,这是一种容易出错的细胞修复途径,其导致在切割位点核苷酸的插入或缺失。在某些实施例中,基因敲除包括使用zfn分子进行的插入、缺失、突变、或其组合。
[0149]
如本文所用,“转录激活因子样效应物核酸酶”(talen)是指包含tale dna结合结构域和dna切割结构域的融合蛋白,如foki核酸内切酶。“tale dna结合结构域”或“tale”由一个或多个tale重复结构域/单元组成,每个通常具有高度保守的33至35氨基酸序列,具有不同的第12个和第13个氨基酸。tale重复结构域参与tale与靶dna序列的结合。不同的氨基酸残基称为重复可变双残基(rvd),与特定的核苷酸识别相关。已经确定了用于这些tale的dna识别的天然(典型)编码,使得在tale的位置12和13处的hd(组氨酸-天冬氨酸)序列导致tale与胞嘧啶(c)结合,ng(天冬酰胺-甘氨酸)与t核苷酸结合,ni(天冬酰胺-异亮氨酸)与a结合,nn(天冬酰胺-天冬酰胺)与g或a核苷酸结合,并且ng(天冬酰胺-甘氨酸)与t核苷酸结合。非规范(非典型)rvd也是已知的(参见,例如,美国专利公开号us 2011/0301073,其非典型rvd通过引用整体并入本文)。talen可用于指导t细胞基因组中的位点特异性双链断裂(dsb)。非同源末端连接(nhej)连接来自双链断裂两侧的dna,其中几乎没有或根本没有序列重叠用于退火,从而引入敲除基因表达的错误。或者,同源定向修复可以在dsb位点引入转基因,前提是转基因中存在同源侧翼序列。在某些实施例中,基因敲除包括插入、缺失、突变、或其组合,并且使用talen分子进行。
[0150]
如本文所用,“成簇的规律间隔短回文重复序列/cas”(crispr/cas)核酸酶系统是指采用crispr rna(crrna)引导的cas核酸酶通过碱基配对互补性识别基因组内的靶位点(称为原间隔区),如果短的、保守的原间隔区相关基序(pam)紧跟在互补靶序列的3'端,则切割dna的系统。根据cas核酸酶的序列和结构,crispr/cas系统分为三种类型(即i型、ii型和iii型)。i型和iii型中的crrna引导的监测复合物需要多个cas亚基。研究最多的ii型系统至少包括三种组分:rna引导的cas9核酸酶、crrna和反式作用crrna(tracrrna)。tracrrna包括双链体形成区。crrna和tracrrna形成双链体,该双链体能够与cas9核酸酶相互作用,并通过crrna上的间隔区和pam上游的靶dna上的原间隔区之间的watson-crick碱
基配对将cas9/crrna:tracrrna复合物引导到靶dna上特定的位点。cas9核酸酶在crrna间隔区所限定的区域内切割双链断裂。nhej的修复导致插入和/或缺失,从而破坏靶基因座的表达。或者,可以通过同源定向修复在dsb位点引入具有同源侧翼序列的转基因。crrna和tracrrna可以设计成单个指导rna(sgrna或grna)(参见,例如,jinek et al.,science 337:816-21,2012)。此外,可以改变或编程与靶位点互补的指导rna的区域以靶向所需序列(xie et al.,plos one 9:e100448,2014;美国专利申请公开号us 2014/0068797;美国专利申请公开号us 2014/0186843;美国专利号8,697,359和pct公开号wo 2015/071474;每一项都通过引用并入)。在某些实施例中,基因敲除包括插入、缺失、突变、或其组合,并且使用crispr/cas核酸酶系统进行。
[0151]
示例性grna序列和使用其敲除编码免疫细胞蛋白的内源基因的方法包括在ren et al.,clin.cancer res.23(9):2255-2266(2017)中所描述的那些,其grna、cas9 dna、载体和基因敲除技术通过引用整体并入本文。
[0152]
可以使用替代的cas核酸酶,包括但不限于cas 12、cas 13和cas 14核酸酶及其变体。例如,可以使用wo 2019/178427中所公开的cas核酸酶,其通过引用整体并入本文(包括其中所公开的cas核酸酶、crispr-cas系统和相关方法)。
[0153]
如本文所用,“大范围核酸酶(meganuclease)”,也称为“归巢核酸内切酶”,是指以大识别位点(约12至约40个碱基对的双链dna序列)为特征的脱氧核糖核酸内切酶。根据序列和结构基序,大范围核酸酶可分为五个家族:laglidadg、giy-yig、hnh、his-cys盒和pd-(d/e)xk。示例性的大范围核酸酶包括i-scei、i-ceui、pi-pspi、pi-sce、i-sceiv、i-csmi、i-pani、i-sceii、i-ppoi、i-screiii、i-crei、i-tevi、i-tevii和i-teviii,它们的识别序列是已知的(参见,例如,美国专利号5,420,032和6,833,252;belfort et al.,nucleic acids res.25:3379-3388,1997;dujon et al.,gene82:115-118,1989;perler et al.,nucleic acids res.22:1125-1127,1994;jasin,trends genet.12:224-228,1996;gimble et al.,j.mol.biol.263:163-180,1996;argast et al.,j.mol.biol.280:345-353,1998)。
[0154]
在某些实施例中,天然存在的大范围核酸酶可用于促进靶标的位点特异性基因组修饰,所述靶标选自pd-1、lag3、tim3、ctla4、tigit、hla编码基因或tcr组分编码基因。在其他实施例中,对靶基因具有新的结合特异性的工程化大范围核酸酶用于位点特异性基因组修饰(参见,例如,porteus et al.,nat.biotechnol.23:967-73,2005;sussman et al.,j.mol.biol.342:31-41,2004;epinat et al.,nucleic acids res.31:2952-62,2003;chevalier et al.,molec.cell 10:895-905,2002;ashworth et al.,nature441:656-659,2006;paques et al.,curr.gene ther.7:49-66,2007;美国专利公开号us 2007/0117128;us 2006/0206949;us 2006/0153826;us 2006/0078552;和us 2004/0002092)。在进一步的实施例中,使用归巢核酸内切酶产生染色体基因敲除,所述归巢核酸核酸内切酶已被talen的模块化dna结合结构域修饰以产生称为megatal的融合蛋白。megatal不仅可用于敲除一个或多个靶基因,当与编码感兴趣多肽的外源供体模板组合使用时,还可用于引入(敲入)异源或外源多核苷酸。
[0155]
在某些实施例中,染色体基因敲除包括被引入宿主细胞(例如免疫细胞)的抑制性核酸分子,所述宿主细胞包括编码特异性结合肿瘤相关抗原的抗原特异性受体的异源多核
苷酸,其中所述抑制性核酸分子编码靶特异性抑制物,并且其中所述编码的靶特异性抑制物抑制宿主细胞中的内源基因表达(即pd-1、tim3、lag3、ctla4、tigit、hla组分或tcr组分、或其任何组合)。
[0156]
在使用敲除程序或试剂后,可以通过宿主细胞的dna测序直接确认染色体基因敲除。染色体基因敲除也可以从敲除后基因表达的缺失(例如,基因编码的mrna或多肽产物的缺失)推断。
[0157]
在一些实施例中,编码结合蛋白的多核苷酸与宿主细胞异源,并且包含在宿主细胞的内源性tcr基因座中。
[0158]
在另一个方面,本文提供的组合物包含(例如有效量的)本公开的结合蛋白、多核苷酸、载体或宿主细胞,以及药学上可接受的载体、稀释剂或赋形剂。
[0159]
本文还提供了单位剂量,其包含有效量的修饰的免疫细胞或包含宿主细胞的组合物。在某些实施例中,单位剂量包含(i)包含至少约30%、至少约40%、至少约50%、至少约60%、至少约70%、至少约80%、至少约85%、至少约90%、或至少约95%修饰的cd4
+
t细胞的组合物,与(ii)包含至少约30%、至少约40%、至少约50%、至少约60%、至少约70%、至少约80%、至少约85%、至少约90%、或至少约95%修饰的cd8
+
t细胞的组合物,以约1:1的比例组合,其中所述单位剂量包含减少量的或基本上不含幼稚t细胞(即,与具有相当数量的pbmc的患者样本相比,具有小于约50%、小于约40%、小于约30%、小于约20%、小于约10%、小于约5%、或小于约1%以单位剂量存在的幼稚t细胞群体)。
[0160]
在一些实施例中,单位剂量包含(i)包含至少约50%修饰的cd4
+
t细胞的组合物,与(ii)包含至少约50%修饰的cd8
+
t细胞,以约1:1的比例组合,其中单位剂量包含减少量的或基本上不含幼稚t细胞。在进一步的实施例中,单位剂量包含(i)包含至少约60%修饰的cd4
+
t细胞的组合物,与(ii)包含至少约60%修饰的cd8
+
t细胞,以约1:1的比例组合,其中单位剂量包含减少量的或基本上不含幼稚t细胞。在又一个实施例中,单位剂量包含(i)包含至少约70%工程化的cd4
+
t细胞的组合物,与(ii)包含至少约70%工程化的cd8
+
t细胞的组合物,以约1:1比例组合,其中单位剂量包含减少量或基本上不含幼稚t细胞。在一些实施例中,单位剂量包含(i)包含至少约80%修饰的cd4
+
t细胞的组合物,与(ii)包含至少约80%修饰的cd8
+
t细胞,以约1:1的比例组合,其中单位剂量包含减少量的或基本上不含幼稚t细胞。在一些实施例中,单位剂量包含(i)包含至少约85%修饰的cd4
+
t细胞的组合物,与(ii)包含至少约85%修饰的cd8
+
t细胞,以约1:1的比例组合,其中单位剂量包含减少量的或基本上不含幼稚t细胞。在一些实施例中,单位剂量包含(i)包含至少约90%修饰的cd4
+
t细胞的组合物,与(ii)包含至少约90%修饰的cd8
+
t细胞,以约1:1的比例组合,其中单位剂量包含减少量的或基本上不含幼稚t细胞。
[0161]
应当理解,本公开的单位剂量可以包括本文所述的宿主细胞(即,编码并任选地表达对sox2抗原特异性的结合蛋白)和表达对不同抗原特异性结合蛋白的细胞(例如,免疫细胞,如t细胞、nk-t细胞或nk细胞)(所述不同抗原例如,不同的sox2抗原,或来自不同蛋白质或靶标的抗原,例如bcma、cd3、ceacam6、c-met、egfr、egfrviii、erbb2、erbb3、erbb4、epha2、igf1r、gd2、o-乙酰基gd2、o-乙酰基gd3、ghrhr、ghr、flt1、kdr、flt4、cd44v6、cd151、ca125、cea、ctla-4、gitr、btla、tgfbr2、tgfbr1、il6r、gp130、lewis a、lewis y、tnfr1、tnfr2、pd1、pd-l1、pd-l2、hvem、mage-a(例如,包括mage-a1、mage-a3和mage-a4)、间皮素、
ny-eso-1、psma、rank、ror1、tnfrsf4、cd40、cd137、tweak-r、hla、与hla结合的肿瘤或病原体相关肽、与hla连接的htert肽、与hla结合的酪氨酸酶肽、与hla结合的wt-1肽、ltβr、lifrβ、lrp5、muc1、osmrβ、tcrα、tcrβ、cd19、cd20、cd22、cd25、cd28、cd30、cd33、cd52、cd56、cd79a、cd79b、cd80、cd81、cd86、cd123、cd171、cd276、b7h4、tlr7、tlr9、ptch1、wt-1、ha
1-h、robo1、甲胎蛋白(afp)、frizzled、ox40、prame和ssx-2等)。例如,单位剂量可以包括表达特异性结合sox2-hla复合物的结合蛋白的修饰的cd8
+
t细胞和表达特异性结合cd19抗原的结合蛋白(例如car)的修饰的cd4
+
t细胞(和/或修饰的cd8
+
t细胞)。还应理解,本文公开的任何免疫细胞都可以在联合疗法中施用。
[0162]
在本文所述的任何实施例中,单位剂量包括相等或大致相等数量的工程化cd45ra-cd3
+
cd8
+
和修饰的cd45ra-cd3
+
cd4
+
tm细胞。
[0163]
还提供了用于表达根据本公开的tcr模拟抗体或抗原结合片段的宿主细胞,以及包括或包含编码tcr模拟的抗体或抗原-结合片段的载体或多核苷酸的宿主细胞。
[0164]
此类细胞的示例包括但不限于真核细胞(例如酵母细胞、动物细胞、昆虫细胞、植物细胞);以及原核细胞(包括大肠杆菌)。在一些实施例中,所述细胞是哺乳动物细胞。在某些实施例中,所述细胞是b细胞(例如永生化和/或工程化以编码抗体或抗原结合片段)、浆细胞或造血祖细胞。在某些实施例中,所述细胞是哺乳动物细胞系,例如cho细胞(例如dhfr-cho细胞(urlaub et al.,pnas 77:4216(1980))、人胚胎肾细胞(例如hek293t细胞)、per.c6细胞、y0细胞、sp2/0细胞、ns0细胞、人肝细胞(例如hepa rg细胞)、骨髓瘤细胞或杂交瘤细胞。哺乳动物宿主细胞系的其他示例包括小鼠支持细胞(例如tm4细胞);sv40转化的猴肾cv1系(cos-7);幼仓鼠肾细胞(bhk);非洲绿猴肾细胞(vero-76);猴肾细胞(cv1);人宫颈癌细胞(hela);人肺细胞(w138);人肝细胞(hep g2);犬肾细胞(mdck);水牛大鼠肝细胞(brl 3a);小鼠乳腺肿瘤(mmt 060562);tri细胞;mrc 5细胞;和fs4细胞。适用于抗体生产的哺乳动物宿主细胞系还包括在例如yazaki and wu,methods in molecular biology,vol.248(b..k.c.lo,ed.,humana press,totowa,n.j.),pp.255-268(2003)中所描述的那些。
[0165]
在某些实施例中,宿主细胞是原核细胞,例如大肠杆菌。肽在原核细胞(例如大肠杆菌)中的表达已得到很好的证实(参见,例如pluckthun,a.bio/technology9:545-551(1991))。例如,抗体可以在细菌中产生,特别是当不需要糖基化和fc效应器功能时。关于抗体片段和多肽在细菌中的表达,参见例如美国专利号5,648,237;5,789,199;和5,840,523。
[0166]
在特定的实施例中,可以用根据本说明书的载体转染细胞。转染可以使用例如,如电穿孔、脂质转染(例如基于阳离子脂质和/或脂质体)、磷酸钙沉淀、基于纳米颗粒的转染、基于病毒的转染或基于阳离子聚合物(例如deae-葡聚糖或聚乙烯亚胺等)的转染等方法来完成。在某些实施例中,引入是非病毒的。
[0167]
此外,本公开的宿主细胞可以用根据本公开的载体稳定地或瞬时地转染,例如用于表达根据本公开的抗体或其抗原结合片段。在这样的实施例中,可以用本文所述的载体稳定地转染细胞。或者,可以用根据本公开的编码本文所公开的抗体或抗原结合片段的载体瞬时转染细胞。在任何本所公开的实施例中,多核苷酸可以与宿主细胞异源。
[0168]
因此,本公开还提供了表达本文所公开的抗体或抗原结合片段的重组宿主细胞。例如,细胞可以是与完全或部分获得抗体的物种不同的物种(例如,表达人抗体或工程化人
抗体的cho细胞)。在一些实施例中,宿主细胞的细胞类型在自然界中不表达抗体或抗原结合片段。此外,宿主细胞可以对抗体或抗原结合片段进行翻译后修饰(ptm;例如,糖基化或岩藻糖基化),该修饰不存在于抗体或抗原结合片段的天然状态(或由抗体或抗原结合片段工程化或衍生的亲代抗体的天然状态)。这样的ptm可能导致功能差异(例如,降低免疫原性)。因此,由本文公开的宿主细胞产生的本公开的抗体或抗原结合片段可以包括一种或多种翻译后修饰,其不同于处于其天然状态的抗体(或亲代抗体)(例如,由cho细胞产生的人抗体可以包括多个翻译后修饰,其不同于从人分离和/或由天然人b细胞或浆细胞产生的抗体)。
[0169]
可用于表达抗体或抗原结合片段的昆虫细胞包括,例如,草地贪夜蛾(spodoptera frugipera)sf9细胞、粉纹夜蛾(trichoplusia ni)bti-tn5b1-4细胞和草地贪夜蝇sfswt01“mimic
tm”细胞。例如,参见palmberger et al.,j.biotechnol.153(3-4):160-166(2011)。已经鉴定出许多杆状病毒株,它们可以与昆虫细胞结合使用,特别是用于转染草地贪夜蛾细胞。
[0170]
真核微生物(如丝状真菌或酵母)也是用于克隆或表达蛋白质编码载体的合适宿主,其包括具有“人源化”糖基化途径的真菌和酵母菌株,从而产生具有部分或完全人类糖基化模式的抗体。参见gerngross,nat.biotech.22:1409-1414(2004);li et al.,nat.biotech.24:210-215(2006)。
[0171]
植物细胞也可以用作表达本公开的抗体或抗原结合片段的宿主。例如,(例如,在美国专利号5,959,177;6,040,498;6,420,548;7,125,978;和6,417,429中描述的)plantibodies
tm
技术采用转基因植物来产生抗体。
[0172]
在某些实施例中,宿主细胞包括哺乳动物细胞。在特定实施例中,宿主细胞是cho细胞、hek293细胞、per.c6细胞、y0细胞、sp2/0细胞、ns0细胞、人肝细胞、骨髓瘤细胞或杂交瘤细胞。
[0173]
多核苷酸、转基因和载体
[0174]
在进一步的方面,本公开提供了一种分离的多核苷酸,其编码本文所述的免疫原性肽、融合多肽或结合蛋白(例如,sox2特异性tcr、sctv、tcr模拟抗体或其抗原结合片段、sctcr或car,其包含本文所述tcr vα和vβ结构域(且任选地进一步包含本文所述的恒定结构域或其它组分))。
[0175]
在某些实施例中,编码本公开的结合蛋白的两个或多个组分或部分的多核苷酸包括在单个开放阅读框中可操作地缔合的两个或多个编码序列。这样的安排可以有利地允许所需基因产物的协同表达,例如tcr的α链和β链的同时表达,使得它们以约1:1的比例产生。在某些实施例中,本公开的结合蛋白(例如tcr(例如,α链和β链))的两个或多个取代基因产物表达为分离的分子,并在翻译后缔合。在进一步的实施例中,本公开的结合蛋白的两个或多个取代基因产物表达为单个肽,具有由可裂解或可移除的片段分离的部分。例如,可用于表达由单个多核苷酸或载体编码的可分离多肽的自切割肽是本领域已知的,并且包括例如猪捷申病毒2a(porcine teschovirus-1 2a,p2a)肽、thoseaasigna病毒2a(t2a)肽、马鼻炎a病毒(equine rhinitis avirus,erav)2a(e2a)肽和口蹄疫病毒2a(foot-and-mouth disease virus2a,f2a)肽。
[0176]
在一些实施例中,多核苷酸包含dna、rna(任选为mrna)、或两者。在某些实施例中,
多核苷酸包含dna。
[0177]
在某些实施例中,(1)多核苷酸编码以下各项:与seq id nos.:48、96、12、24、36、60、72、84、108、120、132和144中任一项所述的氨基酸序列具有至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性的氨基酸序列、或包含或由seq id nos.:48、96、12、24、36、60、72、84、108、120、132和144中任一项所述的氨基酸序列组成的氨基酸序列;和/或(2)所述多核苷酸包含与seq id nos.:47、95、11、23、35、47、59、71、83、107、119、131和143中任一项所述的核苷酸序列具有至少70%、至少75%、至少80%、至少85%、至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性的多核苷酸,或所述多核苷酸包含或由seq id nos.:47、95、11、23、35、47、59、71、83、107、119、131和143中任一项所述的核苷酸序列组成。
[0178]
在一些实施例中,多核苷酸经过密码子优化用于在宿主细胞中表达,其中,任选地,宿主细胞包括免疫系统细胞,其中,进一步任选地,免疫系统细胞包括t细胞、nk-t细胞或nk细胞。
[0179]
本公开的宿主细胞可以包括编码如本文所述的结合蛋白的单个多核苷酸,或者该结合蛋白可以由超过一个的多核苷酸编码。换句话说,结合蛋白的组分或部分可以由两个或多个多核苷酸编码,其可以包含在单个核酸分子上,也可以包含在两个或多个核酸分子上。
[0180]
在进一步的实施例中,结合蛋白表达为转基因构建体的一部分,其编码一种或多种额外的辅助蛋白,例如安全开关蛋白、标签、选择标记、cd8共受体β链、α链或两者,或其任何组合。多核苷酸和转基因构建体可用于编码和表达结合蛋白和辅助成分(例如,一种或多种安全开关蛋白、选择标记、cd8共受体β链或cd8共受体α链)。
[0181]
在某些实施例中,可以使用同源药物或其他化合物靶向安全开关蛋白,以在需要时选择性地调节(例如,减少或消融)这种细胞的活性。在这方面使用的安全开关蛋白包括,例如,截短的egf受体多肽(huegfrt),其缺乏细胞外n末端配体结合结构域和细胞内受体酪氨酸激酶活性,但保留天然氨基酸序列,具有i型跨膜细胞表面定位,并且具有用于药物级抗egfr单克隆抗体的构象完整的结合表位;西妥昔单抗(erbitux)tegf受体(tegfr;wang et al.,blood 118:1255-1263,2011);半胱天冬酶(caspase)多肽(例如,icasp9;straathof et al.,blood 105:4247-4254,2005;di stasi et al.,n.engl.j.med.365:1673-1683,2011;zhou and brenner,exp.hematol.pii:s0301-472x(16)30513-6.doi:10.1016/j.exphem.2016.07.011);rqr8(philip et al.,blood 124:1277-1287,2014);人类c-myc蛋白质(myc)的10氨基酸标签(kieback et al.,proc.natl.acad.sci.usa105:623-628,2008),如本文所述,以及标记/安全开关多肽,如rqr(cd20+cd34;philip et al.,2014)。
[0182]
可用于治疗细胞的其他辅助成分包括允许识别、分选、分离、富集或追踪细胞的标签或选择标记。例如,可以将具有所需特征(例如抗原特异性tcr和安全开关蛋白)的标记免疫细胞从样品中的未标记细胞中分离出来,并更有效地激活和扩增以包含在所需纯度的治疗产品中。
[0183]
如本文所用,术语“选择标记”包括核酸构建体,其赋予细胞可识别的变化,从而允
许检测和阳性选择用包含选择标记的多核苷酸转导的免疫细胞。rqr是包括一个主要的cd20细胞外环和两个最小的cd34结合位点的选择标记。在一些实施例中,编码rqr的多核苷酸包括编码16氨基酸的cd34最小表位的多核苷酸。在一些实施例中,例如本文示例中提供的某些实施例,cd34最小表位并入cd8茎结构域(q8)的氨基末端位置。在进一步的实施例中,cd34最小结合位点序列可以与cd20的靶表位结合,以形成t细胞的紧密标记/自杀基因(rqr8)(philip et al.,2014,通过引用并入本文)。该构建体允许选择表达该构建体的免疫细胞,例如,cd34特异性抗体与磁珠(miltenyi)结合,并利用临床可接受的药物抗体利妥昔单抗(rituximab),其允许选择性缺失表达转基因的工程t细胞(philip et al.,2014)。
[0184]
其他示例性选择标记还包括几种通常不在t细胞上表达的截短的i型跨膜蛋白:截短的低亲和力神经生长因子、截短的cd19和截短的cd34(参见,例如di stasi et al.,n.engl.j.med.365:1673-1683,2011;mavilio et al.,blood 83:1988-1997,1994;fehse et al.,mol.ther.1:448-456,2000;每一项均整体并入本文)。cd19和cd34的一个特征是现成的miltenyi clinimacs
tm
选择系统的可用性,该系统可以针对这些标记进行临床分级分类。然而,cd19和cd34是相对较大的表面蛋白,它们可能会影响整合载体的载体包装能力和转录效率。也可以使用含有细胞外、非信号传导结构域或各种蛋白质(例如cd19、cd34、lngfr)的表面标记。可以使用任何选择标记,并且应该是良好生产规范可接受的。在某些实施例中,选择标记用编码感兴趣的基因产物(例如,本公开的结合蛋白,例如tcr或car)的多核苷酸表达。选择标记的其他示例包括,例如,报告基因,如gfp、egfp、β-gal或氯霉素乙酰转移酶(cat)。在某些实施例中,选择标记例如cd34由细胞表达并且cd34可用于选择富集或分离(例如,通过免疫磁性选择)感兴趣的转导细胞以用于本文所述的方法。如本文所用,cd34标记不同于抗cd34抗体或例如scfv、tcr或结合cd34的其他抗原识别部分。在某些实施例中,选择标记包括rqr多肽、截短的低亲和力神经生长因子(tngfr)、截短的cd19(tcd19)、截短的cd34(tcd34)、或其任何组合。
[0185]
在某些实施例中,编码本公开的结合蛋白的多核苷酸以及包含其的宿主细胞可以进一步包含编码cd8共受体蛋白或其β链或α链组分的多核苷酸。作为背景,将cd4
+
t细胞包含在免疫治疗细胞产物中可以提供抗原诱导的il-2分泌,并增强转移的细胞毒性cd8
+
t细胞的持久性和功能(参见,例如,kennedy et al.,immunol.rev.222:129(2008);nakanishi et al.,nature 462(7272):510(2009))。在某些情况下,cd4
+
t细胞中的i类限制性tcr可能需要cd8共受体的转移,以增强tcr对i类hla肽复合物的敏感性。cd4共受体在结构上与cd8不同,并且不能有效地替代cd8共受体(参见,例如stone&kranz,front.immunol.4:244(2013);另见cole et al.,immunology137(2):139(2012))。因此,用于本公开的组合物和方法的另一种辅助蛋白包括cd8共受体或其组分。
[0186]
在一些实施例中,编码的cd8共受体包括β链(参见例如uniprotkb标识符p10966-1、p10966-2、p10966-3、p10966-4、p10966-6、p10966-7、p10966-8和p10966-9)。在进一步的实施例中,编码的cd8共受体是进一步包含rqr多肽的重组cd8共受体。不希望受理论束缚,据信与宿主细胞表面的距离对于rqr多肽发挥作为选择标记/安全开关的作用是重要的(philip et al.,2010(同上))。在一些实施例中,编码的rqr多肽包含在编码的cd8共受体的β链、α链或两者中。在特定实施例中,修饰的免疫细胞包含编码icasp9的异源多核苷酸和编码重组cd8共受体蛋白的异源多核苷酸,所述重组cd8共受体蛋白包含含有rqr多肽的β链
(pntcrβ);(v)(pntcrβ)-(pnscp1)-(pntcrα)-(pnscp2)-(pncd8α)-(pnscp3)-(pncd8β);(vi)(pntcrβ)-(pnscp1)-(pntcrα)-(pnscp2)-(pncd8β)-(pnscp3)-(pncd8α);(vii)(pntcrα)-(pnscp1)-(pntcrβ)-(pnscp2)-(pncd8α)-(pnscp3)-(pncd8β);或(viii)(pntcrα)-(pnscp1)-(pntcrβ)-(pnscp2)-(pncd8β)-(pnscp3)-(pncd8α),其中pncd8α是编码包含cd8共受体α链的细胞外部分的多肽的多核苷酸,其中pncd8β是编码包含cd8共受体α链的细胞外部分的多肽的多核苷酸;其中pntcrα是编码tcrα链的多核苷酸,其中pntcrβ是编码tcrβ链的多核苷酸,并且其中pnscp1、pnscp2和pnscp3各自独立地为编码自切割肽的多核苷酸,其中所述多核苷酸和/或编码的自切割肽任选相同或不同。
[0193]
在某些实施例中,分离的多核苷酸的至少一部分经过密码子优化,用于在宿主细胞(例如本文所公开的抗原呈递细胞或工程化免疫细胞)中表达。
[0194]
特别地,宿主细胞中包含的任何上述异源多核苷酸(例如,编码本公开的任何结合蛋白)也可以或可替代地以分离的形式提供。在一些实施例中,多核苷酸经过密码子优化用于在宿主细胞中表达。
[0195]
在某些实施例中,编码tcr vα或α-多肽的异源多核苷酸和编码tcr vβ或β-多肽的异源多核苷酸包含在宿主细胞中的单个开放阅读框中,其中所述单个开放阅读框进一步包含编码自切割肽的多核苷酸,其设置在编码vα(或α-多肽)的多核苷酸和编码vβ(或β-多肽)的多核苷酸之间。
[0196]
在本文所述的任何实施例中,分离的多核苷酸经过密码子优化用于在免疫细胞(例如t细胞)中表达。
[0197]
本文还提供了包含本公开的转基因构建体的载体。载体的一些例子包括质粒、病毒载体、粘粒等。一些载体可能能够在它们被引入的宿主细胞中自主复制(例如,具有细菌复制起点的细菌载体和附加型哺乳动物载体),而其他载体可以整合到宿主细胞的基因组中或在引入宿主细胞后促进多核苷酸插入物的整合,从而与宿主基因组一起复制(例如,慢病毒载体、逆转录病毒载体)。此外,一些载体能够指导与其操作地连接的基因的表达(这些载体可以称为“表达载体”)。根据相关实施例,还应理解,如果一种或多种试剂(例如,编码本文所述的结合蛋白的多核苷酸)共同施用于受试者,则每种试剂可以存在于单独或相同的载体中,并且可以将多个载体(每个载体含有不同的试剂或相同的试剂)引入细胞或细胞群体或施用于受试者。
[0198]
在某些实施例中,本公开的多核苷酸可以操作地连接到载体的某些元件。例如,影响与其连接的编码序列的表达和处理所需的多核苷酸序列可以操作地连接。表达控制序列可以包括适当的转录起始、终止、启动子和增强子序列;有效的rna处理信号,例如剪接和多腺苷酸化信号;稳定细胞质mrna的序列;提高翻译效率的序列(即kozak共有序列);增强蛋白质稳定性的序列;以及可能增强蛋白质分泌的序列。如果表达控制序列与感兴趣基因和在反式或在一定距离上作用以控制感兴趣基因的表达控制序列连续,则它们可以操作地连接。
[0199]
在某些实施例中,载体包括质粒载体或病毒载体(例如,选自慢病毒载体或γ-逆转录病毒载体的载体)。病毒载体包括逆转录病毒、腺病毒、细小病毒(例如,腺相关病毒)、冠状病毒、负链rna病毒(如正粘病毒(例如,流感病毒))、弹状病毒(例如,狂犬病和水疱性口炎病毒)、副粘病毒(例如,麻疹和仙台)、正链rna病毒(例如,细小核糖核酸病毒和α病毒)、
以及双链dna病毒,包括腺病毒、疱疹病毒(例如,单纯疱疹病毒1型和2型、eb病毒、巨细胞病毒)和痘病毒(例如,牛痘、鸡痘和金丝雀痘)。例如,其他病毒包括诺如病毒、披膜病毒(togavirus)、黄病毒、呼肠孤病毒、乳多空病毒、嗜肝dna病毒(hepadnavirus)和肝炎病毒。逆转录病毒的示例包括禽白血病肉瘤、哺乳动物c型、b型病毒、d型病毒、htlv-blv组、慢病毒和泡沫病毒(spumavirus)(coffin,j.m.,retroviridae:the viruses and their replication,in fundamental virology,third edition,b.n.fields et al.,eds.,lippincott-raven publishers,philadelphia,1996)。
[0200]“逆转录病毒”是具有rna基因组的病毒,使用逆转录酶将其逆转录为dna,然后将逆转录的dna掺入宿主细胞基因组中。“γ逆转录病毒”是指逆转录病毒科的一个属。γ逆转录病毒的示例包括小鼠干细胞病毒、小鼠白血病病毒、猫白血病病毒、猫肉瘤病毒和禽网状内皮组织增生病病毒。“慢病毒”是指逆转录病毒科的一个属。如本文所用,“慢病毒载体”是指用于基因递送的基于hiv的慢病毒载体,其可以是整合的或非整合的,具有较大的包装能力,并且可以转导一系列不同的细胞类型。慢病毒载体通常是在三种(包装、包膜和转移)或更多质粒瞬时转染到生产细胞后产生的。与hiv一样,慢病毒载体通过病毒表面糖蛋白与细胞表面受体的相互作用进入靶细胞。在进入时,病毒rna进行逆转录,这是由病毒逆转录酶复合物介导的。逆转录的产物是双链线性病毒dna,它是病毒整合到受感染细胞dna中的底物。
[0201]
在某些实施例中,病毒载体可以是或衍生自γ逆转录病毒,例如莫洛尼鼠类白血病病毒(mlv)衍生的载体。在其他实施例中,病毒载体可以是更复杂的逆转录病毒衍生载体,例如慢病毒衍生载体。hiv-1衍生的载体属于这一类。其他示例包括衍生自hiv-2、fiv、马传染性贫血病毒、siv和梅迪维斯纳病毒(maedi-visna virus)(绵羊慢病毒)的慢病毒载体。使用逆转录病毒和慢病毒载体和包装细胞用于用含有tcr或car转基因的病毒颗粒转导哺乳动物宿主细胞的方法是本领域已知的,并且先前已经在例如美国专利8,119,772;walchli et al.,plos one 6:327930,2011;zhao et al.,j.immunol.174:4415,2005;engels et al.,hum.gene ther.14:1155,2003;frecha et al.,mol.ther.18:1748,2010;和verhoeyen et al.,methods mol.biol.506:97,2009中进行了描述。逆转录病毒和慢病毒载体构建体和表达系统也是可商购的。其他病毒载体也可用于多核苷酸递送,包括dna病毒载体,包括例如基于腺病毒的载体和基于腺相关病毒(aav)的载体;源自单纯疱疹病毒(hsv)的载体,包括扩增子载体、复制缺陷型hsv和减毒型hsv(krisky et al.,gene ther.5:1517,1998)。
[0202]
开发用于基因治疗用途的其他载体也可以与本公开的组合物和方法一起使用。此类载体包括源自杆状病毒和α-病毒的载体(jolly,d j.1999.emerging viral vectors.pp209-40in friedmann t.ed.the development of human gene therapy.new york:cold spring harbor lab),或质粒载体(如sleeping beauty或其他转座子载体)。
[0203]
当病毒载体基因组包含将在宿主细胞中表达为单独转录物的多个多核苷酸时,病毒载体还可以包含两个(或多个)转录物之间的附加序列,从而允许双顺反子或多顺反子表达。用于病毒载体的此类序列的示例包括内部核糖体进入位点(ires)、弗林蛋白酶切割位点、病毒2a肽、或其任何组合。
[0204]
在某些实施例中,载体能够将转基因构建体递送到宿主细胞(例如,造血祖细胞或
人类免疫系统细胞)。在具体实施例中,载体能够将转基因构建体递送至人类免疫系统细胞,例如cd4
+
t细胞、cd8
+
t细胞、cd4-cd8-双阴性t细胞、γδt细胞、自然杀伤细胞、树突状细胞、或其任何组合。在进一步的实施例中,载体能够将转基因构建体递送至幼稚t细胞、中央记忆t细胞、效应记忆t细胞、或其任何组合。在一些实施例中,编码本公开的多核苷酸或转基因构建体的载体可进一步包含编码核酸酶的多核苷酸,所述核酸酶可用于在宿主细胞中进行染色体敲除(例如,crispr-cas核酸内切酶或如本文所公开的另一种核酸内切酶),或可用于在基因治疗替代或基因修复治疗中将治疗性转基因或其部分递送至宿主细胞。或者,用于染色体敲除或基因替代或基因修复治疗的核酸酶可以独立于编码本公开的多核苷酸或转基因构建体的载体递送至宿主细胞。
[0205]
用途
[0206]
在其他方面,本公开提供了引发针对与根据seq id nos:2-7中任一种的sox2抗原表达相关的癌症(例如血液系统恶性肿瘤(例如多发性骨髓瘤))的免疫应答(例如,细胞因子的产生、t细胞的增殖、t细胞活化(例如,cd137的表达增加、细胞内钙的产生、tcr信号蛋白的磷酸化增加)、b细胞的增殖、抗体的产生、或其任何组合)的方法,其中所述方法包括将有效量的免疫原性组合物或表达该组合物的宿主细胞、sox2特异性结合蛋白、sox2特异性融合蛋白、或编码并能够表达本文所述sox2特异性结合蛋白的宿主细胞(如t细胞)施用于患有或疑似患有癌症的人类受试者。
[0207]
还提供了用于扩增与根据seq id nos:2-7中任一项的sox2抗原(任选在抗原:hla复合物的情况下)特异性结合的t细胞群体的方法,其中所述方法包括使包含特异性结合抗原的一个或多个t细胞的样品与本公开的免疫原性组合物(或编码免疫原性sox2肽或融合多肽的宿主细胞)接触。
[0208]
还提供了用于产生和/或分离t细胞的方法,其中所述方法包括使外周血细胞或全血与以下物质接触:(a)本公开的免疫原性组合物;或(b)抗原呈递细胞(apc),其表达sox2抗原(例如,存在于hla分子的情况下)或已用sox2抗原脉冲处理,所述sox2抗原包含根据seq id nos:2-7中任一个或多个的氨基酸序列,或(iv)(i)-(iii)的任何组合;以及任选地从外周血细胞中分选t细胞,从而分离和/或产生t细胞。
[0209]
在其他方面,本公开提供了用于治疗受试者中与根据seq id nos:2-7中任一项所述的sox2抗原相关(例如,表达或被认为或已知表达或被证实表达)的疾病或病症的方法,其中所述方法包括向受试者施用本公开的sox2特异性宿主(例如,免疫)细胞、结合蛋白、多核苷酸、载体、融合蛋白、组合物或免疫原性组合物,从而治疗疾病或病况。还提供了本公开结合蛋白、多核苷酸、载体、宿主细胞、组合物和免疫原性组合物在治疗与根据seq id nos:2-7中任一项的sox2抗原相关的疾病或病症的用途和/或在制备用于治疗与seq id no:2-7中任一项所述sox2抗原相关的疾病或病症的药物的用途。
[0210]
术语“治疗(treat)”、“治疗(treatment)”或“改善”是指对受试者(例如,人类或非人类哺乳动物,如灵长类动物、马、猫、狗、山羊、小鼠或大鼠)的疾病、病症或病况的医学管理。通常,以足以引发治疗或预防益处的量施用包含本公开的修饰的免疫细胞和任选的佐剂的适当剂量或治疗方案。治疗性或预防性(prophylactic)/预防性(preventive)益处包括改善临床结果;减轻或缓解与疾病相关的症状;降低症状发生率;提高生活质量;更长的无病状态;疾病程度的减轻,疾病状态的稳定;疾病进展的延迟;缓解;生存;延长生存期;或
其任何组合。
[0211]
如本文所用,“治疗有效量”或“有效量”是指足以产生治疗效果的组合物的量(以统计学显著的方式),所述治疗效果包括改善的临床结果;减轻或缓解与疾病相关的症状;降低症状发生率;提高生活质量;更长的无病状态;疾病程度的减轻,疾病状态的稳定;疾病进展的延迟;缓解;生存;或延长生存期。当涉及单独施用的单个活性成分或表达单一活性成分的细胞时,治疗有效量是指该成分或单独表达该成分的细胞的效果。当涉及组合时,治疗有效量是指活性成分或辅助活性成分与表达活性成分的细胞组合的组合量,无论是连续施用还是同时施用,都会产生治疗效果。组合也可以是表达超过一种活性成分的细胞。
[0212]
如本文所用,“统计学显著”是指使用学生t-检验计算时p值为0.050或更小,并表明所测量的特定事件或结果不太可能是偶然出现的。
[0213]
术语“药学上可接受的赋形剂或载剂”或“生理学上可接受的赋形剂或载剂”是指生物可相容的媒介,例如生理盐水,其在本文中更详细地描述,其适用于施用于人类或其他非人类哺乳动物受试者,并且通常被认为是安全的或不会引起严重不良事件。
[0214]
在某些实施例中,根据本公开的方法治疗的受试者是hla-a*02:01
+
。在一些实施例中,所述疾病或病况是癌症。在某些实施例中,癌症包括血液系统恶性肿瘤或实体肿瘤。
[0215]
在某些实施例中,血液系统恶性肿瘤包括骨髓瘤,例如多发性骨髓瘤。在某些实施例中,血液系统恶性肿瘤包括白血病(例如,急性白血病或慢性白血病)。在具体的实施例中,白血病包括急性髓细胞白血病(aml)、急性淋巴细胞白血病(all)、混合表型急性白血病(mpal)、慢性髓细胞性白血病(cml)、b细胞前淋巴细胞白血病、毛细胞性白血病或慢性淋巴细胞白血病(cll)。在某些实施例中,血液系统恶性肿瘤包括淋巴瘤。在某些实施例中,淋巴瘤包括霍奇金淋巴瘤(hl)、非霍奇金淋巴瘤(nhl)、中枢神经系统淋巴瘤、小淋巴细胞淋巴瘤(sll)、cd37+树突状细胞淋巴瘤、淋巴浆细胞淋巴瘤、脾边缘区淋巴瘤、浆细胞性骨髓瘤、骨外浆细胞瘤、粘膜相关(malt)淋巴组织的淋巴结外边缘带b细胞淋巴瘤、淋巴结边缘带b细胞淋巴瘤、滤泡性淋巴瘤、套细胞淋巴瘤、弥漫性大b细胞淋巴瘤、纵隔(胸腺)大b细胞淋巴瘤、前体b淋巴细胞淋巴瘤、免疫母细胞大细胞淋巴瘤、血管内大b细胞淋巴瘤、原发性渗出性淋巴瘤、伯基特(burkitt's)淋巴瘤/白血病、恶性潜能不确定的b细胞增殖、淋巴瘤样肉芽肿和移植后淋巴增生性疾病。在某些实施例中,血液系统恶性肿瘤包括骨髓增生异常疾病,例如,如难治性血细胞减少伴单系发育异常(难治性贫血、难治性中性粒细胞减少症和难治性血小板减少症)、难治性贫血伴环形铁粒幼细胞(rars)、难治性贫血伴环状铁粒幼细胞-血小板增多症(rars-t)、难治性血细胞减少伴多系发育异常(rcmd)、难治性血细胞减少伴发性多系发育异常和环形铁粒幼细胞(rcmd-rs)、难治性贫血伴原始细胞过多(raeb)、无法分类的骨髓发育不良和儿童的难治性血细胞减少。
[0216]
可以用本公开的组合物和方法靶向或治疗的、会形成实体瘤的示例性癌症包括肉瘤和癌,包括例如软骨肉瘤;纤维肉瘤(成纤维细胞肉瘤);隆突性皮肤纤维肉瘤(dfsp);骨肉瘤;横纹肌肉瘤;尤文肉瘤(ewing's sarcoma);胃肠道间质瘤;平滑肌肉瘤;血管肉瘤(angiosarcoma)(血管肉瘤(vascular sarcoma));卡波西肉瘤(kaposi's sarcoma);脂肪肉瘤;多形性肉瘤;滑膜肉瘤;鳞状细胞癌;腺癌;腺鳞癌;间变性癌;大细胞癌;小细胞癌;乳腺癌(例如导管原位癌(非侵袭性)、小叶原位癌(非侵袭性)、侵袭性导管癌、侵袭性小叶癌、非侵袭性癌);肝癌(例如,肝细胞癌、胆管癌或胆管癌症);肺癌(例如,腺癌、鳞状细胞癌(表
皮样癌)、大细胞未分化癌、细支气管肺泡癌);卵巢癌(例如表面上皮间质瘤(腺癌)或卵巢上皮癌(包括浆液性肿瘤、子宫内膜样肿瘤和粘液性囊腺癌)、表皮样瘤(鳞状细胞癌)、胚胎癌和绒毛膜癌(生殖细胞瘤));肾癌(例如,肾腺癌、肾上腺样瘤、移行细胞癌(肾盂)、鳞状细胞癌、贝氏管癌(bellini duct carcinoma)、透明细胞腺癌、移行细胞癌、肾盂类癌瘤);肾上腺癌(例如,肾上腺皮质癌)、睾丸癌(例如,生殖细胞癌(精原细胞瘤、绒毛膜癌、胚胎癌、畸胎癌)、浆液性癌);胃癌(例如,腺癌);肠癌(例如,十二指肠腺癌);结肠癌;或皮肤癌(例如,基底细胞癌、鳞状细胞癌)、神经母细胞瘤、肝母细胞瘤、脑肿瘤亚型(例如,神经胶质瘤、pnet、颅咽管瘤(cranipharyngioma)、脉络丛肿瘤、神经鞘瘤、脑膜瘤)、肾母细胞瘤和生殖细胞瘤。
[0217]
在某些实施例中,本公开的方法针对或治疗由选自以下癌症形成的实体瘤:卵巢癌、卵巢上皮癌、宫颈腺癌或小细胞癌、胰腺癌、结直肠癌(例如,腺癌或鳞状细胞癌)、肺癌、乳腺导管癌、或前列腺腺癌。
[0218]
在一些实施例中,癌症包括多发性骨髓瘤、浆细胞白血病、卵巢癌、胶质瘤(参见,例如schmitz et al.br j cancer 96(8):1293-1301(2007))、肺癌、颈癌、宫颈癌、或其任何组合。
[0219]
针对实体瘤的免疫应答水平(例如ctl(细胞毒性t淋巴细胞)免疫应答)可以通过本文所述的多种免疫方法中的任一种来确定。ctl免疫应答的水平可以在施用本文所述的由例如t细胞表达的抗原特异性结合受体中的任一种之前和施用之后测定。用于测定ctl活性的细胞毒性试验可以使用几种技术和方法中的任一种(参见,例如henkart et al.,"cytotoxic t-lymphocytes"in fundamental immunology,paul(ed.)(2003lippincott williams&wilkins,philadelphia,pa),pages 1127-50,以及其中引用的参考文献);试验(如本文所述)进行。
[0220]
在一些实施例中,通过本公开的方法可治疗的癌症包括胶质母细胞瘤、髓母细胞瘤、乳腺癌、结直肠癌、肺癌(例如非小细胞肺癌)、食管癌、淋巴瘤、白血病(例如,急性髓细胞白血病)、黑色素瘤、胆管癌、膀胱癌、宫颈癌、胰腺癌或肝细胞癌、神经母细胞瘤、肝母细胞瘤、脑肿瘤亚型(例如,神经胶质瘤、pnet、颅咽管瘤、脉络丛肿瘤、神经鞘瘤、脑膜瘤)、肾母细胞瘤和生殖细胞瘤。
[0221]
本发明可以治疗的受试者通常是人类和其他灵长类受试者,例如用于兽医目的的猴子和猿。在任何前述实施例中,受试者可以是人类受试者。受试者可以是男性或女性,也可以是任何合适年龄的受试者,包括婴儿、少年、青少年、成人和老年受试者。儿童受试者是指婴儿、少年或青少年受试者。根据本公开的细胞可以以适合于医学领域技术人员确定的待治疗的疾病、病况或病症的方式施用。在上述实施例的任一项中,将本文所述的工程免疫细胞或单位剂量经静脉内、腹膜内、瘤内、脑内、骨髓、淋巴结或脑脊液施用,以便遇到靶细胞(例如,癌症细胞)。组合物的适当剂量、适当持续时间和给药频率取决于诸如患者状况等因素;疾病、病况或病症的大小、类型和严重程度;活性成分的特定形式;以及给药方法。
[0222]
对于治疗性宿主细胞,组合物或单位剂量中的细胞数量为至少一个细胞(例如,一个sox2特异性cd8
+
t细胞亚群;一个sox2特异性cd4
+
t细胞亚群),或者更典型地大于102个细胞,例如,高达106个、高达107个、高达108个细胞、高达109个细胞、或超过10
10
个细胞,如10
11
个细胞。在某些实施例中,细胞以约106至约10
10
个细胞/m2的范围施用,优选以约105至约
10
11
个细胞/m2范围施用。细胞的数量将取决于组合物的最终用途以及其中包含的细胞的类型。例如,经修饰以含有对特定抗原有特异性的融合蛋白的细胞将包含含有至少30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或更多这样的细胞的细胞群。对于本文提供的用途,细胞的体积通常为1升或更小、500毫升或更小、250毫升或更小、或100毫升或更小。在实施例中,所需细胞的密度通常大于104个细胞/ml,并且通常大于107个细胞/ml,通常为108个细胞/ml或更大。细胞可以以单次输注或在一段时间内多次输注的方式施用。临床相关数量的免疫细胞可以分配到累积等于或超过106、107、108、109、10
10
或10
11
个细胞的多次输注中。在某些实施例中,单位剂量的修饰免疫细胞可以与来自同种异体供体的造血干细胞共同给药(例如,同时(simultaneously)或同时期(contemporaneously))。
[0223]
还考虑了药物组合物(即组合物),其包含本文公开的sox2特异性结合蛋白、多核苷酸、载体、宿主细胞、融合蛋白或免疫原性组合物以及药学上可接受的载体、稀释剂或赋形剂。合适的赋形剂包括水、盐水、葡萄糖、甘油等及其组合。在实施例中,包含本文公开的融合蛋白或宿主细胞的组合物进一步包含合适的输注介质。合适的输注介质可以是任何等渗介质制剂,通常是生理盐水、normosol r(abbott)或plasma-lyte a(baxter)、5%葡萄糖水溶液,可以使用林格氏乳酸盐。输注介质可以补充有人血清白蛋白或其他人血清成分。
[0224]
如医学领域的技术人员所确定的,药物组合物可以以适合于待治疗(或预防)的疾病或病症的方式施用。组合物的适当剂量、适当持续时间和给药频率将取决于诸如患者的健康状况、患者的体型(即重量、质量或身体面积)、患者状况的类型和严重程度、活性成分的特定形式和给药方法。通常,适当剂量和治疗方案提供的组合物的量足以提供治疗和/或预防益处(如本文所述,包括改善的临床结果,如更频繁的完全或部分缓解,或更长的无病和/或总生存期,或症状严重程度的减轻)。
[0225]
如本文所述,药物组合物的有效量是指在所需的剂量和时间段内足以实现所需临床结果或有益治疗的量。可以在一次或多次给药中递送有效量。如果对已知或确认患有疾病或疾病状态的受试者给药,则术语“治疗量”可用于指代治疗,而“预防有效量”可用于描述将有效量施用于易感或有发展疾病或疾病状态(例如,复发)风险的受试者作为预防过程。
[0226]
通常,抗体或抗原结合片段的治疗有效剂量为(对于70kg哺乳动物)约0.001mg/kg(即0.07mg)至约100mg/kg(即7.0g);优选治疗有效剂量为(对于70kg哺乳动物)约0.01mg/kg(即0.7mg)至约50mg/kg(即3.5g);更优选治疗有效剂量为(对于70kg哺乳动物)约1mg/kg(即70mg)至约25mg/kg(即1.75g)。对于本公开的多核苷酸、载体、宿主细胞和相关组合物,治疗有效剂量可以不同于抗体或抗原结合片段。
[0227]
在一些实施例中,提供了一种载体,其包含编码tcr模拟抗体或抗原结合片段或其部分的dna质粒构建体(例如,所谓的“dmab”;参见,例如,muthumani et al.,j infect dis.214(3):369-378(2016);muthumani et al.,hum vaccin immunother 9:2253-2262(2013);flingai et al.,sci rep.5:12616(2015);和elliott et al.,npj vaccine s18(2017),其编码抗体的dna构建体和相关的使用方法,包括其给药,通过引用并入本文)。在某些实施例中,dna质粒构建体包含编码抗体或抗原结合片段的重链和轻链(或vh和vl)的单个开放阅读框,其中编码重链的序列和编码轻链的序列任选地通过编码蛋白酶切割位点
的多核苷酸和/或通过编码自切割肽的多核苷酸分离。在一些实施例中,抗体或抗原结合片段的取代组分由包含在单个质粒中的多核苷酸编码。在其他实施例中,抗体或抗原结合片段的取代组分由包含在两个或多个质粒中的多核苷酸编码(例如,第一质粒包含编码重链、vh或vh+ch的多核苷酸,并且第二质粒包含编码同源轻链、vl或vl+cl的多核苷酸)。示例性表达载体是pvax1,可从获得。本公开的dna质粒可以通过例如电穿孔(例如肌内电穿孔)或用合适的制剂(例如透明质酸酶)递送给受试者。
[0228]
本文所述的药物组合物可以采用单位剂量或多剂量容器呈现,例如密封安瓿或小瓶。这样的容器可以被冷冻以保持制剂的稳定性,直到输注到患者体内。在某些实施例中,单位剂量包括本文所述的sox2特异性免疫细胞,其剂量为约107个细胞/m2至约10
11
个细胞/m2。开发合适的给药和治疗方案,用于在各种治疗方案中使用本文所述的特定组合物,包括例如胃肠外或静脉内给药或制剂。
[0229]
如果所述受试者组合物是肠胃外给药,则所述组合物还可以包括无菌水性或油性溶液或悬浮液。合适的无毒肠胃外可接受的稀释剂或溶剂包括水、林格氏溶液、等渗盐溶液、1,3-丁二醇、乙醇、丙二醇或与水混合的聚己二醇。水溶液或悬浮液可进一步包含一种或多种缓冲剂,例如乙酸钠、柠檬酸钠、硼酸钠或酒石酸钠。当然,用于制备任何剂量单位制剂的任何材料都应该是药学纯的,并且在所使用的量上基本是无毒的。此外,活性化合物可以掺入缓释制剂和制剂中。如本文所用,剂量单位形式是指适合作为待治疗受试者的单一剂量的物理离散单位;每个单元可以包含预定量的工程化免疫细胞或活性化合物,其经计算为与适当的药物载体结合产生所需的效果。
[0230]
通常,适当的剂量和治疗方案以足以提供益处的量提供活性分子或细胞。与未治疗的受试者相比,可以通过在治疗的受试者中建立改善的临床结果(例如,更频繁的缓解、完全或部分或更长的无病生存期)来监测这种反应。对肿瘤蛋白的预先存在的免疫反应的增加通常与临床结果的改善相关。这种免疫反应通常可以使用标准的增殖、细胞毒性或细胞因子试验来评估,这些都是常规的。
[0231]
对于预防性使用,剂量应足以预防、延迟与疾病或病症相关的疾病的发作或减轻其严重程度。根据本文所述方法施用的免疫原性组合物的预防益处可以通过进行临床前(包括体外和体内动物研究)和临床研究并通过适当的统计、生物学和临床方法和技术分析从中获得的数据来确定,所有这些都可以由本领域技术人员容易地实践。
[0232]
如本文所用,组合物的施用是指将其递送至受试者,而不管递送途径或方式。给药可以连续或间歇进行,也可以胃肠外给药。给药可以用于治疗已经确认为具有公认病症、疾病或疾病状态的受试者,或用于治疗易患或有风险发展此类病症、疾病或疾病状态的受试者。与辅助疗法的共同给药可包括以任何顺序和以任何给药方案同时和/或顺序递送多种药剂(例如,具有一种或多种细胞因子的工程化免疫细胞;免疫抑制疗法,例如钙调神经磷酸酶抑制剂、皮质类固醇、微管抑制剂、低剂量的霉酚酸前药、或其任何组合)。
[0233]
在某些实施例中,向受试者施用多个剂量的本文所述的结合蛋白、多核苷酸、载体、宿主细胞或组合物,其可以以约两周至约四周的施用间隔施用。
[0234]
本公开的治疗或预防方法可以作为治疗过程或方案的一部分施用于受试者,其可以包括在施用本公开的单位剂量、细胞或组合物之前或之后的额外治疗。例如,在某些实施例中,接受单位剂量宿主细胞的受试者正在接受或先前已经接受过造血细胞移植(hct;包
括清髓性和非清髓性hct)。进行hct的技术和方案是本领域已知的,并且可以包括移植任何合适的供体细胞,例如来源于脐带血、骨髓或外周血的细胞、造血干细胞、动员的干细胞或来自羊水的细胞。因此,在某些实施例中,本公开的宿主细胞可以在修饰的hct疗法中与造血干细胞一起施用或在其之后不久施用。
[0235]
在进一步的实施例中,受试者在接受sox2特异性免疫细胞或hct之前已经接受过淋巴清除性化学疗法。在某些实施例中,淋巴清除性化学疗法包括包含环磷酰胺、氟达拉滨(fludarabine)、抗胸腺细胞球蛋白、或其组合的调理方案。
[0236]
在某些实施例中,受试者先前接受过手术;放射疗法或化学疗法中的一种或多种,所述疗法包括本文所述或本领域已知的那些疗法。在某些实施例中,例如,化学疗法包括长春新碱(vincristine)、顺铂(cisplatin)、环磷酰胺(cyclophosphamide)、非格司亭(filgrastim)、依托泊苷(etoposide)、噻替帕(thiotepa)、或其任何组合。
[0237]
根据本公开的方法可以进一步包括施用一种或多种额外的药剂以在联合疗法中治疗疾病或病症。例如,在某些实施例中,联合疗法包括将本公开的组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与免疫检查点抑制剂(同期(concurrently)、同时(simultaneously)或依次)一起施用。在一些实施例中,联合疗法包括将组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与刺激性免疫检查点试剂的激动剂一起施用。在进一步的实施例中,联合治疗包括将组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与二级疗法一起施用,例如化学治疗剂、放射疗法、手术、抗体、或其任何组合。
[0238]
如本文所用,术语“免疫抑制剂(immune suppression agent)”或“免疫抑制剂(immunosuppression agent)”是提供抑制信号以帮助控制或抑制免疫反应的一种或多种细胞、蛋白质、分子、化合物或复合物。例如,免疫抑制剂包括部分或完全阻断免疫刺激;减少、预防或延迟免疫激活;或增加、激活或上调免疫抑制的那些分子。靶向(例如,用免疫检查点抑制剂)的示例性免疫抑制剂包括pd-1、pd-l1、pd-l2、lag3、ctla4、b7-h3、b7-h4、cd244/2b4、hvem、btla、cd160、tim3、gal9、kir、pvr1g(cd112r)、pvrl2、腺苷、a2ar、免疫抑制细胞因子(例如il-10、il-4、il-1ra、il-35)、ido、精氨酸酶、vista、tigit、lair1、ceacam-1、ceacam-3、ceacam-5、treg细胞、或其任何组合。免疫抑制剂(也称为免疫检查点抑制剂)可以是化合物、抗体、抗体片段或融合多肽(例如fc融合,如ctla4-fc或lag3-fc)、反义分子、核酶或rnai分子、或低分子量有机分子。
[0239]
在本文所公开的任何实施例中,一种方法可以单独包括组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与一种或多种以下免疫抑制组分中任一种的抑制剂,单独地或以任何组合。在某些实施例中,组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与pd-1抑制剂组合使用,例如pd-1特异性抗体或其结合片段,例如匹地利珠单抗(pidilizumab)、纳武单抗(nivolumab)、派姆单抗(pembrolizumab)、medi0680(原amp-514)、amp-224、bms-936558、或其任何组合。在进一步的实施例中,本公开的组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与pd-l1特异性抗体或其结合片段组合使用,例如bms-936559、度伐鲁单抗(durvalumab)(medi4736)、阿特朱单抗(atezolizumab)(rg7446)、阿维单抗(avelumab)(msb0010718c)、mpdl3280a、或其任何组合。在某些实施例中,本公开的组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与lag3抑制剂组合使用,例如lag525、imp321、imp701、9h12、bms-986016、或其任何组合。在某些实施例中,
组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与ctla4抑制剂组合使用。在特定实施例中,sox2特异性免疫细胞与ctla4特异性抗体或其结合片段组合使用,例如,伊匹单抗(ipilimumab)、替西木单抗(tremelimumab)、ctla4-ig融合蛋白(例如,阿巴西普(abatacept)、贝拉西普(belatacept))、或其任何组合。在某些实施例中,组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与b7-h3特异性抗体或其结合片段组合使用,例如依诺妥珠单抗(enoblituzumab)(mga271)、376.96、或两者。b7-h4抗体结合片段可以是scfv或其融合蛋白,例如在dangaj et al.,cancer res.73:4820,2013中所述,以及美国专利号9,574,000和pct专利公开号wo/201640724a1和wo 2013/025779a1中所述的那些。
[0240]
在某些实施例中,组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与cd244抑制剂组合使用。
[0241]
在某些实施例中,组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与blta、hvem、cd160或其任何组合的抑制剂组合使用。抗cd-160抗体在例如pct公开号wo 2010/084158中进行了描述。在某些实施例中,组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与tim3抑制剂组合使用。在某些实施例中,组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与gal9抑制剂组合使用。在某些实施例中,组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与腺苷信号传导抑制剂(例如诱饵腺苷受体)组合使用。在某些实施例中,组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与a2ar抑制剂组合使用。在某些实施例中,组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与kir抑制剂如如利瑞鲁单抗(lirilumab)(bms-986015)组合使用。在某些实施例中,组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与抑制性细胞因子(通常是除tgfβ以外的细胞因子)或treg发育或活性的抑制剂组合使用。在某些实施例中,组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与ido抑制剂组合使用,例如左旋-1-甲基色氨酸、依帕司他(epacadostat)(incb024360;liu et al.,blood 115:3520-30,2010)、依布硒啉(ebselen)(terentis et al.,biochem.49:591-600,2010)、吲哚莫德(indoximod)、nlg919(mautino et al.,american association for cancer research 104th annual meeting 2013;apr 6-10,2013)、1-甲基-色氨酸(1-mt)-替拉扎明、或其任何组合。在某些实施例中,组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与精氨酸酶抑制剂组合使用,例如n(ω)-硝基-l-精氨酸甲酯(l-name)、n-ω-羟基-nor-l-精氨酸(nor-noha)、l-noha、2(s)-氨基-6-溴己酸(abh)、s-(2-硼酸基乙基)-l-半胱氨酸(bec)、或其任何组合。在某些实施例中,组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与vista抑制剂如ca-170(curis,lexington,ma)组合使用。在某些实施例中,组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与tigit抑制剂(例如,如com902(compugen,toronto,ontario canada))、cd155抑制剂(例如,如com701(compugen))、或两者组合使用。在某些实施例中,组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与pvrig、pvrl2、或两者的抑制剂组合使用。抗pvrig抗体描述于例如pct公开号wo 2016/134333中。抗pvrl2抗体描述于例如pct公开号wo 2017/021526中。在某些实施例中,组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与lair1抑制剂组合使用。在某些实施例中,组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与ceacam-1、ceacam-3、ceacam-5、或其任何组合的抑制剂组合使用。
[0242]
在某些实施例中,组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)与增加刺激性免疫检查点分子的活性的试剂(即激动剂)组合使用。例如,组合物可与cd137(4-1bb)激动剂(例如,如urelumab)、cd134(ox-40)激动剂,例如,medi6469、medi6383或medi0562)、来那度胺(lenalidomide)、泊马度胺(pomalidomide)、cd27激动剂(例如,如cdx-1127)、cd28激动剂(例如,如tgn1412、cd80或cd86)、cd40激动剂(例如,如cp-870,893、rhucd40l或sgn-40)、cd122激动剂(例如,如il-2)、gitr激动剂(例如,如pct专利公开号wo 2016/054638中描述的人源化抗gitr单克隆抗体)、icos激动剂(cd278)(例如,如gsk3359609、mab 88.2、jtx-2011、icos 145-1、icos 314-8、或其任何组合)。在本文所公开的任何实施例中,一种方法可以包括施用组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)和一种或多种刺激性免疫检查点分子激动剂(包括前述任何一种),单独地或以任何组合。
[0243]
在某些实施例中,联合治疗包括组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)和包含以下一种或多种的二级疗法:对由非炎症实体瘤的癌抗原具有特异性的抗体或其抗原结合片段、放射治疗、手术、化学治疗剂、细胞因子、rnai或其任何组合表达。
[0244]
在某些实施例中,联合治疗包括施用组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物),并进一步给予放射治疗或手术。放射疗法在本领域是众所周知的,并且包括x射线疗法,例如γ-辐射和放射性药物疗法。适合治疗受试者的特定癌症的手术和手术技术是本领域普通技术人员众所周知的。
[0245]
在某些实施例中,联合治疗方法包括施用组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)和进一步施用化学治疗剂。化学治疗剂包括但不限于染色质功能抑制剂、拓扑异构酶抑制剂、微管抑制剂、dna损伤剂、抗代谢剂(如叶酸拮抗剂、嘧啶类似物、嘌呤类似物和糖修饰的类似物)、dna合成抑制剂、dna相互作用剂(如嵌入剂)和dna修复抑制剂。示例性化学治疗剂包括但不限于以下组:抗代谢/抗癌剂,例如嘧啶类似物(5-氟尿嘧啶、氟尿苷、卡培他滨、吉西他滨和阿糖胞苷)和嘌呤类似物、叶酸拮抗剂和相关抑制剂(巯基嘌呤、硫鸟嘌呤,喷司他丁和2-氯脱氧腺苷(克拉屈滨));抗增殖/抗有丝分裂剂,包括天然产物,如长春花生物碱(长春花碱(vinbalstine)、长春新碱(vincristine)和长春瑞滨)、微管破坏剂,如紫杉烷(紫杉醇(paclitaxel)、多西他赛)、新长春碱(vincristin)、长春花碱(vinbalstin)、诺考达唑、埃博霉素和异长春花碱、表鬼臼毒素(epidipodophyllotoxin)(依托泊苷、替尼泊苷)、dna损伤剂(放线菌素、安吖啶、蒽环类、博来霉素、白消安、喜树碱、卡铂、苯丁酸氮芥、顺铂、环磷酰胺(cyclophosphamide)、cytoxan、更生霉素(dactinomycin)、柔红霉素、多柔比星(doxorubicin)、表柔比星(epirubicin)、六甲密胺、奥沙利铂、异磷酰胺、美法仑、二氯甲基二乙胺(merchlorehtamine)、丝裂霉素、米托蒽醌、亚硝基脲、普卡霉素、丙卡巴肼、紫杉醇(taxol)、紫杉特尔(taxotere)、替莫唑胺、替尼泊甙、三亚乙基硫代磷酰胺和依托泊苷(vp 16));抗生素,如更生霉素(放线菌素d)、柔红霉素、多柔比星(阿霉素)、伊达比星、蒽环类、米托蒽醌、博来霉素、普卡霉素(光辉霉素)和丝裂霉素;酶(l-天冬酰胺酶,其系统地代谢l-天冬酰胺并剥夺不具有合成自身天冬酰胺能力的细胞);抗血小板剂;抗增殖/抗有丝分裂烷化剂,如氮芥(二氯甲基二乙胺、环磷酰胺和类似物、美法仑、苯丁酸氮芥)、乙烯亚胺和甲基三聚氰胺(六甲三聚氰胺和噻替帕)、烷基磺酸盐-白消安、亚硝基脲(卡莫司汀(bcnu)和类似物、链脲佐菌素)、四氮烯-达卡巴嗪(dtic);
抗增殖/抗有丝分裂抗代谢物,如叶酸类似物(甲氨蝶呤);铂配位络合物(顺铂、卡铂)、丙卡巴肼、羟基脲、米托坦、氨格鲁米特;激素、激素类似物(雌激素、他莫昔芬、戈舍瑞林、比卡鲁胺、尼鲁米特)和芳香酶抑制剂(来曲唑、阿那曲唑);抗凝剂(肝素、合成肝素盐和其他凝血酶抑制剂);纤溶剂(如组织纤溶酶原激活剂、链激酶和尿激酶)、阿司匹林、双嘧达莫、噻氯匹定、氯吡格雷、阿昔单抗;抗迁移剂;抗分泌剂(breveldin);免疫抑制剂(环孢菌素、他克莫司(fk-506)、西罗莫司(雷帕霉素)、硫唑嘌呤、霉酚酸酯);抗血管生成化合物(tnp470、染料木黄酮)和生长因子抑制剂(血管内皮生长因子(vegf)抑制剂、成纤维细胞生长因子(fgf)抑制剂);血管紧张素受体阻滞剂;一氧化氮供体;反义寡核苷酸;抗体(曲妥珠单抗、利妥昔单抗);嵌合抗原受体;细胞周期抑制剂和分化诱导剂(维甲酸);mtor抑制剂、拓扑异构酶抑制剂(多柔比星(阿霉素)、安吖啶、喜树碱、柔红霉素、更生霉素、替尼泊苷、表柔比星、依托泊苷、伊达比星、伊立替康(cpt-11)和米托蒽醌、拓扑替康、伊立替康)、皮质类固醇(可的松、地塞米松、氢化可的松、甲泼尼龙(methylpednisolone)、泼尼松和泼尼松龙(prenisolone));生长因子信号转导激酶抑制剂;线粒体功能障碍诱导剂,毒素如霍乱毒素、蓖麻毒素、假单胞菌外毒素、百日咳博德特氏菌腺苷酸环化酶毒素或白喉毒素,以及半胱天冬酶激活剂;和染色质干扰物。
[0246]
细胞因子可用于操纵宿主对抗癌活性的免疫反应。参见,例如,floros&tarhini,semin.oncol.42(4):539-548,2015。可用于促进免疫抗癌或抗肿瘤反应的细胞因子包括,例如ifn-α、il-2、il-3、il-4、il-10、il-12、il-13、il-15、il-16、il-17、il-18、il-21、il-24和gm-csf,单独地或与本公开的组合物(例如结合蛋白、多核苷酸、载体、宿主细胞或组合物)的任何组合。
[0247]
本公开还提供了以下非限制性实施例:
[0248]
实施例1.一种分离的结合蛋白,其能够与sox2肽抗原:hla复合物结合,其中所述sox2肽抗原包含或由seq id no.:5、2、3、4、6或7中所述的氨基酸序列组成,并且其中,任选地,所述结合包含特异性结合。
[0249]
实施例2.实施例1中所述的结合蛋白,其中所述sox2肽抗原包含或由seq id no.:5所述的氨基酸序列组成。
[0250]
实施例3.实施例1中所述的结合蛋白,其中所述sox2肽抗原包含或由seq id no.:2所述的氨基酸序列组成。
[0251]
实施例4.实施例1中所述的结合蛋白,其中所述sox2肽抗原包含或由seq id no.:3所述的氨基酸序列组成。
[0252]
实施例5.实施例1中所述的结合蛋白,其中所述sox2肽抗原包含或由seq id no.:4所述的氨基酸序列组成。
[0253]
实施例6.实施例1中所述的结合蛋白,其中所述sox2肽抗原包含或由seq id no.:6所述的氨基酸序列组成。
[0254]
实施例7.实施例1中所述的结合蛋白,其中所述sox2肽抗原包含或由seq id no.:7所述的氨基酸序列组成。
[0255]
实施例8.实施例1-7中任一项所述的结合蛋白,其中所述hla包括hla-a*02:01。
[0256]
实施例9.实施例1-8中任一项所述的结合蛋白,其包含免疫球蛋白超家族可变结构域。
[0257]
实施例10.实施例1-9中任一项所述的结合蛋白,其包含tcrα链可变结构域(vα)和/或tcrβ链可变结构域(vβ)。
[0258]
实施例11.实施例1-9中任一项所述的结合蛋白,其包含tcr模拟抗体的重链可变结构域(vh)和/或轻链可变结构域(vl)。
[0259]
实施例12.实施例1-11中任一项所述的结合蛋白,其中所述结合蛋白包含:(i)seq id nos.:52、53、100、101、16、17、28、29、40、41、64、65、76、77、88、89、112、113、124、125、136、137、148和149中任一项中所述的氨基酸序列,或其包含一个、两个或三个氨基酸取代的变体,其中所述氨基酸序列任选为cdr3β;(ii)seq id nos.:51、99、15、27、39、63、75、87、111、123、135和147中任一项所述的氨基酸序列,或其包含一个、两个或三个氨基酸取代的变体,其中所述氨基酸序列任选为cdr2β;(iii)seq id nos.:50、98、14、26、38、62、74、86、110、122、134和146中任一项所述的氨基酸序列,或其包含一个、两个或三个氨基酸取代的变体,其中所述氨基酸序列任选为cdr1β;(iv)seq id nos.:57、58、105、106、21、22、33、34、45、46、69、70、81、82、93、94、117、118、129、130、141、142、153和154中任一项所述的氨基酸序列,或其包含一个、两个或三个氨基酸取代的变体,其中所述氨基酸序列任选为cdr3α;(v)seq id nos.:56、104、20、32、44、68、80、92、116、128、140和152中任一项中所述的氨基酸序列,或其包含一个、两个或三个氨基酸取代的变体,其中所述氨基酸序列任选为cdr2α;和/或(vi)seq id nos.:55、103、19、31、43、67、79、91、115、127、139和151中任一项所述的氨基酸序列,或其包含一个、两个或三个氨基酸取代的变体,其中所述氨基酸序列任选为cdr1α。
[0260]
实施例13.实施例1-10和12中任一项所述的结合蛋白,其包含:(1)包含cdr1α、cdr2α和cdr3α的tcr vα;和(2)包含cdr1β、cdr2β和cdr3β的tcr vβ,其中所述cdr1α、cdr2α、cdr3α、cdr1β、cdr2β和cdr3β为如下各项序列所述:(i)分别为seq id nos.:55、56、57或58、50、51、和52或53;(ii)分别为seq id nos.:103、104、105或106、98、99、和100或101;(iii)分别为seq id nos.:19、20、21或22、14、15、和16或17;(iv)分别为seq id nos.:31、32、33或34、26、27、和28或29;(v)分别为seq id nos.:43、44、45或46、38、39、和40或41;(vi)分别为seq id nos.:67、68、69或70、62、63、和64或65;(vii)分别为seq id nos.:79、80、81或82、74、75、和76或77;(viii)分别为seq id nos.:91、92、93或94、86、87、和88或89;(ix)分别为seq id nos.:115、116、117或118、110、111、和112或113;(x)分别为seq id nos.:127、128、129或130、122、123、和124或125;(xi)分别为seq id nos.:分别为139、140、141或142、134、135、和136或137;或(xii)分别为seq id nos.:151、152、153或154、146、147、和148或149。
[0261]
实施例14.实施例10和12-13中任一项所述的结合蛋白,其中所述vα包含或由与seq id nos.:54、102、18、30、42、66、78、90、114、126、138和150中任一项所述的氨基酸序列具有至少80%、至少85%、至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%或至少99%同一性的氨基酸序列组成。
[0262]
实施例15.实施例10和12-14中任一项所述的结合蛋白,其中所述vβ包含或由与seq id nos.:49、97、13、25、37、61、73、85、109、121、133和145中任一项所述的氨基酸序列具有至少80%、至少85%、至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%或至少99%同一性的氨基酸序列组成。
[0263]
实施例16.实施例10和12-15中任一项所述的结合蛋白,其包含vα和vβ,所述vα和vβ包含或由与下述氨基酸序列具有至少80%、至少85%、至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%或至少99%同一性的氨基酸序列组成:(i)分别为seq id nos.:54和49;(ii)分别为seq id nos.:102和97;(iii)分别为seq id nos.:18和13;(iv)分别为seq id nos.:30和25;(v)分别为seq id nos.:42和37;(vi)分别为seq id nos.:66和61;(vii)分别为seq id nos.:78和73;(viii)分别为seq id nos.:90和85;(ix)分别为seq id nos.:114和109;(x)分别为seq id nos.:126和121;(xi)分别为seq id nos.:138和133;或(xii)分别为seq id nos.:150和145。
[0264]
实施例17.实施例10和12-16中任一项所述的结合蛋白,其包含vα和vβ,所述vα和vβ包含或由根据以下各项的氨基酸序列组成:(i)分别为seq id nos.:54和49;(ii)分别为seq id nos.:102和97;(iii)分别为seq id nos.:18和13;(iv)分别为seq id nos.:30和25;(v)分别为seq id nos.:42和37;(vi)分别为seq id nos.:66和61;(vii)分别为seq id nos.:78和73;(viii)分别为seq id nos.:90和85;(ix)分别为seq id nos.:114和109;(x)分别为seq id nos.:126和121;(xi)分别为seq id nos.:138和133;或(xii)分别为seq id nos.:150和145。
[0265]
实施例18.实施例10和12-17中任一项所述的结合蛋白,其中所述结合蛋白包含在以下各项中:与seq id nos.:48、96、12、24、36、60、72、84、108、120、132和144中任一项所述的氨基酸序列具有至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%或至少99%同一性的氨基酸序列、或包含或由seq id nos.:48、96、12、24、36、60、72、84、108、120、132和144中任一项所述的氨基酸序列组成的氨基酸序列。
[0266]
实施例19.实施例1-11中任一项所述的结合蛋白,其中所述结合蛋白包含:(i)t细胞的tcr的cdr3β、cdr2β和/或cdr1β,所述t细胞来自:供体1系1、供体1系3、供体2系8、供体2系1、供体2系13、供体2系11或供体2系19;和/或(ii)t细胞的tcr的cdr3α、cdr2α和/或cdr1α,所述t细胞来自:供体1系1、供体1系3、供体2系8、供体2系1、供体2系13、供体2系11或供体2系19。
[0267]
实施例20.实施例1-11中任一项所述的结合蛋白,其中所述结合蛋白包含:(i)与t细胞的tcr的vα具有至少90%的氨基酸同一性的vα,所述t细胞来自:供体1系1、供体1系3、供体2系8、供体2系1、供体2系13、供体2系11或供体2系19;和/或(ii)与t细胞的tcr的vβ具有至少90%的氨基酸同一性的vβ,所述t细胞来自:供体1系1、供体1系3、供体2系8、供体2系1、供体2系13、供体2系11或供体2系19,条件是(a)至少三个或四个cdr没有突变;(b)具有突变的cdr仅具有至多两个氨基酸取代、至多连续的五个氨基酸缺失、或其组合;和(c)所述结合蛋白保留其与sox2肽:hla复合物结合的能力。
[0268]
实施例21.实施例1-20中任一项所述的结合蛋白,其进一步包含tcrβ-多肽恒定结构域(cβ)、tcrα-多肽恒定域(cα)或两者,其中,任选地,(1)所述vβ和所述cβ一起包括tcrβ链和/或所述vα和所述cα一起包括tcrα链,和/或(2)所述cβ包含或由以下各项组成:与seq id no.:156或157中所述氨基酸序列具有至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%或至少99%同一性的氨基酸序列、或包含或由seq id no.:156或157中所述的氨基酸序列组成的氨基酸序列,和/或所述cα包含或由以
(pnscp2)-(pncd8β);或(vi)(pncd8β)-(pnscp1)-(pnbp)-(pnscp2)-(pncd8α),其中pncd8α是编码包含cd8共受体α链的细胞外部分的多肽的多核苷酸,其中pncd8β是编码包含cd8共受体α链的细胞外部分的多肽的多核苷酸,其中pnbp是编码结合蛋白的多核苷酸,并且其中pnscp1和pnscp2各自独立地是编码自切割肽的多核苷酸,其中所述多核苷酸和/或所述编码的自切割肽任选地相同或不同。
[0284]
实施例36.实施例30-35中任一项所述的多核苷酸,其中所述编码的结合蛋白包含tcrα链和tcrβ链,其中所述多核苷酸包含编码自切割肽的多核苷酸,所述编码自切割肽的多核苷酸位于编码tcrα链的多核苷酸和编码tcrβ链的多核苷酸之间。
[0285]
实施例37.实施例36所述的多核苷酸,其包含在框内可操作地连接的:
[0286]
(i)(pncd8α)-(pnscp1)-(pncd8β)-(pnscp2)-(pntcrβ)-(pnscp3)-(pntcrα);
[0287]
(ii)(pncd8β)-(pnscp1)-(pncd8α)-(pnscp2)-(pntcrβ)-(pnscp3)-(pntcrα);
[0288]
(iii)(pncd8α)-(pnscp1)-(pncd8β)-(pnscp2)-(pntcrα)-(pnscp3)-(pntcrβ);
[0289]
(iv)(pncd8β)-(pnscp1)-(pncd8α)-(pnscp2)-(pntcrα)-(pnscp3)-(pntcrβ);
[0290]
(v)(pntcrβ)-(pnscp1)-(pntcrα)-(pnscp2)-(pncd8α)-(pnscp3)-(pncd8β);
[0291]
(vi)(pntcrβ)-(pnscp1)-(pntcrα)-(pnscp2)-(pncd8β)-(pnscp3)-(pncd8α);
[0292]
(vii)(pntcrα)-(pnscp1)-(pntcrβ)-(pnscp2)-(pncd8α)-(pnscp3)-(pncd8β);或
[0293]
(viii)(pntcrα)-(pnscp1)-(pntcrβ)-(pnscp2)-(pncd8β)-(pnscp3)-(pncd8α),其中pncd8α是编码包含cd8共受体α链的细胞外部分的多肽的多核苷酸,其中pncd8β是编码包含cd8共受体α链的细胞外部分的多肽的多核苷酸;其中pntcrα是编码tcrα链的多核苷酸,其中pntcrβ是编码tcrβ链的多核苷酸,并且其中pnscp1、pnscp2和pnscp3各自独立地为编码自切割肽的多核苷酸,其中所述多核苷酸和/或编码的自切割肽任选相同或不同。
[0294]
实施例38.实施例30-37中任一项所述的多核苷酸,其中所述多核苷酸包含dna、rna(任选为mrna)、或两者。
[0295]
实施例39.实施例38所述的多核苷酸,其包含dna。
[0296]
实施例40.实施例30-39中任一项所述的多核苷酸,其中(1)所述多核苷酸编码以下各项:与seqidnos.:48、96、12、24、36、60、72、84、108、120、132和144中任一项所述的氨基酸序列具有至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性的氨基酸序列、或包含或由seqidnos.:48、96、12、24、36、60、72、84、108、120、132和144中任一项所述的氨基酸序列组成的氨基酸序列;和/或(2)所述多核苷酸包含与seqidnos.:47、95、11、23、35、47、59、71、83、107、119、131和143中任一项所述的核苷酸序列具有至少70%、至少75%、至少80%、至少85%、至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性的多核苷酸、包含或由seqidnos.:47、95、11、23、35、47、59、71、83、107、119、131和143中任一项所述的核苷酸序列组成。
[0297]
实施例41.一种载体,其包含实施例30-40中任一项所述的多核苷酸。
[0298]
实施例42.实施例41所述的载体,其中所述载体包括病毒载体。
[0299]
实施例43.实施例42所述的载体,其中所述病毒载体包括慢病毒载体或γ-逆转录病毒载体。
[0300]
实施例44.实施例41-43中任一项所述的载体,其中所述载体能够将所述多核苷酸递送至宿主细胞。
[0301]
实施例45.实施例44所述的载体,其中所述宿主细胞是造血祖细胞或人类免疫系统细胞。
[0302]
实施例46.实施例45所述的载体,其中所述人类免疫系统细胞是cd4
+
t细胞、cd8
+
t细胞、cd4-cd8-双阴性t细胞、γδt细胞、自然杀伤细胞、自然杀伤t细胞、巨噬细胞、单核细胞、树突状细胞、或其任何组合。
[0303]
实施例47.实施例46所述的载体,其中所述t细胞是幼稚t细胞、中央记忆t细胞、效应记忆t细胞、或其任何组合。
[0304]
实施例48.一种宿主细胞,其包含实施例30-40中任一项所述的多核苷酸和/或实施例41-47中任一项所述的载体,和/或其表达实施例1-29中任一项所述的结合蛋白,其中所述多核苷酸、载体或结合蛋白任选与宿主细胞异源。
[0305]
实施例49.实施例48所述的宿主细胞,其中所述宿主细胞包括造血祖细胞和/或免疫细胞,任选地是人类免疫细胞。
[0306]
实施例50.实施例49所述的宿主细胞,其中所述宿主细胞包括t细胞、nk细胞、nk-t细胞、树突状细胞、巨噬细胞、单核细胞、b细胞、浆细胞、或其任何组合。
[0307]
实施例51.实施例50所述的宿主细胞,其中所述宿主细胞包括cd4
+
t细胞、cd8
+
t细胞、cd4-cd8-双阴性t细胞、γδt细胞、或其任何组合,
[0308]
其中,任选地,所述宿主细胞包含cd4+t细胞和cd8
+
t细胞,其中,进一步任选地,cd4
+
t细胞、cd8
+
t细胞或两者包含(i)编码包含cd8共受体α链的细胞外部分的多肽的多核苷酸,其中,任选地,编码的多肽是或包含cd8共受体α链;(ii)编码包含cd8共受体β链的细胞外部分的多肽的多核苷酸,其中,任选地,编码的多肽是或包含cd8共受体β链;或(iii)(i)的多核苷酸和(ii)的多核苷酸。
[0309]
实施例52.实施例50或51所述的宿主细胞,其中所述宿主细胞包括cd8
+
t细胞和/或cd4
+
t细胞。
[0310]
实施例53.实施例48-52中任一项所述的宿主细胞,其中所述宿主细胞包含pd-1基因;lag3基因;tim3基因;ctla4基因;hla组分基因;tigit基因;tcr组分基因、fasl基因、或其任何组合的染色体基因敲除。
[0311]
实施例54.实施例53所述的宿主细胞,其中所述染色体基因敲除包括hla组分基因的敲除,所述hla组分基因选自α1巨球蛋白基因、α2巨球蛋白基因、α3巨球蛋白基因、β1微球蛋白基因或β2微球蛋白基因。
[0312]
实施例55.实施例53或54所述的宿主细胞,其中所述染色体基因敲除包括tcr组分基因的敲除,所述tcr组分基因选自tcrα可变区基因、tcrβ可变区基因、tcr恒定区基因、或其组合。
[0313]
实施例56.实施例48-55中任一项所述的宿主细胞,其中编码结合蛋白的多核苷酸与宿主细胞异源,并且包含在内源性tcr基因座中。
[0314]
实施例57.实施例48-56中任一项所述的宿主细胞,其进一步包含编码以下各项的异源多核苷酸:(i)安全开关蛋白;(ii)选择标记;(iii)cd8共受体β链;(iv)cd8共受体α链;或(v)其任何组合。
[0315]
实施例58.实施例48-57中任一项所述的宿主细胞,其在sox2抗原:hla复合物存在时产生ifn-γ,其中,任选地,所述sox2抗原:hla复合物在靶细胞的表面上表达。
[0316]
实施例59.实施例48-58中任一项所述的宿主细胞,其中所述结合蛋白能够与ylpgaevpepa(seq id no.:5):hla复合物结合,ifnγ产生pec
50
在6.0至9.0之间(即包括6.0、9.0及其之间的任何值)、在6.0至8.5之间、在6.0至8.0之间、在6.0至7.5之间、在6.0至7.0之间、在6.0至6.5之间、在6.5至9.0之间、在6.5至8.5之间、在6.5至8.0之间、在6.5至7.5之间、在6.5至7.0之间、在7.0至9.0之间、在7.0至8.5之间、在7.0至8.0之间、在7.0至7.5之间、在7.5至9.0之间、在7.5至8.5之间、在7.5至8.0之间、在8.0至9.0之间、在8.0至8.5之间、或在8.2至9.0之间。
[0317]
实施例60.实施例48-59中任一项所述的宿主细胞,其中所述结合蛋白能够与ylpgaevpepa(seq id no.:5):hla复合物结合,ifnγ产生pec
50
为约6.0、约6.1、约6.2、约6.3、约6.4、约6.5、约6.6、约6.7、约6.8、约6.9、约7.0、约7.1、约7.2、约7.3、约7.4、约7.5、约7.6、约7.7、约7.8、约7.9、约8.0、约8.1、约8.2、约8.3、约8.4、约8.5、约8.6、约8.7、约8.8、约8.9、或约9.0。
[0318]
实施例61.实施例48-60中任一项所述的宿主细胞,其中所述结合蛋白能够与ylpgaevpepa(seq id no.:5):hla复合物结合,ifnγ产生pec
50
为6.0或更高。
[0319]
实施例62.实施例48-61中任一项所述的宿主细胞,其中所述结合蛋白能够与ylpgaevpepa(seq id no.:5):hla复合物结合,ifnγ产生pec
50
为6.5或更高。
[0320]
实施例63.实施例48-62中任一项所述的宿主细胞,其中所述结合蛋白能够与ylpgaevpepa(seq id no.:5):hla复合物结合,ifnγ产生pec
50
为7.0或更高。
[0321]
实施例64.实施例48-63中任一项所述的宿主细胞,其中所述结合蛋白能够与ylpgaevpepa(seq id no.:5):hla复合物结合,ifnγ产生pec
50
为7.5或更高。
[0322]
实施例65.实施例48-64中任一项所述的宿主细胞,其中所述结合蛋白能够与ylpgaevpepa(seq id no.:5):hla复合物结合,ifnγ产生pec
50
为8.0或更高。
[0323]
实施例66.实施例48-65中任一项所述的宿主细胞,其中当以下肿瘤细胞系中的任一种或多种的细胞存在时:cfpac1、h441、panc08.13、sw620、sw527、l363、表达hla-a2的mm1r和表达hla-a2的ina6,所述宿主细胞表达cd137,其中,任选地,在宿主细胞与一种或多种所述肿瘤细胞系的一个或多个细胞孵育后,通过宿主细胞的流式细胞术评估cd137的表达。
[0324]
实施例67.实施例48-66中任一项所述的宿主细胞,其中,在样品中存在的多个宿主细胞中,在与以下肿瘤细胞系中的任一种或多种孵育后:cfpac1、h441、panc08.13、sw620、sw527、l363、表达hla-a2的mm1r、表达hla-a2的ina6,5%或更多、10%或更多、15%或更多、20%或更多、25%或更多、30%或更多、35%或更多、40%或更多、45%或更多、50%或更多、55%或更多、60%或更多、65%或更多、70%或更多、75%或更多、或80%或更多的所述多个宿主细胞对cd137的表达呈阳性。
[0325]
实施例68.实施例67所述的宿主细胞,其中所述孵育包括约16小时至约18小时的持续时间,任选地,其中所述孵育包括16至18小时之间的持续时间。
[0326]
实施例69.实施例66-68中任一项所述的宿主细胞,其中,在孵育之前,将在肿瘤细胞系的细胞中增加hla-a2表达的试剂施用于肿瘤细胞系的细胞,其中,任选地,所述试剂包
括ifn-γ。
[0327]
实施例70.一种组合物,其包括:(i)实施例1-29中任一项所述的结合蛋白;(ii)实施例30-40中任一项所述的多核苷酸;(iii)实施例41-47中任一项所述的载体;和/或(iv)实施例48-49中任一项所述的宿主细胞,任选地包含cd4
+
t细胞、cd8
+
t细胞或两者,以及药学上可接受的载剂、赋形剂或稀释剂。
[0328]
实施例71.实施例70所述的组合物,其包括宿主细胞,其中所述宿主细胞包括免疫细胞,任选cd8
+
t细胞和/或cd4
+
t细胞,其中,进一步任选地,cd8
+
t细胞和cd4
+
t细胞以约1:1的比例存在,和/或所述组合物基本上不含幼稚t细胞。
[0329]
实施例72.一种在受试者中用于治疗与sox2抗原表达相关或与sox2表达或活性相关的疾病或病症的方法,所述sox2抗原包含或由根据seq id nos:2-7中任一项的氨基酸序列组成,所述方法包括向所述受试者施用有效量的:(i)实施例1-29中任一项所述的结合蛋白;(ii)实施例30-40中任一项所述的多核苷酸;(iii)实施例41-47中任一项所述的载体;(iv)实施例48-49中任一项所述的宿主细胞;和/或(v)实施例70或71中所述的组合物,从而治疗所述疾病或病况。
[0330]
实施例73.一种在患有与sox2抗原表达相关或与sox2表达或活性相关的疾病或病症的受试者中用于诱导免疫应答和/或在受试者中用于治疗该疾病或病症的方法,所述sox2抗原包含或由根据seq id nos:2-7中任一项的氨基酸序列组成,所述方法包括向所述受试者施用有效量的t细胞,所述t细胞表达tcr,所述tcr与在靶细胞表面上表达的肽:hla复合物特异性结合,其中所述肽包含或由根据seq id nos:2-7中任一项的氨基酸序列组成,且其中所述hla任选为hla-a*02:01。
[0331]
实施例74.实施例1-29中任一项所述的结合蛋白、实施例30-40中任一项所述的多核苷酸、实施例41-47中任一项所述的载体、实施例48-49中任一项所述的宿主细胞;和/或实施例70或71所述的组合物,在受试者中用于治疗与sox2抗原表达相关或与sox2表达或活性相关的疾病或病症的方法中的用途,所述sox2抗原包含或由根据seq id nos:2-7中任一项的氨基酸序列组成。
[0332]
实施例75.实施例1-29中任一项所述的结合蛋白、实施例30-40中任一项所述的多核苷酸、实施例41-47中任一项所述的载体、实施例48-49中任一项所述的宿主细胞;和/或实施例70或71所述的组合物,在制备用于治疗与sox2抗原表达相关或与sox2表达或活性相关的疾病或病症的药物中的用途,所述sox2抗原包含或由根据seq id nos:2-7中任一项的氨基酸序列组成。
[0333]
实施例76.实施例72或73所述的方法、或实施例74或75所述的结合蛋白、多核苷酸、载体、宿主细胞或组合物的用途,其中所述受试者是hla-a*02:01
+
。
[0334]
实施例77.实施例72、73或76或72或73中任一项所述的方法,或实施例74-76中任一项所述的结合蛋白、多核苷酸、载体、宿主细胞或组合物的用途,其中所述疾病或病况为癌症。
[0335]
实施例78.实施例77中所述的方法或实施例77所述的结合蛋白、多核苷酸、载体、宿主细胞或组合物的用途,其中所述癌症包括血液系统恶性肿瘤或实体肿瘤。
[0336]
实施例79.实施例77或78所述的方法或实施例77或78所述的结合蛋白、多核苷酸、载体、宿主细胞或组合物的用途,其中所述癌症包括多发性骨髓瘤、浆细胞白血病、卵巢癌、
胶质瘤、肺癌、颈癌、宫颈癌、或其任何组合。
[0337]
实施例80.实施例72、73或76-79中任一项所述的方法,或实施例74-79中任一项所述的结合蛋白、多核苷酸、载体、宿主细胞或组合物的用途,其中所述受试者是人。
[0338]
实施例81.实施例72、73或76-80中任一项所述的方法,或实施例74-80中任一项所述的结合蛋白、多核苷酸、载体、宿主细胞或组合物的用途,其中所述受试者先前已接受以下的一种或多种:(i)外科手术;(ii)放射疗法;(iii)化学疗法;(iv)造血干细胞移植(hsc);和(v)过继细胞疗法,所述过继细胞疗法任选包含表达car的t细胞,并且其中所述疾病或病症任选地对先前的疗法是难治性的。
[0339]
实施例82.实施例72、73或76-81中任一项所述的方法,或实施例74-81中任一项所述的结合蛋白、多核苷酸、载体、宿主细胞或组合物的用途,其中组合物中所包含的一种或多种宿主细胞是受试者自体的。
[0340]
实施例83.实施例72、73或76-82中任一项所述的方法,或实施例74-81中任一项所述的结合蛋白、多核苷酸、载体、宿主细胞或组合物的用途,进一步包括向受试者施用免疫检查点分子的抑制剂。
[0341]
实施例84.一种免疫原性组合物,其包括:(i)包含或由seq id no:2的氨基酸序列组成的分离的肽或多肽;(ii)包含或由seq id no:3的氨基酸序列组成的分离的肽或多肽;(iii)包含或由seq id no:4的氨基酸序列组成的分离的肽或多肽;(iv)包含或由seq id no:5的氨基酸序列组成的分离的肽或多肽;(v)包含或由seq id no:6的氨基酸序列组成的分离的肽或多肽;(vi)包含或由seq id no:7的氨基酸序列组成的分离的肽或多肽;和/或(vii)与seq id no:2、3、4、5、6或7相比具有1个、2个或3个氨基酸差异的(i)至(vi)中任一项的分离的肽或多肽的变体,其中(i)至(vii)中任一项的分离的肽或多肽不包含分离的全长人sox2。
[0342]
实施例85.实施例84所述的免疫原性组合物,其中(a)(i)至(vii)中任一项的一个或多个拷贝和/或(b)(
ⅰ
)至(vii)中任一种或多种存在于融合多肽中,其中所述融合多肽任选地进一步包含自切割肽的氨基酸序列。
[0343]
实施例86.实施例84或85所述的免疫原性组合物,其中所述免疫原性组合物能够在受试者中引发针对癌症细胞的免疫应答,其中,任选地,所述癌症细胞包括多发性骨髓瘤细胞、浆细胞白血病细胞和/或卵巢癌细胞。
[0344]
实施例87.实施例84-86中任一项所述的免疫原性组合物,其进一步包含佐剂。
[0345]
实施例88.一种分离的多核苷酸,其编码:(i)包含或由seq id no:2的氨基酸序列组成的肽或多肽;(ii)包含或由seq id no:3的氨基酸序列组成的肽或多肽;(iii)包含或由seq id no:4的氨基酸序列组成的肽或多肽;(iv)包含或由seq id no:5的氨基酸序列组成的肽或多肽;(v)包含或由seq id no:6的氨基酸序列组成的肽或多肽;(vi)包含或由seq id no:7的氨基酸序列组成的肽或多肽;和/或(vii)与seq id no:2、3、4、5、6或7相比具有1个、2个或3个氨基酸差异的(i)至(vii)中任一项的肽或多肽的变体,其中所述多核苷酸任选地包含在载体中和/或(i)至(vii)中任一项的肽或多肽不包含全长人sox2。
[0346]
实施例89.实施例88所述的多核苷酸,其中所述多核苷酸经过密码子优化用于在宿主细胞中表达,其中所述宿主细胞任选地是树突状细胞或t细胞。
[0347]
实施例90.一种宿主细胞,其包含实施例88或89所述的多核苷酸,其中所述多核苷
酸与宿主细胞异源,并且其中所述宿主细胞任选地是免疫细胞,并且进一步任选地是专职性抗原呈递细胞。
[0348]
实施例91.实施例90所述的宿主细胞,其中所述宿主细胞是树突状细胞或t细胞。
[0349]
实施例92.一种在受试者中引发针对与sox2表达或活性相关的疾病或病症的免疫应答的方法,所述方法包括向受试者施用实施例1-29中任一项所述的结合蛋白、实施例30-40中任一项所述的多核苷酸、实施例41-48中任一项所述的载体、实施例49-69中任一项所述的宿主细胞、实施例70或71所述的组合物、实施例84-87中任一项所述的免疫原性组合物、实施例88或89所述的多核苷酸和/或实施例90或91所述的宿主细胞。
[0350]
实施例93.一种扩增t细胞群的方法,所述t细胞群与选自以下各项的肽(例如,包含在肽:hla复合物中的肽)结合:(i)包含或由seq id no:2的氨基酸序列组成的肽;(ii)包含或由seq id no:3的氨基酸序列组成的肽;(iii)包含或由seq id no:4的氨基酸序列组成的肽;(iv)包含或由seq id no:5的氨基酸序列组成的肽;(v)包含或由seq id no:6的氨基酸序列组成的肽;和/或(vi)包含或由seq id no:7的氨基酸序列组成的肽,
[0351]
所述方法包括将包含与所述肽结合的一个或多个t细胞的样品与实施例84-87中任一项所述的免疫原性组合物、实施例88或89所述的多核苷酸、实施例90或91所述的宿主细胞和/或抗原呈递细胞接触,所述抗原呈递细胞已与包含或由seq id nos:2-7中任一项所述的氨基酸序列组成的肽或多肽接触。
[0352]
实施例94.一种产生和/或分离t细胞的方法,所述方法包括将包含t细胞的样品(其中所述样品任选地包含外周血细胞)与以下各项接触:(i)实施例84-87中任一项所述的免疫原性组合物;(ii)实施例88或89所述的多核苷酸;(iii)实施例90或91所述的宿主细胞;和/或(iv)抗原呈递细胞(apc),所述抗原呈递细胞表达或已与sox2抗原接触,所述sox2抗原包含或由seq id nos:2-7中任一项所述的氨基酸序列组成,并且任选地从样品中的其他细胞分选t细胞,从而分离和/或产生t细胞。
[0353]
实施例95.通过实施例94所述的方法分离和/或产生的t细胞。
[0354]
本公开还提供了以下非限制性附加实施例:
[0355]
附加实施例1.一种修饰的免疫细胞,其包含编码结合蛋白的异源多核苷酸,所述结合蛋白包括t细胞受体(tcr)α链可变结构域(vα)和tcrβ链可变结构域(vβ),其中所述编码的结合蛋白能够与sox2抗原:hla复合物特异性结合,其中所述sox2抗原包含或由seq id no.:2、3、4、5、6或7中所述的氨基酸序列组成。
[0356]
附加实施例2.附加实施例1所述的修饰的免疫细胞,其中所述hla包括hla-a*02:01。
[0357]
附加实施例3.附加实施例1或2所述的修饰的免疫细胞,其中所述编码的结合蛋白包含:(i)t细胞的tcr的cdr3β、cdr2β和/或cdr1β,所述t细胞来自:供体1系1、供体1系3、供体2系8、供体2系1、供体2系13、供体2系11或供体2系19;和/或(ii)t细胞的tcr的cdr3α、cdr2α和/或cdr1α,所述t细胞来自:供体1系1、供体1系3、供体2系8、供体2系1、供体2系13、供体2系11或供体2系19。
[0358]
附加实施例4.附加实施例1-3中任一项所述的修饰的免疫细胞,其中所述编码的结合蛋白包含:(i)与t细胞的tcr的vα结构域具有至少90%的氨基酸同一性的vα结构域,所述t细胞来自:供体1系1、供体1系3、供体2系8、供体2系1、供体2系13、供体2系11或供体2系
nos.:18和13;(ii)分别为seq id nos.:30和25;(iii)分别为seq id nos.:42和37;(iv)分别为seq id nos.:54和49;(v)分别为seq id nos.:66和61;(vi)分别为seq id nos.:78和73;(vii)分别为seq id nos.:90和85;(viii)分别为seq id nos.:102和97;(ix)分别为seq id nos.:114和109;(x)分别为seq id nos.:126和121;(xi)分别为seq id nos.:138和133;或(xii)分别为seq id nos.:150和145。
[0364]
附加实施例10.附加实施例1-9中任一项所述的修饰的免疫细胞,其中编码的结合蛋白包含在与seq id nos.:12、24、36、48、60、72、84、96、108、120、132或144中任一项所述的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一性的氨基酸序列中。
[0365]
附加实施例11.附加实施例1-10中任一项所述的修饰免疫细胞,其中编码结合蛋白的多核苷酸包含与seq id nos.:11、23、35、47、59、71、83、95、107、119、131或143中任一项所述的核苷酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一性的多核苷酸。
[0366]
附加实施例12.附加实施例1-11中任一项所述的修饰的免疫细胞,其中编码的结合蛋白包含tcr、单链tcr(sctcr)、sctv、嵌合抗原受体(car)、或其任何组合。
[0367]
附加实施例13.附加实施例1-12中任一项所述的修饰的免疫细胞,其进一步包含编码tcrβ-多肽恒定结构域(cβ)的多核苷酸、编码tcrα-多肽恒定结构域(cα)的多核苷酸、或两者。
[0368]
附加实施例14.附加实施例13所述的修饰的免疫细胞,其包含编码tcr cβ的多核苷酸和编码tcr cα的多核苷酸,其中编码的tcr cβ包含在氨基酸位置57处的半胱氨酸氨基酸,且其中编码的tcr cα包含在氨基酸位置48处的半胱氨酸氨基酸。
[0369]
附加实施例15.附加实施例1-14中任一项所述的修饰的免疫细胞,其中所述免疫细胞包括t细胞、nk细胞、nk-t细胞、或其任何组合。
[0370]
附加实施例16.附加实施例15所述的修饰的免疫细胞,其中所述免疫细胞包括cd8
+
t细胞和/或cd4
+
t细胞。
[0371]
附加实施例17.附加实施例1-16中任一项所述的修饰的免疫细胞,其中编码结合蛋白的异源多核苷酸经过密码子优化用于在宿主细胞中表达。
[0372]
附加实施例18.附加实施例1-17中任一项所述的修饰的免疫细胞,其中所述免疫细胞包含pd-1基因;lag3基因;tim3基因;ctla4基因;hla组分基因;tcr组分基因、或其任何组合的染色体基因敲除。
[0373]
附加实施例19.附加实施例18所述的修饰的免疫细胞,其中所述染色体基因敲除包括hla组分基因的敲除,所述hla组分基因选自α1巨球蛋白基因、α2巨球蛋白基因、α3巨球蛋白基因、β1微球蛋白基因、或β2微球蛋白基因、或其任何组合。
[0374]
附加实施例20.附加实施例18或19所述的修饰的免疫细胞,其中所述染色体基因敲除包括tcr组分基因的敲除,所述tcr组分基因选自tcrα可变区基因、tcrβ可变区基因、tcr恒定区基因、或其任何组合。
[0375]
附加实施例21.一种组合物,其包含附加实施例1-20中任一项所述的修饰的免疫细胞和药学上可接受的载剂、稀释剂或赋形剂。
[0376]
附加实施例22.一种在受试者中用于治疗与sox2抗原表达相关或与sox2表达或活
性相关的疾病或病症的方法,所述sox2抗原包含或由根据seq id nos:2-7中任一项的氨基酸序列组成,所述方法包括向受试者施用有效量的附加实施例1-20中任一项所述的修饰的免疫细胞或附加实施例21所述的组合物,从而治疗所述疾病或病况。
[0377]
附加实施例23.一种在患有与sox2抗原表达相关或与sox2表达或活性相关的疾病或病症的受试者中用于诱导免疫应答和/或在受试者中用于治疗该疾病或病症的方法,所述sox2抗原包含或由根据seq id nos:2-7中任一项的氨基酸序列组成,所述方法包括向所述受试者施用有效量的t细胞,所述t细胞表达tcr,所述tcr与在靶细胞表面上表达的肽:hla复合物特异性结合,其中所述肽包含或由根据seq id nos:2-7中任一项的氨基酸序列组成,且其中所述hla任选为hla-a*02:01。
[0378]
附加实施例24.附加实施例22或23所述的方法,其中所述受试者是hla-a*02:01
+
。
[0379]
附加实施例25.附加实施例22-24中任一项所述的方法,其中所述疾病或病况为癌症。
[0380]
附加实施例26.附加实施例25所述的方法,其中所述癌症包括血液系统恶性肿瘤或实体肿瘤。
[0381]
附加实施例27.附加实施例25或26所述的方法,其中所述癌症包括多发性骨髓瘤、浆细胞白血病或卵巢癌。
[0382]
附加实施例28.附加实施例22-27中任一项所述的方法,其中所述受试者是人。
[0383]
附加实施例29.根据附加实施例22-28中任一项所述的方法,其中所述受试者先前已接受以下的一种或多种:(i)外科手术;(ii)放射疗法;(iii)化学疗法;(iv)造血干细胞移植(hsc);或(v)过继细胞疗法,所述过继细胞疗法任选包含表达car的t细胞,并且其中所述疾病或病症任选地对先前的疗法是难治性的。
[0384]
附加实施例30.附加实施例22-29中任一项所述的方法,其中所述组合物中所包含的一种或多种修饰的免疫细胞是受试者自体的。
[0385]
附加实施例31.附加实施例22-30中任一项所述的方法,进一步包括向受试者施用免疫检查点分子的抑制剂。
[0386]
附加实施例32.一种分离的多核苷酸,其编码结合蛋白,所述结合蛋白包括t细胞受体(tcr)α多肽可变结构域(vα)和tcrβ多肽可变结构域(vβ),其中所述编码的结合蛋白能够与sox2抗原:hla复合物特异性结合,其中所述sox2抗原包含或由seq id no:2、3、4、5、6或7中所述的氨基酸序列组成,其中所述多核苷酸任选经过密码子优化用于在宿主细胞中表达。
[0387]
附加实施例33.附加实施例32所述的分离的多核苷酸,其中所述hla包括hla-a*02:01。
[0388]
附加实施例34.附加实施例33所述的分离的多核苷酸,其中编码的结合蛋白包含:(i)t细胞的tcr的cdr3β、cdr2β和/或cdr1β,所述t细胞来自:供体1系1、供体1系3、供体2系8、供体2系1、供体2系13、供体2系11或供体2系19;和/或(ii)t细胞的tcr的cdr3α、cdr2α和/或cdr1α,所述t细胞来自:供体1系1、供体1系3、供体2系8、供体2系1、供体2系13、供体2系11或供体2系19。
[0389]
附加实施例35.附加实施例32-34中任一项所述的分离的多核苷酸,其中编码的结合蛋白包含:(i)与t细胞的tcr的vα结构域具有至少90%的氨基酸同一性的vα结构域,所述
t细胞来自:供体1系1、供体1系3、供体2系8、供体2系1、供体2系13、供体2系11或供体2系19;和/或(ii)与t细胞的tcr的vβ结构域具有至少90%的氨基酸同一性的vβ结构域,所述t细胞来自:供体1系1、供体1系3、供体2系8、供体2系1、供体2系13、供体2系11或供体2系19,条件是(a)至少三个或四个cdr没有突变;(b)具有突变的cdr仅具有至多两个氨基酸取代、至多连续的五个氨基酸缺失、或其组合;和(c)编码的结合蛋白保留其与sox2肽:hla复合物结合的能力。
[0390]
附加实施例36.附加实施例32或33所述的分离的多核苷酸,其中编码的结合蛋白包含:(i)根据seq id nos.:16、17、28、29、40、41、52、53、64、65、76、77、88、89、100、101、112、113、124、125、136、137、148或149中任一项的cdr3β氨基酸序列,或其包含一个、两个或三个氨基酸取代的变体;(ii)根据seq id nos.:15、27、39、51、63、75、87、99、111、123、135或147中任一项的cdr2β氨基酸序列,或其包含一个、两个或三个氨基酸取代的变体;(iii)根据seq id nos.:14、26、38、50、62、74、86、98、110、122、134、146中任一项的cdr1β氨基酸序列,或其包含一个、两个或三个氨基酸取代的变体;(iv)根据seq id nos.:21、22、33、34、45、46、57、58、69、70、81、82、93、94、105、106、117、118、129、130、141、142、153或154中任一项的cdr3α氨基酸序列,或其包含一个、两个或三个氨基酸取代的变体;(v)根据seq id nos.:20、32、44、56、68、80、92、104、116、128、140、152中任一项的cdr2α氨基酸序列,或其包含一个、两个或三个氨基酸取代的变体;和/或(vi)根据seq id nos.:19、31、43、55、67、79、91、103、115、127、139或151中任一项的cdr1α氨基酸序列,或其包含一个、两个或三个氨基酸取代的变体。
[0391]
附加实施例37.附加实施例36所述的分离的多核苷酸,其中编码的结合蛋白包含cdr1α、cdr2α、cdr3α、cdr1β、cdr2β和cdr3β氨基酸序列,其根据:(i)分别为seq id nos.:19、20、21或22、14、15、和16或17;(ii)分别为seq id nos.:31、32、33或34、26、27、和28或29;(iii)分别为seq id nos.:43、44、45或46、38、39、和40或41;(iv)分别为seq id nos.:55、56、57或58、50、51、和52或53;(v)分别为seq id nos.:67、68、69或70、62、63、和64或65;(vi)分别为seq id nos.:79、80、81或82、74、75、和76或77;(vii)分别为seq id nos.:91、92、93或94、86、87、和88或89;(viii)分别为seq id nos.:103、104、105或106、98、99、和100或101;(ix)分别为seq id nos.:115、116、117或118、110、111、和112或113;(x)分别为seq id nos.:127、128、129或130、122、123、和124或125;(xi)分别为seq id nos.:139、140、141或142、134、135、和136或137;或(xii)分别为seq id nos.:151、152、153或154、146、147、和148或149。
[0392]
附加实施例38.附加实施例32、33、36或37中任一项所述的分离的多核苷酸,其中编码的vα结构域包含或由与seq id nos.:18、30、42、54、66、78、90、102、114、126、138或150中任一项所述的氨基酸序列具有至少80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一性的氨基酸序列组成。
[0393]
附加实施例39.附加实施例32、33或36-38中任一项所述的分离的多核苷酸,其中编码的vβ结构域包含或由与seq id nos.:13、25、37、49、61、73、85、97、109、121、133或145中任一项所述的氨基酸序列具有至少80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一性的氨基酸序列组成。
[0394]
附加实施例40.附加实施例36-39中任一项所述的分离的多核苷酸,其中编码的vα
结构域和编码的vβ结构域包含或由根据以下各项的氨基酸序列组成:(i)分别为seq id nos.:18和13;(ii)分别为seq id nos.:30和25;(iii)分别为seq id nos.:42和37;(iv)分别为seq id nos.:54和49;(v)分别为seq id nos.:66和61;(vi)分别为seq id nos.:78和73;(vii)分别为seq id nos.:90和85;(viii)分别为seq id nos.:102和97;(ix)分别为seq id nos.:114和109;(x)分别为seq id nos.:126和121;(xi)分别为seq id nos.:138和133;或(xii)分别为seq id nos.:150和145。
[0395]
附加实施例41.附加实施例32-40中任一项所述的分离的多核苷酸,其编码与seq id nos.:12、24、36、48、60、72、84、96、108、120、132或144中任一项所述的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的氨基酸序列。
[0396]
附加实施例42.附加实施例32-41中任一项所述的分离的多核苷酸,其包含与seq id nos.:11、23、35、47、59、71、83、95、107、119、131或143中任一项所述的核苷酸序列具有至少70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%同一性的多核苷酸。
[0397]
附加实施例43.附加实施例32-42中任一项所述的分离的多核苷酸,其中编码的结合蛋白包含tcr、单链tcr(sctcr)、sctv、嵌合抗原受体(car)、或其任何组合。
[0398]
附加实施例44.附加实施例32-43中任一项所述的分离的多核苷酸,其进一步包含编码tcrβ-多肽恒定结构域(cβ)的多核苷酸、编码tcrα-多肽恒定域(cα)的多核苷酸、或两者。
[0399]
附加实施例45.附加实施例44所述的分离的多核苷酸,其包含编码tcr cβ的多核苷酸和编码tcr cα的多核苷酸,其中编码的tcr cβ包含在氨基酸位置57处的半胱氨酸氨基酸,并且其中编码的tcr cα包含在氨基酸位置48处的半胱氨酸氨基酸。
[0400]
附加实施例46.附加实施例32-45中任一项所述的分离的多核苷酸,其中所述多核苷酸经过密码子优化用于在宿主细胞中表达。
[0401]
附加实施例47.附加实施例46所述的分离的多核苷酸,其中所述免疫细胞是t细胞、nk细胞或nk-t细胞。
[0402]
附加实施例48.附加实施例47所述的分离的多核苷酸,其中所述免疫细胞包括cd8
+
t细胞和/或cd4
+
t细胞。
[0403]
附加实施例49.附加实施例32-48中任一项所述的分离的多核苷酸,其包含编码自切割肽的多核苷酸,所述编码自切割肽的多核苷酸位于编码vβ的多核苷酸和编码vα的多核苷酸之间,或位于编码tcrβ多肽的多核苷酸与编码tcrα多肽的多核苷酸之间。
[0404]
附加实施例50.一种载体,其包含附加实施例32-49中任一项所述的分离的多核苷酸。
[0405]
附加实施例51.一种免疫原性组合物,其包括:(i)包含或由seq id no:2的氨基酸序列组成的sox2抗原;(ii)包含或由seq id no:3的氨基酸序列组成的sox2抗原;(iii)包含或由seq id no:4的氨基酸序列组成的sox2抗原;(iv)包含或由seq id no:5的氨基酸序列组成的sox2抗原;(v)包含或由seq id no:6的氨基酸序列组成的sox2抗原;(vi)包含或由seq id no:7的氨基酸序列组成的sox2抗原;和/或(vii)与seq id no:2、3、4、5、6或7相比具有一个、两个或三个氨基酸差异的sox2抗原的变体。
[0406]
附加实施例52.附加实施例51所述的免疫原性组合物,其中(a)(i)-(vi)中任一项的两个或多个拷贝和/或(b)(i)-(vi)中任何两个或多个存在于融合多肽中,其中所述融合多肽任选地进一步包含自切割肽的氨基酸序列。
[0407]
附加实施例53.附加实施例51或52所述的免疫原性组合物,其中所述免疫原性组合物能够诱导对多发性骨髓瘤细胞、浆细胞白血病细胞和/或卵巢癌细胞的免疫应答。
[0408]
附加实施例54.附加实施例51-53中任一项所述的免疫原性组合物,其进一步包含佐剂。
[0409]
附加实施例55.一种分离的多核苷酸,其编码:(i)包含或由seq id no:2的氨基酸序列组成的sox2抗原;(ii)包含或由seq id no:3的氨基酸序列组成的sox2抗原;(iii)包含或由seq id no:4的氨基酸序列组成的sox2抗原;(iv)包含或由seq id no:5的氨基酸序列组成的sox2抗原;(v)包含或由seq id no:6的氨基酸序列组成的sox2抗原;(vi)包含或由seq id no:7的氨基酸序列组成的sox2抗原;和/或(vii)与seq id no:2、3、4、5、6或7相比具有一个、两个或三个氨基酸差异的sox2抗原的变体,其中所述多核苷酸任选包含在载体中。
[0410]
附加实施例56.附加实施例55所述的分离的多核苷酸,其中所述多核苷酸经过密码子优化用于在宿主细胞中表达,其中所述宿主细胞任选地是树突状细胞或t细胞。
[0411]
附加实施例57.一种宿主细胞,其包含附加实施例47或48所述的分离的多核苷酸,其中所述宿主细胞任选地为免疫细胞,且进一步任选地为专职性抗原呈递细胞。
[0412]
附加实施例58.附加实施例57所述的宿主细胞,其中所述宿主细胞是树突状细胞或t细胞。
[0413]
附加实施例59.一种在受试者中引发针对与sox2表达或活性相关的疾病或病症的免疫应答的方法,所述方法包括向受试者施用附加实施例1-20中任一项所述的修饰的免疫细胞、附加实施例21所述的组合物、附加实施例51-54中任一项所述的修饰的免疫原性组合物、附加实施例55或56所述的多核苷酸和/或附加实施例57或58所述的宿主细胞。
[0414]
附加实施例60.一种扩增t细胞群的方法,所述t细胞群与sox2抗原特异性结合,所述sox2抗原选自:(i)包含或由seq id no:2的氨基酸序列组成的sox2抗原;(ii)包含或由seq id no:3的氨基酸序列组成的sox2抗原;(iii)包含或由seq id no:4的氨基酸序列组成的sox2抗原;(iv)包含或由seq id no:5的氨基酸序列组成的sox2抗原;(v)包含或由seq id no:6的氨基酸序列组成的sox2抗原;和/或(vi)包含或由seq id no:7的氨基酸序列组成的sox2抗原,
[0415]
所述方法包括将包含与抗原特异性结合一种或多种的t细胞的样品与附加实施例51-54中任一项所述的免疫原性组合物、附加实施例55或56所述的多核苷酸、附加实施例57或58所述的宿主细胞,和/或或已用sox2抗原脉冲处理的抗原呈递细胞接触,所述sox2抗原包含或由seq id nos:2-7中任一项所述的氨基酸序列组成。
[0416]
附加实施例61.一种产生和/或分离t细胞的方法,所述方法包括使外周血细胞与以下各项接触:(i)附加实施例51-54中任一项所述的免疫原性组合物;(ii)附加实施例55或56所述的多核苷酸;(iii)附加实施例57或58所述的宿主细胞;和/或(iv)抗原呈递细胞(apc),其已用sox2抗原脉冲处理或以其他方式接触sox2抗原,所述sox2抗原包含或由seq id nos:2-7中任一项所述的氨基酸序列组成,并且任选地从外周血细胞分选t细胞,从而分
离和/或产生t细胞。
[0417]
序列
[0418]
seq id no.:1(人sox2氨基酸序列)
[0419]
mynmmetelk ppgpqqtsgg gggnstaaaa ggnqknspdr
[0420]
vkrpmnafmv
[0421]
wsrgqrrkma qenpkmhnse iskrlgaewk llsetekrpf ideakrlral
[0422]
hmkehpdyky rprrktktlm kkdkytlpgg llapggnsma
[0423]
sgvgvgaglg
[0424]
agvnqrmdsy ahmngwsngs ysmmqdqlgy pqhpglnahg
[0425]
aaqmqpmhry dvsalqynsm tssqtymngs ptysmsysqq
[0426]
gtpgmalgsm gsvvkseass sppvvtsssh srapcqagdl rdmismylpg
[0427]
aevpepaaps rlhmsqhyqs gpvpgtaing tlplshm
[0428]
seq id no.:2(sox2肽(275-283))
[0429]
smylpgaev
[0430]
seq id no.:3(sox2肽(216-225))
[0431]
ymngsptysm
[0432]
seq id no.:4(sox2肽(306-314))
[0433]
taingtlpl
[0434]
seq id no.:5(sox2肽(277-287))
[0435]
ylpgaevpepa
[0436]
seq id no.:6(sox2肽(58-66))
[0437]
kmaqenpkm
[0438]
seq id no.:7(sox2肽(118-127))
[0439]
tlmkkdkytl
[0440]
seq id no.:8(htcr_cα-r)
[0441]
cagccgcagcgtcatgagcagatta
[0442]
seq id no.:9(htcr_cb1-r)
[0443]
ccacttccagggctgccttcagaaatc
[0444]
seq id no.:10(htcr_cb2-r)
[0445]
tgggatggttttggagctagcctctgg
[0446]
序列图例
–
颜色编码:
[0447]
前导序列
[0448]
v-β
[0449]
cdr1,cdr2-β
[0450]
cdr3-β;连接
[0451]
j-β
[0452]
c-β
[0453]
p2a
[0454]
前导序列
[0455]
v-α
[0456]
cdr1,cdr2-α
[0457]
cdr3-α;连接
[0458]
j-α
[0459]
c-α
[0460]
seq id no.:11(sox2 tcr#01tcrβ-p2a-tcrα,密码子优化的核苷酸)
[0461]
atggcttctctcctgttcttctgtggcgccttttacctgctgggaacaggctctatggatgctgatgtgacacagacccccagaaacagaatcaccaagacaggcaagcggatcatgctggagtgtagccagacaaaaggccacgaccggatgtactggtatagacaagatcctgggttgggccttcgactgatctactacagcttcgacgtgaaggacatcaacaagggcgagatctctgacggctacagcgtgagcagacaagctcaggccaagttttctctgtctctggaatctgccatccctaatcagacagccctgtacttctgtgccaccagcgagtgggatagcacagatacacagtactttggccccggcaccaggctgacagtgcttgaggacctgaagaacgtgttccccccagaggtggccgtgttcgagcctagcgaggccgagatcagccacacccagaaagccaccctcgtgtgcctggccaccggcttttaccccgaccacgtggaactgtcttggtgggtcaacggcaaagaggtgcacagcggcgtctgcaccgacccccagcccctgaaagagcagcccgccctgaacgacagccggtactgtctgagcagcagactgagagtgtccgccaccttctggcagaacccccggaaccacttcagatgccaggtgcagttctacggcctgagcgagaacgacgagtggacccaggaccgggccaagcccgtgacccagatcgtgtctgctgaggcctggggcagagccgattgcggcttcaccagcgagagctaccagcagggcgtgctgagcgccaccatcctgtacgagatcctgctgggcaaggccaccctgtacgccgtgctggtgtccgccctggtgctgatggccatggtcaagcggaaggacagccggggcggttccggagccacgaacttctctctgttaaagcaagcaggagacgtggaagaaaaccccggtcccatggagacactgcttggcgtatcactggtgattctgtggctgcaactggctagagtgaactctcagcagggagaagaggatcctcaagctctgagcattcaggaaggcgaaaacgctaccatgaattgctcctacaagaccagcatcaacaacctgcagtggtaccggcagaatagcggaagaggactggttcacctgatcctgatcagaagcaatgaaagggagaagcacagcggcagactgagagttaccctggatacatccaagaaaagtagctctctgctgattacagcctctagagccgccgatacagccagctacttttgtgccacattaggacagggagcccagaaactggtgtttggacagggcacaagactgaccatcaatcccaacatccagaatcctgatcccgccgtgtaccagctgcgggacagcaagagcagcgacaagagcgtgtgcctgttcaccgacttcgacagccagaccaacgtgtcccagagcaaggacagcgacgtgtacatcaccgataagtgcgtgctggacatgcggagcatggacttcaagagcaacagcgccgtggcctggtccaacaagagcgacttcgcctgcgccaacgccttcaacaacagcattatccccgaggacacattcttcccaagccccgagagcagctgcgacgtgaagctggtggaaaagagcttcgagacagacaccaacctgaacttccagaacctcagcgtgatcggcttccggatcctgctgctgaaggtggccggcttcaacctgctgatgaccctgcggctgtggtccagctga
[0462]
seq id no.:12(sox2 tcr#01tcrβ-p2a-tcrα,氨基酸)
[0463]
masllffcgafyllgtgsmdadvtqtprnritktgkrimlecsqtkghdrmywyrqdpglglrliyysfdvkdinkgeisdgysvsrqaqakfslslesaipnqtalyfcatsewdstdtqyfgpgtrltvledlknvfppevavfepseaeishtqkatlvclatgfypdhvelswwvngkevhsgvctdpqplkeqpalndsryclssrlrvsatfwqnprnhfrcqvqfyglsendewtqdrakpvtqivsaeawgradcgftsesyqqgvlsatilyeillgkatlyavlvsalvlmamvkrkdsrggsgatnfsllkqagdveenpgpmetllgvslvilwlqlarvnsqqgeedpqalsiqegenatmncsyktsinnlqwyrqnsgrglvhlilirsnerekhsgrlrvtldtskksssllitasraadtasyfcatlgqgaqklvfgqgtrltinpniqnpdpavyqlrdskssdksvclftdfdsqtnvsqskdsdvyitdkcvldmrsmdfksnsavawsnksdfacanafnnsiipedtffpspesscdvklveksfetdtnlnfqnlsvigfrilllkvagfnllmtlrlwss
[0464]
seq id no.:13(sox2 tcr#01tcrvβ,氨基酸)
[0465]
dadvtqtprnritktgkrimlecsqtkghdrmywyrqdpglglrliyysfdvkdinkgeisdgysvsrqaqakfslslesaipnqtalyfcatsewdstdtqyfgpgtrltvle
[0466]
seq id no.:14(sox2 tcr#01cdr1β,氨基酸)
[0467]
kghdr
[0468]
seq id no.:15(sox2 tcr#01cdr2β,氨基酸)
[0469]
sfdvkd
[0470]
seq id no.:16(sox2 tcr#01cdr3β,氨基酸)
[0471]
atsewdstdtqy
[0472]
seq id no.:17(sox2 tcr#01cdr3β-连接,氨基酸)
[0473]
catsewdstdtqyf
[0474]
seq id no.:18(sox2 tcr#01tcrvα,氨基酸)
[0475]
sqqgeedpqalsiqegenatmncsyktsinnlqwyrqnsgrglvhlilirsnerekhsgrlrvtldtskksssllitasraadtasyfcatlgqgaqklvfgqgtrltinpn
[0476]
seq id no.:19(sox2 tcr#01cdr1α,氨基酸)
[0477]
tsinn
[0478]
seq id no.:20(sox2 tcr#01cdr2α,氨基酸)
[0479]
irsnere
[0480]
seq id no.:21(sox2 tcr#01cdr3α,氨基酸)
[0481]
atlgqgaqklv
[0482]
seq id no.:22(sox2 tcr#01cdr3α-连接,氨基酸)
[0483]
catlgqgaqklvf
[0484]
seq id no.:23(sox2 tcr#02tcrβ-p2a-tcrα,密码子优化的核苷酸)
[0485]
atgggcatcagactcctttgcagggtggccttttgctttctggctgtgggattagtggacgtgaaggttacccagtccagtagataccttgtcaagagaaccggcgagaaggtgttcctggaatgtgtgcaggacatggatcacgagaatatgttctggtacagacaggaccctggactgggactgagactgatctacttcagctacgacgtgaagatgaaggagaagggcgatatccctgagggctacagcgtgagcagagagaaaaaggagaggttcagcctgattctggaaagcgccagcacaaatcaaacatctatgtatttatgcgcctcttctctgattctggccggaagaaatacaggcgagctgttttttggcgagggctctagactgaccgtgcttgaggacctgaagaacgtgttccccccagaggtggccgtgttcgagcctagcgaggccgagatcagccacacccagaaagccaccctcgtgtgcctggccaccggcttttaccccgaccacgtggaactgtcttggtgggtcaacggcaaagaggtgcacagcggcgtctgcaccgacccccagcccctgaaagagcagcccgccctgaacgacagccggtactgtctgagcagcagactgagagtgtccgccaccttctggcagaacccccggaaccacttcagatgccaggtgcagttctacggcctgagcgagaacgacgagtggacccaggaccgggccaagcccgtgacccagatcgtgtctgctgaggcctggggcagagccgattgcggcttcaccagcgagagctaccagcagggcgtgctgagcgccaccatcctgtacgagatcctgctgggcaaggccaccctgtacgccgtgctggtgtccgccctggtgctgatggccatggtcaagcggaaggacagccggggcggttccggagccacgaacttctctctgttaaagcaagcaggagacgtggaagaaaaccccggtcccatgaagaagcacctgaccacgttcctggtgattctgtggctgtacttctacaggggcaacggcaagaatcaggttgagcagtctcctcagtccctgattattcttgagggcaagaattgtaccctgcagtgcaactacacagtgagccctttcagcaacctgaggtggtacaagcaggatacaggaagaggacctgtgagtttgacaatcatgacc
ttcagcgagaacaccaagagcaacggcagatatacagccaccctggatgccgacacaaagcagtcttctctgcacattacagcctctcagctgagcgattctgccagctacatctgcgtggtgagagacagcaattaccagctgatttggggagctggcacaaagctgatcatcaagcccgacatccagaatcccgatcctgctgtgtaccagctgcgggacagcaagagcagcgacaagagcgtgtgcctgttcaccgacttcgacagccagaccaacgtgtcccagagcaaggacagcgacgtgtacatcaccgataagtgcgtgctggacatgcggagcatggacttcaagagcaacagcgccgtggcctggtccaacaagagcgacttcgcctgcgccaacgccttcaacaacagcattatccccgaggacacattcttcccaagccccgagagcagctgcgacgtgaagctggtggaaaagagcttcgagacagacaccaacctgaacttccagaacctcagcgtgatcggcttccggatcctgctgctgaaggtggccggcttcaacctgctgatgaccctgcggctgtggtccagctga
[0486]
seq id no.:24(sox2 tcr#02tcrβ-p2a-tcrα,氨基酸)
[0487]
mgirllcrvafcflavglvdvkvtqssrylvkrtgekvflecvqdmdhenmfwyrqdpglglrliyfsydvkmkekgdipegysvsrekkerfslilesastnqtsmylcasslilagrntgelffgegsrltvledlknvfppevavfepseaeishtqkatlvclatgfypdhvelswwvngkevhsgvctdpqplkeqpalndsryclssrlrvsatfwqnprnhfrcqvqfyglsendewtqdrakpvtqivsaeawgradcgftsesyqqgvlsatilyeillgkatlyavlvsalvlmamvkrkdsrggsgatnfsllkqagdveenpgpmkkhlttflvilwlyfyrgngknqveqspqsliilegknctlqcnytvspfsnlrwykqdtgrgpvsltimtfsentksngrytatldadtkqsslhitasqlsdsasyicvvrdsnyqliwgagtkliikpdiqnpdpavyqlrdskssdksvclftdfdsqtnvsqskdsdvyitdkcvldmrsmdfksnsavawsnksdfacanafnnsiipedtffpspesscdvklveksfetdtnlnfqnlsvigfrilllkvagfnllmtlrlwss
[0488]
seq id no.:25(sox2 tcr#02tcrvβ,氨基酸)
[0489]
dvkvtqssrylvkrtgekvflecvqdmdhenmfwyrqdpglglrliyfsydvkmkekgdipegysvsrekkerfslilesastnqtsmylcasslilagrntgelffgegsrltvle
[0490]
seq id no.:26(sox2 tcr#02cdr1β,氨基酸)
[0491]
mdhen
[0492]
seq id no.:27(sox2 tcr#02cdr2β,氨基酸)
[0493]
sydvkm
[0494]
seq id no.:28(sox2 tcr#02cdr3β,氨基酸)
[0495]
asslilagrntgelf
[0496]
seq id no.:29(sox2 tcr#02cdr3β-连接,氨基酸)
[0497]
casslilagrntgelff
[0498]
seq id no.:30(sox2 tcr#02tcrvα,氨基酸)
[0499]
knqveqspqsliilegknctlqcnytvspfsnlrwykqdtgrgpvsltimtfsentksngrytatldadtkqsslhitasqlsdsasyicvvrdsnyqliwgagtkliikpd
[0500]
seq id no.:31(sox2 tcr#02cdr1α,氨基酸)
[0501]
vspfsn
[0502]
seq id no.:32(sox2 tcr#02cdr2α,氨基酸)
[0503]
mtfsent
[0504]
seq id no.:33(sox2 tcr#02cdr3α,氨基酸)
[0505]
vvrdsnyqli
[0506]
seq id no.:34(sox2 tcr#02cdr3α-连接,氨基酸)
[0507]
cvvrdsnyqliw
[0508]
seq id no.:35(sox2 tcr#04tcrβ-p2a-tcrα,密码子优化的核苷酸)
[0509]
atgggacctggactgttatgttgggttctgctgtgtctgcttggagctggacctgttgatgctggagttacacagagccctacacacctgatcaagacaagaggacagcaggtgaccctgagatgtagccctatttctggccacaagagcgtgagctggtatcagcaggttttaggacagggaccccagttcatcttccagtactacgagaaggaggagagaggcagaggcaatttccctgacagatttagcgcccggcagttccccaattatagctctgagctgaacgtgaatgccctgctgcttggcgattctgctctgtacctgtgtgcctcttctctgtttatcagcctgatgctggatacccagtacttcggccctggcacaagactgacagtgctggaagacctgaagaacgtgttccccccagaggtggccgtgttcgagcctagcgaggccgagatcagccacacccagaaagccaccctcgtgtgcctggccaccggcttttaccccgaccacgtggaactgtcttggtgggtcaacggcaaagaggtgcacagcggcgtctgcaccgacccccagcccctgaaagagcagcccgccctgaacgacagccggtactgtctgagcagcagactgagagtgtccgccaccttctggcagaacccccggaaccacttcagatgccaggtgcagttctacggcctgagcgagaacgacgagtggacccaggaccgggccaagcccgtgacccagatcgtgtctgctgaggcctggggcagagccgattgcggcttcaccagcgagagctaccagcagggcgtgctgagcgccaccatcctgtacgagatcctgctgggcaaggccaccctgtacgccgtgctggtgtccgccctggtgctgatggccatggtcaagcggaaggacagccggggcggttccggagccacgaacttctctctgttaaagcaagcaggagacgtggaagaaaaccccggtcccatggtgaagatccggcagttcctcctggctattctgtggctgcaactgtcttgtgtgtcagcagccaagaatgaagtggagcagtcccctcagaacctgaccgcacaggaaggcgagtttatcaccatcaactgcagctactccgtaggcataagcgccctgcattggctccagcagcaccctggaggaggaattgtgtctctgtttatgctgagcagcggaaaaaaaaagcacggccggctgattgccaccatcaacatccaggagaagcatagcagcctacacattacagcgtctcatcccagggattctgccgtgtacatctgtgccacactgacacaaggaggaagcgaaaaactggtgtttggcaagggcacaaagctgaccgtgaatccctacatccagaatcccgatcctgccgtgtaccagctgcgggacagcaagagcagcgacaagagcgtgtgcctgttcaccgacttcgacagccagaccaacgtgtcccagagcaaggacagcgacgtgtacatcaccgataagtgcgtgctggacatgcggagcatggacttcaagagcaacagcgccgtggcctggtccaacaagagcgacttcgcctgcgccaacgccttcaacaacagcattatccccgaggacacattcttcccaagccccgagagcagctgcgacgtgaagctggtggaaaagagcttcgagacagacaccaacctgaacttccagaacctcagcgtgatcggcttccggatcctgctgctgaaggtggccggcttcaacctgctgatgaccctgcggctgtggtccagctga
[0510]
seq id no.:36 (sox2 tcr#04 tcrβ-p2a-tcrα, 氨基酸)
[0511]
mgpgllcwvllcllgagpvdagvtqspthliktrgqqvtlrcspisghksvswyqqvlgqgpqfifqyyekeergrgnfpdrfsarqfpnysselnvnalllgdsalylcasslfislmldtqyfgpgtrltvledlknvfppevavfepseaeishtqkatlvclatgfypdhvelswwvngkevhsgvctdpqplkeqpalndsryclssrlrvsatfwqnprnhfrcqvqfyglsendewtqdrakpvtqivsaeawgradcgftsesyqqgvlsatilyeillgkatlyavlvsalvlmamvkrkdsrggsgatnfsllkqagdveenpgpmvkirqfllailwlqlscvsaakneveqspqnltaqegefitincsysvgisalhwlqqhpgggivslfmlssgkkkhgrliatiniqekhsslhitashprdsavyicatltq
[0512]
ggseklvfgkgtkltvnpyiqnpdpavyqlrdskssdksvclftdfdsqtnvsqskdsdvyitdkcvldmrsmdfksnsavawsnksdfacanafnnsiipedtffpspesscdvklveksfetdtnlnfqnlsvigfrilllkvagfnllmtlrlwss
[0513]
seq id no.:37(sox2 tcr#04tcrvβ,氨基酸)
[0514]
dagvtqspthliktrgqqvtlrcspisghksvswyqqvlgqgpqfifqyyekeergrgnfpdrfsarqfpnysselnvnalllgdsalylcasslfislmldtqyfgpgtrltvle
[0515]
seq id no.:38(sox2 tcr#04cdr1β,氨基酸)
[0516]
sghks
[0517]
seq id no.:39(sox2 tcr#04cdr2β,氨基酸)
[0518]
yyekee
[0519]
seq id no.:40(sox2 tcr#04cdr3β,氨基酸)
[0520]
asslfislmldtqy
[0521]
seq id no.:41(sox2 tcr#04cdr3β-连接,氨基酸)
[0522]
casslfislmldtqyf
[0523]
seq id no.:42(sox2 tcr#04tcrvα,氨基酸)
[0524]
kneveqspqnltaqegefitincsysvgisalhwlqqhpgggivslfmlssgkkkhgrliatiniqekhsslhitashprdsavyicatltqggseklvfgkgtkltvnpy
[0525]
seq id no.:43(sox2 tcr#04cdr1α,氨基酸)
[0526]
vgisa
[0527]
seq id no.:44(sox2 tcr#04cdr2α,氨基酸)
[0528]
lssgk
[0529]
seq id no.:45(sox2 tcr#04cdr3α,氨基酸)
[0530]
atltqggseklv
[0531]
seq id no.:46(sox2 tcr#04cdr3α-连接,氨基酸)
[0532]
catltqggseklvf
[0533]
seq id no.:47(sox2 tcr#05tcrβ-p2a-tcrα,密码子优化的核苷酸)
[0534]
atgggcatcagactcctttgcagggtggccttttgctttctggctgtgggattagtggacgtgaaggttacccagtccagcagatacctggttaagagaaccggcgagaaggtgttcctggaatgtgtgcaggacatggatcacgaaaatatgttttggtacagacaggaccctggactgggactgagactgatctacttcagctacgacgtgaagatgaaggagaagggcgatatccctgagggctacagcgtgagcagagagaaaaaggagaggttcagcctgattctggaaagcgccagcacaaatcaaacatctatgtacctttgcgcctctagacctgaaatgggcggaagaggaaatcagcctcagcattttggcgatggcacaagactgagcatcctggaggatctgaacaaggtgttccccccagaggtggccgtgttcgagccttctgaggccgagatctcccacacccagaaagccaccctcgtgtgcctggccaccggctttttccccgaccacgtggaactgtcttggtgggtcaacggcaaagaggtgcactccggcgtgtgcaccgatccccagcctctgaaagaacagcccgccctgaacgacagccggtactgcctgagcagcagactgagagtgtccgccaccttctggcagaacccccggaaccacttcagatgccaggtgcagttctacggcctgagcgagaacgacgagtggacccaggacagagccaagcccgtgacacagatcgtgtctgccgaagcctggggcagagccgattgcggctttacctccgtgtcctatcagcagggcgtgctgagcgccacaatcctgtacgagatcctgctgggcaaggccaccctgtacgccgtgctggtgtctgccctggtgctgatggccatggtcaagcggaaggacttcggttccggagccacgaacttctctctgttaaagcaagcaggagacgtggaagaaaaccccggtcccatgagcctgtcttctctgctgaaggtggtgactgctagcctctggttaggacctggaattgcccagaagatcacccagacacaacctggcatgtttgtgcaggagaaagaggctgtgaccctggattgcacctacgataccagcgatccttcttacggccttttctggtacaaacagcctagctccggcgagatgatcttcctgatctaccagggcagctacgaccagcagaacgcaaccgagggtagatatagcctgaattttcagaaggcaagaaagtcagccaacctggtgatctctgcctctcaactgggcgattctgccatgtacttttgtgccatgagagagggcatgggcttccagaaactggtgtttggcacaggcacaaggctgctggtttctcccaatatccagaatcctgaccctgccgtgtaccagctgcgggacagcaag
agcagcgacaagagcgtgtgcctgttcaccgacttcgacagccagaccaacgtgtcccagagcaaggacagcgacgtgtacatcaccgataagtgcgtgctggacatgcggagcatggacttcaagagcaacagcgccgtggcctggtccaacaagagcgacttcgcctgcgccaacgccttcaacaacagcattatccccgaggacacattcttcccaagccccgagagcagctgcgacgtgaagctggtggaaaagagcttcgagacagacaccaacctgaacttccagaacctcagcgtgatcggcttccggatcctgctgctgaaggtggccggcttcaacctgctgatgaccctgcggctgtggtccagctga
[0535]
seq id no.:48(sox2 tcr#05tcrβ-p2a-tcrα,氨基酸)
[0536]
mgirllcrvafcflavglvdvkvtqssrylvkrtgekvflecvqdmdhenmfwyrqdpglglrliyfsydvkmkekgdipegysvsrekkerfslilesastnqtsmylcasrpemggrgnqpqhfgdgtrlsiledlnkvfppevavfepseaeishtqkatlvclatgffpdhvelswwvngkevhsgvctdpqplkeqpalndsryclssrlrvsatfwqnprnhfrcqvqfyglsendewtqdrakpvtqivsaeawgradcgftsvsyqqgvlsatilyeillgkatlyavlvsalvlmamvkrkdfgsgatnfsllkqagdveenpgpmslssllkvvtaslwlgpgiaqkitqtqpgmfvqekeavtldctydtsdpsyglfwykqpssgemifliyqgsydqqnategryslnfqkarksanlvisasqlgdsamyfcamregmgfqklvfgtgtrllvspniqnpdpavyqlrdskssdksvclftdfdsqtnvsqskdsdvyitdkcvldmrsmdfksnsavawsnksdfacanafnnsiipedtffpspesscdvklveksfetdtnlnfqnlsvigfrilllkvagfnllmtlrlwss
[0537]
seq id no.:49(sox2 tcr#05tcr vβ,氨基酸)
[0538]
dvkvtqssrylvkrtgekvflecvqdmdhenmfwyrqdpglglrliyfsydvkmkekgdipegysvsrekkerfslilesastnqtsmylcasrpemggrgnqpqhfgdgtrlsile
[0539]
seq id no.:50(sox2 tcr#05cdr1β,氨基酸)
[0540]
mdhen
[0541]
seq id no.:51(sox2 tcr#05cdr2β,氨基酸)
[0542]
sydvkm
[0543]
seq id no.:52(sox2 tcr#05cdr3β,氨基酸)
[0544]
asrpemggrgnqpqh
[0545]
seq id no.:53(sox2 tcr#05cdr3β-连接,氨基酸)
[0546]
casrpemggrgnqpqhf
[0547]
seq id no.:54(sox2 tcr#05tcr vα,氨基酸)
[0548]
aqkitqtqpgmfvqekeavtldctydtsdpsyglfwykqpssgemifliyqgsydqqnategryslnfqkarksanlvisasqlgdsamyfcamregmgfqklvfgtgtrllvspn
[0549]
seq id no.:55(sox2 tcr#05cdr1α,氨基酸)
[0550]
tsdpsyg
[0551]
seq id no.:56(sox2 tcr#05cdr2α,氨基酸)
[0552]
qgsydqqn
[0553]
seq id no.:57(sox2 tcr#05cdr3α,氨基酸)
[0554]
amregmgfqklv
[0555]
seq id no.:58(sox2 tcr#05cdr3α-连接,氨基酸)
[0556]
camregmgfqklvf
[0557]
seq id no.:59(sox2 tcr#06tcrβ-p2a-tcrα,密码子优化的核苷酸)
[0558]
atgcttttactccttctcttgctcggacctgctggatctggattaggagctgttgtgtctcagcaccct
tcttgggtgatctgtaaaagcggcacaagcgtgaaaattgagtgcaggagcctggattttcaggccaccaccatgttctggtataggcagttccccaagcagtctctgatgctgatggccacctctaatgagggctctaaggccacatatgagcagggcgtagagaaggacaagttcctgatcaaccacgcctctctgaccctgtctaccctgacagttacatctgcccaccctgaggatagcagcttttacatctgtagcgccagaggcaagacaagccctagacctgaaacccagtacttcggacctggcacaagactgttagttctggaggacctgaagaacgtgttccccccagaggtggccgtgttcgagcctagcgaggccgagatcagccacacccagaaagccaccctcgtgtgcctggccaccggcttttaccccgaccacgtggaactgtcttggtgggtcaacggcaaagaggtgcacagcggcgtctgcaccgacccccagcccctgaaagagcagcccgccctgaacgacagccggtactgtctgagcagcagactgagagtgtccgccaccttctggcagaacccccggaaccacttcagatgccaggtgcagttctacggcctgagcgagaacgacgagtggacccaggaccgggccaagcccgtgacccagatcgtgtctgctgaggcctggggcagagccgattgcggcttcaccagcgagagctaccagcagggcgtgctgagcgccaccatcctgtacgagatcctgctgggcaaggccaccctgtacgccgtgctggtgtccgccctggtgctgatggccatggtcaagcggaaggacagccggggcggttccggagccacgaacttctctctgttaaagcaagcaggagacgtggaagaaaaccccggtcccatggagtcttcattgggtggtgtgctgctgattctgtggctgcaggtagattgggtcaagagccagaagatcgagcagaattctgaagccctgaacatccaggagggcaagacagctacactgacctgcaactacaccaactactctcctgcttacctgcagtggtacagacaggatcctggcagaggacctgtgtttctgctgctgattagagaaaacgaaaaggagaaaagaaaagagagactgaaggttaccttcgacacaaccctgaagcagagcctgtttcacattacagccagccaacccgccgattctgccacatacctgtgtgctctgggacacaagctgacatttggaggaggaacaagagttctggtgaagcccaacatccagaatcccgatcctgccgtgtaccagctgcgggacagcaagagcagcgacaagagcgtgtgcctgttcaccgacttcgacagccagaccaacgtgtcccagagcaaggacagcgacgtgtacatcaccgataagtgcgtgctggacatgcggagcatggacttcaagagcaacagcgccgtggcctggtccaacaagagcgacttcgcctgcgccaacgccttcaacaacagcattatccccgaggacacattcttcccaagccccgagagcagctgcgacgtgaagctggtggaaaagagcttcgagacagacaccaacctgaacttccagaacctcagcgtgatcggcttccggatcctgctgctgaaggtggccggcttcaacctgctgatgaccctgcggctgtggtccagctga
[0559]
seq id no.:60(sox2 tcr#06tcrβ-p2a-tcrα,氨基酸)
[0560]
mlllllllgpagsglgavvsqhpswvicksgtsvkiecrsldfqattmfwyrqfpkqslmlmatsnegskatyeqgvekdkflinhasltlstltvtsahpedssfyicsargktsprpetqyfgpgtrllvledlknvfppevavfepseaeishtqkatlvclatgfypdhvelswwvngkevhsgvctdpqplkeqpalndsryclssrlrvsatfwqnprnhfrcqvqfyglsendewtqdrakpvtqivsaeawgradcgftsesyqqgvlsatilyeillgkatlyavlvsalvlmamvkrkdsrggsgatnfsllkqagdveenpgpmesslggvllilwlqvdwvksqkieqnsealniqegktatltcnytnyspaylqwyrqdpgrgpvflllirenekekrkerlkvtfdttlkqslfhitasqpadsatylcalghkltfgggtrvlvkpniqnpdpavyqlrdskssdksvclftdfdsqtnvsqskdsdvyitdkcvldmrsmdfksnsavawsnksdfacanafnnsiipedtffpspesscdvklveksfetdtnlnfqnlsvigfrilllkvagfnllmtlrlwss
[0561]
seq id no.:61(sox2 tcr#06tcrvβ,氨基酸)
[0562]
gavvsqhpswvicksgtsvkiecrsldfqattmfwyrqfpkqslmlmatsnegskatyeqgvekdkflinhasltlstltvtsahpedssfyicsargktsprpetqyfgpgtrllvle
[0563]
seq id no.:62(sox2 tcr#06cdr1β,氨基酸)
[0564]
dfqatt
[0565]
seq id no.:63(sox2 tcr#06cdr2β,氨基酸)
[0566]
snegska
[0567]
seq id no.:64(sox2 tcr#06cdr3β,氨基酸)
[0568]
sargktsprpetqy
[0569]
seq id no.:65(sox2 tcr#06cdr3β-连接,氨基酸)
[0570]
csargktsprpetqyf
[0571]
seq id no.:66(sox2 tcr#06tcrvα,氨基酸)
[0572]
sqkieqnsealniqegktatltcnytnyspaylqwyrqdpgrgpvflllirenekekrkerlkvtfdttlkqslfhitasqpadsatylcalghkltfgggtrvlvkpn
[0573]
seq id no.:67(sox2 tcr#06cdr1α,氨基酸)
[0574]
nyspay
[0575]
seq id no.:68(sox2 tcr#06cdr2α,氨基酸)
[0576]
ireneke
[0577]
seq id no.:69(sox2 tcr#06cdr3α,氨基酸)
[0578]
alghklt
[0579]
seq id no.:70(sox2 tcr#06cdr3α-连接,氨基酸)
[0580]
calghkltf
[0581]
seq id no.:71(sox2 tcr#07tcrβ-p2a-tcrα,密码子优化的核苷酸)
[0582]
atgggcacaagactccttttctgggtcgccttttgtctgcttggagccgatcataccggcgccggcgtgagccagtctcccagcaataaggtcaccgagaagggcaaagatgtggagctgagatgcgaccctatttctggccataccgccctgtactggtacagacaatctctgggacaggggctagagttcctgatctactttcagggcaatagcgcccccgacaaatctggacttcctagcgacaggttttctgccgagagaacaggaggatctgtttctaccctgaccatccagagaacacagcaggaggattctgccgtgtacctgtgtgccagcagaagaacaggatggagctacaatgagcagttctttggccctggaaccagactgacagtgctggaggacctgaagaacgtgttccccccagaggtggccgtgttcgagcctagcgaggccgagatcagccacacccagaaagccaccctcgtgtgcctggccaccggcttttaccccgaccacgtggaactgtcttggtgggtcaacggcaaagaggtgcacagcggcgtctgcaccgacccccagcccctgaaagagcagcccgccctgaacgacagccggtactgtctgagcagcagactgagagtgtccgccaccttctggcagaacccccggaaccacttcagatgccaggtgcagttctacggcctgagcgagaacgacgagtggacccaggaccgggccaagcccgtgacccagatcgtgtctgctgaggcctggggcagagccgattgcggcttcaccagcgagagctaccagcagggcgtgctgagcgccaccatcctgtacgagatcctgctgggcaaggccaccctgtacgccgtgctggtgtccgccctggtgctgatggccatggtcaagcggaaggacagccggggcggttccggagccacgaacttctctctgttaaagcaagcaggagacgtggaagaaaaccccggtcccatgatcagcctgagagtcctgctcgtgattctgtggctgcaactgtcttgggtttggagccagagaaaagaagtggagcaggatcctggcccctttaatgtgcctgaaggagctacagtggccttcaactgcacatacagcaacagcgcctcacagagcttcttctggtacagacaggactgcaggaaggagcctaagctgctgatgtctgtgtatagcagcggcaatgaggatggcagatttacagcccagctgaaccgggcttctcagtacatctctctgctgatcagggatagcaagctgagcgattctgctacatacctctgcgtggtgtacgtggagtctggaggcagctatatccctacattcggcagaggaacaagcctgattgtgcacccctatatccagaatcccgaccctgctgtgtaccagctgcgggacagcaagagcagcgacaagagcgtgtgcctgttcaccgacttcgacagccagaccaacgtgtcccagagcaaggacagcgacgtgtacatcaccgataagtgcgtgctggacatgcggagcatggacttcaagagcaacagcgccgtggcctggtccaacaagagcgacttcgcctgcgccaacgccttcaacaacagcattatccccgaggacacattcttcccaagccccgagagcagctgcgacgtgaagctggtggaaaagagcttcgagacagacaccaacctgaacttccagaacctcagcgtgatcggctt
ccggatcctgctgctgaaggtggccggcttcaacctgctgatgaccctgcggctgtggtccagctga
[0583]
seq id no.:72(sox2 tcr#07tcrβ-p2a-tcrα,氨基酸)
[0584]
mgtrllfwvafcllgadhtgagvsqspsnkvtekgkdvelrcdpisghtalywyrqslgqglefliyfqgnsapdksglpsdrfsaertggsvstltiqrtqqedsavylcasrrtgwsyneqffgpgtrltvledlknvfppevavfepseaeishtqkatlvclatgfypdhvelswwvngkevhsgvctdpqplkeqpalndsryclssrlrvsatfwqnprnhfrcqvqfyglsendewtqdrakpvtqivsaeawgradcgftsesyqqgvlsatilyeillgkatlyavlvsalvlmamvkrkdsrggsgatnfsllkqagdveenpgpmislrvllvilwlqlswvwsqrkeveqdpgpfnvpegatvafnctysnsasqsffwyrqdcrkepkllmsvyssgnedgrftaqlnrasqyisllirdsklsdsatylcvvyvesggsyiptfgrgtslivhpyiqnpdpavyqlrdskssdksvclftdfdsqtnvsqskdsdvyitdkcvldmrsmdfksnsavawsnksdfacanafnnsiipedtffpspesscdvklveksfetdtnlnfqnlsvigfrilllkvagfnllmtlrlwss
[0585]
seq id no.:73(sox2 tcr#07tcrvβ,氨基酸)
[0586]
gagvsqspsnkvtekgkdvelrcdpisghtalywyrqslgqglefliyfqgnsapdksglpsdrfsaertggsvstltiqrtqqedsavylcasrrtgwsyneqffgpgtrltvle
[0587]
seq id no.:74(sox2 tcr#07cdr1β,氨基酸)
[0588]
sghta
[0589]
seq id no.:75(sox2 tcr#07cdr2β,氨基酸)
[0590]
fqgnsa
[0591]
seq id no.:76(sox2 tcr#07cdr3β,氨基酸)
[0592]
asrrtgwsyneqf
[0593]
seq id no.:77(sox2 tcr#07cdr3β-连接,氨基酸)
[0594]
casrrtgwsyneqff
[0595]
seq id no.:78(sox2 tcr#07tcrvα,氨基酸)
[0596]
rkeveqdpgpfnvpegatvafnctysnsasqsffwyrqdcrkepkllmsvyssgnedgrftaqlnrasqyisllirdsklsdsatylcvvyvesggsyiptfgrgtslivhpy
[0597]
seq id no.:79(sox2 tcr#07cdr1α,氨基酸)
[0598]
nsasqs
[0599]
seq id no.:80(sox2 tcr#07cdr2α,氨基酸)
[0600]
vyssgn
[0601]
seq id no.:81(sox2 tcr#07cdr3α,氨基酸)
[0602]
vvyvesggsyipt
[0603]
seq id no.:82(sox2 tcr#07cdr3α-连接,氨基酸)
[0604]
cvvyvesggsyiptf
[0605]
seq id no.:83(sox2 tcr#09tcrβ-p2a-tcrα,密码子优化的核苷酸)
[0606]
atggatacctggctcgtctgttgggccatcttttctctgctgaaagctggcctgacagaacctgaggttacacagacacctagccaccaggtgactcagatgggacaggaagtgatcctgagatgtgtgcccatcagcaatcacctgtacttttattggtacaggcagattctgggccagaaggtcgaattcctggtgagcttttacaataacgagattagcgagaaatccgaaatcttcgacgatcagttctcagtggagagacctgatggcagcaattttaccctgaagattcgcagcacaaagctggaggatagcgccatgtacttttgtgcgagttctagacgaggcgggcctattgaaacccagtattttgg
ccctggaacaagactgctggtccttgaggacctgaagaacgtgttccccccagaggtggccgtgttcgagcctagcgaggccgagatcagccacacccagaaagccaccctcgtgtgcctggccaccggcttttaccccgaccacgtggaactgtcttggtgggtcaacggcaaagaggtgcacagcggcgtctgcaccgacccccagcccctgaaagagcagcccgccctgaacgacagccggtactgtctgagcagcagactgagagtgtccgccaccttctggcagaacccccggaaccacttcagatgccaggtgcagttctacggcctgagcgagaacgacgagtggacccaggaccgggccaagcccgtgacccagatcgtgtctgctgaggcctggggcagagccgattgcggcttcaccagcgagagctaccagcagggcgtgctgagcgccaccatcctgtacgagatcctgctgggcaaggccaccctgtacgccgtgctggtgtccgccctggtgctgatggccatggtcaagcggaaggacagccggggcggttccggagccacgaacttctctctgttaaagcaagcaggagacgtggaagaaaaccccggtcccatgatgaagagcctgcgagtcctcctggtgattctgtggctgcaactttcttgggtgtggtctcagcagaaagaagtggagcaggatcctggacctctgtctgtgcctgaaggagctattgtgagcctcaattgtacttacagcaatagcgccttccagtacttcatgtggtaccggcagtacagcaggaagggccctgaactgctcatgtatacctattctagcggcaataaggaggatggcaggtttacagcccaggtggacaagagctccaagtatataagtttattcatcagagatagccagcctagcgattctgccacctacctgtgtgccatgtctgccgacaatgcaggtaatatgctgacatttggaggcggaacaaggctgatggtgaaaccccacatccagaaccccgaccccgctgtgtaccagctgcgggacagcaagagcagcgacaagagcgtgtgcctgttcaccgacttcgacagccagaccaacgtgtcccagagcaaggacagcgacgtgtacatcaccgataagtgcgtgctggacatgcggagcatggacttcaagagcaacagcgccgtggcctggtccaacaagagcgacttcgcctgcgccaacgccttcaacaacagcattatccccgaggacacattcttcccaagccccgagagcagctgcgacgtgaagctggtggaaaagagcttcgagacagacaccaacctgaacttccagaacctcagcgtgatcggcttccggatcctgctgctgaaggtggccggcttcaacctgctgatgaccctgcggctgtggtccagctga
[0607]
seq id no.:84(sox2 tcr#09tcrβ-p2a-tcrα,氨基酸)
[0608]
mdtwlvcwaifsllkagltepevtqtpshqvtqmgqevilrcvpisnhlyfywyrqilgqkveflvsfynneisekseifddqfsverpdgsnftlkirstkledsamyfcassrrggpietqyfgpgtrllvledlknvfppevavfepseaeishtqkatlvclatgfypdhvelswwvngkevhsgvctdpqplkeqpalndsryclssrlrvsatfwqnprnhfrcqvqfyglsendewtqdrakpvtqivsaeawgradcgftsesyqqgvlsatilyeillgkatlyavlvsalvlmamvkrkdsrggsgatnfsllkqagdveenpgpmmkslrvllvilwlqlswvwsqqkeveqdpgplsvpegaivslnctysnsafqyfmwyrqysrkgpellmytyssgnkedgrftaqvdksskyislfirdsqpsdsatylcamsadnagnmltfgggtrlmvkphiqnpdpavyqlrdskssdksvclftdfdsqtnvsqskdsdvyitdkcvldmrsmdfksnsavawsnksdfacanafnnsiipedtffpspesscdvklveksfetdtnlnfqnlsvigfrilllkvagfnllmtlrlwss
[0609]
seq id no.:85(sox2 tcr#09tcrvβ,氨基酸)
[0610]
epevtqtpshqvtqmgqevilrcvpisnhlyfywyrqilgqkveflvsfynneisekseifddqfsverpdgsnftlkirstkledsamyfcassrrggpietqyfgpgtrllvle
[0611]
seq id no.:86(sox2 tcr#09cdr1β,氨基酸)
[0612]
snhly
[0613]
seq id no.:87(sox2 tcr#09cdr2β,氨基酸)
[0614]
fynnei
[0615]
seq id no.:88(sox2 tcr#09cr3β,氨基酸)
[0616]
assrrggpietqy
[0617]
seq id no.:89(sox2 tcr#09cr3β-连接,氨基酸)
[0618]
cassrrggpietqyf
[0619]
seq id no.:90(sox2 tcr#09tcrvα,氨基酸)
[0620]
qkeveqdpgplsvpegaivslnctysnsafqyfmwyrqysrkgpellmytyssgnkedgrftaqvdksskyislfirdsqpsdsatylcamsadnagnmltfgggtrlmvkph
[0621]
seq id no.:91(sox2 tcr#09cdr1α,氨基酸)
[0622]
nsafqy
[0623]
seq id no.:92(sox2 tcr#09cdr2α,氨基酸)
[0624]
tyssgn
[0625]
seq id no.:93(sox2 tcr#09cdr3α,氨基酸)
[0626]
amsadnagnmlt
[0627]
seq id no.:94(sox2 tcr#09cdr3α-连接,氨基酸)
[0628]
camsadnagnmltf
[0629]
seq id no.:95(sox2 tcr#10tcrβ-p2a-tcrα,密码子优化的核苷酸)
[0630]
atgaccattcgactgctgtgctacatgggcttctacttcctgggagctggactgatggaagccgacatctaccaaacacccagatacctggtgatcggaacaggcaagaagatcaccctggagtgtagccagacaatgggacacgacaagatgtactggtaccagcaggatcctggaatggaactgcacctgatccactacagctatggcgtgaacagcacagagaaaggcgatctgagcagcgagtctacagtgagcagaatcagaaccgagcacttccctctgacactggaatctgctagacctagccacacaagccagtacctgtgtgctagctctagaggacctgaggccttttttggacagggaacaagactgacagtggtggaggatctgaacaaggtgttccccccagaggtggccgtgttcgagccttctgaggccgagatctcccacacccagaaagccaccctcgtgtgcctggccaccggctttttccccgaccacgtggaactgtcttggtgggtcaacggcaaagaggtgcactccggcgtgtgcaccgatccccagcctctgaaagaacagcccgccctgaacgacagccggtactgcctgagcagcagactgagagtgtccgccaccttctggcagaacccccggaaccacttcagatgccaggtgcagttctacggcctgagcgagaacgacgagtggacccaggacagagccaagcccgtgacacagatcgtgtctgccgaagcctggggcagagccgattgcggctttacctccgtgtcctatcagcagggcgtgctgagcgccacaatcctgtacgagatcctgctgggcaaggccaccctgtacgccgtgctggtgtctgccctggtgctgatggccatggtcaagcggaaggacttcggttccggagccacgaacttctctctgttaaagcaagcaggagacgtggaagaaaaccccggtcccatgaagacctttgccggattctcattcctatttctctggctgcagctggattgtatgagcagaggcgaagatgtggaacagagcctgtttctgagcgtgagagagggcgatagctctgtgatcaattgcacatacacggatagcagcagcacctacctgtactggtataaacaggagccgggcgcgggcctgcaactgctgacatacatcttcagcaatatggatatgaagcaggaccagaggttgaccgtcttactcaataagaaagacaagcacctgtctctgagaatcgctgacactcagactggcgatagcgccatctacttctgtgctggacctcttggcggatctcagggaaatcttatcttcggtaagggcacaaagctgagcgtgaagcccaatatacaaaacccagaccccgccgtgtaccagctgcgggacagcaagagcagcgacaagagcgtgtgcctgttcaccgacttcgacagccagaccaacgtgtcccagagcaaggacagcgacgtgtacatcaccgataagtgcgtgctggacatgcggagcatggacttcaagagcaacagcgccgtggcctggtccaacaagagcgacttcgcctgcgccaacgccttcaacaacagcattatccccgaggacacattcttcccaagccccgagagcagctgcgacgtgaagctggtggaaaagagcttcgagacagacaccaacctgaacttccagaacctcagcgtgatcggcttccggatcctgctgctgaaggtggccggcttcaacctgctgatgaccctgcggctgtggtccagctga
[0631]
seq id no.:96(sox2 tcr#10tcrβ-p2a-tcrα,氨基酸)
[0632]
mtirllcymgfyflgaglmeadiyqtprylvigtgkkitlecsqtmghdkmywyqqdpgmelhlihysy
gvnstekgdlssestvsrirtehfpltlesarpshtsqylcassrgpeaffgqgtrltvvedlnkvfppevavfepseaeishtqkatlvclatgffpdhvelswwvngkevhsgvctdpqplkeqpalndsryclssrlrvsatfwqnprnhfrcqvqfyglsendewtqdrakpvtqivsaeawgradcgftsvsyqqgvlsatilyeillgkatlyavlvsalvlmamvkrkdfgsgatnfsllkqagdveenpgpmktfagfsflflwlqldcmsrgedveqslflsvregdssvinctytdssstylywykqepgaglqlltyifsnmdmkqdqrltvllnkkdkhlslriadtqtgdsaiyfcagplggsqgnlifgkgtklsvkpniqnpdpavyqlrdskssdksvclftdfdsqtnvsqskdsdvyitdkcvldmrsmdfksnsavawsnksdfacanafnnsiipedtffpspesscdvklveksfetdtnlnfqnlsvigfrilllkvagfnllmtlrlwss
[0633]
seq id no.:97(sox2 tcr#10tcrvβ,氨基酸)
[0634]
eadiyqtprylvigtgkkitlecsqtmghdkmywyqqdpgmelhlihysygvnstekgdlssestvsrirtehfpltlesarpshtsqylcassrgpeaffgqgtrltvve
[0635]
seq id no.:98(sox2 tcr#10 cdr1β,氨基酸)
[0636]
mghdk
[0637]
seq id no.:99(sox2 tcr#10 cdr2β,氨基酸)
[0638]
sygvns
[0639]
seq id no.:100(sox2 tcr#10 cr3β,氨基酸)
[0640]
assrgpeaf
[0641]
seq id no.:101(sox2 tcr#10 cr3β-连接,氨基酸)
[0642]
cassrgpeaff
[0643]
seq id no.:102(sox2 tcr#10 tcrvα,氨基酸)
[0644]
gedveqslflsvregdssvinctytdssstylywykqepgaglqlltyifsnmdm
[0645]
kqdqrltvllnkkdkhlslriadtqtgdsaiyfcagplggsqgnlifgkgtklsvk
[0646]
pn
[0647]
seq id no.:103(sox2 tcr#10 cdr1α,氨基酸)
[0648]
dsssty
[0649]
seq id no.:104(sox2 tcr#10 cdr2α,氨基酸)
[0650]
ifsnmdm
[0651]
seq id no.:105(sox2 tcr#10 cdr3α,氨基酸)
[0652]
agplggsqgnli
[0653]
seq id no.:106(sox2 tcr#10 cdr3α-连接,氨基酸)
[0654]
cagplggsqgnlif
[0655]
seq id no.:107(sox2 tcr#11tcrβ-p2a-tcrα,密码子优化的核苷酸)atgggacctcagcttcttggatacgttgtgctgtgtctgcttggagccggacctttagaggctcaggttacccagaaccccagatacctgattacagtgacaggcaagaagctgaccgtgacctgtagccagaacatgaaccacgagtacatgagctggtacagacaggatcctggactgggactccggcaaatttactacagcatgaacgtggaggtgaccgataaaggagatgtgcccgaaggctacaaggtgagcaggaaggagaagaggaatttccccctgatcctggaatctcctagccctaatcagaccagcctgtacttctgtgccagcagcccaaggtctcccgaaggaggaagagcctacaatgagcagttctttggccctggaacaagactgaccgtgctggaagacctgaagaacgtgttccccccagaggtggccgtgttcgagcctagcgaggccgagatcagccacacccagaaagccaccctcgtgtgcctggccaccggcttttaccccgaccacgtggaactgtcttggtgggtcaacggcaaagaggtgcacagcggcgtctgcaccgacccccagcccctgaaagagcagcccgccctgaacgaca
gccggtactgtctgagcagcagactgagagtgtccgccaccttctggcagaacccccggaaccacttcagatgccaggtgcagttctacggcctgagcgagaacgacgagtggacccaggaccgggccaagcccgtgacccagatcgtgtctgctgaggcctggggcagagccgattgcggcttcaccagcgagagctaccagcagggcgtgctgagcgccaccatcctgtacgagatcctgctgggcaaggccaccctgtacgccgtgctggtgtccgccctggtgctgatggccatggtcaagcggaaggacagccggggcggttccggagccacgaacttctctctgttaaagcaagcaggagacgtggaagaaaaccccggtcccatggagaagatgctggagtgtgcgttcatcgttctgtggctgcaacttggatggctgtctggagaggatcaggttacacagtctcctgaagccctgagactgcaagaaggagagagctcatcgttgaactgcagctacacagtgtctggactgagaggcctgttctggtataggcaggatccgggcaaaggacctgagttcctgtttaccctctattcagctggggaggagaaggagaaggagagactgaaggctacactgaccaagaaggagagctttcttcacattactgcccccaaacctgaggattctgccacatacctgtgtgctgctctggacagagacaattatggccaaaatttcgtgtttggccctggaaccagactgtctgtgctgccttacattcagaaccccgatcctgccgtgtaccagctgcgggacagcaagagcagcgacaagagcgtgtgcctgttcaccgacttcgacagccagaccaacgtgtcccagagcaaggacagcgacgtgtacatcaccgataagtgcgtgctggacatgcggagcatggacttcaagagcaacagcgccgtggcctggtccaacaagagcgacttcgcctgcgccaacgccttcaacaacagcattatccccgaggacacattcttcccaagccccgagagcagctgcgacgtgaagctggtggaaaagagcttcgagacagacaccaacctgaacttccagaacctcagcgtgatcggcttccggatcctgctgctgaaggtggccggcttcaacctgctgatgaccctgcggctgtggtccagctga
[0656]
seq id no.:108(sox2 tcr#11tcrβ-p2a-tcrα,氨基酸)
[0657]
mgpqllgyvvlcllgagpleaqvtqnprylitvtgkkltvtcsqnmnheymswyrqdpglglrqiyysmnvevtdkgdvpegykvsrkekrnfplilespspnqtslyfcassprspeggrayneqffgpgtrltvledlknvfppevavfepseaeishtqkatlvclatgfypdhvelswwvngkevhsgvctdpqplkeqpalndsryclssrlrvsatfwqnprnhfrcqvqfyglsendewtqdrakpvtqivsaeawgradcgftsesyqqgvlsatilyeillgkatlyavlvsalvlmamvkrkdsrggsgatnfsllkqagdveenpgpmekmlecafivlwlqlgwlsgedqvtqspealrlqegessslncsytvsglrglfwyrqdpgkgpeflftlysageekekerlkatltkkesflhitapkpedsatylcaaldrdnygqnfvfgpgtrlsvlpyiqnpdpavyqlrdskssdksvclftdfdsqtnvsqskdsdvyitdkcvldmrsmdfksnsavawsnksdfacanafnnsiipedtffpspesscdvklveksfetdtnlnfqnlsvigfrilllkvagfnllmtlrlwss
[0658]
seq id no.:109(sox2 tcr#11tcrvβ,氨基酸)
[0659]
eaqvtqnprylitvtgkkltvtcsqnmnheymswyrqdpglglrqiyysmnvevtdkgdvpegykvsrkekrnfplilespspnqtslyfcassprspeggrayneqffgpgtrltvle
[0660]
seq id no.:110(sox2 tcr#11cdr1β,氨基酸)
[0661]
mnhey
[0662]
seq id no.:111(sox2 tcr#11cdr2β,氨基酸)
[0663]
smnvev
[0664]
seq id no.:112(sox2 tcr#11cdr3β,氨基酸)
[0665]
assprspeggrayneqf
[0666]
seq id no.:113(sox2 tcr#11cdr3β-连接,氨基酸)
[0667]
cassprspeggrayneqff
[0668]
seq id no.:114(sox2 tcr#11tcrvα,氨基酸)
[0669]
edqvtqspealrlqegessslncsytvsglrglfwyrqdpgkgpeflftlysageekekerlkatltkk
esflhitapkpedsatylcaaldrdnygqnfvfgpgtrlsvlpy
[0670]
seq id no.:115(sox2 tcr#11cdr1α,氨基酸)
[0671]
vsglrg
[0672]
seq id no.:116(sox2 tcr#11cdr2α,氨基酸)
[0673]
lysagee
[0674]
seq id no.:117(sox2 tcr#11cdr3α,氨基酸)
[0675]
aaldrdnygqnfv
[0676]
seq id no.:118(sox2 tcr#11cdr3α-连接,氨基酸)
[0677]
caaldrdnygqnfvf
[0678]
seq id no.:119(sox2 tcr#13tcrβ-p2a-tcrα,密码子优化的核苷酸)
[0679]
atgaccattcgactgctgtgctacatgggcttctacttcctgggagctggactgatggaagccgacatctaccaaacacccagatacctggtgatcggaacaggcaagaagatcaccctggagtgtagccagacaatgggacacgacaagatgtactggtaccagcaggatcctggaatggaactgcacctgatccactacagctatggcgtgaacagcacagagaaaggcgatctgagcagcgagtctacagtgagcagaatcagaaccgagcacttccctctgacactggaatctgctagacctagccacacaagccagtacctgtgtgcttctagcgagaacagcaatcagccccagcatttcggcgatggcacccgcttgtccatcttggaggatctgaacaaggtgttccccccagaggtggccgtgttcgagccttctgaggccgagatctcccacacccagaaagccaccctcgtgtgcctggccaccggctttttccccgaccacgtggaactgtcttggtgggtcaacggcaaagaggtgcactccggcgtgtgcaccgatccccagcctctgaaagaacagcccgccctgaacgacagccggtactgcctgagcagcagactgagagtgtccgccaccttctggcagaacccccggaaccacttcagatgccaggtgcagttctacggcctgagcgagaacgacgagtggacccaggacagagccaagcccgtgacacagatcgtgtctgccgaagcctggggcagagccgattgcggctttacctccgtgtcctatcagcagggcgtgctgagcgccacaatcctgtacgagatcctgctgggcaaggccaccctgtacgccgtgctggtgtctgccctggtgctgatggccatggtcaagcggaaggacttcggttccggagccacgaacttctctctgttaaagcaagcaggagacgtggaagaaaaccccggtcccatgaccagcattagagccgtgttcatcttcctgtggctgcagctggatctggtgaatggcgagaatgtggaacagcatcctagcacactgtctgttcaggagggcgattctgccgtgatcaagtgcacctatagcgattctgccagcaactacttcccttggtacaagcaggagctgggcaaaggacctcagctgatcatcgacatcaggagcaatgtgggagagaagaaggatcagagaatcgccgtgacattaaataagaccgccaagcactttagcctgcacatcacagagacacaacctgaggattctgccgtgtacttttgtgccgcccctaacgacatgagattcggcgccgggacacgtctgacagtgaagcccaacatccaaaatcctgatcccgccgtgtaccagctgcgggacagcaagagcagcgacaagagcgtgtgcctgttcaccgacttcgacagccagaccaacgtgtcccagagcaaggacagcgacgtgtacatcaccgataagtgcgtgctggacatgcggagcatggacttcaagagcaacagcgccgtggcctggtccaacaagagcgacttcgcctgcgccaacgccttcaacaacagcattatccccgaggacacattcttcccaagccccgagagcagctgcgacgtgaagctggtggaaaagagcttcgagacagacaccaacctgaacttccagaacctcagcgtgatcggcttccggatcctgctgctgaaggtggccggcttcaacctgctgatgaccctgcggctgtggtccagctga
[0680]
seq id no.:120(sox2 tcr#13tcrβ-p2a-tcrα,氨基酸)
[0681]
mtirllcymgfyflgaglmeadiyqtprylvigtgkkitlecsqtmghdkmywyqqdpgmelhlihysygvnstekgdlssestvsrirtehfpltlesarpshtsqylcassensnqpqhfgdgtrlsiledlnkvfppevavfepseaeishtqkatlvclatgffpdhvelswwvngkevhsgvctdpqplkeqpalndsryclssrlrvsatfwqnprnhfrcqvqfyglsendewtqdrakpvtqivsaeawgradcgftsvsyqqgvlsatilyeillgkatlyavlvsalvlm
amvkrkdfgsgatnfsllkqagdveenpgpmtsiravfiflwlqldlvngenveqhpstlsvqegdsavikctysdsasnyfpwykqelgkgpqliidirsnvgekkdqriavtlnktakhfslhitetqpedsavyfcaapndmrfgagtrltvkpniqnpdpavyqlrdskssdksvclftdfdsqtnvsqskdsdvyitdkcvldmrsmdfksnsavawsnksdfacanafnnsiipedtffpspesscdvklveksfetdtnlnfqnlsvigfrilllkvagfnllmtlrlwss
[0682]
seq id no.:121(sox2 tcr#13tcrvβ,氨基酸)
[0683]
eadiyqtprylvigtgkkitlecsqtmghdkmywyqqdpgmelhlihysygvnstekgdlssestvsrirtehfpltlesarpshtsqylcassensnqpqhfgdgtrlsileseq id no.:122(sox2 tcr#13cdr1β,氨基酸)
[0684]
mghdk
[0685]
seq id no.:123(sox2 tcr#13cdr2β,氨基酸)
[0686]
sygvns
[0687]
seq id no.:124(sox2 tcr#13cdr3β,氨基酸)
[0688]
assensnqpqh
[0689]
seq id no.:125(sox2 tcr#13cdr3β-连接,氨基酸)
[0690]
cassensnqpqhf
[0691]
seq id no.:126(sox2 tcr#13tcrvα,氨基酸)
[0692]
genveqhpstlsvqegdsavikctysdsasnyfpwykqelgkgpqliidirsnvgekkdqriavtlnktakhfslhitetqpedsavyfcaapndmrfgagtrltvkpn
[0693]
seq id no.:127(sox2 tcr#13cdr1α,氨基酸)
[0694]
dsasny
[0695]
seq id no.:128(sox2 tcr#13cdr2α,氨基酸)
[0696]
irsnvge
[0697]
seq id no.:129(sox2 tcr#13cdr3α,氨基酸)
[0698]
aapndmr
[0699]
seq id no.:130(sox2 tcr#13cdr3α-连接,氨基酸)
[0700]
caapndmrf
[0701]
seq id no.:131(sox2 tcr#15tcrβ-p2a-tcrα,密码子优化的核苷酸)
[0702]
atgggcacatctcttctctgttgggttgtgctgggctttctgggcacagatcatacaggagctggagttagccagtctcctaggtataaggtgaccaagaggggacaggatgtggctctgagatgtgaccctatttctggccacgtgagcctttactggtacagacaagctctgggacaaggacccgagtttctgacctacttcaactacgaggcccagcaggataaatctggactgcccaacgacagattcagcgccgaaagacctgaaggctctatcagcacactgaccattcagagaacagagcagagggattctgccatgtacagatgcgccagctctctttggggaagagccgttgatgagcagttttttggccctggaaccagactgacagttctggaggacctgaagaacgtgttccccccagaggtggccgtgttcgagcctagcgaggccgagatcagccacacccagaaagccaccctcgtgtgcctggccaccggcttttaccccgaccacgtggaactgtcttggtgggtcaacggcaaagaggtgcacagcggcgtctgcaccgacccccagcccctgaaagagcagcccgccctgaacgacagccggtactgtctgagcagcagactgagagtgtccgccaccttctggcagaacccccggaaccacttcagatgccaggtgcagttctacggcctgagcgagaacgacgagtggacccaggaccgggccaagcccgtgacccagatcgtgtctgctgaggcctggggcagagccgattgcggcttcaccagcgagagctaccagcagggcgtgctgagcgccaccatcctgtacgagatcctgctgggcaaggccaccctgtacgccgtgctggtgtccgccctggtgctgatggccatgg
tcaagcggaaggacagccggggcggttccggagccacgaacttctctctgttaaagcaagcaggagacgtggaagaaaaccccggtcccatgaactactctcctggccttgtcagcctgattctgctgctgctgggaagaacaagaggcgatagcgttacacagatggaaggacctgtgacactgtctgaagaggccttcctgaccatcaattgcacctacacagccactggttacccgtcccttttctggtatgtgcagtaccctggagagggactgcaactgctgttaaaggccacaaaagccgacgataagggcagcaataagggctttgaggccacctacaggaaggagacaaccagctttcatctggagaagggaagcgtgcaagtgtctgattcagccgtgtacttttgtgccctgctgggctctaatgactacaagctgagctttggagccggcacaacagtgaccgttagagccaatatccaaaaccccgacccagctgtgtaccagctgcgggacagcaagagcagcgacaagagcgtgtgcctgttcaccgacttcgacagccagaccaacgtgtcccagagcaaggacagcgacgtgtacatcaccgataagtgcgtgctggacatgcggagcatggacttcaagagcaacagcgccgtggcctggtccaacaagagcgacttcgcctgcgccaacgccttcaacaacagcattatccccgaggacacattcttcccaagccccgagagcagctgcgacgtgaagctggtggaaaagagcttcgagacagacaccaacctgaacttccagaacctcagcgtgatcggcttccggatcctgctgctgaaggtggccggcttcaacctgctgatgaccctgcggctgtggtccagctga
[0703]
seq id no.:132(sox2 tcr#15tcrβ-p2a-tcrα,氨基酸)
[0704]
mgtsllcwvvlgflgtdhtgagvsqsprykvtkrgqdvalrcdpisghvslywyrqalgqgpefltyfnyeaqqdksglpndrfsaerpegsistltiqrteqrdsamyrcasslwgravdeqffgpgtrltvledlknvfppevavfepseaeishtqkatlvclatgfypdhvelswwvngkevhsgvctdpqplkeqpalndsryclssrlrvsatfwqnprnhfrcqvqfyglsendewtqdrakpvtqivsaeawgradcgftsesyqqgvlsatilyeillgkatlyavlvsalvlmamvkrkdsrggsgatnfsllkqagdveenpgpmnyspglvslillllgrtrgdsvtqmegpvtlseeafltinctytatgypslfwyvqypgeglqlllkatkaddkgsnkgfeatyrkettsfhlekgsvqvsdsavyfcallgsndyklsfgagttvtvraniqnpdpavyqlrdskssdksvclftdfdsqtnvsqskdsdvyitdkcvldmrsmdfksnsavawsnksdfacanafnnsiipedtffpspesscdvklveksfetdtnlnfqnlsvigfrilllkvagfnllmtlrlwss
[0705]
seq id no.:133(sox2 tcr#15tcrvβ,氨基酸)
[0706]
gagvsqsprykvtkrgqdvalrcdpisghvslywyrqalgqgpefltyfnyeaqqdksglpndrfsaerpegsistltiqrteqrdsamyrcasslwgravdeqffgpgtrltvle
[0707]
seq id no.:134(sox2 tcr#15cdr1β,氨基酸)
[0708]
sghvs
[0709]
seq id no.:135(sox2 tcr#15cdr2β,氨基酸)
[0710]
fnyeaq
[0711]
seq id no.:136(sox2 tcr#15cdr3β,氨基酸)
[0712]
asslwgravdeqf
[0713]
seq id no.:137(sox2 tcr#15cr3β-连接,氨基酸)
[0714]
casslwgravdeqff
[0715]
seq id no.:138(sox2 tcr#15tcrvα,氨基酸)
[0716]
gdsvtqmegpvtlseeafltinctytatgypslfwyvqypgeglqlllkatkaddkgsnkgfeatyrkettsfhlekgsvqvsdsavyfcallgsndyklsfgagttvtvran
[0717]
seq id no.:139(sox2 tcr#15cdr1α,氨基酸)
[0718]
atgyps
[0719]
seq id no.:140(sox2 tcr#15cdr2α,氨基酸)
[0720]
atkaddk
[0721]
seq id no.:141(sox2 tcr#15cdr3α,氨基酸)
[0722]
allgsndykls
[0723]
seq id no.:142(sox2 tcr#15cdr3α-连接,氨基酸)
[0724]
callgsndyklsf
[0725]
seq id no.:143(sox2 tcr#16tcrβ-p2a-tcrα,密码子优化的核苷酸)atgtctatcggtctgctgtgctgtgtagcattcagtctactttgggcttctcccgtgaatgctggagttacacaaacccccaagttccaggtgttaaagaccggccagagcatgacactgcagtgtgctcaggacatgaatcacaacagtatgtattggtacagacaggatcccggcatgggactgagactgatctactacagcgcttctgagggaactacagacaaaggagaggtgcccaacggctacaacgtgagcaggctgaacaagagggagtttagcctgagactggaatccgctgccccgtctcagacaagcgtgtacttctgcgcctcttctgagggatacggctatgagcagtattttggccctggcacaagactgacagtgacagaggacctgaagaacgtgttccccccagaggtggccgtgttcgagcctagcgaggccgagatcagccacacccagaaagccaccctcgtgtgcctggccaccggcttttaccccgaccacgtggaactgtcttggtgggtcaacggcaaagaggtgcacagcggcgtctgcaccgacccccagcccctgaaagagcagcccgccctgaacgacagccggtactgtctgagcagcagactgagagtgtccgccaccttctggcagaacccccggaaccacttcagatgccaggtgcagttctacggcctgagcgagaacgacgagtggacccaggaccgggccaagcccgtgacccagatcgtgtctgctgaggcctggggcagagccgattgcggcttcaccagcgagagctaccagcagggcgtgctgagcgccaccatcctgtacgagatcctgctgggcaaggccaccctgtacgccgtgctggtgtccgccctggtgctgatggccatggtcaagcggaaggacagccggggcggttccggagccacgaacttctctctgttaaagcaagcaggagacgtggaagaaaaccccggtcccatgctgctggaacacctactgatcatcctgtggatgcagctgacatgggtgtctggacagcagctgaatcagtctcctcagagcatgttcattcaggagggagaggatgtgagcatgaactgcacatcgtccagcatcttcaacacctggctgtggtataagcaggatcctggagaaggacctgtgctgctgattgccctgtataaagccggagagctgacctctaatggaagactgacagcccagtttggcatcaccagaaaggacagcttcctgaacatctccgcatccattccttctgatgtgggcatctacttctgtgccggccacattacacaaggcggatctgagaagctggtgtttggcaaaggcaccaagctgacagttaacccctacatccagaatcccgatcctgccgtgtaccagctgcgggacagcaagagcagcgacaagagcgtgtgcctgttcaccgacttcgacagccagaccaacgtgtcccagagcaaggacagcgacgtgtacatcaccgataagtgcgtgctggacatgcggagcatggacttcaagagcaacagcgccgtggcctggtccaacaagagcgacttcgcctgcgccaacgccttcaacaacagcattatccccgaggacacattcttcccaagccccgagagcagctgcgacgtgaagctggtggaaaagagcttcgagacagacaccaacctgaacttccagaacctcagcgtgatcggcttccggatcctgctgctgaaggtggccggcttcaacctgctgatgaccctgcggctgtggtccagctga
[0726]
seq id no.:144(sox2 tcr#16tcrβ-p2a-tcrα,氨基酸)
[0727]
msigllccvafsllwaspvnagvtqtpkfqvlktgqsmtlqcaqdmnhnsmywyrqdpgmglrliyysasegttdkgevpngynvsrlnkrefslrlesaapsqtsvyfcassegygyeqyfgpgtrltvtedlknvfppevavfepseaeishtqkatlvclatgfypdhvelswwvngkevhsgvctdpqplkeqpalndsryclssrlrvsatfwqnprnhfrcqvqfyglsendewtqdrakpvtqivsaeawgradcgftsesyqqgvlsatilyeillgkatlyavlvsalvlmamvkrkdsrggsgatnfsllkqagdveenpgpmllehlliilwmqltwvsgqqlnqspqsmfiqegedvsmnctsssifntwlwykqdpgegpvllialykageltsngrltaqfgitrkdsflnisasipsdvgiyfcaghitqggseklvfgkgtkltvnpyiqnpdpavyqlrdskssdksvclftdfdsqtnvsqskdsdvyitdkcvldmrsmdfksnsavawsnksdfacanafnnsiipedtffpspesscdvklveksfetdtnlnfqnlsvigfrilllkvagfnllmtlrlwss
[0728]
seq id no.:145(sox2 tcr#16tcrvβ,氨基酸)
[0729]
nagvtqtpkfqvlktgqsmtlqcaqdmnhnsmywyrqdpgmglrliyysasegttdkgevpngynvsrlnkrefslrlesaapsqtsvyfcassegygyeqyfgpgtrltvte
[0730]
seq id no.:146(sox2 tcr#16cdr1β,氨基酸)
[0731]
mnhns
[0732]
seq id no.:147(sox2 tcr#16cdr2β,氨基酸)
[0733]
sasegt
[0734]
seq id no.:148(sox2 tcr#16cdr3β,氨基酸)
[0735]
assegygyeqy
[0736]
seq id no.:149(sox2 tcr#16cdr3β-连接,氨基酸)
[0737]
cassegygyeqyf
[0738]
seq id no.:150(sox2 tcr#16tcrvα,氨基酸)
[0739]
gqqlnqspqsmfiqegedvsmnctsssifntwlwykqdpgegpvllialykageltsngrltaqfgitrkdsflnisasipsdvgiyfcaghitqggseklvfgkgtkltvnpy
[0740]
seq id no.:151(sox2 tcr#16cdr1α,氨基酸)
[0741]
sifnt
[0742]
seq id no.:152(sox2 tcr#16cdr2α,氨基酸)
[0743]
lykagel
[0744]
seq id no.:153(sox2 tcr#16cdr3α,氨基酸)
[0745]
aghitqggseklv
[0746]
seq id no.:154(sox2 tcr#16cdr3α-连接,氨基酸)
[0747]
caghitqggseklvf
[0748]
seq id no.:155(tcr cα1)
[0749]
iqnpdpavyq lrdskssdks vclftdfdsq tnvsqskdsd vyitdktvldmrsmdfksns avawsnksdf acanafnnsi ipedtffpsp esscdvklveksfetdtnln fqnlsvigfr illlkvagfn llmtlrlwss
[0750]
seq id no:156(tcr cβ2)
[0751]
dlknvfppkv avfepseaei shtqkatlvc latgfypdhv elswwvngkevhsgvstdpq plkeqpalnd sryclssrlr vsatfwqnpr nhfrcqvqfyglsendewtq drakpvtqiv saeawgradc gftsesyqqg vlsatilyeillgkatlyav lvsalvlmam vkrkdsrg
[0752]
seq id no:157(tcr cβ1)
[0753]
dlnkvfppev avfepseaei shtqkatlvc latgffpdhv elswwvngkevhsgvstdpq plkeqpalnd sryclssrlr vsatfwqnpr nhfrcqvqfyglsendewtq drakpvtqiv saeawgradc gftsvsyqqg vlsatilyeillgkatlyav lvsalvlmam vkrkdf
[0754]
seq id no:158(cd8共受体α链,无信号序列)
[0755]
sqfrvspldrtwnlgetvelkcqvllsnptsgcswlfqprgaaasptfllylsqnkpkaaegldtqrfsgkrlgdtfvltlsdfrrenegyyfcsalsnsimyfshfvpvflpakptttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlycnhrnrrrvckcprpvvksgdkpslsaryv
[0756]
seq id no:159(cd8共受体β链同种型1,无信号序列)
[0757]
lqqtpayikvqtnkmvmlsceakislsnmriywlrqrqapssdshheflalwdsakgtihgeeveqeki
avfrdasrfilnltsvkpedsgiyfcmivgspeltfgkgtqlsvvdflpttaqptkkstlkkrvcrlprpetqkgplcspitlgllvagvlvllvslgvaihlccrrrrarlrfmkqfyk
[0758]
seq id no:160(cd8共受体β链同种型2,无信号序列)
[0759]
lqqtpayikvqtnkmvmlsceakislsnmriywlrqrqapssdshheflalwdsakgtihgeeveqekiavfrdasrfilnltsvkpedsgiyfcmivgspeltfgkgtqlsv
[0760]
vdflpttaqptkkstlkkrvcrlprpetqkgplcspitlgllvagvlvllvslgvaihlccrrrrarlrfmkqlrlhplekcsrmdy
[0761]
seq id no:161(cd8共受体β链同种型3,无信号序列)
[0762]
lqqtpayikvqtnkmvmlsceakislsnmriywlrqrqapssdshheflalwdsakgtihgeeveqekiavfrdasrfilnltsvkpedsgiyfcmivgspeltfgkgtqlsvvdflpttaqptkkstlkkrvcrlprpetqkgplcspitlgllvagvlvllvslgvaihlccrrrrarlrfmkqkfnivclkisgfttcccfqilqisreygfgvllqkdigq
[0763]
seq id no:162(cd8共受体β链同种型4,无信号序列)
[0764]
lqqtpayikvqtnkmvmlsceakislsnmriywlrqrqapssdshheflalwdsakgtihgeeveqekiavfrdasrfilnltsvkpedsgiyfcmivgspeltfgkgtqlsvvdflpttaqptkkstlkkrvcrlprpetqkgplcspitlgllvagvlvllvslgvaihlccrrrrarlrfmkqkfnivclkisgfttcccfqilqisreygfgvllqkdigq
[0765]
seq id no:163(cd8共受体β链同种型5,无信号序列)
[0766]
lqqtpayikvqtnkmvmlsceakislsnmriywlrqrqapssdshheflalwdsakgtihgeeveqekiavfrdasrfilnltsvkpedsgiyfcmivgspeltfgkgtqlsvvdflpttaqptkkstlkkrvcrlprpetqkgplcspitlgllvagvlvllvslgvaihlccrrrrarlrfmkqpqgegisgtfvpqclhgyysntttsqkllnpwilkt
[0767]
示例
[0768]
示例1
[0769]
sox2表位的识别及sox2抗原反应性t细胞系的产生
[0770]
多发性骨髓瘤(mm)是由骨髓中产生克隆抗体的浆细胞不受控制的生长引起的。它是美国第二常见的血液系统恶性肿瘤,而且几乎总是致命的。过继细胞疗法(act)是一种新兴的mm治疗方法,但提供可重复有效的护理标准的工作仍在进行中。靶向在mm细胞的表面表达的细胞表面cd19、bcma或cd138抗原的嵌合抗原受体(car)t细胞已经取得了一些成功。不幸的是,许多患者由于抗原阴性mm细胞的过度生长而复发。靶向参与诱导或维持恶性表型的蛋白质可能是成功act的重要途径。转录因子sox2可以调节mm和其他癌症的细胞增殖和自我更新,并代表了act的一个有希望的靶点。
[0771]
方法:使用bimas、syfpeithi、netmhc、iedb和hmmhc(alspach et al,nature 2019)表位预测算法来预测是否有任何sox2衍生的肽与hla-a*02:01等位基因有利结合,该等位基因存在于美国约40%的人群中(iedb人群数据)。这些在电脑中进行的研究确定了17种肽,这些肽被预测为与hla-a*02:01有利结合。
[0772]
为了产生特异于sox2的cd8
+
t细胞系,将来自10个健康hla-a*02:01
+
供体的cd8
+
t细胞与用sox2肽脉冲的自体树突状细胞共培养,所述sox2肽被预测与hla-a*02:01等位基因亲合结合。这个过程产生了10个不同的cd8
+
t细胞系/供体(总共100个系)。在培养10-14天后(“刺激1”),用自体外周血单核细胞重新刺激每个cd8
+
t细胞系,外周血单核细胞用同
一组sox2衍生肽照射和脉冲(“刺激2”)。再重复该过程1-2更多次,总共3-4轮刺激。在最后一次刺激后,测试t细胞系对sox2肽库、单个sox2肽或结合的hla-a*02:01/sox2四聚体的应答。对应答细胞进行分选并快速扩增持续10-14天。按照快速扩增方案,进行靶向杀伤试验。这些试验在下文中进一步描述。
[0773]
示例2
[0774]
t细胞对特定的sox2表位有反应
[0775]
方法:用sox2肽库单独刺激cd8
+
t细胞系,以确定是否有任何t细胞系含有sox2反应性cd8
+
t细胞。简言之,在高尔基抑制剂和高尔基阻断剂的存在下,将来自每个系的50,000-100,000个cd8
+
t细胞与1μg/ml sox2肽、培养基或细胞刺激剂孵育4小时。孵育期结束后,用抗cd8抗体对细胞进行染色,固定并透性化细胞,并用抗ifnγ抗体进行染色。样品在配备有3条激光线的bd canto 2仪器上运行。使用diva software(bd biosciences)获取数据,并使用flowjo(flowjo inc.)进行分析。
[0776]
结果:如果肽刺激后ifnγ
+
cd8
+
t细胞的百分比显著高于背景,则该细胞系被认为是sox2反应性的。图1示出了sox2反应性t细胞系(21.5%ifnγ
+
细胞;上图;供体18575,系3)和不被认为是sox2反应性的细胞系(0.27%ifnγ
+
细胞;下图;供体18575,系4)的示例。对被认为是反应性的细胞系进行了进一步的功能表征。总的来说,根据该试验,49/100个cd8
+
t细胞系是sox2反应性的。
[0777]
示例3
[0778]
对sox2肽特异性的示例性t细胞是hla-a*02:01限制性的
[0779]
对已确认的sox2特异性cd8
+
t细胞系进行hla-a*02:01限制性检查。这是为了确保所观察到的结果不是由于t细胞使用内源性hlai支架蛋白来呈递sox2肽。为了确保sox2肽呈递仅通过hla-a*02:01发生,使用hla-a*02:01
+
t2淋巴母细胞作为肽呈递细胞。t2细胞缺乏对hla介导的内源性肽呈递至关重要的转运蛋白,但t2细胞可以呈递外源性提供的肽(条件是肽与hla亲合结合;loft et al,j immunol 2001)。
[0780]
方法:在高尔基抑制剂和高尔基阻断剂的存在下,将来自每个系的50,000-100,000个cd8
+
t细胞与1μg/ml sox2肽、预加载sox2肽的t2细胞(持续至少1小时,然后进行洗涤)、预加载的t2细胞加肽或培养基孵育4小时。孵育期结束后,用抗cd8抗体对细胞进行染色,固定并透性化细胞,并用抗ifnγ抗体进行染色。样品在配备有3条激光线的bd canto 2仪器上运行。使用diva software(bd biosciences)获取数据,并使用flowjo(flowjo inc.)进行分析。示出了不同孵育条件下ifnγ
+
cd8
+
t细胞的频率。切片上显示了供体和系号。
[0781]
结果:图2示出了示例性cd8
+
t细胞系(供体18648,系2),当(1)t细胞有机会相互呈递sox2肽时,以及当(2)sox2肽呈递仅限于t2细胞时,该细胞系产生相似量的ifnγ。这一结果被解释为表明t细胞系限制于hla-a*02:01。总的来说,47/49个sox2特异性t细胞系是hla-a*02:01限制性的。
[0782]
示例4
[0783]
sox2特异性t细胞系的验证
[0784]
研究了47个sox2特异性和hla-a*02:01限制性的cd8
+
t细胞系对sox2肽的识别。
[0785]
方法:如上所述,用单个肽对50,000-100,000个cd8
+
t细胞进行脉冲,并在4小时后检测ifnγ的产生。简言之,在高尔基抑制剂和高尔基阻断剂的存在下,用1μg/ml单个sox2
肽、培养基或细胞刺激剂刺激来自每个系的50,000-100,000个cd8
+
t细胞持续4小时。孵育期结束后,用抗cd8抗体对细胞进行染色,固定并透性化细胞,并用抗ifnγ抗体进行染色。样品在配备有3条激光线的bd canto 2仪器上运行。使用diva software(bd biosciences)获取数据,并使用flowjo(flowjo inc.)进行分析。示出了ifnγ
+
cd8
+
t细胞的频率。指示了供体和系号以及相应的刺激条件。
[0786]
结果:cd8
+
t细胞系对6种肽有反应。图3提供了ifnγ
+
cd8
+
t细胞在培养基或指示的sox2肽存在下的示例图。从这项研究中,在hla-a*02:01的背景下,以下6种肽被鉴定为潜在的免疫原性:
[0787]
·
sox2肽(58-66)kmaqenpkm(seq id no.:6)
[0788]
·
sox2肽(118-127)tlmkkdkytl(seq id no.:7)
[0789]
·
sox2肽(216-225)ymngsptysm(seq id no.:3)
[0790]
·
sox2肽(275-283)smylpgaev(seq id no.:2)
[0791]
·
sox2肽(277-287)ylpgaevpepa(seq id no.:5)
[0792]
·
sox2肽(306-314)taingtlpl(seq id no.:4)。
[0793]
示例5
[0794]
sox2表位处理
[0795]
进行以下实验以确定如何处理和呈递sox2表位。
[0796]
多发性骨髓瘤是一种浆细胞恶性肿瘤,浆细胞通常表达免疫蛋白酶体(“ip”)。然而,蛋白酶体抑制剂有时被用于治疗多发性骨髓瘤患者(rajkumar et al,nat rev dis primers 2017),它可以改变蛋白酶体亚基的表达,影响蛋白酶体催化能力并改变hla i类配体组。sox2也在小细胞肺癌细胞(rudin et al,nat genet 2012)和胶质母细胞瘤细胞(alonso et al,plos one 2011)中表达。这些实体瘤细胞可能表达标准蛋白酶体(“sp”),并且可以在ifng(由t细胞产生)存在的情况下激活免疫蛋白酶体(ip)。
[0797]
sp和ip切割肽的方式不同。因此,蛋白酶体处理可能潜在地影响靶向sox2肽:hla复合物的免疫治疗的广度、有效性和安全性。例如,靶向sp和ip依赖性肽的tcr免疫治疗可能对骨髓瘤和实体瘤有益。这种tcr免疫治疗在ip亚基丢失的情况下可能仍然有效(greenberg and chapuis et al.,未发表)。仅靶向源自标准蛋白酶体(sp)处理途径的一个或多个表位的tcr免疫治疗在骨髓瘤的情况下可能用处不大或没有用处,但在非造血系统恶性肿瘤中可能有用。相反,靶向源自免疫蛋白酶体(ip)处理途径的一个或多个表位的tcr免疫治疗在骨髓瘤的情况下可能有用,但在实体瘤的情况中用处不大或没有用处。
[0798]
为了解决如何处理sox2表位,293e细胞被修饰以表达标准蛋白酶体(293e-sp)或免疫蛋白酶体(293e-ip);(描述于guillame et al,pnas 2010)。
[0799]
图4示出了通过流式细胞术测定的293e-sp和293-ip细胞中sox2的表达。简言之,将150,000个细胞固定并透性化,并用pe标记的同种型对照或pe标记的抗sox2抗体染色。样品在配备有3条激光线的bd canto 2仪器上运行。使用diva software(bd biosciences)获取数据,并使用flowjo(flowjo inc.)进行分析。图中示出pe通道中的荧光染色强度。
[0800]
方法:在incucyte杀伤试验中使用293e-sp或293e-ip细胞作为靶细胞。图5示意性地说明了实验设计。用rapidred cytolight染料(sartorius)标记293e细胞(sp或ip),并在96孔板中以5,000个细胞/孔的密度铺板过夜,以促进它们粘附在板上。第二天加入对示例4
中所提到的6种不同的sox2肽特异性的t细胞系,或不是sox2特异性的、但与sox2特异性t细胞处于相同快速扩增周期的t细胞。还添加了一种caspase报告试剂,如果caspase 3/7在细胞(sartorius)内具有活性,则会发出绿色荧光。将板加载到incucyte s3系统中,并在两天内以2小时的间隔采集每个孔4张图像。使用incucyte s3软件对凋亡靶细胞(cytolight red
+
caspase 3/7green
+
)的量进行定量。
[0801]
结果:图6示出了在sox2特异性cd8
+
t细胞系存在的情况下凋亡的293e-sp靶细胞的数量。将不相关特异性的t细胞作为对照。附图图例中的方框文本表示诱导最佳杀伤的两个t细胞系——17530系6(特异于sox2 58-66)和22058系19(特异性于sox2 277-287)。这些结果表明sox2表位58-66和277-287被标准蛋白酶体(sp)处理。图7示出了在sox2特异性cd8
+
t细胞系存在的情况下凋亡的293e-ip靶细胞的数量。附图图例中的方框文本表示诱导最佳杀伤的两个t细胞系——17530系6(特异于sox2 58-66)和22058系19(特异性于sox2 277-287)。这些结果表明sox2表位58-66和277-287也被免疫蛋白酶体(ip)处理。sox2 277-287肽序列是sox2所特有的,并且选择对该表位特异的t细胞进行功能表征。
[0802]
示例6
[0803]
sox2(277-287)特异性cd8
+
t细胞杀伤肿瘤细胞
[0804]
为了确定sox2(277-287)特异性t细胞系是否能够识别并杀伤表达sox2的肿瘤细胞,使用来自扩增了sox2(277-287)表位的hla-a*02:01供体的t细胞系进行incucyte杀伤试验。靶细胞包括浆细胞白血病(晚期骨髓瘤)细胞系l363和卵巢癌细胞系ovcar3。
[0805]
方法:如上所述进行incucyte实验,并使用incucyte s3软件对凋亡靶细胞(cytolight rapidred
+
caspase 3/7green
+
)的量进行定量。
[0806]
结果:如图8和图9所示,sox2(277-287)特异性t细胞诱导l363和ovcar3细胞凋亡,表明这些对该表位特异性的t细胞具有功能相关性。
[0807]
示例7
[0808]
sox2(277-287)特异性t细胞的分选和测序
[0809]
在测序之前,将来自不同供体的感兴趣的t细胞系汇集,分成相等的部分,并用不同浓度的相关hla-a*02:01/肽四聚体染色。然后对四聚体
+
细胞(在每种染色条件下的团块和顶部结合物)以及四聚体阴性细胞进行分选并制备用于测序(adaptive biotechnologies和10x genomics)。不同的四聚体浓度允许鉴定强结合的tcr,因为这些tcr将在“顶部结合物”类别中富集,特别是在具有较低四聚体浓度的染色条件下。
[0810]
基于hla-a*02:01/sox2(277-287)四聚体滴定的结果,设计了从五个供体(17861、18315、22058、22087、22214)汇集的t细胞系的染色和分选策略。用1:200(最佳四聚体浓度)和1:2000(低四聚体浓度)hla-a*02:01/sox2(277-287)四聚体对细胞进行染色,并进行分选。示例数据如图10所示。
[0811]
adaptive biotechnologies的样品在分选后进行冷冻(作为细胞颗粒),10x genomics的样品立即进行处理。adaptive biotechnologies的immunoseq分析产生了在样本中发现的tcrβ序列,并允许计算每个tcrβ的倍数富集(通过独特的cdr3序列鉴定)。对单个细胞进行10x genomics测序,并允许在immunoseq中“高度富集”的每个tcrβ与其相应的tcrα配对。表1总结了tcr基因的使用情况。
[0812]
表1某些sox2特异性tcr的基因使用
[0813][0814][0815]
野生型tcra和tcrb序列经过密码子优化,并与p2a自切割肽连接。将互补半胱氨酸残基掺入tra和trb恒定结构域,以增加外源性tcr配对并减少与内源性tcr的错配对(参见,例如,dossa et al.,blood 131:108-120(2018))。
[0816]
使用gibson组装将这些tcr表达盒插入prrlsin载体中,用于慢病毒的产生和在原代cd8
+
t细胞中的测试。
[0817]
示例8
[0818]
原代cd8
+
t细胞中sox2(277-287)特异性tcr的验证
[0819]
方法:在gibson组装后对tcr表达载体进行测序,以确认tcr表达盒成功插入prrlsin载体。使用293t/17包装细胞系和effectene试剂盒(qiagen)产生慢病毒颗粒。使用负磁分离(easy sep试剂盒,stemcell technologies)从健康供体(18648)中分离cd8
+
t细胞,用抗cd3/cd28磁珠(dynabeads)刺激持续4小时,并用从293t/17细胞中收集的编码sox2-tcr的慢病毒颗粒转导。在转导后第5天对转导的cd8
+
t细胞进行评估用于四聚体染色。对sox2-tcr
+
cd8
+
t细胞进行分选用于快速扩增,并评估其对不同肽浓度的反应和靶向杀伤。
[0820]
示例9
[0821]
l363骨髓瘤细胞在人类免疫系统功能的小鼠模型中表现出进行性肿瘤生长,并在体内保留sox2表达
[0822]
通过股动脉内注射给人源化小鼠注射0.5e6或1e6 l363细胞,并跟踪存活情况。通过流式细胞术证实sox2在骨髓浸润的l363细胞中的表达,并将其与体外生长的l363细胞进行比较。
[0823]
示例10
[0824]
附加研究
[0825]
在一项实验中,在高尔基抑制剂和高尔基阻断剂存在的情况下,用不同浓度的sox2 277-287肽(10μg/ml
–
0.01ng/ml)、培养基或细胞刺激剂刺激50,000-100,000个tcr转导的cd8
+
t细胞(来自两个不同的供体)持续4小时。孵育期结束后,用抗cd8抗体对细胞进行染色,固定并透性化细胞,并用抗ifnγ抗体进行染色。样品在配备有3条激光线的bd canto 2仪器上运行。使用diva software(bd biosciences)获取数据,并使用flowjo(flowjo inc.)进行分析。使用非线性回归分析在prism(v9,graphpad)中计算每个tcr的logec
50
。数据如图12所示。在另一项实验中,表达sox2的hla-a2+肿瘤细胞以3:1的比例与sox2-tcr转导的cd8
+
t细胞铺板。在某些情况下,用ifnγ预处理肿瘤细胞,以促进hla-a2表达的增加。将细胞共培养过夜(16-18h),并通过流式细胞术评估cd8
+
t细胞上cd137的表达。共培养设置的方案如图13所示。
[0826]
在另一项实验中,用tcr5或tcr10转导cd8
+
t细胞,并与表达hla-a2和sox2的肿瘤细胞(未经处理或用ifn-γ预处理)孵育过夜。cd137的表达(两个供体的+/-sem)如图14所示。
[0827]
可以组合上述各种实施例以提供进一步的实施例。本说明书中提及和/或申请数据表中列出的所有美国专利、美国专利申请出版物、美国专利申请、外国专利、外国专利申请和非专利出版物(包括于2020年9月24日提交的美国临时专利申请号63/083,069)的全部内容通过引用并入本文。如果需要采用各种专利、申请和出版物的概念来提供另外的实施例,则可以修改实施例的各方面。
[0828]
根据以上详细描述,可以对实施例进行这些和其他改变。通常,在以下权利要求中,所使用的术语不应被解释为将权利要求限于说明书和权利要求中公开的特定实施例,但应被解释为包括所有可能的实施例以及这些权利要求所授权的等效物的完整范围。因此,权利要求不受本公开的限制。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1