一种普适的可降低肿瘤细胞表面PD-L1表达的装置和方法
一种普适的可降低肿瘤细胞表面pd-l1表达的装置和方法
技术领域
1.本发明属于生物技术及医学技术领域,特别涉及一种普适的可降低肿瘤细胞表面pd-l1表达的装置和方法。
背景技术:
2.细胞程序性死亡配体1(programmed cell death 1ligand 1,pd-l1)是由cd274基因编码的一类免疫检查点蛋白,在多种肿瘤细胞中高表达。肿瘤细胞pd-l1的高表达与肿瘤的转移能力、患者死亡率成正相关,通常作为患者愈后不良的重要标志。研究发现,肿瘤细胞表面的pd-l1通过抑制t细胞活化的第二信号来抑制t细胞的活化与增殖,使得t细胞丧失对肿瘤细胞的杀伤作用,引起免疫逃逸。因此,针对性地阻断pd-1/pd-l1信号通路,可增强t细胞对肿瘤细胞的杀伤。多种pd-1/pd-l1抑制剂,通过阻断pd-1/pd-l1通路可以增强t细胞活性以激活抗肿瘤免疫响应,已广泛应用于多种恶性肿瘤的治疗。但是,随着抑制剂的广泛应用,耐药现象也随之出现,且现有抑制剂仅对pd-l1阳性或带有高度微卫星不稳定性或错配修复缺陷基因的不可切除实体瘤的部分患者有效,同时这类抑制剂生产成本昂贵、免疫原性不良反应严重。因此,急需需求一种简便、安全、具有普适性的对肿瘤细胞表面pd-l1的直接调控手段。
3.针对肿瘤表面pd-l1表达调控已有一定的发展,例如中国专利cn202110382332.0,该专利提出了一种可选择性降解肿瘤细胞膜上pd-l1蛋白的多肽,利用小分子控制肿瘤细胞膜蛋白的表达水平。但该方案中多肽的储存条件严格,且时效性较短,无法满足患者长期治疗的需求。再如中国专利cn202110388011.1,该专利提出了一种抑制黑素瘤细胞膜表面pd-l1表达的靶向药物,用于抑制黑素瘤细胞膜表面pd-l1的表达,进一步促进细胞毒性t淋巴细胞活化。但该方案中使用的药物为携带shrna的慢病毒,制约了进一步的临床应用。再如中国专利cn202110627894.7,该专利提出了双氢青篙素类化合物调控三阴乳腺癌细胞pd-l1的表达,但该方案中高剂量的青篙素会带来不可避免的毒副作用。
4.磁热是基于磁性纳米材料在交变磁场作用下产热杀伤肿瘤细胞,具有无组织穿透限制、选择性高、普适范围广、安全性良好、不易产生耐受等优势,在尽可能减小对周边组织损伤的同时抑制肿瘤的生长(acs nano 2020,14,1033-1044,nano lett.2019,19,4287-4296,j.am.chem.soc.2021,143,8116-8128,acs nano 2020,14,1936-1950,acs nano 2019,13,8811-8825,adv.sci.2019,6,1901690)。
技术实现要素:
5.为了克服上述现有技术的缺点,本发明的目的在于提供一种普适的可降低肿瘤细胞表面pd-l1表达的装置和方法,基于磁热降低肿瘤细胞表面pd-l1表达,具有普适、安全的特点。
6.为了实现上述目的,本发明采用的技术方案是:
7.一种普适的可降低肿瘤细胞表面pd-l1表达的装置,包括:交变磁场发生器和可被
肿瘤细胞内吞的磁性纳米材料,所述交变磁场发生器用于产生并向内吞磁性纳米材料的肿瘤细胞施加交变磁场,使所述磁性纳米材料产生磁热和活性氧。
8.在一个实施例中,所述交变磁场发生器产生频率和磁场强度可调节的交变磁场。
9.在一个实施例中,所述交变磁场发生器产生的交变磁场频率为50khz-1mhz,强度为10oe-1000oe。
10.在一个实施例中,所述磁性纳米材料的浓度为10-1000μg fe/ml完全培养基。
11.在一个实施例中,所述磁性纳米材料为铁基磁性纳米材料,例如fept、fe3o4、feco或mfe2o4,其中m为mn、co、ni、zn、cu等金属。
12.在一个实施例中,所述磁热的可测量宏观温度范围为40-50℃。
13.在一个实施例中,所述活性氧包括羟基自由基、单线态氧中的至少一种。
14.本发明还提供了基于所述普适的可降低肿瘤细胞表面pd-l1表达的装置降低肿瘤细胞表面pd-l1表达的方法,包括以下步骤:
15.步骤1、使肿瘤细胞内吞磁性纳米材料;
16.步骤2、对内吞磁性纳米材料后的肿瘤细胞施加交变磁场,所述磁性纳米材料与施加的所述交变磁场在细胞内产生效应,降低所述肿瘤细胞膜表面pd-l1表达量。
17.在一个实施例中,交变磁场作用于肿瘤细胞内磁性纳米材料产生磁热和活性氧,使得其能抑制信号通路pi3k-akt-mtor。
18.与现有技术相比,本发明具有普适性。磁性氧化铁纳米颗粒及交变磁场通过干扰pi3k-akt-mtor通路降低pd-l1蛋白水平,是潜在的安全、经济、有效的肿瘤pd-l1抑制手段。
附图说明
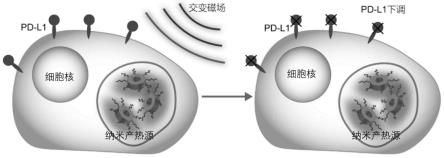
19.图1为所述下调pd-l1方法的示意图。
20.图2为所述装置处理mda-mb-231细胞后pd-l1的蛋白免疫印迹结果。
21.图3为所述装置处理mda-mb-231细胞后pd-l1的免疫荧光结果。
22.图4为所述装置处理mda-mb-231细胞后显著pi3k-akt-mtor信号通路。
23.图5为所述装置处理非小细胞肺癌a549细胞后pd-l1免疫荧光结果。
24.图6为所述装置处理肝癌hepg2细胞后pd-l1的免疫荧光结果。
具体实施方式
25.下面结合附图和实施例详细说明本发明的实施方式。
26.本发明公开了一种新型、普适、安全的可降低肿瘤细胞表面pd-l1表达的装置和方法。其中,装置包括:交变磁场发生器和磁性纳米材料,其中磁性纳米材料可被肿瘤细胞内吞,交变磁场发生器用于产生并向内吞磁性纳米材料的肿瘤细胞施加交变磁场,使磁性纳米材料能够产生磁热和活性氧。
27.本发明可用于实验环境下降低肿瘤细胞表面pd-l1表达的研究与探索,显然,为满足不同环境,本发明的交变磁场发生器产生的交变磁场的频率和磁场强度应该是可调节的。示例地,其交变磁场频率为50khz-1mhz,强度为10oe-1000oe。
28.以fe和完全培养基为参考,本发明磁性纳米材料的浓度为10-1000μg/ml,实验中,可通过输送装置送入,也可直接混合。示例地,本发明的磁性纳米材料为铁基磁性纳米材
料,例如fept、fe3o4、feco或mfe2o4,其中m为mn、co、ni、zn、cu等金属。
29.在交变磁场作用下,本发明磁性纳米材料所产生磁热的可测量宏观温度范围宜为40-50℃。所产生活性氧包括羟基自由基、单线态氧中的至少一种。
30.相应地,如图1所示,本发明可降低肿瘤细胞表面pd-l1表达的方法包括:肿瘤细胞内吞磁性纳米颗粒并施加交变磁场,可减少肿瘤细胞膜表面pd-l1蛋白,由此,可解除肿瘤细胞对免疫系统的控制,促进cd8
+
毒性t淋巴细胞浸润和活化,利于肿瘤生长和发展。
31.实施例1,对mda-mb-231细胞pd-l1的调控
32.1.细胞培养与处理
33.mda-mb-231细胞获取自atcc。mda-mb-231细胞培养在rpmi-1640培养基,并补充10%胎牛血清、100μg/ml链霉素和100μg/ml青霉素。mda-mb-231细胞培养均维持在37℃和5%co2条件下。
34.2.装置处理
35.待肿瘤细胞生长至80%时,加入10-1000μg/ml的磁性纳米颗粒(fe3o4,70nm),与细胞共孵育6~12小时,将孵育好的细胞置于交变磁场(10-1000oe,50khz-1mhz)当中处理0~30分钟。将处理后的细胞继续培养24小时。
36.3.蛋白免疫印迹
37.带有蛋白酶抑制剂的ripa裂解液用于蛋白提取。将裂解产物在4℃下以12000rpm离心10分钟。使用bca蛋白测定试剂盒(thermo fisher)定量上清液中的蛋白质浓度。将相同量的蛋白质添加到每个孔中进行sds-page电泳,然后转移到pvdf膜上。将膜在3%bsa中封闭1小时。将1:1000稀释的一抗与pvdf膜在4℃孵育过夜。将膜用1x tbst洗涤3次,然后在室温下与1:10000稀释的二抗(invitrogen)一起孵育1小时。通过ecl化学发光仪进行显影。我们发现在人乳腺癌mda-mb-231细胞中,经交变磁场装置(10-1000oe,50khz-1mhz)处理后极显著地降低了pd-l1蛋白水平,如图2所示。
38.4.免疫荧光检测
39.将所述装置处理后的细胞在室温下于4%多聚甲醛中固定15分钟,与pd-l1单克隆抗体(invitrogen)4℃孵育过夜,然后与fitc缀合的二抗(武汉三鹰)在室温下孵育1小时。细胞核用dapi染色。使用共聚焦显微镜(nis-elements,ti2)对细胞成像。如图3所示,实验结果同样显示所述装置可以降低pd-l1蛋白水平。
40.5.所述装置调控mda-mb-231细胞中pi3k-akt-mtor的表达
41.pi3k(磷脂酰肌醇激酶)是由调节亚基p85和催化亚基p110构成二聚体。当它与生长因子受体(如egfr)结合后,可改变akt的蛋白结构并使其活化,并以磷酸化作用激活或抑制下游一系列底物如凋亡相关蛋白bad、caspase9活性,从而调节细胞的增殖、分化、凋亡以及迁移等表型。我们评估了所述装置处理mda-mb-231细胞后,pi3k,akt,mtor的表达水平及磷酸化表达变化,如图4所示,蛋白印迹结果表明处理后的mda-mb-231细胞中pi3k,akt,mtor的表达水平及磷酸化水平显著降低。
42.实施例2,对a549细胞pd-l1的调控
43.a549细胞获取自atcc。a549细胞培养在dmem高糖培养基,并补充10%胎牛血清、100μg/ml链霉素和100μg/ml青霉素。a549细胞培养均维持在37℃和5%co2条件下。取对数期生长状况良好的a549细胞,与磁性纳米颗粒(10-1000μg/ml)共孵育6~12小时,将孵育好
的细胞置于交变磁场(10-1000oe,50khz-1mhz)当中处理0~30分钟。将处理后的细胞继续培养24小时。利用共聚焦显微镜观察到所述装置可显著降低a549细胞pd-l1的表达,如图5所示。
44.实施例3,对hepg2细胞pd-l1的调控
45.hepg2细胞获取自atcc。hepg2细胞培养在dmem高糖培养基,并补充10%胎牛血清、100μg/ml链霉素和100μg/ml青霉素。hepg2细胞培养均维持在37℃和5%co2条件下。取对数期生长状况良好的hepg2细胞,与磁性纳米颗粒(10-1000μg/ml)共孵育6~12小时,将孵育好的细胞置于交变磁场(10-1000oe,50khz-1mhz)当中处理0~30分钟。将处理后的细胞继续培养24小时。利用共聚焦显微镜观察到本发明装置可显著降低hepg2细胞pd-l1的表达,如图6所示。
46.本发明装置在温和(40-50℃)磁热处理肿瘤细胞后pd-l1水平显著降低,其中,肿瘤细胞包括人乳腺癌mda-mb-231细胞、肝癌hepg2细胞、非小细胞肺癌a549细胞、黑色素瘤a375细胞但不限于这些类型。本发明在临床应用时,输入装置可以是介入装置或静脉注射装置。
47.应当指出,对于本领域的普通技术人员来说,在不脱离本发明创造构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1