光催化烯烃氧化裂解成酮的方法
4-(1-苯乙烯基)苯、1-甲基-2-(1-苯乙烯基)苯、1,2-二甲基-4-(1-苯乙烯基)苯、4,4'-(乙烯-1,1-二基)双(甲苯)、4,4'-(乙烯-1,1-二基)双(氯苯)、9-亚甲基-9h-芴、3-(1-苯基乙烯基)吡啶、2-(1-苯基乙烯基)噻吩、2-苯基-1-丙烯、3-甲氧基苯乙烯、2-异丙烯基萘中的任意一种。
9.光催化剂为曙红eosin y、酸性红、溴化乙啶或玫瑰露。
10.氧化剂为氧气。
11.溶剂为甲醇。
12.烯烃、光催化剂及溶剂的摩尔比为15:1:1240。
13.光照时间为10-24h。
14.洗涤所用试剂为二氯甲烷和乙酸乙酯中的至少一种;去溶剂采用减压蒸馏的方式进行;纯化过程使用薄层色谱制备板分离;薄层色谱制备板所用的流动相为石油醚和乙酸乙酯;石油醚与乙酸乙酯的体积比为20-50:1。
15.薄层色谱制备板为硅胶薄层色谱制备板。
16.采用的光照为蓝光光照。
17.本发明的有益效果是:
18.本发明方法将取代的1,1-二苯乙烯和取代的α-甲基苯乙烯,与光催化剂曙红、氧气、溶剂甲醇相混合,在蓝光光照及室温条件下反应得到酮化合物。该方法利用光催化氧化还原的反应机制,直接将烯烃的碳-碳双键氧化裂解得到酮化合物,反应条件温和,操作步骤简单,底物范围广泛,具有良好的反应产率。其产物酮是重要的医药、香料、农用化学品中间体和食品添加剂。
具体实施方式
19.下面结合具体实施方式对本发明进行详细说明。
20.本发明提供一种光催化烯烃氧化裂解成酮的方法,具体为:将烯烃、光催化剂、氧化剂以及溶剂的混合物在室温条件下进行光照,光照后将得到的反应混合物洗涤、去溶剂、纯化,最终得到酮化合物;
21.烯烃为取代的1,1-二苯乙烯或取代的α-甲基苯乙烯,其结构式为酮化合物结构式为其中,结构式中r为烷基、烷氧基、(杂)芳基、卤素、硝基、三氟甲基中任一种。
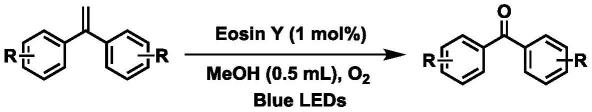
22.本发明中光催化烯烃氧化裂解成酮的化学反应通式可参照下式:
[0023][0024]
烯烃为1,1-二苯乙烯、1-甲基-4-(1-苯乙烯基)苯、1-乙基-4-(1-苯乙烯基)苯、1-叔丁基-4-(1-苯乙烯基)苯、1-甲氧基-4-(1-苯乙烯基)苯、1-苯基-4-(1-苯乙烯基)苯、1-氟-4-(1-苯乙烯基)苯、1-氯-4-(1-苯乙烯基)苯、1-三氟甲基-4-(1-苯乙烯基)苯、1-硝基-4-(1-苯乙烯基)苯、1-甲基-2-(1-苯乙烯基)苯、1,2-二甲基-4-(1-苯乙烯基)苯、4,4'-(乙
烯-1,1-二基)双(甲苯)、4,4'-(乙烯-1,1-二基)双(氯苯)、9-亚甲基-9h-芴、3-(1-苯基乙烯基)吡啶、2-(1-苯基乙烯基)噻吩、2-苯基-1-丙烯、3-甲氧基苯乙烯、2-异丙烯基萘中的任意一种。
[0025]
烯烃结构式依次如下:结构式依次如下:结构式依次如下:
[0026]
光催化剂为曙红、酸性红、溴化乙啶或玫瑰露;光催化剂为曙红eosin y;氧化剂为氧气;溶剂为甲醇。氧化剂为氧气。
[0027]
烯烃、光催化剂及溶剂的摩尔比为15:1:1240。
[0028]
光照时间为10-24h。
[0029]
洗涤所用试剂为二氯甲烷和乙酸乙酯中的至少一种;去溶剂采用减压蒸馏的方式进行;纯化过程使用薄层色谱制备板分离;薄层色谱制备板所用的流动相为石油醚和乙酸乙酯;石油醚与乙酸乙酯的体积比为20-50:1。
[0030]
薄层色谱制备板为硅胶薄层色谱制备板。
[0031]
采用的光照为蓝光光照。
[0032]
本技术提供的光催化烯烃氧化裂解成酮的方法通过取代的1,1-二苯乙烯和取代的α-甲基苯乙烯、光催化剂曙红eosin y、氧气以及甲醇的混合物进行光照,得到酮化合物。该方法利用光催化氧化还原的反应机制,直接将烯烃的碳-碳双键氧化裂解得到酮化合物,反应条件温和,操作步骤简单,底物范围广泛,具有良好的反应产率。
[0033]
以下结合实施例对本发明的特征和性能作进一步的详细描述。
[0034]
以下实施例中化合物的核磁共振波谱:bruker dpx-400mhz核磁共振仪1h nmr:(溶剂:cdcl3,内标tms);
13
c nmr:(溶剂:cdcl3,内标tms)。
[0035]
本发明实施例中所用到的试剂:甲醇为分析纯。
[0036]
薄层色谱制备板【hfgf 254硅胶板】(青岛海洋化工厂)。
[0037]
实施例中所用到的部分烯烃试剂是根据相应文献的方法由酮化合物和甲基三苯基溴化膦(organic letters,2019,21(8),2800-2803)制得。其它烯烃和溶剂都是在tci、aldrich和adamas等试剂公司直接购得,未经进一步纯化处理。
[0038]
实施例1
[0039]
本实施例中提供了光催化烯烃氧化裂解成酮的反应制备如式i-a所示的化合物的方法。
[0040][0041]
其具体的步骤如下:在空气中,向一个干燥的25ml的石英管中加入搅拌子,1,1-二苯乙烯(0.15mmol)、曙红eosin y(0.01mmol)及甲醇(0.5ml),待试剂加入完毕后,盖上塞子。在塞子上同时插上长针和短针,长针下端通入液面,上端通氧气球,短针起到排气的作用,保证整个反应过程在氧气气氛下进行。通气十五分钟后,拔掉两根针,密封好胶塞上的针孔。然后,在30w蓝色led照射及室温条件下搅拌20h(通过gc-ms或tlc监测)。将反应混合物冷却至室温,用二氯甲烷或乙酸乙酯洗涤,减压蒸去溶剂,用薄层色谱制备板(石油醚/乙酸乙酯=20:1)纯化残渣,得到纯的产品。
[0042]
本实施例产物产率为90%。
[0043]
式i-a所示的化合物为白色固体,其结构表征如下:
[0044]1h nmr(400mhz,cdcl3)δ7.80(d,j=8.1hz,4h),7.60-7.56(m,2h),7.49-7.45(m,4h).
[0045]
13
c nmr(101mhz,cdcl3)196.8,137.7,132.5,130.1,128.4.
[0046]
实施例2
[0047]
本实施例中提供了光催化烯烃氧化裂解成酮的反应制备如式i-b所示的化合物的方法。
[0048][0049]
本实施例中以1-甲基-4-(1-苯乙烯基)苯代替实施例1中的1,1-二苯乙烯,将酸性红代替曙红eosin y,在30w蓝色led照射及室温条件下搅拌10h(通过gc-ms或tlc监测),其余制备条件和步骤均与实施例1相同。
[0050]
本实施例产物产率为88%。
[0051]
式i-b所示的化合物为无色油状物,其结构表征如下:
[0052]1h nmr(400mhz,cdcl3)δ7.80
–
7.77(m,2h),7.74
–
7.71(m,2h),7.62
–
7.53(m,1h),7.53
–
7.43(m,2h),7.30
–
7.27(m,2h),2.44(s,3h).
[0053]
13
c nmr(101mhz,cdcl3)196.6,143.3,138.1,135.0,132.3,130.4,130.0,129.1,
128.3,21.8.
[0054]
实施例3
[0055]
本实施例中提供了光催化烯烃氧化裂解成酮的反应制备如式i-c所示的化合物的方法。
[0056][0057]
本实施例中以1-乙基-4-(1-苯乙烯基)苯代替实施例1中的1,1-二苯乙烯,将酸性红代替曙红eosin y,在30w蓝色led照射及室温条件下搅拌24h(通过gc-ms或tlc监测)其余制备条件和步骤均与实施例1相同。
[0058]
本实施例产物产率为90%。
[0059]
式i-c所示的化合物为无色油状物,其结构表征如下:
[0060]1h nmr(400mhz,cdcl3)δ7.81
–
7.78(m,2h),7.77
–
7.73(m,2h),7.60
–
7.55(m,1h),7.50
–
7.45(m,2h),7.31(d,j=8.4hz,2h),2.74(q,j=7.6hz,2h),1.29(t,j=7.6hz,3h).
[0061]
13
c nmr(101mhz,cdcl3)δ196.5,149.4,138.0,135.1,132.2,130.4,130.0,128.2,127.8,29.0,15.3.
[0062]
实施例4
[0063]
本实施例中提供了光催化烯烃氧化裂解成酮的反应制备如式i-d所示的化合物的方法。
[0064][0065]
本实施例中以1-叔丁基-4-(1-苯乙烯基)苯代替实施例1中的1,1-二苯乙烯,将玫瑰露代替曙红eosin y,其余制备条件和步骤均与实施例1相同。
[0066]
本实施例产物产率为85%。
[0067]
式i-d所示的化合物为无色油状物,其结构表征如下:
[0068]1h nmr(400mhz,cdcl3)δ7.83
–
7.76(m,4h),7.60
–
7.55(m,1h),7.52
–
7.45(m,4h),1.37(s,9h).
[0069]
13
c nmr(101mhz,cdcl3)196.5,156.3,138.0,134.9,132.3,130.2,130.1,128.3,125.3,35.2,31.3.
[0070]
实施例5
[0071]
本实施例中提供了光催化烯烃氧化裂解成酮的反应制备如式i-e所示的化合物的方法。
[0072][0073]
本实施例中以1-甲氧基-4-(1-苯乙烯基)苯代替实施例1中的1,1-二苯乙烯,其余制备条件和步骤均与实施例1相同。
[0074]
本实施例产物产率为67%。
[0075]
式i-e所示的化合物为白色固体,其结构表征如下:
[0076]1h nmr(400mhz,cdcl3)δ7.85
–
7.81(m,2h),7.78
–
7.74(m,2h),7.59
–
7.54(m,1h),7.52
–
7.43(m,2h),6.99
–
6.94(m,2h),3.89(s,3h).
[0077]
13
c nmr(101mhz,cdcl3)δ195.6,163.2,138.3,132.6,131.9,130.1,129.7,128.2,113.6,55.5.
[0078]
实施例6
[0079]
本实施例中提供了光催化烯烃氧化裂解成酮的反应制备如式i-f所示的化合物的方法。
[0080][0081]
本实施例中以1-苯基-4-(1-苯乙烯基)苯代替实施例1中的1,1-二苯乙烯,其余制备条件和步骤均与实施例1相同。
[0082]
本实施例产物产率为70%。
[0083]
式i-f所示的化合物为白色固体,其结构表征如下:
[0084]1h nmr(400mhz,cdcl3)δ7.92
–
7.88(m,2h),7.87
–
7.83(m,2h),7.73
–
7.70(m,2h),7.67
–
7.58(m,3h),7.53
–
7.47(m,4h),7.44
–
7.39(m,1h).
[0085]
13
c nmr(101mhz,cdcl3)196.4,145.3,140.1,137.9,136.3,132.5,130.8,130.1,129.1,128.4,128.3,127.4,127.1.
[0086]
实施例7
[0087]
本实施例中提供了光催化烯烃氧化裂解成酮的反应制备如式i-g所示的化合物的方法。
[0088][0089]
本实施例中以1-氟-4-(1-苯乙烯基)苯代替实施例1中的1,1-二苯乙烯,其余制备条件和步骤均与实施例1相同。
[0090]
本实施例产物产率为72%。
[0091]
式i-g所示的化合物为无色油状物,其结构表征如下:
[0092]1h nmr(400mhz,cdcl3)δ7.88
–
7.82(m,2h),7.80
–
7.75(m,2h),7.62
–
7.57(m,1h),7.51
–
7.46(m,2h),7.19
–
7.13(m,2h).
[0093]
13
c nmr(101mhz,cdcl3)δ195.4,165.5(d,j=252.0hz),137.6,133.9(d,j=3.0hz),132.8(d,j=10.0hz),132.6,130.0,128.5,115.6(d,j=22.0hz).
[0094]
实施例8
[0095]
本实施例中提供了光催化烯烃氧化裂解成酮的反应制备如式i-h所示的化合物的方法。
[0096][0097]
本实施例中以1-氯-4-(1-苯乙烯基)苯代替实施例1中的1,1-二苯乙烯,其余制备条件和步骤均与实施例1相同。
[0098]
本实施例产物产率为68%。
[0099]
式i-h所示的化合物为白色固体,其结构表征如下:
[0100]1h nmr(400mhz,cdcl3)δ7.79
–
7.72(m,4h),7.63
–
7.58(m,1h),7.52
–
7.44(m,4h).
[0101]
13
c nmr(101mhz,cdcl3)195.5,139.0,137.3,135.9,132.7,131.5,130.0,128.7,128.5.
[0102]
实施例9
[0103]
本实施例中提供了光催化烯烃氧化裂解成酮的反应制备如式i-i所示的化合物的方法。
[0104][0105]
本实施例中以1-三氟甲基-4-(1-苯乙烯基)苯代替实施例1中的1,1-二苯乙烯,其余制备条件和步骤均与实施例1相同。
[0106]
本实施例产物产率为68%。
[0107]
式i-i所示的化合物为白色固体,其结构表征如下:
[0108]1h nmr(400mhz,cdcl3)δ7.90(d,j=8.0hz,2h),7.83
–
7.79(m,2h),7.76(d,j=8.1hz,2h),7.66
–
7.61(m,1h),7.54
–
7.49(m,2h).
[0109]
13
c nmr(101mhz,cdcl3)195.6,140.8,136.8,133.8(q,j=33.0hz),133.2,130.3,130.2,128.6,125.5(q,j=4.0hz),123.8(q,j=271.0hz).
[0110]
实施例10
[0111]
本实施例中提供了光催化烯烃氧化裂解成酮的反应制备如式i-j所示的化合物的
方法。
[0112][0113]
本实施例中以1-硝基-4-(1-苯乙烯基)苯代替实施例1中的1,1-二苯乙烯,其余制备条件和步骤均与实施例1相同。
[0114]
本实施例产物产率为58%。
[0115]
式i-j所示的化合物为白色固体,其结构表征如下:
[0116]1h nmr(400mhz,cdcl3)δ8.37
–
8.32(m,2h),7.96
–
7.92(m,2h),7.82
–
7.78(m,2h),7.68
–
7.63(m,1h),7.56
–
7.50(m,2h).
[0117]
13
c nmr(101mhz,cdcl3)δ194.7,149.8,142.8,136.3,133.4,130.6,130.1,128.6,123.5.
[0118]
实施例11
[0119]
本实施例中提供了光催化烯烃氧化裂解成酮的反应制备如式i-k所示的化合物的方法。
[0120][0121]
本实施例中以1-甲基-2-(1-苯乙烯基)苯代替实施例1中的1,1-二苯乙烯,其余制备条件和步骤均与实施例1相同。
[0122]
本实施例产物产率为58%。
[0123]
式i-k所示的化合物为白色固体,其结构表征如下:
[0124]1h nmr(400mhz,cdcl3)δ7.83
–
7.79(m,2h),7.60
–
7.56(m,1h),7.48
–
7.43(m,2h),7.42
–
7.35(m,1h),7.34
–
7.21(m,3h),2.34(s,3h).
[0125]
13
c nmr(101mhz,cdcl3)198.8,138.7,137.8,136.9,133.3,131.1,130.4,130.3,128.6x 2,125.3,20.1.
[0126]
实施例12
[0127]
本实施例中提供了光催化烯烃氧化裂解成酮的反应制备如式i-l所示的化合物的方法。
[0128][0129]
本实施例中以1,2-二甲基-4-(1-苯乙烯基)苯代替实施例1中的1,1-二苯乙烯,其余制备条件和步骤均与实施例1相同。
[0130]
本实施例产物产率为76%。
[0131]
式i-l所示的化合物为无色油状物,其结构表征如下:
[0132]1h nmr(400mhz,cdcl3)δ7.82
–
7.75(m,2h),7.62(s,1h),7.60
–
7.52(m,2h),7.50
–
7.45(m,2h),7.23(d,j=7.8hz,1h),2.35(s,3h),2.33(s,3h).
[0133]
13
c nmr(101mhz,cdcl3)δ196.7,142.0,138.1,136.8,135.3,132.1,131.2,123.0,129.5,128.2,128.1,20.0,19.8.
[0134]
实施例13
[0135]
本实施例中提供了光催化烯烃氧化裂解成酮的反应制备如式i-m所示的化合物的方法。
[0136][0137]
本实施例中以4,4'-(乙烯-1,1-二基)双(甲苯)代替实施例1中的1,1-二苯乙烯,其余制备条件和步骤均与实施例1相同。
[0138]
本实施例产物产率为83%。
[0139]
式i-m所示的化合物为白色固体,其结构表征如下:
[0140]1h nmr(400mhz,cdcl3)δ7.65
–
7.60(m,4h),7.19(dd,j=8.4,0.5hz,4h),2.36(s,6h).
[0141]
13
c nmr(101mhz,cdcl3)δ196.4,143.0,135.3,130.3,129.0,21.7.
[0142]
实施例14
[0143]
本实施例中提供了光催化烯烃氧化裂解成酮的反应制备如式i-n所示的化合物的方法。
[0144][0145]
本实施例中以4,4'-(乙烯-1,1-二基)双(氯苯)代替实施例1中的1,1-二苯乙烯,其余制备条件和步骤均与实施例1相同。
[0146]
本实施例产物产率为61%。
[0147]
式i-n所示的化合物为白色固体,其结构表征如下:
[0148]1h nmr(400mhz,cdcl3)δ7.75
–
7.71(m,4h),7.49
–
7.45(m,4h).
[0149]
13
c nmr(101mhz,cdcl3)δ194.2,139.1,135.4,131.3,128.7.
[0150]
实施例15
[0151]
本实施例中提供了光催化烯烃氧化裂解成酮的反应制备如式i-o所示的化合物的方法。
[0152][0153]
本实施例中以9-亚甲基-9h-芴代替实施例1中的1,1-二苯乙烯,其余制备条件和步骤均与实施例1相同。
[0154]
本实施例产物产率为78%。
[0155]
式i-o所示的化合物为无色油状物,其结构表征如下:
[0156]1h nmr(400mhz,cdcl3)δ7.68
–
7.64(m,2h),7.54
–
7.46(m,4h),7.32
–
7.27(m,2h).
[0157]
13
c nmr(101mhz,cdcl3)δ193.9,144.4,134.7,134.1,129.0,124.3,120.3.
[0158]
实施例16
[0159]
本实施例中提供了光催化烯烃氧化裂解成酮的反应制备如式i-p所示的化合物的方法。
[0160][0161]
本实施例中以3-(1-苯基乙烯基)吡啶代替实施例1中的1,1-二苯乙烯,其余制备条件和步骤均与实施例1相同。
[0162]
本实施例产物产率为43%。
[0163]
式i-p所示的化合物为无色油状物,其结构表征如下:
[0164]1h nmr(400mhz,cdcl3)δ8.99(dd,j=2.1,0.7hz,1h),8.81(dd,j=4.9,1.7hz,1h),7.86
–
7.77(m,1h),7.56
–
7.47(m,2h),7.65
–
7.61(m,1h),7.53
–
7.48(m,2h),7.47
–
7.42(m,1h).
[0165]
13
c nmr(101mhz,cdcl3)δ194.7,152.4,150.6,137.6,136.6,133.3,133.2,130.0,128.7,123.5.
[0166]
实施例17
[0167]
本实施例中提供了光催化烯烃氧化裂解成酮的反应制备如式i-q所示的化合物的方法。
[0168][0169]
本实施例中以2-(1-苯基乙烯基)噻吩代替实施例1中的1,1-二苯乙烯,其余制备条件和步骤均与实施例1相同。
[0170]
本实施例产物产率为66%。
[0171]
式i-q所示的化合物为无色油状物,其结构表征如下:
[0172]1h nmr(400mhz,cdcl3)δ7.90
–
7.83(m,2h),7.72(dd,j=5.0,1.1hz,1h),7.65(dd,j=3.8,1.1hz,1h),7.62
–
7.57(m,1h),7.55
–
7.45(m,2h),7.16(dd,j=5.0,3.8hz,1h).
[0173]
13
c nmr(101mhz,cdcl3)δ188.3,143,7,138.2,134.9,134.2,132.3,129.2,128.4,128.0.
[0174]
实施例18
[0175]
本实施例中提供了光催化烯烃氧化裂解成酮的反应制备如式i-r所示的化合物的方法。
[0176][0177]
本实施例中以2-苯基-1-丙烯代替实施例1中的1,1-二苯乙烯,其余制备条件和步骤均与实施例1相同。
[0178]
本实施例产物产率为75%。
[0179]
式i-r所示的化合物为无色油状物,其结构表征如下:
[0180]1h nmr(400mhz,cdcl3)δ8.00
–
7.93(m,2h),7.59
–
7.54(m,1h),7.50
–
7.44(m,2h),2.61(s,3h).
[0181]
13
c nmr(101mhz,cdcl3)δ198.1,137.1,133.1,128.6,128.3,26.6.
[0182]
实施例19
[0183]
本实施例中提供了光催化烯烃氧化裂解成酮的反应制备如式i-s所示的化合物的方法。
[0184][0185][0186]
本实施例中以3-甲氧基苯乙烯代替实施例1中的1,1-二苯乙烯,其余制备条件和步骤均与实施例1相同。
[0187]
本实施例产物产率为63%。
[0188]
式i-s所示的化合物为无色油状物,其结构表征如下:
[0189]1h nmr(400mhz,cdcl3)δ7.54
–
7.50(m,1h),7.49
–
7.44(m,1h),7.35(t,j=7.9hz,1h),7.12
–
7.06(m,1h),3.84(s,3h),2.58(s,3h).
[0190]
13
c nmr(101mhz,cdcl3)δ198.2,140.2,138.9,129.9,121.4,119.9,112.8,55.8,27.0.
[0191]
实施例20
[0192]
本实施例中提供了光催化烯烃氧化裂解成酮的反应制备如式i-t所示的化合物的方法。
[0193][0194]
本实施例中以2-异丙烯基萘代替实施例1中的1,1-二苯乙烯,其余制备条件和步骤均与实施例1相同。
[0195]
本实施例产物产率为75%。
[0196]
式i-t所示的化合物为无色油状物,其结构表征如下:
[0197]1h nmr(400mhz,cdcl3)δ8.47(s,1h),8.04(dd,j=8.6,1.7hz,1h),7.97(d,j=8.0hz,1h),7.92
–
7.87(m,2h),7.63
–
7.54(m,2h),2.73(s,3h).
[0198]
13
c nmr(101mhz,cdcl3)δ198.1,135.6,134.5,132.5,130.2,129.6,128.5,127.8,126.8,123.9,26.7.
[0199]
综上所述,本技术提供的光催化烯烃裂解成酮的方法产率最高可达到90%,反应条件温和,操作步骤简单,官能团兼容性好,底物可转化为多种其它有用的分子,具有很强的实用性。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1