SARS-CoV-2编码蛋白来源的T细胞表位多肽HLVDFQVTI及其应用的制作方法
sars-cov-2编码蛋白来源的t细胞表位多肽hlvdfqvti及其应用
技术领域
1.本发明涉及生物医学技术领域,具体涉及新型冠状病毒(sars-cov-2)编码蛋白来源的t细胞表位多肽hlvdfqvti及其应用。
背景技术:
2.由sars-cov-2引起的新型冠状病毒肺炎(covid-19)是世界范围内当前最为迫切急需解决的公共卫生问题。
3.靶向sars-cov-2编码的病毒蛋白(不局限于s蛋白)的特异性t细胞反应存在于covid-19患者体内,在抑制sars-cov-2感染、病毒清除中发挥着重要的作用,可能有助于患者康复。近期的多项研究证实covid-19重症患者体内t淋巴细胞数量会显著的较轻症患者少,表明t细胞在控制或杀灭病毒方面发挥着重要作用。同时,针对covid-19患者的临床研究证实,部分患者在体内靶向结构蛋白的中和性抗体持续阴性的情况下也能清除病毒的感染。多项研究表明靶向sars-cov-2结构蛋白的中和性抗体在体内存在的时间较短。相较而言特异性记忆性t细胞在体内存活的时间会显著的较长,这一特点在针对与sars-cov-2高度相似的mers-cov(中东呼吸综合征冠状病毒)和 sars-cov-1(严重急性呼吸综合征冠状病毒)的研究中已经得到了验证。
4.此外,在一项使用缺乏t细胞和b细胞的免疫缺陷小鼠作为宿主的模型中,研究者发现给感染了sars-cov-1(ma15 strain,mouse adapted 15 strain)的小鼠回输经一个sars-cov-1 s蛋白来源的t细胞表位(s366)诱导的病毒特异性cd8+t细胞能加速病毒在小鼠体内的清除以及临床病理的恢复。使用上述表位对具有正常免疫系统的balb/c小鼠进行免疫,7天后使用致死剂量的sars-cov-1感染小鼠,发现经免疫的小鼠能加速病毒在体内的清除以及100%免于病毒的致死作用;相反,未经免疫或经空载树突状细胞免疫的小鼠的死亡率分别为70%和50%。在另一项更进一步的研究t细胞表位作为疫苗对 sars-cov-1的感染提供持续性保护的动物实验中,研究者使用一个 sars-cov-1 s蛋白来源的t细胞表位(s525)对balb/c小鼠进行免疫,发现这个表位能诱导剧烈的t细胞免疫反应,且能在肺部和脾脏中检测到病毒特异性t细胞的存在。为了研究病毒特异性记忆型t细胞的保护作用,在免疫后的第42-45天,使用致死剂量的sars-cov-1感染小鼠,发现经表位s525免疫的小鼠有80%的存活,相比之下,未免疫和使用gfp免疫的对照组小鼠存活率分别为0和20%。在sars-cov-1感染康复者体内检测到病毒特异性记忆型cd8+t 细胞能持续存在并维持功能达11年之久,而在此时间点,中和性抗体以及能产生中和性抗体的b细胞均不能检测到。相似的,使用mers-cov感染的小鼠模型也发现,被一个mers-cov的t细胞表位免疫的小鼠能加速病毒清除,更快的从感染状态恢复。这些研究结果表明cov(冠状病毒)抗原特异性t细胞介导的细胞免疫应答在控制cov感染和病毒清除中发挥着重要作用。
5.当抗原呈递细胞(antigen presenting cell,apc)或被病毒感染的宿主细胞表达病毒蛋白后,胞浆中的病毒蛋白质抗原会被蛋白酶体降解成肽段,经转运、加工后与人类白
细胞抗原(human leukocyte antigen,hla)类分子结合,形成抗原肽—hla分子复合物,转移至细胞表面,被t细胞识别,活化t细胞。有效激发特异性t细胞免疫应答发挥抗病毒效能的关键在于鉴定sars-cov-2编码蛋白来源的t细胞表位,这对开发安全有效的基于t细胞抗原表位的 covid-19预防性和治疗性多肽疫苗有重要意义。
技术实现要素:
6.本发明所要解决的技术问题是鉴定sars-cov-2编码蛋白来源的t细胞表位,以有效激发特异性t细胞免疫应答发挥抗病毒效能。
7.为了解决上述问题,本发明提出以下技术方案:
8.第一方面,本发明提供一种sars-cov-2编码蛋白来源的t细胞表位多肽,其氨基酸序列如seq id no.1、seq id no.2、seq id no.3、seq id no.4、seqid no.5、seq id no.6、seq id no.7中的任一项所示。
9.本发明还提供一种核酸分子,所述核酸分子包含编码所述的sars-cov-2 病毒蛋白来源的t细胞表位多肽的核苷酸序列或其互补序列。
10.本发明还提供含有所述核酸分子的载体。
11.本发明还提供一种融合蛋白,所述融合蛋白包含所述的sars-cov-2病毒编码蛋白来源的t细胞表位多肽。
12.本发明还提供一种抗原递呈细胞,所述抗原递呈细胞是被所述的 sars-cov-2病毒编码蛋白来源的t细胞表位多肽致敏的。
13.进一步地,所述抗原递呈细胞经过分离和纯化。
14.进一步地,所述的抗原递呈细胞选自:树突状细胞、巨噬细胞、b细胞、成纤维细胞或内皮细胞。
15.本发明还提供一种针对所述的sars-cov-2病毒编码蛋白来源的t细胞表位多肽的特异性免疫效应细胞。
16.本发明提供了含所述的sars-cov-2病毒编码蛋白来源的t细胞表位多肽的药物组合物,该药物组合物可含有核酸分子、载体、融合蛋白、抗原递呈细胞或特异性免疫效应细胞作为活性成分;所述药物组合物还包含药学上可接受的载体或赋形剂,其药用形式可为疫苗。
17.所述“药学上可接受的载体”是指用于治疗剂给药的载体,是指这样一些药剂载体:它们本身不诱导产生对接受该组合物的个体有害的抗体,且给药后没有过分的毒性。这些载体是本领域普通技术人员所熟知的。在remington’s pharmaceutical sciences(mackpub.co.,n.j.1991)中可找到关于药学上可接受的赋形剂的充分讨论。这类载体包括(但并不限于):盐水、缓冲液、葡萄糖、水、甘油、乙醇、佐剂、及其组合。
18.药物组合物中药学上可接受的载体可含有液体,如水、盐水、甘油和乙醇。另外,这些载体中还可能存在辅助性的物质,如润湿剂或乳化剂、ph缓冲物质等。此外,免疫组合物中还可以含有免疫佐剂。
19.通常,可将治疗性组合物制成可注射剂,例如液体溶液或悬液;还可制成在注射前适合配入溶液或悬液中、液体载体的固体形式。
20.一旦配成本发明的药物组合物,可将其直接给予对象。待预防或治疗的对象可以
是动物;尤其是人。
21.含本发明sars-cov-2病毒编码蛋白来源的t细胞表位多肽的治疗或预防性药物组合物(包括疫苗),可以经口服、皮下、皮内、静脉注射等方式应用。治疗剂量方案可以是单剂方案或多剂方案。
22.本发明提供了所述sars-cov-2编码蛋白来源的t细胞表位多肽、核酸分子、载体、融合蛋白、抗原递呈细胞、特异性免疫效应细胞或药物组合物在制备治疗或预防sars-cov-2病毒感染的药物中的用途。
23.本发明的优点在于,本发明经过筛选获得的sars-cov-2编码蛋白来源的t 细胞表位多肽,具有诱导sars-cov-2特异性t细胞,协助控制sars-cov-2 感染和病毒清除的特性。通过体外实验验证了该表位多肽具有诱导sars-cov-2 特异性t细胞的能力,为后续研制基于sars-cov-2蛋白来源表位的多肽疫苗以及诊断制剂提供了理论基础。
附图说明
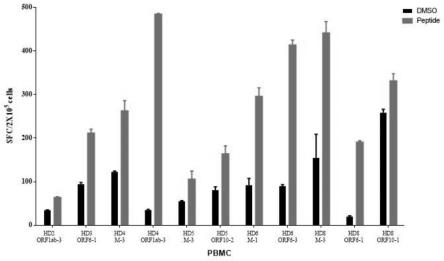
24.图1为本发明sars-cov-2编码蛋白来源的t细胞表位多肽体外诱导特异性t细胞,使用靶向ifn-γ的elispot实验检测特异性t细胞的数量,得到的 elispot斑点的统计图。
25.图2为本发明sars-cov-2编码蛋白来源的t细胞表位多肽体外诱导特异性t细胞,使用靶向ifn-γ的elispot实验检测特异性t细胞的斑点图。
具体实施方式
26.下面结合实施例对本技术做进一步介绍说明,如无特别说明,本发明中所涉及实验试剂、实验设备、实验材料均为本领域常用或市售产品,所涉及名词、缩写均为本领域常规含义,如il-2(白细胞介素-2)。
27.下列实施例中未注明具体条件的实验方法,通常按照常规条件,例如 sambrook等人,分子克隆:实验室手册(new york:cold spring harbor laboratorypress,1989)中所述的条件,或按照制造厂商所建议的条件。
28.除非另行定义,文中所使用的所有专业与科学用语与本领域熟练人员所熟悉的意义相同。此外,任何与所记载内容相似或均等的方法及材料皆可应用于本发明中。文中所述的较佳实施方法与材料仅作示范之用。
29.实施例
30.本发明提供如下任一种sars-cov-2编码蛋白来源的表位多肽:
31.m-1、m-3、orf6-1、orf6-3、orf10-1、orf10-2、orf1ab-3,其氨基酸序列依次为seq id no.1、seq id no.2、seq id no.3、seq id no.4、seq id no.5、 seq id no.6、seq id no.7所示。
32.验证实验:
33.利用表位多肽在体外诱导可用于covid-19治疗的sars-cov-2特异性t 细胞。
34.(1)使用x-vivo 15培养基(添加5%hab)将pbmc重悬,加入24孔板中至浓度为2-4m/孔,分别加入上述抗原表位多肽至终浓度为10-20μm。
35.(2)在多肽刺激24小时后,补加终浓度为25-50iu/ml的il-2。
36.(3)在恒温培养箱培养8-10天后收集多肽刺激的pbmc,洗2遍后,重悬至x-vivo 15
培养基进行静息。
37.(4)静息24-48小时后,使用酶联免疫斑点(elispot)实验检测特异性 t细胞。将上述刺激后的细胞分至4个已包被ifn-γ(干扰素-γ)一抗的elispot 板孔中(1-2
×
105个细胞每孔),随后各2孔分别加入表位多肽和溶剂对照(dmso) 孵育17-24小时后进行后续操作。
38.(5)后续elispot实验具体步骤参见商品化试剂盒的说明书(mabtech, 3420-2h)进行。
39.(6)进行读板。
40.结果如附图1、图2所示。
41.可见,本发明筛选获得的sars-cov-2编码蛋白来源的t细胞表位多肽,通过体外实验验证了该表位多肽具有诱导sars-cov-2特异性t细胞的能力,协助控制sars-cov-2感染和病毒清除的特性。
42.本发明筛选获得的sars-cov-2编码蛋白来源的t细胞表位多肽可为后续研制基于sars-cov-2蛋白来源表位的多肽疫苗以及诊断制剂提供理论基础。
43.以上所述,为本发明的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,可轻易想到各种等效的修改或替换,这些修改或替换都应涵盖在本发明的保护范围之内。因此,本发明的保护范围应以权利要求的保护范围为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1