一种含有吲哚酮结构的硫酯化合物的制备方法
1.本发明属于有机合成领域,尤其涉及一种含有吲哚酮结构的硫酯化合物的制备方法。
背景技术:
2.吲哚酮是一类十分重要的杂环分子,广泛存在于各种天然产物、生物活性分子和药物中(eur.j.med.chem.2021,216,113334)。此外,作为关键的反应中间体,吲哚酮在有机合成中有着非常广泛的应用。因此,多种合成吲哚酮的方法被开发出来。其中最具有吸引力的方法是基于过渡金属催化的级联环化反应,因为在反应中生成的有机金属络合物可以通过进一步的转化来合成官能团化的吲哚酮衍生物。
3.近年来,过渡金属催化的羰基化反应作为合成含羰基化合物的重要方法在学术和工业领域都取得了重大的进展(chem 2019,5,526)。吲哚酮衍生物也同样能够通过过渡金属催化的环化/羰基化反应来构建。在这些反应中,含有吲哚酮结构的硫酯化合物的合成引起了广泛的关注,因为硫酯化合物被认为是生命科学和合成化学中具有独特化学性质的一类有机化合物。然而,有关合成含有吲哚酮结构的硫酯化合物的报道却非常有限。因此,探索更多的反应途径来构建含有吲哚酮结构的硫酯化合物是十分必要的。
4.近年来,过渡金属催化的硫羰基化反应已成为合成硫酯化合物的重要手段。在大多数硫羰基化反应中,通常使用硫醇作为硫源,硫醇由于其对过渡金属的强亲硫性,容易使催化剂中毒,使该类反应具有一定的局限性(chem.rev.1989,89,1)。因此,开发基于替代硫源的羰基化反应仍然是化学家们工作的重点之一。磺酰氯作为一类廉价易得、操作简单的化学试剂,在有机合成中有着非常重要的应用。近年来,我们团队开发了一系列以磺酰氯作为硫源的硫羰基化反应。因此,在前期工作的基础上,我们发展了钯催化的环化/硫羰基化反应来合成含有吲哚酮结构的硫酯化合物。值得注意的是,磺酰氯在反应中作为重要的硫源,不论是芳基还是烷基取代的磺酰氯都可以很好的兼容该反应。同时羰基钼既作为羰源又作为还原剂,使该方法有着良好的应用前景。
技术实现要素:
5.本发明提供了一种含有吲哚酮结构的硫酯化合物的制备方法,该反应原料廉价易得,底物适用性好,反应效率高,同时以羰基钼既作为羰基来源又作为还原剂,操作简单。此外,该方法以磺酰氯化合物作为硫源,为含有吲哚酮结构的硫酯化合物的构建提供了新的途径,并突出了磺酰氯化合物在羰基化反应中的应用。
6.一种含有吲哚酮结构的硫酯化合物的制备方法,包括如下步骤:将钯催化剂、三环己基膦、羰基钼、碳酸铯、水、碘代芳烃以及磺酰氯化合物于90~110℃反应20~28小时,反应完全后,后处理得到所述的含有吲哚酮结构的硫酯化合物;
7.所述的碘代芳烃的结构如式(ii)所示:
[0008][0009]
所述的磺酰氯化合物的结构如式(iii)所示:
[0010]r4-so2cl
ꢀꢀꢀꢀꢀꢀꢀꢀ
(iii);
[0011]
所述的含有吲哚酮结构的硫酯化合物的结构如式(i)所示:
[0012][0013]
式(ⅰ)~(iii)中,r1为h,c1~c4烷基,三氟甲基或卤素;
[0014]
r2为c1~c4烷基或对甲苯磺酰基;
[0015]
r3为h或c1~c7烃基;
[0016]
r4为c1~c6烷基、c1~c6环烷基或取代的苯基,所述苯基上的取代基为c1~c4烷基,甲氧基,苯基。
[0017]
所述的钯催化剂、三环己基膦和碳酸铯的摩尔比为0.01:0.04:0.3;
[0018]
r1的取代位置为对位和间位。
[0019]
反应式如下:
[0020][0021]
本发明中,可选用的后处理过程包括:过滤,硅胶拌样,最后经过柱层析纯化得到相应的含有吲哚酮结构的硫酯化合物,采用柱层析纯化为本领域常用的技术手段。
[0022]
作为优选,r1为h,甲基,叔丁基,三氟甲基,f或br;r2为甲基,乙基,正丁基或对甲苯磺酰基;r3为甲基或苄基。此时,所述的碘代芳烃容易得到,并且反应的产率较高。
[0023]
作为优选,r4为环己基,取代的苯基,所述苯基上的取代基为甲基,异丙基,叔丁基,甲氧基或苯基。此时,所述的磺酰氯化合物容易得到,并且反应的产率较高。
[0024]
所述的用来制备含有吲哚酮结构的硫酯化合物的碘代芳烃和磺酰氯化合物价格较便宜,在自然界中广泛存在,作为优选,以摩尔量计,碘代芳烃:磺酰氯化合物:钯催化剂=1:1~1.5:0.05~0.1;作为进一步的优选,以摩尔量计,碘代芳烃:磺酰氯化合物:钯催化剂=1:1.5:0.05。
[0025]
作为优选,所述的反应的时间为24小时,反应时间过长增加反应成本,相反则难以保证反应的完全。
[0026]
作为优选,反应在n,n-二甲基甲酰胺中进行,所述的n,n-二甲基甲酰胺的用量能将原料较好的溶解即可,0.2mmol的碘代芳烃使用的n,n-二甲基甲酰胺的量约为1~2ml。
[0027]
作为优选,所述的钯催化剂为醋酸钯,在众多钯催化剂中醋酸钯价格比较便宜,而且使用醋酸钯为催化剂时反应效率较高。
[0028]
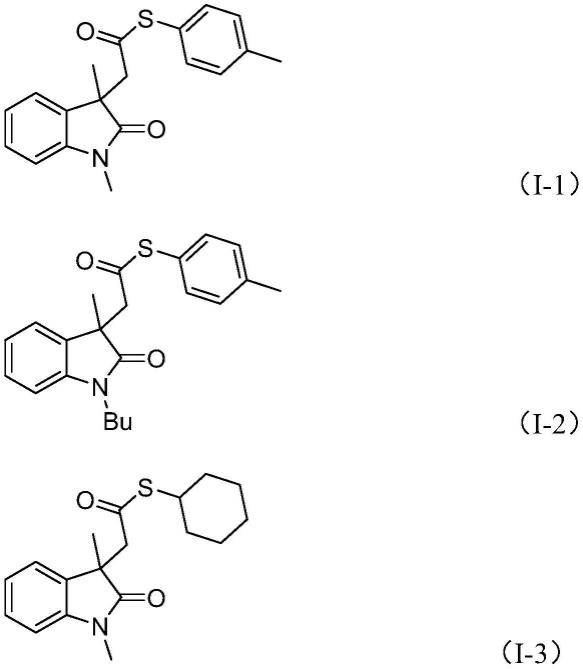
作为进一步的优选,所述的含有吲哚酮结构的硫酯化合物为式(i-1)-式(i-5)所示化合物中的一种:
[0029][0030]
上述制备方法中,所述的醋酸钯、三环己基膦以及碳酸铯一般采用市售产品,都能从市场上方便地得到。
[0031]
同现有技术相比,本发明的有益效果体现在:该反应原料廉价易得,制备方法简单,易于操作,后处理简便,底物官能团兼容性强,反应效率高。该方法以磺酰氯化合物作为硫源,以羰基钼既作为羰基来源又作为还原剂,为含有吲哚酮结构的硫酯化合物的构建提供了新的途径。可根据实际需要合成多种含有吲哚酮结构的硫酯化合物,实用性较强。
具体实施方式
[0032]
下面结合具体实施例对本发明做进一步的描述。
[0033]
实施例1~15
[0034]
按照表1的原料配比在15ml的封管中加入醋酸钯、三环己基膦、羰基钼、碳酸铯、水、碘代芳烃(ii)和磺酰氯化合物(iii),然后加入n,n-二甲基甲酰胺(1ml),混合搅拌均匀,按照表2的反应条件反应,反应完成后,过滤,硅胶拌样,经过柱层析纯化得到相应的含有吲哚酮结构的硫酯化合物(ⅰ),反应过程如下式所示:
[0035][0036]
表1实施例1~15的原料加入量
[0037][0038]
表2
[0039][0040]
表1和表2中,t为反应温度,t为反应时间,me为甲基,bu为正丁基,cy为环己基,cf3为三氟甲基,ipr为异丙基,tbu为叔丁基,ome为甲氧基,ph为苯基,et为乙基,ts为对甲苯磺酰基,bn为苄基。
[0041]
实施例1~5制备得到化合物的结构确认数据:
[0042]
由实施例1制备得到的含有吲哚酮结构的硫酯化合物(i-1)的核磁共振(1h nmr和
13
c nmr)检测数据为:
[0043][0044]1h nmr(400mhz,cdcl3)δ7.28
–
7.24(m,2h),7.12(d,j=8.1hz,2h),7.07
–
7.03(m,3h),6.82(d,j=8.0hz,1h),3.27(d,j=16.0hz,1h),3.25
–
3.19(m,4h),2.31(s,3h),1.40(s,3h).
[0045]
13
c nmr(101mhz,cdcl3)δ193.9,179.3,143.4,139.7,134.3,132.2,129.9,128.1,123.6,122.8,122.3,108.2,49.7,46.2,26.4,24.1,21.3.
[0046]
由实施例2制备得到的含有吲哚酮结构的硫酯化合物(i-2)的核磁共振(1h nmr和
13
c nmr)检测数据为:
[0047]
[0048]1h nmr(400mhz,cdcl3)δ7.27
–
7.22(m,2h),7.12(d,j=8.1hz,2h),7.06(d,j=8.2hz,2h),7.02(t,j=7.5hz,1h),6.83(d,j=7.8hz,1h),3.77
–
3.62(m,2h),3.25
–
3.16(m,2h),2.31(s,3h),1.69
–
1.62(m,2h),1.40
–
1.35(m,5h),0.93(t,j=7.4hz,3h).
[0049]
13
c nmr(101mhz,cdcl3)δ193.7,179.1,142.8,139.6,134.3,132.4,129.9,128.0,123.9,123.1,122.0,108.5,49.6,46.2,39.9,29.4,24.2,21.2,20.1,13.7.
[0050]
由实施例3制备得到的含有吲哚酮结构的硫酯化合物(i-3)的核磁共振(1h nmr和
13
c nmr)检测数据为:
[0051][0052]1h nmr(400mhz,cdcl3)δ7.27
–
7.24(m,1h),7.21
–
7.19(m,1h),7.03(td,j=7.5,0.8hz,1h),6.84(d,j=7.8hz,1h),3.33
–
3.27(m,1h),3.25(s,3h),3.16(d,j=15.7hz,1h),3.06(d,j=15.7hz,1h),1.75
–
1.54(m,4h),1.36(s,3h),1.33
–
1.15(m,6h).
[0053]
13
c nmr(101mhz,cdcl3)δ195.0,179.6,143.4,132.3,128.0,122.7,122.2,108.1,50.4,46.2,42.2,32.8,32.6,26.4,25.71,25.70,25.4,24.1.
[0054]
由实施例4制备得到的含有吲哚酮结构的硫酯化合物(i-4)的核磁共振(1h nmr和
13
c nmr)检测数据为:
[0055][0056]1h nmr(400mhz,cdcl3)δ7.54(d,j=8.2hz,1h),7.47(s,1h),7.13(d,j=8.1hz,2h),7.08(d,j=8.2hz,2h),6.87(d,j=8.2hz,1h),3.33(d,j=16.4hz,1h),3.27
–
3.23(m,4h),2.31(s,3h),1.41(s,3h).
[0057]
13
c nmr(101mhz,cdcl3)δ194.0,179.3,146.5,140.0,134.4,132.9,130.1,126.0(q,j=3.9hz),124.5(q,j=32.4hz),124.4(q,j=271.5hz),123.3,119.7(q,j=3.5hz),108.0,49.5,46.0,26.6,24.1,21.3.
[0058]
由实施例5制备得到的含有吲哚酮结构的硫酯化合物(i-5)的核磁共振(1h nmr和
13
c nmr)检测数据为:
[0059]
[0060]1h nmr(400mhz,cdcl3)δ7.18(dd,j=8.2,5.3hz,1h),7.13(d,j=8.0hz,2h),7.08(d,j=8.2hz,2h),6.71(ddd,j=10.3,8.3,2.3hz,1h),6.55(dd,j=8.9,2.3hz,1h),3.26(d,j=16.1hz,1h),3.21
–
3.17(m,4h),2.31(s,3h),1.38(s,3h).
[0061]
13
c nmr(101mhz,cdcl3)δ193.9,179.6,163.0(d,j=244.6hz),144.9(d,j=11.6hz),139.8,134.3,130.0,127.4(d,j=2.8hz),123.7(d,j=9.8hz),123.5,108.2(d,j=22.4hz),97.1(d,j=27.6hz),49.7,45.7,26.5,24.1,21.2。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1