一类选择性抑制PTP1B的化合物及其制备方法和应用与流程
一类选择性抑制ptp1b的化合物及其制备方法和应用
技术领域
1.本发明属于生物医药领域,具体涉及一类来源于天然药物的具有选择性抑制ptp1b活性的蒽醌苷新化合物及其制备方法和用途。
背景技术:
2.糖尿病已成为当前威胁全球人类健康最重要的非传染性疾病之一。据国际糖尿病联盟(idf)统计,2011年全球糖尿病患者人数已达3.7亿,其中80%在发展中国家,估计到2030年全球将有近5.5亿糖尿病患者。我国患病人群中,以2型糖尿病(非胰岛素依赖型)为主,占90%以上,其所致的慢性高血糖症及引起的视网膜病变、慢性肾脏疾病、神经病变、高血压等多种慢性并发症,不仅给患者带来肉体和精神上的损害,也给个人和国家带来沉重的经济负担。因此,降糖药物研发对于我国社会和经济的健康发展具有重要意义。
3.蛋白酪氨酸磷酸酶1b(ptp1b)是蛋白酪氨酸磷酸酶(ptp)家族的一个亚型,最早由人胎盘组织分离得到,广泛分布于肝脏、肾脏和胎盘等组织中。ptp1b与胰岛素抵抗和肥胖密切相关,在胰岛素和瘦素信号通路中起负调节作用,通过促胰岛素受体脱磷酸化,下调胰岛素和瘦素水平,引起机体对胰岛素的耐受,而引发高血糖和肥胖。因此,ptp1b是治疗2型糖尿病和肥胖的有效靶点。但蛋白酪氨酸磷酸酶家族的催化活性位点保守性高,针对催化位点设计的ptp1b抑制剂选择性差,副作用明显。其中,t-细胞蛋白酪氨酸磷酸酶(tcptp)与ptp1b的同源度最高,二者催化区域近80%的氨基酸序列一致,但tcptp的生理功能与ptp1b不同,尤其是有研究表明tcptp基因敲除小鼠的死亡率高,对tcptp的交叉抑制可能会引起严重的副作用。因此,大量研究致力于寻找能够有效抑制ptp1b,但对tcptp抑制作用低的药物。近年来,报道了几个ptp1b的别构位点,如由α3和α6螺旋组成的别构位点,位于c-末端部分α9
′
螺旋的别构位点,他们距离活性位点较远,而且具有亲脂性、同源度低等特点,靶向该类位点的抑制剂具有选择性高和良好的生物利用度等优点,尤其是对tcptp的作用较弱,具有更好的成药性。但靶向该类别构位点的抑制剂报道非常少。
4.近年来,发明人致力于从天然药物中寻找ptp1b别构抑制剂,以解决ptp1b抑制剂选择性差、缺乏新型别构抑制剂等技术不足。发明人从中药红大戟knoxia valerianoides发现一系列蒽醌苷新化合物,是由茜草素型蒽醌与葡萄糖或樱草糖结合形成的苷类化合物,其蒽醌部分结构特殊,结构两侧的a/b苯环均有羟基或甲氧基取代,分子对接实验表明,a/b环的羟基和/或甲氧基对提高ptp1b抑制活性具有重要贡献。本发明所涉及的蒽醌苷类新化合物是一类新型的ptp1b别构抑制剂,目前尚没有关于蒽醌苷类化合物具有ptp1b别构抑制作用或选择性抑制ptp1b活性的报道。本发明的蒽醌苷类化合物对ptp1b抑制作用强、对tcptp的作用很弱,显示出很高的选择性;能够逆转胰岛素抵抗的骨骼肌c2c12细胞对葡萄糖的摄取效率;可用于制备选择性ptp1b抑制剂,研发特异性高、副作用低的2型糖尿病和/或肥胖治疗药物。
chp20p,流动相是甲醇/水,浓度为40%~90%。
14.优选地,步骤(2)中,hplc法中,色谱柱的固定相为ods;制备型hplc法中,流动相为40%~80%甲醇/水;半制备型hplc法中,流动相为30%~50%乙腈/水或45%~65%甲醇/水。
15.更为优选地,步骤(2)中,部位kvb用制备型hplc、53%甲醇/水纯化,再用半制备型hplc、30%乙腈/水纯化得到本发明化合物kv-9,用半制备型hplc、49%甲醇/水纯化得到本发明化合物kv-1。部位kvc先用制备型hplc、55%甲醇/水纯化,再用半制备型hplc、50%~57%甲醇/水纯化得到本发明化合物kv-4、kv-5、kv-6和kv-7。部位kvd先用制备型hplc、60%甲醇/水纯化,再用半制备型hplc、56%甲醇/水纯化得到本发明化合物kv-3和kv-8。部位kve先用制备型hplc、65%甲醇/水纯化,再用半制备型hplc、52%甲醇/水纯化得到本发明化合物kv-2。
16.本发明的目的之三是提供该类化合物或其药学上可接受的盐、酯、立体异构体、溶剂化合物在制备选择性ptp1b抑制剂、2型糖尿病治疗药物和/或肥胖症治疗药物中的应用。
17.本发明的系列化合物可以一种单独或多种联合使用。如果作为一组化合物使用,则可以将这些化合物同时、分别或有序地对受试对象给药。
18.本发明的系列化合物属于茜草素型蒽醌与糖形成的苷类化合物,每个化合物对ptp1b均有显著的抑制作用,其中化合物kv-4、kv-7和kv-8对ptp1b的抑制强度比对tcptp的抑制强度分别高73、25和63倍,是一类特异性ptp1b抑制剂。大部分茜草素型蒽醌的a环无取代基,而本发明的茜草素型蒽醌a环有羟基和/或甲氧基取代,初步的构效关系和分子对接实验表明a环的羟基和/或甲氧基对活性强度有重要贡献。而且酶抑制动力学和分子对接实验表明本发明的系列化合物是一类新型ptp1b别构抑制剂。本发明所涉及化合物的结构、选择性ptp1b抑制活性、作用于ptp1b别构位点的机制均为首次报道,为进一步研发特异性高的ptp1b抑制剂提供了参考,在开发靶向ptp1b的新型降糖药物、2型糖尿病治疗药物和/或肥胖症治疗药物方面有广阔的应用前景。
附图说明
19.图1:化合物kv-4的酶抑制动力学实验结果
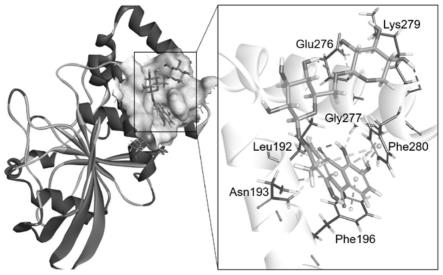
20.图2:化合物kv-4的分子对接结果
21.图3:化合物kv-1(a)、kv-3(b)和kv-8(c)对胰岛素抵抗的骨骼肌c2c12细胞葡萄糖摄取量的变化
具体实施方式
22.以下通过具体实施例对本发明的化合物、制备步骤和活性筛选实验过程作进一步的说明,以下实例是用于阐释本发明的技术内容,并不是对本
技术实现要素:
的限定,所有基于本发明所作出的变化或等同替换,均应属于本发明的保护范围。
23.实施例1化合物kv-1~kv-9的制备
24.红大戟20kg,粉碎后用95%乙醇于常温超声提取,提取液合并减压蒸干溶剂得浸膏3.9kg。浸膏溶于水后,用乙酸乙酯萃取3次,剩余的水溶液用大孔吸附树脂充分吸附,然后依次用0%、30%、50%、70%和95%的乙醇/水洗脱。70%乙醇/水洗脱部分再用mci柱色
谱分离,用40%~90%的甲醇/水洗脱,得到6个部位(kva、kvb、kvc、kvd、kve和kvf)。部位kvb用制备型高效液相色谱纯化,53%甲醇/水洗脱得到部位kvb-1、kvb-4和kvb-5。部位kvb-1用半制备型高效液相色谱纯化,30%乙腈/水洗脱得到化合物kv-9。部位kvb-4和kvb-5用半制备型高效液相色谱纯化,49%甲醇/水洗脱得到化合物kv-1。部位kvc用制备型高效液相色谱纯化,55%甲醇/水洗脱得到部位kvb-2、kvb-3和kvb-4。kvb-2用半制备型高效液相色谱纯化,57%甲醇/水洗脱得到化合物kv-6和kv-7。kvb-3和kvb-4用半制备型高效液相色谱纯化,50%甲醇/水洗脱得到化合物kv-4和kv-5。部位kvd先用制备型hplc纯化,60%甲醇/水洗脱,再用半制备型hplc纯化,56%甲醇/水洗脱得到化合物kv-3和kv-8。部位kvd先用制备型hplc纯化,65%甲醇/水洗脱,再用半制备型hplc纯化,52%甲醇/水洗脱得到化合物kv-2。得到的化合物根据表1、表2、表3和下列波谱学信息确定结构。
25.kv-1:uv(meoh):λ
max
(logε)413(4.85),337(3.93),301(4.35),272(4.85),218(4.70)nm;irν
max 3320,2886,1669,1632,1594,1481,1367,1296,1234,1077,1038,1004,922,895,765cm-1
;hr-esi-ms m/z 593.1480[m-h]-(calcd for c
27h29o15
,593.1501).
[0026]
kv-2:uv(meoh)λ
max
(logε)413(4.19),339(4.05),304(4.40),274(5.00),214(4.81)nm;irν
max 3544,3361,2923,2852,1672,1622,1595,1488,1414,1361,1308,1293,1239,1095,1074,1011,926,780,671cm-1
;(-)-hresims m/z 577.1519[m-h]-(calcd for c
27h29o14
,577.1552).
[0027]
kv-3:uv(meoh)λ
max
(logε)447(4.08),312(4.01),270(4.58),229(4.50)nm;irν
max 3342,2933,2883,1624,1604,1456,1438,1371,1318,1099,1074,1051,991,949,806,768cm-1
;(-)-hresims m/z 593.1478[m-h]-(calcd for c
27h29o15
,593.1501).
[0028]
kv-4:uv(meoh)λ
max
(logε)453(3.85),315(4.00),270(4.49),229(4.35)nm;irν
max 3273,2988,2901,1624,1599,1453,1412,1367,1276,1039,1015,892,769cm-1
;(-)-hresims m/z 579.1324[m-h]-(calcd for c
26h27o15
,579.1350)
[0029]
kv-5:uv(meoh)λ
max
(logε)447(4.05),266(4.57),215(4.83)nm;irν
max 3545,3306,2901,1625,1589,1484,1456,1421,1367,1263,1100,1080,1049,937,741cm-1
;(-)-hresims m/z 609.1410[m-h]-(calcd for c
27h29o16
,609.1450).
[0030]
kv-6:uv(meoh)λ
max
(logε)427(4.10),338(4.21),305(4.51),275(4.81),215(4.79)nm;irν
max 3330,2891,1668,1623,1593,1440,1368,1285,1035,1007,931,817cm-1
;(-)-hresims m/z 593.1468[m-h]-(calcd for c
27h29o15
,593.1501).
[0031]
kv-7:uv(meoh)λ
max
(logε)415(4.03),280(4.60),245(4.66)nm;irν
max 3569,3196,2918,1671,1611,1590,1443,1403,1330,1289,1244,1195,1154,1127,1073,1017,941,904,878,825,762,735,716cm-1
;(-)-hresims m/z 431.0955[m-h]-(calcd for c
21h19o10
,431.0973).
[0032]
kv-8:uv(meoh)λ
max
(logε)413(4.06),337(3.93),304(4.30),272(4.82),217(4.73)nm;irν
max 3319,2897,1665,1632,1593,1479,1446,1371,1330,1233,1095,1070,1027,1008,938,853,769cm-1
;(-)-hresims m/z 461.1046[m-h]-(calcd for c
22h21o11
,461.1078).
[0033]
kv-9:uv(meoh)λ
max
(logε)447(4.06),311(4.02),266(4.51),231(4.54)nm;irν
max 3281,2918,1621,1591,1456,1426,1374,1299,1224,1124,1070,985,940,765,727cm-1
;
(-)-hresims m/z 477.1003[m-h]-(calcd for c
22h21o12
,477.1028)。
[0034]
表1.化合物kv-1~kv-5的核磁共振氢谱数据
[0035][0036][0037]
表2.化合物kv-6~kv-9的核磁共振氢谱数据.
[0038][0039][0040]
表3.化合物kv-1~kv-9的核磁共振碳谱数据
[0041][0042]
实施例2ptp1b和tcptp抑制活性评价
[0043]
化合物用dmso配制成梯度浓度。将预先配制好的酶溶液(缓冲液含25mm hepes ph 7.5,150mm nacl,5mm dtt,2mm edta,含0.1μg ptp1b或0.15μg tcptp)加入96孔板中,每孔90μl,各加入1μl化合物溶液,以dmso为空白对照,每个浓度设置三个平行复孔,将96孔板放入恒温振荡器中,37℃振摇15min。15min后,加入10μl终浓度为4mm的p-npp溶液,于恒温振荡器中37℃振摇30min。30min后取出,依次加入20μl 3m naoh溶液终止反应,最后在酶标仪405nm处测od值,计算化合物对ptp1b的抑制率及ic
50
值。以钒酸钠(na3vo4)为阳性对照药。
[0044]
计算公式:抑制率=(od
空白-od
样品
)/od
空白
×
100%
[0045]
对以上数据釆用graphpad prism 8.0软件开展统计学分析,重复三次独立实验,数据用均数
±
标准差表示。
[0046]
表4.化合物kv-1~kv-9的酶抑制活性
[0047][0048]
si是ic
50
(tcptp)/ic
50
(ptp1b);nt是未检测。
[0049]
表4的数据表明化合物kv-1~kv-9均显示显著的ptp1b抑制活性。由于部分化合物的量不足,无法检测对tcptp的抑制作用,只检测了化合物kv-1、kv-3、kv-4、kv-7和kv-8对tcptp的抑制作用。阳性对照药na3vo4是一个经典的蛋白酪氨酸磷酸酶竞争性抑制剂,与底物竞争磷酸酶的活性位点,表4数据显示,na3vo4对ptp1b和tcptp抑制作用相当,无选择性。而kv-1、kv-3、kv-7和kv-8在最高浓度100μm时对tcptp仍无显著抑制作用,只有kv-4显示弱抑制作用。实验结果表明,该类化合物对ptp1b表现出高选择性,kv-4的选择性最高达74倍。
[0050]
实施例3ptp1b酶抑制动力学实验
[0051]
将预先配制好的ptp1b溶液加入96孔板中,每孔90μl,分别加入kv-4溶液1μl,终浓度分别为1、2、4μm,每个浓度设置三个复孔,以dmso为空白对照,将96孔板放入恒温振荡器中,37℃振摇15min。然后加入p-npp溶液(终浓度分别为2、4、8mm),立刻用酶标仪测405nm处15min内od值变化,计算酶解初速率。通过lineweaver-burk plot以底物浓度分之一和酶解初速率作图,分析对ptp1b的抑制类型。
[0052]
图1为动力学实验结果,各组曲线交汇至xy轴区域,说明kv-4是一种ptp1b混合型抑制剂,能与ptp1b的催化活性区域之外的其他位点结合,提示可能是与ptp1b的别构位点结合发挥抑制作用。
[0053]
实施例4分子对接
[0054]
应用分子对接软件biovia discovery studio 2021的c-docker模块,对kv-1~kv-9与ptp1b晶体结构的活性位点和变构位点进行分子对接模拟。ptp1b的晶体结构来自蛋白晶体库,编号为1t49。首先使用discovery studio 3.0软件对kv-1~kv-9的3d结构进行计算,得到最优构象。ptp1b蛋白结构经去水加氢后,用charm force field结构最优化。然后将化合物的最优构象与ptp1b的晶体结构进行对接计算,经软件打分,分析最高分构象的作用位点和结合方式。
[0055]
结果表明,化合物kv-1~kv-9无法与ptp1b的催化活性口袋对接成功,而能与ptp1b的变构位点良好结合,并通过一系列作用稳定酶-抑制剂形成的复合物构象,该结果与酶抑制动力学实验结果一致。以化合物kv-4的对接结果为例(图2),kv-4将蒽醌插入变构口袋,与phe196和leu192形成强π-π堆积作用,并与asn193形成氢键,增强结合作用力,同时结构中的糖与glu276、gly277和lys279形成氢键,进一步加强与变构位点的结合强度。因
此,本发明的化合物是一类新型ptp1b别构抑制剂,可开发为高效、高选择性的ptp1b抑制剂。
[0056]
实施例5化合物对胰岛素抵抗的骨骼肌c2c12细胞葡萄糖消耗的影响
[0057]
细胞分化:将c2c12小鼠成肌细胞培养至80%的密度时传代。培养足够量细胞后,将细胞消化、离心、重悬,按照2
×
104个/100μl进行种板,于细胞培养箱中培养12h,待细胞贴壁后,弃上清,每孔加入100μl pbs润洗三次后,每孔加入新鲜分化培养液200μl,继续培养24h。自此之后每24h更换一次新鲜的分化培养液,共分化培养96h,直至将单个梭形细胞分化为规则排列的多核融合的肌细胞。
[0058]
胰岛素抵抗的肌细胞模型构建:吸弃已分化的肌细胞培养液,每孔加入100μl pbs润洗细胞3次,正常组细胞每孔加入200μl高糖dmem培养基,模型组及加药组细胞每孔加入200μl配制好的建模胰岛素溶液,将细胞放置在37℃、5%co2的细胞培养箱中继续培养48h。48h后,若模型组与空白组比较,细胞葡萄糖摄取量显著降低,证明建模成功。
[0059]
给药:将化合物用高糖dmem培养基稀释,终浓度依次为50μm、33.3μm、22.2μm,吸弃每孔的培养液后,正常组及模型组细胞每孔加入200μl高糖dmem培养基,加药组每孔加入200μl各浓度药物,每个浓度设置三个复孔,重复三次独立实验。
[0060]
葡萄糖含量检测:将细胞放置在培养箱中继续培养。48h后,按照试剂盒中说明书的操作方法配制葡萄糖含量检测液,在新的96孔板中,每孔加入180μl葡萄糖含量检测液,分别加入20μl各孔的细胞上清液,在37℃的恒温震荡器中震荡孵育15min。15min后将96孔板于酶标仪上测定505nm处od值,按照试剂盒说明书的计算公式计算每孔葡萄糖含量。将含有细胞的96孔板的上清中分别加入20μl预先配制好的mtt溶液,置细胞培养箱中培养4h后,用酶标仪测定490nm处od值。为了去除细胞数对检测结果的影响,采用葡萄糖含量/mtt数值作为最终葡萄糖含量。
[0061]
图3为不同浓度的kv-1、kv-3和kv-8对胰岛素抵抗的骨骼肌c2c12细胞对葡萄糖消耗量的变化。与正常组相比,模型组细胞对葡萄糖消耗量显著降低,而给药组细胞对葡萄糖消耗量显著增加,且具有量效关系。这说明kv-1、kv-3和kv-8能逆转骨骼细胞对胰岛素的低敏感性,提高骨骼肌细胞对胰岛素的响应,从而提高对葡萄糖的摄取与消耗。因此,该类蒽醌苷化合物有望开发成为一种新型的降糖药物、治疗2型糖尿病和/或肥胖症的药物。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1