一种羧基修饰和负载的聚苯乙烯化学发光纳米球及其制备方法
1.本发明属于材料技术领域,具体涉及一种羧基修饰和负载的聚苯乙烯化学发光纳米球及其制备方法。
背景技术:
2.光激化学发光免疫分析法和酶联免疫吸附分析法(elisa)、荧光免疫分析法等传统方法相比,具有明显优势。一是均相反应,免去了洗涤步骤;二是发射波长短于激发波长,避免了背景荧光的干扰。
3.光激化学发光免疫分析法所用到的纳米探针包含供体球和受体球。供体球是粒径在200nm左右的纳米球,负载光敏剂,在波长为680nm的激光激发下,产生单线态氧。受体球是粒径在200nm左右的纳米球,负载化学发光剂和荧光剂。当受体球与单线态氧接触时,受体球上的化学发光剂被单线态氧氧化,产生的激发态产物通过化学发光能量共振转移(cret)过程激发荧光剂,荧光剂跃迁回基态时发出波长为615nm的红光。将待测抗原的两种不同的单克隆抗体,分别修饰受体球和供体球。当含有待测抗原的样品与供体球、受体球在样品池中一起孵育时,“供体球-抗体1-抗原-抗体2-受体球”夹心复合物形成。用波长为680nm的激光照射样品池,在夹心复合物中,供体球产生的单线态氧扩散至受体球,与受体球作用而发光。因为单线态氧在水中扩散距离仅有200nm,所以未形成夹心复合物的纳米球不参与发光,因此样品池的发光强度与夹心复合物含量成正比,以此可测出被测抗原含量,且免去了洗涤步骤。
4.目前,商用的光激化学发光免疫分析供体球、受体球都存在许多问题:
5.1.形貌差,形状不规则。
6.2.单分散性差,纳米粒子的粒径分布范围很宽。
7.3.团聚、粘连严重。
8.4.产物形貌与粒径难以控制。
9.5.信号强度还有提升空间。
技术实现要素:
10.针对现有技术的不足,提供一种形貌为完美球形、分散性好、单分散性高、形貌与粒径可控的化学发光纳米球的制备方法,该化学发光纳米球可用作光激化学发光免疫分析受体球,还可用于活性氧的检测与成像。
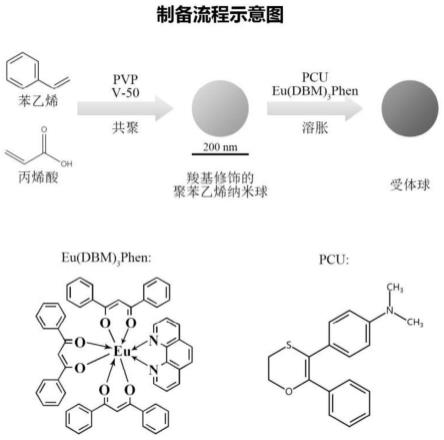
11.为了实现上述发明目的,本发明提供的技术方案如图1所示,包括羧基修饰的聚苯乙烯纳米球(以下简称ps-cooh)的制备和光激化学发光免疫分析受体球(负载eu(dbm)3phen和pcu的化学发光纳米球,以下简称eu&pcu@ps-cooh)的制备。
12.具体的,本发明通过以下技术方案来实现:
13.一种聚苯乙烯化学发光纳米球的制备方法,包括:
14.(1)羧基修饰的聚苯乙烯纳米球(以下简称ps-cooh)的制备;
15.(2)在步骤(1)获得羧基修饰的聚苯乙烯纳米球上负载eu(dbm)3phen和pcu。
16.作为本发明的一种优选技术方案:所述步骤(1)包括:
17.(1.1)n2保护下,在去离子水中,加入聚乙烯吡咯烷酮,苯乙烯,搅拌回流;
18.(1.2)加入引发剂搅拌回流,优选偶氮二异丁脒盐酸盐(v-50);
19.(1.3)加入丙烯酸搅拌回流,反应后,加入无水乙醇离心,去除上清液,后加入去离子水超声分散。
20.作为本发明的一种优选技术方案:每5.5ml苯乙烯对应的聚乙烯吡咯烷酮用量为76~380mg。
21.作为本发明的一种优选技术方案:每5.5ml苯乙烯对应的偶氮二异丁脒盐酸盐用量为75mg。
22.作为本发明的一种优选技术方案:每5.5ml苯乙烯对应的丙烯酸用量为0.2ml。
23.作为本发明的一种优选技术方案:加入v-50引发剂6h后加入丙烯酸,继续反应18h,所述步骤中,搅拌转速800r/min,回流温度70℃。
24.通过大量试验研究,选择该优选技术方案,可制得尺寸约为200nm的纳米球,符合光激化学发光免疫分析法对受体球粒径的要求,分散性与单分散性好,可作为光激化学发光免疫分析受体球的基材。
25.作为本发明的一种优选技术方案:所述步骤(2)包括:
26.(2.1)配制溶胀剂:ch2cl2溶解eu(dbm)3phen和pcu配制溶胀剂。
27.优选,按每1ml ch2cl2溶解0.5g eu(dbm)3phen和0.1g pcu配制溶胀剂。溶胀剂配制后不可久置,应现配现用。
28.(2.2)将ps-cooh分散于十二烷基硫酸钠(sds)水溶液:聚苯乙烯(ps)和sds的浓度分别为20mg/ml和5mg/ml。
29.(2.3)在棕色小瓶中,取步骤(2)所得的分散液,800r/min搅拌下,滴加溶胀剂,盖上瓶盖维持800r/min转速搅拌24h,开盖继续维持800r/min转速搅拌24h挥发ch2cl2;
30.(2.4)ch2cl2挥发后,将步骤(3)所得的分散液离心,弃上清液,沉淀分散于水中,即得eu&pcu@ps-cooh水分散液。
31.通过大量试验研究,选择该优选技术方案,所得产物没有可见的变形,分散性和单分散性好,化学发光强烈。
32.在此过程中,不需要用有机溶剂洗涤纳米球去除未溶胀进纳米球的pcu和eu(dbm)3phen。因为cret要求pcu分子和eu(dbm)3phen分子之间的距离在10nm以内,所以未能溶胀进纳米球而随着溶胀剂挥发而析出的pcu晶体和eu(dbm)3phen晶体不参与发光。若使用有机溶剂洗涤纳米球,会造成pcu分子和eu(dbm)3phen分子被从纳米球中抽提出来。
33.本发明相对于现有技术的有益效果包括:
34.本发明通过简单的方法,制得了分散性好、单分散性高、粒径约为200nm的羧基修饰的聚苯乙烯纳米球和化学发光纳米球。本发明提供的化学发光纳米球可以与包括单线态氧在内的ros作用而发出615nm的红光,适合作为光激化学发光免疫分析法受体球,本发明提供的化学发光纳米球克服了商用光激化学发光免疫分析受体球形貌差、单分散性差、团聚严重、形貌与粒径难控制等问题。此外,本发明提供的化学发光纳米球还可以应用于体内
肿瘤与炎症部位的化学发光成像。肿瘤和炎症部位的ros过度表达,ros与本发明提供的化学发光纳米球作用发出615nm的红光,以此成像。这种成像具有明显优势。一是不需要外界激发光,因此可以避免组织的自身荧光干扰,也避免了激发光对被穿透组织的伤害;二是615nm红光对组织的穿透力较强,成像效果好;三是pcu和eu(dbm)3phen水溶性很低,且不易从纳米球中泄露,对人体毒性低。
附图说明
35.图1 ps-cooh的制备和eu&pcu@ps-cooh制备流程示意图;
36.图2 ps-cooh的粒径分布;
37.图3 ps-cooh的sem图像;
38.图4 eu&pcu@ps-cooh的粒径分布;
39.图5 eu&pcu@ps-cooh的sem图像。
具体实施方式
40.下面结合实施例和附图对本发明作进一步说明,但本发明不局限于此:
41.实施例1
42.制备过程如图1所示
43.(1).ps-cooh的制备
44.(1.1)n2保护下,在100ml三口瓶中加入49ml去离子水、380mg平均分子量为58000的聚乙烯吡咯烷酮(pvp)、5.5ml苯乙烯,搅拌回流升温至70℃。(搅拌转速800r/min)
45.(1.2)通n230min后,逐滴加入75mg/ml的偶氮二异丁脒盐酸盐(v-50引发剂)水溶液1ml,继续通n2,并维持搅拌回流。(搅拌转速800r/min,回流温度70℃)
46.(1.3)加入v-50引发剂6h后,逐滴加入0.2ml丙烯酸,继续通n2,并维持搅拌回流。(搅拌转速800r/min,回流温度70℃)
47.(1.4)加入丙烯酸18h后,停止反应,将所得的产物分散液大致等分成4份,加入至4根50ml离心试管中,每管加入约20ml无水乙醇并用无水乙醇配平,振荡混匀,9000r/min离心30min,弃上清液,每管加入无水乙醇10ml,用玻璃棒搅拌的同时用超声清洗机超声,直至沉淀完全分散。将4管中的分散液合并为2管,合并后的2管用无水乙醇定容至约35ml并用无水乙醇配平,9000r/min离心5min,弃上清液,每管加入无水乙醇35ml,用玻璃棒搅拌的同时用超声清洗机超声,直至沉淀完全分散,用无水乙醇配平,9000r/min离心5min,弃上清液,每管加入35ml去离子水,用玻璃棒搅拌的同时用超声清洗机超声,直至沉淀完全分散,即得ps-cooh水分散液。
48.(1.5)标定浓度:标定前,为确保步骤4所得的ps-cooh分散液已被充分混匀,先用超声细胞破碎仪在300w功率下将其超声5min。取一根1.5ml离心管,称出空管质量(记为m0),置于离心管架上,用移液枪加入ps-cooh分散液1ml,然后敞开管盖,在烘箱中60℃烘24h将水完全烘干,盖上管盖,称出全管质量(记为m总),即可算出步骤4所得的分散液中ps-cooh的浓度为c=(m
总-m0)/1ml,大约为60mg/ml。
49.(1.6)动态光散射(dls)测定ps-cooh水分散液:测得数均水合粒径为257.4nm,多分散系数(pdi)为0.116,粒径分布如图2所示,平均zeta电位为-24.7mv。
50.(1.7)如图3所示,ps-cooh的扫描电子显微镜(sem)图像显示其形貌呈完美的球形,粒径约为200nm,单分散性高。
51.(2).eu&pcu@ps-cooh的制备
52.(2.1)配制溶胀剂:按每1ml ch2cl2溶解0.5g eu(dbm)3phen和0.1g pcu配制溶胀剂。溶胀剂配制后不可久置,应现配现用。
53.(2.2)将ps-cooh分散于十二烷基硫酸钠(sds)水溶液:用超声细胞破碎仪在300w功率下将ps-cooh水分散液超声5min,按测得的ps-cooh浓度加入去离子水和sds水溶液,使得最终聚苯乙烯(ps)和sds的浓度分别为20mg/ml和5mg/ml。
54.(2.3)用超声细胞破碎仪在300w功率下将步骤(2)所得的分散液超声5min,在10ml棕色小瓶中,取4ml刚超声后的步骤(2)所得的分散液,800r/min搅拌下,滴加0.1ml溶胀剂,盖上瓶盖维持800r/min转速搅拌24h,开盖继续维持800r/min转速搅拌24h挥发ch2cl2。
55.(2.4)ch2cl2挥发后,将步骤(3)所得的分散液转移至50ml离心试管中,加入20ml去离子水,11000r/min离心30min,弃上清液,沉淀分散于20ml水中,即得eu&pcu@ps-cooh水分散液。
56.不需要用有机溶剂洗涤纳米球去除未溶胀进纳米球的pcu和eu(dbm)3phen。因为cret要求pcu分子和eu(dbm)3phen分子之间的距离在10nm以内,所以未能溶胀进纳米球而随着溶胀剂挥发而析出的pcu晶体和eu(dbm)3phen晶体不参与发光。若使用有机溶剂洗涤纳米球,会造成pcu分子和eu(dbm)3phen分子被从纳米球中抽提出来。
57.(2.5)dls测定eu&pcu@ps-cooh水分散液:测得数均水合粒径为244.3nm,pdi为0.036,粒径分布如图4所示,平均zeta电位为-13.3mv。
58.(2.6)如图5所示,eu&pcu@ps-cooh的sem图像显示其形貌呈完美的球形,粒径约为200nm,单分散性高,形貌和ps-cooh无明显差异。
59.实施例2
60.如表1所示,用爱兴生物的均相化学发光免疫分析仪分别测试实施例1获得ps-cooh和eu&pcu@ps-cooh在亚甲基蓝(mb)水溶液产生的单线态氧作用下的化学发光(测试条件:用到ps球时,ps球浓度一律为0.1mg/ml;用到游离染料时,染料浓度一律为1μg/ml;总体积一律为0.2ml;激发波长680nm,发射波长615nm),测出了eu&pcu@ps-cooh强烈的化学发光。表明eu&pcu@ps-cooh在接触到单线态氧、h2o2等活性氧(ros)时,纳米球上负载的pcu被氧化裂解,裂解产物处于激发态,通过化学发光共振能量转移(cret)激发eu(dbm)3phen,使之发出波长为615nm的红光,eu&pcu@ps-cooh可作为光激化学发光免疫分析受体球,可用于活性氧检测和成像。
61.表1:ps-cooh和eu&pcu@ps-cooh的光激化学发光
62.供/受体eu&pcu@ps-coohps-cooh去离子水mb水溶液116637132133去离子水187193172
63.对比实施例1
64.参照实施例1的技术方案,当每5.5ml苯乙烯对应的聚乙烯吡咯烷酮用量为76mg时,产物的平均粒径约为500nm,当每5.5ml苯乙烯对应的聚乙烯吡咯烷酮用量为152mg时,产物的平均粒径约为410nm。
65.当每5.5ml苯乙烯对应的聚乙烯吡咯烷酮用量为380mg时,产物的平均粒径约为200nm。每5.5ml苯乙烯对应的偶氮二异丁脒盐酸盐用量为75mg,当每5.5ml苯乙烯对应的丙烯酸用量为0.2ml时,产物的分散性、单分散性最好。
66.以上内容是结合具体的优选实施方式对本发明所作的进一步详细说明,不能认定本发明的具体实施只局限于这些说明。对于本发明所属技术领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干简单推演或替换,都应当视为属于本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1