一种基于人源细胞的不同突变率标准品制备方法与流程
1.本发明涉及基因检测技术领域,尤其涉及一种基于人源细胞的不同突变率标准品制备方法。
背景技术:
2.基因检测技术具有准确率高、速度快的优点,在临床上广泛应用。通常采用试剂盒进行基因检测,试剂盒内包含了引物和溶剂等试剂,以扩增方式完成目的基因的筛查。应用于临床的基因检测试剂盒通常具有较高的检测准确率。在进行基因检测试剂盒研发时,为了测试试剂盒的检测准确性,通常以具有准确目的基因突变率的标准品作为检测对象,对比检测结果突变率和标准品突变率,得出试剂盒的检测准确性。
3.目前,用于基因检测试剂盒的标准品主要以人工化学合成的方式制备,即对已知碱基顺序的基因,利用基因合成仪,设置好特定的程序,并加入酶等原料,使dntp按照固定的顺序进行化学反应,从而合成目的基因。然后这样人工合成的基因只是一个片段,只是复杂基因组dna的一部分,与从病变细胞系提取出的基因组dna背景相差甚远。可见,这种人工化学合成的标准品结构单一、环境简单,与临床样品相比相差甚远。这就导致对基因检测试剂盒的检测准确性的判断不够精准,应用于临床疾病筛查时容易出现假阳性。
4.有鉴于此,需要开发一种接近临床样本、可量化、精确且具有重复性的标准品,以满足基因检测试剂盒开发的准确性,进而提高临床检测的正确率。
技术实现要素:
5.本发明的目的在于提出一种基于人源细胞的不同突变率标准品制备方法,以人源细胞的点突变材料制备标准品,能很好的模拟临床样本,基因检测试剂盒检测准确性的判断更为准确。
6.为达此目的,本发明采用以下技术方案:
7.一种基于人源细胞的不同突变率标准品制备方法,包括以下步骤:
8.(1)通过基因编辑技术对人源细胞系进行点突变,得到突变材料;
9.(2)对突变材料进行基因组dna提取,纯化得到突变型gdna;
10.(3)以人源野生型细胞系gdna与突变型gdna进行混合,得到目标突变率的标准品;
11.(4)设计突变基因的ddpcr检测探针,并用ddpcr进行质检。
12.进一步的,所述步骤(3)中,以人源野生型细胞系gdna与突变型gdna进行混合的方法为:
13.预设标准品的目标突变率、目标浓度、gdna总量和目标体积;
14.根据预设值计算标准品中人源野生型细胞系gdna和突变型gdna的质量;
15.根据提取的含突变型gdna溶液中突变型gdna的浓度,计算需进行混合的含突变型gdna溶液体积;
16.计算含人源野生型细胞系gdna溶液体积;
17.将对应体积的含突变型gdna溶液和含人源野生型细胞系gdna溶液进行混合得到标准品;
18.验证标准品中突变型gdna的突变率,若与目标突变率一致,则进入产品分装工序,若与目标突变率不一致则调整混合体积后再次验证。
19.进一步的,所述根据预设值计算标准品中人源野生型细胞系gdna和突变型gdna的质量的方法中,计算突变型gdna的质量的公式如下:
[0020][0021]
其中:
[0022]mt=x
:1μg标准品在x突变率下所需突变细胞的gdna质量,单位ng;
[0023]
t:标准品突变率,x=0%、2%、5%、10%、20%、50%或100%;
[0024]
t0:细胞理论突变率;
[0025]
q为预设的gdna总量:1μg;
[0026]
计算得到对应标准品中所需人源野生型细胞系gdna的质量m,单位ng,计算公式为:m=q—m
t=x
。
[0027]
进一步的,所述调整混合体积的公式如下:
[0028][0029]c1v1’+c
2v2’=q公式b-2;
[0030]
其中:
[0031]
t:标准品突变率;
[0032]
t':验证检测的实际突变率;
[0033]v1
:t值下,第一次验证检测调配的突变型gdna的母液体积;
[0034]v2
:t值下,第一次验证检测调配的人源野生型细胞系gdna的母液体积;
[0035]v1
':重新调回t值时,突变型gdna所需母液体积;
[0036]v2
':重新调回t值时,人源野生型细胞系gdna所需的母液体积;
[0037]
c1:突变型gdna的母液浓度;
[0038]
c2:人源野生型细胞系gdna的母液浓度。
[0039]
进一步的,当计算所得的含突变型gdna溶液体积和含人源野生型细胞系gdna溶液体积之和小于目标体积时,加入溶剂达到目标体积。
[0040]
进一步的,所述步骤(1)中,突变材料为杂合或纯合的目的突变细胞系;
[0041]
所述步骤(2)中,对突变材料进行gdna提取,对提取的gdna进行凝胶电泳检测和分光光度计检测合格后,得到突变位点杂合或纯合的条带单一且不含其它杂质的突变型gdna。
[0042]
本发明提供的技术方案可以包括以下有益效果:
[0043]
本发明的标准品制备方法中,以人源细胞的点突变材料,以人源野生型细胞系gdna与突变型gdna混合实现标准品中突变型gdna突变率的调节,能很好的模拟临床样本,基因检测试剂盒检测准确性的判断更为准确。可以理解的,突变型gdna具有多种突变率,采
用不同突变率的突变型gdna可制备得到不同突变率标准品。
附图说明
[0044]
图1是目标突变率50%的标准品样本的荧光检测融合图;
[0045]
图2是目标突变率50%的标准品样本的荧光检测突变型阳性微滴计数图;
[0046]
图3是目标突变率50%的标准品样本的荧光检测野生型阳性微滴计数图。
具体实施方式
[0047]
下面结合具体实施方式进一步说明本发明的技术方案。
[0048]
本发明提供一种基于人源细胞的不同突变率标准品制备方法,包括以下步骤:
[0049]
(1)通过基因编辑技术对人源细胞系进行点突变,得到突变材料;
[0050]
(2)对突变材料进行基因组dna提取,纯化得到突变型gdna;
[0051]
(3)以人源野生型细胞系gdna与突变型gdna进行混合,得到目标突变率的标准品;
[0052]
(4)设计突变基因的ddpcr检测探针,并用ddpcr进行质检。
[0053]
本发明的标准品制备方法中,以人源细胞的点突变细胞系为材料,将人源野生型细胞系gdna与突变型gdna混合实现标准品中突变型gdna突变率的调节,能很好的模拟临床样本,基因检测试剂盒检测准确性的判断更为准确。可以理解的,突变型gdna具有多种突变率,采用不同突变率的突变型gdna 可制备得到不同突变率标准品和不同突变位点的标准品。
[0054]
为了得到目的突变率更为准确的标准品,进一步的,步骤(3)中,以人源野生型细胞系gdna与突变型gdna进行混合的方法为:
[0055]
预设标准品的目标突变率、目标浓度、gdna总量和目标体积;
[0056]
根据预设值计算标准品中人源野生型细胞系gdna和突变型gdna的质量;
[0057]
根据提取的含突变型gdna的溶液中突变型gdna的浓度,计算需进行混合的含突变型gdna的溶液体积;
[0058]
计算含人源野生型细胞系gdna的溶液体积;
[0059]
将对应体积的含突变型gdna的溶液和含人源野生型细胞系gdna的溶液进行混合得到目标突变率的标准品;
[0060]
验证标准品中突变型gdna的突变率,若与目标突变率一致,则进入产品分装工序,若与目标突变率不一致则调整混合体积后再次验证。
[0061]
具体的,根据预设值计算标准品中人源野生型细胞系gdna和突变型gdna 的质量的方法中,计算突变型gdna的质量的公式如下:
[0062][0063]
其中:
[0064]mt=x
:1μg标准品在x突变率下所需突变细胞的gdna质量,单位ng;
[0065]
t:标准品突变率,x=0%、2%、5%、10%、20%、50%或100%;
[0066]
t0:细胞理论突变率,100%或50%;
[0067]
q为预设的gdna总量:1μg;计算得到对应标准品中所需人源野生型细胞系gdna的
质量m,单位ng,计算公式为:m=q—m
t=x
。
[0068]
具体的,调整混合体积的公式如下:
[0069][0070]c1v1’+c
2v2’=q
ꢀꢀ
公式b-2;
[0071]
其中:
[0072]
t:标准品突变率;
[0073]
t':验证检测的实际突变率;
[0074]v1
:t值下,第一次验证检测调配的突变型gdna的母液体积;
[0075]v2
:t值下,第一次验证检测调配的人源野生型细胞系gdna的母液体积;
[0076]v1
':重新调回t值时,突变型gdna所需母液体积;
[0077]v2
':重新调回t值时,人源野生型细胞系gdna所需的母液体积;
[0078]
c1:突变型gdna的母液浓度;
[0079]
c2:人源野生型细胞系gdna的母液浓度。
[0080]
当提取的含突变型gdna的溶液中突变型gdna浓度较高时,会出现计算所得的含突变型gdna的溶液体积和含人源野生型细胞系gdna的溶液体积之和小于目标体积的情况,此时,加入溶剂达到目标体积。该溶剂采用溶解gdna 的溶剂,可采用基因组dna提取试剂盒中的洗脱液。
[0081]
更进一步说明,步骤(1)中,突变材料为杂合或纯合的目的突变细胞系;步骤(2)中,对突变材料进行gdna提取,对提取的gdna进行凝胶电泳检测和分光光度计检测合格后,得到突变位点杂合或纯合的条带单一且不含其它杂质的突变型gdna。
[0082]
以下通过实施例进一步阐述本发明。
[0083]
本实施例基于人源细胞的不同突变率标准品制备方法步骤如下:
[0084]
通过基因编辑技术对人源细胞系hek293进行c.1799t》a点突变,得到纯合突变材料,同时设计ddpcr检测所用探针,序列如下:
[0085]
braf p.v600e-f1:gttttcctttacttactacacctca
[0086]
braf p.v600e-r1:tagcctcaattcttaccatcc
[0087]
对纯合突变和野生型hek293细胞分别进行gdna提取,对提取的gdna 进行凝胶电泳检测和分光光度计检测合格后,得到条带单一且不含其它杂质的突变型和野生型gdna。
[0088]
预设标准品的目标浓度为50ng/μl、gdna总量1μg和目标体积20μl,根据公式a计算并列出配置突变率为50%、20%和5%的标准品样品所需hek293 的突变型和野生型gdna的质量需求表,如下表所示。
[0089]
[0090]
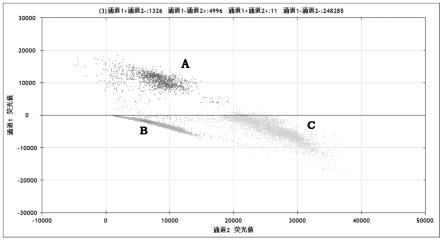
再根据含突变型gdna溶液(母液)和含野生型gdna溶液(母液)中的 gdna浓度,计算出所需体积,最后用te补充总体积至20μl,用ddpcr先检测配置突变率为50%的标准品样品是否符合配置突变率,图1、图2和图3 是所得配置突变率50%的标准品样本的ddpcr荧光检测图,其中,a(蓝色) 为突变型阳性微滴,b(灰色)为阴性微滴,c(绿色)为野生型阳性微滴,检测结果如下:
[0091][0092]
再次测定母液浓度,根据公式b-1和公式b-2以及ddpcr检测的配置突变率50%样品的实际突变率,计算配置突变率为20%和5%的样品体系(如下表所示),然后对配置突变率20%和5%的标准品样品进行ddpcr检测即可。
[0093][0094]
对配置突变率20%和5%的标准品样品进行ddpcr检测的结果如下表所示。
[0095]
[0096]
ddpcr实际检测结果与配置突变率的差异可接受范围如下表所示。
[0097]
x=0%可接受范围≤0.1%;0《x<5%可接受范围=
±
30%;5%≤x<10%可接受范围=
±
20%;x≥10%可接受范围=
±
10%;
[0098]
可见,配置突变率20%和5%的标准品样品的ddpcr实际检测结果与配置突变率的差异在可接受范围之内,故该检测合格。接下来根据相应的gdna体积进行扩大混合和分装并进行包装。
[0099]
以上结合具体实施例描述了本发明的技术原理。这些描述只是为了解释本发明的原理,而不能以任何方式解释为对本发明保护范围的限制。基于此处的解释,本领域的技术人员不需要付出创造性的劳动即可联想到本发明的其它具体实施方式,这些方式都将落入本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1