一种雪菊提取物的制备方法及其应用
1.本发明涉及医药技术领域,涉及一种雪菊提取物的制备方法及其在改善酒精性脂肪肝病和糖尿病肾病的药物和保健品中的用途。
背景技术:
2.雪菊,学名蛇目菊,为菊科金鸡菊属植物两色金鸡菊(coreopsis tinctoria)的头状花序。雪菊原产于美国中西部地区,后在我国引种栽培,主要分布在昆仑山北麓的高海拔地区,俗称“昆仑雪菊”,目前已在新疆和田地区大面积种植。生长于我国新疆和田地区昆仑山北麓海拔3000米以上雪域的野生雪菊,因其高寒的特殊生长环境而具有独特的降压、降脂和降糖功效,加之产量少,采摘困难而显得尤为珍贵,是新疆的特色珍稀药用植物资源。长期以来,雪菊在民间被作为花茶应用,近年来被开发为保健产品用于防治高血压、高血脂和高血糖等疾病,并是新疆地区的维吾尔族医院的常用药材。刘江云等利用乙醇回流提取,再经大孔树脂精制得到雪菊提取物,其中马里苷和黄诺玛苷总含量大于10%,并利用体内实验研究了雪菊提取物对高脂血症的调节作用和抗氧化作用,结果表明该雪菊提取物大小剂量组可降低血清中tg水平(p《0.05),降低血清中tc但无统计学差异(cn 104173400 a)。至目前,尚未见雪菊治疗非酒精性脂肪肝病相关的报道。鲁南等报道了一种改善糖尿病肾病的雪菊提取物的制备方法,其利用水提取雪菊粉末,再利用强电场萃取雪菊水溶液得到雪菊提取物,该雪菊提取物含有黄酮、绿原酸和皂苷,体内实验提示该雪菊提取物对肝、肾功能无毒性,可改善高血脂症(cn 109010406 a)。毛新民等采用高糖诱导的大鼠肾小球系膜细胞建立糖尿病肾病体外模型,发现雪菊乙酸乙酯提取物可能通过抑制大鼠肾小球系膜细胞增殖及纤维化因子表达发挥其对糖尿病肾病肾脏保护作用[中国实验方剂学杂志。2017,23(19):134]。马里苷是雪菊中的主要活性成分,毛新民等报道其可抑制糖尿病小鼠和高糖诱导的人肾小管上皮细胞(hk-2)中的钠-葡萄糖共转运蛋白2(sglt2)活性,激活腺苷酸激活蛋白激酶(ampk)信号通路,可以改善糖尿病肾病(biomedicine&pharmacotherapy,2020,131:110684)。
[0003]
非酒精性脂肪肝病(nafld)是指除外酒精和其他明确的损肝因素所致的肝细胞内脂肪过度沉积为主要特征的临床病理综合征,其发生和发展与脂代谢紊乱、炎性因子增加、ii型糖尿病、代谢综合征及高血压病、动脉粥样硬化等危险因素密切相关,其中以胰岛素抵抗、热量及脂肪类物质摄入过量为诱发nafld的最重要因素。nafld是一种进行性疾病,从非酒精性脂肪肝(nafl)到非酒精性脂肪性肝炎(nash),再到肝纤维化,最后可能发展成为肝硬化(nafld-lc)和肝癌(hcc),是引发肝脏相关疾病死亡率增加的危险因素。nafld在全球患病率呈现持续上升趋势,在我国已成为最常见的肝脏疾病。
[0004]
糖尿病肾脏病变是糖尿病患者的一个重要并发症,其中最具特征性的是糖尿病肾小球硬化症,即所谓的糖尿病肾病(diabetic nephropathy,dn)。dn的病因和发病机制目前尚不十分明确,一般认为可能为多因素所致,主要包括代谢紊乱、肾小球血流动力学改变和遗传易感性等,其中代谢紊乱可能为其先决条件。dn是糖尿病最主要的微血管并发症质疑,
约三分之一的糖尿病患者合并dn,目前已取代慢性肾小球肾炎,成为全球范围内导致终末期肾病的最主要病因。传统的ⅱ糖尿病肾病动物模型的建立方法主要有3种,包括自发性、诱发性和转基因动物模型。临床上的糖尿病肾病一般都是由生活习惯和环境因素造成,其中只有很少部分是由遗传因素引起的,所以自发性与转基因动物模型与临床上糖尿病肾病的病理特点并不完全相符。同时自发性和转基因动物模型比较稀有且价格高昂,极大地限制了相关研究的开展。因此,综合发病机制及可操作性等方面考虑,诱发性动物模型中高能量饮食联合链脲佐菌素(stz)诱导的动物模型是目前较为理想的ⅱ型糖尿病肾病模型。
技术实现要素:
[0005]
本发明目的在于,提供一种雪菊提取物的制备方法及其应用,该方法从雪菊头状花序中采用乙醇提取、大孔树脂柱层析后得到雪菊提取物中七个主要活性成分黄诺玛苷、槲皮万寿菊素-7-o-β-吡喃葡萄糖苷、圣草酚-7-o-β-吡喃葡萄糖苷、槲皮素-7-o-β-吡喃葡萄糖苷、马里苷、海生菊甙和奥卡宁的含量为70-79%,通过动物实验证明该雪菊提取物具有改善非酒精性脂肪肝病的能力,可显著改善高脂诱导的非酒精性脂肪肝病小鼠的肝脏脂肪沉积和炎症反应,降低体重增加和血液学指标,改善肝功能和调节脂代谢紊乱,显示出改善非酒精性脂肪肝病的作用;同时动物实验表明:该雪菊提取物具有改善糖尿病肾病的功效,可改善糖尿病肾病小鼠糖的脂代谢和肾功能,显示出改善糖尿病肾病的作用。即该提取物在非酒精性脂肪肝病和糖尿病肾病药物中的用途。
[0006]
本发明所述的一种雪菊提取物的制备方法,按下列步骤进行:
[0007]
a、提取:将干燥的雪菊粉碎后,用浓度为50-80%乙醇按重量体积比雪菊:乙醇=1:10-30热回流提取,温度60-90℃,每次0.5-3小时,重复提取2-3次,合并提取液;
[0008]
b、浓缩:将步骤a得到提取液进行减压蒸馏至无醇味,除去乙醇,得到浓缩液;
[0009]
c、大孔树脂柱层析:将步骤b得到的浓缩液加水稀释,上样至预处理好的hpd-300、hpd-100、d101或ab-8大孔树脂柱,依次用水、40-100%乙醇梯度洗脱,收集40-80%乙醇洗脱部位,浓缩,干燥,即得雪菊提取物,其中雪菊提取物中七个主要活性成分黄诺玛苷、槲皮万寿菊素-7-o-β-吡喃葡萄糖苷、圣草酚-7-o-β-吡喃葡萄糖苷、槲皮素-7-o-β-吡喃葡萄糖苷、马里苷、海生菊甙和奥卡宁的含量为70-79%。
[0010]
所述方法获得的雪菊提取物在制备改善非酒精性脂肪肝病的药物中的用途。
[0011]
所述方法获得的雪菊提取物在制备用于改善糖尿病肾病的药物中的用途。
[0012]
本发明的优点是:本发明获得的一种雪菊提取物可应用于制备非酒精性脂肪肝病和糖尿病肾病药物。所述雪菊提取物与现有技术相比,该提取物制备工艺更为简洁,化学组成稳定,活性成分纯度高,功效稳定。
附图说明
[0013]
图1为本发明获得的雪菊提取物ce的高效液相色谱图;
[0014]
图2为本发明获得的雪菊提取物ce对nafld小鼠体重变化的影响;
[0015]
图3为本发明获得的雪菊提取物ce对nafld小鼠肝脏指数、附睾脂肪和皮下脂肪指数变化的影响,其中a,b,c,d,e用于表明组间通过tukey's的anova统计学差异,p《0.05;各组间有相同字母即代表两组之间无显著性差异,各组间没有相同字母则代表两组之间差异
显著。
[0016]
图4为本发明获得的雪菊提取物ce对nafld小鼠血清中alt和ast的影响,其中a为alt含量,b为ast含量,nd为正常对照组,hfd为高脂模型组,si100为水飞蓟宾组,ce150为雪菊提取物低剂量组,ce300为雪菊提取物中剂量组,ce600为雪菊提取物高剂量组,a,b,c,d,e用于表明组间通过tukey's的anova统计学差异,p《0.05;各组间有相同字母即代表两组之间无显著性差异,各组间没有相同字母则代表两组之间差异显著。
[0017]
图5为本发明获得的雪菊提取物ce对nafld小鼠血清中tc和tg的影响,其中a为tc含量,b为tg含量,nd为正常对照组,hfd为高脂模型组,si100为水飞蓟宾组,ce150为雪菊提取物低剂量组,ce300为雪菊提取物中剂量组,ce600为雪菊提取物高剂量组;a,b,c,d用于表明组间通过tukey's的anova统计学差异,p《0.05;各组间有相同字母即代表两组之间无显著性差异,各组间没有相同字母则代表两组之间差异显著。
[0018]
图6为正常对照组、高脂模型组、水飞蓟宾组和雪菊提取物ce各剂量组小鼠的肝脏组织病理学变化(he染色,200倍光镜)。
[0019]
图7为本发明获得的雪菊提取物ce对糖尿病肾病大鼠肾脏指数的影响((x)
‑±
s,n=10)。,其中a,b,c,d用于表明组间通过tukey's的anova统计学差异,p《0.05;各组间有相同字母即代表两组之间无显著性差异,各组间没有相同字母则代表两组之间差异显著。
[0020]
图8为本发明获得的雪菊提取物ce对糖尿病肾病大鼠血糖值的影响(n=10)。
[0021]
图9为本发明获得的雪菊提取物ce对糖尿病肾病大鼠血清中血肌酐scr和血尿素氮bun的影响(n=10),其中control为正常对照组,dn为模型组,me200为二甲双胍组,ce150为雪菊提取物低剂量组,ce300为雪菊提取物中剂量组,ce600为雪菊提取物高剂量组;a,b,c,d用于表明组间通过tukey's的anova统计学差异,p《0.05;各组间有相同字母即代表两组之间无显著性差异,各组间没有相同字母则代表两组之间差异显著。
[0022]
图10为本发明获得的雪菊提取物ce对糖尿病肾病大鼠血清中总胆固醇tc和甘油三酯tg的影响(n=10),其中control为正常对照组,dn为模型组,me200为二甲双胍组,ce150为雪菊提取物低剂量组,ce300为雪菊提取物中剂量组,ce600为雪菊提取物高剂量组;a,b,c,d,e用于表明组间通过tukey's的anova统计学差异,p《0.05;各组间有相同字母即代表两组之间无显著性差异,各组间没有相同字母则代表两组之间差异显著。
具体实施方式
[0023]
实施例1
[0024]
a、提取:将干燥的雪菊头状花序粉碎后,用浓度为50%乙醇按重量体积比雪菊:乙醇=1:10热回流提取3次,温度60℃,每次0.5小时,合并提取液;
[0025]
b、浓缩:将步骤a得到提取液进行减压蒸馏至无醇味,除去乙醇,得到浓缩液;
[0026]
c、大孔树脂柱层析:将步骤b得到的浓缩液加水稀释,上样至预处理好的hpd-300大孔树脂柱(柱体积1.0l/bv),依次用4bv水,3bv 50%乙醇,2bv 70%乙醇和3bv 95%乙醇梯度洗脱,流速1.5-2.5bv/h,收集50%和70%乙醇洗脱部位,浓缩,干燥,获得雪菊提取物,其中雪菊提取物中七个主要活性成分黄诺玛苷、槲皮万寿菊素-7-o-β-吡喃葡萄糖苷、圣草
酚-7-o-β-吡喃葡萄糖苷、槲皮素-7-o-β-吡喃葡萄糖苷、马里苷、海生菊甙和奥卡宁的含量为70%。
[0027]
实施例2
[0028]
a、提取:将干燥的雪菊头状花序粉碎后,用浓度为75%乙醇按重量体积比雪菊:乙醇=1:20热回流提取2次,温度65℃,每次1小时,合并提取液;
[0029]
b、浓缩:将步骤a得到提取液进行减压蒸馏至无醇味,除去乙醇,得到浓缩液;
[0030]
c、大孔树脂柱层析:将步骤b得到的浓缩液加水稀释,上样至预处理好的hpd-300大孔树脂柱(柱体积1.0l/bv),依次用4bv水,3bv 50%乙醇,2bv 70%乙醇和3bv 95%乙醇梯度洗脱,流速1.5-2.5bv/h,收集50%和70%乙醇洗脱部位,浓缩,干燥,获得雪菊提取物,其中雪菊提取物中七个主要活性成分黄诺玛苷、槲皮万寿菊素-7-o-β-吡喃葡萄糖苷、圣草酚-7-o-β-吡喃葡萄糖苷、槲皮素-7-o-β-吡喃葡萄糖苷、马里苷、海生菊甙和奥卡宁的含量为72%。
[0031]
实施例3
[0032]
a、提取:将干燥的雪菊头状花序粉碎后,用浓度为80%乙醇按重量体积比雪菊:乙醇=1:30热回流提取3次,温度80℃,每次2小时,合并提取液;
[0033]
b、浓缩:将步骤a得到提取液进行减压蒸馏至无醇味,除去乙醇,得到浓缩液;
[0034]
c、大孔树脂柱层析:将步骤b得到的浓缩液加水稀释,上样至预处理好的hpd-100大孔树脂柱(柱体积1.0l/bv),依次用4bv水,3bv 40%乙醇,2bv 60%乙醇和3bv 100%乙醇洗脱,流速1.5-2.5bv/h,收集40%和60%乙醇洗脱部位,浓缩,干燥,获得雪菊提取物。该雪菊提取物中七个主要活性成分黄诺玛苷、槲皮万寿菊素-7-o-β-吡喃葡萄糖苷、圣草酚-7-o-β-吡喃葡萄糖苷、槲皮素-7-o-β-吡喃葡萄糖苷、马里苷、海生菊甙和奥卡宁的含量为74%。
[0035]
实施例4
[0036]
a、提取:将干燥的雪菊头状花序粉碎后,用浓度为50%乙醇按重量体积比雪菊:乙醇=1:20热回流提取3次,温度90℃,每次3小时,合并提取液;
[0037]
b、浓缩:将步骤a得到提取液进行减压蒸馏至无醇味,除去乙醇,得到浓缩液;
[0038]
c、大孔树脂柱层析:将步骤b得到的浓缩液加水稀释,上样至预处理好的d101大孔树脂柱(柱体积1.0l/bv),依次用3bv水,3bv 50%乙醇,2bv 75%乙醇和2bv 100%乙醇洗脱,流速1.5-2.5bv/h,收集50%和75%乙醇洗脱部位,浓缩,干燥,获得雪菊提取物。该雪菊提取物中七个主要活性成分黄诺玛苷、槲皮万寿菊素-7-o-β-吡喃葡萄糖苷、圣草酚-7-o-β-吡喃葡萄糖苷、槲皮素-7-o-β-吡喃葡萄糖苷、马里苷、海生菊甙和奥卡宁的含量为76%。
[0039]
实施例5
[0040]
取干燥的,粉碎后,用浓度为50%乙醇按重量体积比雪菊:乙醇=1:20在90℃热回流提取,每次0.5小时,重复提取3次,其余提取方法同实施例1。合并提取液,将提取液减压蒸馏除去其中的乙醇,得到浓缩液。将浓缩液加水稀释,上样ab-8大孔树脂柱(柱体积1.0l/bv),依次用3bv水,3bv 50%乙醇,2bv 80%乙醇和2bv 100%乙醇洗脱,流速1.5-2.5bv/h,收集50%和80%乙醇洗脱部位,浓缩,干燥,获得雪菊提取物,该雪菊提取物中七个主要活性成分黄诺玛苷、槲皮万寿菊素-7-o-β-吡喃葡萄糖苷、圣草酚-7-o-β-吡喃葡萄糖苷、槲皮素-7-o-β-吡喃葡萄糖苷、马里苷、海生菊甙和奥卡宁的含量为79%。
[0041]
a、提取:将干燥的雪菊头状花序粉碎后,用浓度为60%乙醇按重量体积比雪菊:乙醇=1:10热回流提取2次,温度90℃,每次0.5小时,合并提取液;
[0042]
b、浓缩:将步骤a得到提取液进行减压蒸馏至无醇味,除去乙醇,得到浓缩液;
[0043]
c、大孔树脂柱层析:将步骤b得到的浓缩液加水稀释,上样至预处理好的ab-8大孔树脂柱(柱体积1.0l/bv),依次用3bv水,3bv 50%乙醇,2bv 80%乙醇和2bv 100%乙醇洗脱,流速1.5-2.5bv/h,收集50%和80%乙醇洗脱部位,浓缩,干燥,获得雪菊提取物,该雪菊提取物中七个主要活性成分黄诺玛苷、槲皮万寿菊素-7-o-β-吡喃葡萄糖苷、圣草酚-7-o-β-吡喃葡萄糖苷、槲皮素-7-o-β-吡喃葡萄糖苷、马里苷、海生菊甙和奥卡宁的含量为79%。
[0044]
实施例6
[0045]
雪菊提取物ce对高脂诱导nafld小鼠肝损伤的保护作用
[0046]
选取4-5周龄c57bl6雄性小鼠随机分为空白对照组和模型组,空白对照组12只,给予普通饲料饲养;模型组60只,给予60%高脂饲料饲养,高脂饲养16周后,模型组小鼠随机分为模型组、阳性药组、雪菊提取物ce低、中、高剂量组,每组12只。第17周开始,正常饮食组和模型组灌胃给予药物空白溶剂,阳性药组小组灌胃给予水飞蓟宾100mg/kg,雪菊提取物ce低、中、高剂量组分别按照150mg/kg、300mg/kg和600mg/kg的剂量灌胃给予实施例1-5得到的雪菊提取物,每日一次灌胃,连续给药8周,每天测量进食量,每周测定体重,末次灌胃给药后,禁食不禁水12小时,称取空腹体重,然后摘眼球取血后立即处死。检测总胆固醇tc,甘油三酯tg,谷丙转氨酶alt和谷草转氨酶ast。
[0047]
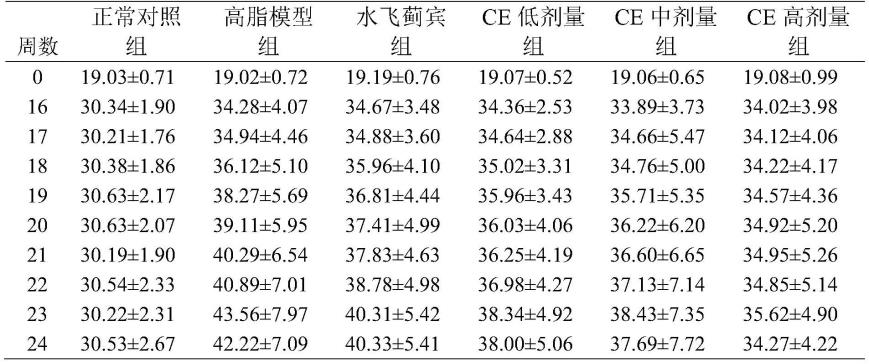
结果表明,与模型组比较,雪菊提取物各剂量组小鼠体重曲线增长缓慢,ce高剂量600mg/kg组体重增长最慢,结果见图2和表1,说明ce能够改善高脂饮食诱发的小鼠体重增加,并有剂量效应关系,给药8周后,与模型组比较,高剂量组动物体重显著下降,差异具有统计学意义(p《0.05);
[0048]
表1.雪菊提取物ce对nafld小鼠体重变化的影响
[0049][0050]
对小鼠日进食量统计结果显示,与正常饮食组比较,高脂饮食组的日进食量显著降低,各高脂饮食组之间的进食量并没有明显差异;
[0051]
脏器指数结果显示,与正常饮食组比较,高脂饮食诱导的所有动物肝脏、附睾脂肪和皮下脂肪的指数显著升高(p《0.05),与高脂饮食组比较,水飞蓟宾和雪菊提取物ce各剂量组给药干预8周后各组肝脏指数下降显著(p《0.05),雪菊提取物ce各剂量组给药干预后附睾脂肪和皮下脂肪指数下降显著(p《0.05),结果见图3和表2,同时,与高脂饮食模型组比
较,ce给药干预后,小鼠肝脏、附睾脂肪和皮下脂肪的重量和体积也不同程度的显著性降低;
[0052]
表2.雪菊提取物ce对nafld小鼠脏器指数变化的影响
[0053][0054]
注:字母a,b,c,d,e用于表明组间通过tukey's的anova统计学差异,p《0.05;各组间有相同字母即代表两组之间无显著性差异,各组间没有相同字母则代表两组之间差异显著。
[0055]
与正常饮食组比较,高脂饮食模型组小鼠血清中alt和ast水平显著升高(p《0.01);与高脂饮食模型组比较,阳性药组水飞蓟宾组的ast水平显著下降(p《0.01),雪菊提取物中高剂量组的alt水平显著降低(p《0.01);雪菊提取物ce各剂量组均能显著降低血清中ast的水平(p《0.01),结果见图4和表3。表明雪菊提取物ce可降低高脂饮食小鼠血清alt、ast水平,对肝脏具有直接保护作用;
[0056]
表3.雪菊提取物ce对nafld小鼠血清中alt和ast的影响
[0057][0058][0059]
注:字母a,b,c,d,e用于表明组间通过tukey's的anova统计学差异,p《0.05;各组间有相同字母即代表两组之间无显著性差异,各组间没有相同字母则代表两组之间差异显著。
[0060]
雪菊提取物ce各剂量组均能显著降低血清中tc、tg水平(p《0.01),结果见图5和表4,表明雪菊提取物ce能降低高脂饮食小鼠血清血脂,调节脂质代谢紊乱,且呈剂量相关性。
[0061]
表4.雪菊提取物ce对nafld小鼠血清中tc和tg的影响
[0062][0063]
注:字母a,b,c,d用于表明组间通过tukey's的anova统计学差异,p《0.05;各组间
有相同字母即代表两组之间无显著性差异,各组间没有相同字母则代表两组之间差异显著。
[0064]
肝组织形态学观察结果表明,正常饮食组小鼠肝小叶、肝细胞结构正常,肝索排列整齐;模型组肝细胞脂肪变性明显,小叶界限不清,肝索结构紊乱,肝组织可见弥漫性、混合性的空泡及气球样改变,中性粒细胞浸润明显;与模型组相比较,各给药干预组有不同程度减轻,损伤面积明显减少,胞内炎性细胞浸润减少,空泡及气球样变减少,细胞及小叶结构不同程度恢复。
[0065]
亚太地区非酒精性脂肪性肝病诊断与治疗共识推荐脂肪性肝炎nash(non-alcoholic steatohepatitis,nash)的病理诊断标准采用美国国立卫生研究院nash临床研究网络病理委员会2005年所定的指南,根据其指定的nafld活动度积分(nafld activity score,nas)进行评估,结果可见雪菊提取物ce各剂量组可不同程度抑制肝细胞脂肪变、气球样变和缓解炎症症状,结果见图6和表5;
[0066]
表5.各组小鼠肝细胞脂肪变性、肝小叶炎症及肝细胞气球样变评分(n=12)
[0067][0068]
注:字母a,b,c,d用于表明组间通过tukey's的anova统计学差异,p《0.05;各组间有相同字母即代表两组之间无显著性差异,各组间没有相同字母则代表两组之间差异显著。
[0069]
实施例7
[0070]
雪菊提取物ce对高能量饮食联合链脲佐菌素(stz)诱导的糖尿病肾病大鼠的保护作用
[0071]
选取无特殊病原菌级(specific pathogen free,spf)级sd雄性大鼠100只,6-8周龄,体重180-220g,随机分为空白对照组和模型组,空白对照组10只,给予普通饲料饲养;其余动物均为高糖高脂饮食组,给予高糖高脂饲料饲养,模型组所有动物喂养4周后,测量大鼠体重及随机血糖,高脂高糖饮食组动物腹腔注射1%链脲佐菌素stz,注射剂量为35mg/kg,7天后尾静脉注射取血检测随机血糖,血糖值大于16.7mmol/l视为造模成功,将成模后大鼠按血糖体重值均衡随机分组,采用随机数字表法将大鼠分为5组,分别为模型组,二甲双胍组(200mg/kg),雪菊提取物ce低(150mg/kg)、中(300mg/kg)、高(600mg/kg)三个剂量组;分组时,将空腹血糖值、肾功能指标(血肌酐scr和尿素氮bun)和体重离均值最大或最小的动物剔除,每组10只。分组后的各组大鼠从第9周开始,每天相同时间按照设置的剂量灌胃1次,空白对照组和模型组灌胃给予药物空白溶剂,连续灌胃给药4周。末次灌胃给药后,禁食不禁水12小时,称取空腹体重,给予2.5%戊巴比妥钠腹腔注射麻醉大鼠,将大鼠固定,解剖,腹主动脉采血及标本进行检测,检测血清中血糖(fbg),甘油三酯(tg),总胆固醇(tc),血肌酐(scr),尿素氮(bun);
[0072]
结果表明:模型组的肾脏指数升高,且与其他各组比较均有非常显著差异(p《0.05);ce高剂量组与正常组比较无显著性差异(p》0.05);肾脏指数的变化说明,模型组大鼠肾脏发生了肥大,复合dn早期病理改变;各组给药干预后能显著降低肾脏指数,且ce各剂量组具有剂效关系,二甲双胍组与雪菊提取物ce低剂量组(ce150)效果相当,ce高剂量组效果最好,结果见图7和表6:
[0073]
表6.雪菊提取物ce对糖尿病肾病大鼠肾脏指数的影响(n=10)
[0074][0075]
注:字母a,b,c,d用于表明组间通过tukey's的anova统计学差异,p《0.05;各组间有相同字母即代表两组之间无显著性差异,各组间没有相同字母则代表两组之间差异显著。
[0076]
糖尿病肾病大鼠模型组血糖上升至25mmol/l左右,雪菊提取物ce及二甲双胍组给药4周后,与模型组比较,各给药组空腹血糖均有显著下降,说明ce各剂量组及二甲双胍组均具有降低血糖的作用,结果见图8及表7。
[0077]
表7.雪菊提取物ce对糖尿病肾病大鼠血糖值变化的影响(n=10)
[0078][0079][0080]
经过4周给药干预后,血清中血肌酐scr和尿素氮bun水平发生显著逆转,说明大鼠肾小球滤过功能得到改善。以上结果表明,雪菊提取物ce能改善dn大鼠的肾功能损伤,结果见图9和表8;
[0081]
表8.雪菊提取物ce对糖尿病肾病大鼠血清中scr和bun的影响(n=10)
[0082][0083]
注:字母a,b,c,d用于表明组间通过tukey's的anova统计学差异,p《0.05;各组间有相同字母即代表两组之间无显著性差异,各组间没有相同字母则代表两组之间差异显
著。
[0084]
与正常组比较,dn组的tc、tg水平明显升高(p《0.05);与dn组比较,二甲双胍组与雪菊提取物ce各剂量组的tc、tg水平均显著降低(p《0.05),且ce各剂量组对tc、tg的降低水平具有显著的量效关系,见图10和表9。提示雪菊提取物ce可降低dn大鼠tc、tg水平,对血脂具有改善作用。
[0085]
表9.雪菊提取物ce对糖尿病肾病大鼠血清中tc和tg的影响(n=10)
[0086][0087]
注:字母a,b,c,d,e用于表明组间通过tukey's的anova统计学差异,p《0.05;各组间有相同字母即代表两组之间无显著性差异,各组间没有相同字母则代表两组之间差异显著。
[0088]
结果表明:通过本发明所述方法获得的雪菊提取物中活性成分含量高,具有改善非酒精性脂肪肝病和糖尿病肾病的功效,可应用于治疗非酒精性脂肪肝病和糖尿病肾病的药物用途。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1