体内DNA组装和分析
背景技术:
1、重组寡核苷酸技术的最新进展点燃了传统生物学和生物工程领域的研究。然而,寡核苷酸组装过程可以是昂贵且耗时的,需要多个纯化步骤和各种酶。此外,当前的分子生物学方法在可组合的dna元件的大小和组成方面存在限制。因此,需要用于将dna元件(例如,启动子、基因片段等)组装到一起的方法,以解决这些限制并绕过对大量且昂贵的酶(例如连接酶等)的需要。需要新的方法以在大规模并行的规模上高效、高通量和多功能地组装dna片段。
2、测序技术的进步允许dna长片段的鉴定。然而,由于复杂的纯化要求、样本回收低或测序工作流低效以及其他问题,鉴定和分离复杂混合物中的独特dna序列仍然具有挑战性。
3、本文特别提供本领域中这些和其他问题的解决方案。
技术实现思路
1、本文特别提供用于体内dna元件组装和寡核苷酸序列dna条形码化的方法和组合物。
2、本发明提供在受体细胞中将多个dna元件组装成组装的dna元件的方法,该方法包括:(a)使包含第一供体质粒的第一供体细胞与包含受体寡核苷酸的受体细胞在以下条件下接触:(i)通过接合,使第一供体质粒从第一供体细胞转移至受体细胞,以及(ii)通过同源重组,在受体细胞中使第一供体质粒和受体寡核苷酸重组,其中第一供体质粒依次包含:任选存在的第一核酸内切酶位点(c1)、第一同源重组区(hr1)、包含第一dna元件片段(oligo1)的第一寡核苷酸、包含两个同源重组区(hr2.1、hr2.2)的第二同源重组区(hr2)和任选存在的第三核酸内切酶位点(c3);受体寡核苷酸包含与hr1同源的第三同源重组区(hr3),以及与hr2.2同源的第四同源重组区(hr4);从而在hr1与hr3以及hr2.2与hr4同源重组之后,提供包含第一dna元件片段的第一重组受体寡核苷酸;(b)使包含第二供体质粒的第二供体细胞与包含第一重组受体寡核苷酸的受体细胞在以下条件下接触:(i)通过接合,将第二供体质粒从第二供体细胞转移至第一受体细胞,以及(ii)通过同源重组,在受体细胞中使所述第二供体质粒和第一重组受体寡核苷酸重组,以形成第二重组受体寡核苷酸,其中第二供体质粒依次包含:任选存在的第五核酸内切酶位点(c5)、与hr2.1同源的第五同源重组区(hr5)、编码第二dna元件片段(oligo2)的第二寡核苷酸、包含两个同源重组区(hr6.1、hr6.2)的第六同源重组区(hr6)和任选存在的第六核酸内切酶位点(c6);从而在hr5与hr2.1以及hr6.2与hr4同源重组之后,提供包含第一和第二dna元件片段(oligo1、oligo2)的第二重组受体寡核苷酸,第一和第二dna元件片段形成dna组装物。在实施方案中,hr2.1和hr2.2位于包含一个(c2)或两个核酸内切酶位点(c2.1、c2.2)的非同源区两侧;任选地,其中hr3和hr4位于包含一个(c4)或两个核酸内切酶位点(c4.1、c4.2)的非同源区两侧。在实施方案中,hr6.1和hr6.2位于包含一个(c7)或两个核酸内切酶位点(c7.1、c7.2)的非同源区两侧。在实施方案中,受体寡核苷酸位于受体细胞质粒或受体细胞基因组中。在实施方案中,dna组装物包含基因、启动子、增强子、终止子、内含子、基因间区域、条形码、向导rna (grna)或其组合的至少一部分。
3、在实施方案中,用第三或后续供体细胞重复步骤(b)一次或多次重复,所述第三或后续供体细胞包含第三或后续供体质粒,所述第三或后续供体质粒包含相容的hr区域和编码第三或后续dna元件片段(oligo3、oligo4…oligon)的第三或后续寡核苷酸,从而形成包含第一、第二和第三或后续dna元件片段的第三或后续重组受体寡核苷酸,第一、第二和第三或后续dna元件片段一起形成dna组装物。
4、在实施方案中,步骤(a)包括多个第一供体细胞,每个细胞包含不同的第一供体质粒;以及步骤(b)包括多个第二、第三或后续供体细胞,每个细胞包含不同的第二、第三或后续供体质粒;任选地,其中每个第一供体细胞位于第一有序阵列以及每个第二、第三或后续供体细胞位于第二、第三或后续有序阵列;任选地,其中所述方法产生包含多个不同的组装的dna元件的组合文库。
5、在实施方案中,在第一供体质粒上和/或在受体细胞中存在编码靶向第一、第三和/或第四核酸内切酶位点的第一核酸内切酶的寡核苷酸。在实施方案中,在第二供体质粒上和/或在受体细胞中存在编码靶向第二、第五和/或第六核酸内切酶位点的第二核酸内切酶的寡核苷酸。在实施方案中,所述第一和/或第二核酸内切酶的表达是可诱导的,并且所述方法进一步包括诱导第一和/或第二核酸内切酶的表达。在实施方案中,所述第一和/或第二核酸内切酶选自rna-引导的核酸内切酶、归巢核酸内切酶、转录激活因子样效应物核酸酶和锌指核酸酶。
6、在实施方案中,所述第一、第二或后续供体质粒包含选择标记,所述选择标记就所述第一寡核苷酸、第二寡核苷酸或后续寡核苷酸整合到所述受体寡核苷酸中进行选择;任选地,其中所述选择标记位于hr2.1与hr2.2之间和/或hr6.1与hr6.2之间,和/或后续hr区域之间的非同源区内。在实施方案中,所述受体寡核苷酸包含反选择标记,所述反选择标记针对不包含第一、第二、第三或后续寡核苷酸的受体细胞进行选择;任选地,其中所述反选择标记位于hr2.1与hr2.2之间和/或hr6.1与hr6.2之间,和/或后续hr区域之间的非同源区内。
7、在实施方案中,所述供体质粒包含转移起点.
8、在实施方案中,所述供体质粒包含条件复制起点。在实施方案中,所述条件复制起点依赖于寡核苷酸的存在或细胞生长条件。在实施方案中,所述供体质粒或受体寡核苷酸包含可诱导的高拷贝复制起点。
9、在实施方案中,所述供体质粒或受体寡核苷酸包含可以复制长度大于30千碱基的质粒的复制子。
10、在实施方案中,所述供体质粒或受体寡核苷酸是酵母人工染色体(yac)、哺乳动物人工染色体(mac)、人类人工染色体(hac)或植物人工染色体。
11、在实施方案中,所述供体质粒或受体寡核苷酸是病毒载体。
12、在实施方案中,所述供体质粒包含使质粒能接合的寡核苷酸。
13、在实施方案中,所述供体质粒或受体细胞包含编码一个或多个同源dna修复基因的寡核苷酸;任选地,其中所述一个或多个同源dna修复基因的表达是可诱导的。
14、在实施方案中,所述供体质粒或受体细胞包含编码一个或多个重组介导的遗传工程基因的寡核苷酸。
15、在实施方案中,所述供体细胞和受体细胞独立地为细菌细胞;任选地,其中所述细菌细胞是大肠杆菌(e.coli)、纳氏弧菌(vibrio natriegens)或霍乱弧菌(v.cholerae)。
16、在实施方案中,所述组装的dna元件的长度从100个核苷酸至500,000个核苷酸。
17、在实施方案中,所述第一、第二或后续同源重组(hr)区域及它们在受体寡核苷酸上相应的hr区域各自包含从约20个碱基对至约500个碱基对;任选地,约50个至100个碱基对。
18、在实施方案中,任一前述方法可以进一步包括一个或多个以下步骤:裂解受体细胞;扩增组装的dna元件;分离组装的dna元件;分离受体寡核苷酸;测序组装的dna元件以及测序受体寡核苷酸。
19、在实施方案中,同时进行使第一和第二或后续供体细胞与第一受体细胞接触的步骤;任选地,其中仅有最终供体质粒包含选择标记,或者每个供体质粒包含受体寡核苷酸上不存在的选择标记。
20、在任一前述方法的实施方案中,包含形成部分组装的dna元件的最后dna元件的供体质粒包含条形码同源重组(bhr)区域以产生受体细胞,每个受体细胞含有重组受体寡核苷酸,所述重组受体寡核苷酸包含组装的dna元件、bhr和进一步的hr;并且所述方法进一步包括:(i)构建或获取条形码供体细胞阵列,每个细胞含有条形码供体质粒,所述条形码供体质粒包含与bhr同源的hr、独特的条形码寡核苷酸和与重组受体寡核苷酸的进一步的hr同源的第二hr;(ii)使条形码供体细胞阵列在以下条件下与受体细胞阵列接触:(a)通过接合,使条形码供体质粒从条形码供体细胞转移至受体细胞,以及(b)通过同源重组,在受体细胞中使条形码供体质粒和受体寡核苷酸重组,从而产生包含条形码化的组装物的受体细胞阵列。
21、在任一前述方法的实施方案中,每个供体质粒包含进一步的独特的核酸内切酶位点cx、cy对,其位于条形码同源重组(bhr)区域两侧,并且所述方法进一步包括使受体细胞阵列与条形码供体细胞阵列接触,以产生包含条形码化的组装物的受体细胞阵列,每个受体细胞包含dna组装物,每个条形码供体细胞含有条形码供体质粒,所述条形码供体质粒包含一对hr区域,hr区域与位于独特的条形码寡核苷酸两侧的bhr同源。
22、在任一前述方法的实施方案中,所述方法进一步包括使包含重置(reset)供体质粒的重置供体细胞与包含重组受体寡核苷酸的受体细胞接触,其中所述重置供体质粒依次包含,与dna组装物的末端序列同源的同源重组区(hrt)、重置核酸内切酶位点、选择标记、重置核酸内切酶位点、同源重组区(hrx)以及转移起点;其中重组受体寡核苷酸依次包含,重置核酸内切酶位点、dna组装物、与hrx同源的同源重组区(hrxa)以及重置核酸内切酶位点;从而在hrt与dna组装物的末端序列之间以及hrx和hrxa之间的同源重组之后,提供包含转移起点和dna组装物的重置质粒。在实施方案中,重置质粒在供体细胞中。在实施方案中,重置质粒含有限制复制起点,所述限制复制起点在供体细胞和受体细胞中均起作用。在实施方案中,通过包括以下的方法构建重置供体质粒:引入寡核苷酸插入物,所述寡核苷酸插入物包含位于两个核酸内切酶位点(c1、c2)和反选择标记(cm)两侧的同源重组区hrt、hrx,hrt-c1-cm-c2-hrx;或者引入这种寡核苷酸插入物的文库;允许核酸内切酶切割核酸内切酶位点,并使用同源重组在切割位点引入反选择标记。
23、在任一前述方法的实施方案中,所述受体寡核苷酸包含能够将dna组装物转移至其他细胞类型的可移动遗传元件,其他细胞类型包括酵母细胞、植物细胞、哺乳动物细胞或其他细菌细胞。
24、在任一前述方法的实施方案中,所述方法包括利用两个或更多个具有相容同源重组区的受体寡核苷酸来构建dna文库。
25、在任一前述方法的实施方案中,供体质粒寡核苷酸包含第一接头寡核苷酸和第二接头寡核苷酸,第一接头寡核苷酸与第一dna组装物的末端序列同源,第二接头寡核苷酸与第二寡核苷酸同源。在实施方案中,接头寡核苷酸进一步包含额外dna元件片段,额外dna元件片段与第一dna组装物或第二dna寡核苷酸不同源。在实施方案中,方法用于:组装诱变文库;用于组合来自不同物种的遗传区域例如基因、启动子、终止子和调节区域;用于构建和/或组合遗传调控途径;用于构建组合grna文库;或者用于组装含有用于筛选实验的质粒的细菌阵列。
26、在任一前述方法的实施方案中,在步骤(a)和(b)之前,将第一和第二寡核苷酸插入至第一和第二供体质粒中,所述第一和第二寡核苷酸包含第一和第二dna元件片段。
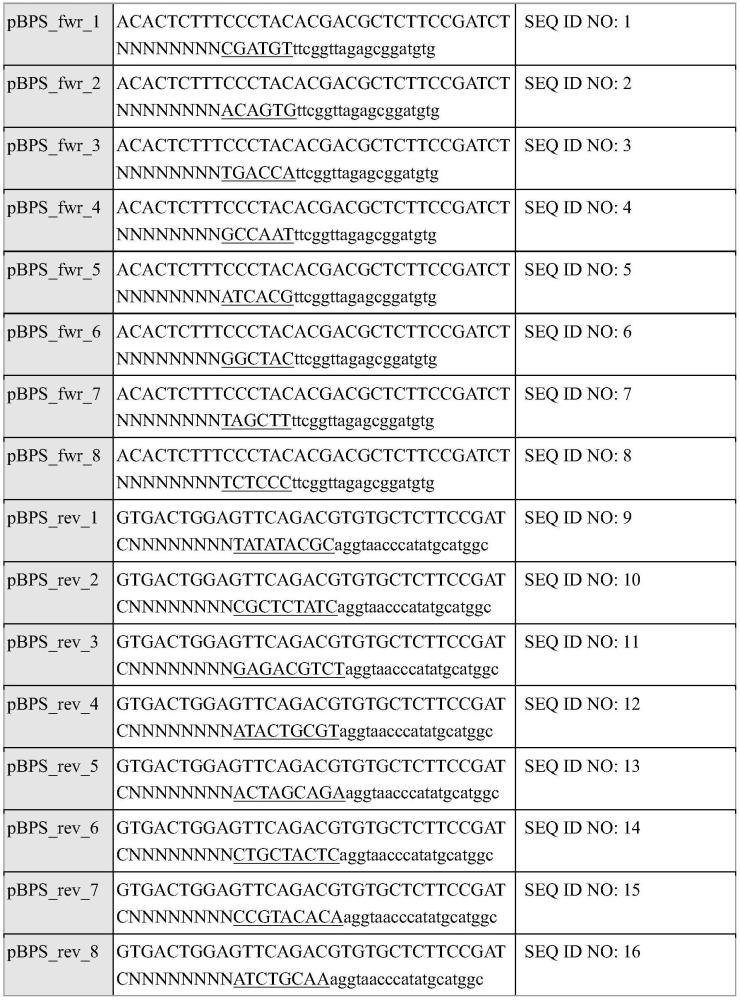
27、本发明还提供将条形码与寡核苷酸缀合的方法,该方法包括:(a)将寡核苷酸混合物的每个寡核苷酸插入至供体质粒中,每个供体质粒依次包含,任选存在的第一核酸内切酶位点(c1)、第一同源重组区(hr1)、第二同源重组区(hr2)和任选存在的第二核酸内切酶位点(c2);其中每个寡核苷酸插入到hr1和hr2之间,从而提供多个包含供体寡核苷酸的供体质粒,每个供体质粒包含来自寡核苷酸混合物的单个供体寡核苷酸:c1-hr1-oligo-hr2-c2;(b)用所述多个供体质粒转化多个细胞,使得每个细胞包含供体质粒,从而形成多个供体细胞;(c)铺板并培养所述多个供体细胞,每个供体细胞位于第一有序阵列上的独特位置,从而提供供体细胞的第一有序阵列;(d)在第二有序阵列中提供多个受体细胞,其中每个受体细胞包含受体寡核苷酸,所述受体寡核苷酸依次包含独特的条形码序列、与hr1同源的第三同源重组区(hr3)、任选存在的第三核酸内切酶位点(c3)和与hr2同源的第四同源重组区(hr4),其中所述独特的条形码序列表明在第二有序阵列中受体细胞的位置;(e)使供体细胞的第一有序阵列与受体细胞的第二有序阵列在以下条件下接触:(i)通过接合,使供体质粒从供体细胞转移至在阵列上相应位置的受体细胞,(ii)任选地,切割所述第一、第二和第三核酸内切酶位点,以及(ii)通过同源重组,使所述寡核苷酸从供体质粒转移至受体细胞寡核苷酸,从而形成融合寡核苷酸的第三阵列,每个融合寡核苷酸包含独特的条形码序列和来自寡核苷酸混合物的供体寡核苷酸;以及(f)任选地,测序融合寡核苷酸,并且从而通过其条形码序列来鉴定阵列中的每个寡核苷酸。在实施方案中,受体寡核苷酸位于受体细胞质粒或受体细胞基因组中。在实施方案中,供体质粒包含在hr1和hr2之间的选择标记,选择标记就所述寡核苷酸整合到所述受体细胞寡核苷酸中进行选择;任选地,其中供体质粒包含反选择标记。在实施方案中,受体细胞寡核苷酸包含第四核酸内切酶位点(c4)。
28、本发明还提供从多个寡核苷酸鉴定寡核苷酸的方法,方法包括(a)在第一有序阵列中提供多个供体细胞,其中每个供体细胞包含供体质粒,每个供体质粒依次包含,任选存在的第一核酸内切酶位点(c1)、第一同源重组区(hr1)、独特的条形码序列、第二同源重组区(hr2)以及任选存在的第二核酸内切酶位点(c2),其中独特的条形码序列表明在第一有序阵列中宿主细胞的位置;(b)提供多个受体细胞,其中每个受体细胞包含受体质粒,受体质粒依次包含来自多个寡核苷酸的寡核苷酸、与hr1同源的第三同源重组区(hr3)、任选存在的第三核酸内切酶位点(c3),以及与hr2同源的第四同源重组区(hr4);(c)铺板并培养所述多个受体细胞,每个受体细胞在第二有序阵列上的独特位置,从而提供受体细胞的第二有序阵列;(d)在以下条件下使第一有序阵列与第二有序阵列接触:(i)通过细菌接合,使供体质粒从供体细胞转移至在阵列上相应位置的受体细胞,(ii)切割第一、第二和第三核酸内切酶位点,以及(ii)通过同源重组,使条形码序列从供体质粒转移至受体细胞寡核苷酸,从而形成融合寡核苷酸的第三阵列,每个融合寡核苷酸包含独特的条形码序列和来自寡核苷酸混合物的寡核苷酸;以及(e)测序融合寡核苷酸,从而通过其条形码序列来鉴定阵列中的每个寡核苷酸。在实施方案中,受体寡核苷酸位于受体细胞质粒或受体细胞基因组中。在实施方案中,供体质粒包含在hr1和hr2之间的选择标记,选择标记就条形码序列整合到受体细胞寡核苷酸中进行选择;任选地,其中供体质粒包含反选择标记。在实施方案中,受体细胞寡核苷酸包含第四核酸内切酶位点(c4)。在实施方案中,第一核酸内切酶位点、第二核酸内切酶位点和第三核酸内切酶位点相同或不同。在实施方案中,供体质粒包含转移起点和/或条件复制起点;任选地,其中转移起点来自可移动元件;进一步任选地,其中条件复制起点依赖于寡核苷酸的存在或细胞生长的条件。在实施方案中,供体质粒或受体质粒包含复制子,复制子可以复制长度至少30千碱基的质粒,任选地,其中复制子来自p1-衍生的人工染色体或细菌人工染色体。在实施方案中,供体质粒或受体细胞寡核苷酸包含可诱导的高拷贝复制起点。在实施方案中,供体质粒或受体细胞寡核苷酸包含酵母人工染色体(yac)、哺乳动物人工染色体(mac)、人类人工染色体(hac)或植物人工染色体。在实施方案中,供体质粒或受体细胞寡核苷酸包含病毒载体。在实施方案中,一种或多种核酸内切酶切割核酸内切酶位点,所述一种或多种核酸内切酶由受体细胞中一种或多种寡核苷酸编码,和/或在供体质粒中编码;任选地,其中所述一种或多种核酸内切酶是归巢核酸内切酶,或者rna-引导的dna核酸内切酶;进一步任选地,其中核酸内切酶是ho。在实施方案中,供体细胞或受体细胞包含(i)使质粒能接合的寡核苷酸;(ii)编码一种或多种同源dna修复基因的寡核苷酸;或(iii)编码一种或多种重组介导的遗传工程基因的寡核苷酸。在实施方案中,供体细胞、受体细胞或重组受体细胞被转移至第三有序阵列、第四有序阵列或后续有序阵列上的位置。在实施方案中,供体细胞和受体细胞独立地为细菌细胞;任选地,其中细菌细胞是大肠杆菌、纳氏弧菌或霍乱弧菌。在实施方案中,条形码序列的长度为从约四个核苷酸至约100个核苷酸,任选地,其中条形码序列的长度为约30个核苷酸。在实施方案中,寡核苷酸混合物是dna合成或组装技术的产物,所述dna合成或组装技术选自化学偶联、使用聚合酶核苷酸结合物(conjugate)的不依赖模板的酶促合成、聚合酶链组装(聚合酶循环组装)、gibson组装(chew back、退火和修复)、连接酶链反应/连接酶循环反应、phi29聚合酶、滚环扩增、环介导等温扩增(lamp)、链置换扩增(sda)、解旋酶依赖扩增(had)、重组酶聚合酶扩增(rpa)、基于核酸序列扩增(nasba)、golden gate克隆、moclo克隆、biobricks或组装的biobricks、热力学平衡内外合成、dna克隆、不依赖连接的克隆、选择性连接克隆、重组工程、酵母组装、pcr、由分子倒置探针或lasso探针捕获、dropsynth以及酶促dna合成。在实施方案中,寡核苷酸混合物是汇集的诱变技术的产物,诱变技术选自聚合酶链反应技术,包括易错pcr、用简并寡核苷酸的pcr和常规pcr,化学或光诱变,用编辑寡核苷酸文库进行的体外合成,体内编辑,例如mage、magestic、crispr、先导编辑、反转录子编辑和用crispr、talen和锌指核酸酶的碱基修饰。在实施方案中,寡核苷酸混合物包含基因组dna、cdna、细胞器dna或天然质粒dna的至少一个片段。在实施方案中,寡核苷酸混合物包含捕获的或扩增的dna,所述dna源于gdna、cdna或细胞器dna,例如来自平衡的cdna文库、pcr产物如多重pcr产物、分子倒置探针,包括lasso探针、退火或消减杂交捕获物、共转化和同源重组、滚环扩增或lamp。在实施方案中,寡核苷酸混合物包含从质粒或质粒文库捕获或扩增的dna,例如开放阅读框(orf)文库、启动子文库、终止子文库、内含子文库、bac文库、pac文库、慢病毒文库、grna文库、pcr产物、限制性消化产物或gateway穿梭产物。在实施方案中,通过包括共转化和重组工程、转化和重组工程或接合和重组工程的方法将寡核苷酸混合物的寡核苷酸整合至供体质粒中。在实施方案中,共转化和重组工程的方法包括:构建线性或环状供体质粒,供体质粒包含选择标记和两个同源重组区,每个同源重组区与混合物中寡核苷酸末端序列同源;将供体质粒和寡核苷酸共转化至细胞中;诱导同源重组;以及就选择标记进行选择;任选地,其中方法用供体质粒和/或寡核苷酸的文库或池(pool)进行。在实施方案中,转化和重组工程的方法包括:构建线性或环状供体质粒,供体质粒包含选择标记和两个同源重组区,每个同源重组区与混合物中寡核苷酸末端序列同源,其中寡核苷酸存在于宿主细胞内的质粒上;用供体质粒转化宿主细胞;诱导同源重组;以及就选择标记进行选择。在实施方案中,接合和重组工程的方法包括:构建线性或环状供体质粒,供体质粒包含两侧为两个任选存在的核酸内切酶位点和两个同源重组(hr)区域的反选择标记(-1);其中供体质粒存在于含有残缺的f-质粒的供体细胞,所述残缺的f-质粒可以诱导接合但不可以接合,并且混合物的寡核苷酸存在于受体细胞内的质粒上,每个寡核苷酸两侧为与供体质粒的hr区域同源的hr区域并且与至少一个选择标记(+1)相邻,以就每个寡核苷酸重组到供体质粒中进行选择;提供同源重组酶以及任选存在的一种或多种核酸内切酶,其在受体细胞中或由供体质粒编码;在以下条件下使供体细胞与受体细胞接触:(i)通过细菌接合,使供体质粒从供体细胞转移至受体细胞,以及(ii)通过同源重组,使供体质粒和受体质粒重组;以及选择包含选择标记而不包含反选择标记的细胞。在实施方案中,方法用供体质粒和/或受体质粒文库进行。在实施方案中,寡核苷酸包含文库,例如orf文库、启动子文库、终止子文库、内含子文库、bac文库、pac文库、慢病毒文库、grna文库、gdna文库、cdna文库、蛋白结构域文库、启动子文库、终止子文库、调节元件文库、结构元件文库或来源于dna诱变的dna变体文库。在实施方案中,寡核苷酸混合物包含细胞阵列,细胞阵列包含质粒文库,例如grna文库、gdna文库、cdna文库、开放阅读框(orf)文库、蛋白结构域文库、启动子文库、终止子文库、调节元件文库、结构元件文库或来源于dna诱变的dna变体文库。在实施方案中,寡核苷酸混合物包含细胞阵列,所述细胞阵列包含用于权利要求1-35中任一项的方法的dna元件片段。
29、
30、
31、
32、
33、
34、
35、
36、
37、
38、
39、
40、
41、
42、
43、
- 还没有人留言评论。精彩留言会获得点赞!