作为mGlu7受体的负别构调节剂的稠合杂环衍生物的制作方法
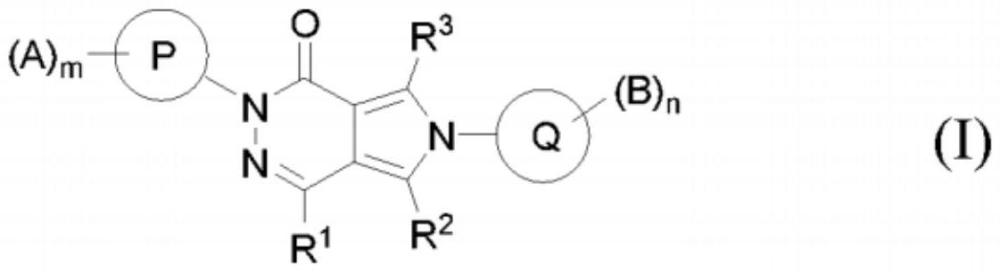
本发明涉及新的式(i)化合物,其中p、q、a、b、m、n、r1、r2和r3根据式(i)中所限定;所述化合物是代谢型谷氨酸受体亚型7(metabotropic glutamate receptor subtype 7,mglu7)的负别构调节剂,并且可用于治疗或预防与谷氨酸功能障碍相关的神经系统、耳和精神障碍以及其中涉及代谢型受体亚型mglu7的疾病。本发明还涉及包含这样的化合物的药物组合物、制备这样的化合物和这样的组合物的方法、以及这样的化合物用于预防或治疗神经系统、耳和精神障碍以及其中涉及mglu7的疾病的用途。
背景技术:
1、谷氨酸是哺乳动物中枢神经系统(central nervous system,cns)中的主要氨基酸递质(transmitter)。谷氨酸与许多生理功能,学习和记忆、感官知觉、突触可塑性的发育、运动控制、呼吸、以及心血管功能的调节相关。此外,谷氨酸处于数种不同的神经系统和精神疾病的中心,这些疾病之中存在谷氨酸能神经传递的不平衡。
2、谷氨酸通过激活以下来介导突触的神经传递:离子通道型谷氨酸受体通道(ionotropic glutamate receptor,iglur),nmda,ampa和红藻氨酸受体,其负责快速的兴奋性传导(nakanishi et al.(1998)brain res.rev.,26:230-235)。
3、另外,谷氨酸激活具有调节作用的代谢型谷氨酸受体(metabotropic glutamatereceptor,mglur),其有助于突触效力的微调(niswender&conn(2010)ann.rev.pharmacol.toxicol.50:295-322)。与iglur相反,mglur不是介导而是“调节”在由轴突末梢、树突棘和星形胶质细胞连接形成的三方突触的不同水平上起作用的突触传递。mglur是含有七个跨膜结构域的g蛋白偶联受体(g protein-coupled receptor,gpcr),与钙敏感受体、gabab受体和信息素受体一起属于家族3gpcr。谷氨酸通过与受体的大的胞外氨基末端结构域上的位点(本文称作正构结合位点(orthosteric binding site))结合来激活mglur。该激活诱导了受体其余部分的构象变化,这导致g蛋白的激活以及随后大量胞内信号传导途径的激活。mglur家族由八个成员构成。根据序列同源性、药理学特征以及所激活胞内信号传导级联的性质,将其分类成三个组(包含mglu1和mglu5的组i;包含mglu2和mglu3的组ii;包含mglu4、mglu6、mglu7和mglu8的组iii)(schoepp et al.(1999)neuropharmacology,38:1431-1476)。
4、在mglu受体中,mglu7亚型分布最广泛,并且在突触前存在于广泛范围的突触中,其被认为对于正常cns功能和一系列精神和神经系统障碍二者是至关重要的(ohishi etal.(1995)j.comp.neurol.360(4):555-570;kinzie et al.(1995)neuroscience,69(1):167-176;corti et al.(1998)eur.j.neurosci,10(12):3629-3641)。mglu7通过激活gαi-蛋白与腺苷酸环化酶负偶联,并且其作为突触前自受体(autoreceptor)的激活导致谷氨酸和gaba在突触中的释放受到抑制(dalezios et al.(2002)cereb.cortex,12(9):961-974;cartmell and schoepp(2000)j.neurochem.,75:889-907;somogyi et al.(2003)eur.j.neurosci.17(12):2503-2520),因此在谷氨酸能突触处形成突触响应,以及是抑制性gaba能传递的关键调节剂,其中最终目标是微调脑的总体兴奋性。
5、先前,大多数可用的靶向mglur的药理学工具是正构配体,其与该家族的数种成员交叉反应,因为它们是谷氨酸的结构类似物(schoepp et al.(1999)neuropharmacology,38:1431-1476)。然而,采用新的筛选方法,已经可鉴定出对单独mglur具有选择性的分子,其通过变构机制发挥作用,通过与不同于高度保守的正构结合位点的位点结合来调节受体。已经发现了针对数种mglur的这些类型的分子(综述于hellyer et al.(2017)curr.opin.pharmacol.32:49-55;stansley&conn(2019)trends pharmacol.sci.40(4):240-52;dogra&conn,(2022)mol.101(5):275-285)。近年来已鉴定靶向mglu7受体的数种小分子(综述于vasquez-villa&trabanco(2019)med.chem.comm.10:193-9)。amn082被描为是具有强效、选择性和全身活性的mglu7变构激动剂(mitsukawa et al.(2005)proc.natl.acad.sci.usa,102:18712-18717)。最近还描述了7-羟基-3-(4-碘苯氧基)-4h-色烯-4-酮(xap044),即mglu7的变构拮抗剂(gee et al.(2014)j.biol.chem.18;289(16):10975-10987),其通过定位于受体的胞外捕蝇夹结构域(venus flytrap domain)的结合袋(binding pocket)发挥作用。最后,描述了数种类别的化合物,例如异唑吡啶酮衍生物、苯基苯甲酰胺衍生物、二氢苯并唑酮衍生物、四氢酞嗪酮衍生物,并且在药理学上表征为选择性mglu7负别构调节剂(suzuki et al.(2007)j.pharmacol.exp.ther.,323:147-156;kalinichev et al.(2013)j.pharmacol.exp.ther.344(3):624-636;reed et al.(2017)acs med.chem.lett.(12):1326-1330和duvey et al(2019)wo2019063569)。
6、特别是,基于对实验动物的实验研究(被认为与临床综合征相关),mglu7的调节剂,并且优选拮抗剂、反向激动剂和负别构调节剂(negative allosteric modulator,nam),被报道具有治疗神经系统、精神、情绪障碍以及疼痛和耳障碍的潜能。
7、在经遗传修饰的小鼠和野生型动物中mglu7的药理学操纵,以及mglu7在脑区域中的组合表达揭示了mglu7在许多cns障碍,包括抑郁症、精神分裂症、焦虑症、强迫性障碍和相关症状中的重要作用(由pallazo et al.(2016)curr.neuropharmacol.14(5):504-513所综述),并且特别是在急性和慢性的应激相关病症中的重要作用(由peterlik et al.(2016)curr neuropharmacol.14(5):514-539所综述)。
8、已经表明mglu7位于边缘系统核心,例如杏仁核(amygdala)、海马和蓝斑核(locuscoerulus),已知该区域对抗抑郁作用和焦虑解除的表现至关重要(kinoshita et al.(1998)j.comp.neurol.,393(3):332-352;makoff et al.(1996)brain res.mol.brainres.,40(1):165-170;kinzie et al.(1995)neuroscience,69(1):167-176)。此外,数种行为模型的研究(明暗箱测试(light-dark box test)、高架十字迷宫(elevated plusmaze)、爬梯测试(staircase test)、强迫游泳测试(forced swim test)和尾悬吊测试(tail suspension test))已表明mglu7敲除的动物表现出抗焦虑和抗抑郁表型,但也在杏仁核依赖的行为中存在一些缺陷(恐惧反应和条件性味觉厌恶)(cryan et al.(2003)eur.j.neuroscience,17:2409-2417)。因此,旨在调节mglu7活性的药剂(pharmacologicalagent)可代表用于治疗神经系统和精神障碍(例如焦虑和抑郁)的新的治疗方法。
9、使用变构激动剂amn082激活mglu7提高了应激激素皮质酮和acth的血浆水平(mitsukawa et al.(2005)pnas,102(51):18712-18717)。该作用在mglu7基因敲除小鼠中完全缺失。那些结果与先前的遗传研究一致,表明mglu7是体内应激响应的重要调节剂(mitsukawa et al.(2006)neuropsychopharm.,31(6):1112-1122)。在该文章中,mitsukawa et al.表明mglu7的消融导致hpa轴的调节异常并使海马bdnf蛋白水平提高,表明该受体可与应激相关精神病学障碍,例如焦虑、抑郁、创伤后应激综合征、由先天恐惧诱导的行为(例如条件性恐惧或条件性味觉厌恶的获得和消退)有关。这些数据还证实了先前的观察结果,其中mglu7-缺陷小鼠表现出足部电击期间由恐惧介导的僵立响应显著下降,并且味觉刺激与引起不安的licl注射(条件性味觉厌恶(conditioned taste aversion,cta))之间的关联能力削弱(masugi et al.(1999)j.neurosc.,19(3):955-963)。与野生型动物相比,这些小鼠在条件响应的获得和消失学习中也表现出缺陷(goddyn et al.(2008)neurobiol.learn.mem.,90(1):103-111)。
10、用变构激动剂amn082观察到的矛盾效应可由快速和持久的mglu7受体内化来解释,这与功能拮抗作用相一致,并且其在体内的缺乏的选择性表明了潜在的脱靶参与(sukoff rizzo et al.(2011)j.pharmacol.exp.ther.,338(1):345-352;pelkey et al.(2007)neuropharmacology52(1):108-117)。
11、数种负别构调节剂的最近发现有助于更好地理解mglu7在神经功能中的功能作用。体内施用6-(4-甲氧基苯基)-5-甲基-3-吡啶-4-基异唑并[4,5-c]吡啶-4(5h)-酮(mmpip)已经显示出抗焦虑、抗抑郁类特性,以及改善的认知表现(在啮齿动物模型中)(palazzo et al.(2015)pain,156(6):1060-1073)。7-羟基-3-(4-碘苯氧基)-4h-色烯-4-酮(xap044)显示出产生抗应激、抗抑郁和抗焦虑样作用,以及降低了在恐惧调节化范式中的僵立(gee et al.(2014)j.biol.chem.289(16):10975-10987)。此外,(s)-6-(2,4-二甲基苯基)-2-乙基-6,7-二氢苯并[d]唑-4(5h)-酮(adx71743)在高架十字迷宫和弹珠埋藏测试(marble burying test)中显示出抗焦虑样作用,以及在不改变基线自主活动的情况下降低了苯丙胺诱导的活动过度(kalinichev et al.(2013)j.pharmacol.exp.ther.344(3):624-636)。总之,这些数据表明用调节剂抑制mglu7可用于治疗与焦虑、抑郁和ptsd相关的情绪障碍。
12、另外,mglu7受体还涉及在疼痛期间受影响的途径。考虑到其在周围神经系统和中枢神经系统二者中均有高且广的表达,发现mglu7在调节疼痛行为中发挥作用。最近还使用将amn082直接注射到杏仁核的中央核(central nucleus of the amygdala,cea)或导水管周围灰质(periaqueductal gray,pag)中表明了mglu7在疼痛中的作用。在正常状况下,杏仁核mglu7的激活促进了疼痛响应,如脊髓撤回反射阈值(spinal withdrawal reflexthreshold)的降低和由短暂膝压迫诱导的听觉和超声发声的提高所示(palazzo et al.(2008)neuropharmacol.,55(4):537-545)。以类似的方式,在大鼠中,pag mglu7的激活降低了使用甩尾潜伏期(tail flick latency)测量的热感受阈值(marabese et al.(2007)j.neurophysiol.,98:43-53)。在啮齿动物的疼痛模型中,amn082抑制痛觉过敏(dolan etal.(2009)behav.pharmacol.20(7):596-604);osikowicz et al.(2008)pain 139(1):117-126)。另外,mglu7负别构调节剂adx71743在内脏过敏的应激敏感模型中显示出减轻内脏疼痛(moloney et al.(2015)neurobiol.stress 2:28-33)。总之这些数据表明,mglu7受体的激活使疼痛感觉恶化,而mglu7抑制使其减轻,因此表明该受体的负别构调节剂可用于治疗疼痛和疼痛相关病症。
13、全基因组研究还表明了mglu7受体与年龄相关性听力损伤(age-related hearingimpairment,arhi)(还称作老年性耳聋)相关。这导致鉴定出位于grm7(编码mglu7受体的基因)中的高显著性的和重复的单核苷酸多态性(single nucleotide polymorphism,snp)(van laer et al.(2010)eur.j.hum.genet.,18(6):685-693;friedman et al.(2009)hum.mol.genet.,18(4):785-796;newman et al.(2012)hear res.294:125-132;luo etal.(2013)plos one,8(10):e77153;haider et al.(2017)front.aging neurosci.9:346;matyas et al.(2019)pathol.oncol.res.25(4):1645-52;chang et al.(2018)j.int.adv.otol.14(2):170-175)。grm7变体也被鉴定为与噪声诱导的听力损失相关,如luet al.(bmc med.genet.(2018),19(1):4)所报道,与耳鸣相关,如haider et al.(front.aging neurosci.(2017),9:346)所报道。最后,通过免疫组织化学研究的mglu7表达位于螺旋神经节的神经元、corti器官的内和外毛细胞、以及由球囊(sacculus)、椭圆囊(utriculus)和壶腹嵴(crista ampullaris)形成的前庭器官的毛细胞中(friedman etal.(2008)wo2008131439)。这些数据表明,mglu7受体调节剂在实验性治疗与内耳以及听觉神经系统相关的耳障碍(例如年龄相关性听力损伤(老年性耳聋)、噪声诱导的听力损失、急性和慢性听力损失、耳鸣、梅尼埃病(meniere’s disease)和前庭障碍)的实验性治疗中具有潜在用途。
14、最后,除了mglu7在整个cns中广泛分布之外,mglu7还表现出所有mglur的最高程度的进化保守性(flor et al.(1997)neuropharmacol.,36:153-159),表明该受体在cns功能中的重要作用。此外,其对谷氨酸具有相对低的亲和力(okamato et al.(1994)j.biol.chem.,269:1231-1236),因此其在正常传递期间可保持无活性,仅在过度谷氨酸释放的时期期间才变得具有活性(ferraguti f.and shigemoto r.(2006)cell tissueres.,326:483-504)。总之,这些数据强有力地强调了mglu7调节剂在临床适应证例如神经保护作用(治疗卒中和头损伤、缺血性损伤和神经毒性)中的潜能。
15、总之,这些药理和遗传数据强有力地支持了mglu7调节剂用于治疗广泛的精神、神经系统、神经发育、耳和疼痛障碍中的疾病和相关症状的潜能。
16、bantick et al在国际公布wo9929695中已表明吡咯并哒嗪酮可用作免疫抑制剂。b.a.stearns et al.在bioorg.&med.chem.let((2004),14,1295-1298)中描述了6-芳基-6h-吡咯并[3,4-d]哒嗪衍生物,其显示出对电压门控钙通道的α2δ亚基的高亲和性。然而,没有具体公开的化合物在结构上与本发明化合物相关。
技术实现思路
1、本发明涉及具有代谢型谷氨酸受体7调节剂活性的化合物。在其最一般的化合物方面中,本发明提供了根据式(i)的化合物:
2、
3、其可药用酸加成盐或碱加成盐、其立体化学异构形式或者其n-氧化物形式,其中:
4、r1选自氢、-ch3和-cf3的组(例如由其组成的组);
5、r2和r3各自独立地选自(例如由以下组成的组):氢、-(c1-c6)烷基、-(c1-c6)卤代烷基和-cf3;
6、p代表下式的环烷基、芳基或杂芳基:
7、
8、其中每个环烷基、芳基或杂芳基环任选地被m个基团a取代,其中m是等于0、1、2、3或4的整数;
9、其中z1、z2、z3、z4、z5、z6和z7各自独立地选自c、n、o或s;前提是z1、z2、z3、z4、z5、z6和z7中的至少一者是n;
10、(a)m或每个(a)m独立地选自(例如由以下组成的组):氢、卤素、-cn、-oh、-no2、-cf3、-sh、-nh2和任选地经取代的选自以下(例如由以下组成的组)的基团:-(c1-c6)烷基、-(c1-c6)卤代烷基、-(c2-c6)炔基、-(c2-c6)烯基、-(c3-c7)环烷基、-(c1-c6)亚烷基-(c3-c7)环烷基、-(c3-c8)环烯基、-(c1-c6)氰烷基、-(c1-c6)亚烷基-杂芳基、-(c1-c6)亚烷基-芳基、芳基、杂芳基、-(c1-c6)亚烷基-杂环、杂环、-(c0-c6)亚烷基-or4、-o-(c2-c6)亚烷基-or4、-nr4(c2-c6)亚烷基-or5、-(c3-c6)亚炔基-or4、-(c3-c6)亚炔基-nr4r5、-(c3-c6)亚烯基-or4、-(c3-c6)亚烯基-nr4r5、-(c0-c6)亚烷基-s-r4、-o-(c2-c6)亚烷基-s-r4、-nr4-(c2-c6)亚烷基-s-r5、-(c0-c6)亚烷基-s(=o)-r4、-o-(c1-c6)亚烷基-s(=o)-r4、-nr4-(c1-c6)亚烷基-s(=o)-r5、-(c0-c6)亚烷基-s(=o)2-r4、-o-(c1-c6)亚烷基-s(=o)2-r4、-nr4-(c1-c6)亚烷基-s(=o)2-r5、-(c0-c6)亚烷基-nr4r5、-o-(c2-c6)亚烷基-nr4r5、-nr4-(c2-c6)亚烷基-nr5r6、-(c0-c6)亚烷基-s(=o)2nr4r5、-o-(c1-c6)亚烷基-s(=o)2nr4r5、-nr4-(c1-c6)亚烷基-s(=o)2nr5r6、-(c0-c6)亚烷基-nr4-s(=o)2r5、-o-(c2-c6)亚烷基-nr4-s(=o)2r5、-nr4-(c2-c6)亚烷基-nr5-s(=o)2r6、-(c0-c6)亚烷基-c(=o)-nr4r5、-o-(c1-c6)亚烷基-c(=o)-nr4r5、-nr4-(c1-c6)亚烷基-c(=o)-nr5r6、-(c0-c6)亚烷基-nr4c(=o)-r5、-o-(c2-c6)亚烷基-nr4c(=o)-r5、-nr4-(c2-c6)亚烷基-nr5c(=o)-r6、-(c0-c6)亚烷基-oc(=o)-r4、-o-(c2-c6)亚烷基-oc(=o)-r4、-nr4-(c2-c6)亚烷基-oc(=o)-r5、-(c0-c6)亚烷基-c(=o)-or4、-o-(c1-c6)亚烷基-c(=o)-or4、-nr4-(c1-c6)亚烷基-c(=o)-or5、-(c0-c6)亚烷基-c(=o)-r4、-o-(c1-c6)亚烷基-c(=o)-r4、-nr4-(c1-c6)亚烷基-c(=o)-r5、-(c0-c6)亚烷基-nr4-c(=o)-or5、-c(=o)-(c1-c6)亚烷基-nr4-c(=o)-or5、-(c0-c6)亚烷基-o-c(=o)-nr4r5、-(c0-c6)亚烷基-nr4-c(=o)-nr5r6、-o-(c2-c6)亚烷基-nr4-c(=o)-nr5r6、-nr4-(c2-c6)亚烷基-nr5-c(=o)-nr6r7、-(c0-c6)亚烷基-nr4-c(=s)-nr5r6和-(c0-c6)亚烷基-nr4-c(=nr5)-nr6r7;
11、r4、r5、r6和r7各自独立地为氢或任选地经取代的选自以下(例如由以下组成的组)的基团:-(c1-c6)卤代烷基、-(c1-c6)烷基、-(c1-c6)氰烷基、-(c3-c7)环烷基、-(c1-c6)亚烷基-(c3-c7)环烷基、杂芳基、-(c1-c6)亚烷基-杂芳基、芳基、-(c1-c6)亚烷基-杂环、杂环、-(c1-c6)亚烷基-芳基、-(c0-c6)亚烷基-o-(c0-c6)烷基和-(c0-c6)亚烷基-n-((c0-c6)烷基)2;
12、q是任选地被n个基团b取代的芳基或杂芳基,其中n是等于0、1、2、3、4或5的整数;
13、(b)n或每个(b)n独立地选自选自(例如由以下组成的组):氢、卤素、-cn、-oh、-no2、-cf3、-sh、-nh2和任选地经取代的选自以下(例如由以下组成的组)的基团:-(c1-c6)烷基、-(c1-c6)卤代烷基、-(c2-c6)炔基、-(c2-c6)烯基、-(c3-c7)环烷基、-(c1-c6)亚烷基-(c3-c7)环烷基、-(c3-c8)环烯基、-(c1-c6)氰烷基、-(c1-c6)亚烷基-杂芳基、-(c1-c6)亚烷基-芳基、芳基、杂芳基、-(c1-c6)亚烷基-杂环、杂环、-(c0-c6)亚烷基-or8、-o-(c2-c6)亚烷基-or8、-nr8(c2-c6)亚烷基-or9、-(c3-c6)亚炔基-or8、-(c3-c6)亚炔基-nr8r9、-(c3-c6)亚烯基-or8、-(c3-c6)亚烯基-nr8r9、-(c0-c6)亚烷基-s-r8、-o-(c2-c6)亚烷基-s-r8、-nr8-(c2-c6)亚烷基-s-r9、-(c0-c6)亚烷基-s(=o)-r8、-o-(c1-c6)亚烷基-s(=o)-r8、-nr8-(c1-c6)亚烷基-s(=o)-r9、-(c0-c6)亚烷基-s(=o)2-r8、-o-(c1-c6)亚烷基-s(=o)2-r8、-nr8-(c1-c6)亚烷基-s(=o)2-r9、-(c0-c6)亚烷基-nr8r9、-o-(c2-c6)亚烷基-nr8r9、-nr8-(c2-c6)亚烷基-nr9r10、-(c0-c6)亚烷基-s(=o)2nr8r9、-o-(c1-c6)亚烷基-s(=o)2nr8r9、-nr8-(c1-c6)亚烷基-s(=o)2nr9r10、-(c0-c6)亚烷基-nr8-s(=o)2r9、-o-(c2-c6)亚烷基-nr8-s(=o)2r9、-nr8-(c2-c6)亚烷基-nr9-s(=o)2r10、-(c0-c6)亚烷基-c(=o)-nr8r9、-o-(c1-c6)亚烷基-c(=o)-nr8r9、-nr8-(c1-c6)亚烷基-c(=o)-nr9r10、-(c0-c6)亚烷基-nr8c(=o)-r9、-o-(c2-c6)亚烷基-nr8c(=o)-r9、-nr8-(c2-c6)亚烷基-nr9c(=o)-r10、-(c0-c6)亚烷基-oc(=o)-r8、-o-(c2-c6)亚烷基-oc(=o)-r8、-nr8-(c2-c6)亚烷基-oc(=o)-r9、-(c0-c6)亚烷基-c(=o)-or8、-o-(c1-c6)亚烷基-c(=o)-or8、-nr8-(c1-c6)亚烷基-c(=o)-or9、-(c0-c6)亚烷基-c(=o)-r8、-o-(c1-c6)亚烷基-c(=o)-r8、-nr8-(c1-c6)亚烷基-c(=o)-r9、-(c0-c6)亚烷基-nr8-c(=o)-or9、-(c0-c6)亚烷基-o-c(=o)-nr8r9、-(c0-c6)亚烷基-nr8-c(=o)-nr9r10、-o-(c2-c6)亚烷基-nr8-c(=o)-nr9r10、-nr8-(c2-c6)亚烷基-nr9-c(=o)-nr10r11、-(c0-c6)亚烷基-nr8-c(=s)-nr9r10和-(c0-c6)亚烷基-nr8-c(=nr9)-nr10r11;
14、r8、r9、r10和r11各自独立地为氢或任选地经取代的选自以下(例如由以下组成的组)的基团:-(c1-c6)卤代烷基、-(c1-c6)烷基、-(c1-c6)氰烷基、-(c3-c7)环烷基、-(c1-c6)亚烷基-(c3-c7)环烷基、杂芳基、-(c1-c6)亚烷基-杂芳基、芳基、-(c1-c6)亚烷基-杂环、杂环、-(c1-c6)亚烷基-芳基、-(c0-c6)亚烷基-o-(c0-c6)烷基和-(c0-c6)亚烷基-n-((c0-c6)烷基)2;其中任选的任意两个基团a与间插原子组合以形成3至10元的双环杂环、芳基或杂芳基环,其中每个环任选地进一步被1至5个基团取代,所述基团独立地选自(例如由以下组成的组):卤素、-cn、硝基、-(c1-c6)烷基、-(c0-c6)亚烷基-o-(c0-c6)烷基和-(c0-c6)亚烷基-n-((c0-c6)烷基)2;
15、其中任选地,取代基r4、r5、r6或r7中的二者与间插原子组合以形成3至10元的杂环、芳基或杂芳基环,其中每个环任选地进一步被1至5个基团取代,所述基团独立地选自(例如由以下组成的组):卤素、氰基、硝基、-(c1-c6)烷基、-(c0-c6)亚烷基-o-(c0-c6)烷基和-–(c0-c6)亚烷基-n-((c0-c6)烷基)2;
16、其中任选地,来自r8、r9、r10或r11的两个取代基与间插原子组合以形成3至10元的杂环、芳基或杂芳基环,其中每个环任选地进一步被1至5个基团取代,所述基团独立地选自(例如由以下组成的组):卤素、氰基、硝基、-(c1-c6)烷基、-(c0-c6)亚烷基-o-(c0-c6)烷基和-(c0-c6)亚烷基-n-((c0-c6)烷基)2;
17、其中任选地任意两个基团b与间插原子组合以形成3至10元的双环杂环、芳基或杂芳基环,其中每个环任选地进一步被1至5个基团取代,所述基团独立地选自(例如由以下组成的组):卤素、-cn、硝基、-(c1-c6)烷基、-(c0-c6)亚烷基-o-(c0-c6)烷基和-(c0-c6)亚烷基-n-((c0-c6)烷基)2。
18、出乎意料地,现已发现通式(i)化合物表现出对mglu7受体强效的活性和选择性。本发明的化合物相比于现有技术化合物显示出有益特性。已在本发明化合物的以下特征中的一者或更多者中观察到改进:对靶标的效力、对靶标的选择性、生物利用度、脑渗透和药效学。
19、优选地,
20、q代表下式的芳基或杂芳基基团:
21、
22、其中每个基团任选地被n个基团b取代,其中n是等于0、1、2、3、4或5的整数。b1可以是上述的基团b。例如,b1可以是氢、-(c1-c6)烷基或-(c3-c7)环烷基。
23、例如,q可代表下式的芳基或杂芳基基团:
24、其中每个基团任选地被n个基团b取代,其中n是等于0、1、2、3、4或5的整数。b1可以是如上所述的基团b。例如,b1可以是氢、-(c1-c6)烷基或-(c3-c7)环烷基。
25、例如,p可代表下式的环烷基、芳基或杂芳基:
26、
27、其中每个基团任选地被m个基团a取代,其中m是等于0、1、2、3或4的整数。
28、例如,p可以是任选地被m个基团a取代的其中m是等于0、1、2、3、4或5的整数;并且q可以是任选地被n个基团b取代的苯基,其中n是等于0、1、2、3、4或5的整数。
29、(a)m的环烷基、杂环、芳基和杂芳基环系可选自(例如由以下组成的组):氮杂环丁烷基、苯并咪唑基、苯并异噻唑基苯并异唑基、苯并呋喃基、苯并吡唑基、苯并噻唑基、苯并噻吩基、苯并三唑基、苯并唑基、二氢呋喃基、二氢噻吩基、二氧戊环基(dioxolanyl)、1,1-二氧代-硫代吗啉基、呋吖基、呋喃基、咪唑烷基、咪唑啉基、咪唑啉酮基、咪唑基、咪唑并哒嗪基、咪唑并吡啶基、吲哚基、异吲哚基、异喹啉基、异噻唑啉基、异噻唑基、异唑烷基、异唑啉基、异唑基、吗啉基、萘基、萘啶基、二唑基、唑烷基、唑啉基、唑酮基、唑并哒嗪基、唑并吡啶基、唑基、氧杂环丁烷基、苯基、哌嗪酮基、哌嗪基、哌啶酮基、哌啶基、酞嗪基、蝶啶基、嘌呤基、吡喃基、吡嗪基、吡唑并吡啶基、吡唑基、哒嗪基、吡啶酮基、吡啶基、嘧啶基、吡咯烷酮基、吡咯烷基、吡咯啉基、吡咯基、喹唑啉基、喹啉基、喹喔啉基、四氢呋喃基、四氢吡喃基、四氢硫代吡喃基、四氢三唑并吡啶基、四氢三唑并嘧啶基、四唑基、噻二唑基、噻唑烷基、噻唑啉基、噻唑酮基、噻唑并哒嗪基、噻唑并吡啶基、噻唑基、噻吩基、硫代吗啉基、硫代萘基、硫代吡喃基、三唑啉基、三嗪基、三唑基、环丙基、环丁基、环戊基、环戊烯基、环己基、环己烯基、环庚基、环庚烯基、环辛基和环辛烯基,并且所述环系的每个环任选地独立地被1至4个取代基r4、r5、r6或r7取代。
30、(b)n的环烷基、杂环、芳基和杂芳基环系可选自(例如由以下组成的组):氮杂环丁烷基、苯并咪唑基、苯并异噻唑基苯并异唑基、苯并呋喃基、苯并吡唑基、苯并噻唑基、苯并噻吩基、苯并三唑基、苯并唑基、二氢呋喃基、二氢噻吩基、二氧戊环基、1,1-二氧代-硫代吗啉基、呋吖基、呋喃基、咪唑烷基、咪唑啉基、咪唑啉酮基、咪唑基、咪唑并哒嗪基、咪唑并吡啶基、吲哚基、异吲哚基、异喹啉基、异噻唑啉基、异噻唑基、异唑烷基、异唑啉基、异唑基、吗啉基、萘基、萘啶基、二唑基、唑烷基、唑啉基、唑酮基、唑并哒嗪基、唑并吡啶基、唑基、氧杂环丁烷基、苯基、哌嗪酮基、哌嗪基、哌啶酮基、哌啶基、酞嗪基、蝶啶基、嘌呤基、吡喃基、吡嗪基、吡唑并吡啶基、吡唑基、哒嗪基、吡啶酮基、吡啶基、嘧啶基、吡咯烷酮基、吡咯烷基、吡咯啉基、吡咯基、喹唑啉基、喹啉基、喹喔啉基、四氢呋喃基、四氢吡喃基、四氢硫代吡喃基、四氢三唑并吡啶基、四氢三唑并嘧啶基、四唑基、噻二唑基、噻唑烷基、噻唑啉基、噻唑酮基、噻唑并哒嗪基、噻唑并吡啶基、噻唑基、噻吩基、硫代吗啉基、硫代萘基、硫代吡喃基、三唑啉基、三嗪基、三唑基、环丙基、环丁基、环戊基、环戊烯基、环己基、环己烯基、环庚基、环庚烯基、环辛基和环辛烯基,并且所述环系的每个环任选地独立地被1至4个取代基r8、r9、r10或r11取代。
31、r4、r5、r6、r7、r8、r9、r10或r11的环烷基、杂环、芳基和杂芳基环系可选自(例如由以下组成的组):氮杂环丁烷基、苯并咪唑基、苯并异噻唑基苯并异唑基、苯并呋喃基、苯并吡唑基、苯并噻唑基、苯并噻吩基、苯并三唑基、苯并唑基、二氢呋喃基、二氢噻吩基、二氧戊环基、1,1-二氧代-硫代吗啉基、呋吖基、呋喃基、咪唑烷基、咪唑啉基、咪唑啉酮基、咪唑基、咪唑并哒嗪基、咪唑并吡啶基、吲哚基、异吲哚基、异喹啉基、异噻唑啉基、异噻唑基、异唑烷基、异唑啉基、异唑基、吗啉基、萘基、萘啶基、二唑基、唑烷基、唑啉基、唑酮基、唑并哒嗪基、唑并吡啶基、唑基、氧杂环丁烷基、苯基、哌嗪酮基、哌嗪基、哌啶酮基、哌啶基、酞嗪基、蝶啶基、嘌呤基、吡喃基、吡嗪基、吡唑并吡啶基、吡唑基、哒嗪基、吡啶酮基、吡啶基、嘧啶基、吡咯烷酮基、吡咯烷基、吡咯啉基、吡咯基、喹唑啉基、喹啉基、喹喔啉基、四氢呋喃基、四氢吡喃基、四氢硫代吡喃基、四氢三唑并吡啶基、四氢三唑并嘧啶基、四唑基、噻二唑基、噻唑烷基、噻唑啉基、噻唑酮基、噻唑并哒嗪基、噻唑并吡啶基、噻唑基、噻吩基、硫代吗啉基、硫代萘基、硫代吡喃基、三唑啉基、三嗪基、三唑基、环丙基、环丁基、环戊基、环戊烯基、环己基、环己烯基、环庚基、环庚烯基、环辛基和环辛烯基,并且所述环系的每个环任选地被1至5个基团取代,所述基团独立地选自氢、卤素、-cn、硝基、-(c1-c6)烷基、-(c0-c6)亚烷基-o-(c0-c6)烷基和-(c0-c6)亚烷基-n-((c0-c6)烷基)2。
32、例如,r2和r3可各自独立地选自(例如由以下组成的组):氢、甲基和乙基,例如甲基。例如r2和r3二者均可以是甲基。
33、(a)m或每个(a)m可独立地选自(例如由以下组成的组):氢、卤素、-cn、-oh、-cf3和任选地经取代的选自以下(例如由以下组成的组)的基团:-(c1-c6)烷基、-(c1-c6)卤代烷基、-(c3-c7)环烷基、-(c1-c6)氰烷基、芳基、杂环、-(c0-c6)亚烷基-or4、-o-(c2-c6)亚烷基-or4、-(c0-c6)亚烷基-s(=o)2-r4、-(c0-c6)亚烷基-nr4r5、-(c0-c6)亚烷基-s(=o)2nr4r5、-(c0-c6)亚烷基-c(=o)-nr4r5、-(c0-c6)亚烷基-nr4c(=o)-r5、-(c0-c6)亚烷基-c(=o)-or4、-(c0-c6)亚烷基-c(=o)-r4和-c(=o)-(c1-c6)亚烷基-nr4-c(=o)-or5。任选地经取代的基团可任选地被卤素、-(c1-c6)烷基、oh或cn取代。
34、r4和r5可各自独立地为氢或-(c1-c6)烷基。
35、(b)n或每个(b)n可独立地选自(例如由以下组成的组):氢、卤素、-cn、-cf3和任选地经取代的选自以下(例如由以下组成的组)的基团:-(c1-c6)烷基、-(c3-c7)环烷基、芳基、杂芳基、杂环、-(c0-c6)亚烷基-or8、-nr8(c2-c6)亚烷基-or9、-(c0-c6)亚烷基-nr8r9、-(c0-c6)亚烷基-c(=o)-or8和-(c0-c6)亚烷基-c(=o)-r8。任选地经取代的基团可以任选地被卤素或-(c1-c6)烷基取代。任选地,两个-(c0-c6)亚烷基-or8基团可与间插原子组合以形成9元双环杂环环,例如环二乙基。
36、r8和r9可各自独立地选自(例如由以下组成的组):氢、-(c1-c6)卤代烷基、-(c1-c6)烷基、-(c3-c7)环烷基和芳基。
37、例如,r2和r3可各自独立地选自(例如由以下组成的组):甲基和乙基。例如,r2和r3二者均可以是甲基。
38、(a)m或每个(a)m可独立地选自(例如由以下组成的组):氢、卤素、-cn、-oh、-cf3和任选地经取代的选自以下(例如由以下组成的组)的基团:-(c1-c6)烷基、-(c1-c6)卤代烷基、-(c3-c7)环烷基、-(c1-c6)氰烷基、芳基、杂环、-(c0-c6)亚烷基-or4、-o-(c2-c6)亚烷基-or4、-(c0-c6)亚烷基-s(=o)2-r4、-(c0-c6)亚烷基-nr4r5、-(c0-c6)亚烷基-s(=o)2nr4r5、-(c0-c6)亚烷基-c(=o)-nr4r5、-(c0-c6)亚烷基-nr4c(=o)-r5、-(c0-c6)亚烷基-c(=o)-or4、-(c0-c6)亚烷基-c(=o)-r4和-c(=o)-(c1-c6)亚烷基-nr4-c(=o)-or5。
39、r4和r5可各自独立地为氢或-(c1-c6)烷基。
40、(b)n或每个(b)n可独立地选自(例如由以下组成的组):氢、卤素和任选地经取代的选自以下(例如由以下组成的组)的基团:-(c1-c6)烷基、杂环、-(c0-c6)亚烷基-or8、-nr8(c2-c6)亚烷基-or9、-(c0-c6)亚烷基-nr8r9、-(c0-c6)亚烷基-c(=o)-or8和-(c0-c6)亚烷基-c(=o)-r8。
41、r8和r9可各自独立地为氢或-(c1-c6)烷基。
42、例如,r2和r3可各自独立地选自(例如由以下组成的组):氢、甲基和乙基。例如,r2和r3二者均可以是甲基。
43、(a)m或每个(a)m可独立地选自(例如由以下组成的组):氢、卤素、-cn、-oh、-cf3和任选地经取代的选自以下(例如由以下组成的组)的基团:-–(c1-c6)烷基、-(c3-c7)环烷基、杂环和–-(c0-c6)亚烷基-or4。
44、r4可选自氢或-(c1-c6)烷基。
45、(b)n或每个(b)n可独立地选自(例如由以下组成的组):氢、卤素、-cn、-cf3和任选地经取代的选自以下(例如由以下组成的组)的基团:-(c1-c6)烷基、-(c3-c7)环烷基、芳基、杂芳基、杂环、-(c0-c6)亚烷基-or8、-(c0-c6)亚烷基-nr8r9、-(c0-c6)亚烷基-c(=o)-or8和-(c0-c6)亚烷基-c(=o)-r8。
46、r8和r9可各自独立地选自(例如由以下组成的组):氢、-(c1-c6)卤代烷基、-(c1-c6)烷基、-(c3-c7)环烷基和芳基,例如-(c1-c6)卤代烷基可以是-cf3。例如,-(c3-c7)环烷基可以是-(c3)环烷基。
47、例如,a可以是氢、卤素或-(c1-c6)烷基-oh,并且m可以是1。例如,b可以是-(c1-c6)烷基、-(c3-c7)环烷基、杂环、-o-(c3-c7)环烷基或-o-(c1-c6)烷基,并且n可以是1或2。例如,杂环可以是
48、优选地,式(i)化合物是根据式(ii)的化合物:
49、
50、其可药用酸加成盐或碱加成盐、其立体化学异构形式或者其n-氧化物形式,其中(a)m、p、r2、r3和(b)n根据上述任何陈述中所限定。
51、式(i)化合物可以是根据式(iia)的化合物
52、
53、其可药用酸加成盐或碱加成盐、其立体化学异构形式或者其n-氧化物形式,其中:
54、z1、z2、z3、z4和z5各自独立地选自c或n,并且(a)m、r1、r2、r3、
55、q和(b)根据上述任何陈述中所限定。
56、优选地,式(ii)化合物是根据式(iii):
57、
58、其可药用酸加成盐或碱加成盐、其立体化学异构形式或者其n-氧化物形式,其中:
59、z1、z2、z3、z4和z5各自独立地选自c或n,并且(a)m、r2、r3和(b)n根据上述任何陈述中所限定。
60、优选地,式(iii)化合物是根据下式(iv)的化合物:
61、
62、其可药用酸加成盐或碱加成盐、其立体化学异构形式或者其n-氧化物形式,其中(a)m、r2、r3和(b)n根据上述任何陈述中所限定。
63、优选地,r2和r3独立地选自(例如由以下组成的组):甲基和乙基;
64、(a)m或每个(a)m独立地选自(例如由以下组成的组):氢、卤素、-cn、-oh、-cf3和任选地经取代的选自以下(例如由以下组成的组)的基团:-(c1-c6)烷基、-(c1-c6)卤代烷基、-(c3-c7)环烷基、-(c1-c6)氰烷基、芳基、杂环、-(c0-c6)亚烷基-or4、-o-(c2-c6)亚烷基-or4、-(c0-c6)亚烷基-s(=o)2-r4、-(c0-c6)亚烷基-nr4r5、-(c0-c6)亚烷基-s(=o)2nr4r5、-(c0-c6)亚烷基-c(=o)-nr4r5、-(c0-c6)亚烷基-nr4c(=o)-r5、-(c0-c6)亚烷基-c(=o)-or4、-(c0-c6)亚烷基-c(=o)-r4和-c(=o)-(c1-c6)亚烷基-nr4-c(=o)-or5;
65、r4和r5各自独立地为氢或-(c1-c6)烷基;
66、(b)n或每个(b)n独立地选自(例如由以下组成的组):氢、卤素和任选地经取代的选自以下(例如由以下组成的组)的基团:-(c1-c6)烷基、杂环、-(c0-c6)亚烷基-or8、-nr8(c2-c6)亚烷基-or9、-(c0-c6)亚烷基-nr8r9、-(c0-c6)亚烷基-c(=o)-or8和-(c0-c6)亚烷基-c(=o)-r8;并且
67、r8和r9各自独立地为氢或-(c1-c6)烷基。
68、优选地,r2和r3中的一者或二者均可以是甲基。
69、优选地,式(iii)化合物是下式(v)化合物:
70、
71、其可药用酸加成盐或碱加成盐、其立体化学异构形式或者其n-氧化物形式,其中:
72、z1选自c或n;
73、r2和r3独自地选自(例如由以下组成的组):氢、甲基和乙基;
74、(a)m或每个(a)m独立地选自(例如由以下组成的组):氢、卤素、-cn、-oh、-cf3和任选地经取代的选自以下(例如由以下组成的组)的基团:-(c1-c6)烷基、-(c3-c7)环烷基、杂环和-(c0-c6)亚烷基-or4;
75、r4选自氢或-(c1-c6)烷基;
76、(b)n或每个(b)n独立地选自(例如由以下组成的组):氢、卤素、-cn、-cf3和任选地经取代的选自以下(例如由以下组成的组)的基团:-(c1-c6)烷基、-(c3-c7)环烷基、芳基、杂芳基、杂环、-(c0-c6)亚烷基-or8、-(c0-c6)亚烷基-nr8r9、-(c0-c6)亚烷基-c(=o)-or8和-(c0-c6)亚烷基-c(=o)-r8;并且
77、r8和r9各自独立地选自(例如由以下组成的组):氢、-(c1-c6)卤代烷基、-(c1-c6)烷基、-(c3-c7)环烷基和芳基。
78、优选地,在由式(v)所限定的化合物中,r2和r3中的一者或二者可以是甲基。
79、例如,a可以是氢、卤素或-(c1-c6)烷基-oh,并且m可以是1。例如b可以是-(c1-c6)烷基、-(c3-c7)环烷基、杂环、-o-(c3-c7)环烷基或-o-(c1-c6)烷基,并且n可以是1或2。例如,杂环可以是
80、本发明特别优选的化合物是如以下列表中所提及的化合物,及其可药用酸加成盐或碱加成盐、其立体化学异构形式或者其n-氧化物形式:
81、5,7-二甲基-2-苯基-6-(对甲苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
82、2-(2-甲氧基苯基)-5,7-二甲基-6-(对甲苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
83、6-(4-氯苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
84、5,7-二甲基-2,6-二苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
85、2-(2-甲氧基苯基)-5,7-二甲基-6-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
86、5,7-二甲基-2-苯基-6-(间甲苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
87、5,7-二甲基-2-苯基-6-(邻甲苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
88、6-(4-氯苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
89、5,7-二甲基-6-苯基-2-(吡啶-3-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
90、2-(3-氟苯基)-5,7-二甲基-6-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
91、2-(4-氟苯基)-5,7-二甲基-6-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
92、2-(3-甲氧基苯基)-5,7-二甲基-6-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
93、2-(4-甲氧基苯基)-5,7-二甲基-6-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
94、5,7-二甲基-6-苯基-2-(间甲苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
95、5,7-二甲基-6-苯基-2-(对甲苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
96、3-(5,7-二甲基-1-氧代-6-苯基-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苯甲腈
97、4-(5,7-二甲基-1-氧代-6-苯基-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苯甲腈
98、6-(2-甲氧基苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
99、6-(2-氯苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
100、2-(2-氯苯基)-5,7-二甲基-6-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
101、2-(2-氟苯基)-5,7-二甲基-6-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
102、5,7-二甲基-6-苯基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
103、6-(4-(二甲基氨基)苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
104、6-(4-甲氧基苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
105、5,7-二甲基-2-苯基-6-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
106、6-(3-甲氧基苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
107、2-(4-乙酰基苯基)-5,7-二甲基-6-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
108、4-(5,7-二甲基-1-氧代-6-苯基-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苯磺酰胺
109、6-(2-氟苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
110、5,7-二甲基-2-(4-(甲基磺酰基)苯基)-6-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
111、6-(4-乙酰基苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
112、6-(2,4-二甲基苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
113、5,7-二甲基-6-(3-吗啉代苯基)-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
114、6-(3-溴苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
115、6-(3-(二甲基氨基)苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
116、6-(3-乙酰基苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
117、5,7-二甲基-6-苯基-2-(吡啶-4-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
118、2-(4-(甲氧基甲基)苯基)-5,7-二甲基-6-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
119、5,7-二甲基-2-(吡啶-3-基)-6-(对甲苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
120、5,7-二甲基-2-(吡啶-3-基)-6-(间甲苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
121、6-(3-甲氧基苯基)-5,7-二甲基-2-(吡啶-3-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
122、6-(4-((2-甲氧基乙基)氨基)苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
123、6-(3-((2-甲氧基乙基)氨基)苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
124、6-(3-甲氧基苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
125、5,7-二甲基-2-(吡啶-2-基)-6-(间甲苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
126、6-(4-甲氧基苯基)-5,7-二甲基-2-(吡啶-3-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
127、6-(4-甲氧基苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
128、5,7-二甲基-2-(吡啶-2-基)-6-(对甲苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
129、5,7-二甲基-6-(3-(2-氧代吡咯烷-1-基)苯基)-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
130、5,7-二甲基-2-(6-甲基吡啶-3-基)-6-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
131、6-(3-羟基苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
132、2-(6-甲氧基吡啶-3-基)-5,7-二甲基-6-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
133、5,7-二甲基-2-(吡啶-2-基)-6-(3-(三氟甲基)苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
134、3-(5,7-二甲基-1-氧代-2-(吡啶-2-基)-1h-吡咯并[3,4-d]哒嗪-6(2h)-基)苯甲腈
135、6-(苯并[d][1,3]二氧杂环戊烯-5-基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
136、5,7-二甲基-6-(5-甲基吡啶-2-基)-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
137、4-(5,7-二甲基-1-氧代-6-苯基-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苯甲酰胺
138、5,7-二甲基-6-苯基-2-(嘧啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
139、5,7-二甲基-2-(吡啶-2-基)-6-(3-(吡咯烷-1-基)苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
140、2-(4-乙氧基苯基)-5,7-二甲基-6-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
141、6-(3-甲氧基苯基)-5,7-二甲基-2-(喹啉-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
142、6-(2-甲氧基吡啶-4-基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
143、6-(3-甲氧基苯基)-4,5,7-三甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
144、5,7-二甲基-6-(3-吗啉代苯基)-2-(吡啶-3-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
145、n-(4-(6-(3-甲氧基苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苄基)乙酰胺
146、2-(4-(羟基甲基)苯基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
147、2-(4-甲氧基苯基)-5,7-二甲基-6-(3-吗啉代苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
148、4-(5,7-二甲基-6-(3-吗啉代苯基)-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苯磺酰胺
149、2-(4-(甲氧基甲基)苯基)-5,7-二甲基-6-(3-吗啉代苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
150、6-(3-甲氧基苯基)-5,7-二甲基-2-(4-吗啉代苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
151、2-([1,1'-联苯基]-4-基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
152、6-(4-氯-3-甲氧基苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
153、3-(6-(3-甲氧基苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苯甲酰胺
154、6-(3-甲氧基苯基)-2-(6-甲氧基吡啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
155、4-(6-(3-甲氧基苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)-n,n-二甲基苯甲酰胺
156、6-([1,1'-联苯基]-3-基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
157、6-(3-乙氧基苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
158、7-乙基-6-(3-甲氧基苯基)-5-甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
159、6-(3-甲氧基-4-甲基苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
160、6-(1h-吲哚-6-基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
161、2-(4-甲氧基苯基)-5,7-二甲基-6-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
162、5,7-二甲基-6-(吡啶-2-基)-2-间甲苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
163、6-(3-甲氧基苯基)-2-(5-甲氧基吡啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
164、5,7-二甲基-6-(3-吗啉代苯基)-2-(间甲苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
165、6-(3-乙基苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
166、6-(4-乙基苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
167、4-(5,7-二甲基-1-氧代-6-苯基-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)-n,n-二甲基苯磺酰胺
168、2-(4-(氨基甲基)苯基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
169、7-乙基-6-(3-甲氧基苯基)-5-甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
170、5,7-二甲基-6-(3-吗啉代苯基)-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
171、6-(3-甲氧基苯基)-5,7-二甲基-2-(6-吗啉代吡啶-3-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
172、2-(4-(羟基甲基)苯基)-5,7-二甲基-6-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
173、5,7-二甲基-2-(4-吗啉代苯基)-6-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
174、6-(3-甲氧基苯基)-2-(5-甲氧基吡啶-3-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
175、6-(3-甲氧基苯基)-5,7-二甲基-2-(嘧啶-5-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
176、5,7-二甲基-6-(1-甲基-1h-吲哚-6-基)-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
177、6-(3-甲氧基苯基)-2-(4-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
178、2-(4-(羟基甲基)苯基)-6-(4-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
179、5,7-二甲基-2-(间甲苯基)-6-(对甲苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
180、6-(3-(二乙基氨基)苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
181、5,7-二甲基-2-苯基-6-(3-(吡咯烷-1-基)苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
182、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
183、2,6-双(4-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
184、n-(4-(5,7-二甲基-1-氧代-6-苯基-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苄基)乙酰胺
185、2-甲氧基-4-(6-(3-甲氧基苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苯甲酸甲酯
186、n-(4-(6-(4-甲氧基苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苄基)乙酰胺
187、6-(3-(甲氧基甲基)苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
188、6-(3-(甲氧基甲基)苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
189、6-(3-甲氧基苯基)-5,7-二甲基-2-(4-((甲基氨基)甲基)苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
190、6-(3-(二甲基氨基)苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
191、5,7-二甲基-6-(3-(2-氧代吡咯烷-1-基)苯基)-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
192、3-(6-(3-甲氧基苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)-n,n-二甲基苯甲酰胺
193、4-(6-(3-甲氧基苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)-n-甲基苯甲酰胺
194、2-(3-(羟基甲基)苯基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
195、n-(3-(6-(3-甲氧基苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苄基)乙酰胺
196、2-(3-(甲氧基甲基)苯基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
197、2-(3,4-二甲氧基苯基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
198、2-(4-(3-羟基丙基)苯基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
199、6-(3-甲氧基苯基)-5,7-二甲基-2-(4-(甲基磺酰基)苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
200、4-(6-(3-甲氧基苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苯磺酰胺
201、6-(3-甲氧基苯基)-2-(2-甲氧基吡啶-4-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
202、6-(3-甲氧基苯基)-5,7-二甲基-2-(5-(三氟甲基)吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
203、6-(3-甲氧基苯基)-2-(4-甲氧基吡啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
204、3-(6-(3-甲氧基苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苯甲腈
205、3-(6-(4-甲氧基苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苯甲腈
206、4-(6-(3-甲氧基苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苯甲腈
207、6-(3-甲氧基苯基)-2-(6-甲氧基吡啶-3-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
208、2-(4-(甲氧基甲基)苯基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
209、2-(2-羟基吡啶-4-基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
210、2,6-双(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
211、2-(6-羟基吡啶-3-基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
212、6-(4-乙酰基苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
213、3-(5,7-二甲基-1-氧代-2-(吡啶-2-基)-1h-吡咯并[3,4-d]哒嗪-6(2h)-基)苯甲酸乙酯
214、3-(5,7-二甲基-1-氧代-2-苯基-1h-吡咯并[3,4-d]哒嗪-6(2h)-基)苯甲酸乙酯
215、2-(4-(2-羟基丙烷-2-基)苯基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
216、6-(3-(呋喃-2-基)苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
217、6-(3-环丙基苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
218、2-(4-(1-羟基乙基)苯基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
219、6-(3-异丙氧基苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
220、5-乙基-6-(3-甲氧基苯基)-7-甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
221、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
222、6-(3-(1h-吡咯-1-基)苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
223、5,7-二甲基-6-(3-(哌啶-1-基)苯基)-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
224、2-(3-乙氧基苯基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
225、2-(4-羟基苯基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
226、2-(3-(6-(3-甲氧基苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苯基)乙腈
227、2-(3-乙酰基苯基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
228、2-(2-甲氧基苯基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
229、2-(2-氟苯基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
230、2-(2-氯苯基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
231、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(3-(甲基磺酰基)苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
232、3-(6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苯甲酰胺
233、6-(3-(3,3-二氟氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
234、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(6-甲基吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
235、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(5-甲基吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
236、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(吡啶-4-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
237、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(6-甲基吡啶-3-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
238、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(5-甲基吡啶-3-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
239、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(3-甲基吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
240、6-(6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)烟腈
241、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(4-甲基吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
242、6-(3-(氮杂环丁烷-1-基)苯基)-2-(4-(2-甲氧基乙氧基)苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
243、6-(3-(氮杂环丁烷-1-基)苯基)-2-(3-(羟基甲基)-4-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
244、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(吡啶-3-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
245、6-(3-(氮杂环丁烷-1-基)苯基)-2-(2,6-二甲基吡啶-4-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
246、6-(3-(氮杂环丁烷-1-基)苯基)-2-(4-(羟基甲基)-3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
247、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(3-吗啉代苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
248、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(4-(吡咯烷-1-基)苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
249、6-(3-(氮杂环丁烷-1-基)苯基)-2-(4-(2-羟基乙基)苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
250、6-(3-(氮杂环丁烷-1-基)苯基)-2-(4-(2-羟基丙烷-2-基)苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
251、2-(4-乙酰基苯基)-6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
252、6-(3-甲氧基苯基)-5,7-二甲基-2-(5-甲基吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
253、6-(3-(氮杂环丁烷-1-基)苯基)-2-(5-氟吡啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
254、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(4-(哌嗪-1-基)苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
255、6-(3,5-二甲氧基苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
256、6-(3-(氮杂环丁烷-1-基)苯基)-2-(2-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
257、6-(3-(氮杂环丁烷-1-基)苯基)-2-(2-氟苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
258、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(4-(3-氧代哌嗪-1-基)苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
259、6-(3-(3,3-二甲基吡咯烷-1-基)苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
260、2-(4-(6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苯基)-n-甲基乙酰胺
261、6-(3-(氮杂环丁烷-1-基)苯基)-2-(4-碘苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
262、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(2-甲基吡啶-4-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
263、6-(3-(氮杂环丁烷-1-基)苯基)-2-(5-氯吡啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
264、2-(4-(6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苯基)-2-氧代乙基氨基甲酸叔丁酯
265、2-(4-(6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苯基)乙酰胺
266、6-(4-环丙基苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
267、5,7-二甲基-6-(3-苯氧基苯基)-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
268、6-(3-(氮杂环丁烷-1-基)苯基)-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
269、6-(3-(氮杂环丁烷-1-基)苯基)-2-(4-(2-氟乙基)苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
270、6-(3-(氮杂环丁烷-1-基)苯基)-2-环戊基-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
271、6-(4-氟-2-甲氧基苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
272、6-(3-(氮杂环丁烷-1-基)-4-氟苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
273、6-(2-甲氧基苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
274、6-(2-氟-5-甲氧基苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
275、6-(3-(氮杂环丁烷-1-基)-5-氟苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
276、6-(5-(氮杂环丁烷-1-基)-2-氟苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
277、6-(2-氯-3-甲氧基苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
278、6-(1-环丙基-1h-吲哚-4-基)-5,7-二甲基-2-(嘧啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
279、6-(3-(2h-1,2,3-三唑-2-基)苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
280、6-(3-环丙氧基-2-甲基苯基)-5,7-二甲基-2-(嘧啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
281、6-(2,4-二甲基苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
282、6-(3-(二氟甲氧基)苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
283、6-(2-氯-3-甲氧基苯基)-5,7-二甲基-2-(嘧啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
284、6-(2-氯-3-甲氧基苯基)-5,7-二甲基-2-(5-甲基嘧啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
285、6-(3-环丙氧基-2-甲基苯基)-5,7-二甲基-2-(5-甲基嘧啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
286、2-(5-叔丁基吡啶-2-基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
287、2-(5-环丙基嘧啶-2-基)-6-(3-甲氧基-2-甲基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
288、6-(3-(氮杂环丁烷-1-基)-5-氟苯基)-2-(5-氟嘧啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
289、6-(3-(氮杂环丁烷-1-基)-5-氟苯基)-2-(3-氟吡啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
290、5,7-二甲基-6-(1-甲基二氢吲哚-4-基)-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
291、6-(3-环丙氧基-2-甲基苯基)-2-(3-氟吡啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
292、6-(3-环丙氧基-2-甲基苯基)-2-(5-氟嘧啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
293、6-(1-环丙基-1h-吲哚-4-基)-2-(3-氟吡啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
294、6-(1-环丙基-1h-吲哚-4-基)-2-(5-氟嘧啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
295、6-(2-氯-3-环丙氧基苯基)-5,7-二甲基-2-(嘧啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
296、2-(5-(2-羟基丙烷-2-基)吡啶-2-基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
297、6-(5-(氮杂环丁烷-1-基)-2-氟苯基)-2-(3-氟吡啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
298、6-(5-(氮杂环丁烷-1-基)-2-氟苯基)-2-(5-氟嘧啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
299、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(4-吗啉代苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
300、6-(3-羟基-2-甲基苯基)-5,7-二甲基-2-(4-吗啉代苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
301、6-(3-环丙氧基-2-甲基苯基)-5,7-二甲基-2-(4-吗啉代苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮.
302、6-(3-(氮杂环丁烷-1-基)苯基)-2-(双环[1.1.1]戊烷-1-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
303、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(嘧啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
304、6-(3-(氮杂环丁烷-1-基)苯基)-2-(5-甲氧基嘧啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
305、6-(3-(氮杂环丁烷-1-基)苯基)-2-(3-氟吡啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
306、6-(3-(氮杂环丁烷-1-基)苯基)-2-(5-氟嘧啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
307、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(噻唑基-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
308、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(5-甲基嘧啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
309、6-(3-(氮杂环丁烷-1-基)苯基)-2-(4-甲氧基吡啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
310、6-(3-甲氧基-2-甲基苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
311、6-(3-甲氧基-2-甲基苯基)-5,7-二甲基-2-(嘧啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
312、6-(3-(二氟甲氧基)-2-甲基苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
313、6-(2-氟-3-甲氧基-苯基)-5,7-二甲基-3-(2-吡啶基)吡咯并[3,4-d]哒嗪-4-酮
314、6-(2-氟-3-甲氧基-苯基)-5,7-二甲基-3-嘧啶-2-基-吡咯并[3,4-d]哒嗪-4-酮
315、6-[3-(环丙氧基)-2-氟-苯基]-5,7-二甲基-3-(2-吡啶基)吡咯并[3,4-d]哒嗪-4-酮
316、6-[3-(环丙氧基)-2-氟-苯基]-5,7-二甲基-3-嘧啶-2-基-吡咯并[3,4-d]哒嗪-4-酮
317、6-(2-环丙氧基-3-氟吡啶-4-基)-5-甲基-2-(嘧啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
318、6-(6-甲氧基吡啶-3-基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
319、6-(2-氟-6-甲氧基吡啶-3-基)-5,7-二甲基-2-(嘧啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
320、6-(2-环丙氧基-3-甲基吡啶-4-基)-5-甲基-2-(嘧啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
321、6-(6-甲氧基吡啶-3-基)-5,7-二甲基-2-(嘧啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
322、6-(6-甲氧基-2-甲基吡啶-3-基)-5,7-二甲基-2-(嘧啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮,以及
323、6-(3-环丙氧基-2-氟苯基)-5-甲基-2-(嘧啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮。
324、以上化合物列表也可以通过以下骨架式表示:
325、
326、
327、
328、
329、
330、
331、
332、
333、
334、
335、优选地,化合物是选自以下列表中的一种或更多种,以及可药用酸加成盐或碱加成盐、其立体化学异构形式或者其n-氧化物形式:
336、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
337、6-(3-(氮杂环丁烷-1-基)-5-氟苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
338、6-(5-(氮杂环丁烷-1-基)-2-氟苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
339、6-(1-环丙基-1h-吲哚-4-基)-5,7-二甲基-2-(嘧啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
340、6-(3-环丙氧基-2-甲基苯基)-5,7-二甲基-2-(嘧啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
341、6-(3-(氮杂环丁烷-1-基)-5-氟苯基)-2-(5-氟嘧啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
342、6-(3-(氮杂环丁烷-1-基)-5-氟苯基)-2-(3-氟吡啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
343、6-(3-环丙氧基-2-甲基苯基)-2-(5-氟嘧啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
344、6-(1-环丙基-1h-吲哚-4-基)-2-(5-氟嘧啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
345、2-(5-(2-羟基丙烷-2-基)吡啶-2-基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
346、6-(3-(氮杂环丁烷-1-基)苯基)-2-(3-氟吡啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
347、6-(3-(氮杂环丁烷-1-基)苯基)-2-(5-氟嘧啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮,以及
348、6-[3-(环丙氧基)-2-氟-苯基]-5,7-二甲基-3-嘧啶-2-基-吡咯并[3,4-d]哒嗪-4-酮。
349、以上列出的化合物也可通过以下骨架式表示:
350、
351、优选地,化合物是选自以下列表中的一种或更多种,及其可药用酸加成盐或碱加成盐、其立体化学异构形式或者其n-氧化物形式:
352、6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
353、6-(3-环丙氧基-2-甲基苯基)-5,7-二甲基-2-(嘧啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
354、6-(3-环丙氧基-2-甲基苯基)-2-(5-氟嘧啶-2-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮,以及
355、6-[3-(环丙氧基)-2-氟-苯基]-5,7-二甲基-3-嘧啶-2-基-吡咯并[3,4-d]哒嗪-4-酮。
356、以上列出的化合物也可通过以下骨架式表示:
357、
358、根据以上任何陈述的化合物可表现出代谢型谷氨酸受体7调节剂活性。
359、所公开的化合物也包含所有可药用同位素变化,其中至少一个原子被具有相同原子序数但原子质量不同于自然界中通常所见原子质量的原子取代。适合于包含在所公开化合物内的同位素的一些实例包括但不限于氢的同位素,例如2h和3h;碳的同位素,例如11c、13c和14c;氮的同位素,例如15n;氧的同位素,例如17o和18o;磷的同位素,例如31p、32p和33p;硫的同位素,例如35s;氟的同位素,例如18f;氯的同位素,例如36cl;以及碘的同位素,例如125i。本发明包括多种如本文中所限定的经同位素标记的化合物,例如其中存在放射性同位素(例如3h和14c)的那些化合物,或其中存在非放射性同位素(例如2h和13c)的那些化合物。
360、这样的经同位素标记的化合物可用于代谢研究(用14c)、反应动力学研究(例如用2h或3h)、检测或成像技术(例如正电子发射断层摄影术(positron emission tomography,pet)或单光子发射计算机断层摄影术(single-photon emission computed tomography,spect),包括药物或底物组织分布测定)、或者用于患者的放射性治疗。特别地,11c、18f、15o和13n或者经标记的化合物可特别适合于检查底物受体占位(substrate receptoroccupancy)的pet研究。此外,经较重同位素,特别是氘(例如,2h或d)的取代可因更好的代谢稳定性(例如,提高的体内半衰期或降低的剂量需求或者治疗指数的减轻)而提供某些治疗优势。应理解,该上下文中的氘被视为式(i)至式(v)化合物的取代基。经同位素标记的式(i)至式(v)化合物通常可以通过本领域技术人员已知的常规技术或通过类似于所附实施例中所描述的那些方法使用合适的同位素标记试剂代替先前使用的非标记试剂来制备。
361、在本发明的一个方面中,提供了包含根据上述任何陈述的化合物的药物组合物。该药物组合物可还包含可药用的载体和/或赋形剂。该药物组合物可包含治疗有效量的根据上述任何陈述的化合物。
362、在本发明的一个方面中,提供了在哺乳动物中治疗或预防病症的方法,其包括向需要这样的治疗或预防的哺乳动物施用有效量的根据上述任何陈述的化合物/组合物。
363、该治疗或预防可通过mglu7别构调节剂例如mglu7负别构调节剂的调节作用来实现或促进。
364、该病症可以是中枢神经系统障碍或者耳疾病或病症或者疼痛障碍中的一种或更多种。
365、中枢神经系统障碍可以是创伤后应激障碍(post-traumatic stress disorder,ptsd)。
366、耳疾病和障碍可以是以下中的一种或更多种:内耳损伤、年龄相关性听力损伤(老年性耳聋)、梅尼埃病(meniere’s disease)、突发性听力损失、噪声诱导的听力损失、中耳炎、自身免疫性内耳病、急性耳鸣、慢性耳鸣、药物诱导的听力损失、隐性听力损失、顺铂诱导的听力损失、氨基糖苷类诱导的听力损失、耳毒性、中枢听觉处理障碍或前庭障碍。
367、在本发明的另一个方面中,提供了在哺乳动物中治疗、预防、改善、控制与谷氨酸功能障碍相关的多种神经系统和精神障碍或者降低其风险的方法,其包括向需要这样的治疗或预防的哺乳动物施用有效量的根据以上述任何陈述的化合物/组合物。该治疗或预防可通过mglu7负别构调节剂的调节作用来实现或促进。
368、优选地,该方法用于在人中治疗或预防病症。
369、在本发明的另一个方面中,提供了如以上任何陈述所阐述的化合物或组合物,其用作药物。
370、在本发明的另一个方面中,提供了如以上任何陈述所阐述的化合物或组合物,其用于如上述任何陈述中所限定的治疗或预防的方法。
371、在本发明的另一个方面中,提供了根据上述任何陈述的化合物在制备药物中的用途,所述药物用于如上述任何陈述中所限定的治疗或预防病症。
372、术语定义
373、下面列出的是用于说明书和权利要求书中以描述本发明的多种术语的定义。
374、为避免疑问,应理解在本说明书中“(c1-c6)”意指具有1、2、3、4、5或6个碳原子的碳基团。“(c0-c6)”意指具有0、1、2、3、4、5或6个碳原子的碳基团。在本说明书中“c”意指碳原子,“n”意指氮原子、“o”意指氧原子且“s”意指硫原子。
375、在下标为整数0(零)的情况下,下标所指的基团表示该基团不存在,即基团之间存在直接键。
376、在下标为整数0(零)并且下标所指的基团为烷基的情况下,这表示该基团是氢原子。
377、在本说明书中,除非另有说明,否则术语“键”是指饱和共价键。当两个或更多个键彼此相邻时,它们被假定为等于一个键。例如,基团-a-b-,其中a和b二者均可以是键,该基团表示单键。
378、在本说明书中,除非另有说明,否则术语“烷基”包括直链和支链烷基基团二者,并且可以是甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、异戊基、叔戊基、新戊基、正己基、异己基或叔己基。术语“(c0-c3)烷基”是指具有0、1、2或3个碳原子的烷基基团,并且可以是甲基、乙基、正丙基或异丙基。
379、在本说明书中,除非另有说明,否则术语“亚烷基”包括直链和支链双官能团饱和烃基团二者,并且可以是亚甲基(-ch2-)、亚乙基(-ch2-ch2-)、亚正丙基(-ch2-ch2-ch2-)、亚异丙基(-ch-(ch3)-ch2-)、亚正丁基(-ch2-ch2-ch2-ch2-)、亚异丁基(-ch2-ch-(ch3)-ch2-)、叔亚丁基(-ch2-c-(ch3)-ch2-)、亚正戊基(-ch2-ch2-ch2-ch2-ch2-)、亚异戊基(-ch2-ch(ch3)-ch2-ch2-)、新亚戊基(-ch2-c(ch3)2-ch2-)、亚正己基(-ch2-ch2-ch2-ch2-ch2-ch2-)、亚异己基(-ch2-ch-(ch3)-ch2-ch2-ch2-)或亚新己基(-ch2-c(ch3)2-ch2-ch2-)。术语“o-(c1-c6)亚烷基-芳基”是指在氧原子与芳基之间具有0、1、2、3、4、5或6个碳原子的烷基链。
380、在本说明书中,除非另有说明,否则术语“环烷基”是指任选地经取代的不含杂原子的碳环,包括单环、双环、和三环饱和碳环以及稠环体系。这样的稠环体系可包括部分或完全不饱和的一个环(例如苯环),以形成稠环体系例如苯并-稠合碳环。环烷基包括稠环体系,例如螺稠环体系。环烷基的一些实例包括环丙基、环丁基、环戊基、环己基、双环[1.1.1]戊烷基、十氢萘、金刚烷、茚满基、芴基和1,2,3,4-四氢萘等。术语“(c3-c7)环烷基”可以是环丙基、环丁基、环戊基、环己基、环庚基等。
381、在本说明书中,除非另有说明,否则术语“烯基”包括直链和支链烯基基团二者。术语“(c2-c6)烯基”是指具有2至6个碳原子和一或两个双键的烯基基团,并且可以是但不限于乙烯基、烯丙基、丙烯基、异丙烯基、丁烯基、异丁烯基、巴豆基、戊烯基、异戊烯基或己烯基。
382、在本说明书中,除非另有说明,否则术语“亚烯基”包括直链和支链双取代的烯基基团二者。术语“(c2-c6)亚烯基”是指具有2至6个碳原子和一或两个双键的亚烯基基团,并且可以是但不限于亚乙烯基、亚烯丙基、亚丙烯基、亚异丙烯基、亚丁烯基、亚异丁烯基、亚巴豆基、亚戊烯基、亚异戊烯基或亚己烯基。
383、在本说明书中,除非另有说明,否则术语“炔基”包括直链和支链炔基基团二者。术语(c2-c6)炔基,其具有2至6个碳原子和一或两个三键,并且可以是但不限于乙炔基、炔丙基、丁炔基、异丁炔基、戊炔基、异戊炔基或己炔基。
384、在本说明书中,除非另有说明,否则术语“亚炔基”包括直链和支链双取代的亚炔基基团二者。术语“(c2-c6)亚炔基”,其具有2至6个碳原子和一或两个三键,并且可以是但不限于亚乙炔基、亚炔丙基、亚丁炔基、亚异丁炔基、亚戊炔基、亚异戊炔基或亚己炔基。
385、术语“芳基”是指任选地经取代的包含至少一个不饱和芳环的单环或双环烃环体系。术语“芳基”的一些实例和适当值为苯基、萘基、1,2,3,4-四氢萘基、吲哚基、茚基等。
386、在本说明书中,除非另有说明,否则术语“杂芳基”是指任选地经取代的含有至少一个独立地选自n、o或s的杂原子的单环或双环不饱和芳环环系。“杂芳基”的一些实例可以是但不限于苯并咪唑基、苯并异噻唑基、苯并异唑基、苯并呋喃基、苯并吡唑基、苯并噻唑基、苯并噻吩基、苯并三唑基、苯并唑基、呋吖基、呋喃基、咪唑啉酮基、咪唑基、咪唑并哒嗪基、咪唑并吡啶基、吲哚基、异吲哚基、异喹啉基、异噻唑基、异唑基、萘啶基、二唑基、唑酮基、唑并哒嗪基、唑并吡啶基、唑基、酞嗪基、蝶啶基、嘌呤基、吡嗪基、吡唑并吡啶基、吡唑基、哒嗪基、吡啶酮基、吡啶基、嘧啶基、吡咯基、喹唑啉基、喹啉基、喹喔啉基、四氢三唑并吡啶基、四氢三唑并嘧啶基、四唑基、噻二唑基、噻唑酮基、噻唑并哒嗪基、噻唑并吡啶基、噻唑基、噻吩基、硫代萘基、三嗪基和三唑基。
387、在本说明书中,除非另有说明,否则术语“亚烷基-芳基”、“亚烷基-杂芳基”和“亚烷基-环烷基”分别是指通过烷基基团分别与芳基、杂芳基或环烷基基团连接的取代基。术语“(c1-c6)亚烷基-芳基”包括芳基-c1-c6-烷基基团,例如苄基、1-苯基乙基、2-苯基乙基、1-苯基丙基、2-苯基丙基、3-苯基丙基、1-萘基甲基和2-萘基甲基。术语“(c1-c6)亚烷基-杂芳基”包括杂芳基-c1-c6-烷基基团,其中杂芳基的一些实例与以上定义所阐述的那些相同,例如2-呋喃基甲基、3-呋喃基甲基、2-噻吩基甲基、3-噻吩基甲基、1-咪唑基甲基、2-咪唑基甲基、3-咪唑基甲基、2-唑基甲基、3-唑基甲基、2-噻唑基甲基、3-噻唑基甲基、2-吡啶基甲基、3-吡啶基甲基、4-吡啶基甲基、1-喹啉基甲基等。
388、在本说明书中,除非另有说明,否则术语“杂环”是指任选地经取代的含有至少一个独立地选自n、o和s的杂原子的单环、双环或三环饱和、部分饱和或不饱和的环系。双环或三环环系可由两个或更多个环的增环反应通过桥接原子(例如o、s、n)或通过桥接基团(例如亚烷基)形成。杂环部分的一些实例包括但不限于:氮杂环丁烷基、二氢呋喃基、二氢噻吩基、二氧戊环基、1,1-二氧代-硫代吗啉基、咪唑烷基、咪唑啉基、异噻唑啉基、异唑烷基、异唑啉基、吗啉基、唑烷基、唑啉基、氧杂环丁烷基、哌嗪酮基、哌嗪基、哌啶酮基、哌啶基、吡喃基、吡咯烷酮基、吡咯烷基、吡咯啉基、四氢呋喃基、四氢吡喃基、四氢硫代吡喃基、噻唑烷基、噻唑啉基、硫代吗啉基、硫代吡喃基、三唑啉基、和对应的苯并杂环(例如二氢苯并呋喃基、二氢苯并噻吩基、二氢苯并嗪基、二氢呋喃并吡啶基、二氢喹啉基、二氢噻吩并吡啶基、二氢吲哚基、吡咯并吡啶基、四氢喹啉基、四氢喹喔啉基等)。
389、在本说明书中,除非另有说明,否则含有一个或更多个独立地选自c、n、o和s的原子的5元或6元环包括芳族和杂芳族环以及碳环和杂环,其可以是饱和或不饱和的。这样的环包括螺环的和桥接双环体系。这样的环的一些实例可以是但不限于二氢呋喃基、二氢噻吩基、二氧戊环基、1,1-二氧代-硫代吗啉基、呋吖基、呋喃基、咪唑烷基、咪唑啉基、咪唑啉酮基、咪唑基、异噻唑啉基、异噻唑基、异唑烷基、异唑啉基、异唑基、吗啉基、二唑基、唑烷基、唑啉基、唑酮基、唑基、苯基、哌嗪酮基、哌嗪基、哌啶酮基、哌啶基、吡喃基、吡嗪基、吡唑基、哒嗪基、吡啶酮基、吡啶基、嘧啶基、吡咯烷酮基、吡咯烷基、吡咯啉基、吡咯基、四氢呋喃基、四氢吡喃基、四氢硫代吡喃基、四唑基、噻二唑基、噻唑烷基、噻唑啉基、噻唑酮基、噻唑基、噻吩基、硫代吗啉基、硫代吡喃基、三唑啉基、三嗪基、三唑基、环戊基、环戊烯基、环己基和环己烯基。
390、在本说明书中,除非另有说明,否则含有一个或更多个独立地选自c、n、o和s的原子的3至10元环包括芳环和杂芳环以及碳环和杂环,其可以是饱和的或不饱和的。这样的环的一些实例可以是但不限于氮杂环丁烷基、苯并咪唑基、苯并异噻唑基、苯并异唑基、苯并呋喃基、苯并吡唑基、苯并噻唑基、苯并噻吩基、苯并三唑基、苯并唑基、二氢呋喃基、二氢噻吩基、二氧戊环基、1,1-二氧代-硫代吗啉基、呋吖基、呋喃基、咪唑烷基、咪唑啉基、咪唑啉酮基、咪唑基、咪唑并哒嗪基、咪唑并吡啶基、吲哚基、异吲哚基、异喹啉基、异噻唑啉基、异噻唑基、异唑烷基、异唑啉基、异唑基、吗啉基、萘基、萘啶基、二唑基、唑烷基、唑啉基、唑酮基、唑并哒嗪基、唑并吡啶基、唑基、氧杂环丁烷基、苯基、哌嗪酮基、哌嗪基、哌啶酮基、哌啶基、酞嗪基、蝶啶基、嘌呤基、吡喃基、吡嗪基、吡唑并吡啶基、吡唑基、哒嗪基、吡啶酮基、吡啶基、嘧啶基、吡咯烷酮基、吡咯烷基、吡咯啉基、吡咯基、喹唑啉基、喹啉基、喹喔啉基、四氢呋喃基、四氢吡喃基、四氢硫代吡喃基、四氢三唑并吡啶基、四氢三唑并嘧啶基、四唑基、噻二唑基、噻唑烷基、噻唑啉基、噻唑酮基、噻唑并哒嗪基、噻唑并吡啶基、噻唑基、噻吩基、硫代吗啉基、硫代萘基、硫代吡喃基、三唑啉基、三嗪基、三唑基、环丙基、环丁基、环戊基、环戊烯基、环己基、环己烯基、环庚基、环庚烯基、环辛基和环辛烯基。
391、在本说明书中,除非另有说明,否则术语“卤代”或“卤素”可以是氟代、氯代、溴代或碘代。
392、在本说明书中,除非另有说明,否则术语“卤代烷基”意指经一个或更多个卤代基团取代的如上所限定的烷基基团。术语“(c1-c6)卤代烷基”可包括但不限于氟甲基、二氟甲基、三氟甲基、氟乙基和二氟乙基。术语“o-c1-c6-卤代烷基”可包括但不限于氟甲氧基、二氟甲氧基、三氟甲氧基和氟乙氧基。
393、在本说明书中,除非另有说明,否则术语“氰烷基”意指经一个或更多个氰基取代的如上所限定的烷基基团。
394、在本说明书中,除非另有说明,否则术语“任选地经取代的”是指进一步携带一个或更多个取代基的基团,所述取代基可以是酰基、(c1-c6)烷基、-(c1-c6)卤代烷基、-(c3-c7)环烷基、-(c1-c6)亚烷基-(c3-c7)环烷基、-(c3-c7)环烷基-(c1-c6)亚烷基、-(c0-c6)亚烷基-(c3-c7)螺烷基-(c0-c6)亚烷基、羟基、(c1-c6)亚烷基-氧基、二甲基氨基(c1-c3)烷基、巯基、芳基、杂环、杂芳基、(c1-c6)亚烷基-芳基、(c1-c6)亚烷基-杂环、(c1-c6)亚烷基-杂芳基、卤素、卤代烷基、三氟甲基、五氟乙基、卤代烷氧基、氰基、氰甲基、硝基、氨基、酰氨基(amido)、脒基、氧代、羧基、甲酰胺、(c1-c6)亚烷基-氧基羰基、氨基甲酸酯、磺胺、酯或磺酰基。
395、在本说明书中,除非另有说明,否则术语“独立地”意指在从多个可能的取代基中选择多于一个取代基的情况下,这些取代基可以相同或不同。
396、在本说明书中,除非另有说明,否则术语“溶剂合物”是指由溶质(例如式(i)化合物)和溶剂构成的可变化学计量的复合物。溶剂是可药用溶剂例如水;这样的溶剂可不会干扰溶质的生物活性。
397、在本说明书中,除非另有说明,否则术语“盐”是指本发明化合物的酸加成盐或碱加成盐。“盐”特别包括“可药用盐”。
398、本发明的可药用盐可通过常规化学方法从碱性或酸性部分合成。当碱性基团和酸性基团二者都存在于同一分子中时,本发明的化合物也可以形成内盐,例如两性离子分子。
399、在本说明书中,除非另有说明,否则某些化合物可以以一种或更多种特定的几何、光学、对映体、非对映体、差向异构体、立体异构、互变异构、构象或异头形式存在,包括但不限于顺式和反式形式;e-和z-形式;endo-和exo-形式;r-、s-、和内消旋(meso-)形式;d-和l-形式;d-和l-形式;(+)和(-)形式;酮式(keto-)、烯醇式(enol-)、和烯醇化物-形式;α-和β-形式;轴式(axial)和赤道式(equatorial)形式;及其组合,共同被称为“异构体”或“异构形式”。
400、例如,基团是的互变异构体。
401、术语“异构体”包括具有一个或更多个同位素取代的化合物。例如,h可以是任何同位素形式,包括但不限于1h、2h(d)和3h(t);c可以是任何同位素形式,包括但不限于12c、13c、14c;o可以是任何同位素形式,包括但不限于16o和18o等。f可以是任何同位素形式,包括但不限于19f和18f等。
402、在本说明书中,除非另有说明,否则术语“mglu7的负别构调节剂”或“mglu7的别构调节剂”还是指其可药用酸加成盐或碱加成盐、其立体化学异构形式或者其n-氧化物形式。
403、药物组合物
404、本文中所述的mglu7的别构调节剂,及其可药用的盐、溶剂合物和水合物可以与可药用的载体或稀释剂组合用于药物制剂中。合适的可药用载体包括惰性的固体填充剂或稀释剂和无菌的水性或有机溶液剂。mglu7的别构调节剂将以足以提供本文所述范围内的所期望剂量的量存在于这样的药物组合物中。本发明的化合物的配制和施用的技术可见于remington:the science and practice of pharmacy,第19版,mack publishing co.,easton,pa(1995)。
405、施用于对象的mglu7的别构调节剂的量将取决于疾病或病症的类型和严重程度以及对象的特征,例如一般健康状况、年龄、性别、体重和对药物的耐受性。技术人员将能够根据这些和其他因素确定合适的剂量。通常使用的cns药物的有效剂量是技术人员公知的。每日总剂量的范围通常为约0.05至2000mg。
406、本发明涉及提供每单位剂量约0.01至1000mg活性成分的药物组合物。该组合物可通过任何合适的途径施用。例如,以胶囊剂等形式的经口施用、以用于注射的溶液剂形式的肠胃外施用、以软膏剂或洗剂形式的表面施用、以滴眼剂形式的经眼施用、以栓剂形式的经直肠施用、以像贴剂一样的递送系统形式的鼻内或经皮施用。
407、对于经口施用,其mglu7的别构调节剂可与合适的固体或液体的载体或稀释剂组合以形成胶囊剂、片剂、丸剂、散剂、糖浆剂、溶液剂、混悬剂等。
408、片剂、丸剂、胶囊剂等包含约0.01至约99重量百分比的活性成分,以及黏合剂,例如黄蓍胶、阿拉伯胶、玉米淀粉或明胶;赋形剂,例如磷酸二钙;崩解剂,例如玉米淀粉、马铃薯淀粉、海藻酸;润滑剂例如硬脂酸镁;以及甜味剂,例如蔗糖、乳糖或糖精。当剂量单位形式为胶囊剂时,除了以上类型的物质,其还可含有液态载体,例如脂肪油。
409、多种其他物质可作为包衣存在或者为修饰剂量单位的物理形态而存在。例如,片剂可用虫胶(shellac)、糖或二者包衣。除了活性成分,糖浆剂或酏剂还可包含蔗糖作为甜味剂、甲基和对羟基苯甲酸丙酯作为防腐剂、染料和矫味剂例如樱桃或橙子矫味剂。
410、对于肠胃外施用,所公开的mglu7的别构调节剂或其盐可与无菌的水性或有机介质组合以形成可注射的溶液剂或混悬剂。例如,可使用芝麻油或花生油中的溶液剂、水性丙二醇等,以及化合物的水溶性可药用盐的水溶液。还可在甘油、液体聚乙二醇、及其在油中的混合物中制备分散体。在普通的储存和使用条件下,这些制剂包含防腐剂以防止微生物的生长。
411、除了先前描述的制剂之外,化合物还可配制为储存制剂。这样的长效制剂可例如通过皮下植入或肌内注射来施用。因此,例如,可将化合物配制为在可接受的油或离子交换树脂中的乳剂,或者配制为微溶性衍生物,例如微溶性盐。
412、优选所公开的mglu7的别构调节剂或包含这些化合物的药物制剂以单位剂型施用于哺乳动物。单位剂型可以是本领域已知的任何单位剂型,包括例如胶囊剂、iv袋剂、片剂、或药瓶(vial)。单位剂量组合物中活性成分的量是有效量且可根据所涉及的特定治疗而变化。可以理解的是,可有必要根据患者的年龄和状况对剂量进行常规改变。剂量也将取决于施用途径,其可通过多种途径,包括经口、气雾、经直肠、经皮、皮下、静脉内、肌内、腹膜内和鼻内进行。
413、合成方法
414、根据本发明的化合物,特别是根据式(i)至(v)的化合物,可通过有机合成领域中已知的方法如以下合成方案部分所述来制备。在下述所有的方案中,很好理解的是,根据化学的一般原理,在必要时使用敏感或反应性基团的保护基团。保护基团根据有机合成的标准方法来操作(green t.w.and wuts p.g.m.,(1991)protecting groups in organicsynthesis,john wiley&sons)。使用对本领域中那些技术人员来说显而易见的方法在化合物合成的方便阶段去除这些基团。方法的选择以及反应条件和其执行顺序应与式(i)至(v)化合物的制备相一致。
415、根据本发明的化合物可被表示为对映体的混合物,其可以分解成单独的纯r-或s-对映体。例如,如果需要特定的对映体,则可以通过非对称合成或通过用手性助剂衍生来制备,其中分离所得的非对映混合物并切割助剂基团以提供纯的所期望对映体。或者,当分子包含碱性官能团(例如氨基)或酸性官能团(例如羧基)时,则该解析(resolution)可通过从多种溶剂中以光学活性酸的盐分级结晶或通过文献中已知的其他方法(例如手性柱色谱)方便地进行。
416、最终产物、中间体或起始物质的解析可通过本领域已知的任何合适的方法来进行(eliel e.l.,wilen s.h.and mander l.n.(1984)stereochemistry of organiccompounds,wiley-interscience)。
417、本发明的许多杂环化合物可使用本领域公知的合成途径来制备(katrizkya.r.and.rees c.w.(1984)comprehensive heterocyclic chemistry,pergamon press)。
418、可通过使用标准技术例如萃取、色谱、再结晶和蒸馏对来自该反应的产物进行分离和纯化。
419、本发明的化合物可通过如以下方法中所公开的一般合成途径来制备。
420、在本发明的一个实施方案中,式(i)化合物可根据方案1中所示出的合成顺序来制备。可通过在存在碱(例如,如氢化钠等)的情况下,在合适的溶剂(例如如thf等)中,在合适的温度下,使对应的β-酮酯衍生物g1与卤代乙酰基衍生物进行反应来制备α,γ-二酮衍生物g2。然后,在存在催化剂(例如如酸,例如乙酸、p-甲苯磺酸等)的情况下,在合适的溶剂(例如如甲苯、乙腈等)中,在合适的温度下,中间体g2可通过与合适的苯胺衍生物g3反应而转换成n-芳基吡咯衍生物g4(参见例如bioorg.med.chem.lett.2010,20(1),189;bioorg.med.chem.lett.2008,16(23),10001)。
421、然后,吡咯衍生物g5可通过有机合成领域中已知的羰基化反应(例如但不限于vilsmeier反应)使用适合的试剂在适合的溶剂中和在合适的温度下从衍生物g4来制备(参见例如tetrahedron 2006,62,6018)。
422、最后,在存在催化剂(例如酸,例如乙酸、p-甲苯磺酸等)的情况下,在极性溶剂(例如etoh、二氧六环等)中,在合适的温度下,中间体g5可与合适的苯肼衍生物g6缩合,产生最终化合物g7(参见例如bioorg.med.chem.2010,18(1),202)。
423、
424、方案1
425、类似地,最终化合物g7可根据方案2中示出的合成顺序来制备。首先,在存在催化剂(例如如酸,例如如乙酸、对甲苯磺酸等)的情况下,在极性溶剂(例如etoh、二氧六环等)中,在合适的温度下,中间体g5可通过与肼反应而转换成中间体g8(参见例如bioorg.med.chem.lett.2004,14,1295)。然后,在存在碱(例如三乙胺、吡啶等)的情况下,在反应惰性溶剂(例如dmf或二氧六环等)中,在合适的温度下,可通过由铜络合物催化剂(例如cu(oac)2等)介导的有机合成领域中已知的方法(例如chan-lam偶联反应)来获得最终的化合物g7。
426、
427、方案2
428、在式(i)的另一个具体方面中,用于制备最终化合物g7的中间体衍生物g5可根据方案3来制备。根据方案1制备的,并且其中x代表任何种类的官能团,例如但不限于卤素、氰基、酯、醚、羧酸、羰基的中间体衍生物g10,在反应惰性溶剂(例如dmf或二氧六环等)中,在合适的温度下,可通过由钯络合物催化剂(例如pd(pph3)4、pdcl2(dppf)等)或铜络合物催化剂(例如cui、cu(oac)2等)介导的有机合成领域中技术人员已知的合适的反应,例如但不限于交叉偶联反应,例如buchwald、heck、suzuki、ullmann、stille偶联反应转换成中间体g5。
429、
430、方案3
431、类似地,最终化合物g7可根据方案4中示出的合成顺序来制备。根据方案1或2制备的,并且其中x为官能团,例如但不限于卤素、氰基、酯、醚、羧酸、羰基的中间体g11,可通过如方案3所述的合适的反应转换成最终化合物g7。
432、
433、方案4
434、在式(i)的另一个具体方面中,最终化合物g7可根据方案5来制备。根据方案1或2制备的,并且其中x为官能团,例如但不限于卤素、氰基、酯、醚、羧酸、羰基的中间体g12,可通过如方案3所述的合适的交叉偶联反应转换成最终化合物g7。
435、
436、方案5
437、在式(i)的另一个具体方面中,最终化合物g14可根据方案6来制备。根据方案1或2制备的中间体g13可在酸性条件下(例如在存在hcl的情况下)去甲基化以产生最终化合物g14。
438、
439、方案6
440、在式(i)的另一个具体方面中,最终化合物g20可根据方案7来制备。在存在碱(例如n1,n2-二甲基环己烷-1,2-二胺等)的情况下,在反应惰性溶剂(例如二氧六环等)中,在合适的温度下,中间体g17可通过由铜络合物催化剂(例如cui等)介导的在哒嗪-3(2h)-酮与2-溴吡啶之间的有机合成领域中已知的方法(例如ullmann偶联反应)来获得。然后,在存在碱(例如nah)的情况下,在合适的溶剂(例如thf)中,在合适的温度下,中间体g17可通过与1-(异氰基甲基磺酰基)-4-甲基苯g18反应而转换成2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮衍生物g19。最终化合物g20可通过方法,例如中间体g19与溴芳基(例如g20)之间的针对步骤1所述的ullmann偶联来获得。
441、
442、方案7
443、在酸性条件(例如如乙酸等)下,在极性溶剂(例如etoh、二氧六环等)中,吡咯衍生物g5可与合适的杂芳基肼衍生物g6缩合,随后在纯的条件(neat condition)和合适的温度下环化,产生最终化合物g7。
444、
445、方案8
446、在存在lewis酸(例如bbr3)的情况下可裂解甲基醚芳基g23,以产生相应的羟基芳基g24,该g24可被烷基化以产生醚化合物g25。随后可在酸性条件下用合适的杂芳基肼衍生物g6环化g25,产生最终化合物g26。
447、
448、方案9
449、实验
450、除非另有说明,否则所有起始物质均购自商业供应商,并且无需进一步纯化即可使用。
451、具体地,以下缩写可用于实施例和整个说明书中。
452、
453、
454、所有提及的盐水(brine)均指nacl的饱和水溶液。除非另有说明,否则所有温度均以℃(摄氏度)表示。除非另有说明,否则所有反应均在室温下在惰性气氛下进行。
455、大多数反应通过薄层色谱在0.25mm的merck硅胶板(60f-254)上进行监测,用uv光进行可视化。在预包装的硅胶柱(silica gel cartridge)(15-40μm,merck)上进行快速柱色谱。
456、实施例
457、实施例1:6-(3-甲氧基苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-26)
458、2-乙酰基-4-氧代戊酸乙酯
459、根据方案1步骤1:在0℃下,在2小时内向乙基-3-氧代丁酸酯(200g,1.54mol)在thf(1l)中的搅拌溶液分批添加nah(60%w/w,67.6g,1.70mol)。在30分钟之后,在1小时内添加1-氯丙烷-2-酮(156g,1.70mol),并使反应混合物温热至室温过夜。添加et2o(250ml)并随后添加盐水(500ml),并分离有机层。将水层用et2o(2×250ml)萃取两次。将有机层组合,经na2so4干燥,过滤并在减压下蒸发。将粗油状物蒸馏(126℃/14mmhg)以得到作为淡黄色油状物的标题化合物(140g,49%)。
460、1-(3-甲氧基苯基)-2,5-二甲基-1h-吡咯-3-羧酸乙酯
461、根据方案1步骤2:向2-乙酰基-4-氧代戊酸乙酯(8.00g,43.0mmol)在甲苯(140ml)中的溶液添加3-甲氧基苯胺(6.35g,51.6mmol)和acoh(0.09g,1.5mmol)。将反应混合物在用dean-stark装置回流下加热过夜,然后冷却至室温并在减压下浓缩以得到作为棕色油状物的标题化合物(11.7g,100%),将其用于下一步骤而无需任何进一步纯化。
462、4-甲酰基1-(3-甲氧基苯基)-2,5-二甲基-1h-吡咯-3-羟酸乙酯
463、根据方案1步骤3:在0℃下向pocl3(1.76g,11.5mmol)在dcm(13ml)中的搅拌溶液逐滴添加dmf(0.84g,11.5mmol)在dcm(10ml)中的溶液,同时保持温度在0℃下。在完成添加之后,将反应混合物在0℃下搅拌20分钟并使其加热至室温。然后,在0℃下将1-(3-甲氧基苯基)-2,5-二甲基-1h-吡咯-3-羧酸乙酯(2.85g,10.4mmol)在dcm(13ml)中的溶液逐滴添加至反应混合物并在该温度下搅拌1小时,并随后在室温下过夜。添加冷水并使用6m水性naoh将ph调节至10至11。将所得溶液用dcm萃取。将有机层用盐水洗涤,经mgso4干燥并在减压下浓缩以得到作为棕色固体的标题化合物(3.62g,92%),将其用于下一步骤而无需任何进一步纯化。
464、6-(3-甲氧基苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
465、根据方案1步骤4:向4-甲酰基-1-(3-甲氧基苯基)-2,5-二甲基-1h-吡咯-3-羧酸乙酯(279mg,0.93mmol)在二氧六环(3ml)中的搅拌溶液添加苯肼(103mg,0.93mmol)和acoh(278mg,4.63mmol)。将反应混合物在微波辐照下加热至160℃持续20分钟,冷却至室温,用et2o洗涤,然后过滤并干燥以得到作为白色固体的标题化合物(146mg,46%)。
466、m.p.:213-215℃;uplc-ms:rt=1.09分钟;ms m/z es+=346;1h-nmr(300mhz,dmso-d6)δ:8.34(1h,s),7.56-742(5h,m),7.35-7.29(1h,m),7.18-7.15(1h,dd),7.05-6.98(2h,m),3.82(3h,s),2.40(3h,s),2.27(3h,s).
467、实施例2:2-(2-甲氧基苯基)-5,7-二甲基-6-对甲苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-2)
468、5,7-二甲基-6-对甲苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
469、根据方案2步骤1:向4-甲酰基-2,5-二甲基-1-对甲苯基-1h-吡咯-3-羧酸乙酯(1.66g,5.82mmol)在etoh(50ml)中的搅拌溶液添加一水合肼(2.91g,58.2mmol)。将混合物在回流下搅拌过夜,冷却至室温,浓缩,过滤并干燥以得到作为白色固体的标题化合物(1.31g,89%)。2-(2-甲氧基苯基)-5,7-二甲基-6-对甲苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
470、根据方案2步骤2:向5,7-二甲基-6-对甲苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(0.20g,0.79mmol)在二氧六环(3ml)中的搅拌溶液添加1-碘-2-甲氧基苯(185mg,0.79mmol)、cui、反式-环己烷-1,2-二胺(18mg,158μmol)和k3po4(503mg,2.37mmol)。将反应混合物在110℃下加热过夜,冷却至室温并用etoac萃取。将有机层用盐水洗涤,经na2so4干燥,过滤并在减压下浓缩。使用dcm/meoh(99:1)作为洗脱液,将粗制物质通过快速色谱经硅胶进行纯化以得到作为米色固体的标题化合物(97mg,34%)。
471、m.p.:202℃;lc-ms:rt=2.83分钟;ms m/z es+=360;1h-nmr(300mhz,cdcl3)δ:8.05(1h,s),7.51(2h,d),7.35(2h,d),7.15(2h,d),7.00(2h,d),3.85(3h,s),2.55(6h,s),2.30(3h,s).
472、实施例3:2-(2-氟苯基)-5,7-二甲基-6-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-21)
473、根据方案2步骤2:向5,7-二甲基-6-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(100mg,0.42mmol)在dmf(2ml)中的搅拌溶液添加1-氟-2-碘苯(111mg,0.50mmol)、cui(40.0mg,0.21mmol)和k2co3(116mg,0.84mmol)。将反应混合物在微波辐照下在140℃下加热30min,冷却至室温,倒入水中并用dcm萃取。将有机层组合,用盐水洗涤,经na2so4干燥,过滤,并在减压下浓缩。使用dcm/etoac(95∶5)作为洗脱液,将粗制物质通过快速色谱经硅胶进行纯化以得到作为米色固体的标题化合物(57mg,41%)。
474、m.p.:226℃;uplc-ms:rt=1.05分钟;ms m/z es+=334;1h-nmr(300mhz,dmso-d6)δ:8.34(1h,s),7.69-7.55(3h,m),7.50-7.42(4h,m),7.39-7.29(2h,m),2.38(3h,s),236(3h,s),2.25(3h,s).
475、实施例4:2-(4-甲氧基苯基)-5,7-二甲基-6-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-13)
476、根据方案2步骤2:向5,7-二甲基-6-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(150mg,0.63mmol)在dmf(6ml)中的搅拌溶液添加4-甲氧基苯基硼酸(114mg,0.75mmol)、cu(oac)2(228mg,1.25mmol)和et3n(127mg,1.25mmol)。将混合物在80℃下搅拌6小时,冷却至室温,倒入nh4oh上并用etoac萃取。将有机层用盐水洗涤,经na2so4干燥,过滤,并在减压下浓缩。将粗制物质通过制备型hplc进行纯化以得到作为白色固体的标题化合物(29mg,13%)。
477、uplc-ms:rt=1.05分钟;ms m/z es+=346;1h-nmr(300mhz,dmso-d6)δ:8.32(1h,s),7.68-7.58(3h,m),7.46-7.37(4h,m),7.01(2h,d),3.80(3h,s),2.40(3h,s),2.21(3h,s).
478、实施例5:5,7-二甲基-2-苯基-6-(3-(吡咯烷-1-基)苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-101)
479、4-甲酰基-2,5-二甲基-1-(3-(吡咯烷-1-基)苯基)-1h-吡咯-3-羧酸乙酯
480、根据方案3:向1-(3-溴苯基)-4-甲酰基-2,5-二甲基-1h-吡咯-3-羧酸乙酯(1.00g,2.86mmol)在dmf(14ml)中的搅拌溶液添加吡咯烷(406mg,5.71mmol)、xantphos(248mg,0.43mmol)、pdcl2(dppf)(233mg,0.29mmol)和cs2co3(1.40g,4.28mmol)。将反应混合物在130℃下于密封管中搅拌3小时,冷却至室温,用dcm稀释,经celite过滤并在减压下浓缩。使用dcm/meoh(99:1)作为洗脱液,将粗制物质通过快速色谱经硅胶进行纯化以得到作为黄色固体的标题化合物(513mg,53%)。
481、5,7-二甲基-2-苯基-6-(3-(吡咯烷-1-基)苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
482、根据方案1步骤4:根据最终化合物1-26由4-甲酰基-2,5-二甲基-1-(3-(吡咯烷-1-基)苯基)-1h-吡咯-3-羧酸乙酯(120mg,0.35mmol)制备,并通过制备型hplc进行纯化,产生作为棕色固体的标题化合物(513mg,53%)。
483、m.p.:228-229℃;uplc-ms:rt=1.29分钟,ms m/z es+=385;1h-nmr(300mhz,dmso-d6)δ:8.32(1h,s),7.52-7.29(6h,m),6.70(1h,dd),6.55(1h,dd),6.45-6.44(1h,m),4.45-4.44(1h,m),3.27-3.25(4h,m),2.41(3h,s),2.28(3h,s),1.97-195(4h,m).
484、实施例6:6-(3-乙酰基苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-36)
485、根据方案4:向6-(3-溴苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-34,120mg,0.30mmol)在dmf(1.5ml)中的搅拌溶液添加1-(乙烯氧基)丁烷(152mg,1.52mmol)、et3n(92mg,0.91mmol)和pdcl2(dppf)(25mg,30μmol)。在氮气氛下,将反应混合物在微波辐照下在130℃下搅拌25分钟。添加1m hcl(1.5ml)并将反应混合物在室温下搅拌10分钟,并随后用dcm稀释。将有机层组合,用盐水洗涤,经na2so4干燥,过滤并在减压下浓缩。将粗制物质通过制备型hplc进行纯化以得到作为白色固体的标题化合物(15mg,14%)。
486、m.p.:202-204℃;uplc-ms:rt=0.97分钟;ms m/z es+=358;1h-nmr(300mhz,dmso-d6)δ:8.36(1h,s),8.17-8.14(1h,m),8.00(1h,s),7.83-7.73(2h,m),7.53-7.43(4h,m),7.35-7.31(1h,m),2.65(3h,s),2.40(3h,s),2.27(3h,s).
487、实施例7:6-(3-(2-甲氧基乙基氨基)苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-43)
488、根据方案4:向6-(3-溴苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-34,120mg,0.30mmol)在dmf(1ml)中的搅拌溶液添加2-甲氧基乙胺(34mg,0.46mmol)、xantphos(26mg,46μmol)、pdcl2(dppf)(25mg,30μmol)和cs2co3(149mg,0.46mmol)。将混合物在130℃下于密封管中搅拌4小时,冷却至室温,用dcm稀释,经celite过滤并在减压下浓缩。将粗制物质通过制备型hplc进行纯化以得到作为棕色固体的标题化合物(15mg,13%)。
489、m.p.:116-119℃;uplc-ms:rt=1.04分钟;ms m/z es+=389;1h-nmr(300mhz,dmso-d6)δ:8.31(1h,s),7.52-744(4h,m),7.34-7.25(2h,m),6.80(1h,d),6.53-6.49(2h,m),6.07(1h,t),3.50(2h,t),3.33-3.22(5h,m),2.41(3h,s),2.27(3h,s).
490、实施例8:6-(3-羟基苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-51)
491、根据方案4:在0℃下向6-(3-甲氧基苯基)-5,7-二甲基-2-苯基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-26,实施例1,30mg,87μmol)在dcm(1ml)中的搅拌溶液逐滴添加bbr3(0.17ml,0.17mmol)。将混合物在室温下搅拌1小时,用dcm稀释并用水缓慢水解。将有机层用水和nh4cl洗涤,经mgso4干燥,过滤并在减压下浓缩。将粗制物质用et2o洗涤,过滤并在减压下干燥以得到作为米色固体的标题化合物(12mg,42%)。
492、m.p.:252-254℃;uplc-ms:rt=0.91分钟;ms m/z es+=332;1h-nmr(300mhz,dmso-d6)δ:10.05(1h,s),8.32(1h,s),7.52-7.39(5h,m),7.34-7.29(1h,m),6.98(1h,dd),6.81(1h,d),6.75(1h,s),2.39(3h,s),2.25(3h,s).
493、实施例9:2-(4-(氨基甲基)苯基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-88)
494、4-(6-(3-甲氧基苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苄基氨基甲酸叔丁酯
495、根据方案2步骤2:按照最终化合物1-13由6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(140mg,0.52mmol)、4-((叔-丁氧基羰基氨基)甲基)苯基硼酸(157mg,0.62mmol)、cu(oac)2(103mg,0.52mmol)和k2co3(86mg,0.62mmol)制备,并使用dcm/meoh(99∶1)作为洗脱液,通过快速色谱经硅胶进行纯化以得到作为棕色固体的标题化合物(400mg,89%)。
496、2-(4-(氨基甲基)苯基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
497、根据方案5:向4-(6-(3-甲氧基苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苄基氨基甲酸叔丁酯(100mg,0.21mmol)在dcm(2ml)中的搅拌溶液逐滴添加三氟乙酸(288mg,2.53mmol)。将反应混合物在室温下搅拌4小时,用dcm和水稀释。将有机层用水和nahco3洗涤,经mgso4干燥,过滤并在减压下浓缩。使用dcm/meoh(95∶5)作为洗脱液,将粗制物质通过快速色谱经硅胶进行纯化并在et2o中进行再结晶以得到作为棕色固体的标题化合物(7mg,9%)。
498、m.p.:145-155℃;uplc-ms:rt=0.72分钟;ms m/z es+=375;1h-nmr(300mhz,dmso-d6)δ:8.33(1h,s),7.57-7.41(5h,m),7.16(1h,dd),7.03-6.98(2h,m),3.87(2h,s),3.82(3h,s),2.40(3h,s),2.27(3h,s).
499、实施例10:6-(3-甲氧基苯基)-5,7-二甲基-2-(4-((甲基氨基)甲基)苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-109)
500、4-(6-(3-甲氧基苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苄基(甲基)氨基甲酸叔丁酯
501、根据方案5:向4-(6-(3-甲氧基苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苄基氨基甲酸叔丁酯(235mg,0.49mmol)在dmf(2ml)中的搅拌溶液分批添加碘甲烷(211mg,1.49mmol)和nah(60%w/w,59mg,1.49mmol)。将反应混合物在室温下搅拌3小时并小心添加水。将反应混合物用dcm萃取,并将组合的有机层经mgso4干燥,过滤,并在减压下浓缩以得到作为棕色固体的标题化合物(300mg,99%),将其用于下一步骤而无需任何进一步纯化。
502、6-(3-甲氧基苯基)-5,7-二甲基-2-(4-((甲基氨基)甲基)苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
503、根据方案5:按照最终化合物1-88由4-(6-(3-甲氧基苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苄基(甲基)氨基甲酸叔丁酯(300mg,0.61mmol)制备,通过快速色谱经硅胶使用dcm/meoh/nh4oh(95:5:0.1)作为洗脱液进行纯化,并在et2o中进行再结晶,产生作为淡粉色固体的标题化合物(34mg,14%)。
504、m.p.:150-154℃;uplc-ms:rt=0.73分钟;ms m/z es+=389;1h-nmr(300mhz,dmso-d6)δ:8.33(1h,s),7.56-7.39(5h,m),7.16(1h,dd),7.03-6.98(2h,m),3.82(3h,s),3.79(2h,s),240(3h,s),2.36(3h,s),2.27(3h,s).
505、实施例11:6-([1,1’-联苯基]-3-基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-76)
506、6-(3-溴苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
507、根据方案1步骤4:按照最终化合物1-26由1-(3-溴苯基)-4-甲酰基-2,5-二甲基-1h-吡咯-3-羧酸乙酯(2.00g,5.71mmol)、2-肼基吡啶(1.25g,11.4mmol)和acoh(1.72g,28.6mmol)制备,然后通过快速色谱用dcm/meoh/nh4oh(94∶6∶1)作为洗脱液进行纯化,产生作为米色固体的标题化合物(1.45g,64%)。
508、6-([1,1’-联苯基]-3-基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
509、根据方案4:向6-(3-溴苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(80mg,0.20mmol)在dme/水(8:2,1.6ml)中的搅拌溶液添加苯基硼酸(62mg,0.51mmol)、k3po4(107mg,0.51mmol)和pdcl2(dppf)(15mg,20μmol)。将混合物在氮气氛下在130℃下于密封管中搅拌45分钟,冷却至室温,用dcm稀释,经celite过滤,并在减压下浓缩。将粗制物质通过快速色谱经硅胶使用dcm/meoh(98∶2)作为洗脱液进行纯化以得到作为灰色固体的标题化合物(21mg,26%)。m.p.:106-109℃;uplc-ms:rt=1.06分钟;ms m/z es+=393;1h-nmr(300mhz,dmso-d6)δ:8.58(1h,dd),8.33(1h,s),7.97-7.89(2h,m),7.82-7.69(4h,m),7.55-7.39(6h,m),2.43(3h,s),2.32(3h,s).
510、实施例12:6-(3-(二乙基氨基)苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-100)
511、6-(3-氨基苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
512、根据方案4:向5,7-二甲基-6-(3-硝基苯基)-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(1.10g,3.04mmol)在dcm(12ml)中的搅拌溶液逐滴添加锌粉(2.00g,30.4mmol)和acoh(1.83g,30.4mmol)。将反应混合物在室温下搅拌6小时,经celite过滤并在减压下浓缩。将粗制剩余物用et2o洗涤并干燥以获得作为棕色固体的标题化合物(810mg,80%),将其用于下一步骤而无需任何进一步纯化。
513、6-(3-(二乙基氨基)苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
514、根据方案4:在0℃下向6-(3-氨基苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(100mg,0.30mmol)在acn(4ml)中的搅拌溶液添加乙醛(133mg,3.02mmol)和acoh(181mg,3.02mmol)。将反应混合物在0℃下搅拌20分钟,然后添加nabh(oac)3(192mg,0.91mmol)。将混合物在室温下搅拌1小时,倒入水中并用dcm萃取。将有机层用nahco3和nh4cl洗涤,经mgso4干燥,过滤并在减压下浓缩。将粗制物质通过快速色谱经硅胶使用dcm/meoh(98:2)作为洗脱液进行纯化。将所得固体用et2o洗涤以提供作为橙色固体的标题化合物(26mg,22%)。
515、m.p.<85℃;uplc-ms:rt=0.98分钟;ms m/z es+=388;1h-nmr(300mhz,dmso-d6)δ:8.59-8.54(1h,m),8.29(1h,s),7.98-7.90(1h,m),7.51-7.46(1h,m),7.45-7.39(1h,m),7.39-7.31(1h,m),6.82(1h,dd),6.60-6.55(1h,m),6.52(1h,dd),3.37(4h,q),240(3h,s),2.28(3h,s),1.10(6h,t).
516、实施例13:2-(6-羟基吡啶-3-基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-131)
517、根据方案6:向6-(3-甲氧基苯基)-2-(6-甲氧基吡啶-3-基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(60mg,159μmol)在thf(0.5ml)中的溶液逐滴添加6m hcl(775μl)和nai(23.9mg,159μmol)。将混合物在60℃下搅拌5小时。将溶剂在减压下蒸发。将剩余物用1m nahco3水溶液碱化并用dcm萃取。将有机层经mgso4干燥,过滤并在减压下浓缩以得到红色液体。将粗制品通过制备型hplc进行纯化以得到作为橙色油状物的标题化合物(19.4mg,34%)。
518、m.p.:207-209℃;uplc-ms:rt=0.79分钟;ms m/z es+=363;1h-nmr(300mhz,cdcl3)δ:8.05(1h,s),7.95-7.88(2h,m),7.51-7.43(1h,m),7.07(1h,dd),6.80(1h,dd),675-6.66(2h,m),3.88(3h,s),2.51(3h,s),2.28(3h,s).
519、实施例14:2-(4-(2-羟基丙烷-2-基)苯基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-135)
520、根据方案5:在0℃下向2-(4-乙酰基苯基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(75mg,0.19mmol)在thf(1.5ml)中的溶液添加甲基溴化镁(0.19ml,0.58mmol)。将混合物在0℃下搅拌30分钟。然后将混合物用dcm稀释并用nh4cl水溶液猝灭。将混合物用nahco3、并随后用nh4cl洗涤。将有机层经mgso4干燥,过滤并在减压下浓缩以得到黄色固体。将粗制固体通过快速色谱经硅胶使用dcm/meoh(98/2)作为洗脱液进行纯化,然后用dcm/meoh(1/9)研磨并在减压下浓缩以得到作为米色固体的标题化合物(16mg,20%)。
521、m.p.:103-108℃;uplc-ms:rt=1.01分钟;ms m/z es+=404;1h-nmr(300mhz,dmso-d6)δ:8.32(1h,s),7.59-7.49(3h,m),7.42-7.39(2h,m),7.18-7.15(2h,m),7.04-6.98(2h,m),5.08(1h,s),3.82(3h,s),240(1h,s),2.26(1h,s),1.46(6h,s).
522、实施例15:2-(4-(1-羟基乙基)苯基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-138)
523、根据方案5:在0℃下向2-(4-乙酰基苯基)-6-(3-甲氧基苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(75mg,0.19mmol)在thf(2ml)中的溶液添加nabh4(7mg,0.19mmol)。将混合物在室温下搅拌45分钟。将混合物用dcm稀释,用nh4cl猝灭并用nahco3洗涤。将有机层经mgso4干燥,过滤并在减压下浓缩以得到米色固体。将粗制固体通过快速色谱经硅胶使用dcm/meoh(98/2)作为洗脱液进行纯化以得到固体。将所得固体用et2o洗涤以得到作为米色固体的标题化合物(40mg,53%)。
524、m.p.:192-195℃;uplc-ms:rt=0.97分钟;ms m/z es+=390;1h-nmr(300mhz,dmso-d6)δ:8.32(1h,d),7.58-7.50(1h,m),7.45-7.37(4h,m),7.16(1h,dd),7.04-6.97(2h,m),5.22(1h,d),4.81-4.73(1h,m),3.82(3h,s),2.40(3h,s),2.26(3h,s),1.35(3h,d).
525、实施例16:6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(4-(吡咯烷-1-基)苯基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-168)
526、根据方案5:在氩气下,在密封管中,向6-(3-(氮杂环丁烷-1-基)苯基)-2-(4-溴苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(120mg,0.27mmol)在dmf(5ml)中的溶液添加吡咯烷(56mg,0.80mmol)、xantphos(15mg,27μmol)和cs2co3(0.13g,0.40mmol)。将混合物在氩气下脱气10分钟并向混合物添加pdcl2(dppf)(10mg,13μmol)。将混合物再次脱气5分钟并随后在130℃下搅拌16小时。在添加水(15ml)之后,将反应混合物用etoac(4×25ml)萃取。将有机层组合,用盐水洗涤,经na2so4干燥并在减压下浓缩。将粗制物质通过色谱经二氧化硅使用己烷/etoac(70/30)作为洗脱液进行纯化以得到作为黄色固体的标题化合物(22mg,19%)。
527、uplc-ms:rt=3.61分钟;ms m/z es+=440;1h-nmr(300mhz,cdcl3)δ:8.10(1h,s),7.40-7.30(3h,m),6.60(2h,d),6.55-6.45(2h,m),6.20-6.19(1h,m),3.90(4h,t),3.30(4h,t),2.50(3h,s),2.45-2.35(2h,m),2.30(3h,s),2.10-1.90(4h,m).
528、实施例17:6-(3-(氮杂环丁烷-1-基)苯基)-2-(4-(2-羟基乙基)苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-169)
529、根据方案5:将2-(4-(6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-1-氧代-1h-吡咯并[3,4-d]哒嗪-2(6h)-基)苯基)乙酸乙酯(100mg,0.22mmol)溶解于et2o(4ml)中。在氩气气氛下向溶液中逐滴添加libh4并随后逐滴添加meoh(0.1ml)。在完成添加之后,将混合物在室温下搅拌1小时并将反应混合物在减压下蒸发。向剩余物添加nh4cl饱和溶液并将反应混合物用etoac萃取。将有机层用盐水洗涤,经na2so4干燥并在减压下浓缩以得到油状物。将粗制油状物通过色谱经二氧化硅使用dcm/meoh作为洗脱液进行纯化以得到标题化合物(20mg,22%)。
530、uplc-ms:rt=2.96分钟;ms m/z es+=415;1h-nmr(400mhz,cdcl3)δ:8.10(1h,s),7.50(2h,d),7.40-7.30(3h,m),6.60-6.50(2h,m),6.20-6.19(1h,m),4.00-3.80(6h,m),3.00-2.80(2h,t),2.50(3h,s),2.45-2.35(2h,m),2.30(3h,s).
531、实施例18:6-(3-(氮杂环丁烷-1-基)苯基)-2-(4-(2-羟基丙烷-2-基)苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-170)
532、根据方案5:将2-(4-乙酰基苯基)-6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(200mg,0.48mmol)溶解于无水thf(5ml)中。在将溶液冷却至-30℃之后,向溶液逐滴添加在et2o(0.242ml,0.727mmol)中的甲基碘化镁3m,并将反应混合物在-30℃下搅拌15分钟。然后将混合物温热至室温并搅拌30分钟。将反应混合物用nh4cl水溶液猝灭并将水相用etoac(3×25ml)萃取。将有机层组合,用水(2×10ml)洗涤,经na2so4干燥并在减压下浓缩。将粗制产物通过快速柱色谱经硅胶使用己烷/etoac(75/25)进行纯化以得到作为黄色固体的标题化合物(40mg,19%)。
533、uplc-ms:rt=1.27分钟;ms m/z es+=422;1h-nmr(400mhz,cdcl3)δ:8.07(1h,s),7.60(4h,s),7.37-7.33(1h,m),6.57-6.52(2h,m),6.20-6.19(1h,m),3.90(4h,t),2.50(3h,s),2.45-2.42(2h,m),2.30(3h,s),1.60(6h,s).
534、实施例19:6-(3-(氮杂环丁烷-1-基)苯基)-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-188)
535、2-(吡啶-2-基)哒嗪-3(2h)-酮
536、根据方案7步骤1:按照最终化合物1-2,方案2步骤2,由在二氧六环(10ml)中的cui(99mg,0.52mmol)和n1,n2-二甲基环己烷-1,2-二胺(111mg,0.78mmol)、k3po4(1.10g,5.20mmol)、2-溴吡啶(0.25ml,2.60mmol)、哒嗪-3(2h)-酮(250mg,2.60mmol)进行制备以得到作为橙色油状物的标题化合物(300mg,67%)。
537、2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
538、根据方案7步骤2:在0℃下向nah(520mg,13.0mmol)在thf(15ml)中的溶液添加2-(吡啶-2-基)哒嗪-3(2h)-酮(750mg,4.33mmol)和1-(异氰基甲基磺酰基)-4-甲基苯(930mg,4.76mmol)在thf中的溶液。将反应混合物在室温下搅拌12小时。然后将溶液用水小心猝灭。在溶剂蒸发之后,将所得黑色固体用dcm和meoh处理,并过滤混合物。将溶剂在减压下去除以得到黑色固体,将该黑色固体通过快速色谱经硅胶使用dcm/meoh(95:5)作为洗脱液进行纯化以得到作为米白色固体的标题化合物(340mg,37%)。
539、6-(3-(氮杂环丁烷-1-基)苯基)-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
540、根据方案7步骤3:按照最终化合物1-2,方案2步骤2,由在二氧六环(2ml)中的cui(17.9mg,94μmol)和n1,n2-二甲基环己烷-1,2-二胺(20.1mg,141μmol)、k3po4(200mg,0.94mmol)、1-(3-溴苯基)氮杂环丁烷(100mg,0.47mmol)、2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(100mg,0.47mmol)进行制备以得到作为灰白色固体的标题化合物(18mg,11%)。
541、m.p.:190-192℃;uplc-ms:rt=0.84分钟;ms m/z es+=345;1h-nmr(300mhz,cdcl3)δ:8.60(1h,s),8.21(1h,s),7.91-7.62(3h,m),7.38(1h,d),7.28-7.18(2h,m),6.78-6.71(1h,m),6.43-6.37(2h,m),3.88(4h,t),2.35(2h,q).
542、实施例20:6-(3-(氮杂环丁烷-1-基)苯基)-2-(4-(2-氟乙基)苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-189)
543、根据方案5:在氮气下,在-78℃下,向dast试剂(128μl,0.96mmol)在dcm(5ml)中的溶液逐滴添加6-(3-(氮杂环丁烷-1-基)苯基)-2-(4-(2-羟基乙基)苯基)-5,7-二甲基-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(200mg,0.48mmol)在dcm(33ml)中的溶液。将反应混合物在-78℃下搅拌1小时,在室温下搅拌30分钟。将混合物倒入冰水,并将水层用dcm/meoh萃取三次。将有机层组合,经mgso4干燥并在减压下浓缩。将粗制剩余物通过制备型hplc纯化以得到作为白色固体的标题化合物(10mg,5%)。uplc-ms:rt=0.84分钟;ms m/z es+=345;1h-nmr(300mhz,cdcl3)δ:8.06(1h,s),7.54(2h,d),7.37-7.26(3h,m),6.56(2h,t),6.20(1h,s),4.41(1h,t),4.55(1h,t),3.93(4h,t),3.09(1h,t),3.02(1h,t),2.51(3h,s),2.41(1h,t),2.28(3h,s).
544、实施例21:5,7-二甲基-6-(1-甲基-1h-吲哚-6-基)-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-96)
545、根据方案4:将6-(1h-吲哚-6-基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(44mg,0.124mmol)和nah(4.46mg,186μmol)在氯仿(0.5ml)中的混合物在室温下搅拌30分钟。然后逐滴添加碘甲烷(9.25μl,149μmol),并将溶液在室温下搅拌过夜。将反应混合物用水猝灭并用dcm稀释,并向混合物添加nahco3。将有机层分离,经mgso4干燥,过滤并在减压下蒸发以得到棕色固体。将粗制固体通过制备型lc纯化以得到作为黑色油状物的标题化合物(4.2mg,9%)。uplc-ms:rt=0.94分钟;ms m/z es+=370;1h-nmr(300mhz,cdcl3)δ:8.69-8.63(1h,m),8.16(1h,s),7.85-7.70(3h,m),7.29-7.18(3h,m),6.93(1h,dd),6.61(1h,dd),3.84(3h,s),2.50(3h,s),2.27(3h,s).
546、实施例22:6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-102)
547、(e)-乙基1-(3-溴苯基)-2,5-二甲基-4-((2-(吡啶-2-基)亚肼基)甲基)-1h-吡咯-3-羧酸酯
548、根据方案8,步骤1:向1-(3-溴苯基)-4-甲酰基-2,5-二甲基-1h-吡咯-3-羧酸乙酯(12.0g,34.3mmol)在二氧六环(150ml)中的溶液添加2-肼基吡啶(4.11g,37.7mmol)和乙酸(14.4g,240mmol,13.8ml)。使所得混合物回流2小时。然后,将溶剂在减压下蒸发并添加etoac(200ml)。将有机层用nahco3(水性15%)(75ml)洗涤,经na2so4干燥,并在减压下浓缩。将所得固体用己烷处理以获得(e)-乙基1-(3-溴苯基)-2,5-二甲基-4-((2-(吡啶-2-基)亚肼基)甲基)-1h-吡咯-3-羧酸酯(14g,88%)。
549、lc-ms:rt=1.29分钟;[m+3h]+m/z:443;1h nmr(500mhz,dmso-d6)δ:8.59(1h,s),8.09(1h,d),7.78(1h,d),7.70(1h,s),7.52(2h,m),7.39(1h,d),7.00(1h,d),6.65(1h,t),4.23(2h,q),2.22(3h,s),2.20(3h,s),1.19(3h,t).
550、6-(3-溴苯基)-5,7-二甲基-2-(吡啶-2-基)-1h,2h,6h-吡咯并[3,4-d]哒嗪-1-酮
551、根据方案8,步骤2:在油浴中将(e)-乙基1-(3-溴苯基)-2,5-二甲基-4-((2-(吡啶-2-基)亚肼基)甲基)-1h-吡咯-3-羧酸酯(12.0g,27.2mmol)在165至170℃下加热2小时以获得6-(3-溴苯基)-5,7-二甲基-2-(吡啶-2-基)-1h,2h,6h-吡咯并[3,4-d]哒嗪-1-酮(10.0g,88.4%)。将原产物不经另外的纯化使用。
552、lc-ms:rt=1.38分钟,[m+3h]+m/z:397;1h nmr(400mhz,dmso-d6)δ:8.57(1h,d),8.31(1h,s),7.94(1h,t),7.81(2h,m),7.59(1h,t),7.51(2h,m),742(1h,t),2.39(3h,s),2.26(3h,s).
553、6-(3-(氮杂环丁烷1-基)苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮
554、根据方案4:将6-(3-溴苯基)-5,7-二甲基-2-(吡啶-2-基)-1h,2h,6h-吡咯并[3,4-d]哒嗪-1-酮(11.0g,27.8mmol)、盐酸氮杂环丁烷(5.21g,55.7mmol)、xantphos(1.61g,2.78mmol)、pd(dppf)cl2*dcm(2.27g,2.78mmol)和碳酸铯(31.7g,97.4mmol)在dmf(200ml)中的混合物在130℃下搅拌5小时。然后将混合物用dcm(100ml)稀释并通过硅垫(silicapad)过滤。将滤液在减压下浓缩以得到作为黑色固体的6-(3-(氮杂环丁烷-1-基)苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(11.0g,60%纯度lc/ms,17.8mmol,64%产率)。将粗制固体溶解于etoac(200ml)中、用水(50ml)洗涤,并添加si-硫醇(1g)。将所得悬液在室温下搅拌8小时;将清除剂(scavenger)滤除,并将母液在减压下浓缩。将所得剩余物通过快速色谱(正相,chcl3/mtbe作为洗脱液)纯化以产生4.4g纯度为95%的产物。之后从乙腈结晶、随后从甲苯结晶,并最后用乙腈结晶,得到1.7g。
555、lc-ms:rt=1.37分钟,[m+h]+m/z:372;1h nmr(500mhz,dms-d6)δ:8.56(1h,d),8.28(1h,s),7.93(1h,t),7.48(1h,d),7.41(1h,m),7.37(1h,t),6.63(1h,d),6.57(1h,d),6.37(1h,s),3.85(4h,t),2.39(3h,s),2.32(2h,t),2.26(3h,s).
556、实施例23:6-(2-氯-3-环丙氧基苯基)-5,7-二甲基-2-(嘧啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-215)
557、1-(2-氯-3-羟基-苯基)-4-甲酰基-2,5-二甲基-吡咯-3-羧酸乙酯
558、根据方案9,步骤1:向1-(2-氯-3-甲氧基-苯基)-4-甲酰基-2,5-二甲基-吡咯-3-羧酸乙酯(77.0mg,0.23mmol)在dcm(1ml)中的冷溶液添加bbr3(1m在dcm中的溶液,8ml)。将反应混合物在冰浴上搅拌3小时并随后倒入nahco3的饱和溶液中。将产物用dcm(3×30ml)萃取。将组合的有机萃取物用盐水(45ml)洗涤,经na2so4干燥,过滤并蒸发以得到作为浅棕色固体的标题化合物(60mg)。将粗制产物用于下一步骤而无需任何进一步纯化。
559、uplc-ms/uv(2分钟,低ph):rt=1.04分钟,m/z=322[m+h]+.
560、1-[2-氯-3-(环丙氧基)苯基]-4-甲酰基-2,5-二甲基-吡咯-3-羧酸乙酯
561、根据方案9,步骤2:将1-(2-氯-3-羟基-苯基)-4-甲酰基-2,5-二甲基-吡咯-3-羧酸乙酯(60.0mg,185μmol)、溴环丙烷(67.0mg,554μmol)和碳酸铯(120mg,369μmol)混悬于dmf(0.6ml)中。在170℃下将反应混合物暴露于微波辐照6小时。添加水(15ml)并用etoac(3×15ml)萃取。将组合的有机层用盐水(15ml)洗涤,经na2so4干燥,过滤并蒸发。将粗制品通过fcc(interchym系统,4g 15μm sio2柱,弱洗脱液:环己烷,强洗脱液:环己烷/etoac=1/1,0%至60%的强洗脱液)纯化以得到作为黄色油状物的标题化合物(26mg,纯度约80%)。
562、uplc-ms/uv(2分钟,低ph):rt=1.32分钟,m/z=362/364[m+h]+.
563、6-[2-氯-3-(环丙氧基)苯基]-5,7-二甲基-3-嘧啶-2-基-吡咯并[3,4-d]哒嗪-4-酮
564、根据方案9,步骤3:将1-[2-氯-3-(环丙氧基)苯基]-4-甲酰基-2,5-二甲基-吡咯-3-羧酸乙酯(26.0mg,71.9μmol)和嘧啶-2-基-肼(8.70mg,79.0μmol)溶解于二氧六环(300μl)中并添加乙酸(41μl,719μmol)。在160℃下将反应混合物暴露于mw辐照(biotage)6小时。将反应混合物用饱和的nahco3(15ml)碱化并用etoac(3×15ml)萃取。将有机层用盐水(20ml)洗涤,经na2so4干燥,过滤并蒸发直到干燥。将粗制品通过制备型hplc纯化以得到作为白色固体的标题化合物(14mg)。
565、m.p.:228℃;uplc-ms/uv(8分钟,高ph):rt=4.16分钟,m/z=408/410[m+h]+;1hnmr(300mhz,dmso-d6)δ:8.96(2h,d),8.31(1h,s),7.72-7.66(1h,m),7.65-7.57(2h,m),7.27-7.20(1h,m),4.12-4.03(1h,m),2.28(3h,m),2.18(3h,s),0.93-0.84(2h,m),0.83-0.74(2h,m).
566、实施例24:6-(3-(2h-1,2,3-三唑-2-基)苯基)-5,7-二甲基-2-(吡啶-2-基)-2,6-二氢-1h-吡咯并[3,4-d]哒嗪-1-酮(最终化合物1-199)
567、4-甲酰基-2,5-二甲基-1-[3-(三唑-2-基)苯基]吡咯-3-羧酸乙酯
568、根据方案3:在氩气气氛下将1-(3-溴苯基)-4-甲酰基-2,5-二甲基-吡咯-3-羧酸乙酯(440mg,1.26mmol)、2h-三唑(130mg,1.88mol)、k3po4(800mg,3.77mmol)和2-(二-叔丁基膦基)-2′,4′,6′-三异丙基-3,6-二甲氧基-1,1′-联苯基(60.9mg,0.13mmol)混悬于甲苯(7ml)中。用氩气使悬液鼓泡10分钟并添加tbubrettphos pd g3(53.7g,0.06mmol)。将小瓶密封并在130℃下搅拌反应混合物。在4小时之后,将反应混合物冷却至室温并添加etoac(20ml)和水(50ml)。将层分离并将产物用etoac(2×30ml)萃取。将有机层组合,用盐水(40ml)洗涤,经na2so4干燥,过滤并蒸发。将粗制品使用fcc(interchym系统,12g 15μm sio2柱,弱洗脱液∶环己烷,强洗脱液∶环己烷/etoac=1/1,0%至50%的强洗脱液)纯化以得到作为黄色油状物的标题化合物(276mg)。
569、uplc-ms/uv(2分钟,高ph):rt=1.20分钟,m/z=339.0[m+h]+.
570、5,7-二甲基-3-(2-吡啶基)-6-[3-(三唑-2-基)苯基]吡咯并[3,4-d]哒嗪-4-酮
571、根据方案1步骤4:按照最终化合物1-26,由4-甲酰基-2,5-二甲基-1-[3-(三唑-2-基)苯基]吡咯-3-羧酸乙酯进行制备,并通过制备型hplc进行纯化,产生作为白色固体的标题化合物。
572、m.p.:173℃;uplc-ms/uv(8分钟,高ph):rt=3.97分钟;ms m/z es+=384;1h nmr(500mhz,dmso-d6)δ:8.59-8.55(1h,m),8.33(1h,s),8.28-8.24(1h,m),8.21(2h,s),8.06(1h,s),7.95(1h,dt),7.85(1h,t),7.56-7.53(1h,m),7.51(1h,d),746-7.41(1h,m),2.43(3h,s),2.32(3h,s).
573、下表中的化合物已根据与前述实施例1至24相同的方法合成,如在表示为“exp.nr”的列中所示。在实施例中已经举例说明了用星号表示的化合物。
574、表1:根据实施例制备的化合物。
575、
576、
577、
578、
579、
580、
581、
582、
583、
584、
585、
586、
587、
588、
589、
590、
591、
592、
593、
594、物理化学数据
595、熔点:
596、a)在buchi b-540仪器上进行熔点确定。
597、b)dsc分析
598、在配备有冷藏冷却系统的mettler toledo dsc 822e热量计上收集dsc数据。将样品置于覆盖有针孔穿孔盖(pin-hole punched lid)的铝制dsc盘中。将样品室(samplecell)在25至350℃的温度范围内以10℃/分钟的速率加热。对样品维持50ml/分钟的氮气吹扫。熔点以熔化起始温度的整数表示。
599、uplc-ms方法:
600、方法1:
601、采用以下条件在waters acquity uplc上记录uplc-ms:
602、在来自waters的beh-c18柱(1.7μm,2.1×50mm)上以0.8ml/分钟的流量进行反相hplc。使用的梯度条件为:90% a(水+0.1%甲酸),10% b(acn+0.1%甲酸)至1.3分钟时100% b,保持直到1.7分钟,并在1.8分钟时平衡至初始条件直至2.0分钟。注入体积5μl。使用es ms检测器,在正和负两种电离模式下采集。
603、方法2:
604、采用以下条件在waters acquity uplc上记录uplc-ms:
605、在来自waters的hss t3柱(1.8μm,2.1×50mm)上以0.8ml/分钟的流量进行反相hplc。使用的梯度条件为:98% a(水+0.1%甲酸),2%b(acn+0.1%甲酸)至1.3分钟时70%b,然后在1.35分钟时90%b,保持直到1.75分钟,并在1.8分钟时平衡至初始条件直至2.0分钟。注入体积5μl。使用es ms检测器,在正和负两种电离模式下采集。
606、方法5:
607、waters acquity uplc连同sqd质谱仪系统;高ph方法(2分钟)
608、在来自acquity的beh-c18柱(1.7μm,2.1×50mm)上以0.9ml/分钟的流量进行反相hplc。使用的梯度条件为:97% a(水+0.05%氨),3%b(acn+0.03%氨)至1.50分钟时97%b,保持直到1.90分钟,并在1.91分钟时平衡至初始条件直至2.0分钟。注入体积2μl。使用esms检测器,在正和负两种电离模式下采集。
609、方法6:
610、waters acquity uplc连同sqd质谱仪系统;低ph方法(2分钟)
611、在来自acquity的beh-c18柱(1.7μm,2.1×50mm)上以0.9ml/分钟的流量进行反相hplc。使用的梯度条件为:97% a(水+0.1%甲酸),3%b(acn+0.1%甲酸)至1.50分钟时97%b,保持直到1.90分钟,并在1.91分钟时平衡至初始条件直至2.0分钟。注入体积2μl。使用es ms检测器,在正和负两种电离模式下采集。
612、方法7:
613、waters acquity uplc连同sqd质谱仪系统;高ph方法(8分钟)
614、在来自acquity的beh-c18柱(1.7μm,2.1×100mm)上以0.6ml/分钟的流量进行反相hplc。使用的梯度条件为:97% a(水+0.05%氨),3%b(acn+0.05%氨)至7.0分钟时97%b,保持直到7.50分钟,并在7.6分钟时平衡至初始条件直至8.0分钟。注入体积2μl。使用es ms检测器,在正和负两种电离模式下采集。
615、方法8:
616、waters acquity uplc连同sqd质谱仪系统;低ph方法(8分钟)
617、在来自acquity的beh-c18柱(1.7μm,2.1×100mm)上以0.6ml/分钟的流量进行反相hplc。使用的梯度条件为:97% a(水+0.1%甲酸),3%b(acn+0.1%甲酸)至7.0分钟时97%b,保持直到7.50分钟,并在7.6分钟时平衡至初始条件直至8.0分钟。注入体积2μl。使用esms检测器,在正和负两种电离模式下采集。
618、lc-ms方法:
619、方法3:
620、通过以下条件在waters micromass zq 2996系统上记录lc-ms:
621、在来自agilent的zorbax sb-c18柱(1.8μm,4.6×30mm)上以1.5ml/分钟的流量进行反相hplc。使用的梯度条件为:90% a(水+0.05%甲酸),10% b(acn+0.05%甲酸)至3.5分钟时100% b,保持直到3.7分钟,并在3.8分钟时平衡至初始条件直至4.5分钟。注入体积5至20μl。使用es ms检测器,在正和负两种电离模式下采集。对于正和负两种电离模式,锥孔电压(cone voltage)均为30v。
622、方法4:
623、通过以下条件在agilent model 1200系列系统上记录lc-ms:
624、在来自agilent的atlantis d c18柱(3μm,50×3mm)上以1.2ml/分钟的流量进行反相hplc。使用的梯度条件为:95% a(水+0.1%甲酸),5%b(acn+0.1%甲酸)至3.5分钟时100%b,保持直到3.8分钟,并在3.9分钟时平衡至初始条件直至4.5分钟。注入体积5μl。使用es ms检测器,在正和负两种电离模式下采集。对于正和负两种电离模式,锥孔电压均为30v。
625、方法9:
626、通过以下条件在agilent technologies 1260infinity lc/msd系统上用dad\elsd alltech 3300和agilent lc\msd g6120b质谱仪记录lc-ms:
627、在来自agilent的poroshell 120sb-c18柱(2.7μm,4.6×30mm)与uhplc guardinfinity lab poroshell 120sb-c18柱(2.7μm,4.6×5mm)上以3ml/分钟的流量和在60℃的温度下进行反相uhplc。使用的梯度条件为:1% a(acn:水(99:1%)+0.1%甲酸),99% b(水+0.1%甲酸)至1.5分钟时100% a,保持直到2.2分钟,并在2.21分钟时平衡至初始条件。注入体积0.5μl。使用es ms检测器,在正和负两种电离模式下采集。
628、制备型hplc的纯化:
629、在agilent 1290infinity ii系列制备型hplc系统(1290infinity ii二元泵、1260infinity ii二极管阵列检测器、lc/msd质量检测器)、waters sunfire(c18,19×100mm,5μm)或waters xbridge(c18,19×100mm,5μm)柱上,使用h2o+0.1%甲酸或h2o+0.1%氨(在水中的25%氨)和acn作为洗脱液进行纯化。所使用的梯度覆盖的范围为10% acn至100% acn。
630、nmr:
631、在bruker avance(400mhz,300mhz)或varian 400mhz光谱仪上记录1h nmr谱。化学位移以百万分之一(ppm,δ单位)表示。分裂模式(splitting pattern)描述了明显的多重性并被命名为s(单峰)、d(双重峰)、t(三重峰)、q(四重峰)、m(多重峰)、br(宽峰)。
632、在配备有rt 5mm bbi探头(probe)的bruker dpx 300mhz、配备有rt 5mm bbo探头的bruker av400mhz、配备有rt 5mm sei和txi探头的bruker drx 500mhz、配备有5mm rtbbi探头的bruker avance iii 600光谱仪以及varian unity plus 400mhz光谱仪上记录nmr谱。在25℃下使用dmso-d6、cdcl3、吡啶-d5或甲苯-d8作为溶剂以及tms作为内标来记录样品。
633、表2:物理化学数据。(rt意指以分钟计的保留时间;[mh]+意指化合物(游离碱)的质子化质量;nd=未确定的)。
634、
635、
636、
637、
638、
639、
640、
641、
642、
643、
644、
645、
646、
647、
648、
649、
650、
651、
652、
653、
654、药理学
655、本发明中提供的化合物是mglu7的负别构调节剂。因此,预期这些化合物由于其在与非正构谷氨酸识别位点的位点结合之后阻断受体功能的能力而对mglu7具有作用。
656、一些式(i)化合物已按照以下方法进行了测试。
657、实施例a
658、针对hek表达人mglu7的mglu7测定
659、转染和细胞培养
660、将编码人代谢型谷氨酸7受体(hmglu7)的cdna(登录号nm_181874.2,ncbi核苷酸数据库浏览器(ncbi nucleotide database browser))亚克隆到还包含潮霉素抗性基因的表达载体中。同时,将编码使激活信号转向至胞内钙通量的g蛋白的cdna亚克隆到还包含嘌呤霉素抗性基因的不同表达载体中。用polyfect试剂(qiagen)根据供应商方案将这两种载体都转染到hek293细胞中,并且潮霉素和嘌呤霉素处理允许选择已稳定整合了一个或更多个质粒拷贝的抗生素抗性细胞。在测量响应于谷氨酸和l-ap4或已知mglu7正构拮抗剂的钙通量变化的功能测定中鉴定表达hmglu7的阳性细胞克隆。
661、将表达hmglu7的hek-293细胞在37℃和5% co2于湿润气氛下维持在含有dmem、胎牛血清(10%)、glutamaxtm(2mm)、青霉素(100单位/ml)、链霉素(100μg/ml)、遗传霉素(100μg/ml)和潮霉素-b(40μg/ml)和嘌呤霉素(1μg/ml)的培养基中。
662、基于荧光细胞的ca2+动员测定
663、在基于荧光细胞的钙动员测定之前24小时,使用flipr384测定(moleculardevice,sunnyvale,ca,usa),在黑壁、透明底、聚l-鸟氨酸包被的384孔板上以25,000个细胞/孔的密度在含胎牛血清(10%)、青霉素(100单位/ml)、链霉素(100μg/ml)和强力霉素(1μg/ml)的谷氨酸/无谷氨酸dmem培养基中在37℃和5% co2于湿润气氛下平板接种人mglu7hek-293细胞。
664、在测定当天,抽吸培养基并用3μm的fluo4-am(lubioscience,lucerne,switzerland)在0.03%普朗尼克酸中的溶液加载细胞。在37℃/5%co2下1小时之后,将未并入的染液通过用测定缓冲液洗涤细胞板去除。所有测定均在含有20mm hepes、143mmnacl、6mm kcl、1mm mgso4、1mm cacl2、0.125mm磺吡酮和0.1%葡萄糖的ph 7.4的缓冲溶液中进行。
665、在10秒的基础荧光记录之后,向细胞添加不同浓度的本发明化合物。首先监测荧光水平的变化持续180秒以便检测化合物的任何激动剂活性。然后通过ec80l-ap4浓度将细胞刺激另外的110秒以便测量本发明化合物的抑制活性。ec80l-ap4浓度是是产生80%最大谷氨酸响应的浓度。
666、使用prism graphpad软件(graph pad inc,san diego,usa)生成l-ap4或本发明代表性化合物的浓度响应曲线。将该曲线拟合成四参数的逻辑斯谛方程(four-parameterlogistic equation):
667、(y=底部+(顶部-底部)/(1+10^((logic50-x)*hill斜率)
668、允许确定ic50值。
669、本技术化合物的ic50值小于10μm。
670、下表3示出了从以一式两份进行的所选分子的至少三个独立实验中获得的平均ic50。
671、表3:所选化合物的活性数据
672、
673、
674、*表格文字说明:
675、(+):1μm<ic50<10μm
676、(++):100nm<ic50<1μm
677、(+++):ic50<100nm
678、表3中示出的结果表明了本发明中描述的化合物是人mglu7受体的负别构调节剂。
679、实施例b
680、水相关o迷宫(water associated zero maze):
681、该操作如由ritov和richter-levin(2014)先前所述进行,但稍有修改。该装置由具有两个相对的封闭的象限(quadrant)(壁高35cm)和两个开放的象限(边界高5mm)的环形平台组成。支持(hold)该平台的塑料罐(plastic tank)充满有水(22±2℃,50cm深),上升至低于平台水平10cm。因此,该环形平台和塑料罐构成了一个统一的场地。对于该测试,首先使大鼠对空间(room)适应4分钟,并随后将其放置到开放象限之一中,面向该装置的封闭部分。允许大鼠探索该场地,持续5分钟时间段。在该时间期间通过etho-vision系统(noldus information technology,wageningen,netherlands)跟踪、记录并分析大鼠的行为。所分析的行为测量包括在开放象限中花费的时间、在开放象限中行进的距离、在封闭象限中行进的距离和总的僵立行为(freezing behavior)。使用这些参数对暴露于多种应激源和/或化合物的影响进行评估。不同受试化合物的预处理时间和施用途径基于其药代动力学特性来限定。
682、实施例c
683、高架十字迷宫(elevated plus maze):
684、高架十字迷宫(epm)测试使用sprague–dawley雄性大鼠进行。epm由这样的塑料制品(plastic)制成,其具有两个开放臂(arm)(50cm×10cm)和两个具有相同尺寸的封闭臂(壁高为40cm),高出高于地面86cm。这两种臂均由黑色plexiglas制成。开放臂上的平均照明水平为187lux,封闭臂上为100lux。在实验开始时,将大鼠带入与测试室直接相邻的等候室(holding room)中,并允许其在该环境中适应30分钟。在测试开始时,将大鼠放置于迷宫的中心,面向一个开放臂并观察5分钟。在该时间期间,通过etho-vision系统(noldusinformation technology,wageningen,netherlands)跟踪、记录并分析大鼠的行为。所分析的行为测量包括在开放臂中所花费的时间、进入开放臂的次数以及行进的距离。不同受试化合物的预处理时间和施用途径根据其药代动力学特性来限定。
685、实施例d
686、大鼠中创伤后应激障碍的恐惧调节模型(fear conditioning model):
687、恐惧调节场地(30cm×20cm×25cm,med associates)由不同环境下的plexiglas制成。将该系统放置于隔音的通风箱中。该场地底部(arena floor)由不锈钢废盘(stainless steel waste pan)上方的网格底板(grid floor)(19根平行的直径0.48cm的不锈钢杆(rod),间隔1.6cm)组成。所有杆均与电击发生器和加扰器(scrambler)联通。扬声器被安装在室壁上以提供听觉刺激源。在两天内进行恐惧调节操作。第一天(训练),将大鼠放置于训练环境(环境a)中并在120秒的适应期之后,使它们接受五对的cs和us。cs音(tone)(78db,2khz,5毫秒升/降时间)持续30秒并与简短的us足部电击(0.5秒,0.66ma)共终止。音间间隔(音开始至下一个音开始)范围为60秒。在对象(subject)之间用70%的乙醇清洁调节室(conditioning chamber)。对cs音传递期间的僵立所经过的时间进行评分(cs僵立)。第二天(测试日),将动物放置于新环境(环境b)中并在60秒的适应环境之后暴露于cs(120秒)。在适应环境与cs二者期间测量僵立所经过的时间。在训练期以及测试期之前和/或之后施用受试化合物。不同受试化合物的预处理时间和施用途径根据其药代动力学特性进行调整。
688、实施例e
689、小鼠中噪声诱导的听力损失(noise-induced hearing loss,nihl)模型:
690、使用年轻成年雄性cba/caj小鼠来评估受试化合物对nihl的作用。在2小时内,将动物暴露于声压级(sound pressure level)为110db的倍频程噪声(octave band noise)(8至16khz)。在噪声暴露之前和/或之后施用受试化合物。在声创伤之后24小时、2和4周的不同时间点使用自听觉发射的畸变产物(distorsion product of autoacousticemission,dpoae)或听觉脑干响应(auditory brainstrem response,abr)听力图来测量听力功能。不同受试化合物的预处理时间和施用途径根据其药代动力学特性进行调整。通过测量例如abr阈值或abr阈值偏移,将实验组与经载剂处理组进行比较。
691、实施例f
692、大鼠中内脏疼痛的结直肠扩张测试。
693、本研究中使用了雄性应激敏感的wistar kyoto大鼠(250至300g)。使动物禁食过夜(16小时)并在测试当天使用异氟醚麻醉。将6cm的乳胶球(latex balloon)插入结直肠腔中,距肛门1cm。使动物恢复20分钟,然后开始结直肠扩张。使用的范例(paradigm)是使用计算机驱动的电子稳压器在8分钟内从0mmhg至80mmhg的上升阶段扩张(ascending phasicdistension)。所测量的参数是引起视觉上可识别的内脏疼痛行为的阈压(thresholdpressure)(mmhg),以及疼痛行为的总数目。限定为内脏疼痛行为的姿势是腹部收缩和/或腹部退缩反射。
694、在结直肠扩张之前施用受试化合物。不同受试化合物的预处理时间和施用途径根据其药代动力学特性进行调整。
695、制剂实例
696、本发明制剂的配方的典型实例如下:
697、1.片剂
698、
699、在该实例中,活性成分可以被相同量的根据本发明的任何化合物替代,特别是被相同量的任何例举的化合物替代。
700、2.混悬剂
701、制备用于经口施用的水性混悬剂,使得每1毫升含有1至5mg活性化合物之一、50mg羧基甲基纤维素钠、1mg苯甲酸钠、500mg山梨糖醇和水ad 1ml。
702、3.可注射剂
703、通过在10体积%的丙二醇和水中搅拌1.5重量%的本发明活性成分来制备肠胃外组合物。
704、4.软膏剂
705、
706、在该实例中,活性成分可以用相同量的根据本发明的任何化合物代替,特别是用相同量的任何例举的化合物代替。
707、合理的变化不应被视为脱离本发明的范围。显而易见的是,本领域技术人员可以以多种方式改变所描述的本发明。
- 还没有人留言评论。精彩留言会获得点赞!