一种手性2-喹诺酮化合物及其制备方法与流程
本发明涉及有机合成领域,尤其涉及ipc c07d领域,更具体地,涉及一种手性2-喹诺酮化合物及其制备方法。
背景技术:
1、自1880年捷克化学家斯克劳普制备喹啉以来,这种杂环及其衍生物已在许多学科得到广泛应用。2-喹诺酮类化合物具有多种生物活性,是fda批准的药物中最常见的杂环化合物之一。许多文献公开报道了各种2-喹诺酮类化合物的生物活性,例如:文献:bioorg.med.chem.lett.2009,19,4354–4358;eur.j.med.chem.2011,46,307–319报道了该类化合物的抗病毒活性;文献:heterocycles 2012,85,2421–2436;chem.2014,57,5419–5434报道了该化合物的抗菌活性;文献:chem.2009,52,1639–1647;chem.2010,53,3887–3898报道了该类化合物的抗寄生虫活性;文献:angew.chem.,int.ed.2015,54,6217–6221;chem.lett.2018,9,283–288报道了该类化合物的抗炎症活性;文献:heterocycles 2012,85,2421–2436;chem.lett.2018,9,283–288报道了该类化合物的抗癌活性。
2、2-喹诺酮类化合物在生命科学、药物化学、农业和医药等领域有着广泛的应用前景,同时由于药物分子中起生物活性作用的往往是消旋体中的一种対映异构体,人们迫切地需要发展高效的合成该类化合物的方法,尤其是合成手性的2-喹诺酮类化合物的方法。目前,合成手性2-喹诺酮类化合物的方法包括两种。第一种是过渡金属催化的不对称共轭加成反应,但大多数例子都集中在芳基化反应的研究。2019年,harutyunyan等通过使用grignard试剂探索了不对称烷基化反应,并成功合成了烷基取代的2-喹诺酮类化合物。但该方法存在反应条件苛刻且底物范围有限的弊端。不对称[4+2]环加成反应是构建此类骨架的另一种方法,但该反应的底物需含有特定的官能团,如乙烯基、乙炔基等。因此,仍需开发一种更为通用且具原子经济性的合成二氢-2-喹诺酮类化合物的方法。
3、申请号为cn201710217714.1的专利申请文件,公开了一种制备7-羟基-2-喹诺酮的方法,申请号为cn201810033326.2的专利申请文件,公开了4-羟基-2-喹诺酮-氮-(4-喹唑啉酮)-3-甲酰胺类衍生物,两篇专利制备得到的2-喹诺酮类化合物均非手性。
4、目前,四组分post-ugi反应已经成为构建手性含氮杂环化合物的一种简便高效的方法,而利用该方法来构建手性2-喹诺酮的研究在国内外都是一片空白。因此,合成结构新颖的手性2-喹诺酮化合物以及发展其高效的不对称催化合成方法,对发现具有重要生物活性的药物先导化合物是非常必要的。
技术实现思路
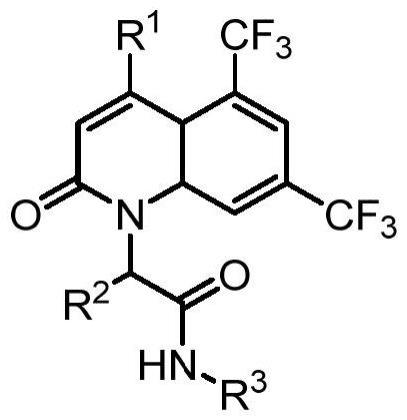
1、为了解决上述问题,本发明第一方面,提供了一种手性2-喹诺酮化合物,其结构通式如下:
2、
3、其中:
4、r1为氢,c6-14的芳基或取代芳基
5、所述的取代芳基为c1-6的烷基取代的芳基、c1-3的烷氧基取代的芳基、硝基取代的芳基或卤代芳基;
6、r2为氢,c6-10的芳基或取代芳基;
7、所述的取代芳基为c1-6的烷基取代的芳基、c1-3的烷氧基取代的芳基、硝基取代的芳基或卤代芳基;
8、r3为氢,c1-6的直链或带有支链的烷基,c3-6的环烷基。
9、优选的,所述c1-6的直链或带有支链的烷基包括正丁基,叔丁基中的任一种。
10、优选的,所述环烷基包括环己基。
11、优选的,所述取代芳基包括4-溴苯基、4-氯苯基、4-氟苯基、4-氰基苯基、4-硝基苯基、4-甲基苯基、4-甲氧基苯基、4-黄酰苯基、苯基、2-溴苯基、2-氯苯基、2-氟苯基、2-三氟甲基苯基、3-氯苯基、3-三氟甲基苯基、4-溴-2-氟苯基、2-呋喃、2-萘、2-吡啶、4-三氟甲基苯基、4-苯甲酸甲酯、4-氟-3-三氟甲基苯基、4-三氟甲基-3-溴苯基、3,5-二三氟甲基苯基中的任一种。
12、本发明第二方面提供了所述手性2-喹诺酮化合物的制备方法,包括以下步骤:
13、将醛类化合物、胺类化合物、酸类化合物、异氰化物混合进行ugi反应,即得。
14、进一步优选的,所述手性2-喹诺酮化合物的制备方法,反应过程示意图如图1所示,具体包括以下步骤:
15、在室温下,将醛类化合物、胺类化合物、手性催化剂、干燥剂和溶剂混合,在室温下搅拌10-15min后,加入酸类化合物,在-35~-25℃下搅拌10-15min后,加入异氰化物,然后在-35~-25℃搅拌30-40h,再恢复室温,加入金属催化剂,然后在室温搅拌8-15h后,将得到的混合物直接通过快速柱层析法纯化,即得。
16、优选的,所述醛类化合物、胺类化合物、酸类化合物和异氰化物的摩尔比为(1-2):1:(2-6):(1-5)。
17、优选的,所述手性催化剂加入的摩尔量为醛类化合物、胺类化合物、酸类化合物和异氰化物的总摩尔量的5-15%。
18、优选的,所述金属催化剂加入的摩尔量为醛类化合物、胺类化合物、酸类化合物和异氰化物的总摩尔量的2-8%。
19、优选的,所述醛类化合物包括对溴苯甲醛、对氟苯甲醛、苯甲醛、对氯苯甲醛、对氰基苯甲醛、对甲基苯甲醛中的一种或多种。
20、优选的,所述胺类化合物包括间二(三氟甲基)苯胺。
21、优选的,所述手性催化剂包括磷中心手性催化剂、钴中心手性催化剂、铑中心手性催化剂、铱中心手性催化剂中的任一种;进一步优选的,为钴中心手性催化剂。
22、优选的,所述钴中心手性催化剂为金属中心手性钴(iii)配阴离子。
23、优选的,所述金属中心手性钴(iii)配阴离子的结构式如下:
24、
25、其中tbu代表叔丁基。
26、所述金属中心手性钴(iii)配阴离子催化剂可采用文献angew.chem.int.ed.2015,54,11209;angew.chem.int.ed.2017,56,11931报道的方法制备。
27、优选的,所述干燥剂为分子筛、无水氯化钙、五氧化二磷、碱石灰中的一种或多种;进一步优选的,为分子筛。
28、优选的,所述分子筛包括型分子筛、型分子筛、型分子筛中的任一种;进一步优选的,为型分子筛。
29、所述型分子筛为活化的型分子筛。
30、优选的,所述酸类化合物包括芳香族羧酸、肉桂酸、线性烷基羧酸、环烷基羧酸、2-呋喃酸和山梨酸中的任一种。
31、优选的,所述酸类化合物包括丙炔酸、苯丙炔酸、2-丁炔酸中的任一种。
32、优选的,所述异氰化物包括叔丁基异氰、环己基异氰、正丁基异氰中的任一种。
33、优选的,所述溶剂包括甲苯、二甲基甲酰胺、二甲基亚砜、乙腈中的一种或多种;进一步优选的,为甲苯。
34、优选的,所述金属催化剂包括三苯基膦氯化金、三苯基膦氯化铑、三氟乙酸镁中的一种或多种;进一步优选的,为三苯基膦氯化金。
35、本技术人意外发现,先将醛类化合物和胺类化合物缩合为亚胺,再与酸类化合物和异氰化物发生四组分ugi反应,能够加快反应的进行。这可能是由于先生成亚胺,再加入酸类化合物和异氰化物,一方面酸类化合物的加入能够对亚胺进行lumo活化,促进异氰化物的加入,另一方面还能作为终止试剂生成手性酰胺。
36、本发明人创造性的发现,选用特定的金属中心手性钴(iii)配阴离子作为ugi反应的手性催化剂,能够提高产物的收率和对映体富集性。这可能是由于在过量的酸类化合物的条件下,金属中心手性钴(iii)配阴离子能够将亚胺激活,生成手性离子对,从而能够结合形成具有手性的中间产物,氢只能从特定位置与反应物相互作用,使最终产物2-喹诺酮化合物也具备手性。此外,环状基团与支链烷基所带来的位阻使反应物更易与金属离子产生相互作用,反应速率明显加快,收率同样得到提高。
37、有益效果:
38、1、本发明先将醛类化合物和胺类化合物缩合为亚胺,再与酸类化合物和异氰化物发生四组分ugi反应,能够加快反应的进行。
39、2、通过选用特定的金属中心手性钴(iii)配阴离子作为ugi反应的手性催化剂,能够提高产物的产率和纯度。
40、3、本发明选用金属中心手性钴(iii)配阴离子作为ugi反应的手性催化剂,并选择特定种类及摩尔含量的醛类化合物、胺类化合物作为原料缩合为亚胺,再与酸类化合物和异氰化物在温和的条件下发生四组分ugi反应,生成了对映体富集的手性酰胺,之后通过分子内金催化的炔烃氢化反应生成手性2-喹诺酮,提高了最终产物的收率。
41、4、本发明使用金属中心手性钴(iii)配阴离子和三苯基膦氯化金联合催化,通过一锅法合成了一系列的手性2-喹诺酮。与现有的技术相比该方法更具有原子经济性且成本低廉,有转化为工业化生产的潜力。
- 还没有人留言评论。精彩留言会获得点赞!