靛红酸酐类化合物及其制备方法和用途
本发明属于药物化学领域,具体涉及一类作为组蛋白去乙酰化酶6(hdac6)选择性抑制剂的靛红酸酐类化合物,及其在制备治疗hdac6相关疾病的药物中的用途。
背景技术:
1、组蛋白去乙酰化酶(histone deacetylases,hdacs)能够催化组蛋白和非组蛋白的去乙酰化过程,和组蛋白乙酰转移酶(histone acetyltransferases,hats)共同调节细胞内乙酰化水平,从而调控基因的表达。目前,已知哺乳动物hdacs有18个亚型,分为四类:i类(hdac1、hdac2、hdac3、hdac8);ii类进一步分为iia(hdac4、hdac5、hdac7、hdac9)和iib(hdac6、hdac10)两个亚家族;iii类(sirt1~sirt7);iv类(hdac11)。
2、目前已上市的组蛋白去乙酰化酶抑制剂(hdaci)共有5个,分别为伏立诺他(vorinostat)、贝利司他(belinostat)、帕比司他(panobinostat)、罗米地辛(romidepsin)和西达本胺(chidamide),前三者均为广谱型抑制剂,后两者选择性作用于i类亚型。伏立诺他和罗米地辛用于治疗皮肤t细胞淋巴瘤(ctcl),贝利司他和西达苯胺用于治疗复发及难治性外周t细胞淋巴瘤(ptcl),帕比司他与硼替佐米和地塞米松联用治疗多发性骨髓瘤(mm)。
3、尽管上述hdac抑制剂在临床上已取得良好疗效,但广谱hdac抑制剂普遍存在如下缺点:(1)较强的毒副作用,如恶心、呕吐、骨髓抑制等;(2)基因毒性;(3)药代动力学特性差,生物利用度低、半衰期短等。以上缺点既为肿瘤患者造成不便,也阻碍广谱hdac抑制剂在肿瘤治疗以外领域的应用。
4、目前hdacs亚型选择性抑制剂成为该领域的研究热点,其中,hdac6亚型抑制剂备受关注。hdac6涉及的疾病领域非常广泛,包括肿瘤、神经退行性疾病、神经精神性疾病、炎症、自身免疫应答、肿瘤及细菌感染等。
5、药理学研究表明hdac6选择性抑制剂能够有效抑制胶质母细胞瘤细胞增殖并诱导其凋亡,且抑制hdac6可以增强胶质母细胞瘤细胞对替莫唑胺的敏感性,提示二者有协同增效作用。具体而言,hdac6可以调节其乙酰化底物如热休克蛋白的活性,热休克蛋白作为分子伴侣可以参与修复错误折叠蛋白及未折叠蛋白;同时,hdac6蛋白的znf-ubp结构域能以高亲和力结合泛素化的错误折叠蛋白并促进其降解。因此,hdac6抑制剂tubastatin a和替莫唑胺(tmz)的联合治疗逆转了hdac6和p97/vcp之间的比例、减弱热休克蛋白的激活,触发了未折叠蛋白应答反应和内质网应激的促凋亡信号,并最终克服了内质网应激耐受,降低了tmz耐药胶质瘤细胞的活力并诱导细胞凋亡。
6、与脑胶质瘤类似,阿尔兹海默症(ad)临床同样亟需有效治疗药物,研究发现hdac6在ad脑的海马(增加91%)和皮质(增加52%)中表达水平显着增加,并且在含有nfts的神经元中微管蛋白乙酰化降低。hdac6参与tau过度磷酸化的过程。hdac6与人脑组织中的tau相互作用,这种相互作用由tau上的微管结合结构域和hdac6上的se14结构域介导。抑制hdac6不影响其与tau的相互作用,但减弱tau的t231磷酸化,t231是tau功能的关键调节位点。hdac6抑制改善ad小鼠的认知。以上研究表明中枢靶向性hdac6抑制剂有望开发成为全新的高效低毒的ad治疗药物。
7、现有抗精神分裂症、抑郁症、双向情感障碍药物存在副作用大(如锥体外系副作用、体重增加)、起效慢、患者依从性差等缺点,此主要与药物作用于多巴胺、五羟色胺受体相关。目前迫切需要作用于新靶点、新机制的抗精神分裂症、抑郁症、双向情感障碍创新药,以规避现有药物的缺点。研究发现大量精神分裂症易感基因启动子区组蛋白修饰(乙酰化)出现显著异常。最新的正电子成像(pet)结果显示,精神分裂症患者多个脑区中组蛋白去乙酰化酶表达异常,提示脑内组蛋白修饰异常与精神分裂症发生密切相关。hdac6基因敲除的小鼠在旷场实验中更活跃,在高架十字迷宫实验中焦虑程度更低,在尾悬挂实验和强迫游泳实验中表现出更强的抗抑郁效果。因而,高选择性hdac6抑制剂可用于治疗精神分裂症、抑郁症、双向情感障碍等,且可避免现有药物锥体外系、体重增加等副作用。
8、因此,有必要进一步开发结构新颖且具高活性、高选择性的hdac6抑制剂,以克服现有或传统hdac抑制剂的恶心、呕吐、骨髓抑制、致突变及qt间期延长等缺点。
技术实现思路
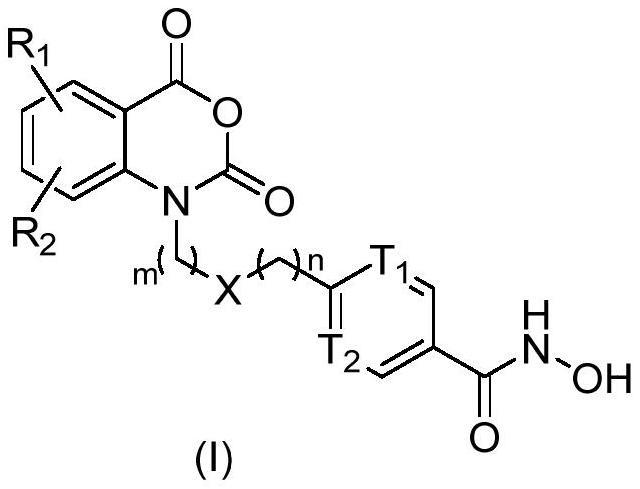
1、一方面本发明提供式(i)所示化合物或其药学上可接受的盐,
2、
3、其中,
4、x选自nh或单键;
5、t1选自ch或n;
6、t2选自ch或n;
7、r1选自氢、卤素、羟基、硝基、c1-6烷基、c1-6烷氧基或卤素取代的c1-6烷基;
8、r2选自氢、卤素、羟基、硝基、c1-6烷基、c1-6烷氧基或卤素取代的c1-6烷基;
9、m选自1或2;
10、n选自0、1或2。
11、在本发明的一些实施方案中,上述结构单元选自:优选
12、在本发明的一些实施方案中,当r1或r2为卤素时,所述卤素选自氟、氯或溴,优选氟或氯。
13、在本发明的一些实施方案中,当r1或r2为c1-6烷基时,所述c1-6烷基选自甲基、乙基、正丙基或异丙基,优选甲基。
14、在本发明的一些实施方案中,当r1或r2为c1-6烷氧基时,所述c1-6烷氧基选自甲氧基、乙氧基、正丙氧基或异丙氧基,优选甲氧基。
15、在本发明的一些实施方案中,当r1或r2为卤素取代的c1-6烷基时,所述卤素选自氟、氯或溴,优选氟。
16、在本发明的一些实施方案中,当r1或r2为卤素取代的c1-6烷基时,所述c1-6烷基选自甲基、乙基、正丙基或异丙基,优选甲基。
17、在本发明的一些实施方案中,当r1或r2为卤素取代的c1-6烷基时,所述卤素取代的c1-6烷基选自-cf3、-ch2f、-chf2、-chfch2f、-ch2chf2或-cf2cf3,优选-cf3。
18、在本发明的一些实施方案中,r1选自氢、氟、氯、硝基、甲基、甲氧基或-cf3。
19、在本发明的一些实施方案中,r2选自氢、氟、氯、硝基、甲基、甲氧基或-cf3。
20、在本发明的一些实施方案中,上述结构单元选自:
21、
22、在本发明的一些实施方案中,式(i)化合物或其药学上可接受的盐选自:
23、其中r1、r2、m和n的定义同前任一方案所述。
24、另一方面,本发明提供下列化合物及其药学上可接受的盐,选自:
25、
26、
27、另一方面,本发明提供式(ii)所示化合物,
28、
29、其中,
30、x选自nh或单键;
31、t1选自ch或n;
32、t2选自ch或n;
33、r1选自氢、卤素、羟基、硝基、c1-6烷基、c1-6烷氧基或卤素取代的c1-6烷基;r2选自氢、卤素、羟基、硝基、c1-6烷基、c1-6烷氧基或卤素取代的c1-6烷基;r3为c1-6烷基;
34、m选自1或2;
35、n选自0、1或2。
36、在本发明的一些实施方案中,式(ii)化合物选自:
37、
38、另一方面,本发明提供式(i)化合物的制备方法,包括方案一和方案二。
39、方案一
40、
41、其中,r1、r2、m和n的定义同前任一方案所述,x为单键。
42、化合物(iii)和化合物(iv)经取代反应制得化合物(ii),然后将化合物(ii)进行羟胺化反应制备得到化合物(i)。
43、方案二
44、
45、其中,r1、r2、m和n的定义同前任一方案所述,x为nh。
46、化合物(iii)经取代反应制得化合物(v),化合物(v)进一步与化合物(vi)经取代反应制得化合物(ii),化合物(ii)经羟胺化反应制得化合物(i)。
47、另一方面,本发明提供了一种药物组合物,包括治疗有效量的上述化合物或其药学上可接受的盐作为活性成分以及药学上可接受的载体。
48、所述的药学上可接受的载体(药用辅料)可为药物生产领域中广泛采用的那些辅料。辅料主要用于提供一个安全、稳定和功能性的药物组合物,还可以提供方法,使受试者接受给药后活性成分以所期望速率溶出,或促进受试者接受组合物给药后活性成分得到有效吸收。所述的药用辅料可以是惰性填充剂,或者提供某种功能,例如稳定该组合物的整体ph值或防止组合物活性成分的降解。所述的药用辅料可以包括下列辅料中的一种或多种:粘合剂、助悬剂、乳化剂、稀释剂、填充剂、成粒剂、胶粘剂、崩解剂、润滑剂、抗粘着剂、助流剂、润湿剂、胶凝剂、吸收延迟剂、溶解抑制剂、增强剂、吸附剂、缓冲剂、螯合剂、防腐剂、着色剂、矫味剂和甜味剂。
49、本发明的药物组合物可根据公开的内容使用本领域技术人员已知的任何方法来制备。例如,常规混合、溶解、造粒、乳化、磨细、包封、包埋或冻干工艺。
50、本发明所述的药物组合物可以任何形式给药,包括注射(静脉内)、粘膜、口服(固体和液体制剂)、吸入、眼部、直肠、局部或胃肠外(输注、注射、植入、皮下、静脉内、动脉内、肌内)给药。本发明的药物组合物还可以是控释或延迟释放剂型(例如脂质体或微球)。固体口服制剂的实例包括但不限于粉末、胶囊、囊片、软胶囊剂和片剂。口服或粘膜给药的液体制剂实例包括但不限于悬浮液、乳液、酏剂和溶液。局部用制剂的实例包括但不限于乳剂、凝胶剂、软膏剂、乳膏剂、贴剂、糊剂、泡沫剂、洗剂、滴剂或血清制剂。胃肠外给药的制剂实例包括但不限于注射用溶液、可以溶解或悬浮在药学上可接受载体中的干制剂、注射用悬浮液和注射用乳剂。所述的药物组合物的其它合适制剂的实例包括但不限于滴眼液和其他眼科制剂;气雾剂:如鼻腔喷雾剂或吸入剂;适于胃肠外给药的液体剂型;栓剂以及锭剂。
51、另一方面,本发明提供了上述化合物或其药学上可接受的盐在制备治疗hdac6相关疾病的药物中的用途。
52、另一方面,本发明提供了上述药物组合物在制备治疗hdac6相关疾病的药物中的用途。
53、在本发明的一些实施方案中,所述的hdac6相关疾病为癌症、神经疾病或自身免疫疾病。
54、在本发明的一些实施方案中,所述的癌症包括卵巢癌、结肠癌、乳腺癌、肝癌、胰腺癌、胆囊癌、胃肠癌、头颈癌、子宫颈癌、前列腺癌、肺癌、黑素瘤、生殖细胞肿瘤、妊娠滋养层肿瘤、胶质母细胞瘤、骨髓瘤、神经母细胞源性cns肿瘤、单核细胞白血病、b细胞源性白血病、t细胞源性白血病、b细胞源性淋巴瘤、t细胞源性淋巴瘤和肥大细胞源性肿瘤,及其组合。
55、在本发明的一些实施方案中,所述的神经疾病包括神经变性疾病、神经精神性疾病、周围神经病,及其组合。
56、在本发明的一些实施方案中,所述的自身免疫疾病包括牛皮癣、炎性疾病、通过免疫调节治疗的病状。
57、在本发明的一些实施方案中,所述的神经变性疾病包括阿尔茨海默氏症、帕金森氏症、亨廷顿氏舞蹈病、肌萎缩侧索硬化症、脊髓小脑变性、雷特氏综合征、疼痛。
58、在本发明的一些实施方案中,所述的神经精神性疾病为精神分裂症、抑郁症、双相情感障碍、焦虑症。
59、在本发明的一些实施方案中,所述的周围神经病包括腓骨肌萎缩症、巨大轴神经病变。
60、在本发明的一些实施方案中,所述的通过免疫调节治疗的病状包括多发性硬化症、自身免疫性糖尿病、狼疮、特应性皮炎、过敏、哮喘、过敏性鼻炎、炎症性肠病。
61、本发明的有益效果在于:作为新型的组蛋白去乙酰化酶6(hdac6)选择性抑制剂,本发明的化合物具有显著的体外活性(对hdac6酶的抑制活性高),及高的酶亚型选择性(对hdac1抑制弱);另外本发明的化合物显示出理想的药代动力学特征、较高的血脑屏障通透性和良好的安全性。
62、定义和说明
63、除非另有说明,本文所用的下列术语和短语旨在具有下列含义。一个特定的术语或短语在没有特别定义的情况下不应该被认为是不确定的或不清楚的,而应该按照普通的含义去理解。当本文中出现商品名时,意在指代其对应的商品或其活性成分。
64、术语“药学上可接受的”,是针对那些化合物、材料、组合物和/或剂型而言,它们在可靠的医学判断的范围之内,适用于与人类和动物的组织接触使用,而没有过多的毒性、刺激性、过敏性反应或其它问题或并发症,与合理的利益/风险比相称。
65、术语“药学上可接受的盐”是指本发明化合物的盐,由本发明发现的具有特定取代基的化合物与相对无毒的酸或碱制备。当本发明的化合物中含有相对酸性的功能团时,可以通过在纯的溶液或合适的惰性溶剂中用足够量的碱与这类化合物的中性形式接触的方式获得碱加成盐。药学上可接受的碱加成盐包括钠、钾、钙、铵、有机胺或镁盐或类似的盐。当本发明的化合物中含有相对碱性的官能团时,可以通过在纯的溶液或合适的惰性溶剂中用足够量的酸与这类化合物的中性形式接触的方式获得酸加成盐。药学上可接受的酸加成盐的实例包括无机酸盐,所述无机酸包括例如盐酸、氢溴酸、硝酸、碳酸,碳酸氢根,磷酸、磷酸一氢根、磷酸二氢根、硫酸、硫酸氢根、氢碘酸、亚磷酸等;以及有机酸盐,所述有机酸包括如乙酸、丙酸、异丁酸、马来酸、丙二酸、苯甲酸、琥珀酸、辛二酸、反丁烯二酸、乳酸、扁桃酸、邻苯二甲酸、苯磺酸、对甲苯磺酸、柠檬酸、酒石酸和甲磺酸等类似的酸;还包括氨基酸(如精氨酸等)的盐,以及如葡糖醛酸等有机酸的盐。本发明的某些特定的化合物含有碱性和酸性的官能团,从而可以被转换成任一碱或酸加成盐。
66、本发明的药学上可接受的盐可由含有酸根或碱基的母体化合物通过常规化学方法合成。一般情况下,这样的盐的制备方法是:在水或有机溶剂或两者的混合物中,经由游离酸或碱形式的这些化合物与化学计量的适当的碱或酸反应来制备。
67、除了盐的形式,本发明所提供的化合物还存在前药形式。本文所描述的化合物的前药容易地在生理条件下发生化学变化从而转化成本发明的化合物。此外,前体药物可以在体内环境中通过化学或生化方法被转换到本发明的化合物。
68、本发明的某些化合物可以以非溶剂化形式或者溶剂化形式存在,包括水合物形式。一般而言,溶剂化形式与非溶剂化的形式相当,都包含在本发明的范围之内。
69、本发明的化合物可以存在特定的几何或立体异构体形式。本发明设想所有的这类化合物,包括顺式和反式异构体、(-)-和(+)-对映体、(r)-和(s)-对映体、非对映异构体、(d)-异构体、(l)-异构体,及其外消旋混合物和其他混合物,例如对映异构体或非对映体富集的混合物,所有这些混合物都属于本发明的范围之内。烷基等取代基中可存在另外的不对称碳原子。所有这些异构体以及它们的混合物,均包括在本发明的范围之内。
70、术语“被取代的”或“取代的”是指特定原子上的任意一个或多个氢原子被取代基取代,可以包括重氢和氢的变体,只要特定原子的价态是正常的并且取代后的化合物是稳定的。当取代基为酮基(即=o)时,意味着两个氢原子被取代。酮取代不会发生在芳香基上。除非另有规定,取代基的种类和数目在化学上可以实现的基础上可以是任意的。
71、当任何变量(例如r)在化合物的组成或结构中出现一次以上时,其在每一种情况下的定义都是独立的。因此,例如,如果一个基团被0-2个r所取代,则所述基团可以任选地至多被两个r所取代,并且每种情况下的r都有独立的选项。此外,取代基和/或其变体的组合只有在这样的组合会产生稳定的化合物的情况下才是被允许的。
72、当一个取代基为空缺时,表示该取代基是不存在的,比如a-x中x为空缺时表示该结构实际上是a。当所列举的取代基中没有指明其通过哪一个原子连接到被取代的基团上时,这种取代基可以通过其任何原子相键合,例如,吡啶基作为取代基可以通过吡啶环上任意一个碳原子连接到被取代的基团上。
73、当一个连接基团的数量为0时,比如-(crr)0-,表示该连接基团为单键。
74、当其中一个变量选自单键时,表示其连接的两个基团直接相连,比如a-l-z中l代表单键时表示该结构实际上是a-z。
75、术语“c1-6烷基”用于表示直链或支链的由1至6个碳原子组成的饱和碳氢基团。所述c1-6烷基包括c1-5、c1-4、c1-3、c1-2、c2-6、c2-4、c6和c5烷基等。c1-6烷基的实例包括但不限于甲基(me)、乙基(et)、丙基(包括n-丙基和异丙基)、丁基(包括n-丁基,异丁基,s-丁基和t-丁基)、戊基(包括n-戊基,异戊基和新戊基)、己基等。
76、术语“c1-6烷氧基”表示通过一个氧原子连接到分子的其余部分的那些包含1至6个碳原子的烷基基团。所述c1-6烷氧基包括c1-4、c1-3、c1-2、c2-6、c2-4、c6、c5、c4和c3烷氧基等。c1-6烷氧基的实例包括但不限于甲氧基、乙氧基、丙氧基(包括正丙氧基和异丙氧基)、丁氧基(包括n-丁氧基、异丁氧基、s-丁氧基和t-丁氧基)、戊氧基(包括n-戊氧基、异戊氧基和新戊氧基)、己氧基等。
77、术语“卤素”是指氟(f)、氯(cl)、溴(br)和碘(i)。
78、术语“卤素取代的c1-6烷基”是指上述“c1-6烷基”被一个或多个卤素基团取代。示例性的所述卤素取代烷基包括但不限于:-cf3、-ch2f、-chf2、-chfch2f、-ch2chf2、-cf2cf3、-ccl3、-ch2cl、-chcl2、2,2,2-三氟-1,1-二甲基-乙基等。
- 还没有人留言评论。精彩留言会获得点赞!