一种低免疫原性多能干细胞及其制备方法和应用
本发明属于基因工程,涉及一种低免疫原性多能干细胞及其制备方法和应用。
背景技术:
1、在干细胞的临床应用中的一大难关就是移植宿主免疫排斥以及移植环境不适应造成的自身凋亡,这导致移植后治疗效果的大大降低。为解决这一问题,通用型多能干细胞(universal stem cell line,uscl)逐渐引起重视,通用型多能干细胞可以移植到体内不引起强力的免疫排斥,即低免疫原性多能干细胞。构建低免疫原性多能干细胞最直接的方法就是去除多能干细胞上引起排斥反应的主要因素。
2、t细胞介导的适应性免疫排斥是引起同种异体排斥的主要原因。人同种异体移植中t细胞介导的排斥反应可以分为两个阶段,包括t细胞进行直接识别即t细胞受体(t cellreceptor,tcr)识别供体抗原递呈细胞(antibody-dependent cell-mediatedcytotoxicity,apc)的hlas(human leukocyte antigens)复合物,hla的不匹配会激活t细胞,导致移植物的急性排斥反应。t细胞通过直接识别和间接识别被激活,对hla复合体不匹配的移植物造成严重的生存威胁。所以只要供体细胞的hla复合体不被识别,t细胞的信号通路就不会激活,t细胞最终无法产生免疫排斥。
3、hla复合体,按其产物的结构、表达方式、组织分布与功能可将这些基因座主要分为两类。第一类hla复合体(hla-i)的蛋白组成具有多样性,它主要由一个跨越细胞膜α链组成,并且在该链上的细胞外处还带有一个β2微球蛋白。第二类hla复合体(hla-ii)中的α链和一个β链交叉结合,双链同时贯穿细胞膜,存在于抗原提呈细胞中,如b细胞、巨噬细胞和dcs等专业apc和胸腺上皮细胞,并且仅仅细胞表面才有。
4、由于hla-i链上只有一个β2微球蛋白,破坏β链可以去除hla-i的表达。已有多个研究团队报道,敲除b2m基因可以获得低免疫原性的多能干细胞。然而,hla-ii由多α链和β链组成,单独的破坏某一条α链或者β链都无法阻断hla-ii蛋白在细胞膜上的抗原递呈。研究人员发现,破坏hla-ii上的转录复合物可以抑制细胞表达hla-ii。当宿主体内的细胞发生被病原体感染,这些病变的细胞会通过抗原递呈的方式将信号传递给t细胞自己被感染,t细胞就会启动急性排斥以及随之而来的非急性排斥,所以病原体会阻止被感染的细胞向t细胞发出求救的信号,即阻止细胞发出hlas信号,防止宿主免疫细胞攻击。
5、如cn104046593a公开一种低免疫原性的人细胞及其制备方法,与相应的野生型细胞相比,所述修饰的人细胞的细胞表面人类白细胞抗原hla蛋白或多肽缺失或表达下调,从而使得所述修饰的人细胞具有降低的免疫原性。cn115551998a公开一种高功能的低免疫原性细胞、即低免疫原性人细胞,其满足:(1)缺损编码人白细胞型抗原(hla)类ia的α链的内源基因、(2)缺损编码hla类ii或其表达调控因子的内源基因、(3)包含编码hla类ib的α链的外源基因、(4)包含编码人pd-l1的外源基因、以及(5)包含编码人pd-l2的外源基因,编码hla类ia的α链的内源基因为编码hla-a的α链的内源基因、编码hla-b的α链的内源基因和编码hla-c的α链的内源基因,编码hla类ii或其表达调控因子的内源基因为以下的(a)或(b):(a)编码hla-dp的α链和/或β链的内源基因、编码hla-dq的α链和/或β链的内源基因、编码hla-dr的α链和/或β链的内源基因、编码hla-dm的α链和/或β链的内源基因、以及编码hla-do的α链和/或β链的内源基因;(b)编码人rfxank的内源基因、编码人rfx5的内源基因、编码人rfxap的内源基因或编码人ciita的内源基因。
6、综上所述,开发新型高效的构建低免疫原性多能干细胞的策略,对于干细胞的临床应用领域具有重要意义。
技术实现思路
1、针对现有技术的不足和实际需求,本发明提供一种低免疫原性多能干细胞及其制备方法和应用,降低多能干细胞免疫原性,推动干细胞的临床应用。
2、为达上述目的,本发明采用以下技术方案:
3、第一方面,本发明提供一种低免疫原性多能干细胞,所述低免疫原性多能干细胞缺失功能性人白细胞型抗原i(hla-i)、人白细胞型抗原ii(hla-ii)、gp130蛋白和tnfsf1a蛋白;过表达pd-l1基因、ctla4基因、lgg1基因、cd24基因和cd47基因。
4、本发明中,设计全新的改造策略,缺失功能性人白细胞型抗原i(hla-i)、人白细胞型抗原ii(hla-ii)降低细胞hla被宿主识别的风险,缺失gp130和tnfsf1a炎症因子受体减少免疫排斥所带来的炎症反应,结合过表达pd-l1基因、ctla4基因、lgg1基因、cd24基因和cd47基因,协同配合,进一步降低多能干细胞的免疫原性,包括同时抑制t细胞、nk细胞和巨噬细胞的排斥作用,提高干细胞移植后存活能力。
5、优选地,所述低免疫原性多能干细胞的底盘细胞包括人诱导型多能干细胞。
6、优选地,所述缺失功能性人白细胞型抗原i包括缺失功能性b2m蛋白。
7、优选地,所述缺失功能性人白细胞型抗原ii包括缺失功能性人白细胞型抗原ii表达调控因子。
8、优选地,所述人白细胞型抗原ii表达调控因子包括ciita蛋白。
9、优选地,所述低免疫原性多能干细胞缺失功能性b2m蛋白、ciita蛋白、gp130蛋白和tnfsf1a蛋白;过表达pd-l1、ctla4、lgg1、cd24和cd47基因。
10、第二方面,本发明提供一种第一方面所述的低免疫原性多能干细胞的制备方法,所述制备方法包括:
11、改造多能干细胞,使其缺失功能性人白细胞型抗原i、人白细胞型抗原ii、gp130蛋白和tnfsf1a蛋白;过表达pd-l1、ctla4、lgg1、cd24和cd47基因,得到所述低免疫原性多能干细胞。
12、优选地,所述缺失功能性人白细胞型抗原i的方法包括使人白细胞型抗原i生物合成或转运途径中的至少一种基因缺失或表达下降,所述基因选自b2m基因。
13、优选地,所述缺失功能性人白细胞型抗原ii的方法包括使至少一种人白细胞型抗原ii或其表达调控因子的基因缺失或表达下降,所述基因选自ciita基因。
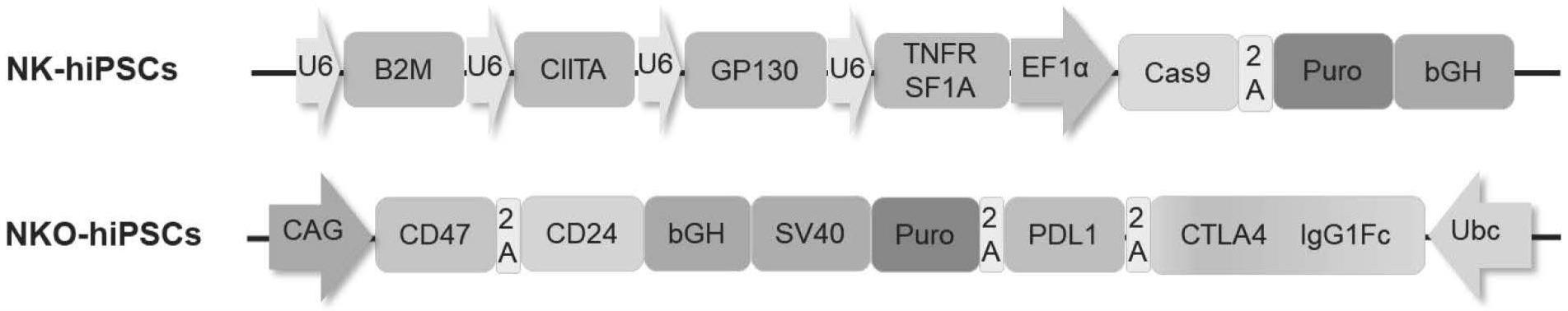
14、可以理解,本领域通用的缺失功能性蛋白的手段如基因敲除、基因沉默等等实现蛋白表达缺失或下降的手段,以及提高基因表达的手段,均适用于本发明,不作特殊限制。例如本发明具体实施例中,利用crispr-cas9打靶系统对nlb-hipscs细胞中的b2m、ciita、gp130和tnfsf1a基因进行基因敲除。将这四个基因的sgrna串联在含有cas9的px459载体上,然后将px459-4u6-puro转染至nilb-hipscs细胞中。将转染的细胞分离为单个细胞,扩增到集落,最后对扩增的单细胞克隆进行pcr测序,得到nk-hipscs细胞系。pd-l1、ctla4、lgg1、cd24和cd47基因,将五个片段连接到到含有puro抗性的piggybac质粒中。将piggybac质粒与转座酶一起转染至nk-hipscs细胞系中,加入puro持续筛选,对扩增的单细胞克隆进行rt-pcr测序,得到nko-hipscs细胞系。
15、第三方面,本发明提供第一方面所述的低免疫原性多能干细胞在建立药物筛选平台中的应用。
16、第四方面,本发明提供第一方面所述的低免疫原性多能干细胞在建立干细胞移植治疗疾病平台中的应用。
17、与现有技术相比,本发明具有以下有益效果:
18、本发明设计全新的改造策略,过表达了cd47抑制nk细胞的攻击,避免单一敲除与t细胞排斥密切相关的hla-i和hla-ii无法抑制nk细胞攻击的问题;过表达igg1 fc、ctla4和pd-l1进一步抑制t细胞的排斥反应,使得细胞在同种异体移植中免受t细胞的排斥;过表达cd24基因,与以降低细胞被巨噬细胞攻击的频率;敲除gp130和tnfsf1a基因,减少促炎因子的激活,整体协同配合,使得多能干细胞在移植中具有更好的存活能力,同时仍具有低免疫原性的能力。
- 还没有人留言评论。精彩留言会获得点赞!