利用生物酶法高效制备莱鲍迪苷M的方法与流程
本发明属于生物催化转化,具体涉及一种利用生物酶法高效制备莱鲍迪苷m的方法。
背景技术:
1、人们发现以甜菊糖苷为代表的一类绿色、健康的天然甜味剂可以广泛的作为代糖使用。甜菊糖苷是从甜叶菊(s.rebaudiana)的叶片中通过植物提取法得到的天然甜味剂。甜叶菊产地源自于南美巴拉圭和巴西的原始森林,几百年以来,当地人一直将甜叶菊的叶子研磨后作为甜味剂使用,这种甜味主要是源于叶子中含有的多种甜菊醇醇糖苷混合物。甜菊糖苷是由一些二萜类糖苷化合物形成的糖苷混合物,它的化学结构是糖配体与甜菊醇苷元连接缩合,甜菊糖苷中的糖苷键大部分无法消化,因此释放的能量很少,可以成为非常有吸引力的糖替代品。甜叶菊叶片中含量最丰富的是甜菊苷(stevioside)和莱鲍迪苷a(rebaudiosidea),其甜度是蔗糖的200倍,是最早开始商业化使用的甜味剂。然而,甜菊苷和莱鲍迪苷a会作用于味蕾中的苦味受体htas2r4和htas2r14,导致其具有明显的后苦味,口感不好,而这降低了人们对二者的接受度,影响了其应用范围及市场接受度。甜叶菊叶片中含量非常少(0.3%)的莱鲍迪苷m具有快速、纯正的甜味且热量极低,在感官特性上与蔗糖最为相似,在食品、医药行业非常具有研究意义,有望代替蔗糖这一传统糖源作为天然甜味剂来广泛使用,被誉为下一代甜味剂。
2、目前商业化的产品莱鲍迪苷a甜味味质不如莱鲍迪苷m,然而甜叶菊中口感最佳的莱鲍迪苷m在甜叶菊中严重缺乏,天然含量非常低,不可能像含量高的甜菊苷和莱鲍迪苷a一样,直接从甜叶菊叶片进行商品化的提炼和纯化,这限制了莱鲍迪苷m的大批量规模化生产和供给。通过转基因甜叶菊或者微生物法来生产莱鲍迪苷m可以提高其产量,但以上两种方法均需要充分了解莱鲍迪苷m的生物合成途径,特别是糖基化过程。
3、目前甜菊糖苷的生物合成途径已经基本明晰,并鉴定出了一系列利用尿苷二磷酸葡萄糖(udp-glucose,udpg)作为糖基供体的糖基转移酶(ugts)。分析莱鲍迪苷m生物合成途径可以发现,位于莱鲍迪苷a的c19-羧基方向的糖基化,即在该位置形成β(1-2)糖苷键,是生成莱鲍迪苷m的必需步骤,决定了莱鲍迪苷m的天然含量大小。甜菊糖苷的糖基化依赖于位于甜叶菊(s.rebaudiana)细胞质中的4个糖基转移酶(ugts)。它们在碳水化合物活性酶(cazy)数据库(www.cazy.org)中均被标注为gt1家族成员,并利用尿苷二磷酸葡萄糖(udp-glucose)作为糖基供体。糖基转移酶ugt85c2和ugt74g1分别在甜菊醇苷元的c13羟基和c19羧基位置上以β-1糖苷键连接第一个葡萄糖基,接着ugt91d2通过β(1-2)糖苷键在第一个葡萄糖基的c2添加一个糖基,最后ugt76g1在第一个葡萄糖基的c3位添加一个糖基。张等发现甜叶菊自身缺乏在甜菊糖苷c19-羧基方向形成β(1-2)糖苷键的能力,是造成甜菊糖苷dm天然含量低的直接原因。
4、目前以莱鲍迪苷a作为底物经糖基化反应生成莱鲍迪苷m,通常需要经过两步转化,首先莱鲍迪苷a糖基化生成莱鲍迪苷d,然后再进一步糖基化生成莱鲍迪苷m,两步催化法生成莱鲍迪苷m的缺点是容易造成中间产物莱鲍迪苷d的累计,不利于后续分离提纯,并且两步法催化莱鲍迪苷a生成莱鲍迪苷m通常需要多种酶,步骤较为繁琐。
5、
6、通常udp-糖基供体依赖的糖基转移酶(ugts)催化的糖基化反应需要使用价格昂贵且稳定性差的udp-糖基供体,如udp-葡萄糖(udpg)等,udpg过于昂贵,作为糖基供体使用会产生巨额的成本,不适用于大规模的工业化生产,这严重限制了ugts的工业化应用。
7、
8、天津大学申请的专利cn110734944b-一步法合成莱鲍迪苷m的方法,该发明以莱鲍迪苷a为底物,加入尿苷二磷酸葡萄糖,硫酸镁或氯化镁,甲醇,利用能够分泌表达糖基转移酶的重组工程菌ugt1和ugt2催化反应,得到莱鲍迪苷m,该方法添加了较多的金属离子和有机溶剂,不利于后续的的分离纯化和食品级生产,且反应中添加了昂贵的尿苷二磷酸葡萄糖,生产成本过高。南京工业大学申请的专利cn109750071a-一种生物催化合成莱鲍迪苷m的方法,该申请是利用番茄来源udp-糖基转移酶和马铃薯来源蔗糖合成酶,以甜菊甙为原料糖基化反应合成莱鲍迪苷e;随后,利用甜叶菊来源udp-糖基转移酶和马铃薯来源蔗糖合成酶,以莱鲍迪苷e为原料进一步糖基化反应合成莱鲍迪苷m,该方法需要先生成莱鲍迪苷e,再进一步生成莱鲍迪苷m。该方法需要经过两步或多步催化反应才能得到最终产物,反应速度慢,催化效率低,副产物较多,不利于分离纯化。
9、因此目前现有生产莱鲍迪苷m的技术中,存在如下的缺点:
10、1)植物提取法步骤繁琐,产量低,成本高,分离提纯困难。
11、2)植物提取法需要大量的甜叶菊,浪费耕地面积。
12、3)化学合成法产生大量有害气体和废液,不利于环境保护。
13、4)催化反应体系中含有较多的金属离子和有机溶剂,不利于后续的的分离纯化和食品级生产。
14、5)需要经过两步或多步催化反应才能得到最终产物,反应速度慢,催化效率低,副产物较多,不利于分离纯化。
15、6)通常所需糖基供体为昂贵的尿苷二磷酸葡萄糖,生产成本高,不适合大规模的工业化生产。
16、7)需要添加多种酶制剂进行催化反应,特异性差,产率较低。
17、所以亟需一种高效低成本生产莱鲍迪苷m的方法。
技术实现思路
1、为了克服现有技术存在的不足,本发明的目的是提供利用生物酶法高效制备莱鲍迪苷m的方法。
2、本发明提供的方法是基于基因挖掘的方法得到糖基转移酶,然后构建工程菌进行蛋白表达,体外催化以莱鲍迪苷a作为底物进行糖基化反应一步合成莱鲍迪苷m。该合成方法催化效率高反应时间短,产物单一易分离,有较大的工业应用前景。并且本发明提供的糖基转移酶还可与蔗糖合成酶进行偶联催化,以蔗糖作为糖基供体,将莱鲍迪苷a一步催化生成莱鲍迪苷m。
3、本发明提供的利用生物酶法高效制备莱鲍迪苷m的方法通过使用催化效率较高的糖基转移酶,能够以莱鲍迪苷a为底物,一步催化生成莱鲍迪苷m,实现莱鲍迪苷m的高效生物合成。该方法可以避免中间产物莱鲍迪苷d的生成,便于后续的分离提纯,精简催化反应的工艺流程。该方法用生物酶法高效合成制备高甜度低热量天然甜味剂-莱鲍迪苷m。
4、本发明的目的至少通过如下技术方案之一实现。
5、本发明提供的一种利用生物酶法高效制备莱鲍迪苷m的方法,包括如下步骤:
6、将莱鲍迪苷a、尿苷二磷酸葡萄糖、糖基转移酶、盐加入缓冲液中,混合均匀,得到混合液,在搅拌状态下进行酶催化反应,得到所述莱鲍迪苷m。
7、进一步地,在所述混合液中,莱鲍迪苷a的浓度为1-100g/l;
8、优选地,在所述混合液中,莱鲍迪苷a的浓度为1g/l。
9、进一步地,在所述混合液中,尿苷二磷酸葡萄糖的浓度为0.5-20mm;
10、优选地,在所述混合液中,尿苷二磷酸葡萄糖的浓度为1mm。
11、进一步地,所述盐为钙盐、钴盐、铁盐、镁盐、锰盐、铵盐、镍盐、锌盐中的一种以上;
12、优选地,所述盐为钙盐、镁盐、锰盐、铁盐中的一种以上;
13、进一步优选地,所述盐为镁盐。
14、进一步地,在所述混合液中,盐的浓度为0.1-10mm;
15、优选地,在所述混合液中,盐的浓度为1mm。
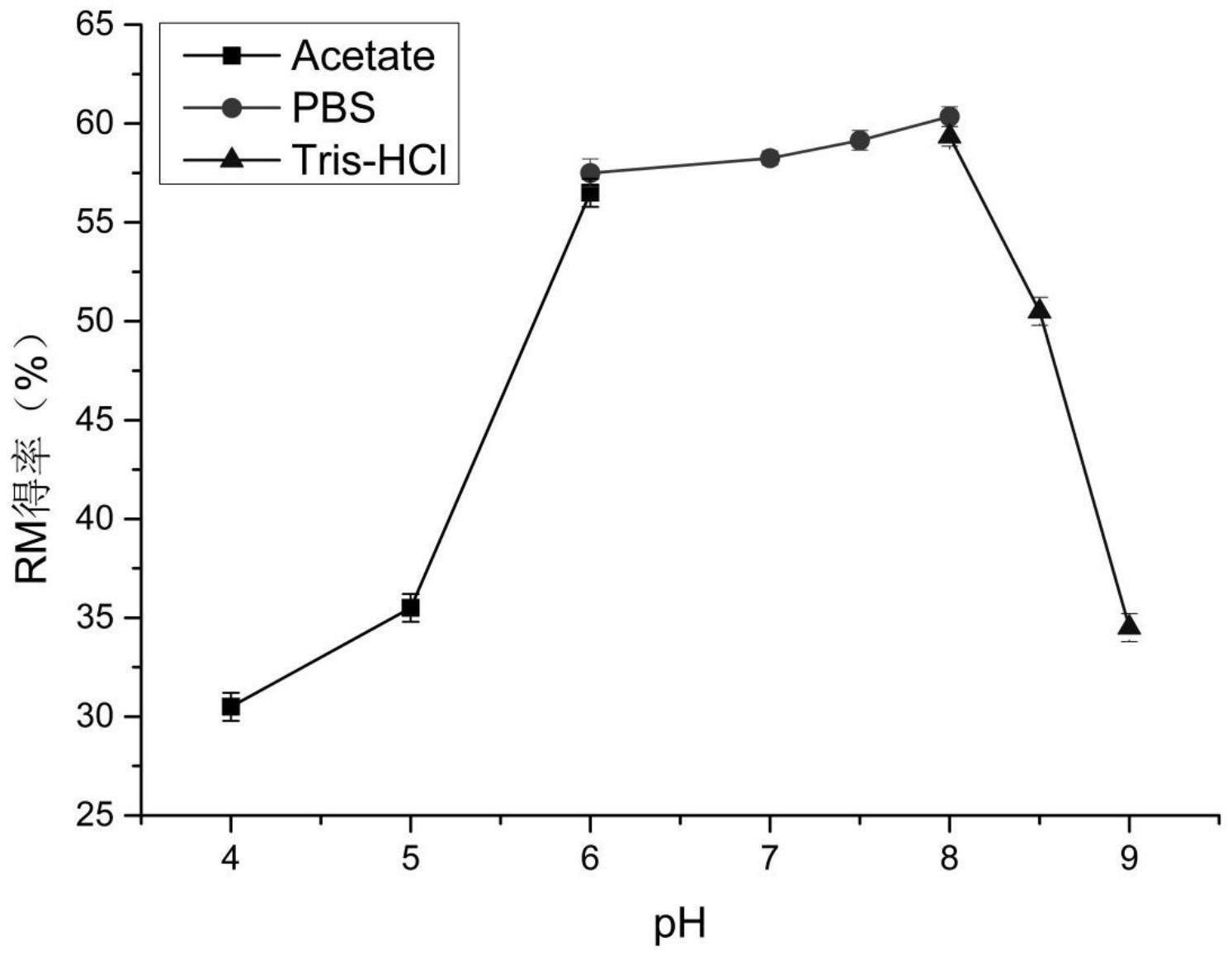
16、进一步地,所述缓冲液的ph为5.0-9.0;
17、优选地,所述缓冲液的ph为6.0-8.0;
18、进一步优选地,所述缓冲液的ph为8.0;
19、进一步地,所述在搅拌状态下的搅拌速率为50-220rpm;
20、优选地,所述在搅拌状态下的搅拌速率为200rpm。
21、进一步地,所述酶催化反应的温度为20-45℃,所述酶催化反应的时间为1-5h。
22、优选地,所述酶催化反应的温度为30-37℃。
23、进一步优选地,所述酶催化反应的温度为37℃。
24、进一步地,在所述混合液中,所述糖基转移酶的浓度为1-20g/l;
25、优选地,在所述混合液中,所述糖基转移酶的浓度为5g/l。
26、进一步地,所述糖基转移酶的序列为如seq id no.1所示、如seq id no.2所示、如seq id no.3所示、如seq id no.4所示、如seq id no.5所示、如seq id no.6所示、如seqid no.7所示、如seq id no.8所示、如seq id no.9所示、如seq id no.10所示、如seq idno.11所示及如seq id no.12所示的氨基酸序列中的一种以上。
27、优选地,所述糖基转移酶的氨基酸序列如seq id no.1所示。
28、本发明提供的方法中,使用的糖基转移酶催化糖基化反应效率较高,以尿苷二磷酸葡萄糖(udpg)作为糖基供体,该酶可以很好地催化莱鲍迪苷a糖基化一步生成高价值甜味剂莱鲍迪苷m,且不需要添加其他任何酶。
29、本发明提供的方法中,使用的糖基转移酶的糖基化反应的最适ph为8.0,最佳反应温度为37℃,是一种金属离子依赖型酶,mg2+、ca2+、mn2+对该酶的催化效率有明显的促进提升作用,其中mg2+的促进作用最强。
30、本发明提供的方法中,该酶的最佳反应条件为:反应体系各种物质的终浓度分别是莱鲍迪苷a为1g/l,udpg为1mm,mgcl2为5mm,反应温度37℃,转速220rpm,反应时间1-2h,在最佳反应条件下,该酶催化莱鲍迪苷a糖基化生成莱鲍迪苷m的催化效率较高,转化率可达95%以上。
31、本发明提供的另一种利用生物酶法高效制备莱鲍迪苷m的方法,包括如下步骤:
32、将莱鲍迪苷a、蔗糖、udp(5-尿苷二磷酸二钠盐)、糖基转移酶、蔗糖合成酶、盐加入缓冲液中,混合均匀,得到混合液,在搅拌状态下进行酶催化反应,得到所述莱鲍迪苷m。
33、进一步地,在所述混合液中,莱鲍迪苷a的浓度为1-100g/l;
34、优选地,在所述混合液中,莱鲍迪苷a的浓度为10g/l。
35、进一步地,在所述混合液中,蔗糖的浓度为1-500mm;
36、优选地,在所述混合液中,蔗糖的浓度为100mm。
37、进一步地,在所述混合液中,udp(5-尿苷二磷酸二钠盐)的浓度为0.1-20mm;
38、优选地,在所述混合液中,udp(5-尿苷二磷酸二钠盐)的浓度为2mm。
39、进一步地,所述盐为钙盐、钴盐、铁盐、镁盐、锰盐、铵盐、镍盐、锌盐中的一种以上;
40、优选地,所述盐为钙盐、镁盐、锰盐、铁盐中的一种以上;
41、进一步地,在所述混合液中,盐的浓度为0.1-10mm;
42、优选地,在所述混合液中,盐的浓度为0.1-5mm。
43、进一步优选地,在所述混合液中,盐的浓度为1mm。
44、进一步地,所述缓冲液的ph为4.0-9.0;
45、优选地,所述缓冲液的ph为6.0-8.0;
46、进一步优选地,所述缓冲液的ph为8.0;
47、进一步地,所述在搅拌状态下的搅拌速率为50-220rpm;
48、优选地,所述在搅拌状态下的搅拌速率为200rpm。
49、进一步地,所述酶催化反应的温度为20-45℃,所述酶催化反应的时间为1-5h。
50、优选地,所述酶催化反应的温度为30-37℃。
51、进一步优选地,所述酶催化反应的温度为37℃。
52、进一步地,在所述混合液中,所述糖基转移酶的浓度为1-20g/l;
53、优选地,在所述混合液中,所述糖基转移酶的浓度为5g/l。
54、进一步地,所述糖基转移酶的序列为如seq id no.1所示、如seq id no.2所示、如seq id no.3所示、如seq id no.4所示、如seq id no.5所示、如seq id no.6所示、如seqid no.7所示、如seq id no.8所示、如seq id no.9所示、如seq id no.10所示、如seq idno.11所示及如seq id no.12所示的氨基酸序列中的一种以上。
55、优选地,所述糖基转移酶的氨基酸序列如seq id no.1所示。
56、进一步地,在所述混合液中,所述蔗糖合成酶的浓度为1-10g/l;
57、优选地,在所述混合液中,所述蔗糖合成酶的浓度为2g/l。
58、进一步地,所述蔗糖合成酶的氨基酸序列为如seq id no.13所示、如seq idno.14所示、如seq id no.15所示、如seq id no.16所示、如seq id no.17所示、如seq idno.18所示、如seq id no.19所示及如seq id no.20所示中的一种以上。
59、优选地,所述蔗糖合成酶的氨基酸序列如seq id no.13所示。
60、本发明提供的第二种利用生物酶法高效制备莱鲍迪苷m的方法,是以蔗糖作为糖基供体,在udp存在的条件下,该糖基转移酶可以与蔗糖合成酶进行偶联催化,使莱鲍迪苷a一步生成高价值甜味剂莱鲍迪苷m,无其他中间产物或副产物生成。该方法中,双酶偶联催化反应的最适ph为8.0,最佳反应温度为37℃,mg2+对该偶联催化反应的催化效率有明显的促进提升作用。该方法中,双酶偶联催化的反应时间短,2h内莱鲍迪苷a即被全部转化生成莱鲍迪苷m。
61、该方法利用糖基转移酶和蔗糖合成酶的偶联催化作用,以蔗糖为糖基供体取代昂贵的udpg,高效催化ra一步生成rm,从而降低生产成本。
62、本发明提供的两个方法中,均使用了催化效率较高的糖基转移酶,能够以莱鲍迪苷a为底物,一步催化生成莱鲍迪苷m,实现莱鲍迪苷m的高效生物合成。这两个方法可以减少体系中的金属离子、副产物等杂质,降低分离纯化的成本,以实现莱鲍迪苷m的绿色生物合成。
63、本发明提供的第二个方法中,是以廉价的蔗糖作为糖基供体,大幅度降低生产成本。
64、与现有技术相比,本发明具有如下优点和有益效果:
65、(1)本发明实施例提供的方法中,使用的酶在最佳反应条件下可以高效催化莱鲍迪苷a一步生成莱鲍迪苷m,催化过程中不需要添加其他酶,能够专一性的催化糖基化反应生成莱鲍迪苷m,无中间产物或其他副产物,且反应时间短,催化效率高,产物莱鲍迪苷m的得率可达95%以上,有利于产物的分离提纯;
66、(2)本发明实施例提供的方法中,通过双酶偶联催化可以在最佳反应条件下将莱鲍迪苷a一步催化生成莱鲍迪苷m,无副产物产生,专一性较好,有利于后续的产物分离提纯,以蔗糖作为糖基供体,生产成本低,有利于莱鲍迪苷m大规模生物合成;
67、(3)本发明实施例提供的方法中,反应终体系中只含有微量金属离子(mg2+),无中间产物或副产物,杂质含量极低且易分离,有利于工业化规模生产的后续分离纯化。
- 还没有人留言评论。精彩留言会获得点赞!