一种比率型近红外荧光探针及其合成方法与应用
本发明属于有机小分子比率型荧光探针,具体涉及一种比率型近红外荧光探针及其合成方法与应用。
背景技术:
1、随着生活条件的不断提高,公众对食品安全问题的关注度也日益增加,而生活节奏的加快也导致食品检测朝着快速、准确、高效、安全的方向发展。
2、食品中的肉类或者蛋白质类因微生物的生长,温度,环境等因素的影响被分解称为食品的腐败,而食品腐败会产生生物胺、挥发性物质、微生物以及其代谢产物等,这些物质对人体都具有一定的危害。因此,检测食品腐败对食品安全和人体的健康具有重要的意义。nahso3在亚硫酸盐类漂白剂中还原性和漂白性最强,做为一种被广泛使用的食品添加剂,被用以抑制食物和饮品中由细菌引起的败坏反应、氧化反应和微生物反应。在我国广泛用于果脯、罐头食品类的漂白,最大使用量可达0.40g/kg。虽然nahso3具有防腐等优点,但是过量的添加对人体的危害非常大。因此,检测食品中nahso3的含量对食品安全和人体健康同样具有重要意义。
3、传统检测有机胺、亚硫酸氢根的方法(如化学发光法、色谱法、电化学法、酶法等)存在一些不足,如灵敏度低、选择性差、响应速度慢、样品的预处理及检测过程繁琐等。荧光探针由于其操作简单、响应快速、灵敏度高、选择性好、可定性定量检测等特性近些年来被广泛应用于食品检测领域。其中,比率型荧光探针是荧光分析中的一项重要技术,可有效地消除激发光源强度波动、荧光试剂光漂白和荧光传感分子浓度变化等外在因素引起的背景误差,从而得到更准确的结果。本发明设计了一种能够在不同工作条件下对有机胺和nahso3微量高灵敏度检测的比率型近红外荧光探针,具有现实意义和良好的应用前景。
技术实现思路
1、为解决现有技术中存在的问题,本发明的目的在于提供一种可调控检测nahso3和有机胺的比率型近红外荧光探针及其合成方法与应用,能够高效地选择检测nahso3和食品腐败时产生的微量生物胺,实现对微量nahso3和微量有机胺的可视化、高灵敏度检测。
2、本发明的技术方案如下:
3、本发明的目的之一在于提供一种比率型近红外荧光探针,所述近红外荧光探针标记为fs-b1,分子式为c32h31n2o3+,化学结构式如ⅰ所示:
4、
5、进一步的,荧光探针fs-b 1在乙腈中其最大吸收波长在640nm,荧光光谱波长在765nm。
6、本发明的目的之二在于提供一种比率型近红外荧光探针的合成方法,包括以下步骤:
7、(1)将3-羟基-n,n-二甲基苯胺和苯甲酰乙酸乙酯混合,加热反应,通过分离纯化得到黄色固体,为化合物1,反应过程如下:
8、
9、(2)将化合物1溶解在四氢呋喃溶液中,冷却至0℃,滴加甲基溴化镁,常温条件下充分反应后,将所得溶液用氟硼酸水溶液进行淬灭,并用氟硼酸萃取到dcm中,干燥并分离纯化获得深红色固体,为化合物2,反应过程如下:
10、
11、(3)将所得化合物2和7-(二乙胺基)香豆素-3甲醛溶于无水乙醇中,加入无水乙酸钠后加热回流,除去溶剂后得紫色化合物,分离纯化后,得到近红外荧光探针fs-b1,反应过程如下:
12、
13、进一步的,所述步骤(1)中3-羟基-n,n-二甲基苯胺和苯甲酰乙酸乙酯的摩尔比为1:1.75。
14、进一步的,所述步骤(1)中,加热反应时间为22-25h,加热反应温度为160-200℃。
15、进一步的,所述步骤(1)中,分离纯化过程采用柱层析分离,层析淋洗液为二氯甲烷/甲醇混合溶液,二者体积比为50:1。
16、进一步的,所述步骤(2)中,化合物1和甲基溴化镁的摩尔比为1:1.5。
17、进一步的,所述步骤(2)中,用于淬灭的氟硼酸水溶液浓度为50%,用于萃取的氟硼酸浓度为5%。
18、进一步的,所述步骤(2)和(3)中分离纯化过程采用柱层析分离,层析淋洗液为二氯甲烷/甲醇混合溶液,二者体积比为50:1。
19、进一步的,所述步骤(3)中化合物2、7-(二乙胺基)香豆素-3甲醛、无水乙酸钠的摩尔比为1:1:0.1。
20、进一步的,所述步骤(3)中,回流过程反应温度为80-90℃,反应时间为15-18h。
21、本发明的目的之三在于提供比率型近红外荧光探针在微量有机胺、nahso3高灵敏度检测中的应用。
22、进一步的,当环境中存在有机胺和nahso3时,所述近红外荧光探针fs-b1与有机胺发生亲核加成反应,产生明显的颜色变化。
23、进一步的,随着有机胺、nahso3浓度的增加,所述近红外荧光探针fs-b1在765nm处的发射峰逐渐下降,在483nm处的发射峰逐渐升高,发射峰蓝移了大约165nm;在640nm处的吸收峰逐渐下降,在400nm处的吸收峰逐渐升高,吸收光谱蓝移了大约240nm,溶液颜色由深蓝色变为淡黄色。
24、相较于现有技术,本发明的有益效果在于:
25、1、本发明设计了一种可调控检测nahso3与有机胺的比率型近红外荧光探针fs-b1,是一种较理想的快速灵敏检测有机胺和nahso3的传感器。此近红外荧光探针荧光性能稳定,在乙腈中其最大吸收波长在640nm,荧光光谱波长在765nm,具有反应灵敏且颜色变化明显的比色和比率传感特性。当环境中存在有机胺和nahso3时,此近红外荧光探针能够发生响应快速(30s)、高灵敏度、高选择性和专一性的强烈传感过程,实现对有机胺和nahso3实时定量的检测。
26、2、当本发明所合成的近红外荧光探针fs-b1能够直接检测有机胺和nahso3,当与有机胺、nahso3反应时,无论是紫外可见吸收光谱还是荧光发射光谱都发生蓝移,溶液的颜色从原本的深蓝色,变为浅蓝色、无色,再逐渐变为淡黄色,颜色变化显著,可以直观地从视觉上实现“裸眼”检测有机胺、nahso3,在可视化检测和检测试纸的开发方面具有广阔的应用前景。
27、3、与现有荧光探针技术相比,本发明中近红外荧光探针fs-b1的合成方法简单,操作步骤简易、所需原料的种类较少,并且产率客观,合成过程中不需要高能量激发,对于环境友好,合成的近红外荧光探针能够应用于nahso3和腐败食物中生物胺的安全性评估,在食品安全领域具有良好的发展前景。
28、附图标记
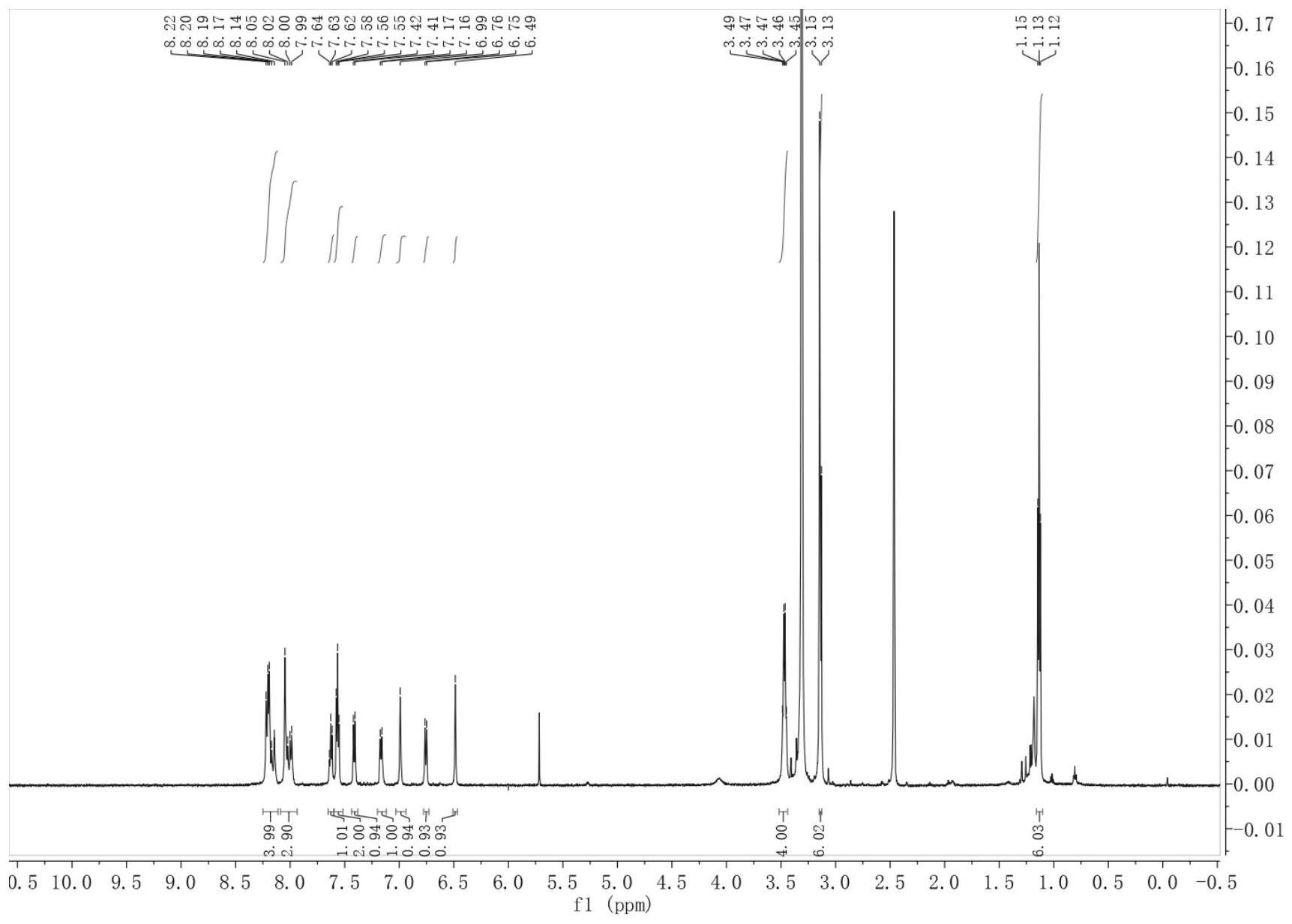
29、图1为本发明实施例1中所合成的近红外荧光探针fs-b1的核磁共振氢谱图;
30、图2为本发明实施例1中所合成的化合物2的核磁共振氢谱图;
31、图3为本发明实施例2中所合成的近红外荧光探针fs-b1用于检测不同天数的实际样品的荧光强度变化图;
32、图4为本发明实施例1中所合成的近红外荧光探针fs-b1在不同极性,不同介电常数的溶剂中与乙二胺作用的紫外光谱特性图;
33、图5为本发明实施例1中所合成的近红外荧光探针fs-b1在有机溶剂和非有机溶剂中与nahso3作用的紫外光谱特性图;
34、图6为本发明实施例1中所合成的近红外荧光探针fs-b1在不同极性,不同介电常数的溶剂中与乙二胺作用的荧光光谱特性图;
35、图7为本发明实施例1中所合成的近红外荧光探针fs-b1在有机溶剂和非有机溶剂中与nahso3作用的荧光光谱特性图;
36、图8为本发明实施例1中所合成的近红外荧光探针fs-b1与不同浓度的乙二胺作用的紫外吸收光谱特性图;
37、图9为本发明实施例1中所合成的近红外荧光探针fs-b1与不同浓度的正己胺作用的紫外吸收光谱特性图;
38、图10为本发明实施例1中所合成的近红外荧光探针fs-b1与不同浓度的二乙烯三胺作用的紫外吸收光谱特性图;
39、图11为本发明实施例1中所合成的近红外荧光探针fs-b1与不同浓度的1,5-戊二胺(尸胺)作用的紫外吸收光谱特性图;
40、图12为本发明实施例1中所合成的近红外荧光探针fs-b1与不同浓度的1,4-丁二胺(腐胺)作用的紫外吸收光谱特性图;
41、图13本发明实施例1中所合成的近红外荧光探针fs-b1与不同浓度的精胺作用的紫外吸收光谱特性图;
42、图14本发明实施例1中所合成的近红外荧光探针fs-b1与不同浓度的酪胺作用的紫外吸收光谱特性图;
43、图15本发明实施例1中所合成的近红外荧光探针fs-b1与不同浓度的组胺作用的紫外吸收光谱特性图;
44、图16本发明实施例1中所合成的近红外荧光探针fs-b1与不同浓度的nahso3作用的紫外吸收光谱特性图;
45、图17本发明实施例1中所合成的近红外荧光探针fs-b1与乙二胺作用的荧光光谱特性图,其中,图17a-b为荧光光谱(a:激发光为415nm,b:激发光为640nm),图17c为483nm处荧光强度与浓度的关系;
46、图18本发明实施例1中所合成的近红外荧光探针fs-b1与正己胺作用的荧光光谱特性图,其中,图18a-b为荧光光谱(a:激发光为415nm,b:激发光为640nm),图18c为483nm处荧光强度与浓度的关系;
47、图19本发明实施例1中所合成的近红外荧光探针fs-b1与二乙烯三胺作用的荧光光谱特性图,其中,图19a-b为荧光光谱(a:激发光为415nm,b:激发光为640nm),图19c为483nm处荧光强度与浓度的关系;
48、图20本发明实施例1中所合成的近红外荧光探针fs-b1与尸胺作用的荧光光谱特性图,其中,图20a-b为荧光光谱(a:激发光为415nm,b:激发光为640nm),图20c为483nm处荧光强度与浓度的关系;
49、图21本发明实施例1中所合成的近红外荧光探针fs-b1与腐胺作用的荧光光谱特性图,其中,图21a-b为荧光光谱(a:激发光为415nm,b:激发光为640nm),图21c为483nm处荧光强度与浓度的关系;
50、图22本发明实施例1中所合成的近红外荧光探针fs-b1与精胺作用的荧光光谱特性图,其中,图22a-b为荧光光谱(a:激发光为415nm,b:激发光为640nm),图22c为483nm处荧光强度与浓度的关系;
51、图23本发明实施例1中所合成的近红外荧光探针fs-b1与酪胺作用的荧光光谱特性图,其中,图23a-b为荧光光谱(a:激发光为415nm,b:激发光为640nm),图23c为483nm处荧光强度与浓度的关系;
52、图24本发明实施例1中所合成的近红外荧光探针fs-b1与组胺作用的荧光光谱特性图,其中,图24a-b为荧光光谱(a:激发光为415nm,b:激发光为640nm),图24c为483nm处荧光强度与浓度的关系;
53、图25本发明实施例1中所合成的近红外荧光探针fs-b1与nahso3作用的荧光光谱特性图,其中,图25a-b为荧光光谱(a:激发光为415nm,b:激发光为640nm),图25c为483nm处荧光强度与浓度的关系;
54、图26本发明实施例1中所合成的近红外荧光探针fs-b1在乙腈溶剂中与不同有机胺作用后的荧光强度变化图。
- 还没有人留言评论。精彩留言会获得点赞!