胺脱氢酶突变体及非α-氨基酸的合成方法
本发明涉及胺脱氢酶突变体及非α-氨基酸的合成方法,属于生物催化工程领域。
背景技术:
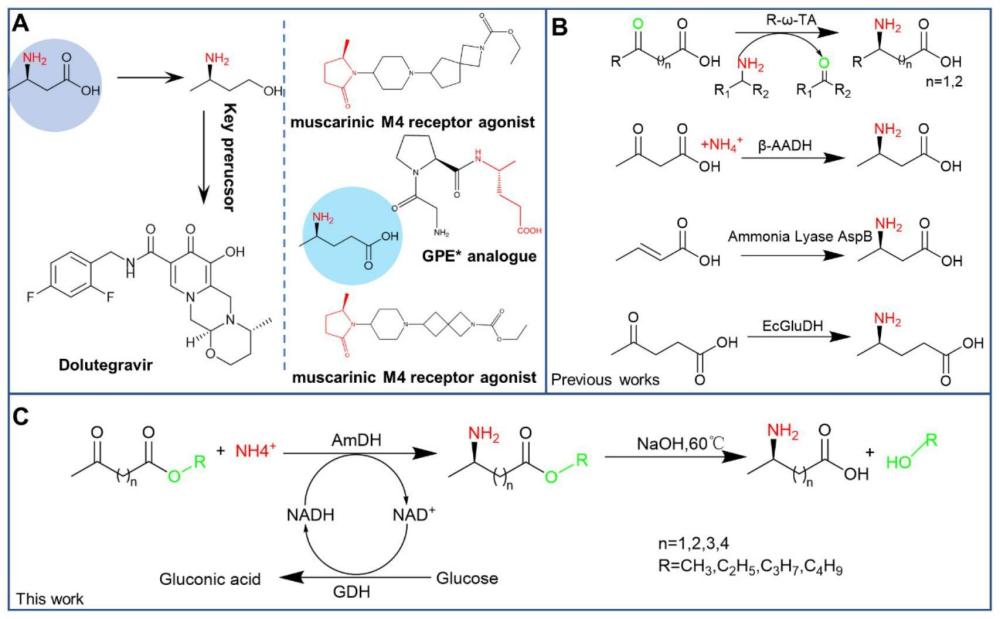
1、根据氨基在碳链上的位置不同,氨基酸可分为α-氨基酸和非α-氨基酸。手性非α-氨基酸在生物技术和精细化工领域有着重要的应用。在制药领域,手性非标准氨基酸是畅销药物的手性基石,如durutevir中的(r)-3-氨基丁酸和某些神经药物中的(r)-4-氨基戊酸(图1中的a)。此外,非α-氨基酸参与肽链折叠,使肽具有抑制蛋白-蛋白相互作用等功能特性。将非α-氨基酸加入酶中,突破了遗传密码只能含有22种天然氨基酸的限制,从而可以设计出效率和特异性更高的生物催化剂,并根据应用需求创造出人工酶。非α-氨基酸可转化为内酰胺,如吡咯烷,是药物、染料和油墨中的关键支架和中间体,也可用作溶剂和表面活性剂。巨大的市场需求凸显了开发新的手性非α-氨基酸合成途径的重要性。
2、手性非α-氨基酸的化学合成面临着巨大的挑战,因为需要在氨基连接的碳原子上精确的手性构型。此外,氨基和羧基在化学合成过程中容易受到破坏,因此需要对其进行保护。传统的非α-氨基酸的化学合成通常采用化学或金属催化剂进行还原性胺化或不对称氢化,这可能对环境不友好,并且具有不一致的立体选择性。近年来,非α-氨基酸的酶不对称合成取得了重大成就,与传统的化学方法相比,提供了一种更温和、更可持续的方法(图1中的b)。氨基转移酶介导的β-氨基酸合成,涉及氨基转移到β-酮酸羰基,由于平衡约束和需要有机胺供体,成本高且效率低。最近,我们通过底物特异性修饰策略成功合成了γ-氨基酸,该策略涉及改变ecgludh谷氨酸脱氢酶的转化特异性识别基团。目前的研究主要集中在酶促合成β-和γ-氨基酸以促进非α-氨基酸的合成。尽管如此,对于生物合成多种非α-氨基酸,特别是对那些远离羧基的取代基如δ和ε-氨基酸,底物特异性仍然是一个挑战。在我们之前的研究中,ecgludh对δ-氨基酸的合成是无效的,因为羧基的强极性阻碍了具有不同取代位点的非α-氨基酸的生成。k92、s378与羧基之间的氢键相互作用阻止了关键催化位点攻击不同取代位置的羰基。如何消除该羧基引起的特异性识别是建立多种非α-氨基酸合成途径的关键。
3、底物工程是调整底物-酶相互作用的关键策略。先前的研究已经证明了其在扩大底物范围和增强对映体选择性方面的功效。在有机合成中,boc、fmoc和sem等保护基团被用来暂时抑制官能团的反应活性,然后在反应后去除它们以产生所需的产物。这个概念可以转移到酶合成,其中非极性基团修饰可以掩盖底物和氨基酸残基之间的强极性相互作用。这种方法绕过了羧基诱导的底物取代位置限制,随后通过简单的化学脱保护便可以获得目标产物。利用酯基来屏蔽羧基诱导的极性作用是底物工程中的一个关键策略,因此需要寻找能够催化酮酯还原胺化的酶。
4、胺脱氢酶(amdhs),包括广泛使用的氨基酸脱氢酶定向进化得到的工程胺脱氢酶及天然胺脱氢酶,它们通过不对称还原胺化催化手性胺的合成,利用具有成本效益的氨供体,实现高产物转化率和对映选择性。含有amdhs的级联催化体系已被开发用于手性胺的合成,具有优异的对映选择性。amdh可以催化侧链上具有非极性基团的小分子。这些研究包括改造底物结合位点以适应更大的非天然底物,将amdh活性扩展到包括双环和杂环酮。目前,amdhs对具有非极性侧链的底物表现出显著的催化潜力,满足催化非极性基团修饰底物的要求。
技术实现思路
1、本研究设计了一种利用amdh的新型酶化学级联,以酮酯为底物合成具有不同取代位置的非α-氨基酸(图1中的c)。构建该级联的两个关键要素包括解除对取代位置的限制和增强amdh对酮酯的催化活性。基于底物工程,将羧基修饰为酯基,去除羰基取代位的限制。底物工程与酶的空间位阻修饰相结合,有效地提高了f-bbamdh对酮类酯的催化活性。β-、γ-、δ-和ε-氨基酸通过一系列酶促反应和化学水解合成。工程突变体丰富了绿色合成非α-氨基酸的工具箱。
2、本发明提供了一种苯丙氨酸胺脱氢酶突变体,所述苯丙氨酸胺脱氢酶突变体为,将氨基酸序列如seq id no.1所示的苯丙氨酸胺脱氢酶的第50位、第124位、第144位、第306位、第309位、第313位中的一个或多个氨基酸进行突变后得到的。
3、seq id no.1:
4、mslvektsiikdftlfekmseheqvvfcndpatglraiiaihdttlgpalggcrmqpynsveealedalrlskgmtyscaasdvdfgggkaviigdpqkdkspelfrafgqfvdslggrfytgtdmgtnmedfihamketncivgvpeayggggdssiptamgvlygikatnkmlfgkddlggvtyaiqglgkvgykvaeglleegahlfvtdineqtleaiqekakttsgsvtvvasdeiysqeadvfvpcafggvvndetmkqfkvkaiagsalnqlltedhgrhladkgilyapdyivnsggliqvadelyevnkervlaktkhiydailevyqqaeldqittmeaanrmceqrmaargrrnsfftssvkpkwdirn
5、在本发明的一种实施方式中,编码亲本酶苯丙氨酸胺脱氢酶的核苷酸序列如seqid no.2所示。
6、seq id no.2:
7、atgtcgttggtggaaaaaacttcaatcattaaggatttcacactgttcgaaaagatgagtgaacatgagcaagttgtcttttgcaatgatcccgcaactggtttacgcgcgatcatcgctatccatgataccactttaggcccagcacttggaggatgtcgcatgcagccttacaatagtgtcgaagaggcattggaggacgcgttgcgcttgtcgaaaggcatgacatatagctgtgcggcctctgacgtggactttggcggcggcaaggcagtgattattggtgatccccaaaaggacaagtccccggagctgtttcgcgcatttggtcagttcgtggatagccttggaggacgtttttacacgggcacagatatggggaccaatatggaagactttattcacgcaatgaaggagacgaattgcatcgtcggagtaccggaggcttatggaggtggaggcgactcgtctattccgactgccatgggggtcctgtatggaatcaaggcaaccaataagatgttgttcggtaaggatgatttaggcggtgttacctacgcgatccagggccttggtaaggtggggtacaaagttgccgaaggtttacttgaagaaggggcacatttgtttgtaaccgatatcaacgaacaaactttagaagccatccaagagaaggcaaagactacttccggctccgtgaccgtggtggcgtccgacgaaatttactcgcaggaagcagatgtgttcgttccctgtgctttcggaggtgtcgtgaacgacgaaaccatgaagcagtttaaagtaaaggcgattgctgggtcagcgctgaatcagttattaaccgaggaccatggccgccacctggccgacaaagggattctgtatgcgcccgactacattgttaattcaggaggccttatccaagtagctgacgaattgtatgaagtgaacaaggaacgtgtgcttgcaaagacaaaacatatctatgacgctatcttagaagtataccagcaggctgaattggatcagattacaaccatggaagctgctaatcgcatgtgcgaacagcgtatggcagcgcgtggtcgccgtaactccttctttacgtctagtgtgaagccgaaatgggacattcgtaattaa
8、在本发明的一种实施方式中,所述苯丙氨酸胺脱氢酶突变体为,将氨基酸序列如seq id no.1所示的苯丙氨酸胺脱氢酶的第50位的亮氨酸突变为丙氨酸得到的,命名为:l50a;
9、在本发明的一种实施方式中,将氨基酸序列如seq id no.1所示的苯丙氨酸胺脱氢酶的第124位的苏氨酸突变为丙氨酸得到的,命名为:t124a;
10、在本发明的一种实施方式中,将氨基酸序列如seq id no.1所示的苯丙氨酸胺脱氢酶的第144位的缬氨酸突变为丙氨酸得到的,命名为:v144a;
11、在本发明的一种实施方式中,将氨基酸序列如seq id no.1所示的苯丙氨酸胺脱氢酶的第306位的亮氨酸突变为丙氨酸得到的,命名为:l306a;
12、在本发明的一种实施方式中,将氨基酸序列如seq id no.1所示的苯丙氨酸胺脱氢酶的第309位的缬氨酸突变为丙氨酸得到的,命名为:v309a;
13、在本发明的一种实施方式中,将氨基酸序列如seq id no.1所示的苯丙氨酸胺脱氢酶的第313位的亮氨酸突变为丙氨酸得到的,命名为:l313a;
14、在本发明的一种实施方式中,将氨基酸序列如seq id no.1所示的苯丙氨酸胺脱氢酶的第309位的缬氨酸突变为丙氨酸,同时将第50位的亮氨酸突变为丙氨酸、甘氨酸或缬氨酸得到的,分别命名为:v309a/l50a、v309a/l50g、v309a/l50v;
15、在本发明的一种实施方式中,将氨基酸序列如seq id no.1所示的苯丙氨酸胺脱氢酶的第309位的缬氨酸突变为丙氨酸,同时将第144位的缬氨酸突变为丙氨酸或甘氨酸得到的,分别命名为:v309a/v144a、v309a/v144g;
16、在本发明的一种实施方式中,将氨基酸序列如seq id no.1所示的苯丙氨酸胺脱氢酶的第309位的缬氨酸突变为丙氨酸,同时将第306位的亮氨酸突变为丙氨酸、甘氨酸或缬氨酸得到的,分别命名为:v309a/l306a、v309a/l306g、v309a/l306v。
17、本发明还提供了编码上述突变体的基因。
18、本发明还提供了携带上述基因的重组载体。
19、本发明还提供了表达上述突变体或携带上述基因或上述重组载体的重组细胞。
20、在本发明的一种实施方式中,所述重组细胞是以细菌或真菌为表达宿主。
21、本发明还提供了一种含有上述苯丙氨酸胺脱氢酶突变体序列的重组酶催化剂,所述催化剂是以下形式中的任意一种:
22、(1)培养所述的重组表达转化体,分离含有所述重组酶的转化体细胞;
23、(2)培养所述的重组表达转化体,分离含有所述重组酶的转化体细胞,对含有所述重组酶的转化体细胞进行破碎,获得的细胞破碎液;
24、(3)培养所述的重组表达转化体,分离含有所述重组酶的转化体细胞,对含有所述重组酶的转化体细胞进行破碎,获得的细胞破碎液,将所述重组酶的细胞破碎液经冷冻干燥而得到的冻干酶粉。
25、本发明还提供了上述苯丙氨酸胺脱氢酶突变体或上述重组细胞或上述重组酶催化剂在催化潜手性酮酸酯类化合物还原制备手性非α-氨基酸中的应用。
26、在本发明的一种实施方式中,所述潜手性酮酸酯类化合物的结构式包括但不限于:
27、
28、在本发明的一种实施方式中,所述应用为,将所述苯丙氨酸胺脱氢酶突变体或所述重组细胞或所述重组酶催化剂,添加至含有葡萄糖脱氢酶、nad+、潜手性酮酸酯类化合物、葡萄糖的反应体系中进行反应,制备得到手性非α-氨基酸。
29、在本发明的一种实施方式中,所述反应体系中还含有nh4oh/nh4cl缓冲液。
30、在本发明的一种实施方式中,所述葡萄糖脱氢酶来源于bacillusamyloliquefaciens。
31、在本发明的一种实施方式中,所述应用为:分别向上述所述苯丙氨酸胺脱氢酶突变体或所述重组细胞或所述重组酶催化剂中添加底物酮酯(1c、2d、3b、4b,50mm,底物溶解于nh4cl/nh4oh缓冲液(ph 9.5,3m))、葡萄糖脱氢酶、nad+、葡萄糖中进行反应。
32、在本发明的一种实施方式中,所述重组突变体酶或重组野生型酶是采用20~40gl-1含有f-bbamdh及其突变体的重组细胞发酵后制备得到的,所述bagludh酶为含有24~48gl-1bagludh的重组细胞发酵后制备得到的,葡萄糖(1.2~120mm),底物1~100mm、nh4oh/nh4cl缓冲液(3m;ph 7~9);30~50℃、0~300rpm、18~24h。
33、在本发明的一种实施方式中,葡萄糖(75mm),nad+(1mm),nh4oh/nh4cl缓冲液(3m;ph 8.5);并将上述反应体系在37℃、200rpm条件下孵育20h。
34、本发明还提供了上述突变体或上述基因或上述重组载体或上述重组细胞或上述方法在食品、生物材料、医药、添加剂或化妆品领域的应用。
35、有益效果
36、(1)我们设计并开发了一种创新的酶化学级联,采用战略性底物工程方法合成具有不同取代位点的非α-氨基酸。该级联利用具有成本效益的无机氨作为胺供体,产生的副产品只有水、增值的葡萄糖酸和易于回收的醇,从而提供了一个绿色和可持续的生物过程。
37、(2)级联途径不仅可以合成常见的β-和γ-氨基酸,还可以合成具有更多远端取代位点的δ-和ε-氨基酸,这是以前用生物学方法无法实现的壮举。
38、(3)为了有效地提高酶的活性,我们对酶和底物进行了基于位阻的工程设计,以寻找最合适的酶-底物匹配。不同底物的活性分别是初始水平的13倍、8倍、9倍和40倍,证明了该策略的有效性。
39、(4)通过该级联途径合成了4种不同取代位置的非α-氨基酸,底物转化率为30.26%~96.58%,立体选择性良好(>99%ee)。
40、(5)这种底物工程与酶进化相结合的思路可以应用于合成更多具有不同取代位置的非α-氨基酸及其衍生物,为这些手性分子的生物合成提供了一种潜在的途径。
- 还没有人留言评论。精彩留言会获得点赞!