一种多维微流控电泳芯片及检测装置,检测方法与流程
本发明涉及微生物检测技术领域,涉及一种多维微流控电泳芯片,以及应用多维微流控电泳芯片的检测装置及检测方法。
背景技术:
在现有的微生物检测技术领域,采用形态学特征、生理生化反应特征等微生物分类检测方法及装置进行微生物检测时,微生物培养耗时长,操作繁琐;而使用基于16s扩增子测序、qpcr、基因芯片、宏基因组和宏转录组的等核酸检测分子生物学技术,存在技术难度大、容易出现假阳性以及成本高的问题;而在蛋白层面上的基于免疫方法的检测装置,成本较高,并且能检测的种属受限于所能得到的抗体。
在本世纪初期,nishimotoh在专利文献(jp2003114215a)就公开了一种用于化学/生物分析的电泳芯片,采用简单的“十字交叉”结构实现westernblot。然而上述专利技术事实上依然只是一维凝胶电泳技术,在面对细胞、微生物等具有复杂蛋白组分的生命体时,分离以及分析能力都存在限制。
为了提升电泳的分离能力,随后出现的电泳微流控芯片在一段时间内的改进主要集中在设计“二维”电泳微流控芯片。例如,毛秀丽在专利文献(cn1469123a)公开了一种蛋白质分析用微流控芯片及其在蛋白质分析中的应用,其设计的微流控芯片在“十字交叉”结构的基础上,进一步增加了包含多个通道的基本单元。再例如,林炳承在专利文献(cn1779431a)公开的芯片包括第二个单元,第二单元为蛋白质浓缩后的电泳分离分析。该芯片的进样通道可以为t字型结构。其它涉及通道整体结构和形态结构调整专利技术还包括,cn2831115y,cn1786988a,cn104148123a,cn105092677a,cn104297327a,us2014332382a1,us8728290b1等。
就本申请发明人所知,非专利技术文献1(emrichca,medintzil,chuwk,etal.microfabricatedtwo-dimensionalelectrophoresisdevicefordifferentialproteinexpressionprofiling[j].analyticalchemistry,2007,79(19):7360-7366.)首次提及了在两维通道之间加工超细的通道进行连接,产生的阻力以阻止扩散并同时降低扩散的体积。尽管上述文献中实施的超细通道设计方式在电泳技术领域中并不少见,例如us2011220499a1,jp2005233944a。但是将其设计在两维通道之间以提高蛋白分离能力,却需要综合考虑等电聚焦通道特性以及凝胶电泳通道特性,使其与电泳领域的一般设计方式显著区分开。以至于,后续很多多维电泳芯片技术都借鉴参考,例如非专利技术文献2(westj,beckerm,tombrinks,etal.micrototalanalysissystems:latestachievements[j].analyticalchemistry,2008,80(12):4403-4419.)
然而,在实际的电泳分离实验过程中,非专利技术文献1中的设计方式却依然存在对于蛋白分离效果欠佳或者与不增加超细的通道的多维微流控电泳芯片蛋白分析效果区分不明显的情况。有鉴于此,本申请首先提出设计一种多维微流控电泳芯片,其能够改善蛋白分离效果不佳的问题。同时提出一种检测系统,其包括上述多维微流控电泳芯片,能够应用于微生物等生物样品进行分析识别,包括但不仅限于基于蛋白质分离荧光图像进行微生物等生物样品的检测。进一步,还包括一种检测方法,其使用本申请提出的检测装置,通过获取高分辨分离图像并借助图像解析技术鉴别单独以及混合微生物。具体分离和分析的技术实现方式可以参照以下提供的非专利技术文献3-10:
非专利技术文献3,fengminglin,xiaochaozhao,jianshewang,shiyongyu,xuefeilv,yulindeng,linageng*,huajunli*,anovelmicrofluidicchipelectrophoresisstrategyforsimultaneous,label-free,multi-proteindetectionbasedonagrapheneenergytransferbiosensor,analyst,2014(139),2890-2895.
非专利技术文献4,linxia,fengminglin,xinwu,jianshewang,chuanliliu,qitang,shiyongyu,kunjiehuang,xuefeilv,yulindeng,linageng*,on-chipproteinisoelectricfocusingusingaphoto-immobilizedphgradient,j.sep.sci.,2014nov;37(21):3174-80
非专利技术文献5,nihou,yuchen,shiyongyu,zongliangquan,hanzhu,chenhuapan,yulindeng,linageng*,nativeproteinseparationbyisoelectricfocusingandbluegelelectrophoresis-coupledtwo-dimensionalmicrofluidicchipelectrophoresis,chromatographia,chromatographia,2014(77)1339-1346
非专利技术文献6,fengminlin,shiyongyu,legu,xuetaozhu,jianshewang,hanzhu,yilu,yihuawang,yulindeng,linageng,insituphoto-immobilisedphgradientisoelectricfocusingandzoneelectrophoresisintegratedtwo-dimensionalmicrofluidicchipelectrophoresisforproteinseparation,microchimicaacta,2015,182(13-14):2321-2328
非专利技术文献7,shiyongyu,jiandongxu,kunjiehuang,juanchen,jinyanduan,yuanqingxu,hongqing,linageng*andyulindeng*,anovelmethodtopredictproteinaggregationsusingtwo-dimensionalnativeproteinmicrofluidicchipelectrophoresis,anal.methods,2016,8,8306-8313
非专利技术文献8,yilu,shiyongyu,fengminglin,fankailin,xiaochaozhao,liqingwu,yunfeimiao,huanjunli,yulindeng,linageng*,simultaneouslabel-freescreeningofg-quadruplexactiveligandsfromnaturalmedicineviaamicrofluidicchipelectrophoresis-basedenergytransfermulti-biosensorstrategy.,analyst.2017,142(22):4257-4264.
非专利技术文献9,zerongliao,jianfengwang,pengjiezhang,yangzhang,yunfeimiao,shimenggao,yulindeng,linageng*,recentadvancesinmicrofluidicchipintegratedelectronicbiosensorsformultiplexeddetection,biosensorsandbioelectronics,2018,121(15)272-280
非专利技术文献10,zerongliao,yangzhang,yongruili,yunfeimiao,shimenggao,yulindeng,linageng*,microfluidicchipcoupledwithopticalbiosensorsforsimultaneousdetectionofmultipleanalytes:areview,biosensorsandbioelectronics,2019,126(1)697-706
技术实现要素:
为实现上述目的,本发明的具体方案如下:
本发明首先涉及一种多维微流控电泳芯片,所述多维微流控电泳芯片设有电泳分离通道的电泳载台,其包括至少包括一组缓冲液储液单元(b,bw);至少包括一组上样/酸碱液储液单元(s,sw);其中,所述上样/酸碱液储液单元s和sw通过芯片电泳通道连通;每个缓冲液储液单元通过凝胶电泳通道与等电聚焦通道连通;至少部分凝胶电泳通道和等电聚焦通道的交接处存在过渡段。
仅作为本发明的一种实施方式,具体的,所述过渡段具有不均匀的横截面面积。所述截面面积的不均匀是因为过渡段在宽度方向上的不均匀引起的,或者所述截面面积的不均匀是因为过渡段在深度方向上的不均匀引起的。优选的,所述过渡段至少包括一个通道宽度逐渐收窄的半圆或者椭圆形结构;优选的,所述过渡段具有至少一组串联的对称的通道形态。
仅作为本发明的另一种实施方式,具体的,所述过渡段至少包括一个非对称的通道形态。优选的,所述非对称的通道形态,可以是一个通道宽度逐渐收窄的倒梯形结构,或者其它常见的几何结构的非对称化。
具体的,所述等电聚焦通道宽度大于所述凝胶电泳通道宽度。
具体的,所述等电聚焦通道为弧线形,所述缓冲液储液单元b为弧线形凹槽,所述缓冲液储液单元bw位于等电聚焦通道圆心处。
具体的,所述等电聚焦通道分别与缓冲液储液单元以及上样/酸碱液储液单元相连。
具体的,本发明还包括将缓冲液储液单元bw具体设置在所述电泳载台外,所述多维微流控电泳芯片(3)还包括毛细管,外置的缓冲液储液单元bw通过两个以上的毛细管与设置在电泳载台上的凝胶电泳通道相连。
本发明进一步涉及一种检测装置,其包括本发明具体限定的多维微流控电泳芯片,并进一步包括数据采集模块(1)、数据解析模块(2)以及高压电源模块(4),所述数据采集模块(1)用于采集待检测物的分离图像;所述数据解析模块(2)用于对所述数据采集模块(1)采集的分离图像进行图像处理,以获得待检测物的成分信息。
本发明进一步还涉及一种检测方法,其包括本发明的检测装置,其电泳和检测过程包括如下步骤:
步骤1,先对多维微流控电泳芯片的电泳通道进行冲洗和前处理;
步骤2,在多维微流控电泳芯片电泳通道内注入凝胶,然后在缓冲液储液单元b以及缓冲液储液单元bw两个储液单元施加电压一段时间,完成预电泳;
步骤3,在多维微流控电泳芯片的等电聚焦通道内注入样品与等电聚焦两性电解质的混合物,或者在已预先形成固定化等电聚焦梯度的等电聚焦通道内注入样品;
步骤4,在等电聚焦通道两端的上样/酸碱液储液单元s和sw中施加电压进行等电聚焦,等电聚焦完成后停止加电;
步骤5,在凝胶电泳通道两端施加电压将第一维等电聚焦完毕后的样品转移至第二维凝胶电泳通道,然后进行凝胶电泳分离;
步骤6,利用数据采集模块采集芯片电泳分离图像,进行生物样品分析。
有益效果:
本发明采用多维微流控电泳芯片进行电泳分离,多维微流控电泳芯片中设有等电聚焦通道和两个以上的凝胶电泳通道,两个以上的凝胶电泳通道提高了下凝胶电泳通道中凝胶电泳的分离通量,进而获得高分辨分离荧光图像。然后借助图像数据分析工具和手段实现微生物快速鉴别,装置成本低、鉴别效率高。
本发明多维微流控电泳芯片中,所述过渡段的非均匀截面面积设计能够进一步改善流体流动,改善分离,进而得到更高分辨率的分离图谱。
对于一些实施方式,所述过渡段的改进在于调整通道宽度和结构形态。具体采用圆形或者椭圆形的结构,可以实现在给定长度和/或深度的前提下,具有更大的储液能力,这主要是因为圆形是周长给定情况下,面积最大的几何结构。本发明技术方案通过局部形态的调整,可以实现聚集储液能力相较于非专利技术文献1至少百分之20以上的提升。
对于一些实施方式,所述过渡段的改进在于具有非对称的通道结构,所述非对称的结构会使得在通道结构的两侧,产生不一致的阻力,从而使得蛋白迁移在一侧的速度与另一侧产生差距,更加有利于实现蛋白在凝胶电泳通道里的分离迁移顺次进行,进而得到更高分辨率(更多蛋白谱峰)的分离图谱。
对于一些实施方式,所述过渡段的改进在于所述过渡段具有至少一组串联的对称的通道形态,采用多次条带累积效果,减少条带扩展,提高检出灵敏度。
附图说明
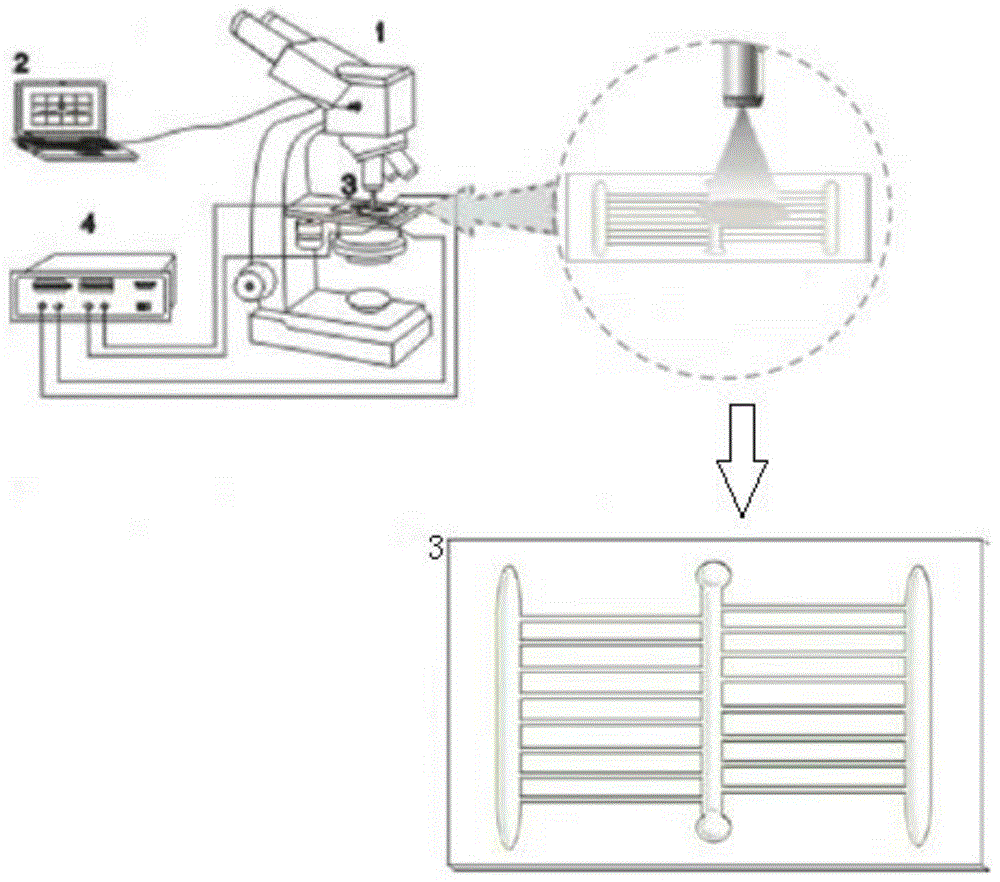
图1为本发明的整体装置图,其中,1-数据采集模块,2-数据解析模块,3-多维微流控电泳芯片,4-高压电源模块;
图2为普通阵列式多维微流控电泳芯片通道结构示意图;
图3为普通阵列式多维微流控电泳芯片实物模拟图
图4为发散形阵列通道式多维微流控电泳芯片通道结构示意图;
图5为外接阵列毛细管的多维微流控电泳芯片通道结构示意图;
图6为耦联板式凝胶电泳的多维微流控电泳芯片通道结构示意图;
图7为不同过渡段结构示意图;
图8为缓冲液储液单元为分离式的多维微流控电泳芯片通道结构示意图;
图9为缓冲液储液单元为分段式的多维微流控电泳芯片通道结构示意图;
图10为上样储液单元(s和sw)与酸碱液储液单元(a和b)分离的多维微流控电泳芯片通道结构示意图。
具体实施方式
下面结合附图并举实施例,对本发明进行详细描述。
微流控芯片是现代生物分析装置向小型化、一体化和自动化发展的前沿领域,有望为微生物检测和定量分子提供快速简便和高效平台。其中,多维微流控电泳芯片以其易于整合的优势,通过构建多维分离平台可以获得更高的分离能力,进而为得到高分辨分离图像,实现微生物等生物样品鉴定/检测创造机会。
实施例1:本发明提供了一种基于多维微流控电泳芯片的微生物检测装置,整体装置如图1所示,包括多维微流控电泳芯片3、数据采集模块1、数据解析模块2以及高压电源模块4;
所述多维微流控电泳芯片3用于产生样品的分离图谱;
所述多维微流控电泳芯片3包括不少于四个储液单元以及设有电泳分离通道的电泳载台;
所述高压电源模块4用于给多维微流控电泳芯片提供电泳电源,输出0-5000v的多路电压,通过可编程多步电压控制,切换快速,输出电压稳定。
所述储液单元用于放置电泳液,四个储液单元分别记为缓冲液储液单元b、缓冲液储液单元bw、上样/酸碱液储液单元s、上样/酸碱液储液单元sw;所述电泳液包括电泳各阶段所用的液体;
所述电泳分离通道包括凝胶电泳通道与等电聚焦通道,所述凝胶电泳通道包括上凝胶电泳通道和下凝胶电泳通道;
其中,所述上样/酸碱液储液单元s和上样/酸碱液储液单元sw通过一个通道连通,该通道为等电聚焦通道;缓冲液储液单元b、缓冲液储液单元bw分别设置在等电聚焦通道两侧;缓冲液储液单元通过不少于两个通道与等电聚焦通道连通,即缓冲液储液单元b与等电聚焦通道之间的通道为上凝胶电泳通道,缓冲液储液单元bw与等电聚焦通道之间的通道为下凝胶电泳通道;
数据采集模块1用于采集通过多维微流控电泳芯片3电泳分离获得的分离图像,数据采集基于光学探测来实现,可以通过倒置显微镜,对准阵列通道或者阵列毛细管末端区域,通过ccd对荧光倒置显微镜中的分离图像进行采集,也可以通过在在阵列通道或者毛细管的末端安装阵列光纤进行数据采集。
可以采用倒置显微镜等图像采集器件同时对多通道进行数据采集,也可以采用阵列光纤等分别收集每一个通道的分离信号。
数据解析模块2用于对数据采集模块1采集的分离图像进行图像处理,以获得待检测微生物的成分信息。
图像处理的步骤包括:
①读入分离图像;
②对分离图像进行图像预处理,主要包括图像归一化和简单的去除噪声;
③对分离图像的图像数据直方图进行分析,并计算图像的熵值和对应分布的统计量,其中参考指标分别为峰度以及偏度,获得待检测微生物的成分信息。
为方便上样,设置所述等电聚焦通道宽度大于凝胶电泳通道;多维微流控电泳芯片为等电聚焦与凝胶电泳偶联的基本形式,本发明中多维微流控电泳芯片结构设计目的是提高凝胶电泳通道中凝胶电泳的分离通量,进而获得高分辨分离荧光图像。多维微流控电泳芯片中设有第一维等电聚焦通道和第二维凝胶电泳通道,第二维凝胶电泳通道采用多通道并行结构,提高芯片电泳的分离通量。
如图2所示多维微流控电泳芯片的电泳分离通道为普通阵列式多维微流控电泳芯片通道结构,图2左图中的上样/酸碱液储液单元s和上样/酸碱液储液单元sw之间为等电聚焦通道,其长度、宽度、深度分别为23mm、150um、30um;等电聚焦通道为直线形,缓冲液储液单元b、缓冲液储液单元bw为直线凹槽,所述凝胶电泳通道相互平行,等电聚焦通道和缓冲液储液单元b之间为16个平行的上凝胶电泳通道,其常规长度、宽度、深度分别为18mm、50um、30um;等电聚焦通道和储液单元bw之间为16个平行的下凝胶电泳通道,其常规长度、宽度、深度分别为32mm、100um、30um。
多维微流控电泳芯片通过掩模制作、光刻、湿法刻蚀、打孔以及键合等步骤制作获得,得到的实体展示如图3,其制作的工艺步骤可以具体参照非专利技术文献11(蛋白质分离玻璃微流控芯片的制作方法,耿利娜,全宗良,侯妮,陈娟,高丽娜,徐建栋,胡定煜,李勤,邓玉林,北京理工大学学报,2013,33(4),436-440)。
实施例2:发散形阵列通道式多维微流控电泳芯片,与实施例1的区别主要在于多维微流控电泳芯片电泳分离通道结构不同,发散形阵列通道式多维微流控电泳芯片通道结构如图4所示,上样/酸碱液储液单元s到上样/酸碱液储液单元sw之间的等电聚焦通道为弧线形,缓冲液储液单元b为弧线形凹槽,上凝胶电泳通道之间相互平行,缓冲液储液单元bw位于等电聚焦通道圆心处,缓冲液储液单元bw可以采用弧线形凹槽,也可以采用圆形凹槽;缓冲液储液单元bw采用弧线形凹槽时,缓冲液储液单元bw的两个以上的下凝胶电泳通道呈发散式连接到等电聚焦通道;缓冲液储液单元bw采用圆形凹槽时,缓冲液储液单元bw的下凝胶电泳通道呈发散式连接到等电聚焦通道。
实施例3:外接阵列毛细管的微流控芯片,电泳载台可以采用与实施例1或实施例2相同的结构,但缓冲液储液单元bw设置在电泳载台之外,另外,多维微流控电泳芯片还包括毛细管,如图5所示,外置的缓冲液储液单元bw通过两个以上的毛细管与设置在电泳载台上的的下凝胶电泳通道相连,下凝胶电泳通道通过毛细管与缓冲液储液单元bw连通。
实施例4:耦联板式凝胶电泳的微流控芯片,如图6所示,耦联板式凝胶电泳的微流控芯片的下凝胶电泳通道包括两个以上的连接通道以及凝胶电泳凹槽,连接通道分别连通整块凝胶电泳凹槽后,通过整块凝胶电泳凹槽连通缓冲液储液单元bw,其他部分与实施例1或实施例2相同。
实施例5:具有过渡段的微流控芯片,所述过渡段存在于等电聚焦通道与凝胶电泳通道衔接处的通道段,过渡段设置具体可以参考图7所示。其余部分可以采用如实施例1-4的任一实施例结构,如图2-图6部分给出了非专利文献1中倒置漏斗形的结构放大图。以等电聚焦通道为观测起点,所述凝胶电泳通道开始的宽度较窄,然后变宽,图中用局部放大图示出了倒置漏斗结构。本发明的过渡段结构改进可以进一步有效的减轻上样之后样品的浓度扩散,并且减小了向等电聚焦通道连接的储液单元加负压时对凝胶电泳通道中纤维素凝胶的吸力,保证上样时凝胶电泳通道清洗过程的顺利进行,提高了电泳分离时,样品的凝胶电泳的分离通量,有助于得到高分辨的分离图像。
以蛋白样品为例,基于多维微流控电泳芯片对样品进行电泳分离的流程包括:
a.芯片前处理:新制得的芯片依次用1mol/l的盐酸处理1h,用三蒸水处理0.5h。每次实验之前先用三蒸水冲洗10min,后用1mol/l的naoh溶液处理10min,再用三蒸水冲洗10min,之后用pbs溶解的bsa(或其他涂层物质)冲洗30min,最后用加有bsa的甲基纤维素溶液处理15min。每次实验之后先用三蒸水冲洗10min,再用98%h2so4处理通道。
b.上样:
①芯片通道冲洗完毕之后,分别将4个储液单元的残液吸干,并用滤纸将芯片表面擦干,之后注入与储液单元等体积的bsa的纤维素凝胶;
②向缓冲液储液单元b、缓冲液储液单元bw两个储液单元两端加电一段时间,完成预电泳;
③分别将4个储液单元的残液吸干,上样/酸碱液储液单元s中注入与其等体积的超纯水,同时缓冲液储液单元b、缓冲液储液单元bw两个储液单元分别注入与其同体积的bsa的纤维素凝胶;
④给上样/酸碱液储液单元sw加较大的负压,直至上样/酸碱液储液单元s里的三蒸水液面能够快速下降;
⑤保持缓冲液储液单元b、缓冲液储液单元bw不变,将上样/酸碱液储液储液单元s、上样/酸碱液储液单元sw操作对换后,分别吸干上样/酸碱液储液单元s、上样/酸碱液储液单元sw的残液;
⑥将样品注入上样/酸碱液储液单元s,然后往上样/酸碱液储液单元sw上加短时、极小的负压;使样品进入一维分离通道即等电聚焦通道;
⑦将上样/酸碱液储液单元s、上样/酸碱液储液单元sw残液吸干并分别加入等体积的酸、碱液,后将缓冲液储液单元b、缓冲液储液单元bw两个储液单元的液面补平。
c.电泳分离:首先进行等电聚焦实验,分别将电源的正负极加到酸碱池上,施加电压进行等电聚焦。聚焦完成之后撤下等电聚焦电极,接着进行凝胶电泳实验,缓冲液储液单元b加正电极,缓冲液储液单元bw加负电极,根据分离条带的位置实时调整芯片位置保证分离条带一直处于荧光诱导显微镜视野之内。实验中利用本发明所述多维微流控电泳芯片对大肠杆菌全蛋白、枯草芽孢杆菌全蛋白、金黄色葡萄球菌全蛋白进行了分离。
在蛋白得到初步分离之后,利用数据采集模块每隔2min截取一张图片,共截取15张图片,对图像进行了噪音去除,灰度图像转换的初步处理,采用一种基于峰强度概率分布的方法进行特征提取,形成谱图的指纹特征,再采用多元统计技术将多维特征降维至二维。使用训练集样品按照已知微生物种类信息完成分类训练后,即可测试未知样品。
实施例6:为缓冲液储液单位为分离式的多维微流控电泳芯片,如图8所示。与实施例2发散形阵列通道式多维微流控电泳芯片的区别主要是缓冲液池采用孤立式,每个储液池配制一个电极,多电极并联。
实施例7:为缓冲液储液单位为分段式的多维微流控电泳芯片,如图9所示。与实施例2发散形阵列通道式多维微流控电泳芯片的区别主要是缓冲液池的长度减小,每个储液池配制一个电极,多电极并联。
实施例:8:如图10所示为上样储液单元(s和sw)与酸碱液储液单元(a和b)分离的多维微流控电泳芯片,。与实施例2发散形阵列通道式多维微流控电泳芯片的区别在于,单独另有一套酸碱池,与样品池s和sw分离。实施例10所示的芯片进行电泳时,在样品池s和sw之间完成上样后,直接在酸碱池加电进行样品等电聚焦,之后再在b和bw池加电完成第二维凝胶电泳。
应当注意,本发明所用词汇中,“包括”、“包含”或“具有”及其变型的使用意指包含其后列出的项目及其等同物以及另外项目。除非另外限制,术语“交接”、“连通”及其变型在这里被概括地使用并且包括直接的和间接的连通、交接。
本发明公开的量纲和值不应理解为严格限于所引用的精确数值。相反,除非另外指明,否则每个这样的量纲旨在表示所述值以及围绕该值功能上等同的范围。例如,公开为“40mm”的量纲旨在表示“约40mm”。
在发明文字中引用的所有文件都在相关部分中以引用方式并入本文中。对于任何文件的引用不应当解释为承认其是有关本发明的现有技术。当本发明中术语的任何含义或定义与以引用方式并入的文件中术语的任何含义或定义矛盾时,应当服从在本发明中赋予该术语的含义或定义。
本发明的原理,代表性实施例和操作模式已经在前述描述中被描述。然而,意图被保护的本发明的数个方面将不被解释为限于所公开的特别实施例。此外,本文所描述的实施例将被看作说明性的而不是限制性的。将理解的是,通过使用其它和等同内容可以作出变化和改变而不偏离本发明的精神。因此,明确地预期所有这些变化、改变和等同内容落在如要求保护的本发明的精神和范围内。
- 还没有人留言评论。精彩留言会获得点赞!