蛋白修饰的聚合物微球复合材料、其制备方法及应用与流程
本发明涉及聚合物微球技术领域,且特别涉及蛋白修饰的聚合物微球复合材料、其制备方法及应用。
背景技术:
聚合物微球通常是指形状为球形的高分子聚集体,一般直径在纳米至微米尺度。目前应用于该类微球的材料主要有无机材料、天然高分子及合成高分子,按照降解性能又分为降解类材料及非降解类材料。聚酯类是目前研究最多、应用最广泛的可生物降解的合成高分子材料,如聚乳酸、聚乙醇酸、聚ε-己内酯、聚β-羟基丁酸、聚β-羟基戊酸以及它们的共聚物。乳酸-乙醇酸的共聚物是被美国食品药品管理局批准应用于临床的高分子材料,具有良好的生物相容性。
目前,利用蛋白结合类溶质制备微球材料主要采用传统的装载模式,如中国专利CN201910276078、中国专利CN201910066613、中国专利CN201611014952等。但是,现有技术普遍存在着应用时突释效应较强的问题,而且工艺较为复杂难以进行产业化应用。
技术实现要素:
本发明的目的在于提供一种蛋白修饰的聚合物微球复合材料及其应用,旨在降低应用时的突释效应,达到长久缓释的效果,可以作为缓释材料得到应用。
本发明的另一目的在于提供一种蛋白修饰的聚合物微球复合材料的制备方法,其利用蛋白修饰聚合物对蛋白结合溶质进行包覆制备微球材料,能够在应用时有效降低突释效应、增强缓释和控制释放的作用。
本发明解决其技术问题是采用以下技术方案来实现的。
本发明提出了一种蛋白修饰的聚合物微球复合材料,包括能与蛋白结合的蛋白结合溶质和包覆蛋白结合溶质的蛋白修饰聚合物,其中,蛋白修饰聚合物是聚合物经蛋白修饰而得。
本发明还提出一种蛋白修饰的聚合物微球复合材料的制备方法,包括如下步骤:
采用蛋白修饰聚合物对蛋白结合溶质进行包覆以形成聚合物微球复合材料。
本发明还提出聚合物微球复合材料在作为缓释材料中的应用。
本发明实施例提供一种蛋白修饰的聚合物微球复合材料的有益效果是:其通过蛋白对聚合物进行化学修饰形成蛋白修饰聚合物,利用该蛋白修饰聚合物对蛋白结合溶质进行包覆形成微球材料。发明人发现,由于蛋白对蛋白结合溶质的作用使微球材料在应用时能达到长久缓释的效果,有效降低了突释效应。
本发明还提供了一种蛋白修饰的聚合物微球复合材料的制备方法,其通过采用蛋白修饰聚合物对蛋白结合溶质进行包覆以形成聚合物微球,方法简便易行适合于工业化应用,制备得到的微球材料缓释性能好,突释效应很低,可以作为优良的缓释材料得到应用。
附图说明
为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
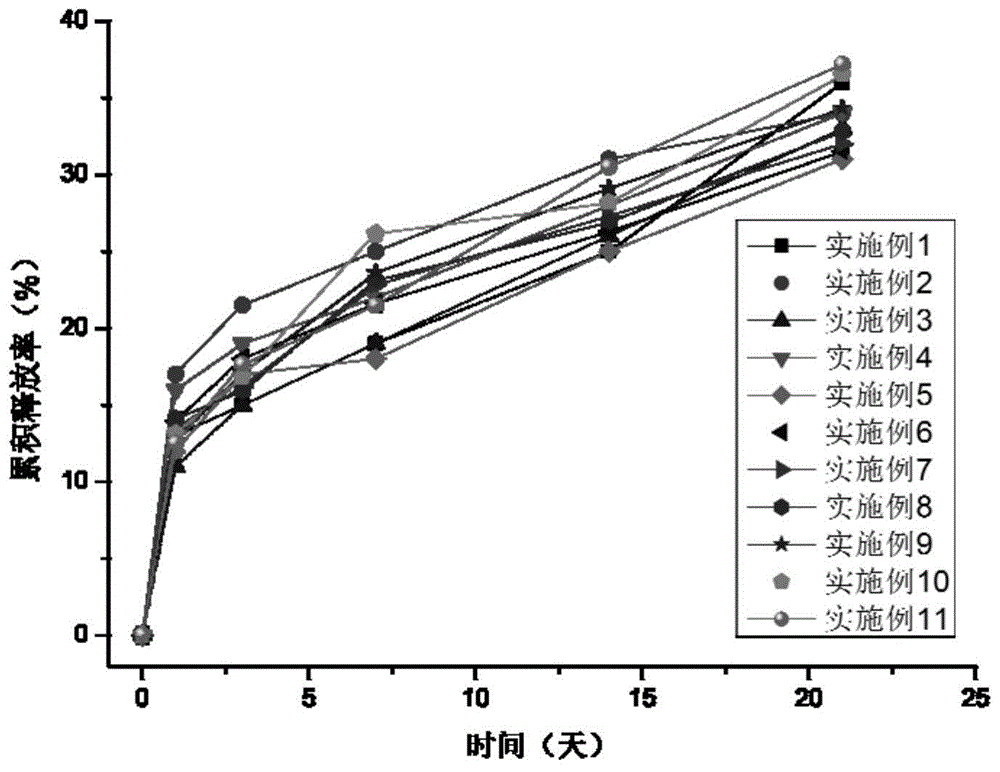
图1为本发明实施例体外溶质释放行为的测试结果图;
图2为本发明实施例和对比例体外溶质释放行为的测试结果图。
具体实施方式
为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
下面对本发明实施例提供的蛋白修饰的聚合物微球复合材料、其制备方法及应用进行具体说明。
本发明实施例提供的一种蛋白修饰的聚合物微球复合材料的制备方法,其包括如下步骤:采用蛋白修饰聚合物对蛋白结合溶质进行包覆以形成聚合物微球。发明人发现,利用蛋白对蛋白结合溶质的作用使微球材料在应用时能达到长久缓释的效果,有效降低了突释效应。
制备微球材料的方法可以参照现有技术,发明人对制备方法进行了优化以进一步提升材料的缓释性能,包括:
S1、蛋白修饰聚合物的制备
将蛋白溶液与含有羧基的聚合物溶液混合反应后,分离固体产物。利用蛋白中的胺基和聚合物中的羧基结合进行修饰,形成微球材料的主要原料。
优选地,混合反应过程是在pH为7-8的条件下搅拌4-8h;在一些实施例中可以采用磷酸盐缓冲液进行pH的调节,蛋白和聚合物的反应在弱酸性条件下能够快速反应,在溶液中沉积下来。
在一些实施例中,在分离固体产物之后,进行水洗并干燥。通过水洗去除未反应的原料和附着在固体上的磷酸盐等杂质,经过干燥后得到纯净的蛋白修饰聚合物产品,便于进行后续操作。
在聚合物与蛋白反应之前进行羧基活化,羧基活化的过程包括:将聚合物粉末与羧基活化溶液混合反应4-6h,分离固体;优选地,分离固体后进行水洗、干燥。发明人发现,采用1-(3-二甲胺基丙基)-3-乙基碳二亚胺盐酸盐和N-羟基琥珀酰亚胺形成的水溶液对聚合物粉末进行活化为宜,能够显著增强聚合物中羧基的官能团强度,在后续与蛋白结合时增强与蛋白的结合强度。在分离固体后通过水洗去除未反应的原料,干燥后便于进行后续反应。
优选地,1-(3-二甲胺基丙基)-3-乙基碳二亚胺盐酸盐在羧基活化溶液中的浓度为1-3mg/mL,N-羟基琥珀酰亚胺在羧基活化溶液中的浓度为1-2.5mg/mL。羧基活化溶液中两种原料的浓度控制在上述范围内为宜,以充分活化聚合物中的羧基,提升与蛋白的结合强度。
在优选地的实施例中,聚合物粉末是由块状聚合物原料进行预处理而得,预处理过程包括:将块状聚合物原料溶解后形成的溶液和质量分数为4-6%聚乙烯醇水溶液混合乳化得到乳液;将乳液与质量分数为0.2-1%的聚乙烯醇水溶液混合8-12h,分离固体粉末,并对固体粉末进行水洗、干燥。一般市购原料为块状,直接进行反应不利于制备得到均匀一致的产品,但是采用研磨的方式不能达到纳米级别的尺寸要求。发明人发现,采用上述的预处理方法能够将块状聚合物分散形成纳米尺寸的粉末,适合于作为缓释微球材料的原料。具体地,混合乳化的过程是在2000-4000rpm的转速下搅拌2-5min。发明人进一步调控反应过程中的参数,以降低得到聚合物粉末的粒径。
优选地,聚合物选自聚3-羟基烷酸酯、聚乳酸、聚己内酯、聚乳酸-羟基乙酸共聚物、聚3-羟基丁酸酯-co-3-羟基戊酸酯、聚(3-羟基丁酸酯)、聚丁二酸丁二酯和聚三亚甲基碳酸酯中的至少一种。以上几种聚合物均适合于本发明实施例提供的反应体系,能够进行蛋白修饰并装载蛋白结合类溶质,能够保证最终制备得到的微球材料的缓释性能。以上几种聚合物均为市购原料,聚合物的分子量一般控制在0.3-300万道尔顿。
蛋白选自白蛋白、脂蛋白和转运蛋白中的至少一种。其中,白蛋白包括人血清白蛋白、牛血清白蛋白和鸡血清白蛋白;脂蛋白包括乳糜微粒、极低密度脂蛋白、中间密度脂蛋白、低密度脂蛋白和高密度脂蛋白;转运蛋白包括有机阴离子转运蛋白。以上几种蛋白均为现有材料,如极低密度脂蛋白、中间密度脂蛋白、低密度脂蛋白和高密度脂蛋白等,均为常规理解的原料,其具体参数不做过多赘述,以上蛋白均购自Sigma公司。本发明实施例使用来源于自然的蛋白修饰可降解高分子,得到既对蛋白结合溶质有较好亲和力、且不明显影响其降解性能的蛋白修饰可降解高分子。
S2、微球的形成
将蛋白结合溶质与蛋白修饰聚合物溶液混合溶解后得到成球混合液;将成球混合液与表面活性剂溶液混合形成微球材料。形成微球材料的原理属于现有技术,其利用表面活性剂的分散效果,形成尺寸较小的微球材料。
蛋白结合溶质选自硫酸对甲酚、硫酸吲哚酚、马尿酸、双香豆素、华法林钠、乙酰水杨酸、复方甲硝唑、红霉素、西咪替丁、乙酰胺基酚、氯贝丁酯、同型半胱氨酸、3-羧基-4-甲基-5-丙基-2-呋喃丙酸、吲哚-3-乙酸、胆固醇、甘油三酯和苏丹红中的至少一种;优选为乙酰水杨酸、双香豆素、复方甲硝唑和华法林钠中的至少一种。以上几种蛋白结合溶质均具备蛋白结合特性,在形成微球材料后达到长久缓释的效果,有效降低材料的突释效应。蛋白结合溶质通过静电力、氢键、亲疏水作用力等非共价键与蛋白结合。
进一步地,表面活性剂选自聚乙烯醇、明胶、吐温、甲基纤维素和司盘中的至少一种;优选地,表面活性剂溶液中表面活性剂的质量分数为0.3-2.5%;表面活性剂溶液的溶剂选自水和/或液体石蜡。以上几种表面活性剂适合于本发明实施例提供的反应体系进行微球成形,制备得到尺寸均匀的微球材料。
优选地,每毫升蛋白修饰聚合物溶液对应蛋白结合溶质的质量为2-50mg;在蛋白修饰聚合物溶液中,蛋白修饰聚合物的浓度为0.05-0.5g/mL,蛋白修饰聚合物溶液所用有机溶剂选自三氯甲烷、二氯甲烷、乙酸乙酯和四氢呋喃中的任意一种。发明人通过控制蛋白修饰聚合物和蛋白结合溶质的用量比,以进一步提升微球材料的缓释性能,若其中蛋白结合溶质的用量过大则会导致突释效应增加。
具体地,与表面活性剂溶液混合过程中是在20-50℃、200-1000r/min的条件下搅拌4-10h。发明人通过进一步优化混合条件,使制备得到的微球材料尺寸更加均匀一致。
在一些实施例中,将成球混合液与表面活性剂溶液混合之前,先将成球混合液与致孔剂的水溶液混合乳化;优选地,致孔剂为碳酸氢铵。利用致孔剂形成多孔结构,有利于增加溶质的容纳量,提高药物的负载量,可进一步地调控溶质的释放行为。
S3、后处理
在成球混合液与表面活性剂溶液混合后分离出微球沉淀,并对微球沉淀进行清洗、干燥。优选地,清洗过程是采用水和/或有机溶剂清洗;干燥是采用室温风干干燥、热干燥和冷冻干燥中的任意一种,干燥时间为24-48h。通过清洗去除材料表面未反应的原料,提升微球材料的纯度,得到干燥的成品。
本发明实施例还提供了一种蛋白修饰的聚合物微球复合材料,包括蛋白结合溶质和包覆于蛋白结合溶质上的蛋白修饰聚合物,其中,蛋白修饰聚合物是由蛋白和聚合物反应而得;优选地,聚合物为含有羧基的可降解聚合物,蛋白中含有胺基。利用蛋白和聚合物反应对聚合物进行修饰,然后再利用聚合物制备微球时可以使蛋白和蛋白结合溶质作用,提升材料在应用时的缓释性能。制备得到的微球材料具备很好的缓释性能,基本避免了突释现象,可以作为优良的缓释材料得到应用。
优选地,聚合物微球复合材料的粒径为20nm-5mm。聚合物微球复合材料中蛋白结合溶质每天的释放速度0.5-30%(质量分数)。
优选地,蛋白结合溶质、蛋白修饰聚合物的质量比为1:1-20;更优选为1:5-15。发明人通过控制材料中蛋白结合溶质和蛋白修饰聚合物质量比,进一步提升制备得到微球材料的缓释性能。在产品中,蛋白结合溶质、蛋白修饰聚合物的质量比控制在上述范围内为宜,超出此范围会导致突释效应增加的问题。
以下结合实施例对本发明的特征和性能作进一步的详细描述。
实施例1
本实施例提供一种蛋白修饰的聚合物微球复合材料的制备方法,其包括以下步骤:
将1.0g聚乳酸(分子量约为5万道尔顿)溶于10mL二氯甲烷,得到PLGA溶液;将该溶液倒入20mL含5.0%的1799型聚乙烯醇的水溶液进行乳化(3000rpm,3min);随后,将该乳液倒入含0.5%的1799型聚乙烯醇的水溶液中,300rpm持续搅拌10h后;对该产物进行水洗并离心三次(20000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到聚乳酸粉末。将0.6g该聚乳酸粉末浸泡于100mL含150mg1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐及120mgN-羟基琥珀酰亚胺的水溶液5h,随后收集产物进行水洗并离心三次(20000rpm,30min,10℃),得到羧基活化的聚乳酸粉末。随后,取等同摩尔浓度的羧基活化的聚乳酸粉末与鸡血清白蛋白,分别分散和溶解于100mL的磷酸盐缓冲液(pH=7.4)中,300rpm持续搅拌6h后,对该产物进行水洗并离心三次(15000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到鸡血清白蛋白修饰的聚乳酸粉末。以此方法制得足够量的鸡血清白蛋白修饰的聚乳酸。
将250mg乙酰水杨酸溶解于10mL含1.5g鸡血清白蛋白修饰的聚乳酸的四氢呋喃溶液中,超声分散30min;该混合液与1.5mL含30mg碳酸氢铵的水溶液混合并进行超声乳化5min;将上述混合液加入到500mL含6g1799型聚乙烯醇的水溶液中,在35℃下以700rpm持续搅拌5h;使用去离子水清洗并离心3次(1500rpm,10min)、室温下风干干燥36h后得到用于乙酰水杨酸释放的鸡血清白蛋白修饰的聚乳酸微球。
实施例2
本实施例提供一种蛋白修饰的聚合物微球复合材料的制备方法,其包括以下步骤:
将1.0g聚3-羟基丁酸酯-co-3-羟基戊酸酯(分子量约为10万道尔顿)溶于10mL二氯甲烷,得到聚3-羟基丁酸酯-co-3-羟基戊酸酯溶液;将该溶液倒入20mL含5.0%的1799型聚乙烯醇的水溶液进行乳化(3000rpm,3min);随后,将该乳液倒入含0.5%的1799型聚乙烯醇的水溶液中,300rpm持续搅拌10h后;对该产物进行水洗并离心三次(20000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到聚3-羟基丁酸酯-co-3-羟基戊酸酯粉末。将0.6g该聚3-羟基丁酸酯-co-3-羟基戊酸酯粉末浸泡于100mL含150mg1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐及120mgN-羟基琥珀酰亚胺的水溶液5h,随后收集产物进行水洗并离心三次(20000rpm,30min,10℃),得到羧基活化的聚3-羟基丁酸酯-co-3-羟基戊酸酯粉末。随后,取等同摩尔浓度的羧基活化的聚3-羟基丁酸酯-co-3-羟基戊酸酯粉末与牛血清白蛋白,分别分散和溶解于100mL的磷酸盐缓冲液(pH=7.4)中,300rpm持续搅拌6h后,对该产物进行水洗并离心三次(15000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到牛血清白蛋白修饰的聚3-羟基丁酸酯-co-3-羟基戊酸酯粉末。以此方法制得足够量的牛血清白蛋白修饰的聚3-羟基丁酸酯-co-3-羟基戊酸酯。
将80mg华法林钠溶解于10mL含1.0g牛血清白蛋白修饰的聚3-羟基丁酸酯-co-3-羟基戊酸酯的三氯甲烷溶液中,机械搅拌3000rpm分散5min;将上述混合液加入到500mL含10g1788型聚乙烯醇的水溶液中,在50℃下以500rpm持续搅拌4h;使用去离子水清洗并离心3次(1500rpm,10min)、冷冻干燥36h后得到用于华法林钠释放的牛血清白蛋白修饰的聚3-羟基丁酸酯-co-3-羟基戊酸酯微球。
实施例3
本实施例提供一种蛋白修饰的聚合物微球复合材料的制备方法,其包括以下步骤:
将1.0g聚(3-羟基丁酸酯)(分子量约为10万道尔顿)溶于10mL二氯甲烷,得到聚(3-羟基丁酸酯)溶液;将该溶液倒入20mL含5.0%的1799型聚乙烯醇的水溶液进行乳化(3000rpm,3min);随后,将该乳液倒入含0.5%的1799型聚乙烯醇的水溶液中,300rpm持续搅拌10h后;对该产物进行水洗并离心三次(20000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到聚(3-羟基丁酸酯)粉末。将0.6g该聚(3-羟基丁酸酯)浸泡于100mL含150mg1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐及120mgN-羟基琥珀酰亚胺的水溶液5h,随后收集产物进行水洗并离心三次(20000rpm,30min,10℃),得到羧基活化的聚(3-羟基丁酸酯)粉末。随后,取等同摩尔浓度的羧基活化的聚(3-羟基丁酸酯)粉末与鸡血清白蛋白,分别分散和溶解于100mL的磷酸盐缓冲液(pH=7.4)中,300rpm持续搅拌6h后,对该产物进行水洗并离心三次(15000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到鸡血清白蛋白修饰的聚(3-羟基丁酸酯)粉末。以此方法制得足够量的鸡血清白蛋白修饰的聚(3-羟基丁酸酯)。
将20mg乙酰胺基酚溶解于10mL含0.5g鸡血清白蛋白修饰的聚(3-羟基丁酸酯)的二氯甲烷溶液中,涡旋震荡2min;该混合液与3.0mL含15mg碳酸氢铵的水溶液混合并进行超声乳化5min;将上述混合液加入到500mL含12.5g甲基纤维素的水溶液中,在40℃下以400rpm持续搅拌12h;使用去离子水清洗并离心3次(1500rpm,10min)、40℃干燥15h后得到用于乙酰氨基酚释放的鸡血清白蛋白修饰的聚(3-羟基丁酸酯)微球。
实施例4
本实施例提供一种蛋白修饰的聚合物微球复合材料的制备方法,其包括以下步骤:
将1.0g聚乳酸-羟基乙酸共聚物(分子量约为3.0万道尔顿)溶于10mL二氯甲烷,得到聚乳酸-羟基乙酸共聚物溶液;将该溶液倒入20mL含5.0%的1799型聚乙烯醇的水溶液进行乳化(3000rpm,3min);随后,将该乳液倒入含0.5%的1799型聚乙烯醇的水溶液中,300rpm持续搅拌10h后;对该产物进行水洗并离心三次(20000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到聚乳酸-羟基乙酸共聚物粉末。将0.6g该聚乳酸-羟基乙酸共聚物浸泡于100mL含150mg1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐及120mgN-羟基琥珀酰亚胺的水溶液5h,随后收集产物进行水洗并离心三次(20000rpm,30min,10℃),得到羧基活化的聚乳酸-羟基乙酸共聚物粉末。随后,取等同摩尔浓度的羧基活化的聚乳酸-羟基乙酸共聚物粉末与人血清白蛋白,分别分散和溶解于100mL的磷酸盐缓冲液(pH=7.4)中,300rpm持续搅拌6h后,对该产物进行水洗并离心三次(15000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到人血清白蛋白修饰的聚乳酸-羟基乙酸共聚物粉末。以此方法制得足够量的人血清白蛋白修饰的聚乳酸-羟基乙酸共聚物。
将100mg硫酸吲哚酚溶解于10mL含1.0g人血清白蛋白修饰的聚乳酸-羟基乙酸共聚物的二氯甲烷溶液中,机械搅拌3000rpm分散3min;将上述混合液加入到500mL含5g1799型聚乙烯醇的水溶液中,在30℃下以300rpm持续搅拌11h;使用去离子水清洗并离心3次(1500rpm,10min)、冷冻干燥48h后得到用于硫酸吲哚酚释放的人血清白蛋白修饰的聚乳酸-羟基乙酸共聚物微球。
实施例5
本实施例提供一种蛋白修饰的聚合物微球复合材料的制备方法,其包括以下步骤:
将1.0g聚乙醇酸(分子量约为8.0万道尔顿)溶于10mL二氯甲烷,得到聚乙醇酸溶液;将该溶液倒入20mL含5.0%的1799型聚乙烯醇的水溶液进行乳化(3000rpm,3min);随后,将该乳液倒入含0.5%的1799型聚乙烯醇的水溶液中,300rpm持续搅拌10h后;对该产物进行水洗并离心三次(20000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到聚乙醇酸粉末。将0.6g该聚乙醇酸浸泡于100mL含150mg1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐及120mgN-羟基琥珀酰亚胺的水溶液5h,随后收集产物进行水洗并离心三次(20000rpm,30min,10℃),得到羧基活化的聚乙醇酸粉末。随后,取等同摩尔浓度的羧基活化的聚乙醇酸粉末与机阴离子转运蛋白,分别分散和溶解于100mL的磷酸盐缓冲液(pH=7.4)中,300rpm持续搅拌6h后,对该产物进行水洗并离心三次(15000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到机阴离子转运蛋白修饰的聚乙醇酸粉末。以此方法制得足够量的机阴离子转运蛋白修饰的聚乙醇酸。
将500mg硫酸对甲酚溶解于10mL含5.0g有机阴离子转运蛋白修饰的聚乙醇酸的乙酸乙酯溶液中,机械搅拌3000rpm分散2min;将上述混合液加入到500mL含7.5g明胶的水溶液中,在30℃下以1000rpm持续搅拌7h;使用去离子水清洗并离心3次(1500rpm,10min)、45℃干燥12h后得到用于硫酸对甲酚释放的有机阴离子转运蛋白修饰的聚乙醇酸微球。
实施例6
本实施例提供一种蛋白修饰的聚合物微球复合材料的制备方法,其包括以下步骤:
将1.0g聚3-羟基烷酸酯(分子量约为9.0万道尔顿)溶于10mL二氯甲烷,得到聚3-羟基烷酸酯溶液;将该溶液倒入20mL含5.0%的1799型聚乙烯醇的水溶液进行乳化(3000rpm,3min);随后,将该乳液倒入含0.5%的1799型聚乙烯醇的水溶液中,300rpm持续搅拌10h后;对该产物进行水洗并离心三次(20000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到聚3-羟基烷酸酯粉末。将0.6g该聚3-羟基烷酸酯浸泡于100mL含150mg1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐及120mgN-羟基琥珀酰亚胺的水溶液5h,随后收集产物进行水洗并离心三次(20000rpm,30min,10℃),得到羧基活化的聚3-羟基烷酸酯粉末。随后,取等同摩尔浓度的羧基活化的聚3-羟基烷酸酯粉末与人血清白蛋白,分别分散和溶解于100mL的磷酸盐缓冲液(pH=7.4)中,300rpm持续搅拌6h后,对该产物进行水洗并离心三次(15000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到人血清白蛋白修饰的聚3-羟基烷酸酯粉末。以此方法制得足够量的人血清白蛋白修饰的聚3-羟基烷酸酯。
将150mg马尿酸溶解于10mL含1.0g人血清白蛋白修饰的聚3-羟基烷酸酯的四氢呋喃溶液中,超声分散3min;该混合液与0.5mL含1mg碳酸氢铵的水溶液混合并进行超声乳化5min;将上述混合液加入到500mL含1.5g明胶的水溶液中,在25℃下以200rpm持续搅拌8h;使用去离子水清洗并离心3次(1500rpm,10min)、冷冻干燥24h后得到用于马尿酸释放的人血清白蛋白修饰的聚3-羟基烷酸酯微球。
实施例7
本实施例提供一种蛋白修饰的聚合物微球复合材料的制备方法,其包括以下步骤:
将1.0g聚丁二酸丁二酯(分子量约为6.0万道尔顿)溶于10mL二氯甲烷,得到聚丁二酸丁二酯溶液;将该溶液倒入20mL含5.0%的1799型聚乙烯醇的水溶液进行乳化(3000rpm,3min);随后,将该乳液倒入含0.5%的1799型聚乙烯醇的水溶液中,300rpm持续搅拌10h后;对该产物进行水洗并离心三次(20000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到聚丁二酸丁二酯粉末。将0.6g该聚丁二酸丁二酯浸泡于100mL含150mg1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐及120mgN-羟基琥珀酰亚胺的水溶液5h,随后收集产物进行水洗并离心三次(20000rpm,30min,10℃),得到羧基活化的聚丁二酸丁二酯粉末。随后,取等同摩尔浓度的羧基活化的聚丁二酸丁二酯粉末与牛血清白蛋白,分别分散和溶解于100mL的磷酸盐缓冲液(pH=7.4)中,300rpm持续搅拌6h后,对该产物进行水洗并离心三次(15000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到牛血清白蛋白修饰的聚丁二酸丁二酯粉末。以此方法制得足够量的牛血清白蛋白修饰的聚丁二酸丁二酯。
将50mg苏丹红溶解于10mL含2.5g牛血清白蛋白修饰的聚丁二酸丁二酯的三氯甲烷溶液中,涡旋震荡分散2min;将上述混合液加入到500mL含1.5g124型聚乙烯醇的水溶液中,在45℃下以600rpm持续搅拌8h;使用去离子水清洗并离心3次(1500rpm,10min)、室温下风干干燥24h后得到用于马尿酸释放的牛血清白蛋白修饰的聚丁二酸丁二酯微球。
实施例8
本实施例提供一种蛋白修饰的聚合物微球复合材料的制备方法,其包括以下步骤:
将1.0g聚乳酸-羟基乙酸共聚物(分子量约为5.0万道尔顿)溶于10mL二氯甲烷,得到聚乳酸-羟基乙酸共聚物溶液;将该溶液倒入20mL含5.0%的1799型聚乙烯醇的水溶液进行乳化(3000rpm,3min);随后,将该乳液倒入含0.5%的1799型聚乙烯醇的水溶液中,300rpm持续搅拌10h后;对该产物进行水洗并离心三次(20000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到聚乳酸-羟基乙酸共聚物粉末。将0.6g该聚乳酸-羟基乙酸共聚物浸泡于100mL含150mg1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐及120mgN-羟基琥珀酰亚胺的水溶液5h,随后收集产物进行水洗并离心三次(20000rpm,30min,10℃),得到羧基活化的聚乳酸-羟基乙酸共聚物粉末。随后,取等同摩尔浓度的羧基活化的聚乳酸-羟基乙酸共聚物粉末与低密度脂蛋白,分别分散和溶解于100mL的磷酸盐缓冲液(pH=7.4)中,300rpm持续搅拌6h后,对该产物进行水洗并离心三次(15000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到低密度脂蛋白修饰的聚乳酸-羟基乙酸共聚物粉末。以此方法制得足够量的低密度脂蛋白修饰的聚乳酸-羟基乙酸共聚物。
将300mg胆固醇溶解于10mL含2.0g低密度脂蛋白修饰的聚乳酸-羟基乙酸共聚物的二氯甲烷溶液中,超声分散2min;该混合液与2.0mL含20mg碳酸氢铵的水溶液混合并进行超声乳化5min;将上述混合液加入到500mL含6g司盘80的液体石蜡溶液中,在20℃下以800rpm持续搅拌7h;使用去离子水清洗并离心3次(1500rpm,10min)、35℃干燥12h后得到用于胆固醇释放的低密度脂蛋白修饰的聚乳酸-羟基乙酸共聚物微球。
实施例9
本实施例提供一种蛋白修饰的聚合物微球复合材料的制备方法,其包括以下步骤:
将1.0g聚己内酯(分子量约为9.0万道尔顿)溶于10mL二氯甲烷,得到聚己内酯溶液;将该溶液倒入20mL含5.0%的1799型聚乙烯醇的水溶液进行乳化(3000rpm,3min);随后,将该乳液倒入含0.5%的1799型聚乙烯醇的水溶液中,300rpm持续搅拌10h后;对该产物进行水洗并离心三次(20000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到聚己内酯粉末。将0.6g该聚己内酯浸泡于100mL含150mg1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐及120mgN-羟基琥珀酰亚胺的水溶液5h,随后收集产物进行水洗并离心三次(20000rpm,30min,10℃),得到羧基活化的聚己内酯粉末。随后,取等同摩尔浓度的羧基活化的聚己内酯粉末与低密度脂蛋白,分别分散和溶解于100mL的磷酸盐缓冲液(pH=7.4)中,300rpm持续搅拌6h后,对该产物进行水洗并离心三次(15000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到低密度脂蛋白修饰的聚己内酯粉末。以此方法制得足够量的低密度脂蛋白修饰的聚己内酯。
将400mg甘油三酯溶解于10mL含1.5g低密度脂蛋白修饰的聚己内酯的四氢呋喃溶液中,机械搅拌3000rpm分散2min;将上述混合液加入到500mL含2.5g吐温80的液体石蜡溶液中,在25℃下以900rpm持续搅拌7h;使用去离子水清洗并离心3次(1500rpm,10min)、室温下风干干燥48h后得到用于甘油三酯释放的低密度脂蛋白修饰的聚己内酯微球。
实施例10
本实施例提供一种蛋白修饰的聚合物微球复合材料的制备方法,其包括以下步骤:
将1.0g聚乳酸(分子量约为10.0万道尔顿)溶于10mL二氯甲烷,得到聚乳酸溶液;将该溶液倒入20mL含4.0%的1799型聚乙烯醇的水溶液进行乳化(2000rpm,2min);随后,将该乳液倒入含0.2%的1799型聚乙烯醇的水溶液中,300rpm持续搅拌8h后;对该产物进行水洗并离心三次(20000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到聚乳酸粉末。将0.6g该聚乳酸粉末浸泡于100mL含100mg1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐及100mgN-羟基琥珀酰亚胺的水溶液4h,随后收集产物进行水洗并离心三次(20000rpm,30min,10℃),得到羧基活化的聚乳酸粉末。随后,取等同摩尔浓度的羧基活化的聚乳酸粉末与鸡血清白蛋白,分别分散和溶解于100mL的磷酸盐缓冲液(pH=7.4)中,300rpm持续搅拌4h后,对该产物进行水洗并离心三次(15000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到鸡血清白蛋白修饰的聚乳酸粉末。以此方法制得足够量的鸡血清白蛋白修饰的聚乳酸。
将250mg复方甲硝唑溶解于10mL含1.5g鸡血清白蛋白修饰的聚乳酸的四氢呋喃溶液中,超声分散30min;该混合液与1.5mL含30mg碳酸氢铵的水溶液混合并进行超声乳化5min;将上述混合液加入到500mL含6g1799型聚乙烯醇的水溶液中,在35℃下以700rpm持续搅拌5h;使用去离子水清洗并离心3次(1500rpm,10min)、室温下风干干燥36h后得到用于乙酰水杨酸释放的鸡血清白蛋白修饰的聚乳酸微球。
实施例11
本实施例提供一种蛋白修饰的聚合物微球复合材料的制备方法,其包括以下步骤:
将1.0g聚3-羟基丁酸酯-co-3-羟基戊酸酯(分子量约为8.0万道尔顿)溶于10mL二氯甲烷,得到聚3-羟基丁酸酯-co-3-羟基戊酸酯溶液;将该溶液倒入20mL含6.0%的1799型聚乙烯醇的水溶液进行乳化(4000rpm,5min);随后,将该乳液倒入含1.0%的1799型聚乙烯醇的水溶液中,300rpm持续搅拌12h后;对该产物进行水洗并离心三次(20000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到聚3-羟基丁酸酯-co-3-羟基戊酸酯粉末。将0.6g该聚3-羟基丁酸酯-co-3-羟基戊酸酯粉末浸泡于100mL含300mg1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐及250mgN-羟基琥珀酰亚胺的水溶液6h,随后收集产物进行水洗并离心三次(20000rpm,30min,10℃),得到羧基活化的聚3-羟基丁酸酯-co-3-羟基戊酸酯粉末。随后,取等同摩尔浓度的羧基活化的聚3-羟基丁酸酯-co-3-羟基戊酸酯粉末与牛血清白蛋白,分别分散和溶解于100mL的磷酸盐缓冲液(pH=7.4)中,300rpm持续搅拌8h后,对该产物进行水洗并离心三次(15000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到牛血清白蛋白修饰的聚3-羟基丁酸酯-co-3-羟基戊酸酯粉末。以此方法制得足够量的牛血清白蛋白修饰的聚3-羟基丁酸酯-co-3-羟基戊酸酯。
将80mg红霉素溶解于10mL含1.0g牛血清白蛋白修饰的聚3-羟基丁酸酯-co-3-羟基戊酸酯的三氯甲烷溶液中,机械搅拌3000rpm分散5min;将上述混合液加入到500mL含10g1788型聚乙烯醇的水溶液中,在50℃下以500rpm持续搅拌4h;使用去离子水清洗并离心3次(1500rpm,10min)、冷冻干燥36h后得到用于华法林钠释放的牛血清白蛋白修饰的聚3-羟基丁酸酯-co-3-羟基戊酸酯微球。
对比例1
本对比例提供一种蛋白修饰的聚合物微球复合材料的制备方法,与实施例4大致相同,不同之处在于:不采用人血清白蛋白对聚合物进行修饰,其包括以下步骤:
将100mg硫酸吲哚酚溶解于10mL含1.0g聚乳酸-羟基乙酸共聚物的二氯甲烷溶液中,机械搅拌3000rpm分散3min;将上述混合液加入到500mL含5g1799型聚乙烯醇的水溶液中,在30℃下以300rpm持续搅拌11h;使用去离子水清洗并离心3次(1500rpm,10min)、冷冻干燥48h后得到用于硫酸吲哚酚释放的聚乳酸-羟基乙酸共聚物微球。
对比例2
本对比例提供一种蛋白修饰的聚合物微球复合材料的制备方法,与实施例4大致相同,不同之处在于:增加碳酸氢铵进行乳化,其包括以下步骤:
将1.0g聚乳酸-羟基乙酸共聚物溶于10mL二氯甲烷,得到聚乳酸-羟基乙酸共聚物溶液;将该溶液倒入20mL含5.0%的1799型聚乙烯醇的水溶液进行乳化(3000rpm,3min);随后,将该乳液倒入含0.5%的1799型聚乙烯醇的水溶液中,300rpm持续搅拌10h后;对该产物进行水洗并离心三次(20000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到聚乳酸-羟基乙酸共聚物粉末。将0.6g该聚乳酸-羟基乙酸共聚物浸泡于100mL含150mg1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐及120mgN-羟基琥珀酰亚胺的水溶液5h,随后收集产物进行水洗并离心三次(20000rpm,30min,10℃),得到羧基活化的聚乳酸-羟基乙酸共聚物粉末。随后,取等同摩尔浓度的羧基活化的聚乳酸-羟基乙酸共聚物粉末与人血清白蛋白,分别分散和溶解于100mL的磷酸盐缓冲液(pH=7.4)中,300rpm持续搅拌6h后,对该产物进行水洗并离心三次(15000rpm,30min,10℃),收集沉淀产物、冷冻干燥48h得到人血清白蛋白修饰的聚乳酸-羟基乙酸共聚物粉末。以此方法制得足够量的人血清白蛋白修饰的聚乳酸-羟基乙酸共聚物。
将100mg硫酸吲哚酚溶解于10mL含1.0g人血清白蛋白修饰的聚乳酸-羟基乙酸共聚物的二氯甲烷溶液中,机械搅拌3000rpm分散3min;该混合液与0.5mL含5mg碳酸氢铵的水溶液混合并进行超声乳化5min;将上述混合液加入到500mL含5g1799型聚乙烯醇的水溶液中,在30℃下以300rpm持续搅拌11h;使用去离子水清洗并离心3次(1500rpm,10min)、冷冻干燥48h后得到用于硫酸吲哚酚释放的人血清白蛋白修饰的聚乳酸-羟基乙酸共聚物微球。
试验例1
将实施例1-11和对比例1-2中制备得到的微球材料进行体外溶质释放评价,结果见图1-2。评价方法:体外溶质释放实验是在37℃,60rpm条件下,在恒温摇床中进行的。将50mg的微球浸渍在20mLPBS(pH=7.4)中,定期收集测试液,并补充等量的PBS,将收集的测试液用高效液相色谱法(HPLC)测定溶质含量。将某时间点溶质的吸光度代入到其标准曲线中,得到这一时间点溶质释放的实际量。将实际量除以材料中负载溶质的总量即得到这一时间点溶质的累积释放量。
图1-2可知,实施例1-11均无明显突释行为,与对比例1-2相比,实施例4的突释效应更小,提示本发明方法制得的经蛋白修饰的微球(这里仅提供PLGA微球)对溶质的缓释作用有明显的调控作用。与实施例4相比,对比例1不采用人血清白蛋白对聚合物进行修饰,缺少实施例4中蛋白-蛋白结合溶质的亲和结合力,使其前期溶质释放速率加快,出现突释现象;与实施例4相比,对比例2增加碳酸氢铵进行乳化而得到多孔微球,大幅度增大微球的比表面积,使嵌入于微球表面的蛋白结合溶质的数量大幅增大,从而突释现象更为明显。
综上所述,本发明提供的一种蛋白修饰的聚合物微球复合材料,其通过蛋白对聚合物进行化学修饰形成蛋白修饰聚合物,利用该蛋白修饰聚合物对蛋白结合溶质进行包覆形成微球材料,应用时能达到长久缓释的效果,有效降低了突释效应。
本发明提供的一种蛋白修饰的聚合物微球复合材料的制备方法,其通过采用蛋白修饰聚合物对蛋白结合溶质进行包覆以形成聚合物微球,制备得到的微球材料缓释性能好,突释效应很低,可以作为优良的缓释材料得到应用。
以上所描述的实施例是本发明一部分实施例,而不是全部的实施例。本发明的实施例的详细描述并非旨在限制要求保护的本发明的范围,而是仅仅表示本发明的选定实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
- 还没有人留言评论。精彩留言会获得点赞!