一种高效吸附低浓度氨气的多级孔聚合物固体酸的制备方法与流程
本发明属于有机材料制备及应用领域,具体涉及到一种高效吸附低浓度氨气的多级孔聚合物固体酸的制备方法。
背景技术:
随着全球经济的高速发展,化石燃料的过度开发和使用带来的一系列问题促使人们不得不处理环境污染问题并寻求新的可替代清洁能源。尤其是大气污染,其中36%的肺癌死亡是由空气污染造成的。而且,空气污染还增加了患急性呼吸道感染的风险。在大气污染中,nh3作为一种污染物广泛存在于工业生产和畜牧业生产中。且nh3对环境的危害已经引起各国的关注,各个国家都在通过各种途径减少nh3的排放量,并据此设置了相关的排放标准。此外,在众多新能源中,氢被认为是有史以来最为高效的清洁能源,具有安全、热值高、零污染等诸多优点。迄今为止,虽然人们在氢能的开发和利用方面取得了一系列重要进展,但在氢燃料电池的应用方面还面临许多难题。其中,如何为氢燃料电池提供高质量且廉价的氢气是当前面临的主要难题之一。以纯氢为燃料直接用于燃料电池无论在运输还是储存方面都存在诸多问题,而氨分解在线制氢技术可以有效的解决上述两大难题。氨气是一种富氢化合物,能量密度远远高于甲醇、汽油等燃料,常温下容易以液体形式进行存储,且制备技术完善,成本低廉。此外,由于氨气中不含碳元素,因此可从源头上杜绝cox等有毒气体的生成。将氨分解反应用于在线制氢领域是目前解决燃料电池氢能来源的有效途径。受制于热力学限制,氨分解过程并不能达到百分之百转化,而nh3作为一种典型的污染性和强腐蚀性的碱性气体,对人体和环境都有极大危害。直接排放或燃烧等不仅会产生二次污染,还会造成nh3资源严重浪费。从环境保护和资源节约的角度,nh3的净化分离与回收具有重要意义。
目前nh3回收工艺主要包括溶剂吸收法、催化转化法和吸附法。溶剂吸收法又分为化学吸收法和物理吸收法。化学吸收法主要是利用nh3的碱性与酸性物质发生化学反应生成氮肥,具有吸收快、净化度高及操作方便等优点,但存在腐蚀性强和难再生等缺点,正逐渐被淘汰。物理吸收法主要是指水洗法,即先用软水吸收nh3,再通过蒸馏得到浓氨水,进而得到nh3,最后加压冷凝制成液氨再加以利用。物理吸收法是目前脱除nh3最普遍的方法,技术较成熟,但也存在耗水量大、能耗高、回收率低等缺点,限制了工业应用的进一步发展。催化分解法是将nh3催化分解为n2和h2,但催化能耗高、不易回收及运行成本高等缺点在一定程度上制约了该技术的商业化应用。吸附法将nh3组分积聚或浓集在多孔固体吸附剂表面,达到分离nh3的目的。根据作用力不同,吸附类型主要有化学吸附和物理吸附两种,其中依靠分子间范德华力发生的吸附为物理吸附,由物质表面化学键引起的吸附为化学吸附。工业吸附剂一般具有如下优势:(1)吸附能力较大;(2)选择性高;(3)能再生和重复使用;(4)机械强度足够高;(5)化学性质稳定;(6)供应量大、价格低。吸附法可有效去除低浓度nh3,设备简单,去除效率高且可回收有用组分。随着环境保护和绿色可持续发展及对吸附材料研究的深入,多孔吸附材料在气体分离领域展现出越来越重要的应用前景,开发新型nh3吸附分离技术成为该领域的重要发展方向,尤其针对氨分解制氢过程中残留的微量hn3导致氢燃料电池效率低的问题。吸附法主要基于吸附剂的孔道与nh3相互作用,选择高性能的吸附剂是开发吸附新工艺的关键。
有机多孔聚合物具有较大的比表面积、孔径可控、骨架密度低、良好的化学性、可修饰性以及制备方法多样性等特点在气体吸附方面取得了很大的进展。孔结构包括孔径、孔径分布、孔容和微孔孔容等直接影响着气体的吸附性能。固体酸在工业上可替代矿物液体酸而备受关注,其优点是容易从反应介质中分离出催化剂,还原腐蚀,良好的可回收性,绿色化学过程以及增强的产品选择性。基于上述情况,我们报道了强酸性多级孔聚合物固体酸的制备,通过二乙烯基苯在对苯乙烯磺酸钠的官能单体存在情况下进行溶剂热共聚合,然后与酸性溶液进行离子交换,合成的多级孔聚合物固体酸具有较大的bet表面积,分层纳米孔和强酸度。上述特点使得该固体酸具有优良的nh3的吸附性能,并且在混合气体(nh3,n2和h2)吸附中表现出高吸附量与选择性。
技术实现要素:
本发明克服以上不足之处,提供了高效吸附低浓度氨气的多级孔聚合物固体酸的制备方法,以有机溶剂和去离子水为溶剂,二乙烯苯和苯乙烯磺酸钠为单体,偶氮二异丁腈为引发剂进行溶剂热共聚合反应,溶剂蒸发得到具有整体形貌的中间产物,之后再通过与酸性溶液进行离子交换,最后进行干燥处理得到多级孔聚合物固体酸。
为实现上述目的,本发明的技术方案为:
一种高效吸附低浓度氨气的多级孔聚合物固体酸的制备方法,包括以下步骤:
a,二乙烯苯、苯乙烯磺酸钠,偶氮二异丁腈、有机溶剂按照一定摩尔比进行混合,滴加微量的去离子水,在聚四氟乙烯内衬反应釜搅拌均匀;
b,将盛有上述混合物的内衬放入反应釜并转移至烘箱进行溶剂热共聚合反应;
c,待反应结束后将得到的产物在室温下蒸发溶剂后,得到具有整体形貌的固体样品。固体样品放入酸溶液处理后,用大量去离子水洗涤。
d,将上述产物干燥后得到用于氨气选择性吸附的多级孔聚合物固体酸。
进一步地,所述步骤a中二乙烯苯、苯乙烯磺酸钠,偶氮二异丁腈、有机溶剂和水的摩尔比为1:x:0.02:16.1:7.23(x=0.3~1.5),搅拌时间为2-12h。
所述步骤b,优选溶剂热反应温度为60-180℃,时间为12-48h。
所述步骤c,优选酸性溶液为三氟甲磺酸或硫酸,其浓度为0.5-2m,添加量为20-100ml。
所述步骤d,优选干燥温度为60-120℃,干燥时间为12-48h。
上述用于碱性气体吸附的多级孔聚合物固体酸在氨气吸附的应用,具体为:所述nh3吸附分为静态和动态吸附。静态吸附条件为室温,吸附压力为0~1bar。动态穿透吸附温度为30-70℃,原料气体流速为20ml/min,原料气组成:0.1%nh3/24.9%n2/75%h2。
本发明的优点在于:(1)本发明制备多级孔聚合物固体酸,具有较高的bet表面积,分层纳米孔和酸度,以及良好的热稳定性。(2)本发明操作简单,且结构可控,可大规模生产,具有广阔的应用前景。
附图说明
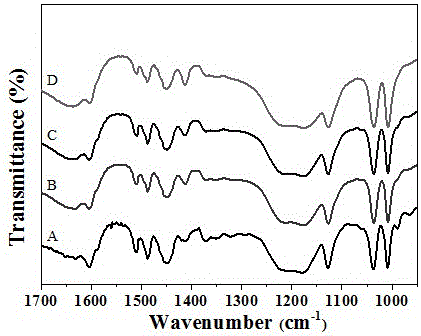
图1为实施例1-4制备的多级孔聚合物固体酸的ftir谱图;
图2为实施例1-4制备的多级孔聚合物固体酸的n2吸附-脱附等温线和孔径分布;
图3为实施例1-4制备的多级孔聚合物固体酸的sem图;
图4为吸附剂d室温下的nh3、n2和h2吸附曲线;
图5为吸附剂d室温下的nh3穿透实验测试。
具体实施方法
以下对本发明的具体实施方法进行详细说明。此处所描述的具体实施方法仅用于说明和解释本发明,并不用于限制本发明。
实施例1:称取2.0g二乙烯苯(dvb)加入到含有0.06g偶氮二异丁腈(aibn)和24ml四氢呋喃的溶液中,然后加入2ml去离子水,最后引入0.3g对苯乙烯磺酸钠。在室温下搅拌2h,将混合物在60℃下溶剂热处理12h。然后在室温下蒸发溶剂后,获得具有整体形貌的样品h-pdvb-0.3-so3na;(h-pdvb-x-so3na代表二乙烯苯(dvb)和对苯乙烯磺酸钠聚合之后的产物,x代表所使用的对苯乙烯磺酸钠的质量)
将0.5g的h-pdvb-0.3-so3na分散在20ml硫酸溶液(0.5m)中,在室温下搅拌12h后,将样品用大量水洗涤直至滤液为中性。最后在烘箱中于60℃干燥12h,待自然冷却后得到多级孔聚合物固体酸h-pdvb-0.4-so3h,记为吸附剂a,其比表面积为569m2/g,平均孔径为6.17nm。
实施例2:将2.0g二乙烯苯(dvb)加入到含有0.065g偶氮二异丁腈(aibn)和25ml乙酸乙酯的溶液中,然后加入2.5ml去离子水,最后引入0.7g对苯乙烯磺酸钠。在室温下搅拌5h,将混合物在120℃下溶剂热处理24h。然后在室温下蒸发溶剂后,获得具有整体形貌的样品(h-pdvb-0.7-so3na)。(命名同上)
将0.6g的h-pdvb-0.7-so3na分散在60ml硫酸溶液(1.2m)中,在室温下搅拌16h后,将样品用大量水洗涤直至滤液为中性。最后在烘箱中于80℃℃干燥16h,待自然冷却后便得到用于有氨气选择性吸附的多级孔聚合物固体酸h-pdvb-0.7-so3h,记为吸附剂b,其比表面积为458m2/g,平均孔径为6.24nm。
实施例3:将2.0g二乙烯苯(dvb)加入到含有0.067g偶氮二异丁腈(aibn)和27ml四氢呋喃的溶液中,然后加入2.5ml去离子水,最后引入1.0g对苯乙烯磺酸钠。在室温下搅拌8h,将混合物在160℃下溶剂热处理36h。然后在室温下蒸发溶剂后,获得具有整体形貌的样品(h-pdvb-1.0-so3na)。
将0.5g的h-pdvb-1.0-so3na分散在65ml三氟甲磺酸溶液(1.5m)中,在室温下搅拌20h后,将样品用大量水洗涤直至滤液为中性。最后在烘箱中于100℃干燥24h,待自然冷却后便得到用于有氨气选择性吸附的多级孔聚合物固体酸h-pdvb-1.0-so3h,记为吸附剂c,其比表面积为398m2/g,平均孔径为6.52nm。
实施例4:将2.0g二乙烯苯(dvb)加入到含有0.075g偶氮二异丁腈(aibn)和28ml二氯甲烷的溶液中,然后加入3.0ml去离子水,最后引入1.5g对苯乙烯磺酸钠。在室温下搅拌12h,将混合物在180℃下溶剂热处理48h。然后在室温下蒸发溶剂后,获得具有整体形貌的样品(h-pdvb-1.5-so3na)。
将0.6g的h-pdvb-1.5-so3na分散在60ml硫酸溶液(2.0m)中,在室温下搅拌24h后,将样品用大量水洗涤直至滤液为中性。最后在烘箱中于120℃干燥48h,待自然冷却后便得到用于有氨气选择性吸附的多级孔聚合物固体酸h-pdvb-1.5so3h,记为吸附剂d,其比表面积为319m2/g,平均孔径为6.78nm。
对比例1:将4.0g的聚环氧乙烷-聚环氧丙烷-聚环氧乙烷三嵌段共聚物(p123)溶于125g的1.9mhcl中。加热至40℃后,将7.2ml的硅酸四乙酯(teos)加入上述溶液中,搅拌40min后,快速加入0.77ml的3-巯基丙基三甲氧基硅烷(3-mptms)和1.25g(30wt%)过氧化氢(h2o2)溶液,并将溶液在40℃搅拌20h。然后将混合物转移到高压釜中,并在100℃下热处理24h。通过提取乙醇和硫酸的混合物来进行p123模板的去除,然后用大量水洗涤并在60℃下干燥12h得到sba-15-so3h,记为吸附剂e。
对比例2:将0.75gpdvb在圆底烧瓶中于100℃脱气3h,然后取50ml含氯磺酸(10ml)的二氯甲烷于0℃加入烧瓶中,并将溶液于n2气氛下搅拌12h得到pdvb-so3h,记为吸附剂f。
对得到的多级孔聚合物固体酸进行物化性质表征和氨气选择性吸附测试:
表征相关信息:采用美国thermofisherscientific公司生产的型号为nicolet6700的傅里叶红外光谱仪对所制备的固体酸吸附剂进行官能团的表征。采用美国micrometric公司生产的型号为tristarⅱ物理吸附仪对所制备的固体酸吸附剂进行比表面积、孔结构以及孔径分布分析。采用日本hitachi公司生产的型号为s-4800场发射扫描电子显微镜对所制备的固体酸吸附剂的微观形貌特征进行观察。
吸附性能测试:采用由南通市飞宇石油科技开发有限公司生产的nh3吸收罐和缓冲罐,以及由南京天从电气有限公司生产的压力传感器对所制备的固体酸吸附剂进行nh3吸附性能评价。采用美国micrometric公司生产的型号为tristarⅱ物理吸附仪进行固体酸的n2和h2的吸附。
穿透试验:nh3穿透试验在美国micromeritics公司autochem2920型自动吸附仪上进行。称取50mg催化剂(40~60目),先用高纯氩气在150oc吹扫2h后降至一定温度,切换为nh3混合气(0.1%nh3/24.9%n2/75%h2)。首先混合气不经过样品管,并由质谱(hiden,hpr-20r&d)对管路中的气体进行跟踪记录。待信号稳定后切换气路经过样品,并继续对经过吸附剂的混合气体用质谱跟踪记录,等各组分气体恢复至原料气浓度后停止记录。
图1为不同固体酸吸附剂的ftir谱图,从图中可看出所有吸附剂均在1010、1035、1125和1174cm-1处出现红外谱峰。值得注意的是,在1035cm-1附近的谱带与苯环上存在c-s键相关,而在1010、1125和1174cm-1附近的谱带与非对称和对称拉伸信号相关。红外结果表明,磺酸基通过共聚途径成功引入多级孔聚合物网络中。
图2为不同固体酸吸附剂的n2吸脱附曲线和孔径分布图,所有样品均表现出典型的iv型等温线,n2吸附量在0.6<p/p0<0.9范围内急剧增加,表明存在中孔性。值得注意的是,随着对苯乙烯磺酸钠含量的增加,bet表面积和孔体积趋于减少。
图3为不同固体酸吸附剂的扫描电镜图,均表现出粗糙的丰富纳米孔的表面特性。
表1为本发明实施例1-4,对比例1和2的氨气穿透曲线结果统计表
实施例中,不同对苯乙烯磺酸钠用量制备的固体酸吸附剂,其中对于相同样品在不同温度下,其nh3穿透时间随温度的升高呈现出减少趋势;对于不同对苯乙烯磺酸钠用量在相同温度下,其nh3穿透时间随苯乙烯磺酸钠用量的增加呈现出递增趋势;表1我们可以看出实施例1-4所制备固体酸吸附剂穿透时间明显高于对比例1-2。同时对不同产物经过升温脱附后,在相同温度下(30℃)进行循环吸附测试实验,结果表明,我们所制备的固体酸吸附剂在重复循环3次之后仍然有很好的穿透性能,说明所制备的固体酸吸附剂重复利用性好。
图4为固体酸吸附剂d在室温下的nh3、n2和h2吸附曲线,该样品表现出很好的nh3选择性吸附。如在1bar时,nh3吸附量为9.29mmol/g,而n2和h2在相同条件下的吸附量仅有0.03mmol/g。
图5为固体酸吸附剂d在室温下的nh3穿透实验曲线,结果表明该吸附在在室温下的穿透效果可达2000min/g,且3000min/g之后才吸附饱和,该穿透结果表明所制备固体酸吸附剂在去除低浓度nh3方面的优异性能。
- 还没有人留言评论。精彩留言会获得点赞!