一种仿生纳米酶及其制备方法和应用
1.本发明涉及纳米酶的技术领域,具体涉及一种仿生纳米酶及其制备方法和应用。
背景技术:
2.漆酶是一类多铜基氧化还原酶类,以分子氧为电子受体催化底物发生单电子氧化,仅产生水作为副产物,被认为是一种绿色、高效及全能的生物催化剂,广泛应用于多种生物催化过程,尤其是环境污染物的生物降解。然而,天然漆酶存在易失活、难回首、稳定性差等缺点,导致其应用受限。
3.纳米酶是一类具有类似天然酶催化功能的纳米材料,能够结合化学催化剂和生物催化剂的优势。目前,具有漆酶活性的纳米酶(漆酶纳米酶)已吸引了广泛关注,然而,已有报道的漆酶纳米酶主要局限于铜基纳米材料,制备工艺多较为复杂,产物多以非晶态的形式存在,机械强度较差,催化活性有待提高,应用范围较为局限,而高性能非铜基漆酶纳米酶及其仿生化制备的策略尚不多见。
4.因此,亟需开发一种制备简单、结构有序、活性高、稳定性好、可循环再生和具有高应用价值的非铜基仿生漆酶纳米酶。
技术实现要素:
5.为了克服现有技术存在的问题,本发明的目的之一在于提供一种。
6.本发明的目的之二在于提供上述仿生纳米酶的制备方法。
7.本发明的目的之三在于提供上述仿生纳米酶的应用。
8.本发明的发明构思为:天然漆酶活性中心由铜原子(分为3类,t1-cu,t2-cu,t3a/b-cu)与不同氨基酸残基配位组合形成,其中,顺磁性t1-cu是底物氧化的活性位点,而t2-cu和t3a/b-cu结合形成三核铜簇,为分子氧提供电子并使其还原成水。在此催化循环过程中,一价和二价铜(cu
2+
/cu
1+
)之间的循环氧化还原在将电子从底物转移到氧气中起着关键作用。受天然漆酶cu
2+
/cu
1+
氧化还原模型启发,多价态铈(ce
4+
/ce
3+
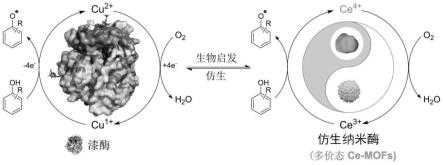
)纳米材料及其氧化还原反应性有望模拟天然漆酶的结构和功能。据此,本发明采用仿生化策略创制了新型多铈基漆酶纳米酶(见图1),并探究了其性质和应用,为新型纳米酶的创制提供了理论和实践参考。
9.本发明设计的多价态铈(ce
4+
/ce
3+
)仿生纳米酶能够模仿天然漆酶的结构和功能,利用分子氧催化底物氧化,仅产生氧化产物和水,没有二次污染,符合绿色催化理念。
10.为了实现上述目的,本发明所采取的技术方案是:
11.第一方面,本发明提供了一种仿生纳米酶,是由ce
3+
、ce
4+
和配体配位形成的金属有机框架纳米粒子,所述金属有机框架纳米粒子的表面同时含有ce
3+
和ce
4+
;所述配体为二元羧酸或三元羧酸。
12.优选的,所述ce
3+
、ce
4+
的摩尔比为1:0.5~1:1.5。
13.进一步优选的,所述ce
3+
、ce
4+
的摩尔比为1:0.7~1:1.2。
14.优选的,所述配体选自对苯二甲酸、均苯三甲酸、2,6-萘二羧酸、丁炔二酸、富马酸、1,3,5-三(4-羧基苯基)苯中的一种。
15.进一步优选的,选自对苯二甲酸、均苯三甲酸的一种。
16.优选的,所述仿生纳米酶的粒径为20nm~1.5μm。
17.进一步优选的,所述仿生纳米酶的粒径为40nm~1.0nm。
18.第二方面,本发明提供了第一方面所述的仿生纳米酶的制备方法,包括如下步骤:将可溶性铈盐的水溶液和配体混合,进行反应,得到仿生纳米酶。
19.优选的,所述可溶性铈盐选自(nh4)2ce(no3)6、ce(so4)2、cef4中的一种或多种。
20.进一步优选的,所述可溶性铈盐选自(nh4)2ce(no3)6。
21.具体地,可溶性铈盐为含有四价铈的可溶性盐。
22.优选的,所述配体选自对苯二甲酸、均苯三甲酸、2,6-萘二羧酸、丁炔二酸、富马酸、1,3,5-三(4-羧基苯基)苯中的一种。
23.进一步优选的,选自对苯二甲酸、均苯三甲酸的一种。
24.优选的,所述反应在15℃~110℃下进行,反应时间为10min~20min。
25.进一步优选的,所述反应在80℃~100℃下进行,反应时间为15min。。
26.优选的,所述可溶性铈盐和所述配体的摩尔比为1:0.2~1:4。
27.进一步优选的,所述可溶性铈盐和所述配体的摩尔比为1:0.3~1:3。
28.优选的,所述配体在混合前先要溶于n,n-二甲基甲酰胺或去离子水制成溶液。
29.优选的,所述反应中还添加了甲酸。
30.优选的,所述甲酸与所述配体的摩尔比为40:1~70:1。
31.进一步优选的,所述甲酸与所述配体的摩尔比为60:1~65:1。
32.具体地,所述甲酸是调制剂,其作用为:提高仿生纳米酶结晶度。
33.优选的,所述反应还包括搅拌的步骤。
34.优选的,所述的仿生纳米酶的制备方法还包括:固液分离、洗涤、溶剂交换、干燥的步骤。
35.优选的,所述固液分离的具体操作为离心或过滤。
36.进一步优选的,所述固液分离的具体操作为离心。
37.优选的,所述离心的转速10000r/min。
38.优选的,所述离心的时间为5min。
39.优选的,所述洗涤是选用强极性溶剂和丙酮进行洗涤处理。
40.优选的,所述强极性溶剂为水、n,n-二甲基甲酰胺、二甲基亚砜中的一种或多种。
41.优选的,所述溶剂交换是在将洗涤后的固体置于丙酮中浸泡24小时。
42.优选的,所述干燥为真空干燥。
43.优选的,所述真空干燥在60℃、-0.1mpa条件下进行。
44.优选的,所述真空干燥的时间为24h。
45.第三方面,本发明提供了第一方面所述仿生纳米酶在催化氧化酚类或胺类中的应用。
46.优选的,所述酚类为三氯苯酚、二氯酚、氯酚、苯酚、二甲氧基苯酚、萘酚、苯二酚、苯三酚、愈创木酚、双酚a、烷基酚中的一种。
47.进一步优选的,所述酚类为双酚a或烷基酚。
48.更进一步优选的,所述酚类为双酚a。
49.优选的,所述胺类为苯胺或苯胺的衍生物。
50.具体地,本发明中的仿生纳米酶不仅能够在在催化氧化酚类或胺类中表现出典型的米氏动力学,具有类似或优于天然漆酶的催化活性,而且可催化氧化多种酚类及胺类等典型漆酶模型底物。更重要的是,所述仿生纳米酶能够有效降解环境雌激素中的酚类(特别是,双酚a)的污染物,可用于环境治理、检测等方面。
51.第四方面,本发明提供了第一方面所述仿生纳米酶在检测硫醇类污染物中的应用。
52.优选的,所述硫醇类污染物为2-巯基苯并噻唑、叔丁硫醇、苄硫醇中的一种。
53.进一步优选的,所述硫醇类污染物为苄硫醇。
54.优选的,所述应用中选用650nm吸光度的检测的条件。
55.优选的,所述应用中测得的标准曲线r2值为0.99~0.9999。
56.优选的,所述应用中的检测限为0.1ppm~5.0ppm。
57.进一步优选的,所述应用中的检测限为0.15ppm~4.3ppm。
58.具体地,所述2-巯基苯并噻唑的检测限为0.70ppm~0.90ppm,所述叔丁硫醇的检测限为4.0ppm~4.3ppm,所述苄硫醇的检测限为0.15ppm~0.20ppm。
59.优选的,所述应用中的检测范围为0~1500μm。
60.具体地,所述2-巯基苯并噻唑的检测线性范围为0~100μm,所述叔丁硫醇的检测线性范围为0~1500μm,所述苄硫醇的检测线性范围为0~40μm。
61.本发明的有益效果是:本发明的仿生纳米酶为含有多价态铈的金属有机框架(即ce-mofs),不仅能够模拟天然漆酶的结构和功能,而且具有活性高、稳定性强、功能性多,可循环利用和制备简单的优势,适合实际应用与推广。
62.具体地,与现有技术相比,本发明具有以下优点:
63.(1)现有基于模仿漆酶的作用机理设计出的纳米酶(漆酶仿生酶)多为铜基(纳米)材料,本质为铜基催化剂,其活性易于预见。本发明受启发于天然漆酶多铜基活性中心及其催化机理,采用多铈基金属有机框架仿生天然漆酶,其固有的多价态铈(ce
4+
/ce
3+
)及其氧化还原反应性可有效模拟天然漆酶的结构和功能,实现了纳米酶的理性仿生设计。
64.(2)基于本发明的核心原理,本发明的仿生纳米酶可经一步反应得到,具有原料来源广泛、成本低廉,制备过程简单、条件温和、稳定性好等特点,易于重复和推广。
65.(3)本发明所得到的的仿生纳米酶ce-bdc和ce-btc不仅具有良好的模拟漆酶活性(优于等质量浓度天然漆酶)及拟酶催化特性(米氏动力学),而且表现出优异的催化稳定性及重复利用性能,为其实际应用奠定了良好基础。
66.(4)本发明提供了一种硫醇污染物简单快速的比色传感检测方法,具有便捷、准确、灵敏、专一的特点,这是纳米酶在硫醇污染物检测方面较早的探索和实践,拓宽漆酶纳米酶应用范围。
67.(5)本发明中的仿生酶纳米酶ce-bdc和ce-btc可应用于环境污染bpa(双酚a)的降解,降解能力优于等质量浓度的天然漆酶,并能够便捷回收及循环利用,为bpa治理提供了备选策略。
68.(6)本发明采用仿生化策略制备了一系列新型铈基漆酶纳米酶,具有理性、便捷、高效、广适的特点,为新型纳米酶的创制提供了新的思路参考,并为纳米酶在环境催化方面的应用提供了实践例证,具有良好的参考价值及应用前景。
附图说明
69.图1为本发明的仿生纳米酶的反应机理图。
70.图2为实施例1~6中的仿生纳米酶的pxrd谱图。
71.图3为实施例1~6中的仿生纳米酶的sem图。
72.图4为实施例1~6中的仿生纳米酶的ce 3d精细谱图。
73.图5为实施例1和实施例2中的配体、铈离子、仿生纳米酶的催化氧化2,4-dp结果图。
74.图6为实施例1~6中的仿生纳米酶催化氧化2,4-dp初速率v0对比图和米氏动力学曲线图。
75.图7为实施例1和实施例2中的仿生纳米酶催化氧化不同酚类底物的活性对比图。
76.图8为实施例1和实施例2中的仿生纳米酶催化氧化邻苯二胺和愈创木酚的相对活性图。
77.图9为实施例1和实施例2中的仿生纳米酶催化氧化对苯二胺和abts的相对活性图。
78.图10为实施例1和实施例2中的仿生纳米酶催化氧化对苯二酚的相对活性图。
79.图11为实施例1和实施例2中的仿生纳米酶的催化稳定性能图。
80.图12为实施例1和实施例2中的仿生纳米酶用于检测硫醇污染物的紫外光谱图和标准曲线图。
81.图13为实施例2中的仿生纳米酶用于检测tbm和bm的标准曲线图。
82.图14为实施例1和实施例2中的仿生纳米酶用于硫醇污染物检测的抗干扰实验结果图。
83.图15为实施例1和实施例2中的仿生纳米酶、铈离子、配体、离心上清液用于降解双酚a的性能图。
84.图16为实施例1和实施例2中的仿生纳米酶的降解bpa的米氏动力学曲线图。
85.图17为实施例1和实施例2中的仿生纳米酶在不同循环次数条件下测得的相对活性图。
具体实施方式
86.以下通过具体的实施例对本发明的内容作进一步详细的说明。
87.实施例1
88.一种仿生纳米酶的制备方法,具体包括以下步骤:
89.1)金属和配体预溶解:称取584mg(1.066mmol)的硝酸铈铵(即(nh4)2ce(no3)6)溶于2.0ml去离子水,另取对苯二甲酸(h2bdc)177mg(1.066mmol)溶于6.0mln,n-二甲基甲酰胺(dmf),分别得到澄清透明的含铈金属离子溶液和配体溶液;
90.2)水热反应:将步骤1)所得的两种溶液均匀混合于10ml玻璃反应瓶中,拧紧瓶盖,
转移至100℃油浴中,温和搅拌反应15min后冷却至室温(25℃),离心(转速:10000r/min,时间:5min)收集沉淀;
91.3)洗涤:采用dmf(3
×
6ml,即3次、6ml的dmf进行洗涤)和丙酮(3
×
6ml,即3次、6ml的丙酮进行洗涤)依次洗涤沉淀,洗涤后将沉淀分散于6.0ml丙酮中浸渍24h以充分置换dmf,离心收集沉淀(转速:10000r/min,时间:5min);
92.4)干燥:将步骤3)所得沉淀置于真空干燥箱中,设置在60℃、-0.1mpa条件下干燥24h,充分干燥后用药匙碾碎至粉末状,得到仿生纳米酶(记为ce-bdc,米白色粉末状,产率:50.97%)。
93.实施例2
94.一种仿生纳米酶的制备方法,具体包括以下步骤:
95.1)金属和配体预溶解:称取877mg(1.599mmol)的硝酸铈铵(即(nh4)2ce(no3)6)溶于3.0ml去离子水,另取均苯三甲酸(h3btc)112mg(0.533mmol)溶于6.0mldmf,其中加入1.285ml(34.15mmol)甲酸,分别得到澄清透明的含铈金属离子溶液和配体(含调制剂)溶液;
96.2)水热反应:将步骤1)所得的两种溶液均匀混合于10ml玻璃反应瓶中,拧紧瓶盖,转移至100℃油浴中,温和搅拌反应15min后冷却至室温(25℃),离心(转速:10000r/min,时间:5min)收集沉淀;
97.3)洗涤:采用dmf(3
×
6ml)和丙酮(3
×
6ml)依次洗涤沉淀,洗涤后将沉淀分散于6.0ml丙酮中浸渍24h以充分置换dmf,离心收集沉淀(转速:10000r/min,,时间:5min);
98.4)干燥:将步骤3)所得沉淀置于真空干燥箱中,设置在60℃、-0.1mpa条件下干燥24h,充分干燥后用药匙碾碎至粉末状,得到仿生纳米酶(记为ce-btc,黄白色粉末状,产率:62.40%)。
99.实施例3
100.一种仿生纳米酶的制备方法,具体包括以下步骤:
101.1)金属和配体预溶解:称取584mg(1.066mmol)的硝酸铈铵(即(nh4)2ce(no3)6)溶于2.0ml去离子水,另取2,6-萘二羧酸(h2ndc)230mg(1.066mmol)溶于6.0mldmf,分别得到澄清透明的含铈金属离子溶液和配体溶液;
102.2)水热反应:将步骤1)所得的两种溶液均匀混合于10ml玻璃反应瓶中,拧紧瓶盖,转移至100℃油浴中,温和搅拌反应15min后冷却至室温(25℃),离心(转速:10000r/min,时间:5min)收集沉淀;
103.3)洗涤:分别采用二甲基亚砜(dmso,2
×
6ml)、dmf(3
×
6ml)和丙酮(3
×
6ml)依次洗涤沉淀,然后将沉淀分散于6.0ml丙酮中浸渍24h以充分置换dmso和dmf,离心收集沉淀(转速:10000r/min,时间:5min);
104.4)干燥:将步骤3)所得沉淀置于鼓风干燥箱中,60℃干燥24h,充分干燥后用药匙碾碎至粉末状,得到仿生纳米酶(记为ce-ndc,淡黄色粉末状,52.86%)。
105.实施例4
106.一种仿生纳米酶的制备方法,具体包括以下步骤:
107.1)金属和配体预溶解:称取292mg(0.533mmol)的硝酸铈铵(即(nh4)2ce(no3)6)溶于1.0ml去离子水,另取丁炔二酸(h2adc)182mg(1.599mmol)溶于6.0ml去离子水,分别得到
澄清透明的含铈金属离子溶液和配体溶液;
108.2)反应:将步骤1)所得的含铈金属离子溶液在温和搅拌状态下加入到配体溶液中,室温(25℃)下温和搅拌反应15min,离心(转速:10000r/min,时间:5min)收集沉淀;
109.3)洗涤:采用去离子水(3
×
6ml)和丙酮(3
×
6ml)依次洗涤沉淀,洗涤后将沉淀分散于6.0ml丙酮中浸渍24h以充分置换h2o,离心收集沉淀(转速:10000r/min,时间:5min);
110.4)干燥:将步骤3)所得沉淀置于鼓风干燥箱中,60℃下干燥24h,充分干燥后用药匙碾碎至粉末状,得到仿生纳米酶(记为ce-adc,白色粉末状,产率:71.3%)。
111.实施例5
112.一种仿生纳米酶的制备方法,具体包括以下步骤:
113.1)金属和配体预溶解:称取584mg(1.066mmol)的硝酸铈铵(即(nh4)2ce(no3)6)溶于2.0ml去离子水,另取富马酸(h2fum)124mg(1.066mmol)溶于6.0mldmf,分别得到澄清透明的含铈金属离子溶液和配体溶液;
114.2)水热反应:将步骤1)所得的含铈金属离子溶液和配体溶液均匀混合于10ml玻璃反应瓶中,拧紧瓶盖,转移至100℃油浴中,温和搅拌反应15min后冷却至室温(25℃),离心(转速:10000r/min,时间:5min)收集沉淀;
115.3)洗涤:采用dmf(3
×
6ml)和丙酮(3
×
6ml)依次洗涤沉淀,洗涤后将沉淀分散于6.0ml丙酮中浸渍24h以充分置换dmf,离心收集沉淀(转速:10000r/min,,时间:5min);
116.4)干燥:将步骤3)所得沉淀置于鼓风干燥箱中,60℃下干燥24h,充分干燥后用药匙碾碎至粉末状,得到仿生纳米酶(记为ce-fum,淡黄白色粉末状,产率:50.97%)。
117.实施例6
118.一种仿生纳米酶的制备方法,具体包括以下步骤:
119.1)金属和配体预溶解:称取292mg(0.533mmol)的硝酸铈铵(即(nh4)2ce(no3)6)溶于1.0ml去离子水,另取1,3,5-三(4-羧基苯基)苯(h3btb)78.5mg(0.179mmol)溶于3.0mldmf,分别得到澄清透明的含铈金属离子溶液和配体溶液;
120.2)水热反应:将步骤1)所得的配体溶液逐滴加入到含铈金属离子溶液中(80℃),保持80℃温和搅拌反应15min后冷却至室温(25℃),然后重新加热至80℃,温和搅拌反应15min,逐渐产生晶体沉淀,反应结束后冷却至室温(25℃),离心(转速:10000r/min,,时间:5min)收集沉淀;
121.3)洗涤:采用dmf(3
×
4ml)和丙酮(3
×
4ml)依次洗涤沉淀,洗涤后将沉淀分散于4.0ml丙酮中浸渍24h以充分置换dmf,离心收集沉淀(转速:10000r/min,时间:5min);
122.4)干燥:将步骤3)所得沉淀置于鼓风干燥箱中,60℃下干燥24h,充分干燥后用药匙碾碎至粉末状,得到仿生纳米酶(记为ce-btb,黄色粉末状,产率:58.34%)。
123.漆酶纳米酶的表征和性能测试
124.本发明的实施例1~6仿生纳米酶的反应机理图,如图1所示。
125.由图1可知:漆酶(英文名:laccase)是一种含四个铜离子的多酚氧化酶(ρ-二元酚氧化酶,ec 1.10.3.2),属于铜蓝氧化酶,以单体糖蛋白的形式存在。漆酶存在菇、菌及植物中,亦可存活于空气中,发生反应后唯一副产物是水,故其本质上是一种环保型酵素。本发明受天然漆酶多铜基活性中心及其催化过程中cu
2+
/cu
1+
电子转移路径启发,设计制备了一系列铈基金属有机框架(ce-mofs)的仿生纳米酶,其具有的多价态铈(ce
4+
/ce
3+
)为模拟天
然漆酶的结构和功能创设了条件。
126.表征测试的类型:分别采用x-射线粉末衍射(powder x-ray diffraction,简称:pxrd)、扫描电子显微镜(scanning electron microscope,简称:sem)以及x-射线光电子能谱(x-ray photoelectron spectroscopy,简称:xps)对实施例1
–
6所得的漆酶纳米酶进行表征鉴定。
127.表征测试的仪器与条件:采用panalytical x'pert型号粉末x-射线粉末衍射仪记录纳米酶pxrd图谱,测试条件为:cu kα射线,电压40kv,电流40ma,波长扫描速度12
°
/min,扫描范围2-50
°
。采用merlin场发射扫描电子显微镜(zeiss,germany)观测漆酶纳米酶的微观形态:样品水悬浮液经稀释后滴于洁净硅片上,待水挥发(干燥)后喷金,上机测试,加速电压设定为5kv。采用thermo scientific k-alpha xps测试系统记录纳米酶的ce 3d的xps精细图谱,单色al kα源,hv=1486.6ev。
128.1)实施例1~6中的仿生纳米酶的pxrd谱图,如图2所示,其中,a为实施例1和实施例2中的仿生纳米酶的pxrd谱图;b为实施例3~6中的仿生纳米酶的pxrd谱图。
129.由图2可知:实施例1~6中纳米酶的pxrd谱图中都有尖锐的特征峰,且均表现出良好的晶体结构,可证明这些漆酶纳米酶为有序拓扑,而非无序聚集体。以ce-bdc和ce-btc(图2中的a)为例,实验测得的pxrd图谱与模拟数据高度一致,确证了他们具有有序的晶体拓扑结构;其中,ce-bdc是由六核铈簇[ce6o4(oh)4]
12+
与h2bdc通过12连接形成的密集立方体fcc拓扑结构,分子式为[ce6o4(oh)4(bdc)6];ce-btc是由六核铈簇[ce6o4(oh)4]
12+
与h3btc通过6连接形成spn拓扑结构,分子式为[ce6o4(oh)4(btc)6(oh)6(h2o)6]。
[0130]
而实施例3~6中的ce-ndc、ce-adc、ce-fum以及ce-btb的pxrd图谱亦均符合预期,其中,ce-ndc、ce-adc与ce-fum拓扑结构类似于ce-bdc(ce-uio-66);ce-btb类似于ce-btc(ce-mof-808),结晶度稍差。
[0131]
2)实施例1~6中的仿生纳米酶的sem图,如图3所示;其中,a为实施例1中的仿生纳米酶(ce-bdc);b为实施例2中的纳米酶(ce-btc);c为实施例3中的纳米酶(ce-ndc);d为实施例4中的纳米酶(ce-adc);e为实施例5中的纳米酶(ce-fum);f为实施例6中的纳米酶(ce-btb)。
[0132]
由图3可知:实施例1~6中的仿生纳米酶呈现出形貌和尺寸各异的微观形态。具体地,ce-bdc为均一的纳米颗粒,呈现畸变多面体形貌,平均粒径约为400nm~500nm;ce-btc也是较为均一的纳米颗粒,呈流星锤状,颗粒表面均匀分布着刺状突起,平均粒径约为300nm~400nm;ce-ndc、ce-adc与ce-fum也为均一的纳米颗粒,其中,ce-ndc为表面分布褶皱的纳米球,平均粒径约为500nm~1.0μm,ce-adc为超小纳米球,平均粒径小于50nm;ce-fum形貌类似于ce-bdc,ce-btb为不规则纳米片组装成的纳米球,径向尺寸约200nm,宏观呈现粉末状。
[0133]
3)实施例1~6中的仿生纳米酶的x-射线光电子能谱测得的ce 3d精细图谱,如图4所示;其中,a为实施例1中的仿生纳米酶ce-bdc的ce 3d精细图谱;b为实施例2中的仿生纳米酶ce-btc的ce 3d精细谱图;c为为实施例3~6中的仿生纳米酶的ce 3d精细谱图。
[0134]
由图4可知:ce 3d的谱图表示实施例1~6中仿生纳米酶表面均存在混合价态铈离子(ce
3+
/ce
4+
)。以实施例1中的ce-bdc为例(图4中的a),位于917.32ev、907.55ev、901.84ev、888.88ev和882.81ev的信号峰归属于ce
4+
,而位于904.38ev、899.27ev和
885.96ev的峰值则归属于ce
3+
。
[0135]
对于实施例2中的ce-btc(图4中b),917ev,907.09ev,901.54ev,887.08ev以及883.25ev的信号峰为ce
4+
,而位于904.24ev,899.23ev,885.49ev以及881.67ev的信号峰则归属于ce
3+
。同理,ce-ndc、ce-adc、ce-fum以及ce-btb也表明了ce
3+
和ce
4+
的共存(参见图4中的c),以ce-ndc为例,其ce 3d信号包括v0(883.30ev)、v(883.71ev)、v'(886.47ev)、v'(889.47ev)、v'(898.13ev)和u0(899.25ev)、u(901.64ev)、u'(904.63ev)、u'(907.70ev)、u'(917.44ev),其中v0、v'、u0、u'的信号峰归属于ce
3+
,而v、v”、v”、u、u”、u”的信号峰则归属于ce
4+
。这些铈基金属有机框架中多价态铈离子(ce
3+
/ce
4+
)的共存为仿生天然漆酶打下了结构基础。
[0136]
同时,对实施例1~6中的仿生纳米酶进行xps测试,并通过数据处理得出ce
4+
和ce
3+
的摩尔百分比,如表1所示。
[0137]
表1实施例1~6中的中的仿生纳米酶进行xps测试结果
[0138][0139]
注:表1中的分数均为摩尔百分数。
[0140]
由表1可知:实施例1~6中的仿生纳米酶均均有多价态的铈,且实施例1~6中的仿生纳米酶ce
4+
和ce
3+
的摩尔比为0.75:1~1.10:1。
[0141]
应用1:仿生纳米酶的酶活性评价
[0142]
一种酶活性评价方法,具体包括以下步骤:
[0143]
1)以2,4-dp(2,4-二氯酚)为模型底物测定实施例1
–
6所得的漆酶纳米酶的拟酶活性。具体地,将2,4-dp(2,4-二氯酚,2.0mg/ml,50μl)和4-ap(4-氯酚,2.0mg/ml,50μl,用作显色剂)依次加入到800μl的naac-hac缓冲液(0.2m,ph=6.8)中,随后向上述溶液中添加100μl仿生纳米酶的水悬浮液(1.0mg/ml)或其等量参比(金属离子、配体等),充分混合后室温(25℃)下反应45分钟,离心(10000r/min,3min)去除纳米酶,并在uv=510nm(2,4-dp的氧化产物和4-ap的复合物在此波长下有吸收)处测定上清液的吸光度,评价拟酶活性。
[0144]
测试原理:2,4-dp在漆酶纳米酶的存在下被氧化为相应的醌,进一步与4-ap结合生成有色产物,在uv=510nm下有最大吸收。
[0145]
2)采用同样的方法评价了ce-bdc和ce-btc对不同酚类底物的催化氧化能力,酚类底物包括:苯酚、4-氯酚、2,4-二氯酚、2,4,6-三氯苯酚、2,6-二甲氧基苯酚、1-萘酚、2-萘酚、邻苯二酚、对苯二酚、间苯二酚、间苯三酚和焦性没食子酸(1,2,3-三羟基苯)。
[0146]
3)还采用其他经典漆酶底物及模式反应评价了ce-bdc和ce-btc的仿生纳米酶(模
拟漆酶)的活性,包括邻苯二胺、对苯二胺、愈创木酚、对苯二酚和abts(2,2'-联氮-双-3-乙基苯并噻唑啉-6-磺酸,是一种介体物质,常用来测定漆酶的酶活性)。
[0147]
需要说明的是,2,4-dp在漆酶纳米酶的存在下被氧化为相应的醌,进一步与4-ap结合生成有色产物,在uv=510nm下有最大吸收。
[0148]
酶活性评价结果:
[0149]
1)实施例1和实施例2中的配体、铈离子、仿生纳米酶的催化氧化2,4-dp(即2,4-二氯酚)结果,如图5所示;其中,a为不同价态的铈离子、不同种类的配体、实施例1中的仿生纳米酶(ce-bdc)和实施例2中的仿生纳米酶(ce-btc)在正常条件下催化氧化2,4-dp结果图;b为实施例1中的仿生纳米酶(ce-bdc)和实施例2中的仿生纳米酶(ce-btc)在正常条件和缺氧(hypoxia)条件下催化氧化2,4-dp结果对比图。
[0150]
由图5的a可知:为了验证此催化活性是否源自配体或金属离子,在同等条件下测定了ce
3+
、ce
4+
、h2bdc(bdc配体)、h3btc(btc配体)对2,4-dp的氧化能力,结果表明等质量浓度的ce
4+
表现出了中等强度的催化能力,而ce
3+
、h2bdc和h3btc未表现出任何活性。为了排除ce
4+
的可能性,对ce-bdc和ce-btc的离心上清液进行了同样的活性测定,结果表明二者的离心上清液均未表现出模拟酶活性。以上充分表明了ce-bdc和ce-btc固有的模拟漆酶活性。
[0151]
由图5的b可知:天然漆酶以分子氧为最终电子受体氧化还原性底物,为了验证仿生纳米酶ce-bdc和ce-btc是否有类似的特性,分别在正常和乏氧条件下对二者进行了活性测定。结果表明:在缺氧条件下了ce-bdc和ce-btc二者催化活性几乎被完全抑制,表明ce-bdc和ce-btc氧化2,4-dp具有对氧气依赖性,与天然漆酶类似。
[0152]
2)实施例1~6中的仿生纳米酶催化氧化2,4-dp初速率v0对比图和米氏动力学曲线图,如图6所示,其中,a为漆酶、实施例1和实施例2中的仿生纳米酶ce-bdc和ce-btc的催化氧化2,4-dp初速率v0对比图;b为漆酶、实施例3~6中的仿生纳米酶的催化氧化2,4-dp初速率v0对比图;c为漆酶、实施例1和实施例2中的仿生纳米酶ce-bdc和ce-btc的米氏动力学曲线;d为漆酶、实施例3~6中的仿生纳米酶的的米氏动力学曲线。不同类型的酶的催化氧化2,4-dp的动力学参数,如表2所示。
[0153]
由图6和表2可知:ce-bdc和ce-btc对2,4-dp的氧化能力明显优于等质量浓度的天然漆酶,三者催化氧化2,4-dp反应初速率分别为1.319μm
·
min-1
、1.759μm
·
min-1
和0.29μm
·
min-1
。同理可得,ce-ndc、ce-adc、ce-fum以及ce-btb的良好模拟酶活性,其催化氧化2,4-dp反应初速率分别1.40μm
·
min-1
,1.06μm
·
min-1
,0.81μm
·
min-1
,1.23μm
·
min-1
。
[0154]
另外,酶催化的典型特征是符合米氏动力学(michaelis-menten)催化模型。为了验证实施例1~6中的仿生纳米酶也进行米氏动力学非线性曲线拟合,结果如附图6中的c和d所示,其曲线的拟合相关系数均大于0.99,表明实施例1~6中的仿生纳米酶催化2,4-dp符合米氏动力学模型,具有与漆酶类似的催化动力学规律。
[0155]
不同类型的酶的催化氧化2,4-dp的动力学参数,如表2所示。由表2可知:实施例1~6中的仿生纳米酶表现出较高的最大反应速率(v
max
)、较低的米氏常数(km)与相同质量浓度下较高的催化效率(k
cat
/km),其中,催化效率最好的是ce-btc,其次是ce-ndc、ce-btb、ce-adc、ce-bdc、ce-fum(酶活性由高到低排列)。
[0156]
表2不同类型的酶的催化氧化2,4-dp的动力学参数
[0157][0158]
注:表2中的a和b分别代表相同摩尔浓度和质量浓度下的催化效率。
[0159]
综上,实施例1~6中的仿生纳米酶不仅具有良好的酶活性,其催化过程还符合典型的酶动力学规律。
[0160]
3)天然漆酶具有广谱的底物范围,以实施例1和实施例2中的仿生纳米酶为例,还研究了仿生纳米酶ce-bdc和ce-btc对不同种类底物的催化活性,如图7所示。
[0161]
由图7可知:仿生纳米酶ce-bdc和ce-btc不仅能够氧化2,4-dp,对其他酚类底物也表现出了良好的催化活性,包括单酚、双酚、三酚、萘酚、氯酚等,均优于等质量浓度的天然漆酶,尤其对4-氯酚、2,4-二氯苯酚和2,6-二甲氧基苯酚催化活性较高。
[0162]
4)实施例1和实施例2中的仿生纳米酶催化氧化邻苯二胺和愈创木酚的相对活性图,分别如图8中的a和b。实施例1和实施例2中的仿生纳米酶催化氧化对苯二胺和2,2'-联氮-双-3-乙基苯并噻唑啉-6-磺酸(简称:abts)的相对活性图,分别如图9中的a和b所示。图10为实施例1和实施例2中的仿生纳米酶催化氧化对二苯酚的相对活性图。
[0163]
由图8、图9和图10可知:仿生纳米酶ce-bdc和ce-btc可催化氧化芳香胺(邻苯二胺和对苯二胺)、愈创木酚、对苯二酚和abts,且对于芳香胺、愈创木酚和对苯二酚的活性均优于等质量浓度天然漆酶。
[0164]
综上,可以说明本发明的仿生纳米酶具有广谱的底物范围,使用范围广。
[0165]
仿生纳米酶的稳定性及重复利用性能评价
[0166]
仿生纳米酶的稳定性及重复利用性能的评价方法:将实施例1和实施例2中的仿生纳米酶ce-bdc和ce-btc在不同条件处理后测试其活性,通过检测仿生酶活性来评判其稳定性,评价结果如图11所示。
[0167]
1)ph稳定性:分别将ce-bdc、ce-btc及天然漆酶在不同ph(3~10)条件下孵育8.0小时,然后评估催化活性,并与未处理(空白对照)组进行对比,其评价结果如图11中的a所示。
[0168]
由图11中的a可知:经不同ph条件处理后纳米酶的相对活性均高于同等条件处理下的天然漆酶,尤其是在中性(ph≈7)和偏酸性(ph《7)条件下,但经碱性条件处理后纳米酶和天然漆酶的活性均有所降低。
[0169]
2)热稳定性:分别将ce-bdc、ce-btc和天然漆酶在不同温度(-20℃~100℃)下处理1.0小时(在水介质中),然后根据上述活性方法进行评估,并与未处理(空白对照)组进行对比,结果如图11中的b所示。
[0170]
由图11中的b可知:温度过高和过低都会对天然漆酶活性产生明显的抑制,尤其是当温度高于40℃后,天然漆酶逐渐失活,直至70℃以上完全失活,而相同的热处理对纳米酶
ce-bdc和ce-btc活性影响很小,表明纳米酶具有良好的热稳定性。
[0171]
3)不同介质中的稳定性:类似地,采用不同浓度nacl和乙醇处理(孵育)纳米酶或天然漆酶,以评价其对离子强度和有机溶剂耐受性,评价结果如图11中的c和d所示。
[0172]
由图11中的c和d可知:在0~500mm浓度范围内,随着氯化钠浓度的增加,天然漆酶的活性逐渐降低,而纳米酶活性未受到显著影响,表明其良好的离子强度耐受能力;随着乙醇浓度的增大,天然漆酶的活性逐渐降低,直至乙醇浓度高于50%时完全失活,而同等条件下纳米酶ce-bdc的活性未有显著改变,ce-btc活性有所降低,但仍显著高于天然漆酶,表明了纳米酶良好的有机溶剂耐受能力。
[0173]
4)储存稳定性:分别将仿生纳米酶(ce-bdc和ce-btc)水悬浮液和漆酶水溶液在室温(约25℃)下储存20天,在特定时间点测定其活性,结果见图11中的e。
[0174]
由图11中的e可知:随着储存时间的延长,天然漆酶活性显著降低,约12天后完全失活,而纳米酶的相对活性未有显著改变,表明其良好的储存稳定性。
[0175]
5)循环稳定性评价:每一次催化结束后,采用离心、水洗的方式回收纳米酶,并用于下一次循环催化,ce-bdc和ce-btc的循环稳定性测试结果如图11中的f所示。
[0176]
图11中的f表明:仿生纳米酶可经离心水洗后便捷回收,而天然漆酶作为可溶性蛋白则无法实现回收,经过8个批次催化循环之后,ce-bdc和ce-btc的相对活性仍分别保留90.16%和83.04%,表明纳米酶ce-bdc和ce-btc良好的重复利用性能。
[0177]
应用2:漆酶纳米酶ce-bdc和ce-btc用于硫醇污染物的检测
[0178]
硫醇类化合物是一类典型的含硫环境污染物,对环境安全和人体健康具有潜在威胁。本发明所述漆酶纳米酶可用于硫醇污染物的便捷检测,原理在于所述漆酶纳米酶可氧化tmb(3,3',5,5'-四甲基联苯胺)生成蓝色oxtmb(氧化态3,3',5,5'-四甲基联苯胺),而硫醇化合物巯基可使蓝色变浅或褪去,此过程与硫醇化合物浓度线性相关,以此建立比色检测方法。
[0179]
一种硫醇污染物的检测的构建(以ce-bdc和ce-btc为例),其具体包括以下步骤:
[0180]
1)tmb的氧化:取0.5mltmb乙醇溶液(800mm)以及0.5ml漆酶纳米酶(ce-bdc或ce-btc)水悬浮液(1.0mg/ml)依次加入到9.0mlnaac-hac缓冲液中,混匀后反应5min,离心、过膜去除纳米酶,得到蓝色氧化态tmb(oxtmb);
[0181]
2)硫醇污染物标准曲线的建立:取0.1ml系列浓度的mbtz(2-巯基苯并噻唑)加入到0.9ml步骤1)所述的oxtmb中,充分混匀后室温(25℃)下反应约1.0h,测紫外光谱(500
–
800nm)及650nm吸光度值,以mbtz浓度为横坐标、650nm处吸光度差值(即δ650nm,空白组和实验组吸光度差)为纵坐标建立硫醇污染物检测标准曲线;
[0182]
3)硫醇污染物的检测:3份污水样品(人工湖水样)经高速离心后过膜,采用标准添加法加入一定浓度的硫醇污染物,得到待测样品,采用步骤2)所述的方法以ce-btc为催化剂对标准添加mbtz进行比色检测。
[0183]
采用如步骤1)和2)所述方法以ce-btc为例,建立tbm(叔丁硫醇)和bm(苄硫醇)定标准曲线,其曲线构建的结果如图13所示。
[0184]
通过上述方法构建的实施例1(ce-bdc)和实施例2(ce-btc)中的仿生纳米酶用于检测硫醇污染物(简称:mbtz)的紫外光谱图和标准曲线图,如图12所示;其中,a和c分别为ce-bdc检测mbtz的紫外光谱和标准曲线;b和d为分别为ce-btc检测mbtz的紫外光谱和标准
曲线。
[0185]
由图12和图13可知:以ce-bdc和ce-btc仿生纳米酶为催化剂,mbtz检测线性范围均为0~100μm,检测限分别为5.34μm(0.89ppm)和4.26μm(0.71ppm);以ce-btc为催化剂,tbm和bm的检测线性范围分别为0~1500μm和0~40μm,检测限分别为47.61μm(4.29ppm)和1.39μm(0.17ppm)。
[0186]
实施例1和实施例2中的仿生纳米酶用于硫醇污染物检测的抗干扰实验结果图,如图14所示。
[0187]
由图14可知:抗干扰实验结果表明,常见的一些盐离子(na
+
,k
+
,mg
2+
,ca
2+
,cl-,so
42-和co
32-)、小分子(葡萄糖、蔗糖、尿素和甘油)以及氨基酸(丙氨酸、亮氨酸、组氨酸和苯丙氨酸)等对oxtmb(氧化态的tmb)的脱色反应几乎没有响应,表明该方法对硫醇污染物检测的特异性。
[0188]
用于检测硫醇污染物的方法的可信度分析结果,如表3所示。
[0189]
由表3可知:对三份加标污水样品(加入mbtz标样的人工湖水)中mbtz测定的回收率在96.27%到104.19%之间,标准差rsd(n=3)值低于4.53%,表明了该方法的准确性。而且,表3中的回收率是指实测值和理论值的比值,而回收率在100%附近表明该方法的准确性。
[0190]
表3用于检测硫醇污染物的方法的可信度分析结果
[0191][0192]
上述结果表明:本发明中的仿生纳米酶(特别是ce-bdc和ce-btc)可用于硫醇污染物检测,且检测结果具有简易、灵敏、特异、准确的特点。
[0193]
应用3:漆酶纳米酶ce-bdc和ce-btc用于双酚a的降解
[0194]
双酚a(bpa)是现代工业尤其是塑料行业中的一种重要原料,是一种典型的内分泌干扰物,可影响生殖行为和身体发育。
[0195]
本发明所述漆酶纳米酶ce-bdc和ce-btc可作为催化剂,用于bpa的降解。
[0196]
一种双酚a的处理方法,具体包括以下步骤:将0.2mlbpa(5.0mg/ml,乙醇溶液)添加到含有5.0mg纳米酶或天然漆酶的pb缓冲液(磷酸缓冲液,4.8ml)中,室温(25℃)下温和磁力搅拌(300r/min)反应12h,反应结束后取1.0ml反应混合物,离心去除催化剂,上清液用等容积乙酸乙酯萃取残余双酚a(bpa),高效液相色谱(hplc)分析,以测定双酚a(bpa)降解率。
[0197]
通过改变双酚a的处理方法中的催化剂的种类得到不同条件下bpa(双酚a)的降解率,以评价bpa降解的影响因素,其结果如图15所示。
[0198]
由图15中的a可知:结果表明仿生纳米酶ce-bdc和ce-btc具有良好的bpa降解能力,按照上述实验条件,天然漆酶、ce-bdc和ce-btc对bpa的降解率分别为25.10%、75.67%以及86.34%,显然仿生纳米酶降解能力明显优于天然漆酶。
[0199]
从图15中的b可知:图中s-ce-bdc和s-ce-btc表示两种纳米酶的离心上清液。通过比较降解率的结果,可得出仿生纳米酶的这种催化活性源于纳米酶本身,而非其配体或铈离子(ce
4+
)。虽然ce
4+
表现出一定的催化活性,但是仿生纳米酶离心上清液活性很低,降解过程属氧化降解,而非物理吸附。
[0200]
通过调整不同反应条件并测试其对于双酚a(bpa)降解效果,发现bpa的降解较适于在室温(25℃)、ph为6.0条件下进行,提高纳米酶浓度及延长反应时间利于bpa的降解。并且,通过调整不同反应条件测得的相关的动力学的相关参数结果见表4和图16。
[0201]
表4不同仿生纳米酶对于降解双酚a反应的动力学参数
[0202][0203]
注:表4中的a和b分别代表相同摩尔浓度和相同质量浓度下的催化效率。
[0204]
由表4和图16可知:仿生纳米酶催化bpa降解速率与底物浓度正相关,通过非线性曲线拟合可知纳米酶降解bpa催化过程符合米氏动力学规律,具有与天然酶类似的催化特性。
[0205]
同时,测试ce-bdc和ce-btc催化降解bpa的重复利用性能,结果如图17所示。
[0206]
由图17可知:每次使用仿生纳米酶催化降解双酚a后,仿生纳米酶可经简单的离心洗涤过程进行回收,经过6个批次的循环利用之后,ce-bdc和ce-btc的相对活性仍分别保留73.43%以及65.82%,表现出了优异的重复利用性能。
[0207]
上述结果表明:实施例1和实施例2中的仿生纳米酶ce-bdc和ce-btc具有良好的bpa降解能力,可作为天然漆酶的有效替代品。同时,本发明中的仿生纳米酶具有可循环再利用的效果。
[0208]
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1