间隙和置换Sn掺杂的硫化铋材料及其制备方法和应用
间隙和置换sn掺杂的硫化铋材料及其制备方法和应用
技术领域
1.本发明属于材料制备及电催化领域,具体是提出一种用于电催化二氧化碳还原的间隙和置换sn
4+
掺杂的硫化铋材料。
背景技术:
2.将温室气体co2化学转化为有附加值的化工原料或燃料是固定co2的一条有希望的途径,从而缓解co2排放的不断增加以及化石燃料日益短缺所造成的能源压力。以可再生能源(如太阳能、风能和潮汐能)为动力的co2电化学还原反应(co2rr)作为实现环境和能源可持续性的一种有前景的战略,已引起越来越多的关注。然而,同时获得理想的活性和满意的选择性通常受到co2分子的化学惰性、复杂的co2rr途径和水溶液中析氢反应(her)的限制。因此,非常需要开发具有优异活性和选择性的电化学还原co2电催化剂一般来说,通过使用不同的电催化剂,可以从co2rr中获得co、甲酸盐、甲醇、乙烯等。在这些增值产品中,甲酸盐(或液体甲酸)非常有吸引力,因为它是化工产品的关键原料。由于甲酸盐的特点,如易于储存和运输以及高体积氢密度,它也被视为燃料电池中有价值的氢载体。通常,一些金属,如pb、hg、in和cd,被报道为电催化剂,可以有效地将co2还原为甲酸盐。然而,许多重金属具有剧毒性或者价格昂贵,因此不适合实际应用。近年来,环保型铋基电催化剂因其成本低、选择性高而备受关注。但是一些硫化铋基催化剂,它们的选择性和活性往往不尽人意。
3.总体而言,用于co2还原的有前景的电催化剂应具有低过电位、高电流密度和良好稳定性,同时应强烈抑制her以产生具有高选择性的所需产物。
技术实现要素:
4.本发明提出一种间隙和置换sn
4+
掺杂的bi2s3材料的用于电催化二氧化碳还原制甲酸盐的催化剂。该电催化剂具有良好的电催化二氧化碳还原效果、产物利用价值高、成本低、制备工艺简单便捷,为电催化技术领域的发展提供了更多理论依据。
5.为实现上述发明目的,本发明采用如下技术方案:一种间隙和置换sn
4+
掺杂的bi2s3材料——sn
x-bi2s
3 (x代表sn与bi的摩尔比),利用二水氯化亚锡、硫代乙酰胺和氯化铋通过水热反应产生sn
x-bi2s3,其中当x=1/24时,电催化二氧化碳还原制甲酸盐的效果最好。
6.所述的sn
x
‑ꢀ
bi2s3的制备方法如下:首先将氯化铋、二水氯化亚锡、去离子水、盐酸置于烧杯中,充分搅拌至澄清溶液,将硫代乙酰胺加入上述溶液,剧烈搅拌20分钟,将上述溶液置于聚四氟乙烯水热反应釜中,从室温升温至160 ℃,保温6小时,洗涤、干燥得到sn
x
‑ꢀ
bi2s3。
7.优选的锡源是二水氯化亚锡。
8.优选的铋源是氯化铋。
9.优选的反应温度是160℃。
mg/cm2的工作电极。
20.测试采用三电极电解池结构,以上述负载了催化剂的碳纸为工作电极,铂片(1
×
1 cm)作为对电极,ag/agcl作为参比电极;使用chi 660e电化学工作站,在h型电解池中于室温(25℃)和环境压力下进行测量。
21.在整个测试过程中,二氧化碳气流以恒定的10ml
·
min-1 的速率通入到0.1mol/l co2饱和的khco3电解液(ph=6.8)中。
22.在不同的电压下进行电化学测试,每个电位下测量60分钟。气体产物直接通过在线气相色谱(gc8890, agilent, america)来检测,取样间隔20分钟。液体产物则是通过全数字化核磁共振波谱仪 600 m (液)进行检测。
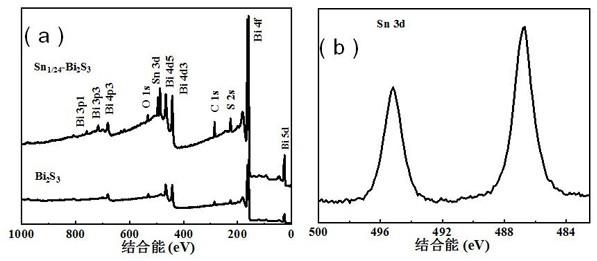
23.图1中(a)为bi2s3和sn
1/24-bi2s3的xps总谱图,通过对比,证明了sn的成功掺杂,并且通过(b)sn
1/24-bi2s3的sn3d 谱图发现495.14和486.72 ev的主峰可归因于sn
4+
的sn 3d
3/2
和sn 3d
5/2
。
24.图2中(a)是bi2s3和sn
x-bi2s
3 (x=1/2, 1/16, 1/24, 1/40)的x射线衍射图,所有样品均与bi2s3的标准卡片相匹配,并且在xrd探测范围内没有观察到第二相的衍射峰,从bi2s3的局部峰位放大图中可以看到,随着sn含量的增加,衍射峰先向低角度偏移,表明晶格常数增大,当sn含量增加到sn
1/16-bi2s3时,反向偏移至高角度,此时晶格常数减小,由于bi
3+
的半径为0.103nm,而sn
4+
的离子半径仅为0.069nm,因此当sn的含量为sn
1/40-bi2s3时,晶格常数增大可解释为sn
4+
优先进入间隙位,而当sn含量增加到sn
1/24-bi2s3,间隙固溶逐渐达到极限,当sn含量增加到sn
1/16-bi2s3和sn
1/2-bi2s3,此时sn离子开始取代bi位,表现为晶格常数开始减小。
25.图3为bi2s3和sn
1/24-bi2s3的扫描电子显微镜图,从扫描电镜图中可以看出为bi2s3为纳米棒堆积的束状结构,而sn
1/24-bi2s3为纳米线束结构,提供了更大的表面积。而当x=1/16和1/40时,sn
x-bi2s
3 产品的形貌与x=1/24产品的形貌相似,说明sn掺杂改变了bi2s3的形貌结构,但是sn的含量对形貌的影响并不大,因此我们可以排除形貌对性能的影响。
26.图4为bi2s3和sn
x-bi2s3的甲酸盐的局部电流密度图,sn掺杂后,与未掺杂的bi2s3相比,sn掺杂bi2s3的局部电流密度显著增加。bi2s3在-1.1 v甲酸盐的局部电流密度仅为-5.94 ma cm-2
,而在相同的电位下,sn
1/16-bi2s3的电流密度为-12.67 ma cm-2
,sn
1/40-bi2s3的电流密度为-7.9 ma cm-2
,而sn
1/24-bi2s3生产甲酸盐的局部电流密度为-14.2 ma cm-2
,提高了2.39倍,说明间隙掺杂的sn
1/24-bi2s3比bi2s3显示出更高的电催化二氧化碳还原活性。
27.图5为bi2s3和sn
x-bi2s3的甲酸盐的法拉第效率图,可以发现sn
1/24-bi2s3对生成甲酸盐表现出高选择性,在-0.9至-1.2 v,优于未掺杂bi2s3、sn
1/16-bi2s3、sn
1/40-bi2s3。此外,在-1.1 v的法拉第效率达到了90%,而纯bi2s3在相同的电位下,甲酸盐的法拉第效率为75%,sn
1/16-bi2s3生产甲酸盐的法拉第效率为79%,sn
1/40-bi2s3生产甲酸盐的法拉第效率为80%,综上,间隙掺杂的sn
1/24-bi2s3作为催化剂对电催化二氧化碳还原为甲酸盐的选择性更好。
28.尽管本发明的内容已经通过上述优选实施例作了详细介绍,但应当认识到上述的描述不应该被认为是对本发明的限制。在本领域技术人员阅读了上述内容后,对于本发明的多种修改和替代都是显而易见的。因此,本发明的保护范围应由所附的权利要求来限定。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1