大鼠血浆中龙虎人丹多种有效成分的检测方法与流程
本发明涉及一种龙虎人丹植物药的检测方法,具体涉及一种大鼠血浆中龙虎人丹多种有效成分HS-SPDE-GC-MS/MS检测方法,属于中药的技术领域。
背景技术:
目前关于龙虎人丹挥发性的药代动力学方面的研究还没有相关报道,其吸收进入体内的成分不清楚,不利于确定其产生药效的物质基础。
薄荷脑是一种单帖醇,具有抗炎、止痒、止痛等作用。龙脑,亦称为冰片可促进血脑屏障(BBB)的生理性开放,促进某些药物透过血脑屏障,以促进药物在脑组织的分布。冰片还能通过对P-gp底物的抑制,提高部分药物的生物利用度。龙脑在生物体内可以被氧化成樟脑。冰片是人的CYP2A6、CYP2B6、CYP3A4、CYP3A5的底物,也是UGT2B7的底物,同时也是CYP2B6中等抑制剂。其中异龙脑更易被CYP2B6代谢。冰片对CYP2C6/11、CYP3A酶的活性具有诱导作用。关于冰片的药代动力学已有研究报道。然而,这些成分和单味药的药代动力学的研究,如血药动力学、吸收、代谢、排泄等,所阐明的药动学规律难以反映龙虎人丹的药动学规律。为了进龙虎人丹多种挥发性成分的药动学研究,必须建立血浆多种挥发性成分的测定方法。
技术实现要素:
本发明的目的在于,提供大鼠血浆中龙虎人丹多种有效成分HS-SPDE-GC-MS/MS检测方法,以克服现有技术所存在的上述缺点和不足。
本发明所需要解决的技术问题,可以通过以下技术方案来实现:
大鼠血浆中龙虎人丹多种有效成分的检测方法,其特征在于,包括以下步骤:
1.材料的准备
准备龙虎人丹、标准品和内标物;
2.方法:
2.1.溶液配制
各标准储备液的配制和内标溶液的配制;
2.2.血浆样品预处理
100μl血浆中加入10μl内标溶液后,涡旋1min,进行GC-MS/MS分析;
2.3.进行固相动态萃取SPDE
采用PDMS萃取头:SPDE萃取头涂层为聚二甲基硅氧烷PDMS内径50μm,长56μm;
2.4.进行GC-MS/MS
色谱:分析柱为VF-WAXms毛细管柱30m×0.25mm ID;Agiletnt Technologies,USA,涂层为100%聚乙二醇0.25μm膜厚度;
质谱:离子源为EI,碰撞气为氦气和氮气,流速分别为2.25及1.5ml·min-1,EI源温度为250℃,电离能量为70Ev,分析时间为14.8min;
2.5.方法学考察
2.5.1.专属性:取空白血浆,除不加内标外,其他按“血浆样品预处理”项下操作,得空白血浆色谱图;分别取6只不同来源的空白大鼠血浆100μl,将一定浓度的标准溶液加入空白血浆中,除不加内标外,其他按“血浆样品预处理”项下操作,进样10μl,得空白血浆加标准品色谱图;取大鼠灌胃给予龙虎人丹后的血浆样品,依同法操作,得给药后血浆色谱图;
2.5.2.标准曲线:以各标准样品血药浓度为横坐标,各标准样品与内标物的峰面积比值为纵坐标,用加权(w=1/x2)最小二乘法进行回归运算,求得的直线回归方程即为标准曲线
2.5.3.准确度和精密度:根据QC样品的各成分实测浓度计算本法的批内和批间精密度与准确度;
2.5.4.提取回收率:每一浓度两种处理方法的峰面积比值计算提取回收 率;
2.5.5.稳定性实验
测试血浆样品室温放置12h稳定性、血浆样品-80℃冻融3次稳定性、血浆样品-80℃冻存15天稳定性,上述样品均按各分析批的随行标准曲线计算出各QC样品的浓度,计算各浓度的平均值与标示浓度的比值,从而得出样品的稳定性;
2.5.6.稀释方法学:配制相当于高浓度QC样品5和10倍的样品,每个平行三样本,用空白血浆基质稀释5和10倍后,按“血浆样品预处理”项下操作,进行GC-MS/MS分析。
其中,所述龙虎人丹上海中华药业有限公司,产地:上海,批号:120503、120504;
所述标准品为樟脑批号:110747-2010008、薄荷脑批号:110728-200005、异龙脑批号:1512-200201、龙脑批号:110881-201107,购自中国药品生物制品检定所;
所述内标物为萘批号:11673-200803购自中国药品生物制品检定所。
其中,所述各标准储备液的配制:精密称取各标准品,樟脑、薄荷脑、异龙脑、龙脑,精确至0.1mg,置10ml量瓶中,用乙酸乙酯溶解并稀释至刻度,摇匀,作为各标准储备液,4℃冰箱内保存备用。
其中,所述内标溶液的配制:精密称取内标物,萘对照品2.46mg,置10ml量瓶中,用乙酸乙酯溶解并稀释至刻度,摇匀,作为储备溶液200μg/ml冰箱4℃内保存备用。将内标溶液用乙酸乙酯稀释至萘浓度为100ng/ml。
步骤(2.3)中,SPDE参数如下:烤箱预加热时间:5min,进样针温度:85℃,烤箱加热温度:80℃,加热搅拌器的转数:500rpm,取样注射针的深度:20mm,萃取次数:40,解析气体量:1000μl,注射针进样口插入深度:45mm,热脱附时间:30s,热脱附注射速度:50μl/s,萃取头老化时间:6min,萃取头老化温度:250℃。
步骤(2.4)中,色谱采用载气为氦气,流速为2.5ml·min-1,程序升温方法:初始温度为50℃维持1min,以12℃每分钟的升温速率升至150℃,以20℃每分钟的升温速率升至200℃,以45℃每分钟的升温速率升至245℃, 维持2min,进样口温度:250℃,不分流,溶剂延迟:6min;
步骤(2.5.3)中,4种成分批内和批间变异及准确度,批内及批间RSD在4.27%-9.53%之间,准确度在95.20%-106.20%。
步骤(2.5.4)中,测得各成分在各浓度血浆样品中的提取回收率为74.95%–88.55%。
步骤(2.5.5)中,稳定性实验的血浆样品在室温下保存12h内稳定,未经处理的血浆样品在-80℃冰箱内反复冻融3次稳定,未经处理的血浆样品在-80℃冰箱内保存15天内稳定。
步骤(2.5.6)中,将3.2μg/ml和1.6μg/ml的含樟脑、薄荷脑、异龙脑、龙脑的血浆样品分别稀释10倍和5倍,血浆样品经稀释后测定结果的RSD在±15%以内,说明血浆样品经5倍及10倍稀释再测定,不会影响样品测定的准确度和精密度。
本发明的有益效果:
本研究建立同时测定龙虎人丹中3种主要成分薄荷脑、异龙脑、龙脑及代谢物樟脑的血浆HS-SPDE-GC-MS/MS检测方法,为进行了龙虎人丹多种挥发性成分的药动学研究提供基础。
附图说明
图1为标准品和内标物的结构式。
结构式1为樟脑Camphor,结构式2为薄荷脑Menthol,结构式3为异龙脑Isoborneol,结构式4为龙脑(亦称为冰片)Borneol,结构式5为萘Naphthalene。
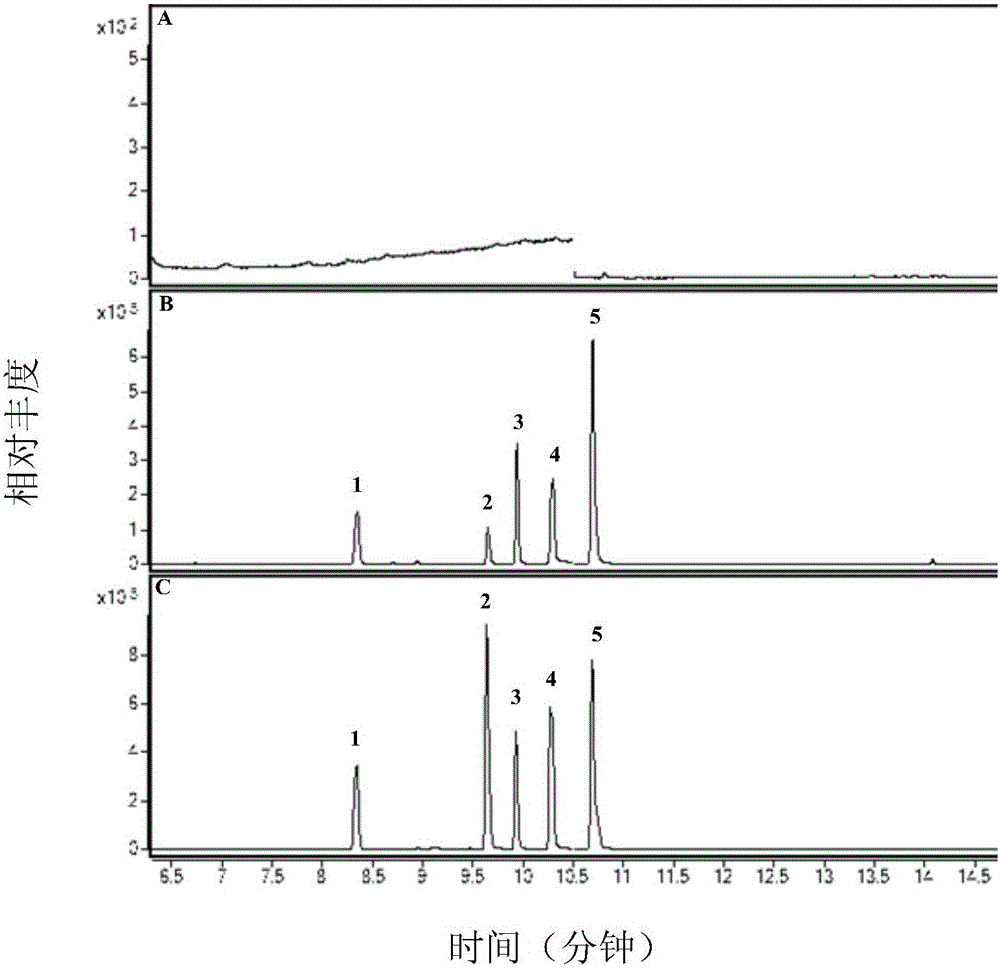
图2为大鼠口服龙虎人丹30分钟后的血浆样品中各成分的多反应监测色谱图。
(A)空白大鼠血浆、(B)空白血浆加标准品及(C)大鼠口服龙虎人丹30分钟后的血浆样品中各成分的多反应监测色谱图,五个峰分别为(1)樟脑、(2)薄荷脑、(3)异龙脑、(4)龙脑和(5)萘。
具体实施方式
以下结合具体实施例,对本发明作进步说明。应理解,以下实施例仅用于说明本发明而非用于限定本发明的范围。
实施例1
1.材料
1.1.仪器
Agilent 7890A气相–Agilent 7000B三重四级杆质谱(Agiletnt Technologies,USA),SPDE固相动态萃取多功能全自动进样器(Idstein,Germany),ScanSpeed 1730MR冷冻离心机(LaboGene,Danmark),JA 1203精密电子天平(上海精密科学仪器公司),XS105DU型电子天平(METTLER TOLEDO,USA),USC-502超声波清洗器(上海波龙电子设备有限公司),QT-1涡旋混合器(上海琪特分析仪器有限公司)。
1.2.药品及试剂
龙虎人丹(上海中华药业有限公司,产地:上海,批号:120503、120504)。
樟脑(批号:110747-2010008)、薄荷脑(批号:110728-200005)、异龙脑(批号:1512-200201)、龙脑(批号:110881-201107)、萘(批号:11673-200803)均购自中国药品生物制品检定所。以上标准品纯度均大于98%,色谱纯甲醇、乙腈购自Burdick&Jackson公司(Ulsan,Korea);乙酸乙酯,乙醇及正己烷为色谱纯,购于国药集团化学试剂有限公司;超纯水由Millipore Milli-Q纯水仪制备。
所有标准品和内标的结构式见图1。
2.方法
2.1.溶液配制
各标准储备液的配制:
精密称取各标准品,樟脑、薄荷脑、异龙脑、龙脑,精确至0.1mg,置10ml量瓶中,用乙酸乙酯溶解并稀释至刻度,摇匀,作为各标准储备液,4℃冰箱内保存备用。
内标溶液的配制:
精密称取内标物,萘对照品2.46mg,置10ml量瓶中,用乙酸乙酯溶解并稀释至刻度,摇匀,作为储备溶液(200μg/ml)冰箱(4℃)内保存备用。将内标溶液用乙酸乙酯稀释至萘浓度为100ng/ml。
以上储备液及系列标准溶液均用经过校正的容量器具配制。
2.2.血浆样品预处理
100μl血浆中加入10μl内标溶液后,涡旋1min,进行GC-MS/MS分析。
2.3.固相动态萃取(SPDE)条件
采用PDMS萃取头:SPDE萃取头涂层为聚二甲基硅氧烷(PDMS)(内径50μm,长56μm)。
SPDE参数如下:烤箱预加热时间:5min,进样针温度:85℃,烤箱加热温度:80℃,加热搅拌器的转数:500rpm,取样注射针的深度:20mm,萃取次数:40,解析气体量:1000μl,注射针进样口插入深度:45mm,热脱附时间:30s,热脱附注射速度:50μl/s,萃取头老化时间:6min,萃取头老化温度:250℃。
2.4.GC-MS/MS条件
色谱条件:分析柱为VF-WAXms毛细管柱(30m×0.25mm ID;Agiletnt Technologies,USA)涂层为100%聚乙二醇(0.25μm膜厚度)。载气为氦气,流速为2.5ml·min-1,程序升温方法:初始温度为50℃维持1min,以12℃每分钟的升温速率升至150℃,以20℃每分钟的升温速率升至200℃,以45℃每分钟的升温速率升至245℃,维持2min,进样口温度:250℃,不分流,溶剂延迟:6min。
质谱条件:离子源为EI,碰撞气为氦气和氮气,流速分别为2.25及1.5ml·min-1,EI源温度为250℃,电离能量为70Ev,分析时间为14.8min。
各成分及内标的质谱检测参数见表1。
表1目标分析物和内标物的GC–MS/MS仪器方法
2.5.方法学考察
2.5.1.专属性
取空白血浆,除不加内标外,其他按“血浆样品预处理”项下操作,得空白血浆色谱图;分别取6只不同来源的空白大鼠血浆100μl,将一定浓度的标准溶液加入空白血浆中,除不加内标外,其他按“血浆样品预处理”项下操作,进样10μl,得空白血浆加标准品色谱图;取大鼠灌胃给予龙虎人丹后的血浆样品,依同法操作,得给药后血浆色谱图,参见图2。
2.5.2.标准曲线
混合标准溶液用大鼠空白血浆稀释至30μg/ml,然后再依次稀释到400、320、80、20、4、1、0.5ng/ml,配制成浓度范围为0.5~400ng/ml的标准系列血浆样品,按“血浆样品预处理”项下的方法操作,每一浓度进行六样本分析,记录色谱图,以各标准样品血药浓度为横坐标,各标准样品与内标物的峰面积比值为纵坐标,用加权(w=1/x2)最小二乘法进行回归运算,求得的直线回归方程即为标准曲线。
2.5.3.准确度和精密度
取空白血浆100μl,按“标准曲线与定量下限”项下的方法制成低、中、高三个浓度(即②、④、⑥浓度)的质量控制(QC)样品,每一浓度进行五样本分析,连续测定3批,根据当日的标准曲线,计算QC样品中各成分的实测浓度。根据QC样品的各成分实测浓度计算本法的批内和批间精密度与准确度。
2.5.4.提取回收率
取空白血浆100μl,按“标准曲线”项下方法制备低、中、高三个浓度(即②、④、⑥浓度)的质量控制(QC)样品,每一浓度进行三样本分析,获得相应峰面积。同时,取水100μl,按“标准曲线”项下方法制备低、中、高三个浓度(即②、④、⑥浓度)的质量控制(QC)样品,每一浓度进行三样本分析,获得相应峰面积进样分析,获得相应峰面积。以每一浓度两种处理方法的峰面积比值计算提取回收率。
2.5.5.稳定性实验
血浆样品室温放置12h稳定性:按“标准曲线”项下方法制备低、中、高三个浓度(即②、④、⑥浓度)的质量控制(QC)样品,混匀后在室温放置12h,再按“血浆样品预处理”项处理样品(n=3),进行测定。
血浆样品-80℃冻融3次稳定性:按“标准曲线”项下方法制备低、中、高三个浓度(即②、④、⑥浓度)的质量控制(QC)样品,放置-80℃冰箱反复冻融3次,第3次融化后,按再按“血浆样品预处理”项处理样品(n=3),进行测定。
血浆样品-80℃冻存15天稳定性:按“标准曲线”项下方法制备低、中、高三个浓度(即②、④、⑥浓度)的质量控制(QC)样品,放置-80℃冰箱冻存15天,再按“血浆样品预处理”项处理样品(n=3),进行测定。
上述样品均按各分析批的随行标准曲线计算出各QC样品的浓度,计算各浓度的平均值与标示浓度的比值,从而得出样品的稳定性。
2.5.6.稀释方法学
对于超出定量上限的血浆样品,需用空白血浆基质按一定比例稀释到标准曲线的线性范围后测定。为了考察稀释过程是否影响血浆样品测定的准确度和精密度,按下列步骤进行了稀释方法确证:配制相当于高浓度QC样品5和10倍的样品,每个平行三样本,用空白血浆基质稀释5和10倍后,按“血浆样品预处理”项下操作,进行GC-MS/MS分析。根据测定结果,计算稀释样品的准确度和精密度。
3.结果
3.1.方法学考察
3.1.1专属性
专属性结果见图2,结果表明:空白血浆中的内源性物质不干扰樟脑、薄荷脑、异龙脑、龙脑以及内标物萘的测定。
图2(A)空白大鼠血浆、(B)空白血浆加标准品及(C)大鼠口服龙虎人丹30分钟后的血浆样品中各成分的多反应监测色谱图(1)樟脑、(2)薄荷脑、(3)异龙脑、(4)龙脑和(5)萘。
3.1.2.标准曲线和定量下限
标准曲线回归方程结果、线性范围和最低定量限见表2。
表2樟脑、薄荷脑、异龙脑和龙脑在大鼠血浆中的标准曲线、线性范围和最低定量下限
3.1.3.准确度和精密度
4种成分批内和批间变异及准确度结果见表3,批内及批间RSD在4.27%-9.53%之间,准确度在95.20%-106.20%,均符合要求。
表3 4种分析物的精密度和准确度
3.1.4.提取回收率及稳定性实验
回收率见表4,测得各成分在各浓度血浆样品中的提取回收率为74.95%–88.55%。
稳定性实验的具体数据见表4,结果表明:血浆样品在室温下保存12h内稳定,未经处理的血浆样品在-80℃冰箱内反复冻融3次稳定,未经处理的血浆样品在-80℃冰箱内保存15天内稳定。
表4樟脑、薄荷脑、异龙脑和龙脑在大鼠血浆中的稳定性和回收率
(n=3)
3.1.7.稀释方法学考察
将3.2μg/ml和1.6μg/ml的含樟脑、薄荷脑、异龙脑、龙脑的血浆样品分别稀释10倍和5倍,测定结果见表5。
表5质控样品稀释倍数的实验数据(n=3)
结果表明,血浆样品经稀释后测定结果的RSD在±15%以内,说明血浆样品经5倍及10倍稀释再测定,不会影响样品测定的准确度和精密度。
以上方法学考察结果说明建立的方法符合按照生物样品分析的规范要求。
以上对本发明的具体实施方式进行了说明,但本发明并不以此为限,只要不脱离本发明的宗旨,本发明还可以有各种变化。
- 还没有人留言评论。精彩留言会获得点赞!