测定纳米级及微米级铁粉中零价铁含量的装置及其用法的制作方法
本发明属于水处理领域,尤其是用铁粉作为修复剂的水处理技术,具体地涉及一种测定纳米级及微米级铁粉中零价铁含量的装置及其用法。
背景技术:
随着化学工业的迅猛发展,抗生素、藻毒素、染料等污染物排入环境中,多数物质及其代谢产物都具有致癌、致畸和致突变的危害,已对环境和人类健康构成极大的威胁,成为人们重点关注的问题之一。近年来,铁粉作为水环境修复新型环保材料的研究得到了人们的关注。尤其是纳米零价铁,由于其颗粒小、比表面积大,反应活性高,能有效去除水或土壤中的重金属、氯代烃等污染物,已经成为环境科学研究的前沿热点之一。另外,零价铁粉在航空、机械制造等领域也有着广泛用途。
合成纳米铁(NZVI)的传统方法主要是化学法,化学合成法对于发展NZVI用于环境修复起着积极作用,然而化学法常使用一些有毒的化学物质如还原剂(硼氢化钠)、有机溶剂和不可生物降解的分散剂、稳定剂,存在成本高和二次污染等问题。在被污染环境的修复中,开发环境友好、成本低廉的铁粉合成技术是其在环境修复中面临的关键问题。目前,绿色合成技术备受关注,目前有许多科学家利用绿茶、高粱麸皮、桉树叶等合成纳米级铁粉,这是由于这些物质中的有机酸和多酚可将Fe2+还原为纳米级的Fe单质,这些成分还可以作为铁粉的分散剂和掩蔽剂阻止其团聚和氧化,保障了其高的反应活性。与传统的化学合成方法相比,绿色合成过程避免使用有毒化学物质、降低能量消耗,具有经济性和环境友好等特点。
由于无论何种方法制作的铁粉,如果保存不善,均会在空气中迅速氧化而失去利用价值。因此,快速测定铁粉中零价铁的含量就成为一项十分重要的工作;对于铁粉中零价铁含量的测定,有必要寻找一种简便可行、测量结果准确可靠的方法,为铁粉在各种领域的应用提供保障。
通常用的化学检测方法如原子吸收光谱、离子色谱等(分析Fe2+或Fe3+的量,由铁粉表面氧化层中氧化态Fe和核心部分的Fe0共同贡献)都难以分析出铁粉在一定老化时间或反应时间后有效零价铁含量。
现有零价铁定量分析方法有铜离子氧化及氢气还原法。铜离子氧化法是根据Cu2+的消耗量测量铁粉中零价铁的含量,Cu2+与Fe0的反应产物包括Cu与Cu2O,但在计算时Cu2O的含量常被忽略,这种方法所测零价铁含量往往偏高。
氢气还原法是利用H2与铁粉中铁氧化物发生还原反应,从而测定反应产物H2O的生成量,计算氧化铁的含量,进而利用差减法推定零价铁的含量。而铁粉中氧化物的形态有多种,且各形态之间没有固定比例关系,根据测定氧含量不可能准确地计算零价铁的含量,故此氢气还原法测定结果的准确性也较差。
专利(申请号为201410243365.7)用Fe3+溶液中投加铁粉,反应一定时间后,向溶液中加入螯合剂或络合剂,最后计算Fe3+测试溶液中溶解态铁元素的增量。该方法中螯合剂或络合剂为乙二胺四乙酸盐、磺基水杨酸盐或硫氰酸盐中的一种以上,整个反应过程中,溶解氧浓度控制在小于1mg/L,整个测试过程需要2-24h。该方法步骤复杂,操作繁琐,造成了试剂的大量浪费,需要在限氧条件下测试,测试条件苛刻,反应时间长,造成测试结果误差大。
专利(申请号为201510176411.0)通过分析偶氮染料溶液与纳米零价铁颗粒反应前、后的光谱特性变化以确定纳米零价铁颗粒中Fe0的含量。该方法包括七个步骤,所用试剂多,同样存在步骤繁琐,操作复杂,试剂浪费的缺点。
现有文献也报道了通过向纳米零价铁溶液中滴加酸液充分反应并收集生成的H2,最后测量其体积的方法来检测有效Fe0的含量,但此方法存在如氢气不好收集等很多操作性难题,很容易产生较大的检测误差。
技术实现要素:
本发明为解决现有技术问题,提供了一种制作成本低、操作简单、可以随时随地准确测定纳米级及微米级铁粉中零价铁含量的装置及其使用方法。
本发明采用的技术方案为:测定纳米级及微米级铁粉中零价铁含量的装置,主要包括U型管和倒Y型管;所述U型管的左侧管带有刻度线,所述U型管的右侧管口借助橡胶管和标准塞与倒Y型管的进样口相连,所述U型管内装有水平面在0刻度线及以上的液体。
进一步地,所述U型管的右侧管设有倒U型支管,所述倒U型支管的末端为第一宝塔嘴,所述标准塞设有第二宝塔嘴;所述倒Y型管的进样口与标准塞的塞口端相连,所述橡胶管分别与第一宝塔嘴和第二宝塔嘴相连。
进一步地,所述第一宝塔嘴与第二宝塔嘴之间的距离小于0.5cm。
进一步地,所述倒Y型管的进样口为磨口,型号为19/26口。
进一步地,所述U型管、倒Y型管和标准塞的材质均为高硼硅玻璃、厚度均为2mm。
进一步地,所述U型管内的液体为水。
进一步地,所述U型管的内径为1cm~3cm、高度为20~30cm,倒U型支管的第一宝塔嘴和标准塞的第二宝塔嘴的直径均小于1cm。
如权利要求1所述测定纳米级及微米级铁粉中零价铁含量装置的使用方法,包括以下步骤:
a、将U型管垂直固定,并将U型管的第一宝塔嘴端用橡胶管与标准塞的第二宝塔嘴紧密连接;往U型管中加入水,使其U型管的左侧管的水平面位于0 ml及以上位置;
b、称取质量为M g的铁粉,将其和过量的稀盐酸分别加入倒Y型管的两支管内,用标准塞将倒Y型管封好,记录此时U型管左侧水平面的刻度为V初ml;
c、用电子气压计记录此时的大气压P1 kpa,气温T ℃;
d、将倒Y型管缓缓倾斜,使其支管内的稀盐酸慢慢流入装有铁粉的支管内,待其与铁粉反应完全后记录此时U型管左侧水平面的刻度为V末 ml;
e、如下面公式,即可获得铁粉中零价铁的含量Y:
。
进一步地,所述稀盐酸由37%的浓盐酸与水按体积比1:1~1:4配制而成。
本发明的实验原理为:本发明装置通过倒Y型管两支管内的铁粉和稀盐酸反应产生氢气,由于装置密封,从而产生的氢气推动U型管右侧管水液面下降,左侧管水液面上升,液面变化的体积即为产生氢气的体积V1,记录当时的大气压P1和气温T1。
根据以下公式计算产生的氢气摩尔数,
其中:n为氢气摩尔数;P1为测量的大气压;V1为获得的氢气体积;TN为273.15K,PN为标准大气压(101325帕);VN为22.4升;T1为测量的温度(摄氏度+273.15K)。
根据铁与稀盐酸的反应方程式Fe+2HCl=FeCl2+H2↑得知Fe的摩尔数与H2的摩尔数n相等,从而得知Fe的质量,根据加入倒Y型管内的铁粉的总质量进而计算得出零价铁的含量。
本发明获得的有益效果为:a、本发明装置测试精度较高,误差范围在5%以内;b、本装置方便携带,不受温度、含氧量等外界因素的影响,可以在野外场地进行使用;c、本装置使用的过程中所使用的药剂简单,只需要浓盐酸和水即可完成测试,环境污染很小;d、本装置采用成本低廉的玻璃管烧制,并使用乳胶管相连接,具有成本低、制作材料和工艺环保无污染的特点;e、本方法操作简单,使用方便,很容易掌握。
附图说明
图1是本发明的结构示意图。
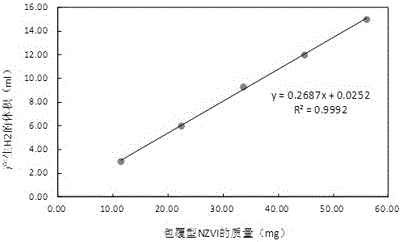
图2是包覆型NZVI的质量与产生H2的体积的关系曲线图。
其中,1代表U型管、2代表倒Y型管、3代表橡胶管、4代表标准塞、5代表第一宝塔嘴、6代表第二宝塔嘴、7代表倒U型支管。
具体实施方式
为了使本发明的技术方案及优点更加清楚明白,下面结合附图和具体实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅用以解释本发明,并不用于限定本发明。
实施例1
a.购买包覆型的NZVI,备用。用50ml量筒量取50ml去离子水倒入100ml烧杯中,再量取50ml浓盐酸倒入去离子水中,用玻璃棒搅拌均匀,配置浓盐酸与水的体积比为1:1的稀盐酸,备用;
b.将U型管1用铁架台垂直固定,在U型管1内注入自来水使其液面与0刻度线齐平,用橡胶管3将第一宝塔嘴5和第二标宝塔嘴6连接;
c.称取购买的包覆型NZVI 11.38mg,用钥匙将称取的NZVI加入倒Y型管2的一个支管内,用滴管吸取过量的稀盐酸加入倒Y型管2的另一个支管内,将标准塞4盖在倒Y型管2的进样口上,记录此时的液面位置为0.6ml;
d.轻轻地将倒Y型管2倾斜使其支管内的稀盐酸缓慢流入NZVI的支管内与包覆型NZVI反应,待反应完全后记录此时的液面位置为3.6ml,于反应前比液面上升了3.0ml,即产生的氢气体积为3.0ml;
e.用电子气压计测量此时的大气压为99.06Kpa,气温为27.9℃;
f.根据公式计算氢气的摩尔数为0.12mM,根据反应方程式Fe+2HCl=FeCl2+H2↑推算纯纳米铁的摩尔数为0.12mM,即为6.72mg,由此计算所测包覆型NZVI中零价铁含量为6.72/11.38*100%=59.05%。
实施例2
a.购买包覆型的NZVI,备用;用50ml量筒量取50ml去离子水倒入100ml烧杯中,再量取50ml浓盐酸倒入去离子水中,用玻璃棒搅拌均匀,配置浓盐酸与水的体积比为1:1的稀盐酸,备用;
b.将U型管1用铁架台垂直固定,在U型管1内注入自来水使其液面与0刻度线齐平,用橡胶管3将第一宝塔嘴5和第二宝塔嘴6连接。
c.称取购买的包覆型NZVI 22.36mg,用钥匙将称取的NZVI加入倒Y型管的一个支管内,用滴管吸取过量的稀盐酸加入倒Y型管2的另一支管内,将标准塞4盖在倒Y型管2的进样口上,记录此时的U型管1内液面位置为0.6ml;
d.轻轻地将倒Y型管2倾斜使其支管内的稀盐酸缓慢流入另一支管内与包覆型NZVI反应,待反应完全后记录此时的液面位置为6.6ml,于反应前比液面上升了6ml,即产生的氢气体积为6ml;
e.用电子气压计测量此时的大气压为99.05Kpa,气温为26.9℃;
f.根据公式计算氢气的摩尔数为0.24mM,根据反应方程式Fe+2HCl=FeCl2+H2↑推算纯纳米铁的摩尔数为0.24mM,即为13.44mg,由此计算所测包覆型NZVI中零价铁含量为13.44/22.36*100%=60.11%。
实施例3
a. 购买包覆型的NZVI,备用。用50ml量筒量取50ml去离子水倒入100ml烧杯中,再量取50ml浓盐酸倒入去离子水中,用玻璃棒搅拌均匀,配置浓盐酸与水的体积比为1:2的稀盐酸,备用;
b.将U型管1用铁架台垂直固定,在U型管1内注入自来水使其液面与0刻度线齐平,用橡胶管3将第一宝塔嘴5和第二宝塔嘴6连接;
c.称取购买的包覆型NZVI 33.63mg,用钥匙将称取的NZVI加入倒Y型管2的一个支管内,用滴管吸取过量的稀盐酸加入倒Y型管2的另一个支管内,将标准塞盖在倒Y型管2进样口上,记录此时的液面位置为0.6ml;
d.轻轻地将倒Y型管2倾斜使其支管内的稀盐酸缓慢流入另一支管内与包覆型NZVI反应,待反应完全后记录此时的液面位置为9.9ml,于反应前比液面上升了9.3ml,即产生的氢气体积为9.3ml;
e.用电子气压计测量此时的大气压为99.01Kpa,气温为26.8℃;
f.根据公式计算氢气的摩尔数为0.37mM,根据反应方程式Fe+2HCl=FeCl2+H2↑推算纯纳米铁的摩尔数为0.37mM,即为20.72mg,由此计算所测包覆型NZVI中零价铁含量为20.72/33.63*100%=61.61%。
实施例4
a. 购买包覆型的NZVI,备用。用50ml量筒量取50ml去离子水倒入100ml烧杯中,再量取50ml浓盐酸倒入去离子水中,用玻璃棒搅拌均匀,配置浓盐酸与水的体积比为1:2的稀盐酸,备用;
b.将U型管1用铁架台垂直固定,在U型管1内注入自来水使其液面与0刻度线齐平,用橡胶管3将第一宝塔嘴5和第二宝塔嘴6连接;
c.称取购买的包覆型NZVI 44.72mg,用钥匙将称取的NZVI加入倒Y型管2一个支管内,用滴管吸取过量的稀盐酸加入倒Y型管2的另一个支管内,将标准塞4盖在倒Y型管2进样口上,记录此时的液面位置为0.6ml;
d.轻轻地将倒Y型管2倾斜使其支管内的稀盐酸缓慢流入另一支管内与包覆型NZVI反应,待反应完全后记录此时的液面位置为12.6ml,于反应前比液面上升了12ml,即产生的氢气体积为12ml;
e.用电子气压计测量此时的大气压为99.04Kpa,气温为26.7℃;
f.根据公式计算得氢气的摩尔数为0.48mM,根据反应方程式Fe+2HCl=FeCl2+H2↑推算纯纳米铁的摩尔数为0.48mM,即为26.88mg,由此计算所测包覆型NZVI的纳米铁中零价铁含量为26.88/44.72*100%=60.11%。
实施例5
a.购买包覆型的NZVI,备用。用50ml量筒量取50ml去离子水倒入100ml烧杯中,再量取50ml浓盐酸倒入去离子水中,用玻璃棒搅拌均匀,配置浓盐酸与水的体积比为1:4的稀盐酸,备用;
b.将U型管1用铁架台垂直固定,在U型管1内注入自来水使其液面与0刻度线齐平,用橡胶管3将第一宝塔嘴5和第二宝塔嘴6连接;
c.称取购买的包覆型NZVI 56.02mg,用钥匙将称取的NZVI加入倒Y型管的一个支管内,用滴管吸取过量的稀盐酸加入倒Y型管2的另一个支管内,将标准塞4盖在倒Y型管2的进样口上,记录此时的U型管1液面位置为0.6ml;
d.轻轻地将倒Y型管2倾斜使其支管内的稀盐酸缓慢流入另一支管内与包覆型NZVI反应,待反应完全后记录此时的液面位置为15.6ml,于反应前比液面上升了15ml,即产生的氢气体积为15ml;
e.用电子气压计测量此时的大气压为99.02Kpa,气温为26.7℃;
f.根据公式计算得氢气的摩尔数为0.6mM,根据反应方程式Fe+2HCl=FeCl2+H2↑推算纯纳米铁的摩尔数为0.6mM,即为33.6mg,由此计算所测包覆型NZVI中零价铁含量为33.6/56.02*100%=59.98%。
根据以上五个实施案例,以加入的包覆型NZVI的质量为X轴,产生H2的体积为Y轴作关系曲线,如图2所示,由图2中可见两者的线性相关性非常好,R2=0.9992。
以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,根据本发明的技术方案及其发明构思加以等同替换或改变,都应涵盖在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!