一种测定氨基酸类注射液色氨酸有关物质的测定方法与流程
本发明提供一种测定氨基酸类注射液色氨酸有关物质的测定方法,涉及医药
技术领域:
。
背景技术:
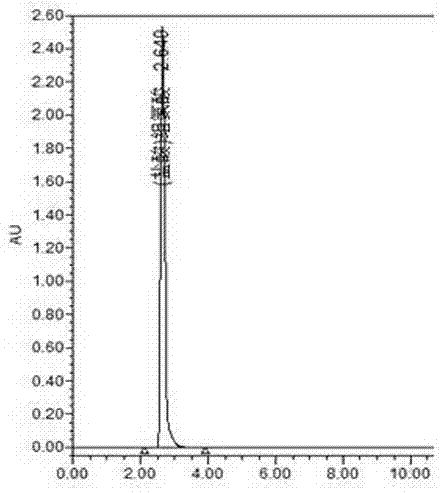
:氨基酸输液品种繁多,各品种所含氨基酸、电解质等种类、数量各不相同,用途亦各异,为临床上应用广泛的营养治疗输液产品。色氨酸是必需氨基酸之一,可转化生成人体大脑中的一种重要神经传递物质即5-羟色胺,是氨基酸注射液中的主要成分之一,由于色氨酸对光、热、氧气等敏感,在氨基酸类注射液的制备过程中,若未合理控制氧气控制过程、灭菌过程等环节,色氨酸易降解产生有关物质,色氨酸降解率即色氨酸有关物质在氨基酸类注射液中所占的比例,可反映出氨基酸类注射液产品的质量。ep、usp药典中均有色氨酸原料药中有关物质的介绍,但是在氨基酸类注射液中未见色氨酸有关物质的文献报道。技术实现要素:本发明解决现有技术中缺乏氨基酸类注射液中色氨酸有关物质的测定方法的技术问题,提供了一种高效、准确高,成本低的测定氨基酸类注射液色氨酸有关物质的测定方法,所述方法如下:采用高效液相色谱法,用十八烷基硅烷键合硅胶为固定相的色谱柱,按以下流动相条件进行梯度洗脱;包括三种流动相,流动相a为0.01mol/l磷酸二氢钠,用氢氧化钠溶液调节ph=7.0~7.4;流动相b为乙腈、甲醇、水按照体积比45:45:10混合所得;流动相c为甲醇、水按照10:90的体积比混合所得;流动相的梯度设置如下:时间(min)流动相a(%)流动相b(%)流动相c(%)流速(ml/min)0100001.230455501.235010001.235.5001001.236001001.540001001.542.5100001.545100001.248100001.2作为进一步优选,所述柱温为40℃,检测波长为220nm。作为进一步优选,所述流动相a的ph是7.2。本发明通过借鉴ep、bp、usp药典中色氨酸原料药中有关物质的检测方法,建立了一种氨基酸类注射液中色氨酸有关物质的分析测定方法。分析过程中以乙酰色氨酸作为自身对照,以色氨酸相对保留时间的方式进行分析计算,规定杂质峰面积之和不得大于乙酰色氨酸对照品峰面积的5倍(1.0%)。通过方法学验证其结果良好,可以有效测定氨基酸类注射液(复方氨基酸注射液(18aa)、复方氨基酸注射液(18aa-ii)、复合氨基酸注射液(17aa)、复方氨基酸(15)双肽(2)注射液等)中色氨酸有关物质,监控其制备工艺中氧气控制过程、灭菌过程等,反映成品质量的优劣。附图说明图1甲硫氨酸色谱图;图2(盐酸)组氨酸色谱图;图3门冬氨酸色谱图;图4丙氨酸色谱图;图5缬氨酸色谱图;图6(盐酸)赖氨酸色谱图;图7亮氨酸色谱图;图8苏氨酸色谱图;图9酪氨酸色谱图;图10(盐酸)精氨酸色谱图;图11异亮氨酸色谱图;图12脯氨酸色谱图;图13苯丙氨酸色谱图;图14甘氨酸色谱图;图15丝氨酸色谱图;图16谷氨酸色谱图;图17色氨酸色谱图;图18复方氨基酸注射液(18aa)色氨酸有关物质色谱图;图19复方氨基酸注射液(18aa-2)色氨酸有关物质色谱图;图20复方氨基酸(15)双肽(2)注射液色氨酸有关物质色谱图;具体实施例以下通过实施例形式,对本发明涉及测定氨基酸类注射液色氨酸有关物质检测方法作进一步的详细说明,但不应将此理解为本发明上述主题的范围仅限于以下的实例,凡基于本发明上述内容所实现的技术均属于本发明的范围。实施例1取本品直接进样;另精密称取色氨酸对照品适量,用水制成每1ml中约含0.9mg的溶液。照高效液相色谱法测定,用十八烷基硅烷键合硅胶为填充剂,作为固定相的色谱柱,选用乙酰色氨酸作为自身对照来检测色氨酸有关物质,流动相包括三种,流动相a是0.01mol/l磷酸二氢钠,并用氢氧化钠溶液调节ph=7.2,流动相b为乙腈、甲醇、水按照45:45:10的体积比混合所得,流动相c为甲醇、水按照10:90的体积比混合所得,柱温40℃,检测波长为220nm;按下表进行梯度洗脱。时间(min)流动相a(%)流动相b(%)流动相c(%)流速(ml/min)0100001.230455501.235010001.235.5001001.236001001.540001001.542.5100001.545100001.248100001.2精密量取上述供试品溶液和色氨酸对照品溶液各20μl,注入液相色谱仪,记录色谱图;另称取乙酰色氨酸对照品适量,加水溶解并稀释至制成每1ml约含2.0μg的溶液作为对照溶液,同法测定。色谱图中色氨酸相对保留时间0.54倍之前的峰不计;该时间后,除去色氨酸相对保留时间0.78倍的峰及色氨酸峰外,30min前如有杂质峰,其峰面积之和不得大于乙酰色氨酸对照品峰面积的5倍(1.0%)。供试品溶液中任何小于乙酰色氨酸对照溶液主峰面积0.1倍的峰可忽略不计。实施例中色氨酸有关物质即杂质,在氨基酸类注射液中所占比例的计算公式为:ru:供试品溶液中色氨酸杂质总面积;rs:乙酰色氨酸峰面积;cs:乙酰色氨酸浓度(mg/ml);cu:色氨酸的处方浓度。下面对氨基酸类注射液色氨酸有关物质的测定方法的以下项目进行了验证:1.色氨酸相对保留时间的确认配制处方量的18种氨基酸溶液,按照实施例中所述的液相条件进样,色谱图见附图1-17,统计内容见表1与表2。表118种氨基酸保留时间项目保留时间胱氨酸未出峰(盐酸)赖氨酸2.108门冬氨酸2.115谷氨酸2.141丝氨酸2.193甘氨酸2.182丙氨酸2.236苏氨酸2.300(盐酸)精氨酸2.329(盐酸)组氨酸2.649脯氨酸2.682缬氨酸3.252甲硫氨酸4.322异亮氨酸5.582酪氨酸5.655亮氨酸5.833苯丙氨酸8.851色氨酸11.328表2色氨酸与甲硫氨酸等的相对保留时间表对比项目色氨酸相对保留时间异亮氨酸0.493酪氨酸0.499亮氨酸0.515苯丙氨酸0.781从表1和表2的内容可以看出,在色谱图中色氨酸相对保留时间0.54倍之前的峰、色氨酸相对保留时间0.78倍的峰(苯丙氨酸)均为阴性样品峰,不含有色氨酸有关物质。从色氨酸相对保留时间0.54倍之后的峰,去除色氨酸相对保留时间0.78倍的峰及色氨酸峰,为色氨酸有关物质,可以计算出色氨酸有关物质即杂质的总面积,从而套用公式得到色氨酸杂质%,从而反映出供试品质量的优劣。2.自身对照物的选用usp、bp、ep里面色氨酸原料药有关物质的检测方法,均使用均用乙酰色氨酸作为自身对照来检测色氨酸有关物质。在实施例1的液相条件下,2μg/ml的色氨酸峰面积为307469,2μg/ml的乙酰色氨酸峰面积为241138;从以上试验数据来看,可以选用乙酰色氨酸作为本实施例的自身对照更为严格。3.方法学研究(1)色谱条件与系统适用性试验系统适用性溶液制备:取乙酰色氨酸对照品适量,制成每1ml约含2.0μg乙酰色氨酸的溶液作为系统适用性溶液。操作方法:取上述系统适用性溶液,进样20μl进行检测,重复六次,记录色谱图。计算乙酰色氨酸峰峰面积的rsd为0.5%;主峰保留时间的rsd为0.01%。(2)专属性(干扰试验)照有关物质项下的检测方法,分别取水溶液、流动相溶液、乙酰色氨酸对照品溶液、色氨酸对照品溶液、阴性溶液(按照处方配制不含色氨酸)及制剂样品各20μl,注入液相色谱仪,记录色谱图。结果证明水溶液、流动相溶液对杂质研究均无干扰,而阴性溶液有干扰,需扣除空白。(3)检测限乙酰色氨酸对照溶液稀释至不同浓度进行测定,以信噪比3:1为标准,此时乙酰色氨酸浓度为0.51μg/ml。(4)定量限乙酰色氨酸对照溶液稀释至不同浓度进行测定,以信噪比10:1为标准,此时乙酰色氨酸浓度为1.82μg/ml。配制6份最低定量限浓度的供试液各进1针,乙酰色氨酸峰保留时间的rsd应为0.01%,峰面积的rsd为0.5%。(5)准确度试验分别精密称取乙酰色氨酸对照品10mg、10mg、10mg;20mg、20mg、20mg;30mg、30mg、30mg;置9个100ml量瓶,加阴性溶液(按照处方配制不含色氨酸)溶解,定容、摇匀。再分别精密量取1.00ml置于9个100ml量瓶中,加阴性溶液(按照处方配制不含色氨酸)溶解,定容、摇匀,作为准确度待测溶液。照有关物质项下的检测方法,依法测定,记录色谱图,计算回收率和回收率的相对标准偏差,各浓度下的平均回收率均应在80%-120%之间。结果见表3:表3乙酰色氨酸准确度试验结果结果表明:乙酰色氨酸含量测定方法的平均回收率为108.1%,rsd为3.8%,在标示量的50%~150%范围内准确度良好。(6)精密度试验—重复性试验、中间精密度试验重复性试验:取b1401001批复方氨基酸注射液(18aa),照有关物质项下的检测方法,取原液装入6个液相瓶中进样,记录色谱图,计算相对标准偏差,应为rsd≦15%。同法取原液装入6个液相瓶中进样,由不同人员在不同仪器上依法测定,记录色谱图,计算测定含量相对标准偏差。本次实验结果与重复性实验结果相比较,所得12个数据的rsd应≦20%。结果记录如下表4所示:表4色氨酸有关物质精密度试验结果由表4可知:重复性试验中,6个样品色氨酸有关物质测定的rsd为12%,表明本含量测定方法的重复性良好。中间精密度试验中,12个样品色氨酸有关物质测定的rsd为12%,表明本含量测定方法的中间精密度良好。(7)耐用性①不同柱温的比较取b1401001批复方氨基酸注射液(18aa),照有关物质项下的检测方法,其他色谱条件不变,分别设定柱温36℃、39℃和42℃时进样,记录色谱图。试验结果见表5:表5不同柱温对色氨酸有关物质影响的试验结果结果表明:复方氨基酸注射液(18aa)在该条件的不同检测温度下,色氨酸有关物质的绝对值在±0.1%以内,稳定性结果良好。②不同流动相ph的比较取b1401001批复方氨基酸注射液(18aa)样品,其他色谱条件不变,设定流动相a的ph分别为7.0,7.2,7.4时进样,记录色谱图。试验结果见表6:表6不同流动相ph对色氨酸有关物质影响的试验结果结果表明:复方氨基酸注射液(18aa)在该条件的不同流动相ph下,色氨酸有关物质的绝对值在±0.1%以内,稳定性结果良好。③不同检测波长的比较取b1401001批复方氨基酸注射液(18aa)样品,其他色谱条件不变,设定检测波长分别为215nm、220nm、225nm时进样,记录色谱图。稳定性试验结果见表7:表7不同检测波长对色氨酸有关物质影响的试验结果结果表明:复方氨基酸注射液(18aa)在该条件的不同检测波长下,色氨酸有关物质的绝对值在±0.1%以内,稳定性结果良好。④不同流速的比较取b1401001批复方氨基酸注射液(18aa)样品,其他色谱条件不变,分别设定流速1.0ml/min、1.2ml/min和1.4ml/min时进样,记录色谱图。试验结果见表8:表8考察不同流速对色氨酸有关物质影响的试验结果结果表明:复方氨基酸注射液(18aa)在该条件的不同流速下,色氨酸有关物质的绝对值在±0.1%以内,稳定性结果良好。(8)溶液稳定性试验取b1401001批复方氨基酸注射液(18aa),照有关物质项下的检测方法,分别于0、2、4、6、8小时各测定一次,计算其杂质峰面积的相对标准偏差,结果见下表9。表9复方氨基酸注射液(18aa)色氨酸有关物质稳定性考察试验结果结果表明:复方氨基酸注射液(18aa)中色氨酸有关物质在8h内测定,色氨酸有关物质的绝对值在±0.1%以内,溶液稳定性结果良好。(9)方法学验证结果如下表10所示。表10方法学验证结果汇总表4、样品测定(1)照色氨酸有关物质测定法,测定复方氨基酸注射液(18aa)参比制剂和试生产连续3批复方氨基酸注射液(18aa)样品中色氨酸有关物质的含量,结果见表11。表11复方氨基酸注射液(18aa)色氨酸有关物质含量测定结果结果表明:参比制剂和3批样品的色氨酸有关物质峰面积均不大于乙酰色氨酸对照品峰面积的5倍(1.0%),结果良好。(2)照色氨酸有关物质测定法,分别测定稳定性24个月的复方氨基酸注射液(18aa)、复方氨基酸注射液(18aa-ii)及复方氨基酸(15)双肽(2)注射液,结果见下表12,其中复方氨基酸注射液(18aa)、复方氨基酸注射液(18aa-ii)及复方氨基酸(15)双肽(2)注射液的色谱图分别参阅图18、图19、图20。表12不同氨基酸类注射液色氨酸有关物质测定结果结果表明:复方氨基酸注射液(18aa)、复方氨基酸注射液(18aa-ii)、15%复合氨基酸注射液(17aa)、复方氨基酸(15)双肽(2)注射液的色氨酸有关物质峰面积均不大于乙酰色氨酸对照品峰面积的5倍(1.0%),结果良好。本发明的方法已通过较佳实施例进行了描述,相关人员明显能在本
发明内容、精神和范围内对本文所述的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1