BioFET器件及其制造方法和传感器阵列与流程
本发明的实施例涉及biofet器件及其制造方法和传感器阵列。
背景技术:
生物传感器是用于感测和检测生物分子的器件,并且在电子、电化学、光学和机械检测原理的基础上操作。包括晶体管的生物传感器是电感测生物实体或生物分子的电荷、光子或机械性能的传感器。可以通过检测生物实体或生物分子自身或通过特定反应物和生物实体/生物分子之间的相互作用和反应来实施检测。这种生物感测器可以使用半导体工艺来制造,可以迅速地转换电信号,以及可以容易地应用于集成电路(ic)和微电子机械系统(mems)。
技术实现要素:
本发明的实施例提供了一种生物场效应晶体管(biofet)器件,包括:半导体衬底,具有第一表面和与所述第一表面相对、平行的第二表面;多个生物场效应晶体管传感器,设置在所述半导体衬底上,每个生物场效应晶体管传感器均包括:栅极,形成在所述半导体衬底的第一表面上;和沟道区域,形成在所述栅极下面的所述半导体衬底内和所述半导体衬底中的源极/漏极(s/d)区域之间,其中,所述沟道区域包括所述半导体衬底的第二表面的部分;隔离层,设置在所述半导体衬底的第二表面上,所述隔离层具有位于所述多个生物场效应晶体管传感器的多于一个生物场效应晶体管传感器的所述沟道区域上方的开口;以及界面层,设置在所述开口中的所述多于一个生物场效应晶体管传感器的所述沟道区域上。
本发明的实施例还提供了一种制造生物场效应晶体管器件的方法,所述方法包括:在半导体衬底的第一表面上形成多个栅极,所述多个栅极的每个均形成在所述半导体衬底中的相应的沟道区域上方;在每个所述沟道区域的两侧上的所述半导体衬底中形成源极/漏极(s/d)区域;在所述半导体衬底的第二表面上的隔离层中形成开口,所述第二表面与所述半导体衬底的第一表面相对和平行,其中,所述沟道区域的每个均包括所述半导体衬底的第二表面的部分,并且其中,所述开口暴露包括多于一个沟道区域的所述半导体衬底的第二表面的部分;以及在所述开口内的所述半导体衬底的第二表面上设置界面层。
本发明的又一实施例提供了一种传感器阵列,包括:半导体衬底,具有第一表面和与所述第一表面相对、平行的第二表面;多个生物场效应晶体管传感器,在所述半导体衬底上以行和列的矩阵布置,每个生物场效应晶体管传感器均包括:栅极,形成在所述半导体衬底的第一表面上;和沟道区域,形成在所述栅极下面的所述半导体衬底内和所述半导体衬底中的源极/漏极(s/d)区域之间,其中,所述沟道区域包括半导体衬底的所述第二表面的部分;隔离层,设置在所述半导体衬底的第二表面上,所述隔离层具有沿着行矩阵的至少一行的长度延伸的开口,从而使得所述开口位于至少一行中的所述多个生物场效应晶体管传感器的多于一个生物场效应晶体管传感器的所述沟道区域上方;以及界面层,设置在所述开口内的所述半导体衬底的第二表面上。
附图说明
当结合附图进行阅读时,从以下详细描述可最佳理解本发明的各个方面。应该指出,根据工业中的标准实践,各个部件未按比例绘制。实际上,为了清楚的讨论,各个部件的尺寸可以任意地增大或减小。
图1示出了根据一些实施例的感测器件的组件。
图2示出了根据一些实施例的示例性双栅极背侧感测fet传感器的截面图。
图3是根据一些实施例的示例性可寻址阵列中配置的多个fet传感器的电路图。
图4是根据一些实施例的双栅极fet传感器和加热器的示例性可寻址阵列的电路图。
图5a和图5b示出了根据一些实施例的示例性双栅极背侧感测fet传感器和非感测fet的截面图。
图6a示出了根据一些实施例的双栅极背侧感测fet传感器和非感测fet的布局。
图6b示出了根据一些实施例的双栅极背侧感测fet传感器和非感测fet的布局的电路表示。
图7a示出了根据一些实施例的具有共同感测阱的双栅极背侧感测fet传感器和非感测fet的多个像素的布局。
图7b示出了根据一些实施例的具有共同感测阱的一行中的双栅极背侧感测fet传感器的侧视图。
图7c示出了根据一些实施例的双栅极背侧感测fet传感器和非感测fet的多个像素的布局的电路表示。
图8a示出了根据一些实施例的具有共同感测阱的多个双栅极背侧感测fet传感器和非感测fet的布局。
图8b示出了根据一些实施例的双栅极背侧感测fet传感器和非感测fet的布局的电路表示。
图9示出了根据一些实施例的制造多个双栅极背侧感测fet传感器的示例性方法的流程图。
图10示出了根据一些实施例的生物感测芯片的示例性布局。
图11a至图11e示出了根据一些实施例的用于压电混合器的制造工艺的阶段。
图12示出了根据一些实施例的混合器与示例性双栅极背侧感测fet传感器的集成。
图13示出了根据一些实施例的用作ph传感器的示例性双栅极背侧感测fet传感器的截面图。
图14a和图14b示出了根据一些实施例的使用双栅极背侧感测fet传感器作为ph传感器。
图15示出了根据一些实施例的检测dna的示例性双栅极背侧感测biofet的截面图。
图16a示出了根据一些实施例的dna在受体表面上的结合机制。
图16b示出了根据一些实施例的基于匹配的分析物结合的示例性双栅极背侧感测biofet的阈值电压的改变。
图17示出了根据一些实施例的具有固定在其感测层上的抗体的示例性双栅极背侧感测biofet的截面图。
图18示出了根据一些实施例的抗原和抗体在受体表面上的结合机制。
具体实施方式
以下公开内容提供了许多用于实现所提供主题的不同特征的不同实施例或实例。下面描述了组件和布置的具体实例以简化本发明。当然,这些仅仅是实例,而不旨在限制本发明。例如,以下描述中,在第二部件上方或者上形成第一部件可以包括第一部件和第二部件直接接触形成的实施例,并且也可以包括在第一部件和第二部件之间可以形成额外的部件,从而使得第一部件和第二部件可以不直接接触的实施例。此外,本发明可在各个实施例中重复参考标号和/或字符。这种重复本身不指示所讨论的各个实施例和/或配置之间的关系。
而且,为便于描述,在此可以使用诸如“在…之下”、“在…下方”、“下部”、“在…之上”、“上部”等空间相对术语,以描述如图所示的一个元件或部件与另一个(或另一些)原件或部件的关系。除了图中所示的方位外,空间相对术语旨在包括器件在使用或操作中的不同方位。装置可以以其他方式定向(旋转90度或在其他方位上),而本文使用的空间相对描述符可以同样地作出相应的解释。
除非另有规定,本文使用的技术术语和科学术语具有与本发明所属领域的普通技术人员通常理解的相同的含义。虽然可以在根据本发明的实践或测试的实施例中使用与本文描述的那些类似或等效的任何方法和材料;但是现在描述该方法、器件和材料。本文提及的所有专利和出版物结合于此以用于描述和公开可能与本发明有关的出版物中报道的材料和方法。
本文使用的缩写“fet”是指场效应晶体管。一种类型的fet是指金属氧化物半导体场效应晶体管(mosfet)。历史上,mosfet是在诸如半导体晶圆的衬底的平面中和上构建的平面结构。但是近年来,半导体制造中的发展已经产生三维鳍式mosfet结构。
术语“biofet”是指包括一层固定的捕获试剂的fet,固定的捕获试剂用作表面受体以检测生物来源的目标分析物的存在。根据一些实施例,biofet是具有半导体转换器的场效应传感器。biofet的一个优势是具有无标记操作的前景。具体地,biofet能够避免昂贵和耗时的标记操作,诸如用例如荧光或放射性探针标记分析物。通过biofet检测的分析物通常是诸如但不限于蛋白质、碳水化合物、脂质、组织碎片或它们的部分的生物来源的。biofet可以是更广泛的fet传感器的一部分,fet传感器也可以检测任何化学化合物(本领域中称为“chemfet”)或包括诸如质子或金属离子的离子的任何其它元素(本领域中称为“isfet”)。本发明适用于所有类型的基于fet的传感器(“fet传感器”)。本文的一种特定类型的fet传感器是双栅极背侧感测fet传感器。
“s/d”是指形成fet的四个端子的两个的源极/漏极结。
表述“高k”是指高介电常数。在半导体器件结构和制造工艺的领域中,高k是指介电常数大于sio2的介电常数(例如,大于3.9)。
术语“分析”通常是指涉及物理、化学、生物化学或生物分析的方法或步骤,其包括但不限于表征、测试、测量、优化、分离、合成、添加、过滤、溶解或混合。
术语“测定”通常是指涉及化学或目标分析物的分析的方法或步骤并且包括但不限于基于细胞的测定、生物化学测定、高通量测定和筛选、诊断测定、ph测定、核酸杂交测定、聚合酶活性测定、核酸和蛋白质测序、免疫测定(例如,抗体-抗原结合测定、酶联免疫吸附测定(elisa)和免疫定量聚合酶链反应(iqpcr))、用于检测基因的甲基化模式的亚硫酸氢盐甲基化测定、蛋白质测定、蛋白质结合测定(例如蛋白质-蛋白质、蛋白-核酸和蛋白-配体结合测定)、酶测定、偶联酶测定、动力学测量(例如,蛋白质折叠的动力学和酶反应动力学)、酶抑制剂和活化剂筛选、化学发光和电化学发光测定、荧光测定、荧光偏振和各向异性测定、吸光度和比色测定(例如,bradford测定、lowry测定、hartree-lowry测定、biuret测定和二喹啉甲酸(bca)测定)、化学测定(例如,用于环境污染和污染物、纳米颗粒或聚合物的检测)和药物发现测定。本文描述的装置、系统和方法可以使用或采用与此处描述的fet传感器设计一起使用的这些测定中的一种或多种。
术语“液体活检”通常是指与受试者的组织样本相比从受试者的体液获得的活检样本。使用体液样本进行测定的能力通常比使用组织样本更可取。使用体液样本的侵入性较小的方法在患者福利、进行纵向疾病监测的能力以及甚至当组织细胞不容易接近时获得表达谱的能力方面具有广泛的意义,例如在前列腺中。用于检测液体活检样本中的目标分析物的测定包括但不限于上述那些。作为非限制性实例,可以在液体活检样本上进行循环肿瘤细胞(ctc)测定。
例如,固定在fet传感器上的捕获试剂(例如,抗体)可用于使用ctc测定的液体活检样本中的目标分析物(例如,肿瘤细胞标记物)的检测。ctc是从肿瘤中流入脉管系统并在例如血液中循环的细胞。通常,ctc以极低的浓度存在于循环中。为了测定ctc,通过本领域已知的各种技术从患者血液或血浆中富集ctc。可以使用本领域已知的方法对ctc染色以具有特定标记,本领域已知的方法包括但不限于基于细胞计数(例如,流式细胞术)的方法和基于免疫组织化学(ihc)的方法。对于本文描述的装置、系统和方法,可以使用捕获试剂捕获或检测ctc。在另一实例中,来自ctc的核酸、蛋白质或其它细胞环境可以被当成用于结合捕获试剂或由捕获试剂检测的目标分析物。
表达或含有ctc的目标分析物的增加可能有助于识别具有可能响应于特定治疗(例如,与目标分析物相关的一种)的癌症的受试者,或允许优化治疗方案,例如,目标分析物的抗体。ctc测量和定量可以提供关于例如肿瘤的阶段、治疗反应、疾病进展或它们的组合的信息。例如,从检测ctc上的目标分析物获得的信息可以用作例如预后、预测或药效动力学生物标志物。此外,用于液体活检样品的ctc测定可以单独使用或与固体活检样品的额外的肿瘤标记分析组合使用。
术语“鉴定”通常是指基于其与已知身份的捕获试剂的结合来确定目标分析物的身份的过程。
术语“测量”通常是指基于其与捕获试剂的结合来确定目标分析物的量、数量、质量或性质的过程。
术语“定量”通常是指基于其与捕获试剂的结合来确定目标分析物的量或浓度的过程。
术语“检测”通常是指基于其与捕获试剂的结合来确定目标分析物的存在或不存在的过程。检测包括但不限于识别、测量和定量。
术语“化学物”是指单质、化合物、混合物、溶液、乳液、分散体、分子、离子、二聚体、诸如聚合物或蛋白质的大分子、生物分子、沉淀物、晶体、化学部分或基团、颗粒、纳米颗粒、试剂、反应产物、溶剂或任何一种可以以固态、液态或气态存在的流体,并且这种流体通常是分析对象。
术语“反应”是指涉及至少一种化学物质的物理、化学、生物化学或生物转化并且通常涉及(例如,在化学、生物化学和生物转化的情况下)破坏或形成一种或多种键,诸如共价、非共价、范德华力、氢或离子键。术语“反应”包括化学反应,诸如合成反应、中和反应、分解反应、置换反应、还原-氧化反应、沉淀、结晶、燃烧反应和聚合反应,以及共价和非共价结合、相变、颜色变化、相形成、结晶、溶解、发光、光吸收或发射性质的变化、温度变化或热吸收或发射、构象变化以及诸如蛋白质的大分子的折叠或展开。
本文使用的“捕获试剂”是能够结合目标分析物或目标试剂的分子或化合物,该分子或化合物可以直接或间接附接至大部分固体材料。捕获剂可以是化学物质,并且特别是天然存在的目标分析物(例如,抗体、多肽、dna、rna、细胞、病毒等)或可以制备的目标分析物的任何物质,并且捕获试剂可以在测定中与一种或多种目标分析物结合。
本文使用的“目标分析物”是使用本发明内容在测试样品中待检测的物质。目标分析物可以是化学物质,并且特别是天然存在的捕获试剂(例如抗体、多肽、dna、rna、细胞、病毒等)或可以制备的捕获试剂的任何物质,并且目标分析物可以在测定中与一种或多种捕获试剂结合。“目标分析物”还包括任何抗原物质、抗体或它们的组合。目标分析物可包括蛋白质、肽、氨基酸、碳水化合物、激素、类固醇、维生素,包括用于治疗目的的药物以及用于非法目的的药物、细菌、病毒以及任何上述物质的代谢物或抗体。
本文使用的“测试样品”是指使用本发明内容检测和测定的含有目标分析物的组合物、溶液、物质、气体或液体。测试样品可以包含除了目标分析物之外的其它组分,可以具有液体或气体的物理属性,并且可以是任何尺寸或体积,包括例如液体或气体的移动流。只要其他物质不干扰目标分析物与捕获试剂的结合或第一结合构件与第二结合构件的特异性结合,则测试样品可以含有除目标分析物之外的任何物质。测试样品的实例包括但不限于天然存在和非天然存在的样品或它们的组合。天然存在的测试样品可以是合成物或合成的。天然存在的测试样品包括受试者的身体或从受试者体内或身体上的任何位置分离的体液,包括但不限于血液、血浆、血清、尿液、唾液或痰液、脊髓液、脑脊液、胸膜液、乳头抽吸物、淋巴液、呼吸道液体、肠道和泌尿生殖道液、泪液、唾液、母乳、淋巴系统液、精液、脑脊液、器官内系统液、腹水,肿瘤囊肿液,羊水以及它们的组合,以及环境样品诸如地下水或废水、土壤提取物、空气和农药残留物或食品相关样品。
检测的物质可以包括例如核酸(包括dna和rna)、激素、不同的病原体(包括对其宿主引起疾病或病的生物制剂,诸如病毒(例如h7n9或hiv)、原生动物(例如,导致疟原虫的疟疾)或细菌(例如,大肠杆菌或结核分枝杆菌))、蛋白质、抗体、各种药物或治疗剂或其它化学或生物物质(包括氢或其它离子、非离子分子或化合物、多糖、小化学化合物诸如化学组合库成员等)。检测或确定的参数可以包括但不限于ph变化、乳糖变化、浓度变化、每单位时间的颗粒(即流体在装置上流过一段时间以检测颗粒(例如,稀疏的颗粒))和其它参数。
本文使用的术语“固定”当用于例如捕获试剂时,包括将分子水平的捕获试剂基本上附接至表面。例如,捕获试剂可以使用包括非共价相互作用(例如,静电力、范德华力和疏水界面的脱水)的吸附技术以及共价键合技术固定在衬底材料的表面上,其中,官能团或链接体有利于将捕获试剂附接至表面。可以根据衬底表面的性质、携带捕获试剂介质的性质和捕获试剂的性质将捕获试剂固定至衬底材料的表面。在一些情况下,可以首先修改衬底表面,以具有与表面结合的官能团。之后,官能团可以与生物分子或生物或化学物质结合以将它们固定在其上。
术语“核酸”通常是指通过磷酸二酯键彼此连接的一组核苷酸,并且是指自然存在的天然存在的核苷酸连接而成的天然存在的核酸,诸如包括具有彼此连接的任何腺嘌呤、鸟嘌呤、胞嘧啶和胸腺嘧啶的脱氧核糖核苷酸的dna和/或包括具有彼此连接的任何腺嘌呤、鸟嘌呤、胞嘧啶和尿嘧啶的核糖核苷酸的rna。此外,非天然存在的核苷酸和非天然存在的核酸均在本发明的核酸的范围内。实例包括肽核酸(pna)、具有磷酸基团的肽核酸(phona)、桥连核酸/锁定核酸(bna/lna)和吗啉核酸。其它实例包括化学修饰的核酸和核酸类似物,例如甲基膦酸酯dna/rna、硫代磷酸酯dna/rna、氨基磷酸酯dna/rna和2'-o-甲基dna/rna。核酸包括可以修饰的那些。例如,核酸中的磷酸基、糖和/或碱可以根据需要进行标记。本领域已知的任何用于核酸标记的物质都可用于标记。其实例包括但不限于放射性同位素(例如,32p、3h和14c)、dig、生物素、荧光染料(例如,fitc、texas、cy3、cy5、cy7、fam、hex、vic、joe、rox、tet、bodipy493、nbd和tamra)和发光物质(例如,吖啶酯)。
本文使用的术语“适体”是指与特定目标分子结合的寡核酸或肽分子。使用单链核酸(适配体)作为蛋白质结合的亲和分子的概念是基于短序列在目标存在下折叠成以高亲和力和特异性结合目标的独特的三维结构的能力。选择剂可以是选择用于与分子目标的高亲和力结合的寡核苷酸配体。
本文使用的术语“抗体”是指能够非共价、可逆地和以特定方式结合相应抗原的免疫球蛋白家族的多肽。例如,天然存在的igg抗体是包括通过二硫键相互连接的至少两个重(h)链和两个轻链(l)链的四聚体。每个重链均包括重链可变区(本文缩写为“vh”)和重链恒定区。重链恒定区包括三个结构域:ch1、ch2和ch3。每个轻链包括轻链可变区(本文缩写为“vl”)和轻链恒定区。轻链恒定区包括一个结构域cl。vh和vl区域可以进一步细分为高变区域,称为互补决定区域(cdr),散布于更保守的区域,称为框架区(fr)。每个vh和vl均由以下顺序:fr1、cdr1、fr2、cdr2、fr3、cdr3和fr4从氨基末端至羧基末端布置的三个cdr和四个fr组成。三个cdr构成约15-20%的可变结构域。重链和轻链的可变区域含有与抗原相互作用的结合结构域。抗体的恒定区域可以介导免疫球蛋白与宿主组织或因子(包括免疫系统的各种细胞(例如,效应细胞))和经典补体系统的第一组分(c1q)的结合。
术语“抗体”包括但不限于单克隆抗体、人抗体、人源化抗体、嵌合抗体和抗独特型(抗id)抗体(包括例如涉及本发明的抗体的抗-id抗体)。抗体可以是任何同种型/类(例如,igg、ige、igm、igd、iga和igy)或亚类(例如,igg1、igg2、igg3、igg4、iga1和iga2)。
术语“聚合物”意味着由两个或多个彼此重复链接的结构单元(“mers”)组成的任何物质或化合物。例如,“二聚体”是其中两个结构单元已经结合在一起的化合物。聚合物包括缩合和加成聚合物。缩聚物的实例包括聚酰胺、聚酯、蛋白质、羊毛状人造纤维、丝状纤维、聚氨酯、纤维素和聚硅氧烷。加成聚合物的实例是聚乙烯、聚异丁烯、聚丙烯腈、聚(氯乙烯)和聚苯乙烯。其它实例包括具有增强的电性质或光学性质(例如,非线性光学性质)的聚合物,诸如导电或光折射聚合物。聚合物包括直链和支链聚合物。
示例性生物感测器件概述
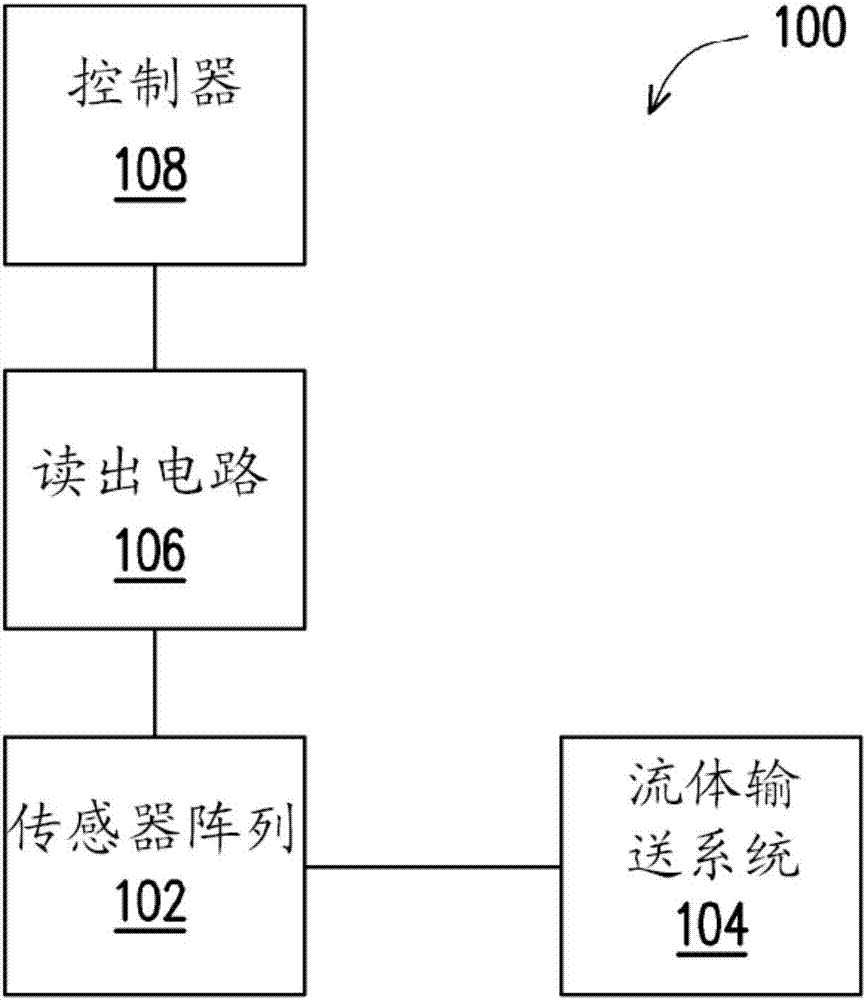
图1示出了可以包括在生物传感器系统100中的组件的概述。生物传感器系统100包括具有用于检测生物或化学分析物的至少一个感测元件的传感器阵列102和设计为将一个或多个流体样本输送至传感器阵列102的流体输送系统104。流体输送系统104可以是放置在传感器阵列102之上的微流体阱以容纳传感器阵列102上方的流体。流体输送系统104也可以包括用于将各种流体输送至传感器阵列102的微流体沟道。流体输送系统104可以包括设计为将流体输送至传感器阵列102的任何数量的阀、泵、室、沟道。
根据一些实施例,提供读出电路106以测量来自传感器阵列102中的传感器的信号并且产生指示存在于目标溶液中的特定分析物的量的可量化的传感器信号。本文描述的读出电路106的不同实施例利用数码组件来减小功耗和管芯面积。
控制器108可以用于向传感器阵列102和读出电路106发送电信号和从传感器阵列102和读出电路106接收电信号,以实施生物或化学感测测量。控制器108也可以用于将电信号发送至流体输送系统104,以例如致动一个或多个阀、泵或电机。
传感器阵列102可以包括biofet的阵列,其中,阵列中的一个或多个biofet被功能化以检测特定的目标分析物。不同的传感器可以使用不同的捕获试剂功能化,以用于检测不同的目标分析物。以下提供关于具体的biofet的示例设计的更多细节。biofet可以布置为多个行和列,形成二维传感器阵列。在一些实施例中,使用不同的捕获试剂功能化biofet的每行。在一些实施例中,使用不同的捕获试剂功能化biofet的每列。
控制器108可以包括一个或多个处理器件,诸如微处理器,并且可以是可编程的以控制读出电路106和/或传感器阵列102的操作。控制器108本身的细节对于理解本文描述的实施例并不重要。然而,下面将更详细地讨论传感器阵列102可以发送和接收的各种电信号。
双栅极背侧式fet传感器
本申请的实施例涉及传感器阵列102中的biofet传感器的各种布局,其允许开口暴露多于一个biofet传感器的沟道区域。如本文更详细地说明,先前的设计在每个biofet传感器上方使用分隔开的开口,这导致一些缺点。该特定部分描述了可以在本申请的实施例中使用的示例biofet传感器设计。
可以在传感器阵列102中使用的一种示例类型的biofet传感器是双栅极背侧式fet传感器。双栅极背侧式fet传感器利用半导体制造技术和生物捕获试剂形成阵列传感器。虽然mosfet可以具有连接至单个电节点的单个栅电极,但是双栅极背侧感测fet传感器具有两个栅电极,两个栅电极的每个均连接到不同的电节点。两个栅电极的第一个在本文中称为“前侧栅极”,并且两个栅电极的第二个在本文中称为“背侧栅极”。前侧栅极和背侧栅极都配置为使得在操作中每一个可以被充电和/或放电,并且从而每个均影响双栅极背侧感测fet传感器的源极/漏极端子之间的电场。前侧栅极是导电的,通过前侧栅极电介质与沟道区域分隔开,并且配置为通过连接的电路充电和放电。背侧栅极通过背侧栅极电介质与沟道区域分隔开并且包括设置在背侧栅极电介质上的生物功能化感测层。背侧栅极上的电荷量是是否发生生物识别反应的函数。在双栅极背侧感测fet传感器的操作中,将前侧栅极充电至预定电压范围内的电压。前侧栅极上的电压确定fet传感器的沟道区域的相应的电导率。背侧栅极上的电荷的相对少量的变化改变了沟道区域的电导率。电导率的这种改变指示生物识别反应。
fet传感器的一个优势是无标记操作的前景。具体地,fet传感器能够避免昂贵且耗时的标记操作,诸如用例如荧光或放射性探针标记分析物。
图2示出了根据一些实施例的示例性双栅极背侧感测fet传感器200。双栅极背侧感测fet传感器200包括形成在衬底214的表面上并且通过设置在衬底214上的中间电介质215与衬底214的表面分隔开的控制栅极202。可以在衬底214的一侧上提供包括多个互连层的互连区域211。衬底214包括源极区域204、漏极区域206以及位于源极区域204和漏极区域206之间的沟道区域208。在一些实施例中,衬底214具有介于约100nm和约130nm之间的厚度。可以使用合适的cmos工艺技术形成栅极202、源极区域204、漏极区域206和沟道区域208。栅极202、源极区域204、漏极区域206和沟道区域208形成fet。隔离层210与栅极202设置在衬底214的相对侧上。在一些实施例中,隔离层210具有约1μm的厚度。在本发明中,在其上方设置栅极202的衬底的侧称为衬底214的“前侧”。类似地,在其上设置隔离层210的衬底214的侧称为“背侧”。
在隔离层210中提供开口212。开口212可以与栅极202基本对准。在一些实施例中,开口212大于栅极202并且可以在多个双栅极背侧感测fet传感器上方延伸。界面层(未示出)可以设置在沟道区域208的表面上的开口212中。界面层可以是可操作的以提供用于定位和固定用于生物分子或生物实体的检测的一个或多个受体的界面。此处提供了关于界面层的更多细节。
双栅极背侧感测fet传感器200包括分别至漏极区域206和源极区域204的电接触件216和218。可以制成至栅极202的前侧栅极接触件220,同时可以制成至沟道区域208的背侧栅极接触件222。应该注意,背侧栅极接触件222不需要物理接触衬底214或位于衬底214上方的任何界面层。因此,虽然fet可以使用栅极接触件控制源极和漏极之间的半导体(例如,沟道)的电导率,但是,双栅极背侧感测fet传感器200允许形成在与fet器件的栅极202相对的侧上的受体来控制电导率,同时栅极202提供控制电导率的另一区域。因此,如此处使用各个实例更详细的讨论的,双栅极背侧感测fet传感器200可以用于检测周围环境中和/或开口212中的一种或多种特定生物分子或生物实体。
双栅极背侧感测fet传感器200可以连接至:额外的无源组件,诸如电阻器、电容器、电感器和/或熔丝;其它有源组件,包括p沟道场效应晶体管(pfet)、n沟道场效应晶体管(nfet)、金属氧化物半导体场效应晶体管(mosfet)、高压晶体管和/或高频晶体管;其它合适的组件;或它们的组合。还应当理解,可以在双栅极背侧感测fet传感器200中添加额外的部件,并且对于双栅极背侧感测fet传感器200的额外的实施例,可以替换或消除所描述的一些部件。
图3示出了连接至位线306和字线308的biofet传感器304的示例性可寻址阵列300的部分的示意图。应该注意,此处使用的术语位线和字线表示与存储器器件中的阵列构造相似之处,然而,并不意味着存储器器件或存储阵列必须包括在阵列中。可寻址阵列300可以与在诸如动态随机存取存储器(dram)阵列的其它半导体器件中采用的具有相似之处。例如,以上参照图2描述的双栅极背侧感测fet传感器200可以形成在dram阵列中将发现电容器的位置中。示意图300仅仅是示例性的并且普通技术人员将意识到其它配置是可能的。
根据一些实施例,biofet传感器304的每个均可以与双栅极背侧感测fet传感器200基本类似。fet302配置为提供biofet传感器304的漏极端子和位线306之间的电连接。通过这种方式,fet302类似于dram阵列中的存取晶体管。在一些实施例中,biofet传感器304是双栅极背侧感测fet传感器并且每个均包括由设置在fet沟道区域(设置在反应位点处)上面的介电层上的受体材料提供的感测栅极以及由设置在fet沟道区域上面的介电层上的栅电极(例如,多晶硅)提供的控制栅极。
可寻址阵列300示出了设计为检测由引入至biofet传感器304的生物分子或生物实体提供的小信号变化的阵列形成。由于相同行或列中的不同的fet的共同的端子连接在一起,因此使用位线306和字线308的阵列格式允许较少数量的输入/输出焊盘。放大器可以用于增强信号强度以提高具有示意图300的电路布置的器件的检测能力。在一些实施例中,当电压施加至特定字线308和位线306时,相应的存取晶体管302将导通(例如,像开关)。当相关的biofet传感器304的栅极(例如,诸如双栅极背侧感测fet传感器200的背侧栅极222)具有受到生物分子存在影响的电荷时,biofet传感器304的阈值电压改变,从而调制用于施加至背侧栅极222的给定电压的电流(例如,ids)。电流(例如,ids)或阈值电压(vt)的改变可以用于指示相关生物分子或生物实体的检测。
参照图4,呈现了示例性示意图400。示例性示意图400包括布置为单独的阵列401的可寻址像素402的存取晶体管302和biofet传感器304。阵列401可以包括任何数量的像素402。例如,阵列401可以包括128x128像素。其它布置可以包括256x256像素或诸如128x256像素的非正方形阵列。
每个像素402均包括存取晶体管302和biofet传感器304以及可以包括一个或多个加热器408和温度传感器410的其它组件。在该实例中,存取晶体管302是n沟道fet。n沟道fet412也可以用作温度传感器410的存取晶体管。在一些实施例中,fet302和412的栅极是连接的,但是这不是必需的。可以使用列解码器406和行解码器404来单独寻址每个像素402(及其相关的组件)。在一些实施例中,每个像素402均具有约10微米x约10微米的尺寸。在一些实施例中,每个像素402均具有约5微米x约5微米的尺寸或具有约2微米x约2微米的尺寸。
列解码器406和行解码器404可以用于控制n沟道fet302和412的on/off状态(例如,一起将电压施加至fet302和412的栅极,并且一起将电压施加至fet302和412的的漏极区域)。导通n沟道fet302提供了至biofet传感器304的s/d区域的电压。当biofet传感器304导通时,电流ids流经biofet传感器304并且可以被测量。
加热器408可以用于局部地增加biofet传感器304周围的温度。加热器408可以使用任何已知的技术构造,诸如形成具有穿过其的高电流的金属图案。加热器408也可以是热电加热器/冷却器,如珀尔帖器件。加热器408也可以在某些生物测试期间使用,诸如以使dna或rna变性或提供某些生物分子的结合环境。温度传感器410可以用于测量biofet传感器304周围的局部温度。在一些实施例中,可以创建控制回路以使用加热器408以及从温度传感器410接收的反馈来控制温度。在一些实施例中,加热器408可以是允许用于局部主动冷却像素402内的组件的热电加热器/冷却器。
参照图5a,根据一些实施例,提供了具有双栅极背侧感测fet传感器502和存取晶体管522的半导体器件500的截面图。双栅极背侧感测fet传感器502包括栅极506、位于栅极506的两侧上的s/d区域510以及位于形成在衬底504内的s/d区域510之间的沟道区域508。在栅极506和沟道区域508之间也存在栅极介电层,但是在图中未示出。为了便于描述某些元件,衬底504示出为具有正面505和相对的平行背面507。应该注意,如相关领域的技术人员将理解的,图5a的各个组件不旨在按比例绘制,并且为了视觉方便而被放大。
双栅极背侧感测fet传感器502包括设置在隔离层512上方以及沟道区域508上方的开口514内的界面层516。在一些实施例中,界面层516具有介于约
根据一些实施例,存取晶体管522可以以诸如具有存取晶体管302和fet传感器304的图3中示出的布置连接至双栅极背侧感测fet传感器502。存取晶体管522类似地包括栅极524、位于栅极524的两侧上的s/d区域528以及位于形成在衬底504内的s/d区域528之间的沟道区域526。存取晶体管522包括位于其沟道区域526上方的隔离层512(即,没有穿过沟道区域526上方的隔离层512形成开口)。如图5a所示,界面层516可以仍沉积在存取晶体管522上方的隔离层512上。如相关领域的技术人员将理解的,存取晶体管522可以使用浅沟槽隔离(sti)530与双栅极背侧感测fet传感器502分隔开。
在一些实施例中,栅极506、栅极524、s/d区域510以及s/d区域528连接至互连区域518内的金属互连件的各个层。金属互连件可以用于制成与形成在衬底504内的各个掺杂区域和其它器件的电连接。可以在互连区域518中使用任何数量层级的金属互连件以及连接在层级之间的金属插塞。相关领域的技术人员将理解形成这种金属互连件的工艺。
根据一些实施例,半导体器件500也可以包括连接至互连区域518的载体衬底520。载体衬底520可以包括一个或多个导电部分以制成与互连区域518的某些金属互连件的电连接。载体衬底520可以用于为构成衬底504和互连区域518的薄层提供物理支撑和稳定性。
双栅极背侧fet传感器502可以连接至在衬底504内制造的额外的电路。额外的电路可以包括mosfet器件、电阻器、电容器和/或电感器以形成有助于双栅极背侧感测fet传感器502的操作的电路。该电路可以表示用于测量来自双栅极背侧fet传感器502的信号的读出电路,该信号指示分析物检测。列举几个实例,该电路可以包括放大器、模数转换器(adc)、数模转换器(dac)、电压发生器、逻辑电路和/或dram存储器。附加电路的所有或一些组件均可以集成在衬底504中。应当理解,许多biofet传感器(每个均与双栅极背侧fet传感器502基本类似)可以集成在衬底504中并且连接至额外的电路。在另一实例中,可以在与衬底504分隔开的另一半导体衬底上提供额外电路的所有或一些组件。在又另一实例中,额外电路的一些组件集成在衬底504中,并且在另一半导体衬底上提供额外电路的一些组件。
图5b示出了具有设置在fet上方的流体532的半导体器件500。流体532可以包括由于例如流体532的ph改变、目标分析物和捕获试剂之间的酶反应,靶分析物和捕获试剂之间的结合反应或其它生物相互作用而产生的离子浓度534。可以提供流体栅极536以形成双栅极背侧fet传感器502的背侧栅极。沟道区域508附近的离子浓度534的存在影响双栅极背侧fet传感器502的背侧栅极的操作并且可以检测为用于施加至栅极506或者流体栅极536的给定电压的漏极电流ids的变化。以下更详细的讨论使用双栅极背侧fet传感器502的一些示例性检测研究。
根据一些实施例,可以通过流经设置在背面507上方的微流体沟道将流体532提供至开口514内。微流体沟道可以直接接合至界面层516或者隔离层512。微流体沟道可以由诸如聚二甲基硅氧烷(pdms)或聚乙二醇(peg)的聚合物材料模制而成。在一些实施例中,流体532设置在静止地保持流体532并且允许流体532通过开口514进入的微流体阱中。
图6a示出了根据一些实施例的双栅极背侧fet传感器502和存取晶体管522的示例性布局。与图5a和图5b中示出的那些相同的元件在图6a中的标号一致。开口514示出为略宽于栅极506以在俯视图中可以看见。开口514的精确尺寸可以在s/d区域510的范围内变化。然而,在该器件中,开口514仅暴露单个双栅极背侧fet传感器502的沟道区域(与栅极506对准)。金属层602用于通过接触件604制成至双栅极背侧fet传感器502的s/d区域510和存取晶体管522的s/d区域528的电接触。可以在图5a和图5b的互连区域518内提供金属层602和接触件604。
图6b示出了根据一些实施例的对应于图6a中示出的布局的双栅极背侧fet传感器502和存取晶体管522的示例性电路表示。可以在感测操作期间将电压(vpg)施加至双栅极背侧fet传感器502的栅极506以偏置传感器(例如,on状态)。为了测量来自双栅极背侧fet传感器502的电流,可以将电压(sel)施加至存取晶体管522的栅极524。如果也将电压施加至端子n2,则之后电流可以流经双栅极背侧fet传感器502和存取晶体管522。如下面更详细的讨论的,电流的大小可以受到由双栅极背侧fet传感器502检测的任何目标分析物的影响。
根据一些实施例,图5a和图6a示出的开口514的宽度为双栅极背侧fet传感器502的栅极长度的数量级。开口514通常限制为仅暴露双栅极背侧fet传感器502的沟道区域508,以避免有流体532影响衬底504中的其它fet(例如存取晶体管522)的操作。由于界面层516的表面张力和疏水性,流体532可能难以进入开口514。这些因素有助于防止流体532直接在沟道区域508之上润湿界面层516的表面。由于半导体器件500的示出的布局(其中,双栅极背侧fet传感器502和存取晶体管522基本并排),开口514的扩展也可以暴露存取晶体管522的沟道区域526,这影响了存取晶体管522的操作。
根据一些实施例,多个双栅极背侧fet传感器并排布置为行,以允许扩展的开口跨越每个双栅极背侧fet传感器。图7a示出了根据一些实施例的布置为单行的多个像素702-1至702-n的示例性布局700,其中,每个像素均具有双栅极背侧fet传感器704和存取晶体管706。应当理解,单个像素的以下描述同样适用于阵列中的所有其它像素。此外,虽然仅示出了单行像素,但是应当理解,可以使用多行像素来提供像素的二维矩阵,每个像素矩阵均包含双栅极背侧fet传感器和相应的存取晶体管。使用诸如图7a中示出的像素布局与图6a中示出的像素布局的像素布局导致传感器阵列的器件覆盖区减小约20%。
根据一些实施例,布局700包括开口708以暴露每个双栅极背侧fet传感器704的沟道区域。由于横跨像素的行的每个双栅极背侧fet传感器均并排布置,因此,开口708可以跨越像素的整个行(例如,在x方向上)。
根据一些实施例,如像素702-n所示,每个双栅极背侧fet传感器704均可以具有包括位于两个沟道区域上方的两个栅极的栅极结构710与布置在两个栅极之间的s/d区域712a、712b和712c。s/d区域712b可以使用金属互连件714与存取晶体管706的s/d区域716电连接。当双栅极背侧fet传感器704偏置为on时,具有两个栅极的双栅极背侧fet传感器704的这种设计通过使第一电流从712b流至712a并且使第二电流从712b流至712c有效地使每个双栅极背侧fet传感器704的电流输出加倍。s/d区域712a和712c可以接地。根据实施例,每个双栅极背侧fet传感器704均具有其s/d区域712a和712c。当每个双栅极背侧fet传感器704是n沟道器件时,s/d区域712a和712c可以表示每个双栅极背侧fet传感器704的源极端子。当每个双栅极背侧fet传感器704是p沟道器件时,s/d区域712a和712c可以表示每个双栅极背侧fet传感器704的漏极端子。由于每个双栅极背侧fet传感器704的并排布局,邻近的fet传感器可以共用相同的s/d区域712a和712c。
应当理解,如图7a中示出的,每个像素中均使用两个栅极设计仅仅是一个实例,并且也可以在一个或多个或所有像素中使用单栅极设计。图6a中的双栅极背侧fet传感器502的布局图中示出了单栅极设计的实例。通过共用邻近的像素之间的s/d区域712a和712c,可以通过消除邻近的像素之间的无效空间来减小感测阵列的整体尺寸。
根据一些实施例,像素702-1至702-n的每个双栅极背侧fet传感器704的栅极结构710连接在一起。通过这种方式,每个双栅极背侧fet传感器704可以同时偏置为on,并且通过施加至特定存取晶体管706的栅极718的电压实施要测量的传感器的选择。每个存取晶体管706的s/d区域720均可以通过金属互连件722电连接至电压源。根据实施例,每个存取晶体管706的s/d区域720电连接在一起,从而使得仅施加至栅极718的电压确定偏置为on的存取晶体管。此外,可以从电连接至金属互连件722的任何节点测量来自相应的双栅极背侧fet传感器704的电流。
图7b示出了根据一些实施例的横跨像素702-1和702-n之间的双栅极背侧fet传感器704的行截取的截面图。开口708在x方向上横跨多个biofet传感器,以暴露衬底504的背面507的部分。背面507的暴露部分包括跨越多于一个双栅极背侧fet传感器的多个沟道区域508的表面。衬底504的正面505包括在沟道区域508上方图案化的多个栅极710。
根据一些实施例,界面层516设置在开口708内以提供用于结合各种捕获试剂的表面。由于开口708的较大的宽度,携带捕获试剂或者与捕获试剂相互作用的目标分析物的流体可以更容易地进入直接位于背面507上的界面层516。
根据一些实施例,可以通过流经设置在背面507上方的微流体沟道将流体提供至开口708内。微流体沟道可以直接接合至界面层516或者隔离层512。微流体沟道可以由诸如例如聚二甲基硅氧烷(pdms)或聚乙二醇(peg)的聚合物材料模制而成。微流体沟道可以在x方向上延伸,从而使得流体在横跨开口708的x方向上流动。在一些实施例中,对二维感测阵列中的每行双栅极背侧fet传感器704提供不同的微流体沟道。在其它实施例中,微流体沟道包括足够宽的宽度以覆盖二维感测阵列中的多于一个或所有双栅极背侧fet传感器704的行。
在一些实施例中,流体设置在静止地保持流体并且允许流体通过开口708进入的微流体阱中。根据一些实施例,微流体阱保持介于约1μl和约100μl之间的流体。微流体阱可以设定尺寸和定位,从而使得仅二维感测阵列中的双栅极背侧fet传感器704的总数的部分暴露于阱内的流体。在另一实例中,二维感测阵列中的所有双栅极背侧fet传感器704都暴露于阱内的流体。
图7c示出了根据一些实施例的布局700的电路表示。示出像素702-1至702-n的行,其中,每个存取晶体管706均具有其连接在一起的漏极端子(在n沟道器件的情况下),以用于测量来自选择的双栅极背侧fet传感器704的电流iout。
开口708可以横跨像素702-1至702-n的整个给定行,或者可以横跨像素702-1至702-n的子集。一行像素的总数量(n)可以少至2并且多至4096。此外,开口708不限于仅横跨一行像素。在一些实施例中,开口708也在y方向上延伸以暴露其它行中的双栅极背侧fet传感器的沟道区域。当在x方向和y方向上延伸的开口暴露二维阵列中的多个双栅极背侧fet传感器的沟道区时,每个存取晶体管706均可以位于双栅极背侧fet传感器的二维阵列的外部。
图8a示出了根据一些实施例的双栅极背侧fet传感器bf1至bfn的另一布局800。在布局800中,双栅极背侧fet传感器bf1至bfn再次并排布置为相同的行,从而使得开口708跨越多个传感器以暴露每个双栅极背侧fet传感器bf1至bfn的沟道区域。然而,与布局700不同,每个双栅极背侧fet传感器与两个其它fet器件电连接。在示出的实例中,双栅极背侧fet传感器bf1与存取晶体管s1a和分流晶体管s1b连接,同时双栅极背侧fet传感器bf2与存取晶体管s2a和分流晶体管s2b连接。可以对行中的每个像素重复这种相同的布置。
应该注意,如图8a中示出的,对于每个双栅极背侧fet传感器bf1至bfn使用两个栅极设计仅仅是一个实例,并且也可以使用单栅极设计。在图6a中的双栅极背侧fet传感器502的布局图中示出了单栅极设计的实例。同样,通过共用邻近的传感器之间的接地的s/d区域,可以通过消除邻近的像素之间的无效空间来减小感测阵列的整体尺寸。
图8b示出了根据一些实施例的具有与图8a使用的相同的标记以识别相同的元件的布局800的电路表示。现在将提供示例性操作来描述分流晶体管的功能。当需要测量双栅极背侧fet传感器bf1的电流时,将电压施加至存取晶体管s1a的栅极以将晶体管偏置为on,从而创建至bf1的导电路径,并且可以测量电流iout。当存取晶体管s1a偏置为on时,分流晶体管s1b偏置为off以切断接地的分流路径。根据实施例,逆变器用于确保与在分流晶体管s1b的栅极处接收的信号相比,在存取晶体管s1a的栅极处接收的信号被反转。逆变器可以布置在每个像素中以确保每个存取晶体管s1a和分流晶体管s1b的正确操作。逆变器也可以与具有用于给定像素的相应的位线和字线的输入的nand栅极连接。
因为仅需要双栅极背侧fet传感器bf1的电流,因此存取晶体管s2a偏置为off。分流晶体管s2b偏置为on以确保没有电压施加至未选择的双栅极背侧fet传感器bf2。如果不使用分流晶体管s2b,则可能存在浮置(例如,未知)电压电位,并且引起不必要的电流流经bf2。反之亦然,当需要测量bf2的电流时,应用相同的描述。
图9示出了根据一些实施例的用于制造诸如布局700和800中示出的那些的多个双栅极背侧fet传感器的示例性方法900。方法900可以包括使用与互补金属氧化物半导体(cmos)工艺兼容或典型的互补金属氧化物半导体(cmos)工艺的一个或多个工艺步骤形成双栅极背侧fet传感器。应当理解,可以在方法900之前、期间和之后提供额外的操作,并且对于方法的额外的实施例,可以替换或消除以下描述的一些步骤。此外,应当理解,方法900包括具有典型的cmos技术工艺流程的特征的操作,因此,此处仅简要描述。典型的cmos技术工艺可以包括光刻;离子注入;扩散;沉积,包括物理汽相沉积(pvd)、金属蒸发或溅射、化学汽相沉积(cvd)、等离子体增强化学汽相沉积(pecvd)、大气压化学气相沉积(apcvd)、低压cvd(lpcvd)、高密度等离子体cvd(hdpcvd)、原子层cvd(alcvd)、旋涂;以及蚀刻,包括湿蚀刻、干蚀刻和等离子体蚀刻。可以参照图5a和图7b中示出的某些元件。
方法900开始于提供衬底的块902。该衬底可以是半导体衬底。该半导体衬底可以是硅衬底。可选地,该衬底可以包括另一元素半导体,诸如锗;化合物半导体,包括碳化硅;合金半导体,包括硅锗;或它们的组合。在一些实施例中,该衬底是绝缘体上半导体(soi)衬底。该衬底可以包括掺杂区域,诸如p阱和n阱。在本发明中,晶圆是包括半导体衬底以及形成在半导体衬底中和上方并且附接至半导体衬底的各个部件的工件。该晶圆可以处于制造的各个阶段并且使用cmos工艺处理。在完成制造的各个阶段之后,将晶圆分离成单独的管芯(被封装成集成芯片)。
之后,方法900进入在衬底的正面上形成多个栅极的块904。多个栅极的第一子集可以用作双栅极背侧fet传感器的栅极,而多个栅极的第二子集可以用作衬底中的各个其它晶体管(诸如存取晶体管和/或分流晶体管)的栅极。根据一些实施例,栅极是多晶硅。其它示例性栅极材料包括金属,诸如铜(cu)、钨(w)、钛(ti)、钽(ta)、铬(cr)、铂(pt)、银(ag)、金(au);合适的金属化合物,如氮化钛(tin)、氮化钽(tan)、硅化镍(nisi)、硅化钴(cosi);它们的组合;和/或其它合适的导电材料。
在多个栅极和衬底的正面之间提供栅极电介质。在一些实施例中,栅极电介质是氧化硅。其它示例性栅极电介质包括氮化硅、氮氧化硅、具有高介电常数(高k)的电介质或它们的组合。高k材料的实例包括硅酸铪、氧化铪、氧化锆、氧化铝、五氧化二钽、二氧化铪-氧化铝(hfo2-al2o3)合金或它们的组合。
方法900进入在多个栅极的每个的两侧上的衬底中形成s/d区域的块906。根据fet配置(即,n沟道或p沟道),s/d区域可以包括n型掺杂剂或p型掺杂剂。双栅极背侧fet传感器和其它晶体管(诸如存取晶体管和/或分流晶体管)的s/d区域可以同时形成。可以形成额外的互连层(诸如在互连区域518内形成的那些)以创建至多个栅极和多个s/d区域的每个的电连接。
载体衬底520也可以附接至互连区域518以允许对衬底的背面进行各种随后的操作,而不影响半导体衬底的结构完整性。在一些实施例中,载体衬底520接合至互连区域518的最后的金属互连层。在一些实施例中,载体衬底520接合至形成在互连区域上的钝化层。载体衬底可以使用熔融、扩散、共晶和/或其它合适的接合方法附接至器件衬底。用于载体衬底的示例性组分包括硅、玻璃和石英。在一些实施例中,载体衬底可以包括诸如互连部件、结合位点、限定腔和/或其它合适的部件的其它功能。可以在随后的工艺期间(例如,在减薄之后)去除载体衬底。
根据一些实施例,方法900进入穿过衬底的背侧上的介电层形成开口的块908。例如,可以穿过隔离层512蚀刻开口708以暴露衬底504的背面507。根据一些实施例,开口708足够大以暴露多于一个双栅极背侧fet传感器的沟道区域508。开口708可以跨越并排布置的双栅极背侧fet传感器的行。
可以通过首先实施诸如反应离子蚀刻(rie)或任何等离子体蚀刻的干蚀刻以减薄衬底的背面上的介电层来形成开口。之后,可以使用诸如缓冲氧化物蚀刻(boe)或氢氟酸(hf)的湿蚀刻去除开口内的介电层的薄剩余部分。
根据一些实施例,方法900进入在开口内的暴露的沟道区域上方的衬底的背面上设置界面层516的块910。界面层与生物分子或生物实体结合兼容。例如,界面层可以为生物分子或生物实体提供结合界面。界面层可以包括用于保持受体的介电材料、导电材料和/或其它合适的材料。示例性界面材料包括高k介电膜、金属、金属氧化物、电介质和/或其它合适的材料。如另一实例,示例性界面层材料包括:氧化铪(hfo2)、氧化钽(ta2o5)、pt、au、w、ti、铝(al)、cu;这种金属的氧化物,诸如例如二氧化硅(sio2)、氮化硅(si3n4)、氧化铝(al2o3)、氧化钛(tio2)、tin、氧化锆(zro2)、氧化锡(ii)(sno)、二氧化锡(sno2);和/或其它合适的材料。可以使用诸如例如物理汽相沉积(pvd)(溅射)、化学汽相沉积(cvd)、等离子体增强化学汽相沉积(pecvd)、大气压化学汽相沉积(apcvd)、低压cvd(lpcvd)、高密度等离子体cvd(hdpcvd)或原子层cvd(alcvd)的cmos工艺形成界面层。在一些实施例中,界面层包括多个层。
根据一些实施例,方法900继续在界面层上提供捕获试剂的块912。可以在界面层上提供或结合膜处理或捕获试剂,诸如酶、抗体、配体、肽、核苷酸、器官细胞、生物体或组织片,以用于检测目标分析物。例如,为了检测单链脱氧核糖核酸(ssdna),可以用固定的互补ssdna链功能化界面层。同样,为了检测诸如肿瘤标记物的各种蛋白质,可以用单克隆抗体功能化界面层。捕获试剂可以是分子的自组装单层(sam)的一部分。sam可以具有硅烷基、甲硅烷基、硅烷醇基、膦酸酯基、胺基、硫醇基、烷基、烯基、炔基、叠氮基或环氧基的头基。捕获试剂附接至sam的头基。
在一些实施例中,在给定开口内的所有双栅极背侧fet传感器上方固定相同的捕获试剂。在该实例中,当检测目标分析物时,开口中的每个双栅极背侧fet传感器可以偏置为on,从而收集来自每个双栅极背侧fet传感器的组合电流。集成来自多个双栅极背侧fet传感器的组合信号可以有助于提高相对于目标分析物的传感器阵列的信噪比和灵敏度的之一或两者。在一些实施例中,二维阵列中的每行双栅极背侧fet传感器包括固定在给定行的biofet传感器上方的相同的捕获试剂,但是在不同行之间可以包括不同的捕获试剂。
在一些实施例中,在给定开口内的不同双栅极背侧fet传感器上方固定不同的捕获试剂。在该实例中,可以使用相同的感测阵列检测各种目标分析物。从特定双栅极背侧fet传感器测量的电流将与特定目标分析物的浓度相关,特定目标分析物与固定在特定双栅极背侧fet传感器上方的相应的捕获试剂结合。不同的捕获试剂可以使用液体分配装置设置在相同的开口中的不同的双栅极背侧fet传感器上方,该液体分配装置设计为小心地分配非常少量的液体(例如,小于1nl),以将捕获试剂仅固定在一个或少量的双栅极背侧fet传感器上方。
压电混合器
如上参照图5b讨论的,可以经由一个或多个微流体沟道在布置在传感器阵列中的各个biofet传感器引入流体。使用微流体沟道来引导流体流动也提供了集成其它流体器件(如泵和混合器)的能力。混合器对于增强流体中的分析物和biofet传感器上的捕获分子之间发生的相互作用和反应特别重要。
集成的混合器提供机械力以在流体中引起湍流。湍流提供比单独扩散或对流更高的混合效率。混合作用有助于减小生物反应发生的孵育时间,诸如流体中的分析物和biofet传感器上的捕获分子之间的任何结合反应。
混合器可以沿着芯片上的微流体沟道集成在任何地方。在一些实施例中,可以包括多于一个混合器。图10示出了包括具有入口1006和出口1008的微流体沟道1004的传感器芯片1002的示例性布局。可以通过将沟道模制成诸如聚二甲基硅氧烷(pdms)的聚合物材料,或通过图案化壁(限定位于传感器芯片1002的表面上的沟道)来图案化微流体沟道1004。微流体沟道1004可以具有小于5mm、小于3mm、小于1mm、小于500μm、小于300μm、小于100μm或小于50μm的宽度。
每个入口1006和出口1008均可以通过化学蚀刻、激光钻孔或机械钻孔穿过密封微流体沟道1004的顶部的材料形成。该材料可以是诸如pdms或聚乙二醇的聚合物,或该材料可以是诸如硅或二氧化硅(二氧化硅的实例包括玻璃、石英、熔融石英等)的更刚性的衬底。
根据实施例,微流体沟道1004包括集成泵1010。泵1010可以是任何类型的众所周知的流体泵,诸如蠕动泵、压电泵或电渗泵。
根据实施例,微流体沟道1004包括集成混合器1012。如此处将更详细讨论的,混合器1012可以是压电混合器。混合器1012可以集成在感测区域1014上游的微流体沟道1004(biofet传感器阵列所在的位置)中。因此,可以提供混合器1012以在流体到达任何biofet传感器之前预混合流体。
根据实施例,微流体沟道1004设计为将流体输送至具有至少第一传感器1016a和第二传感器1016b的感测区域1014。在一个实施例中,第一传感器1016a和第二传感器1016b的每个均包括设置在biofet感测表面附近或直接设置在biofet感测表面上方的其自己的集成混合器。这允许直接在生物反应发生的位置发生混合,诸如流体中的分析物和biofet传感器上的捕获分子之间的任何结合反应。传感器1016a和传感器1016b的每个上方的集成混合器均可以是压电混合器。
应当理解,传感器1016a可以表示任何数量的biofet传感器,包括布置在感测阵列中的任何数量的biofet传感器。因此,在实施例中,传感器1016a是在第一感测阵列上方具有其自己的集成混合器的第一传感器阵列,并且传感器1016b是在第二感测阵列上方具有其自己的集成混合器的第二传感器阵列。在另一实施例中,传感器1016a表示第一组biofet传感器,其具有暴露第一组中的每个biofet传感器的背侧的第一共同感测阱,并且传感器1016b表示第二组biofet传感器,其具有暴露第二组中的每个biofet传感器的背侧的第二共同感测阱。第一组的biofet传感器和第二组的biofet传感器可以布置在相同的传感器阵列中,或可以来自不同的传感器阵列。
根据实施例,图11a至图11e中示出了可以集成在微流体沟道1004内的压电混合器1100的示例性制造工艺。图11a示出了混合器的制造中的第一阶段,其中,在衬底1102上形成压电膜堆叠件1101。压电膜堆叠件1101包括第一电极层1104、压电膜1106和第二电极层1108。
衬底1102可以是硅或二氧化硅(二氧化硅的实例包括玻璃、石英、熔融石英等)。在衬底1102是硅的实施例中,在第一电极层1104的形成之前,可以首先在衬底1102上方沉积绝缘层。该绝缘层可以是二氧化硅。
第一电极层1104和第二电极层1108可以是相同的导电材料。列举几个实例,第一电极层1104和第二电极层1108的每个均可以包括铂或金。可以通过诸如例如溅射、蒸发或化学汽相沉积(cvd)的沉积方法来沉积第一电极层1104和第二电极层1108。第一电极层1104和第二电极层1108的每个均可以具有介于约50nm和约500nm之间的厚度。
压电膜1106可以包括具有压电性质的任何材料。当经受施加的电场时,具有压电特性的材料显示出机械应变。在一个实例中,当外部电场施加至材料时,锆钛酸铅(pzt)晶体可以改变其静态尺寸的百分比。由于pzt相对容易沉积至薄层中,显著地表明压电效应,以及它的其低成本,因此pzt可以用于微尺度应用。显示出压电效应并且可以用于压电膜1106的其它示例性材料包括聚偏二氟乙烯(pvdf)和铌酸锂。可以使用例如物理汽相沉积(pvd)或cvd技术来沉积压电膜1106。压电膜1106可以具有介于约100nm和5000nm之间的厚度。
图11b示出了根据实施例的混合器1100的制造工艺中的第二阶段。混合器1100的截面示出了通过一个或多个蚀刻工艺(以蚀刻穿过压电膜堆叠件1101的厚度)形成的多个开口1111。在一个或多个蚀刻工艺期间,各个掩模图案可以用于保护压电膜堆叠件1101的部分,以从自上而下的视角观察时形成不同的混合器图案。根据一些实施例,可以使用利用氩气的离子束蚀刻来蚀刻压电膜堆叠件1101。根据一些实施例,可以使用盐酸蚀刻压电膜堆叠件1101。
根据一些实施例,图11b示出了三个示例性混合器图案(i、ii和iii)。在第一图案i中,在压电膜堆叠件1101的大致方形部分内形成多个开口。在第二图案ii中,在压电膜堆叠件1101的大致圆形部分内形成多个开口。在第三图案iii中,在压电膜堆叠件1101的大致方形部分内形成蛇形开口。应当理解,提供的这些图案仅为实例并且不旨在限制。开口本身可以是任何形状,不限于圆形。类似地,当从自上而下的视角观察时,在一个或多个蚀刻工艺之后,压电膜堆叠件1101的整体形状可以是任何形状,并且不限于圆形或者方形。
根据实施例,另一蚀刻工艺可以用于形成凹槽1110。在蚀刻穿过第二电极层1108和压电膜1106之后,凹槽1110暴露第一电极层1104。由于凹槽1110的存在,电连接可以更容易地提供至第一电极层1104。为了在第一电极层1104和第二电极层1108之间产生电场(在压电膜1106中产生机械应变),必须制成至第一电极层1104和第二电极层1108的每个的电连接。
图11c示出了根据实施例的混合器1100的制造工艺中的第三阶段。实施蚀刻工艺,以通过去除压电膜堆叠件1101下面的衬底1102的部分来释放压电膜堆叠件1101的部分。首先使用光刻胶或硬掩模层保护衬底1102,除了衬底1102上方的图案化的压电膜堆叠件1101之外。之后,实施蚀刻工艺以蚀刻掉开口1111下面的衬底1102的部分。由于蚀刻是各向同性的,该蚀刻也将在横向上在开口1111下面继续,从而使得开口1111之间的衬底1102的部分也被去除。根据实施例,蚀刻的结果示出为腔1112。可以使用湿蚀刻技术或干蚀刻技术来实施“释放”蚀刻。示例性湿蚀刻技术包括当衬底1102是二氧化硅时,将衬底1102暴露于各种可能浓度的氢氟酸以形成腔1112。当衬底1102是二氧化硅时,也可以使用汽化的氢氟酸来形成腔1112。在衬底1102是硅的实例中,使用二氟化氙(xef2)的干式蚀刻工艺可以用于形成腔1112。根据实施例,腔1112的深度介于约100微米和约250微米之间。
在腔1112的形成之后,混合器1100包括经由一个或多个锚固点1114锚固至衬底1102的悬浮压电膜堆叠件1101。图11d示出了以上参照图11b讨论的相同的三个混合器图案(i、ii和iii)的示例性自上而下视图。提供的这些示例性视图再次从自上而下的视角示出腔1112,以及用于每个混合器图案的锚固点1114的示例性位置。
图11e示出了根据实施例的混合器1100的制造工艺中的第四阶段。形成穿过衬底1102的厚度的开口1116以提供流体端口或电端口。电端口可以用于制成与第一电极层1104或者第二电极层1108的电连接。可以使用激光钻孔或使用湿蚀刻剂形成开口1116。例如,氢氧化钾(koh)可以用于蚀刻穿过硅,而氢氟酸可以用于蚀刻穿过二氧化硅。也可以使用诸如深反应离子蚀刻(drie)的干蚀刻工艺。
虽然示出了单个开口1116,但是应当理解,多个开口可以蚀刻穿过衬底1102的厚度以形成一个或多个流体入口和一个或多个流体出口。此外,可以形成一个或多个开口以提供用于制成至第一电极层1104和第二电极层1108的电连接的路径。
图12示出了根据实施例的混合器1100与半导体器件500的示例性集成。在混合器1100的接合之前,可以在界面层516上方图案化沟道壁1202。沟道壁1202可以包括图案化的(如使用uv光的光刻胶)或干蚀刻的介电材料。沟道壁1202可以包括使用uv光图案化的聚合物。
在一些实施例中,首先在界面层516的部分上方沉积接合层,以为沟道壁1202提供更好的接合表面。接合层可以包括与界面层516不同的介电材料,诸如例如二氧化硅。
在已经图案化沟道壁1202之后,混合器1100可以接合在沟道壁1202上方以形成限定微流体沟道的内部体积的封闭流体区域1204。可以使用放置在衬底1102和沟道壁1202之间的粘合剂来实施接合。可以在接合工艺期间施加热和压力以提高接合强度。根据实施例,接合混合器1100,从而使得混合器1100在开口514上方基本对准。
虽然在图12的截面中未示出,但是流体经由穿过衬底1102的开口进入流体区域1204.流体填充流体区域1204,流体区域1204包括在biofet传感器上方图案化的开口514,并且也填充了压电堆叠件1101之上的腔1112。通过施加横跨压电堆叠件1101之上的电极的变化的电场,压电材料将以振荡的方式机械应变,其有效地使压电堆叠件1101上下振动(如双端箭头所示)。振动的频率依赖于施加的电场的交替频率以及压电膜的材料性质。在一个实例中,将电场施加在具有介于约1v和约100v之间的dc偏移的压电堆叠件1101之间,其中ac分量在介于约1khz和约100khz之间的频率下介于约10mv峰到峰值和约1000mv峰到峰值之间。腔1112的存在允许压电堆叠件1101的垂直移动并且将湍流引入至压电堆叠件1101周围的流体。该流体湍流也被开口514周围的流体触及到。因此,由混合器1100引起的湍流可以增加在biofet传感器之上的开口514内发生的生物反应的效率。
应当理解,为了清楚起见,在图12中示出了单个biofet传感器,但是混合器1100也可以以类似的方式集成在多个biofet传感器上方。此外,开口514可以横跨多个biofet传感器的多于一个(如以上参照图7b讨论的),从而使得由混合器1100产生的湍流提高在多个biofet传感器上方发生的生物反应的效率。
在一些实施例中,沟道壁1202由衬底1102的部分替代,从而使得衬底1102直接接合至界面层516。在一些实施例中,可以在将衬底1102接合至界面层516时使混合器1100的组件凹进至衬底1102中以形成封闭流体区域1204。
化学、生物学和界面
现在将参照图13描述作为ph传感器的双栅极背侧fet传感器502的示例性操作。虽然在以下附图中示出的双栅极背侧fet传感器502上方的开口仅位于沟道区域508上方,但是应当理解,开口可以进一步延伸以暴露其它双栅极背侧fet传感器,并且开口的尺寸不改变此处描述的生物感测操作。
简而言之,流体栅极1302用于向双栅极背侧fet传感器502的“背栅极”提供电接触。在双栅极背侧fet传感器502的反应位点上提供溶液1301,并且流体栅极1302放置在溶液1301内。溶液的ph通常与溶液中的氢离子[h+]的浓度有关。在沟道区域508之上的界面层516的表面附近的离子的积聚影响沟道区域508内的反转层的形成,该反转层形成s/d区域510之间的导电路径。在一些实施例中,电流ids从一个s/d区域流至另一个。
可以测量电流ids以确定溶液1301的ph。在一些实施例中,在栅极506保持浮置期间,流体栅极1302用作感测期间的晶体管的栅极。在一些实施例中,当栅极506偏置在给定电位时,流体栅极1302用作感测期间的晶体管的栅极。例如,栅极506可以根据应用偏置在介于-2v和2v之间的电位处,而流体栅极1302在一定范围的电压之间扫描。在一些实施例中,在感测期间,当栅极506用作晶体管的栅极(例如,其电压在一定范围的电位之间扫描)时,流体栅极1302偏置在给定电位处(或接地)。流体栅极1302可以由铂形成,或可以由电化学分析中用于参考电极的任何其它通用的材料形成。参考电极的实例是银/氯化银(ag/agcl)电极,其具有约0.230v的稳定的电位值。
图14a示出了结合到界面层516的表面的溶液中的离子。界面层516的最顶原子层被描绘为各种悬[o-]、[oh]和[oh+]键。当离子积聚在表面上时,总表面电荷影响晶体管的阈值电压。如此处使用的,阈值电压是在fet传感器的源极和漏极之间形成少数载流子的导电路径所需的fet传感器的栅极和源极之间的最小电位。总电荷也直接与溶液的ph有关,因为正电荷的较高积聚意味着较低的ph值,而较高的负电荷积累则意味着较高的ph值。
图14b示出了由于n沟道fet传感器中的不同ph值导致的阈值电压的示例性改变。如在该实施例中可以观察到的,阈值电压增加59mv大致意味着溶液的ph增加1。换句话说,当测量为导通晶体管所需的电压时,一个ph改变导致总表面电荷当量为59mv。
改变双栅极背侧fet传感器502的阈值电压,也改变了形成用于将给定电压输入至流体栅极1302或者栅极506的s/d区域510之间的导电路径所花费的时间。根据一些实施例,“导通”fet传感器的这种时间延迟可以使用数字电路量化并用于确定分析物浓度。
在本发明中描述的装置、系统和方法可以用于监测各种实体之间的相互作用。这些相互作用包括生物和化学反应以检测测试样品中的目标分析物。例如,可以监测包括物理、化学、生物化学或生物转化的反应,以检测中间体、副产物、产物以及它们的组合的产生。此外,本发明的装置、系统和方法可以用于检测此处描述的各种测定中的这些反应,包括但不限于在液体活检中使用的循环肿瘤细胞测定和螯合测定以检测存在的重金属和其它环境污染物。这样的测定和反应可以以单一格式或阵列格式监测,以检测例如多种目标分析物。
参照图15,使用双栅极背侧感测fet传感器502实施示例性生物感测试验。探针dna1504(捕获试剂的实例)经由链接分子1502与界面层516结合。链接分子1502可以具有与界面层516的部分结合的反应性化学基团。链接分子的实例包括硫醇。链接分子也可以通过硅烷化界面层516的表面形成,或者通过将界面层516的表面暴露于氨(nh3)等离子体以在表面上形成反应性nh2基团来形成。如相关领域的技术人员通常所理解的,硅烷化方法涉及将界面层516的表面依次暴露于不同的化学物质,以在界面层516的表面上建立共价结合分子。探针dna1504表示单链dna。图15中示出的双栅极背侧感测fet传感器502是将存在于芯片上的传感器阵列内的一个biofet传感器。
在使fet传感器经受流体样品1501之前,可以将探针dna1504固定在界面层516上。流体样品1501可以包括与其匹配的探针dna1504强烈结合的匹配的单链dna序列1506。额外dna的结合增加了存在于fet传感器的界面层516上和直接在沟道区域508之上的负电荷。
在图16a中概念性地示出了dna结合。这里,具有核酸序列tcga的探针dna与其具有核酸序列agct的互补匹配链结合。任何不匹配的序列都不与探针dna序列杂交。匹配dna的结合增加了在界面层516的界面处建立的负电荷。在图16a示出的实例中,界面层516是氧化铪。
图16b示出了当匹配dna与界面层516的表面结合时双栅极背侧感测fet传感器的阈值电压的偏移。简而言之,可以将电压施加至流体栅极1302直至fet传感器“导通”并且电流在s/d区域510之间流动。在另一实例中,将电压施加至栅极506以导通fet传感器,而流体栅极1302偏置在给定电位处。当由于互补dna结合而在界面层516处存在更多的负电荷时,需要较高的电压以在沟道区域508内形成导电反转层。因此,根据一些实施例,在fet传感器导电和ids电流流动之前,可以将较高的电压施加至流体栅极1302或栅极506。可以测量阈值电压的这种差异,并且这种差异不仅用于确定目标匹配dna序列的存在,还用于确定其浓度。应当理解,界面层516处的净正积聚电荷将导致阈值电压降低而不是增加。此外,与p沟道fet相比,阈值电压的改变对于n沟道fet将具有相反的迹象。
参照图17,使用双栅背侧fet传感器502实施另一示例性生物感测试验。探针抗体1704(捕获试剂的另一实例)通过链接分子1702与界面层516结合。链接分子1702可以具有与界面层516的部分结合的反应性化学基团。可以在探针抗体1704上方提供样品溶液1701,以确定匹配的抗原是否存在于样品溶液1701内。
参考图18,示出了匹配的抗原与探针抗体1704的结合过程。这里,匹配的抗原将与固定的探针抗体结合,而不匹配的抗原将不结合。与上述的dna杂交工艺类似,匹配的抗原将改变在界面层516处存在的积聚电荷。以与以上参照图16b讨论的基本相同的方式测量由于由匹配的抗原与探针抗体结合的积聚电荷引起的阈值电压的偏移。
结束语
本文描述的是包括多个双栅极背侧fet传感器上方的共同开口的biofet器件的实施例。根据一些实施例,biofet器件包括具有第一表面和与第一表面相对、平行的第二表面的半导体衬底以及半导体衬底上的多个biofet传感器。每个biofet传感器均包括形成在半导体衬底的第一表面上的栅极结构以及形成在栅极结构下面的半导体衬底内和半导体衬底中的源极/漏极(s/d)区域之间的沟道区域。沟道区域包括半导体衬底的第二表面的部分。biofet器件还包括设置在半导体衬底的第二表面上的隔离层。隔离层具有位于多个biofet传感器的多于一个biofet传感器的沟道区域上方的开口。biofet器件还包括设置在开口中的多于一个biofet传感器的沟道区域上的界面层。
在上述biofet器件中,还包括多个存取场效应晶体管,所述存取场效应晶体管的每个均包括形成在所述半导体衬底的第一表面上的存取栅极以及形成在所述存取栅极下面的所述半导体衬底内和所述半导体衬底中的源极/漏极区域之间的沟道区域,其中,所述隔离层中的所述开口没有位于任何所述存取场效应晶体管的所述沟道区域上方。
在上述biofet器件中,还包括多个存取场效应晶体管,所述存取场效应晶体管的每个均包括形成在所述半导体衬底的第一表面上的存取栅极以及形成在所述存取栅极下面的所述半导体衬底内和所述半导体衬底中的源极/漏极区域之间的沟道区域,其中,所述隔离层中的所述开口没有位于任何所述存取场效应晶体管的所述沟道区域上方,其中,所述多个生物场效应晶体管传感器的每个的所述源极/漏极区域的一个电连接至所述多个存取场效应晶体管的相应的存取场效应晶体管的所述源极/漏极区域的一个。
在上述biofet器件中,还包括接合在穿过所述隔离层的开口上方的压电混合器。
在上述biofet器件中,其中,每个生物场效应晶体管传感器还包括:第二栅极,形成在所述半导体衬底的第一表面上;以及第二沟道区域,形成在所述第二栅极下面的所述半导体衬底内和所述半导体衬底中的源极/漏极区域之间,其中,邻近于所述第二沟道区域的所述源极/漏极区域的一个与邻近于所述沟道区域的源极/漏极区域的一个是相同的区域。
一种生物场效应晶体管(biofet)器件,包括:半导体衬底,具有第一表面和与所述第一表面相对、平行的第二表面;多个生物场效应晶体管传感器,设置所述半导体衬底上,每个生物场效应晶体管传感器均包括:栅极,形成在所述半导体衬底的第一表面上;和沟道区域,形成在所述栅极下面的所述半导体衬底内和所述半导体衬底中的源极/漏极(s/d)区域之间,其中,所述沟道区域包括所述半导体衬底的第二表面的部分;隔离层,设置在所述半导体衬底的第二表面上,所述隔离层具有位于所述多个生物场效应晶体管传感器的多于一个生物场效应晶体管传感器的所述沟道区域上方的开口;界面层,设置在所述开口中的所述多于一个生物场效应晶体管传感器的所述沟道区域上;以及微流体沟道,位于所述半导体衬底的第二表面上方并且配置为将流体输送至穿过所述隔离层的所述开口内。
在上述生物场效应晶体管器件中,还包括多个存取场效应晶体管,所述存取场效应晶体管的每个均包括形成在所述半导体衬底的第一表面上的存取栅极以及形成在所述存取栅极下面的所述半导体衬底内和所述半导体衬底中的源极/漏极区域之间的沟道区域,其中,所述隔离层中的所述开口没有位于任何所述存取场效应晶体管的所述沟道区域上方。
在上述生物场效应晶体管器件中,其中,所述微流体沟道包括在穿过所述隔离层的所述开口上方对准的压电混合器。
在上述生物场效应晶体管器件中,其中,每个生物场效应晶体管传感器还包括:第二栅极,形成在所述半导体衬底的第一表面上;以及第二沟道区域,形成在所述第二栅极下面的所述半导体衬底内和所述半导体衬底中的源极/漏极区域之间,其中,邻近于所述第二沟道区域的所述源极/漏极区域的一个与邻近于所述沟道区域的源极/漏极区域的一个是相同的区域。
在上述生物场效应晶体管器件中,其中,所述开口具有与x方向对准的最长长度,并且所述微流体沟道配置为在x方向上输送在所述开口上方流动的流体。
根据一些实施例,制造biofet器件的方法包括在半导体衬底的第一表面上形成多个栅极,其中,多个栅极的每个均形成在半导体衬底中的相应的沟道区域上方。该方法还包括在每个沟道区域的两侧上的半导体衬底中形成s/d区域。该方法还包括在半导体衬底的第二表面上的隔离层中形成开口,第二表面与半导体衬底的第一表面相对和平行。衬底中的每个沟道区域均包括半导体衬底的第二表面的部分,并且开口暴露包括多于一个沟道区域的半导体衬底的第二表面的部分。该方法包括在开口内的半导体衬底的第二表面上设置界面层。
在上述方法中,还包括:在所述半导体衬底的第一表面上形成第二多个栅极,所述第二多个栅极的每个均形成在所述半导体衬底中的相应的第二沟道区域上方;以及在每个所述第二沟道区域的两侧上的半导体衬底中形成源极/漏极区域,其中,形成所述隔离层中的所述开口没有暴露任何所述第二沟道区域。
在上述方法中,还包括:在所述半导体衬底的第一表面上形成第二多个栅极,所述第二多个栅极的每个均形成在所述半导体衬底中的相应的第二沟道区域上方;以及在每个所述第二沟道区域的两侧上的半导体衬底中形成源极/漏极区域,其中,形成所述隔离层中的所述开口没有暴露任何所述第二沟道区域,还包括:将至少一个沟道区域的一侧上的源极/漏极区域与相应的第二沟道区域的一侧上的源极/漏极区域电连接。
在上述方法中,还包括:将压电混合器接合在穿过所述隔离层的开口上方。
在上述方法中,其中,在所述隔离层中形成所述开口包括:实施干蚀刻以减小所述隔离层的暴露区域的厚度;以及在实施所述干蚀刻之后,实施湿蚀刻以去除所述暴露区域内的所述隔离层的剩余部分。
一种制造生物场效应晶体管器件的方法,所述方法包括:在半导体衬底的第一表面上形成多个栅极,所述多个栅极的每个均形成在所述半导体衬底中的相应的沟道区域上方;在每个所述沟道区域的两侧上的所述半导体衬底中形成源极/漏极(s/d)区域;在所述半导体衬底的第二表面上的隔离层中形成开口,所述第二表面与所述半导体衬底的第一表面相对和平行,其中,所述沟道区域的每个均包括所述半导体衬底的第二表面的部分,并且其中,所述开口暴露包括多于一个沟道区域的所述半导体衬底的第二表面的部分;在所述开口内的所述半导体衬底的第二表面上设置界面层;以及将微流体沟道连接在所述半导体衬底的第二表面上方,从而经由所述微流体沟道将流体输送至所述隔离层中的开口内。
在上述方法中,还包括:在所述半导体衬底的第一表面上形成第二多个栅极,所述第二多个栅极的每个均形成在所述半导体衬底中的相应的第二沟道区域上方;以及在每个所述第二沟道区域的两侧上的半导体衬底中形成源极/漏极区域,其中,形成所述隔离层中的所述开口没有暴露任何所述第二沟道区域。
在上述方法中,其中,连接包括连接所述微流体沟道,从而使得设置在所述微流体沟道内的压电混合器在穿过所述隔离层的所述开口上方对准。
在上述方法中,其中,所述开口具有与x方向对准的最长长度,并且所述微流体沟道配置为在x方向上输送在所述开口上方流动的流体。
在上述方法中,其中,在所述隔离层中形成所述开口包括:实施干蚀刻以减小所述隔离层的暴露区域的厚度;以及在实施所述干蚀刻之后,实施湿蚀刻以去除所述暴露区域内的所述隔离层的剩余部分。
根据一些实施例,传感器阵列包括具有第一表面和与第一表面相对、平行的第二表面的半导体衬底以及在半导体衬底上以行和列的矩阵布置的多个biofet传感器。每个biofet传感器均包括形成在半导体衬底的第一表面上的栅极以及形成在栅极下面的半导体衬底内和半导体衬底中的s/d区域之间的沟道区域。沟道区域包括半导体衬底的第二表面的部分。传感器阵列还包括隔离层,该隔离层设置在半导体衬底的第二表面上并且具有沿着行矩阵的至少一行的长度延伸的开口,从而使得开口位于至少一行中的多个biofet传感器的多于一个biofet传感器的沟道区域上方。传感器阵列还包括设置在开口内的半导体衬底的第二表面上的界面层。
在上述传感器阵列中,还包括多个存取场效应晶体管,所述存取场效应晶体管的每个均包括形成在所述半导体衬底的第一表面上的存取栅极以及形成在所述存取栅极下面的所述半导体衬底内和所述半导体衬底中的源极/漏极区域之间的沟道区域,其中,所述隔离层中的所述开口没有位于任何所述存取场效应晶体管的所述沟道区域上方。
在上述传感器阵列中,还包括多个存取场效应晶体管,所述存取场效应晶体管的每个均包括形成在所述半导体衬底的第一表面上的存取栅极以及形成在所述存取栅极下面的所述半导体衬底内和所述半导体衬底中的源极/漏极区域之间的沟道区域,其中,所述隔离层中的所述开口没有位于任何所述存取场效应晶体管的所述沟道区域上方,其中,所述多个生物场效应晶体管传感器的每个的所述源极/漏极区域的一个电连接至所述多个存取场效应晶体管的相应的存取场效应晶体管的所述源极/漏极区域的一个。
在上述传感器阵列中,还包括多个存取场效应晶体管,所述存取场效应晶体管的每个均包括形成在所述半导体衬底的第一表面上的存取栅极以及形成在所述存取栅极下面的所述半导体衬底内和所述半导体衬底中的源极/漏极区域之间的沟道区域,其中,所述隔离层中的所述开口没有位于任何所述存取场效应晶体管的所述沟道区域上方,其中,所述多个生物场效应晶体管传感器的每个的所述源极/漏极区域的一个电连接至所述多个存取场效应晶体管的相应的存取场效应晶体管的所述源极/漏极区域的一个,其中,所述相应的存取场效应晶体管布置在所述半导体衬底上以邻近于至少一个生物场效应晶体管传感器。
在上述传感器阵列中,还包括接合在穿过所述隔离层的所述开口上方的压电混合器。
一种传感器阵列,包括:半导体衬底,具有第一表面和与所述第一表面相对、平行的第二表面;多个生物场效应晶体管传感器,在所述半导体衬底上以行和列的矩阵布置,每个生物场效应晶体管传感器均包括:栅极,形成在所述半导体衬底的第一表面上;和沟道区域,形成在所述栅极下面的所述半导体衬底内和所述半导体衬底中的源极/漏极(s/d)区域之间,其中,所述沟道区域包括半导体衬底的所述第二表面的部分;隔离层,设置在所述半导体衬底的第二表面上,所述隔离层具有沿着行矩阵的至少一行的长度延伸的开口,从而使得所述开口位于至少一行中的所述多个生物场效应晶体管传感器的多于一个生物场效应晶体管传感器的所述沟道区域上方;界面层,设置在所述开口内的所述半导体衬底的第二表面上;以及微流体沟道,位于所述半导体衬底的第二表面上并且配置为将流体输送至所述隔离层中的所述开口内。
在上述传感器阵列中,还包括多个存取场效应晶体管,所述存取场效应晶体管的每个均包括形成在所述半导体衬底的第一表面上的存取栅极以及形成在所述存取栅极下面的所述半导体衬底内和所述半导体衬底中的源极/漏极区域之间的沟道区域,其中,所述隔离层中的所述开口没有位于任何所述存取场效应晶体管的所述沟道区域上方。
在上述传感器阵列中,还包括接合在穿过所述隔离层的所述开口上方的压电混合器。
在上述传感器阵列中,其中,所述开口具有与x方向对准的最长长度,并且所述微流体沟道配置为在x方向上输送在所述开口上方流动的流体。
在上述传感器阵列中,其中,所述开口沿着y方向具有跨度,从而使得所述开口位于一个或多个其它行的所述多个生物场效应晶体管传感器的多于一个生物场效应晶体管传感器的所述沟道区域上方。
应当理解,详细描述部分,而不是公开部分的摘要,旨在用于解释权利要求。公开部分的摘要可以阐述发明人所设想的本发明的一个或多个但不是全部的示例性实施例,并且因此,不旨在以任何方式限制本发明和所附权利要求。
应当理解,本文中的措辞或术语是为了描述的目的而不是限制,从而使得本说明书的术语或措辞将由本领域技术人员根据教导和指导来解释。
本发明的宽度和范围不应受任何上述示例性实施例的限制,而应根据所附权利要求及其等同物来限定。
- 还没有人留言评论。精彩留言会获得点赞!