检测促红细胞生成素受体的放射性探针、制备方法及应用与流程
本发明涉及放射性药物化学和临床核医学技术领域,具体地,涉及一种检测促红细胞生成素受体的放射性探针、制备方法及应用。
背景技术:
促红细胞生成素(erythropoietin,epo)及其受体(erythropoietinreceptor,epor)是促进哺乳动物红系祖细胞增值和分化的主要细胞因子。对于epor,以往的研究认为epor仅存在于早期红系细胞中,而近年来大量研究发现,在很多非造血组织和细胞中,如神经系统、心血管系统、内皮细胞、胰腺、肺、肝脏、肾脏、子宫、实质瘤等也有epor的表达。对于epor在非造血组织和细胞中的功能和作用机制的研究是近来的研究热点。
近年来,多种研究表明epo和epor在多种正常非造血组织和恶性肿瘤组织中表达,并在肿瘤的发生发展过程中可能起着重要的作用。研究报道了epo转录体和蛋白在多种肿瘤中的表达,其中epo主要由肿瘤细胞表达,epor则在肿瘤细胞及血管内皮细胞中表达。yasuda等的研究中包括恶性胶质瘤、肺癌、乳腺癌、黑素瘤、胃癌、前列腺癌、胰腺癌、绒毛腺癌、肝癌、白血病等24种恶性肿瘤细胞中均表达epo和epor。膀胱移行细胞癌中也被证实有epo/epor的表达,且其表达强度随着组织学分级的升高而增强。papworth等发现,肾癌中有epo和epor的表达,且两者具有相关性。同时指出,肿瘤组织中epo和epor的表达与血清中epo水平无相关性。giatromanolaki等发现子宫内膜癌中有epor表达,并且与缺氧诱导因子(hypoxia-induciblefactor,hif)1α及血管内皮生长因子的表达有关。kuster等则在脑膜瘤细胞的表面发现有epor的表达,并且其低水平的表达可以作为脑膜瘤复发的指标之一。另外还有一些研究发现,epor与肿瘤血管的形成有着密切的关系。在食管癌、大肠癌组织中均有epor的表达,且表达强度随着epor的增加而增加。因此,检测epor在医学领域有广泛的用途和重要的临床应用价值。
目前,epor的检测因为缺少具有高灵敏性和选择性的epor抗体,所以在肿瘤细胞和肿瘤组织内很难被检测,尤其是缺乏可以同时应用于体内和体外检测的探针。近红外荧光探针epo-cy5.5利用近红外荧光染料cy5.5与重组人红细胞生成素(recombinanthumanerythropoietin,rhuepo)连接,并用于肿瘤模型鼠体内的epor的检测。现在阶段可以利用放射性核素125i和111in标记的放射性探针进行检测。然而,对于近红外荧光染料标记技术,由于近红外荧光应用的局限性,只能用于裸鼠的检测,而难以应用到其他动物和人体上。125i标记的125i-rhuepo已有出售,但是它只能用γ计数器和γ相机检测,常用于体外实验的研究,在活体成像方面成像效果较差。111in核素在国内无供应,所以111in标记的放射性探针在国内无法使用。
技术实现要素:
有鉴于此,本发明提供一种放射性探针,是由放射性锝99mtc标记重组人红细胞生成素rhuepo形成的放射性探针(以下有时仅称作99mtc-rhuep),该探针能够在人体或动物体体内和或体外检测epor的表达,且在动物或人体的体内或体外成像清晰,可以作为临床诊断或进一步研究使用。
为解决上述技术问题,本发明采用了以下技术方案:
根据本发明第一方面实施例的放射性探针,所述放射性探针为99mtc-rhuepo。
根据本发明第二方面实施例的放射性探针99mtc-rhuepo的制备方法,将锝化合物和重组人红细胞生成素rhuepo经过亚锡还原法制备得到所述放射性探针99mtc-rhuepo。
进一步地,包括如下步骤:
步骤s1,提供锝化合物溶液和重组人红细胞生成素rhuepo;
步骤s2,将所述重组人红细胞生成素rhuepo溶于缓冲溶液中,在其中加入亚锡还原剂溶液和所述锝化合物溶液,经化学反应合成所述放射性探针99mtc-rhuepo。
优选地,所述锝化合物溶液为na99mtco4的生理盐水溶液。
优选地,所述锝化合物溶液中的放射性活度为2~20mci。
优选地,所述重组人红细胞生成素:所述锝化合物溶液的比为(2~5μg):(50~200μl)。
优选地,所述亚锡还原剂溶液选用氯化亚锡溶液,所述氯化亚锡溶液的浓度为0.075mol/l。
优选地,所述锝化合物溶液:所述氯化亚锡溶液的体积比为(50~200μl):(5~8μl)。
优选地,所述步骤s2中,加入亚锡还原剂溶液和所述锝化合物溶液后,在室温下震荡10~20分钟以进行所述化学反应。
根据本发明第三方面实施例的放射性探针99mtc-rhuepo在检测促红细胞生成素受体方面的应用。
本发明的上述技术方案至少具有如下效果之一:
(1)探针的制备方法简单;
(2)通过该探针可以特异性的检测epor的表达,并且可以在动物体内产生清晰的全身epor显像的图像;
(3)可以作为科学技术研究的基础或临床诊断使用。
附图说明
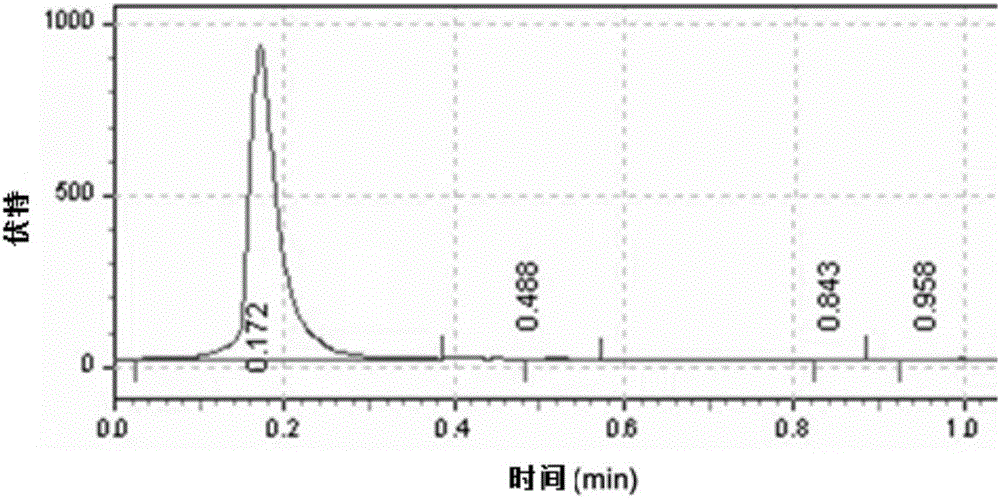
图1为本发明实施例的99mtc-rhuepo制备方法制得的99mtc-rhuepo的放射化学纯度;
图2为本发明的实验4中在加入放射性药物99mtc-rhuepo时加入不同量未标记的rhuepo使细胞中的epor得到抑制后检测h1975细胞中epor的表达的效果图;
图3为大鼠在注射根据本发明实施例的放射性探针99mtc-rhuepo后1,2,4,6小时后各组织器官中epor表达的spect显像。
具体实施方式
为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例的附图,对本发明实施例的技术方案进行清楚、完整地描述。显然,所描述的实施例是本发明的一部分实施例,而不是全部的实施例。基于所描述的本发明的实施例,本领域普通技术人员所获得的所有其他实施例,都属于本发明保护的范围。
根据本发明实施例的放射性锝99mtc标记的重组人红细胞生成素rhuepo,即放射性探针99mtc-rhuepo,该放射性探针99mtc-rhuepo能够在哺乳动物体内或体外检测epor的表达,并且能够在哺乳动物体内产生清晰的全身epor显像的图像,为科学技术的研究和临床诊断提供了坚实的基础。
下面首先具体描述根据本发明第一方面实施例的放射性探针,其是放射性锝99mtc标记的重组人红细胞生成素rhuepo,以下仅记作99mtc-rhuepo。
重组人红细胞生成素rhuepo,能够作为一种新细胞保护剂,其与红系祖细胞的表面受体结合,促进红系细胞生长和分化,促进红母细胞成熟,增多红细胞数和血红蛋白含量;稳定红细胞膜,提高红细胞膜抗氧化酶功能,能有效纠正心衰患者的贫血,改善心脏功能,抑制细胞凋亡。
放射性元素是指能够自发地从不稳定原子核内部放出粒子或射线,如α粒子、β射线、γ射线等,同时释放出能量,最终形成稳定核素的一类元素,本发明选用放射性元素锝锝来标记重组人红细胞生成素rhuepo。
根据本发明实施例的放射性探针99mtc-rhuepo,能够检测epor的表达,并且可以在动物体内产生清晰的全身epor显像的图像,能够用于检测促红细胞生成素受体。
根据本发明第二方面实施例的放射性探针99mtc-rhuepo的制备方法,将锝化合物和重组人红细胞生成素rhuepo经过亚锡还原法制备得到所述放射性探针99mtc-rhuepo。
亚锡还原法是利用亚锡还原剂将高价态的锝离子还原成低价态的锝离子,从而使低价态的锝与重组人红细胞生成素结合形成放射性探针99mtc-rhuepo。
具体地,放射性探针99mtc-rhuepo的制备方法包括以下步骤:
步骤s1,提供放射性元素锝化合物和重组人红细胞生成素rhuepo。
步骤s2,将所述重组人红细胞生成素溶于缓冲溶液中,加入亚锡还原剂溶液和锝化合物溶液形成混合液,所述混合液经过化学反应合成放射性探针99mtc-rhuepo溶液样品。
其中,缓冲溶液指的是由弱酸及其盐、弱碱及其盐组成的混合溶液,能在一定程度上抵消、减轻外加强酸或强碱对溶液酸碱度的影响,从而保持溶液的ph值相对稳定,常用作缓冲溶液的酸类。由弱酸及其共轭酸盐组合成的溶液具有缓冲作用。常见的缓冲体系有:弱酸和它的盐,如:hac、naac,弱碱和它的盐,如:nh3·h2o、nh4cl,多元弱酸的酸式盐及其对应的次级盐,如:nah2po4、na2hpo4的水溶液组成。
锝化合物可以是na99mtco4或k99mtco4等化合物,本发明理想的锝化合物选用na99mtco4,成本相对较低。亚锡还原剂包括氟化亚锡、氯化亚锡和酒石酸亚锡等。亚锡还原剂在酸性介质中产生新和态氢,具有较强还原作用,本发明优选的选用氯化亚锡作为亚锡还原剂,通过氯化亚锡在酸性介质中具有较强的还原性将na99mtco4中的+7价的tc7+还原成+1,+3,+4和+5价锝离子并与含o,n,s,p等供体原子的化合物反应制成放射性探针。
锝化合物溶液的溶剂优选为生理盐水,即为锝化合物的生理盐水溶液,且锝化合物溶液中的放射性活度为2~20mci。进一步地,加入重组人红细胞生成素的质量在2~5μg之间,加入的氯化亚锡溶液的浓度为0.075mol/l,体积为5~8μl之间,加入的锝化合物溶液的体积为50~200μl。根据上述使用范围的量能够保证99mtc-rhuepo的放射化学纯度大于95%。
需要说明的是,上述用量及其比例只是一种示例性的说明,根据所要形成的样品溶液的多少、反应条件等可以进行适当调整。
优选地,步骤s2中的混合液在室温下震荡10~20分钟,混合液中的化合物经过化学反应合成得到放射性探针99mtc-rhuepo样品溶液,该放射性探针99mtc-rhuepo纯度较高,可通过纸层析法或者放射性高效液相色谱分析其放射化学纯度。
本发明第三方面实施例的放射性探针99mtc-rhuepo在检测促红细胞生成素受体方面的应用,例如,在动物体内或体外检测促红细胞生成素受体的表达,可以包括以下步骤:
步骤1,首先获得第一方面实施例的放射性探针99mtc-rhuepo的样品溶液或获取第二方面实施例的放射性探针99mtc-rhuepo制备方法制备的放射性探针99mtc-rhuepo的样品溶液。
步骤2,对放射性探针99mtc-rhuepo样品溶液进行稀释,将体内或体外的细胞或组织器官与稀释后的所述放射性探针99mtc-rhuepo样品溶液进行孵育、或在活体动物体内静脉注射稀释后的所述放射性探针99mtc-rhuepo样品溶液以使所述体内或体外的细胞或组织器官摄取放射性探针99mtc-rhuepo。
其中,稀释液可选为磷酸盐缓冲液(pbs)或生理盐水。
本发明的体内或体外均指哺乳动物的体内或体外,细胞包括肿瘤细胞及血管内皮细胞等,器官包括心脏、血液、肝脏、脾、肾、肺、胃、小肠、大脑、骨、肌肉、肿瘤等。
静脉注射是指用注射器将药液注入动物体的静脉中,通过静脉注射的方法使药液快速被动物体内的细胞或组织器官所吸收。
步骤3,通过计数器检测所述体内或体外的细胞或组织器官内所含探针的数量。
计数器用于检测各器官和细胞中摄取放射性探针99mtc-rhuepo的数量。由于放射性探针99mtc-rhuepo是与epor特异性结合的,因此在器官中或细胞中放射性探针99mtc-rhuepo的量就代表了epor的量。即器官和细胞中摄取放射性探针99mtc-rhuepo的数量为epor在该器官或细胞中表达的量。
优选地,本发明理想的孵育条件为37℃二氧化碳的培养箱中孵育30min~1h。
下面结合具体实验对本发明的放射性药物99mtc-rhuepo的制备方法进一步理解。
实验1:制备放射性探针99mtc-rhuepo
本发明的化学试剂均向美国sigma-aldrich公司购买(st.louis,usa)。h1975细胞从派克生物公司购买;人从红细胞生成素(rhuepo)从mdbioproducts公司购买(md,usa);钼锝发生器购于原子高科股份公司。
取2μgrhuepo溶于磷酸盐缓冲溶液中,加入5μl的0.075mol/l的氯化亚锡溶液和50μl的na99mtco4溶液以形成混合液,其中,na99mtco4溶液中放射性活度为10mci,将混合液在室温下震荡10min得到放射性探针99mtc-rhuepo的样品溶液。
将上述样品溶液经过放射性高效液相色谱分析其放射化学纯度,其纯度>90%,(详见附图1)。
下面结合具体实验对本发明的放射性药物99mtc-rhuepo在检测促红细胞生成素受体方面的应用进一步理解。
实验2:体外检测肿瘤细胞中epor表达
取实验1中的摄取放射性探针99mtc-rhuepo样品溶液用pbs溶液稀释,将肿瘤细胞种植于6孔板中,在每个孔中加入150kbq活度稀释后的放射性探针99mtc-rhuepo溶液,再将装有肿瘤细胞和放射性探针99mtc-rhuepo溶液的6孔板置于37℃的二氧化碳培养箱中孵育30min,取出后用pbs溶液冲洗肿瘤细胞,洗脱肿瘤细胞,使用γ计数器检测肿瘤细胞摄取的放射性探针99mtc-rhuepo的数量,即为epor在该肿瘤细胞中表达的量。
实验3:体外检测大鼠体内各器官中epor的表达
取实验1中的放射性探针99mtc-rhuepo样品溶液用生理盐水进行稀释,选择大鼠作为受试动物,将大鼠分成四组,按照每只大鼠0.5mci,体积0.2ml的量从大鼠的尾部静脉注射稀释后的放射性探针99mtc-rhuepo溶液。根据不同组的划分,分别将大鼠在1、2、4和6小时后处死大鼠,并进行解剖,取出各器官,称重,用γ计数器检测各器官摄取放射性探针99mtc-rhuepo的数量,在计算出每克组织摄取探针的数量占注射剂量的百分数(%id/g),详见表1。
表1为注射后1,2,4,6小时后大鼠主要器官摄取探针99mtc-rhuepo的值
从表1中可以看出,在造血相关器官,尤其是骨骼中的epor表达最高。
实验4:体外检测肿瘤模型鼠中各器官和肿瘤中epor的表达
取实验1中的放射性探针99mtc-rhuepo样品溶液用生理盐水进行稀释,选取6只雄性无胸腺的裸鼠肩背皮下种植h1975细胞,生长2至3周,体积在400mm3左右时进行实验。按照每只模型鼠0.3mci,体积0.15ml的量从模型鼠的尾静脉注射稀释后的放射性探针99mtc-rhuepo溶液。并在2小时后处死大鼠,解剖,取出各器官,称重,用γ计数器检测各器官摄取放射性探针99mtc-rhuepo的数量,在计算出每克组织器官摄取探针的数量占注射剂量的百分数(%id/g),详见表2。
表2为模型鼠在注射2小时后主要器官及肿瘤摄取99mtc-rhuepo的值
从表2中可以看出,除了造血相关器官,肿瘤内有较高的epor表达。
同时另一组实验中,在加入放射性药物99mtc-rhuepo时加入不同量未标记的rhuepo使细胞中的epor得到抑制后检测h1975细胞中epor的表达,从图2上可以看出,加入未标记的rhuepo越多,抑制细胞中的epor被抑制越多,99mtc-rhuepo在细胞中的摄取越少,表明99mtc-rhuepo具有与细胞中的epor特异性结合的特性。
实验5:在大鼠体内进行epor表达的显像方法
将大鼠麻醉,按照每只大鼠1mci,体积1ml的量从大鼠的尾静脉注射放射性探针99mtc-rhuepo。然后将大鼠放置于spect仪器上,分别对注射1,2,4,6小时后的大鼠进行静态显像,观察大鼠体内各组织器官epor的生物分布,如图3所示,显像图中能够看出99mtc-rhuepo主要被造血相关器官中摄取,符合epor在体内的分布趋势,99mtc-rhuepo能够用于活体全身显像,且成像清晰。
以上所述是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明所述原理的前提下,还可以作出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!