基于硼酸亲和作用的传感器及其制备方法和应用与流程
本发明涉及电化学传感器,具体地,涉及一种基于硼酸亲和作用的传感器及其制备方法和应用。
背景技术
分子识别:分子识别过程是指分子在特定的条件下通过分子间作用力的协同作用达到相互结合的过程。类似“钥匙与锁”的关系,形象的描述了分子与分子之间结合的专一性。发展至今,分子识别可以简化的表述为主体对客体选择性结合并产生某种特定功能的过程。生物体内的分子识别通常发生在抗体与抗原,酶与底物,激素与受体之间。以此为平台,酶模拟、药物分析和仿生传感等技术得到了迅速的发展。
肾上腺是人体重要的内分泌器官,其实质由中央部的髓质和周围部的皮质组成。两个部分属内分泌腺,分泌多种激素,维持人体正常生命活动的需要。肾上腺可由于增生、肿瘤或其他疾病导致激素分泌异常,出现相应的肾上腺功能亢进或减退。临床常见肾上腺疾病包括库欣综合征、原发性醛固酮增多症、嗜铬细胞瘤、肾上腺皮质功能减退症等。肾上腺疾病相关激素检测结果是临床诊断最主要的指标之一。因此,建立一种快速灵敏的检测方法十分必要。目前,检测肾上腺素的方法有多种,但操作较为繁琐,仪器较为昂贵。而电化学传感器由于具有快速、灵敏、简便等优点,而且选择性好、易于制作,因此检测肾上腺素的电化学传感器的研究也日益增多。
因此,如何提供一种具备抗干扰能力强、灵敏度高且制备简单、成本低、性能稳定等优点的电化学传感器是目前亟待解决的问题。
技术实现要素:
本发明的目的是提供一种基于硼酸亲和作用的传感器及其制备方法和应用,本发明构建的电化学传感器为双识别电化学传感器,可以实现对肾上腺素的快速灵敏检测,具备抗干扰能力强、灵敏度高且制备简单、成本低、性能稳定等优点。且该传感器的制备方法简单,采用电化学洗脱,即可将分子印迹聚合物中肾上腺素模板的去除,解决了模板分子去除难的问题,具有较高的推广价值。
为了实现上述目的,本发明提供了一种基于硼酸亲和作用的传感器的制备方法,所述方法包括:(1)将3-噻吩硼酸、肾上腺素和缓冲溶液混合,形成预聚合液;(2)将玻碳电极浸入预聚合液中,采用循环伏安法电聚合得到聚合物膜修饰电极;(3)将聚合物膜修饰电极浸在酸液中,采用循环伏安法循环扫描多次,洗脱肾上腺素。
本发明还提供了一种根据前文所述的制备方法制备得到的基于硼酸亲和作用的传感器。
不仅如此,本发明还提供了一种应用前文所述的基于硼酸亲和作用的传感器检测肾上腺素的方法。
通过上述技术方案,本发明引入了一种新的功能单体3-噻吩硼酸(3-tba),用于制备分子印迹聚合物膜,拓展了功能单体的种类。在上述技术方案中,本发明在玻碳电极上电聚合一层以3-噻吩硼酸作为新的功能单体的分子印迹聚合物膜,结合肾上腺素留下的分子印迹,能够实现对肾上腺素的双识别,可以实现对肾上腺素的快速灵敏检测,具备抗干扰能力强、灵敏度高且制备简单、成本低、性能稳定等优点。且该传感器的制备方法简单,采用电化学洗脱,即可将分子印迹聚合物中肾上腺素模板的去除,解决了模板分子去除难的问题,具有较高的推广价值。
本发明的其他特征和优点将在随后的具体实施方式部分予以详细说明。
附图说明
附图是用来提供对本发明的进一步理解,并且构成说明书的一部分,与下面的具体实施方式一起用于解释本发明,但并不构成对本发明的限制。在附图中:
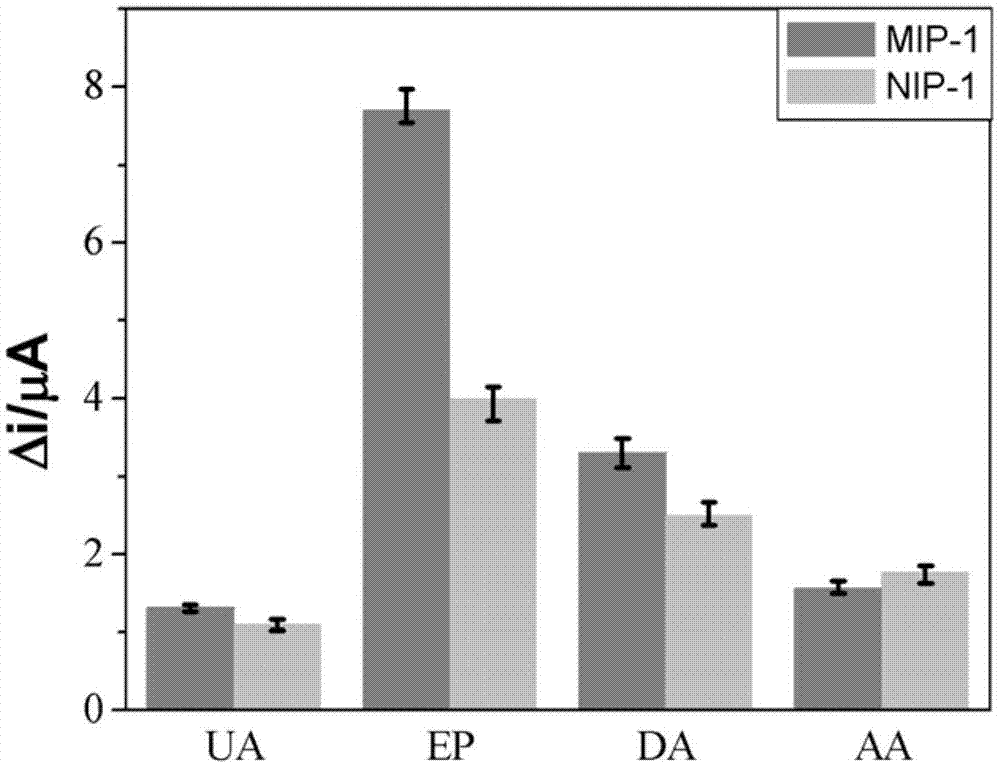
图1是应用例1中mip-1和nip-1的差示脉冲电流响应图;
图2是应用例1中mip-2和nip-2的差示脉冲电流响应图;
图3是应用例1中3-噻吩硼酸中的噻吩基团与具有邻羟基的ep的亲和作用机理。
具体实施方式
以下对本发明的具体实施方式进行详细说明。应当理解的是,此处所描述的具体实施方式仅用于说明和解释本发明,并不用于限制本发明。
在本文中所披露的范围的端点和任何值都不限于该精确的范围或值,这些范围或值应当理解为包含接近这些范围或值的值。对于数值范围来说,各个范围的端点值之间、各个范围的端点值和单独的点值之间,以及单独的点值之间可以彼此组合而得到一个或多个新的数值范围,这些数值范围应被视为在本文中具体公开。
本发明提供了一种基于硼酸亲和作用的传感器的制备方法,所述方法包括:(1)将3-噻吩硼酸、肾上腺素和缓冲溶液混合,形成预聚合液;(2)将玻碳电极浸入预聚合液中,采用循环伏安法电聚合得到聚合物膜修饰电极;(3)将聚合物膜修饰电极浸在酸液中,采用循环伏安法循环扫描多次,洗脱肾上腺素。
通过上述技术方案,本发明引入了一种新的功能单体3-噻吩硼酸(3-tba),用于制备分子印迹聚合物膜,拓展了功能单体的种类。通过在玻碳电极上电聚合一层以3-噻吩硼酸作为新的功能单体的分子印迹聚合物膜,结合肾上腺素留下的分子印迹,能够实现对肾上腺素的双识别,可以实现对肾上腺素的快速灵敏检测,具备抗干扰能力强、灵敏度高且制备简单、成本低、性能稳定等优点。且该传感器的制备方法简单,采用电化学洗脱,即可将分子印迹聚合物中肾上腺素模板的去除,解决了模板分子去除难的问题,具有较高的推广价值。
在上述技术方案中,对于3-噻吩硼酸和肾上腺素的摩尔比,本领域技术人员可灵活调整。为了提高传感器对肾上腺素的快速灵敏检测及抗干扰能力,另一方面利于肾上腺素作为模板的洗脱,优选地,3-噻吩硼酸和肾上腺素的摩尔比为3-5:1。
在本发明一个更优选的实施方式中,为了提高传感器对肾上腺素的快速灵敏检测及抗干扰能力,另一方面利于肾上腺素作为模板的洗脱,进一步优选地,预聚合液中肾上腺素的浓度为0.8-1.5mmol/l。
在本发明一个更优选的实施方式中,为了提高传感器对肾上腺素的快速灵敏检测及抗干扰能力,优选地,步骤(1)中的缓冲溶液的ph为4-8。
在上述技术方案中,对于缓冲溶液的种类,本领域技术人员可灵活选择,只要溶液的ph符合要求即可。为了提高传感器对肾上腺素的快速灵敏检测及抗干扰能力,优选地,缓冲溶液选自磷酸盐缓冲溶液、醋酸盐缓冲溶液、三羟甲基氨基甲烷盐酸盐缓冲溶液和碳酸氢二钠-柠檬酸缓冲溶液中的一种或多种。
在本发明一种更优选的实施方式中,为了提高传感器对肾上腺素的快速灵敏检测及抗干扰能力,进一步优选地,缓冲溶液为磷酸盐缓冲溶液。
其中,对于磷酸盐缓冲溶液的浓度,本领域技术人员可灵活调整,只要能够得到上述ph的磷酸盐缓冲溶液即可。在本发明一种更优选的实施方式中,为了提高传感器对肾上腺素的快速灵敏检测及抗干扰能力,进一步优选地,磷酸盐缓冲溶液的浓度为0.08-0.12mol/l。
其中,对于步骤(2)中循环伏安法的电位范围,本领域技术人员可在较宽范围内进行选择,均能够得到本发明的传感器。为了提高传感器对肾上腺素的快速灵敏检测及抗干扰能力,另一方面,利于肾上腺素模板的洗脱,优选地,步骤(2)中循环伏安法的电位范围为-0.2v~1.2v。
当然,对于循环伏安法的聚合圈数,本领域技术人员可在较宽范围内进行选择,均能够得到本发明的传感器。为了提高传感器对肾上腺素的快速灵敏检测及抗干扰能力,另一方面,利于肾上腺素模板的洗脱,优选地,聚合圈数为:10~30圈。
其中,对于步骤(3)中循环伏安法的电位范围,本领域技术人员可在较宽范围内进行选择,均能够得到本发明的传感器。为了利于肾上腺素模板的洗脱,优选地,步骤(3)中循环伏安法的电位范围为0-1.5v。
当然,对于扫描圈数,本领域技术人员可在较宽范围内进行选择,均能够得到本发明的传感器。为了提高传感器对肾上腺素的快速灵敏检测及抗干扰能力,另一方面,利于肾上腺素模板的洗脱,优选地,扫描圈数为:15-25圈。
对于步骤(3)中的酸液种类,本领域技术人员可较宽范围内进行选择,例如常见的盐酸、硫酸溶液、硝酸溶液、醋酸溶液等。在本发明一种优选的实施方式中,为了提高传感器对肾上腺素的快速灵敏检测及抗干扰能力,另一方面,利于肾上腺素模板的洗脱,优选地,步骤(3)中的酸液为盐酸、硫酸溶液和硝酸溶液中的一种或多种。
而对于酸液中的氢离子的浓度,本领域技术人员可灵活调整,为了提高传感器对肾上腺素的快速灵敏检测及抗干扰能力,另一方面,利于肾上腺素模板的洗脱,优选地,酸液中氢离子的浓度为0.03-0.08mol/l。
在本发明中,对于玻碳电极,本领域技术人员可选择未被修饰的玻碳电极和被修饰的玻碳电极,进一步地,为了提高传感器对肾上腺素的快速灵敏检测及抗干扰能力,所述玻碳电极可选择为被碳纳米粒子修饰的玻碳电极以及被金纳米粒子修饰的玻碳电极。
其中,在本发明一种更优选的实施方式中,为了提高电极的增敏的作用,进而提高传感器对肾上腺素的快速灵敏检测及抗干扰能力,进一步优选地,玻碳电极为被金纳米粒子修饰的玻碳电极。其中,被金纳米粒子修饰的玻碳电极,现有技术中多有报道,例如,公开(公告)号为cn104614527a、cn106093171a、cn103940874a。
为了在保证金纳米粒子对玻碳电极增敏基础上,提高被金纳米粒子修饰的玻碳电极的制备效率,在本发明一种更优选的实施方式中,所述被金纳米粒子修饰的玻碳电极通过以下方法制备得到:用i-t法(电化学安培法)将未被修饰的玻碳电极置于haucl4溶液中,于-0.1v~-0.3v电化学沉积金100-600s。
其中,对于haucl4溶液中haucl4的浓度,本领域技术人员可在较宽范围内进行选择,为了提高被金纳米粒子修饰的玻碳电极的制备效率,优选地,haucl4的浓度为3-5mmol/l。
在前述的技术方案中,需要在反应前保证玻碳电极洁净,处理方式有打磨、酸洗、碱洗等,本领域技术人员可灵活选择,在此不再赘述。
在前述的技术方案中,预聚合液中各组分的添加可以选择多种方式,例如直接精确称量直接添加,也可以采用将3-tba、肾上腺素各自配制成溶液,量取溶液添加等方式。只要最终的浓度和配比在前文的所说的范围内,均能实现本发明,添加方式不同不会影响本发明的最终效果。
本发明还提供了一种根据前文所述的制备方法制备得到的基于硼酸亲和作用的传感器。
通过上述技术方案,本发明引入了一种新的功能单体3-噻吩硼酸(3-tba),用于制备分子印迹聚合物膜,拓展了功能单体的种类。在上述技术方案中,本发明在玻碳电极上电聚合一层以3-噻吩硼酸作为新的功能单体的分子印迹聚合物膜,结合肾上腺素留下的分子印迹,能够实现对肾上腺素的双识别,可以实现对肾上腺素的快速灵敏检测,具备抗干扰能力强、灵敏度高且制备简单、成本低、性能稳定等优点。且该传感器的制备方法简单,采用电化学洗脱,即可将分子印迹聚合物中肾上腺素模板的去除,解决了模板分子去除难的问题,具有较高的推广价值。
不仅如此,本发明还提供了一种应用前文所述的基于硼酸亲和作用的传感器检测肾上腺素的方法。
应用电极对不同浓度的ep进行进行差示脉冲扫描,记录差示脉冲曲线及对应不同浓度的ep所引起的电流变化,绘制校准曲线。通过校准曲线及未知浓度ep的电流,即可推测未知浓度的ep含量。
通过上述技术方案,本发明引入了一种新的功能单体3-噻吩硼酸(3-tba),用于制备分子印迹聚合物膜,拓展了功能单体的种类。在上述技术方案中,本发明在玻碳电极上电聚合一层以3-噻吩硼酸作为新的功能单体的分子印迹聚合物膜,结合肾上腺素留下的分子印迹,能够实现对肾上腺素的双识别,可以实现对肾上腺素的快速灵敏检测,具备抗干扰能力强、灵敏度高且制备简单、成本低、性能稳定等优点。且该传感器的制备方法简单,采用电化学洗脱,即可将分子印迹聚合物中肾上腺素模板的去除,解决了模板分子去除难的问题,具有较高的推广价值。
在上述技术方案中,为了提高对肾上腺素的快速灵敏检测并提高抗干扰能力,优选地,检测底液的ph范围为6.0~9.0。
在本发明一种更优选的实施方式中,为了提高对肾上腺素的快速灵敏检测并提高抗干扰能力,优选地,检测底液为磷酸缓冲溶液。
以下将通过实施例对本发明进行详细描述。
实施例1
在洁净的电解池中加入5ml4.0×10-3mol/lhaucl4溶液,采用i-t法于-0.2v处对打磨好的玻碳电极进行金纳米粒子(aunps)的电化学沉积金,制得金纳米粒子修饰的玻碳电极(aunps/gce);
取400ul3-tba(浓度为0.05mol/l)和100ul肾上腺素(浓度为0.05mol/l)加入到5ml的pbs缓冲溶液(ph6.0)中,混合搅拌形成预聚合液;
将金纳米粒子修饰的玻碳电极浸入预聚合液中,采用循环伏安法(cv)在-0.2v~1.2v的电位范围内电聚合得到聚合物膜修饰电极;
将聚合物膜修饰电极浸没在盐酸(浓度为0.05mol/l)中,采用cv法在0-1.5v的电位范围内循环扫描20次,洗脱模板分子肾上腺素,制得基于硼酸亲和作用的传感器,标记为mip-1。
实施例2
基于硼酸亲和作用的传感器的制备方法:
(1)将3-噻吩硼酸、肾上腺素和磷酸缓冲溶液(ph为4,浓度为0.08mol/l)混合,形成预聚合液,其中,3-噻吩硼酸和肾上腺素的摩尔比为3:1,预聚合液中肾上腺素的浓度为0.8mmol/l;
(2)将玻碳电极浸入预聚合液中,采用循环伏安法电聚合(电位范围为-0.2v~1.2v,聚合圈数为:30圈)得到聚合物膜修饰电极;
(3)将聚合物膜修饰电极浸在盐酸(氢离子的浓度为0.03mol/l)中,采用循环伏安法(电位范围为0-1.5v)循环扫描25圈,洗脱肾上腺素。
实施例3
基于硼酸亲和作用的传感器的制备方法:
(1)将3-噻吩硼酸、肾上腺素和磷酸缓冲溶液(ph为8,浓度为0.12mol/l)混合,形成预聚合液,其中,3-噻吩硼酸和肾上腺素的摩尔比为5:1,预聚合液中肾上腺素的浓度为1.5mmol/l;
(2)将玻碳电极浸入预聚合液中,采用循环伏安法电聚合(电位范围为-0.2v~1.2v,聚合圈数为:10圈)得到聚合物膜修饰电极;
(3)将聚合物膜修饰电极浸在盐酸(氢离子的浓度为0.08mol/l)中,采用循环伏安法(电位范围为0-1.5v)循环扫描15圈,洗脱肾上腺素。
实施例4
基于硼酸亲和作用的传感器的制备方法:
(1)将3-噻吩硼酸、肾上腺素和磷酸缓冲溶液(ph为6,浓度为0.1mol/l)混合,形成预聚合液,其中,3-噻吩硼酸和肾上腺素的摩尔比为4:1,预聚合液中肾上腺素的浓度为1mmol/l;
(2)将玻碳电极浸入预聚合液中,采用循环伏安法电聚合(电位范围为-0.2v~1.2v,聚合圈数为:10~30圈)得到聚合物膜修饰电极;
(3)将聚合物膜修饰电极浸在盐酸(氢离子的浓度为0.05mol/l)中,采用循环伏安法(电位范围为0-1.5v)循环扫描20圈,洗脱肾上腺素。
对比例1
按照实施例1中的方法制备电化学传感器,不同的是,在预聚合液中不添加肾上腺素,所得传感器标记为nip-1。
对比例2
按照实施例1中的方法制备电化学传感器,不同的是,在预聚合液中将3-噻吩硼酸(3-tba)以th(噻吩)替代,所得传感器标记为mip-2。
对比例3
按照对比例2中的方法制备电化学传感器,不同的是,在预聚合液中不添加肾上腺素,所得传感器标记为nip-2。
应用例1
选择抗坏血酸(aa)、尿酸(ua)和多巴胺(da)作为结构类似物和共存物来考察传感器的选择性:在分别含有5×10-5mol/l的aa、ua、da、ep的磷酸缓冲溶液(ph范围为6.0~9.0)中,本次以ph为8为例,分别以mip-1、mip-2、nip-1、nip-2电极作为工作电极,通过差示脉冲伏安法(dpv)检测干扰物氧化峰电流信号的大小。
其中,mip-1、nip-1的检测结果对应图1,mip-2、nip-2的检测结果对应图2。
如图1所示,以3-tba作为功能单体制备的电极mip-1对ep的检测信号明显大于其他干扰物质,这是由于电极上形成的印迹孔穴对ep存在双重识别能力。既有th的印迹识别,又有硼酸的亲和作用,而对干扰物的响应信号都很小,这说明了本发明的电化学传感器能对模板分子ep进行特异性识别。
而nip-1对ep和干扰物的响应差别很小,这是由于nip-1在制备的过程中没有引入模板分子ep,所以没有形成印迹空穴,不能特异性识别模板分子,也不能识别干扰物。
实验结果表明mip-1对ep(肾上腺素)的选择性识别能力良好。
图2是以th作为功能单体制备的电极mip-2,mip-2对ep的响应电流也是大于nip-2,但没有图1中mip-1对ep的效应明显。
图2中mip-2和nip-2对ep和干扰物的响应电流差别较小,这都是因为非特异性结合引起的,实验结果表明th作为功能单体制备的mip-2没有以3-tba作为功能单体制备的mip-1的响应电流明显。
基于上述检测,我们推测,3-噻吩硼酸中的噻吩基团具有印迹效果,而硼酸基团具有亲和作用,硼酸与具有邻羟基的ep的键合的过程包括:1、硼酸基团的构型随着ph发生转变;2、与具有邻羟基的ep间形成强相互作用;3、共价键形成五元或六元环酯。整个过程可逆,且包含平面三角结构的硼酸与立体四面体结构的硼酸盐阴离子的准可逆过程,具体机理见图3。因此,3-噻吩硼酸的硼酸基团可以与ep共价结合,对目标物质进行双识别,提高检测的选择性。
而应用电极对不同浓度的ep进行进行差示脉冲扫描,记录差示脉冲曲线及对应不同浓度的ep所引起的电流变化,绘制校准曲线。通过校准曲线及未知浓度ep的电流,即可推测未知浓度的ep含量。
采用实施例1的方法制备了5根电极,用差示脉冲伏安法检测对相同浓度的ep的相应电流,得到五组响应电流值,相对标准偏差(rsd)为小于5%,表明制备的传感器具有很好的重复性。
将同一根实施例1的方法制备的电极进行洗脱再结合,重复5次,对相同浓度的ep的相应电流,得到五组响应电流值,相对标准偏差(rsd)为小于5%,表明所制备的传感器具有良好的再生性。
将所制备的修饰电极置于4℃下保存,每隔两天用差示脉冲伏安法检测其对相同浓度的ep的响应电流,发现两周后该电极仍保持初始电流的92%以上,表明制备的传感器具有很好的稳定性。
经验证,实施例2-4中制备的电极对ep的响应电流与实施例1中的mip-1接近,均大于6,其中以mip-1最优。
综上可见,本发明制备的基于硼酸亲和作用的传感器具有检测快速,抗干扰能力强、性能稳定、成本低、制备简单等优点。
以上详细描述了本发明的优选实施方式,但是,本发明并不限于上述实施方式中的具体细节,在本发明的技术构思范围内,可以对本发明的技术方案进行多种简单变型,这些简单变型均属于本发明的保护范围。
另外需要说明的是,在上述具体实施方式中所描述的各个具体技术特征,在不矛盾的情况下,可以通过任何合适的方式进行组合,为了避免不必要的重复,本发明对各种可能的组合方式不再另行说明。
此外,本发明的各种不同的实施方式之间也可以进行任意组合,只要其不违背本发明的思想,其同样应当视为本发明所公开的内容。
- 还没有人留言评论。精彩留言会获得点赞!