肿瘤坏死因子α的电致化学发光检测方法及其试剂盒与流程
本发明涉及一种基于高量子产率金纳米团簇探针的电致化学发光肿瘤坏死因子α检测方法及其检测试剂盒,属于分析化学及纳米技术领域。
背景技术:
肿瘤坏死因子α(tumornecrosisfactor,tnf-α)是一种由激活的巨噬细胞产生的能使多种肿瘤发生出血性坏死的非糖基化细胞因子。肿瘤坏死因子α不仅具有抗肿瘤活性,而且还具有免疫调节、抗病毒、促进细胞增殖分化等作用。但是,肿瘤坏死因子α也是一种内源性致热源,在脑型疟疾和感染性休克中其主要作用,危害病人的生命。研究表明,血清中肿瘤坏死因子α的浓度与许多疾病的病理过程相关,例如,新生儿李氏杆菌病、脑膜炎球菌血症、儿童艾滋病、疟疾、系统性红斑狼疮、内毒素休克、类风湿性关节炎等。测定血清中肿瘤坏死因子α的含量有助于这些疾病的诊断与治疗。通常情况下,血清中肿瘤坏死因子α含量非常低,因此,开发高灵敏度的方法用于痕量生物标志物的检测十分重要。电致化学发光免疫分析是近几年发展迅速的一种新型免疫检测方法,通过电致化学发光的信号强度来测定被测物的量,具有灵敏度高、操作简便、线性范围宽、重现性和选择性好、易于控制、连续可测等优点。目前已广泛应用在化学、医学、环境科学和生命科学等领域。
纳米材料由于具有独特的光学、电学、磁学特性,良好的生物相容性,以及催化特性,在生物传感器方面应用广泛。将纳米材料引入电致化学发光体系是电致化学发光分析的重要研究方向。量子点或纳米团簇,因具有良好的光学和电学特性,在发光材料的研发、光敏传感器的构建等方面引起了越来越多的关注。在众多发光体中,金纳米团簇作为一种新型的纳米材料,由于其具有宏观量子效应、表面效应、体积效应、量子尺寸效应等特殊性质,从而表现出许多奇异的电学、磁学、力学、热学、光学与化学方面的特性。目前尽管有关auncs的荧光性能得到广泛研究与应用,但是由于其ecl强度小、量子产率低、发光机制不清楚等问题的限制,auncs在ecl领域的研究还相对较少。针对上述问题,本课题组通过纳米尺度调控制得了高量子产率的金纳米团簇探针新方法,并将其应用于细胞释放多巴胺的检测及小分子生物硫醇等生物分子的高灵敏、快速检测。针对临床肿瘤诊断和治疗的迫切需求,设计和制备基于新型功能化金纳米团簇的高量子产率电致化学发光免疫传感器并将其用于肿瘤标志物的检测具有较重要的学术创新性和临床应用价值。
本发明提供了一种基于高量子产率金纳米团簇探针的电致化学发光肿瘤坏死因子α检测方法,及基于该方法制备的检测试剂盒。
技术实现要素:
本发明的一个目的在于提供一种基于高量子产率金纳米团簇探针的电致化学发光肿瘤坏死因子α检测方法。
本发明的另一个目的在于提供一种基于高量子产率金纳米团簇探针的电致化学发光肿瘤坏死因子α检测试剂盒。
为了实现上述目的,本发明采用以下技术方案:一种基于高量子产率金纳米团簇探针的电致化学发光肿瘤坏死因子α检测方法,其特征在于:首先在电极表面修饰金纳米团簇,通过还原法制备高量子产率金纳米团簇电致化学发光探针,并进一步在电极表面修饰二氧化锰纳米材料,将其作为电致化学发光信号猝灭剂;在空白酶标板固定肿瘤坏死因子α抗体,加入肿瘤坏死因子α,再加入生物素标记的肿瘤坏死因子α抗体,形成夹心免疫复合物;加入链霉亲和素-碱性磷酸酶,再加入2-磷酸-l-抗坏血酸三钠盐,通过碱性磷酸酶选择性水解2-磷酸-l-抗坏血酸三钠盐产生抗坏血酸;取出反应液,将电极浸入反应液中,电极表面的二氧化锰与反应液中的抗坏血酸发生氧化还原反应;采集修饰电极的电致化学发光信号,根据电致化学发光信号的改变实现肿瘤坏死因子α的检测。
所述还原法制备高量子产率金纳米团簇电致化学发光探针采用下述的电化学还原法或化学还原法制备:
(1)电化学还原法:采用三电极体系进行还原,以金纳米团簇修饰玻碳电极为工作电极,铂丝电极为对电极,ag/agcl为参比电极,将上述电极插入0.1mol/l、ph7.4磷酸盐缓冲溶液中,施加-1.4v~-2v范围内负电位电压,进行恒电位还原处理5min~1h,得到电化学发光金纳米团簇探针;
(2)化学还原法:将金纳米团簇修饰玻碳电极浸泡在0.1~1mol/l硼氢化钠溶液反应5min~30min,得到化学还原法制备的金纳米团簇探针修饰电极。
所述电极表面修饰二氧化锰纳米材料采用下述的电化学沉积法或滴涂法制备:
(1)电化学沉积法:采用三电极体系,以还原法处理金纳米团簇修饰电极为工作电极,铂丝电极为对电极,ag/agcl为参比电极,采用i-t法,在1:1v/v的kmno4-h2so4溶液中,电沉积二氧化锰,沉积电位为-0.1v~-0.5v,沉积时间为100s~600s,清洗,氮气吹干;
(2)滴涂法:首先制备二氧化锰纳米片,取500μl10mmol/l的kmno4溶液加入到1.25ml、0.1mol/lph6.0的缓冲溶液中,加入去离子水使溶液最后的体积成5ml后超声30min,结束后12000r.p.m离心10min,用水洗3次,重新分散于2.5ml去离子水中,得到二氧化锰纳米片溶液;取5μl滴涂于金纳米团簇修饰电极表面,自然晾干。
所述在空白酶标板固定肿瘤坏死因子α抗体的方法为自组装法:取空白酶标板,在空白酶标板样品孔中加入1~5mg/ml、ph8.5的多巴胺溶液50~100μl,于4℃反应1~5h,反应结束后用水轻轻漂洗,拍干;再滴加0.1~0.5mg/ml肿瘤坏死因子α抗体溶液,4℃孵育8~12h,漂洗;加入50~100μl1wt%~5wt%的牛血清白蛋白溶液,于4℃反应0.5~2h,洗涤,拍干。
所述加入肿瘤坏死因子α,再加入生物素标记的肿瘤坏死因子α抗体,形成夹心免疫复合物的方法为:在固定有肿瘤坏死因子α抗体酶标板的样品反应孔中加入肿瘤坏死因子α样本,盖上封板膜,轻轻振荡混匀,37℃温育30min~60min,洗涤,拍干;加入0.1~10μg/ml生物素标记的肿瘤坏死因子α抗体50μl,37℃温育30min~60min,洗涤,拍干。
所述加入链霉亲和素-碱性磷酸酶,再加入2-磷酸-l-抗坏血酸三钠盐的方法为:在形成夹心免疫复合物的酶标板孔中每孔分别加入50μl的0.1~1u/ml链霉亲和素-碱性磷酸酶和5~10mmol/l2-磷酸-l-抗坏血酸三钠盐溶液,轻轻振荡混匀,避光反应,37℃温育30min~60min。
所述采集修饰电极的电致化学发光信号方法如下:采用三电极体系进行测试,以修饰电极为工作电极,铂丝电极为对电极,ag/agcl为参比电极,缓冲溶液为磷酸盐缓冲液或tris-hcl缓冲溶液,所用电解质为kcl或kno3;将上述电极插入含有过硫酸根离子共反应剂的缓冲溶液中,施加一定的扫描电压,工作电极表面产生电致化学发光辐射,光电倍增管高压设置为600~800v,检测电致化学发光辐射信号。
所述根据电致化学发光信号的改变实现肿瘤坏死因子α的检测为:电极表面所采集的电致化学发光信号的电致化学发光强度值与肿瘤坏死因子α浓度的对数值在0.06pg/ml~31pg/ml的范围内呈线性关系,检测限为36fg/ml。
本发明所述的基于高量子产率金纳米团簇探针的电致化学发光肿瘤坏死因子α检测方法的检测试剂盒,其特征在于,包括金纳米团簇溶液、二氧化锰纳米材料、肿瘤坏死因子α抗体固定酶标板、肿瘤坏死因子α标准品、生物素标记的肿瘤坏死因子α抗体、链霉亲和素-碱性磷酸酶、2-磷酸-l-抗坏血酸三钠盐、洗涤液、电致化学发光测试电解质溶液。
所述的肿瘤坏死因子α抗体固定酶标板为:取空白酶标板,在空白酶标板样品孔中加入1~5mg/mlph8.5的多巴胺溶液50~100μl,于4℃反应1~5h,反应结束后用水轻轻漂洗,拍干;再滴加0.1~0.5mg/ml肿瘤坏死因子α抗体溶液,4℃孵育8~12h,漂洗;加入50~100μl1wt%~5wt%的牛血清白蛋白溶液,于4℃反应0.5~2h,洗涤,拍干;所述洗涤液为磷酸盐缓冲液或tris-hcl缓冲溶液;所述的电致化学发光测试电解质溶液为含有过硫酸钾的缓冲溶液。
具体地说,为了实现上述目的,本发明采用以下具体技术方案:首先制备高量子产率金纳米团簇电致化学发光探针,以二氧化锰为电致化学发光猝灭剂,进而利用酶联免疫反应,在夹心免疫反应的基础上,基于链霉亲和素-碱性磷酸酶溶液和2-磷酸-l-抗坏血酸三钠盐反应产生的抗坏血酸与二氧化锰的氧化学原反应恢复电致化学发光信号,由此发展一种基于高量子产率金纳米团簇探针的电致化学发光免疫分析方法,用于肿瘤标志物肿瘤坏死因子α的高效检测。本发明包括以下步骤:
(一)高量子产率金纳米团簇探针制备
高量子产率金纳米团簇探针制备方法如下:
(1)电化学还原法:采用三电极体系进行还原,以金纳米团簇修饰玻碳电极为工作电极,铂丝电极为对电极,ag/agcl为参比电极,将上述电极插入缓冲溶液中,施加负电位电压(-1.4v~-2v范围内),进行恒电位还原处理5min~1h,得到电化学发光金纳米团簇探针。
(2)化学还原法:将金纳米团簇修饰玻碳电极浸泡在0.1~1mol/l硼氢化钠溶液反应5~30min(优选0.1mol/l硼氢化钠溶液反应5min),得到化学还原法制备的金纳米团簇探针修饰电极。
所述的金纳米团簇材料为功能化修饰金纳米团簇,如:n-乙酰化-l-半胱氨酸-金纳米团簇,牛血清白蛋白-金纳米团簇等。
(二)电致化学发光信号采集方法
将电极抛光,再依次放入hno3溶液、无水乙醇和去离子水中超声清洗,n2吹干。采用三电极体系进行测试,以修饰玻碳电极为工作电极,铂丝电极为对电极,ag/agcl为参比电极,将上述电极插入含有共反应剂的缓冲溶液中。采用阶跃脉冲法,初始电位为0v,脉冲时间为10s,终止电位为-2v,脉冲时间为1s。光电倍增管高压设置为600v~800v,检测工作电极表面产生的电致化学发光信号。
所述电极为玻碳电极、丝网印刷电极或ito电极等。上述共反应剂为过硫酸根离子,浓度范围为0.01~1mol/l,优选0.1mol/l。所述缓冲溶液为磷酸盐缓冲液或tris-hcl缓冲溶液,在缓冲溶液中所添加电解质为kcl或kno3,浓度为0.01~1mol/l,优选0.1mol/l。
(三)二氧化锰纳米材料修饰方法
(1)电化学沉积法:采用三电极体系,以还原法处理金纳米团簇修饰电极为工作电极,铂丝电极为对电极,ag/agcl为参比电极,采用i-t法,在kmno4-h2so4(1:1v/v)溶液中,电化学沉积二氧化锰,沉积电位为-0.1v~-0.5v,沉积时间为100s~600s,优选-0.2v,300s,之后用双蒸水冲洗干净,氮气吹干备用。
(2)滴涂法:首先制备二氧化锰纳米片,取500μl10mmol/l的kmno4溶液加入到1.25ml0.1mol/lph6.0的缓冲溶液中,加入去离子水使溶液最后的体积成5ml后超声30min,结束后12000r.p.m离心10min,用水洗3次,重新分散于2.5ml去离子水中,得到二氧化锰纳米片溶液。取5μl滴涂于金纳米团簇修饰电极表面,自然晾干。
(四)夹心免疫反应体系构建
夹心免疫反应体系构建具体步骤如下:(1)将空白酶标板设空白孔(空白对照孔不加样品,其余各步骤操作相同)、标准品孔、待测样品孔。取空白酶标板,在空白酶标板样品孔中加入50μl1~5mg/ml的多巴胺溶液(ph8.5的tris-hcl缓冲溶液溶解),于4℃反应1~5h,反应结束后用水轻轻漂洗,拍干。再滴加0.1~0.5mg/ml肿瘤坏死因子α抗体溶液,4℃孵育8~12h,漂洗。加入50~200μl1%~5%的牛血清白蛋白溶液,于4℃反应0.5~2h,反应完成后洗涤(小心揭掉封板膜,弃去液体,甩干,每孔加满洗涤液,静置30秒后弃去,如此重复4次,拍干)。然后在标准品孔中加入肿瘤坏死因子α标准溶液50μl,在样品反应孔中加入50μl样本,盖上封板膜,轻轻振荡混匀,37℃温育30~60min,洗涤,拍干,再加入0.1~10μg/ml生物素标记的肿瘤坏死因子α抗体50μl,37℃温育30~60min,洗涤,拍干。每孔加入0.1~1u/ml链霉亲和素-碱性磷酸酶溶液50μl,轻轻振荡混匀,37℃温育30~60min,用10mmph=7.3tris-hcl缓冲液洗涤,拍干。
(五)肿瘤坏死因子α的测定
肿瘤坏死因子α检测步骤如下:往上述构建的所述的夹心免疫反应体系的酶标板中加入5~10mmol/l2-磷酸-l-抗坏血酸三钠盐溶液50μl,再加入10mmph=8.0tris-hcl缓冲溶液50μl,轻轻振荡混匀,37℃避光反应25~30min。将上述二氧化锰/金纳米团簇修饰电极浸入上述反应液中浸泡4~10min,取出后用双蒸水冲洗干净,n2吹干。采集工作电极表面产生的电致化学发光信号,以电致化学发光信号对肿瘤坏死因子α浓度作图绘制标准曲线。
(六)试剂盒
一种基于高量子产率金纳米团簇探针的电致化学发光肿瘤坏死因子α检测试剂盒,其中包括金纳米团簇溶液、二氧化锰纳米材料、肿瘤坏死因子α抗体固定酶标板、肿瘤坏死因子α标准品、生物素标记的肿瘤坏死因子α抗体、链霉亲和素-碱性磷酸酶、2-磷酸-l-抗坏血酸三钠盐、洗涤液、电致化学发光测试电解质溶液。
与现有技术相比,本发明的有益效果为:
本发明以高量子产率金纳米团簇探针为电致化学发光材料,以纳米二氧化锰为电致化学发光猝灭剂,利用酶联免疫反应产生抗坏血酸恢复其电致化学发光信号实现肿瘤坏死因子α的检测。本发明对肿瘤坏死因子α的检测灵敏度高、操作简单,可有效避免检测过程中实际样品复杂成份的干扰,因而特异性好、准确度高。并且,本发明成本低、制作简单、稳定性好、灵敏度好,线性范围宽(0.06pg/ml~31pg/ml),检测限低(36fg/ml),具有很好的市场价值。
附图说明
图1为金纳米团簇探针修饰玻碳电极的电致化学发光-时间曲线图。
图2为二氧化锰/金纳米团簇探针修饰玻碳电极的电致化学发光-时间曲线图。
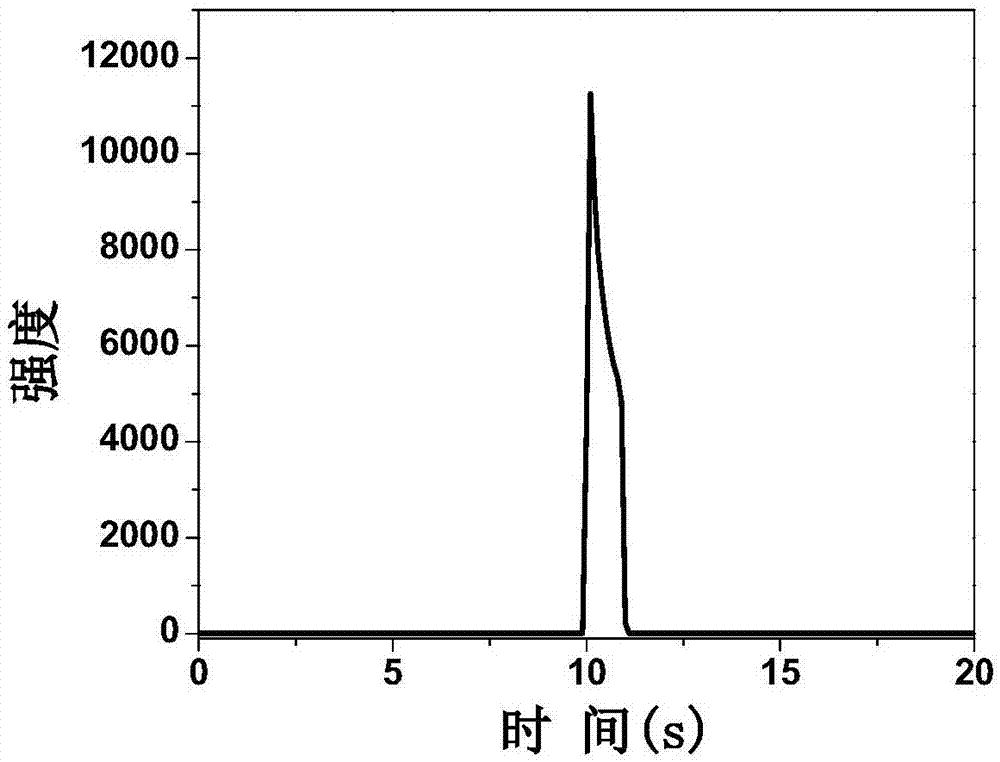
图3为本发明检测肿瘤坏死因子α的电致化学发光-时间曲线图(肿瘤坏死因子α浓度为31pg/ml)。
图4为电致化学发光强度变化与肿瘤坏死因子α浓度对数值之间的线性关系图。
具体实施方式
下面结合附图和具体实施例对本发明作进一步阐述,本发明并不限于此。
本发明所用的肿瘤坏死因子α抗体,肿瘤坏死因子α,生物素标记的肿瘤坏死因子α抗体,链霉亲和素-碱性磷酸酶(均为武汉博士德生物工程有限公司现有技术产品,2-磷酸-l-抗坏血酸三钠盐为sigma-aldrich公司现有技术产品。
实施例1
取0.6ml0.5mol/l的naoh与0.4ml20mg/ml氯金酸溶液加入到4ml0.08mol/l的n-乙酰-l-半胱氨酸溶液中,混匀后置于37℃恒温水槽中孵育3小时。待反应结束后,用分子量为3000的透析袋对反应液透析纯化24h,得到纯化后的n-乙酰-l-半胱氨酸保护的金纳米团簇溶液,于4℃冰箱避光保存。
实施例2
将直径3mm的玻碳电极用1.0μm、0.3μm、0.05μm的al2o3粉末依次抛光,打磨,至光滑镜面,再依次放入hno3溶液,无水乙醇,去离子水中超声清洗3分钟,n2吹干。取5μl实施例1制备的n-乙酰-l-半胱氨酸保护的金纳米团簇溶液滴加在处理好的玻碳电极表面,室温干燥,并进一步将该电极浸泡在0.1mol/l硼氢化钠溶液中反应5分钟,得到金纳米团簇探针修饰电极。将上述电极插入含有0.1mol/l过硫酸钾和0.1mol/lkcl的0.1mol/lph7.4磷酸盐缓冲溶液中。采用阶跃脉冲法,初始电位为0v,脉冲时间为10s,终止电位为-2v,脉冲时间为1s。光电倍增管高压设置为750v,检测工作电极表面产生的电致化学发光信号,得到电化学发光信号(见图1)。
实施例3
将直径3mm的玻碳电极用1.0μm、0.3μm、0.05μm的al2o3粉末依次抛光,打磨,至光滑镜面,再依次放入hno3溶液,无水乙醇,去离子水中超声清洗3分钟,n2吹干。取5μl实施例1制备的n-乙酰-l-半胱氨酸保护的金纳米团簇溶液滴加在处理好的玻碳电极表面,室温干燥,并进一步将该电极浸泡在0.1mol/l硼氢化钠溶液中反应5分钟,得到金纳米团簇探针修饰玻碳电极。采用三电极体系,以金纳米团簇探针修饰玻碳电极为工作电极,铂丝电极为对电极,ag/agcl为参比电极,采用计时电流法,在kmno4-h2so4(1:1v/v)溶液中,电沉积二氧化锰,沉积电位为-0.2v,时间为300s,所得到的电极为二氧化锰/金纳米团簇修饰玻碳电极,之后用双蒸水冲洗干净,n2气轻轻吹干备用。将上述电极插入含有0.1mol/l过硫酸钾和0.1mol/lkcl的0.1mol/lph7.4磷酸盐缓冲溶液中。采用阶跃脉冲法,初始电位为0v,脉冲时间为10s,终止电位为-2v,脉冲时间为1s。光电倍增管高压设置为750v,检测工作电极表面产生的电致化学发光信号,得到电化学发光信号(见图2)。
实施例4
取空白酶标板,在空白酶标板样品孔中加入50μl5mg/ml的多巴胺溶液(ph8.5的tris-hcl缓冲溶液溶解),于4℃反应2h,反应结束后用水轻轻漂洗,拍干。再滴加200μg/ml肿瘤坏死因子α抗体溶液,4℃孵育12h。孵育结束后用水轻轻漂洗,以便除去电极表面非特异性吸附的抗体。接着加入1%的牛血清白蛋白溶液50μl,于4℃反应1h,反应完成后洗涤(小心揭掉封板膜,弃去液体,甩干,每孔加满洗涤液,静置30秒后弃去,如此重复4次,拍干),得到肿瘤坏死因子α抗体固定酶标板。
实施例5
在实施例4制备的肿瘤坏死因子α抗体固定酶标板的标准品孔中加入31pg/ml的肿瘤坏死因子α标准溶液50μl,盖上封板膜,轻轻振荡混匀,37℃温育30min,洗涤,拍干,再加入0.5μg/ml生物素标记的肿瘤坏死因子α抗体50μl,37℃温育30min,洗涤,拍干。每孔加入0.2u/ml链霉亲和素-碱性磷酸酶溶液50μl(37℃预热30min),轻轻振荡混匀,37℃温育45min,洗涤,拍干。再往上述酶标板中加入8mmol/l的2-酸磷-l-抗坏血酸三钠盐溶液50μl(37℃预热30min),再加入ph=8.0tri-hcl50μl,轻轻振荡混匀,37℃避光反应25min。将各个孔中的液体取出,加入2ml的ep管当中,将处理好的电极放入各个对应浓度ep管中浸泡10min,取出后用双蒸水冲洗干净,n2吹干。将上述电极插入含有0.1mol/l过硫酸钾和0.1mol/lkcl的0.1mol/lph7.4磷酸盐缓冲溶液中。采用阶跃脉冲法,初始电位为0v,脉冲时间为10s,终止电位为-2v,脉冲时间为1s。光电倍增管高压设置为750v,检测工作电极表面产生的电致化学发光信号,得到的电化学发光信号比未加肿瘤坏死因子α的溶液明显增大(图3)。
实施例6
取空白酶标板,将空白酶标板设空白孔(空白对照孔不加样品,其余各步骤操作相同)、标准品孔、待测样品孔。在空白酶标板各孔中加入50μl5mg/ml的多巴胺溶液(ph8.5的tris-hcl缓冲溶液溶解),于4℃反应2h,反应结束后用水轻轻漂洗,拍干。再滴加200μg/ml肿瘤坏死因子α抗体溶液,4℃孵育12h。孵育结束后用水轻轻漂洗,以便除去电极表面非特异性吸附的抗体。接着加入1%的牛血清白蛋白溶液50μl,于4℃反应1h,反应完成后洗涤(小心揭掉封板膜,弃去液体,甩干,每孔加满洗涤液,静置30秒后弃去,如此重复4次,拍干)。然后在标准品孔中加入不同浓度的肿瘤坏死因子α标准溶液50μl,盖上封板膜,轻轻振荡混匀,37℃温育30min,洗涤,拍干,再加入0.5μg/ml生物素标记的肿瘤坏死因子α抗体50μl,37℃温育30min,洗涤,拍干。每孔加入0.2u/ml链霉亲和素-碱性磷酸酶溶液50μl(37℃预热30min),轻轻振荡混匀,37℃温育45min,洗涤,拍干。再往上述酶标板中加入8mmol/l的2-酸磷-l-抗坏血酸三钠盐溶液50μl(37℃预热30min),再加入ph=8.0tri-hcl50μl,轻轻振荡混匀,37℃避光反应25min。将各个孔中的液体取出,加入2ml的ep管当中,将处理好的电极放入各个对应浓度ep管中浸泡10min。取出后用双蒸水冲洗干净,n2吹干。将上述电极插入含有0.1mol/l过硫酸钾和0.1mol/lkcl的0.1mol/lph7.4磷酸盐缓冲溶液中。采用阶跃脉冲法,初始电位为0v,脉冲时间为10s,终止电位为-2v,脉冲时间为1s。光电倍增管高压设置为750v,检测工作电极表面产生的电致化学发光信号,在肿瘤坏死因子α浓度为0.06pg/ml~31pg/ml的范围内肿瘤坏死因子α浓度的对数值与电致化学发光强度值呈良好的线性关系,检测限为36fg/ml(见图4)。
实施例7
取500μl10mmol/l的kmno4溶液加入到1.25ml0.1mol/lph6.0的2-(n-吗啉代)乙磺酸(mes)缓冲溶液中,加入去离子水使溶液最后的体积成5ml后超声30min,结束后12000r.p.m离心10min,用水洗3次,重新分散于2.5ml去离子水中,得到二氧化锰纳米片溶液。
实施例8
试剂盒使用方法:(1)取5μl实施例1制备的n-乙酰-l-半胱氨酸保护的金纳米团簇滴加在处理好的玻碳电极表面,室温干燥。并进一步将该电极浸泡在0.1mol/l硼氢化钠溶液中反应5分钟,得到金纳米团簇探针修饰玻碳电极。取6μl实施例7制备的mno2纳米片溶液滴加在上述金纳米团簇探针修饰玻碳电极表面,室温干燥,得到二氧化锰/金纳米团簇修饰玻碳电极。(2)取实施例4制备的肿瘤坏死因子α抗体固定酶标板,将其设为空白孔(空白对照孔不加样品,其余各步骤操作相同)、标准品孔、待测样品孔。在空白酶标板各孔中加入50μl5mg/ml的多巴胺溶液(ph8.5的tris-hcl缓冲溶液溶解),于4℃反应2h,反应结束后用水轻轻漂洗,拍干。再滴加200μg/ml肿瘤坏死因子α抗体溶液,4℃孵育12h。孵育结束后用水轻轻漂洗,以便除去电极表面非特异性吸附的抗体。接着加入50μl1%的bsa溶液,于4℃反应1h,反应完成后洗涤(小心揭掉封板膜,弃去液体,甩干,每孔加满洗涤液,静置30秒后弃去,如此重复4次,拍干)。然后在标准品孔中加入不同浓度的肿瘤坏死因子α标准溶液50μl,盖上封板膜,轻轻振荡混匀,37℃温育30min,洗涤,拍干,再加入0.5μg/ml生物素标记的肿瘤坏死因子α抗体50μl,37℃温育30min,洗涤,拍干。每孔加入0.2u/ml的链霉亲和素-碱性磷酸酶溶液50μl(37℃预热30min),轻轻振荡混匀,37℃温育45min,洗涤,拍干。再往上述酶标板中加入8mmol/l的2-酸磷-l-抗坏血酸三钠盐溶液50μl(37℃预热30min),再加入ph=8.0tri-hcl50μl,轻轻振荡混匀,37℃避光反应25min。(3)将各个孔中的液体取出,加入2ml的ep管当中,将处理好的电极放入各个对应浓度ep管中浸泡10min。取出后用双蒸水冲洗干净,n2吹干。将上述电极插入含有0.1mol/l过硫酸钾和0.1mol/lkcl的0.1mol/lph7.4磷酸盐缓冲溶液中。采用阶跃脉冲法,初始电位为0v,脉冲时间为10s,终止电位为-2v,脉冲时间为1s。光电倍增管高压设置为750v,检测工作电极表面产生的电致化学发光信号,在肿瘤坏死因子α浓度为0.06pg/ml~31pg/ml的范围内肿瘤坏死因子α浓度的对数值与电致化学发光强度变化值呈良好的线性关系,检测限为36fg/ml。
实施例9
血清样品中肿瘤坏死因子α的检测:(1)取5μl实施例1制备的n-乙酰-l-半胱氨酸保护的金纳米团簇滴加在处理好的玻碳电极表面,室温干燥。并进一步将该电极浸泡在0.1mol/l硼氢化钠溶液中反应5分钟,得到金纳米团簇探针修饰玻碳电极。取6μl实施例7制备的mno2纳米片溶液滴加在上述金纳米团簇探针修饰玻碳电极表面,室温干燥,得到二氧化锰/金纳米团簇修饰玻碳电极。(2)取实施例4制备的肿瘤坏死因子α抗体固定酶标板,将其设为空白孔(空白对照孔不加样品,其余各步骤操作相同)、标准品孔、待测样品孔。在空白酶标板各孔中加入50μl5mg/ml的多巴胺溶液(ph8.5的tris-hcl缓冲溶液溶解),于4℃反应2h,反应结束后用水轻轻漂洗,拍干。再滴加200μg/ml肿瘤坏死因子α抗体溶液,4℃孵育12h。孵育结束后用水轻轻漂洗,以便除去电极表面非特异性吸附的抗体。接着加入50μl1%的bsa溶液,于4℃反应1h,反应完成后洗涤(小心揭掉封板膜,弃去液体,甩干,每孔加满洗涤液,静置30秒后弃去,如此重复4次,拍干)。取新鲜的血清样品20µl,加入20mmtris-hcl缓冲液稀释至1ml,然后将25µl稀释后的血清和不同浓度的肿瘤坏死因子α标准溶液25μl混合均匀,加入样品孔中,同时,将50μl不同浓度的肿瘤坏死因子α标准溶液加入标准品孔中,盖上封板膜,轻轻振荡混匀,37℃温育30min,洗涤,拍干,再加入0.5μg/ml生物素标记的肿瘤坏死因子α抗体50μl,37℃温育30min,洗涤,拍干。每孔加入0.2u/ml的链霉亲和素-碱性磷酸酶溶液50μl(37℃预热30min),轻轻振荡混匀,37℃温育45min,洗涤,拍干。再往上述酶标板中加入8mmol/l的2-酸磷-l-抗坏血酸三钠盐溶液50μl(37℃预热30min),再加入ph=8.0tri-hcl50μl,轻轻振荡混匀,37℃避光反应25min。(3)将各个孔中的液体取出,加入2ml的ep管当中,将处理好的电极放入各个对应浓度ep管中浸泡10min。取出后用双蒸水冲洗干净,n2吹干。将上述电极插入含有0.1mol/l过硫酸钾和0.1mol/lkcl的0.1mol/lph7.4磷酸盐缓冲溶液中。采用阶跃脉冲法,初始电位为0v,脉冲时间为10s,终止电位为-2v,脉冲时间为1s。光电倍增管高压设置为750v,检测工作电极表面产生的电致化学发光信号,通过标准曲线进行定量,获得样品中肿瘤坏死因子α的含量,计算得加标回收率在93.5%~108.3%之间(表1)。因此,本实验方法适用于实际样品的检测。
表1为实际样品中肿瘤坏死因子α的加标回收率实验结果
以上所述仅为本发明的典型实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改,等同替换和改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!