CD4+CD70+T细胞亚群在制备辅助诊断极重型再生障碍性贫血试剂盒中的应用的制作方法
本发明属于生物医学领域,特别涉及cd4+cd70+t细胞亚群在制备辅助诊断极重型再生障碍性贫血试剂盒中的应用。
背景技术:
再生障碍性贫血(aplasticanemia,aa)是一种骨髓造血衰竭综合征,以骨髓造血细胞增生减低和全血细胞减少为主要特征。贫血、出血以及感染为aa的主要临床表现。我国aa的年发病率高于欧美。aa的发病机制目前尚不明确,目前认为,aa的发病机制中,t细胞功能异常对骨髓造血功能的损伤是其原因之一。因此,aa也是一种t细胞介导的自身免疫性疾病。在对aa患者t细胞免疫异常研究中发现,t细胞活化异常在aa发病机制中起到重要作用。我们前期研究发现aa患者中与参与t细胞活化的信号分子,如cd3ζ,cd28和ctla-4的mrna异常表达。
cd70是t细胞活化共刺激信号分子cd27的配体,属于肿瘤坏死因子-肿瘤坏死因子受体超家族成员。人的cd70基因定位于染色体19p13,mrna全长913个核苷酸。作为cd27的配体,以往研究表明其表达局限于生发中心的b细胞和少部分的t细胞,通过与cd27相互作用调节t细胞的增殖和分化。最新的研究表明cd70也表达在成熟的树突状细胞及抗原诱导的t和b细胞。换言之,活化的t细胞表达cd70。在一些自身免疫性疾病,如风湿性关节炎和系统性红斑狼疮患者中发现表达于t细胞上的cd70较健康人升高,但是在不同疾病中的作用机制不同。最近,研究发现表达于活化t细胞上的cd70主要对t细胞的活化和功能起到负性调控作用。这说明在不同的病理状态下,活化t细胞上的cd70作用不同。国内有学者发现重型再生障碍性贫血患者(含一部分经免疫抑制剂治疗后复发的重型再生障碍性贫血患者)外周血cd8+t细胞中cd70比例升高,但是目前尚未见aa患者外周血cd4+t细胞中cd70情况的相关研究报道。
目前aa的临床诊断标准主要依据患者的外周血常规检查、多部位骨髓穿刺涂片分析、骨髓活检以及排除先天性和全血细胞减少和骨髓低增生的其他疾病等基础上进行诊断。有关不同病情程度的aa的评判主要根据骨髓细胞增生程度和血常规检查将aa分为非重型再生障碍性贫血(non-severeaplasticanemia,nsaa),重型再生障碍性贫血(severeaplasticanemia,saa)和极重型再生障碍性贫血(verysevereaplasticanemia,vsaa),其中saa和vsaa患者起病急,若无法得到有效治疗,患者的死亡率极高。aa严重程度的确定以camitta标准划分,saa患者如果其中性粒细胞绝对值低于0.2×109/l即可诊断为vsaa。随着对aa的t细胞免疫机制深入研究,aa患者存在t细胞免疫失衡也得到学者们的广泛认可。研究发现与t细胞活化的一些免疫指标,如可溶性cd30等与用于诊断aa的血常规指标存在显著相关性。另外,在不同病情程度的aa患者中与t细胞活化的信号分子表达存在差异。这说明对aa患者t细胞免疫,尤其是t细胞活化相关的免疫指标的检测不仅仅从研究领域探讨aa患者t细胞免疫异常的机制,也有可能作为应用于辅助评判aa患者病情程度的临床指标。因此,近期一些有关aa免疫相关指标检测也逐步引入诊断再生障碍性贫血的必需实验室检测项目中。在最新版的“再生障碍性贫血诊断与治疗中国专家共识”中特别强调了aa患者免疫指标的检测,如增加了调节性t细胞、th1/th2等指标的检测,以便于辅助临床医师进行aa的诊断与鉴别诊断。但是,尚未见报道vsaa患者特征性改变的免疫相关指标。因此,全面了解aa患者,尤其是vsaa和saa患者t细胞免疫特点的异同,在今后临床医师对vsaa的辅助诊断方面具有很好的应用前景。
技术实现要素:
本发明的首要目的在于弥补现有技术的缺点与不足,提供cd4+cd70+t细胞亚群在制备辅助诊断极重型再生障碍性贫血试剂盒中的应用。
本发明的另一目的在于提供一种辅助诊断极重型再生障碍性贫血的试剂盒。
本发明的再一目的在于提供一种cd4+cd70+t细胞亚群的检测方法及其应用。
本发明的目的通过下列技术方案实现:cd4+cd70+t细胞亚群在制备辅助诊断极重型再生障碍性贫血试剂盒中的应用,是基于本发明的发明人首次发现aa患者(本说明书中aa患者包含saa和vsaa患者)外周血中cd4+cd70+t细胞亚群比例在aa患者中显著降低,尤其在vsaa患者中最为显著。
当所述的cd4+cd70+t细胞亚群在cd4+t细胞中所占比例的中位数为1.9%,诊断为vsaa的可能性较大。
一种辅助诊断极重型再生障碍性贫血的试剂盒,包括能用于检测cd4+cd70+t细胞亚群的成分,如如下不同的荧光标记的单克隆抗体:抗cd3抗体、抗cd4抗体和抗cd70抗体。
所述的抗cd3抗体的荧光标记优选为fitc。
所述的抗cd4抗体的荧光标记优选为apc-h7。
所述的抗cd70抗体的荧光标记优选为pe。
所述的试剂盒还包括用于裂解外周血红细胞的红细胞裂解液、细胞染色缓冲液和磷酸盐缓冲溶液(pbs)。
一种非疾病诊断或治疗目的的cd4+cd70+t细胞亚群的检测方法,可应用上述辅助诊断极重型再生障碍性贫血的试剂盒进行检测,包括如下步骤:
(1)处理待检测外周血样本,形成单细胞悬液;
(2)在步骤(1)得到的单细胞悬液中加入标记不同荧光的单克隆抗体:抗cd3抗体、抗cd4抗体、抗cd70抗体,轻轻混匀后避光孵育;
(3)洗涤细胞后加入pbs重悬细胞,流式细胞仪上机检测,获得荧光标记后的cd4+cd70+t细胞亚群的数据。
步骤(1)中所述的处理待检测外周血样本的具体步骤如下:将待测外周血依据常规方法进行全血红细胞裂解处理,离心去上清,并用细胞染色缓冲液重悬得到单细胞悬液。
步骤(1)中所述的外周血样本的体积优选为200μl。
步骤(2)中所述的抗cd3抗体的加入量优选按每100μl的单细胞悬液配比3-6μl抗cd3抗体(浓度为200μg/ml)计算;进一步优选为按每100μl单细胞悬液配比5μl抗cd3抗体计算。
所述的抗cd3抗体的荧光标记优选为fitc。
步骤(2)中所述的抗cd4抗体的加入量优选按每100μl的单细胞悬液配比3-6μl抗cd4抗体计算;进一步优选为按每100μl单细胞悬液配比5μl抗cd4抗体计算。
所述的抗cd4抗体的荧光标记优选为apc-h7。
步骤(2)中所述的抗cd70抗体的加入量优选按每100μl的单细胞悬液配比5-25μl抗cd70抗体计算;进一步优选为按每100μl单细胞悬液配比20μl抗cd70抗体计算。
所述的抗cd70抗体的荧光标记优选为pe。
步骤(2)中所述的避光孵育的具体操作为室温避光孵育15~30分钟;优选为室温避光孵育20分钟。
所述的室温为5~35℃;优选为20~30℃;更优选为24~26℃。
步骤(3)中所述的洗涤是使用细胞染色缓冲液进行洗涤。
步骤(3)中所述的pbs优选为ph值为7.2~7.4、浓度为0.01~0.1m的pbs;更优选为ph值为7.4、浓度为0.01m的pbs。
所述的非疾病诊断或治疗目的的cd4+cd70+t细胞亚群的检测方法用于研究cd4+cd70+t细胞亚群在重型和极重型再生障碍性贫血患者中t细胞免疫异常的机理,也可应用于辅助诊断极重型再生障碍性贫血患者。
所述的应用具体包括如下步骤:对所述的cd4+cd70+t细胞亚群的表达比例进行统计学分析,当检测到cd4+cd70+t细胞亚群表达比例中位数不高于1.9%时,表明是vsaa患者可能性较大,可进一步分析其t细胞免疫系统紊乱的原因。
所述的统计学分析优选秩和检验分析。
目前有关aa的诊断标准主要依据患者的外周血常规、骨髓涂片、骨髓活检以及排除其他一些全血细胞减少和骨髓低增生性疾病,而有关不同病情程度的评判主要依靠骨髓活检和血常规。随着对aa的t细胞免疫机制的深入研究,近期一些有关aa的免疫相关指标检测也逐步引入诊断aa的必需实验室检测项目中。但是,尚未见有关对aa的不同病情程度评判的免疫相关指标。本发明的发明人首次对aa患者中参与对t细胞活化起到调控作用的cd70在aa患者外周血t细胞以及不同细胞亚群中所占比例情况这一研究空白进行了分析,以期提供更为全面的aa患者t细胞免疫异常的特点以及与病情程度有关的检测预判指标。因此本研究结合aa患者临床资料,创新性的利用流式细胞术更为详尽的研究aa患者与t细胞活化调节因素-cd70在aa患者外周血cd4+t细胞中所占比例特点以及与不同病情程度之间的关系,不仅在国际上首次提供aa患者外周血cd4+cd70+t细胞比例与疾病关系的科学研究资料,也为临床上应用上述指标辅助评判vsaa提供了理论支撑。
本发明相对于现有技术具有如下的优点及效果:
1、本发明人首次发现aa患者外周血中cd4+cd70+t细胞比例在aa患者显著降低,尤其在vsaa中最为显著。可以作为辅助诊断vsaa患者的实验室免疫相关检测指标之一,同时,也为今后临床上针对vsaa患者治疗策略的选择提供重要的参考资料。
2、本发明提供了cd4+cd70+t细胞亚群的检测方法,通过该检测方法可将上述t细胞亚群的表型进行定量统计,在辅助诊断vsaa患者的判定方面具有非常广阔的应用前景。
附图说明
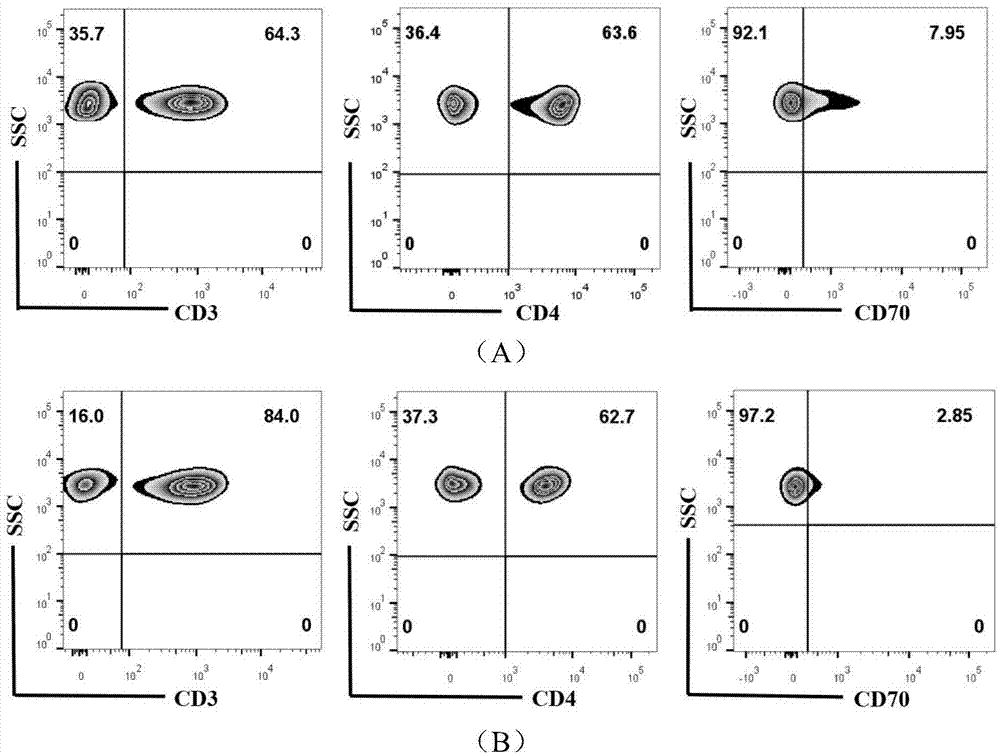
图1是健康对照组与aa患者的外周血cd4+cd70+t细胞功能亚群比例的流式细胞术结果分析图;其中,图(a)是健康对照组,图(b)是aa患者。
图2是健康对照组与aa患者外周血cd4+cd70+细胞功能亚群比例情况分析图;其中,*表示p<0.01。
图3是健康对照组与vsaa和saa两种病情的aa患者外周血cd4+cd70+细胞功能亚群比例情况分析结果图;其中,*表示p<0.01。
具体实施方式
下面结合实施例及附图对本发明作进一步的描述,但本发明的实施方式不限于此。
实例中所用试剂信息具体如下:
fitc标记小鼠抗人cd3(克隆号:hit3a,购自biolegend);
apc-h7标记小鼠抗人cd4(克隆号:rpa-t4,购自bdpharmingen);
pe标记小鼠抗人cd70(克隆号:ki-24,购自bdpharmingen);
细胞染色缓冲液(cellstainingbuffer,购自biolegend);
红细胞裂解液(redcelllysingbuffer,购自bdpharmingen)。
实施例1
(1)在与患者签署知情同意书的前提下采血,所有标本取自于清晨空腹静脉edta抗凝。收集aa共23例外周血样本,其中11例vsaa,12例saa。同时收集健康人样本31例,该部分研究方案已经获得本单位伦理委员会通过。同时收集aa患者临床资料(如表1所示)。
表1
(2)将收集的健康人和aa患者外周血使用红细胞裂解液进行裂红。每200μl外周血配比2ml红细胞裂解液,在室温裂解10min,裂解期间用吸管轻轻吹打混匀一次,然后以200g的转速离心5min,弃上清,加入1×pbs至2ml,以300g的转速离心洗涤,弃上清,加入100μl细胞染色缓冲液重悬形成单细胞悬液。
(3)流式细胞术检测cd4+cd70+细胞亚群比例的情况。
3.1每例样本需准备2个流式管,1管设为待测管,1管设为同型管,每管均为步骤(2)方法中制得的单细胞悬液。
3.2在待测管及同型管分别加入相应的表面分析荧光抗体各5μl,其中包括小鼠抗人fitc-cd3、apc-h7-cd4;待测管加入pe-cd7020μl,轻轻混匀后,室温避光孵育20min。
3.3加入细胞染色缓冲液(cellstainingbuffer)以300g的转速洗涤细胞5min。
3.4离心后去掉上清,用500μlpbs重悬细胞后使用流式分析仪(bdverse,usa)分析获取数据,所得原始数据用flowjosoftware分析,将分析数据汇总后利用spss13.0计算各组数据中位数,并计算p值。
(4)aa患者外周血中cd4+cd70+t细胞亚群比例显著低于健康对照(图1和2);结合aa患者临床资料,进一步按照不同病情程度将aa患者分为saa和vsaa组,并分析各组cd4+cd70+t细胞比例(图3),结果提示vsaa患者外周血中cd4+cd70+t细胞亚群比例显著低于健康对照,cd4+cd70+t细胞亚群表达比例中位数为1.9%。尽管saa患者外周血中cd4+cd70+t细胞亚群比例(中位数为3.05%)低于健康人,但与健康人之间并无显著差异,并且略高于vsaa患者。上述实验结果表明通过检测aa患者外周血cd4+cd70+t细胞亚群比例在辅助诊断vsaa患者中具有重要意义。
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!