一种检测甲霜灵的荧光微球免疫层析试纸条及其制备方法和应用与流程
本发明属于甲霜灵检测领域,具体涉及一种检测甲霜灵残留的荧光微球免疫层析试纸条及其制备方法和应用,其特别适用于烟草及烟草制品中甲霜灵残留的检测。
背景技术
甲霜灵(metalaxyl)是酰胺类内吸性杀菌剂,具有预防和治疗作用,用于防治瓜果、蔬菜霜霉病、疫病,马铃薯早、晚疫病,烟草黑胫病等。虽然甲霜灵对人畜的毒性不高,但属于内吸性杀菌,在农产品和蔬菜中的残留量季节性超标情况较多,因此,甲霜灵在农作物中的残留问题也受到了高度关注。gb2763-2016《食品安全国家标准食品中农药最大残留限量》中规定甲霜灵在谷物、油料和油脂中的最大残留限量在0.05-0.1mg/kg之间,在蔬菜中的最大残留限量在0.05-2mg/kg之间,在水果中的最大残留限量在0.2-5mg/kg之间,在甜菜、可可豆、啤酒花和种子类调味料中的最大残留限量分别为0.05、0.2、10、5mg/kg。美国、加拿大、日本、欧盟等国均制定了本国农产品中甲霜灵的最大残留限量。国际烟草科学研究合作中心(coresta)规定烟草中甲霜灵的指导性残留限量为2mg/kg,我国尚未制定烟草中甲霜灵的最大残留限量。
目前甲霜灵的检测方法主要是仪器检测方法,如气相色谱法、气相色谱-质谱法、气相色谱串联质谱法、液相色谱串联质谱法,等。但是由于这些分析方法需要昂贵的大型仪器设备和专业的检测人员、前处理过程复杂、操作繁琐、检测成本高、分析速度慢,难以满足现场监测和大量样本中农药残留量快速筛查的需要。因此,开发一种不受检测设备限制并且能够实现对大批量样品进行快速检测的产品和方法成为迫切需要解决的问题。
荧光微球免疫层析技术是在荧光染料标记技术上发展起来的,作为一种免疫学检测方法,它是免疫亲和技术、免疫标记技术、免疫层析技术的结合,具有快速、操作简便等优点。相比传统标记物,荧光微球的发光强度可以随激发光的强度增强而增强,所以荧光微球标记有望提高免疫层析技术的检测限;而在微球壳结构的作用下,荧光微球具有相对稳定的形态结构,粒度均一、单分散性好、稳定性好、发光效率高、重复性好,有较好的生物相容性;且形成微球后染料荧光猝灭大大减少,发射强而稳定,且基本不受外界环境介质变化的影响。因此,荧光微球免疫层析技术同时具有检测灵敏度高、操作简便、稳定性好的优点。截至目前,市场上尚未有甲霜灵荧光微球免疫层析试纸条出现。
技术实现要素:
本发明的目的之一是提供一种灵敏度高、操作简单、成本低、检测时间短的甲霜灵残留检测荧光微球免疫层析试纸条;本发明的另一个目的是提供上述试纸条的制备方法;本发明的再一个目的是提供上述试纸条在检测甲霜灵中的应用。
为了实现上述目的,本发明采取的一个技术方案是:
提供一种检测甲霜灵残留的荧光微球免疫层析试纸条,它包括底板及在底板上依次搭接粘贴的样品结合垫、硝酸纤维素膜和吸水垫,所述样品结合垫上包埋有荧光微球标记的甲霜灵单克隆抗体,所述硝酸纤维素膜上固定有检测区和质控区,检测区喷涂有甲霜灵半抗原-载体蛋白偶联物,质控区喷涂有羊抗鼠抗抗体,所述甲霜灵单克隆抗体是以甲霜灵半抗原-载体蛋白偶联物作为免疫原制备获得,所述甲霜灵半抗原-载体蛋白偶联物是由甲霜灵半抗原与载体蛋白偶联得到,所述甲霜灵半抗原是由甲霜灵与4-醛基丁酰氯在氯化铝的催化下进行取代反应得到的,其分子结构式为:
所述甲霜灵半抗原的制备方法如下:
取4-醛基丁酰氯0.53g,加30ml1,2-二氯乙烷溶解,加0.44g氯化铝,室温搅拌3h,滴加含有0.6g甲霜灵的1,2-二氯乙烷溶液20ml,回流反应4h,冷却到室温,加40ml水,0.5ml稀盐酸,振荡分层,分去水相,有机相饱和食盐水洗涤,干燥,浓缩,上硅胶柱,用体积比为1:1的石油醚-乙酸乙酯洗脱分离,得到甲霜灵半抗原产物-4醛丁酰化甲霜灵0.71g。
所述甲霜灵半抗原-载体蛋白偶联物是由甲霜灵半抗原与载体蛋白偶联得到,所述载体蛋白可为牛血清白蛋白、卵清蛋白、血蓝蛋白、甲状腺蛋白、人血清白蛋白。
所述甲霜灵单克隆抗体是由甲霜灵单克隆抗体杂交瘤细胞株分泌获得;所述羊抗鼠抗抗体是将鼠源抗体免疫羊得到。
所述荧光微球是直径为100~300nm的用聚苯乙烯包裹荧光物质的微球,其表面连接有—cooh基团,所述荧光物质为异硫氰酸荧光素。
本发明采取的另一个技术方案是提供一种制备上述检测甲霜灵残留的荧光微球免疫层析试纸条的方法,它包括如下步骤:
1)样品结合垫的制备:用市售的荧光微球标记甲霜灵单克隆抗体,并将其以特定缓冲体系稀释后,将样品结合垫浸泡于稀释缓冲液中,经真空冷冻干燥后制备;
2)硝酸纤维素膜的制备:将甲霜灵半抗原-载体蛋白偶联物喷涂到硝酸纤维素膜上的检测区范围,制成检测区;将羊抗鼠抗抗体喷涂到硝酸纤维素膜上的质控区范围,制成质控区;
3)组装和剪切:在底板上依次搭接粘贴包埋有荧光微球标记甲霜灵单克隆抗体的样品结合垫、固定有检测区和质控区的硝酸纤维素膜及吸水垫,并剪切成所需的宽度即为荧光微球免疫层析试纸条。
具体地说,步骤包括:
1)半抗原制备:甲霜灵与4-醛基丁酰氯在氯化铝的催化下进行取代反应,制备甲霜灵半抗原;
2)将甲霜灵半抗原与载体蛋白偶联,得到甲霜灵半抗原-载体蛋白偶联物;
3)用甲霜灵半抗原-载体蛋白偶联物免疫小鼠,将小鼠脾细胞和骨髓瘤细胞通过融合、筛选,得到甲霜灵单克隆杂交瘤细胞株;
4)提取小鼠igg免疫健康山羊,得到羊抗鼠抗抗体;
5)分别将甲霜灵半抗原-载体蛋白偶联物和羊抗鼠抗抗体喷涂到硝酸纤维素膜的检测区范围(t)和质控区范围(c);
6)将样品结合垫用含牛血清白蛋白(牛血清白蛋白在缓冲体系中的终浓度为0.5%体积百分含量)、ph值为7.2、0.1mol/l的磷酸盐缓冲液均匀浸泡2h,37℃下烘干2h;
7)用市售的荧光微球标记甲霜灵单克隆抗体,并将其以特定缓冲体系稀释后,将6)处理过的样品结合垫浸泡于稀释缓冲液中,经真空冷冻干燥后备用;
8)在底板上依次搭接粘贴包埋有荧光微球标记甲霜灵单克隆抗体的样品结合垫、固定有检测区和质控区的硝酸纤维素膜及吸水垫,并剪切成所需的宽度即为荧光微球免疫层析试纸条。
本发明采取的另一个技术方案是提供一种上述检测甲霜灵残留的荧光微球免疫层析试纸条在检测甲霜灵中的应用,它包括如下步骤:
1)样品前处理;
2)用所述的检测甲霜灵残留的荧光微球免疫层析试纸条进行检测;
3)用荧光检测仪分析检测结果。
与现有技术相比,本发明具有以下有益效果:
(1)特异性强、灵敏度高:本试纸条采用将荧光微球标记的甲霜灵单克隆抗体包埋在样品结合垫上,具有亲水性佳、可大容量吸附抗体偶联物、迅速重湿润、抗体结合物释放充分、性能好、释放快、形态好等优势,从而减少误差,降低成本,增加整个体系的反应灵敏度;
(2)荧光微球表面包裹了聚苯乙烯,实现了对荧光物质异硫氰酸荧光素的保护,减少了外界环境的干扰,增加了荧光微球的稳定性及荧光寿命;
(3)荧光微球表面修饰活性基团—cooh,采用化学偶联的方法来标记抗体,形成抗体与微球的稳定结合。
目前尚无用于检测烟草及烟草制品中甲霜灵的荧光微球免疫层析试纸条,本发明填补了该空白。本发明的半抗原具有适当末端活性基团,修饰位点及间隔臂长度选择合适,且能最大程度模拟甲霜灵的分子结构,以此半抗原为基础开发的试纸条具有灵敏度高、特异性强的特点。同时本发明的试纸条具有成本低、操作简单、检测时间短、适合各种单位使用、储存简单、保质期长的优点。综上,用本发明试纸条检测甲霜灵残留的方法简便、快速、直观、准确、适用范围广、成本低、易推广使用。
附图说明
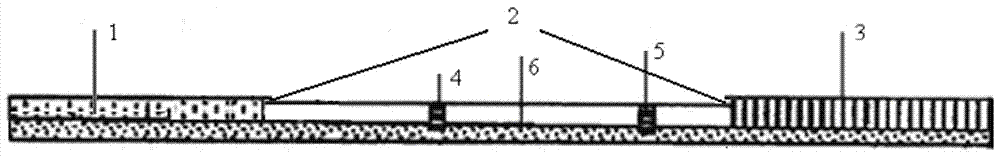
图1为荧光微球免疫层析试纸条剖面结构示意图,图中:1、样品结合垫;2、硝酸纤维素膜;3、吸水垫;4、检测区;5、质控区;6、底板;
图2为荧光微球免疫层析试纸条俯视图;
图3为甲霜灵半抗原合成图(该图作为摘要附图)。
具体实施方式
下面结合具体的实施例来进一步阐述本发明。应理解,这些实施例仅用于说明本发明,而不用来限制本发明的范围。
实施例1检测甲霜灵残留的荧光微球免疫层析试纸条的构成
参见图1、2:所述试纸条是由底板、样品结合垫、硝酸纤维素膜和吸水垫组成。
所述样品结合垫1、硝酸纤维素膜2和吸水垫3依次按顺序搭接粘贴在底板6上,样品结合垫的末端与硝酸纤维素膜的始端相连,硝酸纤维素膜的末端与吸水垫的始端相连,样品结合垫的始端与底板的始端对齐,吸水垫的末端与底板的末端对齐。
所述硝酸纤维素膜上固定有检测区4和质控区5,检测区喷涂有甲霜灵半抗原-载体蛋白偶联物,质控区喷涂有羊抗鼠抗抗体。
所述底板为pvc底板;所述样品结合垫为玻璃棉;所述吸水垫为吸水纸。
实施例2检测甲霜灵残留的荧光微球免疫层析试纸条的制备
该试纸条的制备方法主要包括以下步骤:
1)样品结合垫的制备:用市售的荧光微球标记甲霜灵单克隆抗体,并将其以特定缓冲体系稀释后,将样品结合垫浸泡于稀释缓冲液中,经真空冷冻干燥后制备;
2)硝酸纤维素膜的制备:将甲霜灵半抗原-载体蛋白偶联物喷涂到硝酸纤维素膜上的检测区范围,制成检测区;将羊抗鼠抗抗体喷涂到硝酸纤维素膜上的质控区范围,制成质控区;
3)组装和剪切:在底板上依次搭接粘贴包埋有荧光微球标记甲霜灵单克隆抗体的样品结合垫、固定有检测区和质控区的硝酸纤维素膜及吸水垫,并剪切成所需的宽度即为荧光微球免疫层析试纸条。
下面分步详细叙述:
(一)各部件的制备
1、甲霜灵半抗原的制备
取4-醛基丁酰氯0.53g,加30ml1,2-二氯乙烷溶解,加0.44g氯化铝,室温搅拌3h,滴加含有0.6g甲霜灵的1,2-二氯乙烷溶液20ml,回流反应4h,冷却到室温,加40ml水,0.5ml稀盐酸,振荡分层,分去水相,有机相饱和食盐水洗涤,干燥,浓缩,上硅胶柱,用体积比为1:1的石油醚-乙酸乙酯洗脱分离,得到甲霜灵半抗原产物-4醛丁酰化甲霜灵0.71g,收率89.7%。
取上述半抗原经核磁共振氢谱鉴定,1hnmr(cdcl3,300hz)δ:4.735(4,1h,q,j=7.072),3.661(5,3h),1.403(7,3h,d,j=7.072),4.046(13,2h),2.351(15,3h),7.367(16,1h,d,j=8.304),2.110(17,3h),7.011(20,1h,d,j=8.304),3.206(21,3h),2.608(23,2h,t,j=7.426),2.944(24,2h,td,j=7.426,j=6.840),9.659(25,1h,t,j=6.840)。图谱中化学位移δ=2.944、2.608的为间隔臂上亚甲基氢的共振吸收峰,δ=9.659的是间隔臂上醛基共振吸收峰,这些氢的吸收峰的存在,证明半抗原合成成功。
2、免疫原的制备
甲霜灵半抗原与牛血清白蛋白(bsa)偶联得到免疫原。
取16mg半抗原,溶解于1mln,n-二甲基甲酰胺(dmf)中,搅拌澄清,记为反应液a;称取bsa30mg,使之充分溶解在2.7ml0.1mol/l柠檬酸盐缓冲液(cb,ph值为9.6)中,将反应液a逐滴缓慢滴加到蛋白溶液中,并于室温下搅拌24h,用3m的硼氢化钠水溶液0.5ml还原反应4h,用0.01mol/l磷酸盐缓冲液(pbs)4℃透析3d,每天换3次透析液,以除去未反应的小分子物质,得到免疫原。
3、包被原的制备
甲霜灵半抗原与卵清蛋白(ova)偶联得到包被原。
取12mg半抗原,溶解于1mldmf中溶解澄清,记为反应液a;称取ova30mg,使之充分溶解在2.7ml0.1mol/lcb(ph值为9.6)中,将反应液a逐滴缓慢滴加到蛋白溶液中,并于室温下搅拌24h,用3m的硼氢化钠水溶液0.5ml还原反应4h,用0.01mol/lpbs4℃透析3d,每天换3次透析液,以除去未反应的小分子物质,得到包被原。
4、甲霜灵单克隆抗体的制备
(1)动物免疫
将得到的免疫原注入balb/c小鼠体内,免疫剂量为150μg/只,使其产生抗血清。
(2)细胞融合和克隆化
取免疫balb/c小鼠脾细胞,按8:1(数量配比)比例与sp2/0骨髓瘤细胞融合,筛选得到稳定分泌甲霜灵单克隆抗体的甲霜灵单克隆抗体杂交瘤细胞株。
(3)细胞冻存和复苏
取出甲霜灵单克隆抗体杂交瘤细胞株冻存管,立即放入37℃水浴中速融,离心去除冻存液后,移入培养瓶内培养。
(4)单克隆抗体的制备与纯化
增量培养法:将杂交瘤细胞置于细胞培养基中,在37℃条件下进行培养,用辛酸-饱和硫酸铵法将得到的培养液进行纯化,得到单克隆抗体,-20℃保存。
所述细胞培养基为向rpmi1640培养基中添加小牛血清和碳酸氢钠,使小牛血清在细胞培养基中的终浓度为20%(质量分数),碳酸氢钠在细胞培养基中的终浓度为0.2%(质量分数);所述细胞培养基的ph值为7.4。
(5)单克隆抗体效价的测定
用间接竞争elisa法测定抗体的效价为1:(200000~500000)。
间接竞争elisa方法:用甲霜灵半抗原-ova偶联物包被酶标板,加入甲霜灵标准品溶液、甲霜灵单克隆抗体溶液和辣根过氧化物酶标记的羊抗鼠抗抗体溶液,25℃反应30min,倒出孔内液体,用洗涤液洗涤3~5次,用吸水纸拍干;加入底物显色液,25℃反应15min后,加入终止液终止反应;设定酶标仪于波长450nm处测定每孔吸光度值。
(6)单克隆抗体特异性的测定
抗体特异性是指它同特异性抗原结合的能力与同该类抗原类似物结合能力的比较,常用交叉反应率作为评价标准。交叉反应越小,抗体的特异性则越高。
本实验将甲霜灵及与其结构类似的化合物(毒草胺、甲草胺、乙草胺、异丙甲草胺、丙草胺、丁草胺)做系列稀释,分别与单克隆抗体进行间接竞争elisa,制作标准曲线,分析得到ic50,然后按下式计算交叉反应率:
结果显示甲霜灵及其结构类似物的交叉反应率为:甲霜灵100%、毒草胺<1%、甲草胺<1%、乙草胺<1%、异丙甲草胺<1%、丙草胺<1%、丁草胺<1%。本发明抗体对毒草胺、甲草胺、乙草胺、异丙甲草胺、丙草胺、丁草胺等与甲霜灵结构类似的化合物无交叉反应,只针对甲霜灵有特异性结合。
5、羊抗鼠抗抗体的制备
以羊作为免疫动物,以鼠源抗体为免疫原对无病原体羊进行免疫,得到羊抗鼠抗抗体。
6、荧光微球标记甲霜灵单克隆抗体的制备
(1)活化:取市售的内部包埋荧光染料、表面修饰有羧基官能团的微球悬液100μl混悬于900μl活化缓冲液中,于4℃10000r/min离心10min后弃上清,重悬微球于1ml活化缓冲液中,以此法洗涤微球2次,加入适量活化剂,混匀后室温振荡活化10min;
(2)偶联:将(1)所述混悬液于4℃10000r/min离心10min后弃上清,重悬于偶联缓冲液中,以此法洗涤微球2次,加入10~20μl甲霜灵单克隆抗体溶液(蛋白浓度1mg/ml),混匀后室温振荡偶联120min;
(3)封闭:将(2)所述混悬液于4℃10000r/min离心10min后弃上清,重悬于封闭缓冲液中,以此法洗涤微球1次,混匀后室温震荡封闭30min;
(4)贮存:将(3)所述混悬液于4℃10000r/min离心10min后弃上清,重悬于贮存缓冲液中,以此法洗涤微球1次,混匀后于4℃避光保存。
所述活化缓冲液为ph值为5.5~6.5、0.05mol/l的2-(n-吗啡啉)乙磺酸(mes)缓冲液。
所述活化剂为水溶性碳二亚胺,其中摩尔质量比edc∶nhs∶cooh=(1.5~3)∶(8~20)∶1,临用前用活化缓冲液稀释至所需浓度。
所述偶联缓冲液为ph值为7.5~8.50.05mol/l的硼酸盐缓冲液(避免使用存在游离胺的溶剂)。
所述封闭缓冲液为含0.1~0.4mol/l伯胺(盐酸羟胺、乙醇胺或氨基乙醇)、1%~10%bsa的ph值为7.4的pb缓冲液。
所述贮存缓冲液为含0.01%nan3、0.1%bsa的ph值为7.4的pb缓冲液。
7、样品结合垫的制备
(1)将样品结合垫用含牛血清白蛋白(bsa在缓冲体系中的终浓度为0.5%,体积百分含量)、ph值为7.2、0.1mol/l的磷酸盐缓冲液均匀浸泡2h,37℃下烘干2h;
(2)将贮存的荧光微球标记的甲霜灵单克隆抗体以贮存缓冲液稀释后,将(1)处理过的样品结合垫浸泡于稀释缓冲液中,经真空冷冻干燥后备用。
8、硝酸纤维素(nc)膜的制备
用0.05mol/l、ph值为7.2的pbs缓冲液将甲霜灵半抗原-卵清蛋白偶联物稀释到100μg/ml,用isoflow点膜仪将其喷涂于nc膜上的检测区(t),喷膜量为1.0μl/cm;用0.01mol/l、ph值为7.4的pbs缓冲液将羊抗鼠抗抗体稀释到200μg/ml,用isoflow点膜仪将其喷涂于nc膜上的质控区(c),喷膜量为1.0μl/cm。将制备好的nc膜置于37℃条件下干燥2h,备用。
(二)试纸条的组装
将样品结合垫、硝酸纤维素膜、吸水垫从左至右依次搭接粘贴固定在底板上,样品结合垫的末端与硝酸纤维素膜的始端相连,硝酸纤维素膜的末端与吸水垫的始端相连,样品结合垫的始端与底板的始端对齐,吸水垫的末端与底板的末端对齐,然后用机器切成3.96mm宽的小条,装在特制的塑料制卡中,形成试纸卡。甲霜灵荧光微球免疫层析试纸卡在2~8℃阴凉避光干燥保存,有效期为12个月。
实施例3检测甲霜灵残留的荧光微球免疫层析试纸条的应用
1、烟叶样品前处理
称取1.0±0.05g粉碎的烟叶样本至50ml离心管中,加入10ml50%甲醇水溶液,涡旋1min,3000rpm离心5min,取100μl上清液加入400μl去离子水稀释后待测。
2、用试纸条检测
吸取100μl待检样本溶液垂直滴加于试纸卡加样孔中,液体流动时开始计时,反应10min;将试纸卡插入kft-100a型荧光检测仪的承载器中,通过触摸显示屏选择待检项目,按下“开始检测”按键,荧光检测仪将自动对试纸卡进行扫描测试,通过仪器的显示屏幕上读取或打印检测结果。
3、检测结果分析
测试完成后,仪器将根据检测得到的荧光信号的强弱,自动计算出烟叶样本中甲霜灵的浓度值,并根据预设的阈值给出阴阳性判断。
阴性(-):若荧光检测仪的显示屏幕上结果显示为阴性,表示样本中不含有甲霜灵或其浓度低于检测限。
阳性(+):若荧光检测仪的显示屏幕上结果显示为阳性,表示样本中甲霜灵浓度等于或高于检测限。
无效:若质控区未检出荧光信号强度,表明不正确的操作过程或试纸卡已失效。
实施例4检测甲霜灵残留的荧光微球免疫层析试纸条技术参数的确定
1、检测限试验
取空白烟草样品,在其中分别添加甲霜灵至终浓度为0.05、0.1、0.2mg/kg,取试纸条进行检测,每个样品重复测定三次。
用试纸条检测农产品及烟草样品时,当其中甲霜灵添加浓度为0.05mg/kg时,试纸条上显示出t线显色比c线显色深或与c线显色一致,呈阴性;当其中甲霜灵添加浓度为0.1、0.2mg/kg时,试纸条上显示出t线显色比c线显色浅或t线不显色,呈阳性,表明本试纸条对农产品中甲霜灵的检测限为0.1mg/kg。
2、假阳性率、假阴性率试验
分别取已知甲霜灵含量大于检测限的烟草阳性样本和含量小于检测限的阴性样本各20份,用3个批次生产的荧光微球免疫层析试纸条分别进行检测,计算其阴阳性率。结果见下表。
表1检测阳性、阴性样本结果
结果表明:用3个批次生产的试纸条检测阳性样本时,结果全为阳性,可知阳性符合率为100%,假阴性率为0;检测阴性样本时,结果全为阴性,可知阴性符合率为100%,假阳性率为0。说明本发明的检测甲霜灵残留的荧光微球免疫层析试纸条可以对烟草及烟草制品中甲霜灵残留进行快速检测。
3、特异性试验
用甲霜灵试纸条检测0.1mg/l的毒草胺、甲草胺、乙草胺、异丙甲草胺、丙草胺、丁草胺等其他甲霜灵结构类似物,结果显示呈阴性。说明本试纸条对0.1mg/l的毒草胺、甲草胺、乙草胺、异丙甲草胺、丙草胺、丁草胺等其他甲霜灵结构类似物无交叉反应,特异性良好。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种基于碳量子点的荧光面料及其制备方法与制造工艺
- 基于量子点的CA15‑3免疫层析试纸条的制备方法与制造工艺
- 肌红蛋白荧光免疫层析试纸条用活化荧光乳胶微球及应用的制造方法与工艺
- 铁蛋白荧光免疫层析检测卡用活化荧光乳胶微球的制造方法与工艺
- 全程C‑反应蛋白荧光免疫层析用活化荧光乳胶微球的制造方法与工艺
- 一种微流控芯片上基于荧光量子点磁性富集并分离结核分枝杆菌TB的方法及装置与制造工艺
- 25‑羟基维生素D荧光免疫层析用活化荧光乳胶微球的制造方法与工艺
- 25‑羟基维生素D3荧光免疫层析用活化荧光乳胶微球的制造方法与工艺
- 降钙素原荧光免疫层析检测卡用活化荧光乳胶微球的制造方法与工艺
- 一种改变量子点荧光色的方法与制造工艺