一种杜仲与盐杜仲的特征图谱的构建方法及鉴别方法与流程
本发明涉及中药材检测
技术领域:
,具体涉及一种杜仲及盐杜仲药材特征图谱的构建及其鉴别方法。
背景技术:
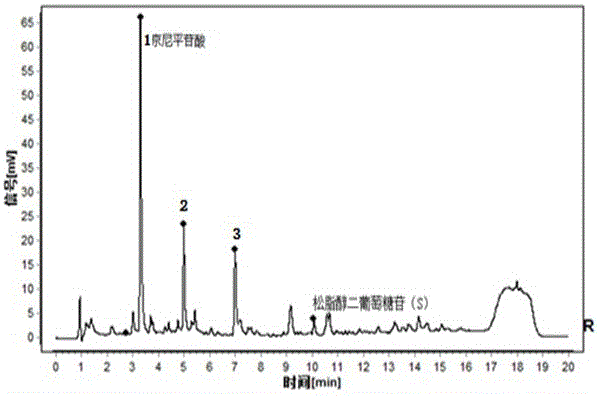
:杜仲为杜仲科植物杜仲eucommiaulmoidesoliv.的干燥树皮。《神农本草经》称:“杜仲,又名思仙、木绵、思仲、玉丝皮等,主腰脊痛,补中益精气,坚筋骨,强志,除阴下痒湿、小便余沥”;《名医别录》记载:“杜仲性温味甘,补肝肾、强筋骨”;《本草正》记载:“止小水梦遗、暖子宫、安胎气”。历版《中国药典》均收载杜仲皮作为药材,其性味甘,温。归肝、肾经。用于肝肾不足,腰膝酸痛,筋骨无力,头晕目眩,妊娠漏血,胎动不安,取自国家二级珍贵保护树种杜仲树的树皮,是中国名贵滋补药材。盐杜仲是杜仲的炮制品。盐制后可走下焦,增强补肝肾、安胎及降血压的作用。由于经过盐制,饮片和炮制品会存在活性成分的差异。因此,对不同炮制方法的同种药材进行鉴别,对于提升中药品质具有重要的实际意义。目前,鉴别方法包括传统方法和与现代科技结合的色谱方法。现阶段,传统的眼看、口尝、鼻闻、手摸等简便方法在中药材鉴别已非常局限,而色谱方法如hplc、ir、nir、tlc中存在大量的假阳性和假阴性问题,容易导致结论的偏差。因此,本发明应用超高效液相色谱法建立杜仲特征图谱,从根本上进行色谱峰的归属和鉴定,从分子层面上鉴别杜仲和盐杜仲之间的特征性差异。技术实现要素:本发明所要解决的技术问题在于,提供了一种杜仲与盐杜仲的特征图谱的构建方法及鉴别方法,应用超高效液相色谱法建立杜仲特征图谱,从根本上进行色谱峰的归属和鉴定,从分子层面上鉴别杜仲和盐杜仲之间的特征性差异。本发明所要解决的上述技术问题,通过如下技术方案予以实现:一种杜仲与盐杜仲的特征图谱的构建方法,包含如下步骤:s1.精密称取杜仲药材、盐杜仲药材,制备得到杜仲、盐杜仲供试品溶液;s2.分别将杜仲供试品、盐杜仲供试品溶液采用超高效液相色谱仪分析,得到杜仲特征图谱、盐杜仲标准特征图谱。作为一种优选方案,步骤s2中超高效液相色谱仪分析的色谱条件为:采用规格为2.1mm×100mm,1.7μm的watersacquitybehc18色谱柱;柱温为30~40℃;以乙腈为流动相a,以0.2%甲酸为流动相b进行梯度洗脱;流速为0.2~0.4ml/min;检测波长为200~300nm;进样量为0.5~5μl。作为一种优选方案,步骤s2中超高效液相色谱仪分析的色谱条件为:采用规格为2.1mm×100mm,1.7μm的watersacquitybehc18色谱柱;柱温为35~40℃;以乙腈为流动相a,以0.2%甲酸为流动相b进行梯度洗脱;流速为0.25~0.35ml/min;检测波长为230~270nm;进样量为0.8~2μl。作为一种优选方案,步骤s2中超高效液相色谱仪分析的色谱条件为:采用规格为2.1mm×100mm,1.7μm的watersacquitybehc18色谱柱;柱温为40℃;以乙腈为流动相a,以0.2%甲酸为流动相b进行梯度洗脱;流速为0.3ml/min;检测波长为254nm;进样量为1μl。上述0.2%甲酸水表示水中含有体积分数为0.2%的甲酸。作为一种优选方案,所述梯度洗脱条件为:0~3min,乙腈的体积分数变化为3~10%;3~6min,乙腈的体积分数为10%;6~15min,乙腈的体积分数变化为10~20%;15~17min,乙腈的体积分数变化为20~55%;17.01~20min,乙腈的体积分数为3%。作为一种优选方案,所述的供试品溶液通过包含如下步骤的方法制备得到:取杜仲药材或盐杜仲药材粉末2.0~4.0g,精密称定,至具塞锥形瓶中,精密加入70~80%甲醇100~200ml,称定重量,加热回流3.5~4.5小时,放冷,称定重量,用70~80%甲醇补足减失重量,摇匀,滤过,取滤液,即得供试品溶液。作为一种优选方案,所述的杜仲药材通过包含如下步骤的方法制备得到:取杜仲原药材,刮去残留粗皮后,用清水洗去泥沙等杂质,晾干或用干布略擦,用铡刀切成2~3mm的细丝,大小分档,在50~60℃下干燥2~5小时,取出,放凉,即得杜仲药材。作为一种优选方案,所述的盐杜仲药材通过包含如下步骤的方法制备得到:取杜仲药材,加入盐水(每100kg杜仲丝加入1.5~2.5kg氯化钠),拌匀,稍闷,待盐水被吸尽后,置炒锅内,以功率为1000~1400w、温度为130~170℃的中火炒20~30min,炒至丝易断、表面焦黑色时,取出,放凉,筛去灰屑,得盐杜仲药材。作为一种优选方案,一种杜仲与盐杜仲的特征图谱的鉴别方法,包括如下步骤:首先按特征图谱的建立方法,得到待检测杜仲药材或盐杜仲药材的特征图谱;然后与杜仲药材或盐杜仲药材的标准特征图谱进行比较,最后鉴别杜仲和盐杜仲之间的特征性差异。作为一种优选方案,所述的杜仲与盐杜仲的特征图谱的鉴别方法,若通过所述方法得到的样品特征图谱与通过所述方法得到的杜仲标准特征图谱一致,则样品为杜仲药材;若通过所述方法得到的样品特征图谱与通过所述方法得到的盐杜仲标准特征图谱一致,则样品为盐杜仲药材。有益效果:(1)本发明首次建立了杜仲药材与盐杜仲药材的特征图谱以及杜仲药材与盐杜仲药材的标准特征图谱;(2)该方法得到的特征图谱以及标准特征图谱可以更全面的反映样品的特征峰信息,且该方法稳定性、精密度和重现性较好;(3)该方法得到的特征图谱,从根本上进行色谱峰的归属和鉴定,从分子层面上鉴别了杜仲和盐杜仲之间的特征性差异;(4)利用该方法得到的特征图谱以及标准特征图谱可以对杜仲与盐杜仲进行真伪或品质鉴别。附图说明图1为杜仲药材的标准特征图谱。图2为盐杜仲药材的标准特征图谱。图3为杜仲药材的标准特征图谱的精密度实验图。图4为盐杜仲药材的标准特征图谱的精密度实验图。图5为杜仲药材的标准特征图谱的重复性实验图。图6为盐杜仲药材的标准特征图谱的重复性实验图。图7为杜仲药材的标准特征图谱的稳定性实验图。图8为盐杜仲药材的标准特征图谱的稳定性实验图。具体实施方式为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。实施例1杜仲与盐杜仲的特征图谱的构建1.主要仪器与试剂超高效液相色谱仪;acquityuplchsst3色谱柱(2.1mm×100mm,1.7μm);ay120型托盘电子分析天平(日本岛津公司);甲醇为色谱纯(欧普森牌);液相用水为屈臣氏蒸馏水;其它试剂为分析纯;杜仲原药材购自药材市场。2.实验方法2.1杜仲药材与盐杜仲药材的制备:杜仲药材的制备:取杜仲原药材,刮去残留粗皮后,用清水洗去泥沙等杂质,晾干或用干布略擦,用铡刀切成2.5mm的细丝,大小分档,在50℃下干燥,取出,放凉,即得杜仲药材。盐杜仲药材的制备:取杜仲药材,加入盐水(每100kg杜仲丝,用食盐2kg)拌匀,稍闷,待盐水被吸尽后,置炒锅内,以功率为1200w、温度为150℃的中火炒20min,炒至丝易断、表面焦黑色时,取出,放凉,筛去灰屑,得盐杜仲药材。2.2杜仲药材与盐杜仲药材供试品溶液的制备分别取杜仲药材、盐杜仲药材粉末约2.0g,精密称定,至具塞锥形瓶中;分别精密加入70%甲醇100ml,称定重量,加热回流4小时,放冷,称定重量,用70%甲醇补足减失重量,摇匀,滤过,取滤液,即得杜仲供试品溶液与盐杜仲供试品溶液。所述的甲醇百分含量均为体积百分含量。2.3对照品溶液的制备取松脂醇二葡萄糖苷对照品适量,精密称定,加甲醇制成每1ml含松脂醇二葡萄糖苷0.25mg,即得对照品溶液。2.4色谱条件采用规格为2.1mm×100mm,1.7μm的watersacquitybehc18色谱柱;柱温为40℃;以乙腈为流动相a,以0.2%甲酸为流动相b进行梯度洗脱;流速为0.3ml/min;检测波长为254nm;进样量为1μl;相梯度洗脱条件为0~3min,乙腈的体积分数变化为3~10%;3~6min,乙腈的体积分数为10%;6~15min,乙腈的体积分数变化为10~20%;15~17min,乙腈的体积分数变化为20~55%;17.01~20min,乙腈的体积分数为3%。2.5测定法分别精密吸取对照品溶液与供试品溶液各1μl,注入超高液相色谱仪,测定,采用“中药色谱指纹图谱相似度评价系统”,建立杜仲与盐杜仲药材对照特征图谱。得到的杜仲药材与盐杜仲药材的标准特征图谱如图1、2所示。3.色谱条件的优化3.1检测波长的确定分别取杜仲药材、盐杜仲药材粉末约2.0g,精密称定,至具塞锥形瓶中;分别精密加入70%甲醇100ml,称定重量,加热回流4小时,放冷,称定重量,用70%甲醇补足减失重量,摇匀,滤过,取滤液,即得杜仲供试品溶液与盐杜仲供试品溶液。所述的甲醇百分含量均为体积百分含量,按上述色谱条件进样分析,记录200~300nm范围内的吸收光谱。实验结果:在254nm左右,杜仲药材、盐杜仲药材样品溶液可以检测到的色谱峰最多,且各色谱峰的峰面积较大,因此选择254nm为检测波长。3.2色谱柱的优化取同一杜仲药材、盐杜仲药材供试品溶液,分别选择常用色谱柱watersbeh(100mm×2.1mm,1.7μm)、watersacquitybehc18色谱柱(2.1mm×100mm,1.7μm)、watershsst3(100mm×2.1mm,1.7μm)和agilentsb(100mm×2.1mm,1.8μm),按上述色谱条件,进样测定,比较不同色谱柱的分离效果。实验结果,watersacquitybehc18柱和agilentsb柱对样品分离效果较好,基线平稳,watersacquitybehc18柱分离效果最佳,最终选择watersacquitybehc18色谱柱为杜仲药材、盐杜仲药材特征图谱使用柱。3.3流动相的优化取同一杜仲药材、盐杜仲药材供试品溶液,分别考察流动项乙腈-水、乙腈-0.05%甲酸、乙腈-0.2%甲酸为洗脱系统,按上述色谱条件进样分析。实验结果,不同浓度的甲酸溶液对峰型影响较大,流动相中不加酸时色谱图中峰个数少于流动相中加酸,流动相中加0.2%的甲酸比加0.05%的峰型好,分离度好。最终选择乙腈-0.2%甲酸作为流动相。3.4进样量优化取同一杜仲药材、盐杜仲药材供试品溶液,分别考察进样体积0.5μl、1μl、2μl,其余按上述色谱条件进样分析。实验结果,不同进样体积对峰型影响较大,当进样体积达到2μl时,峰1和峰2裂峰明显,可能是溶剂效应到时出峰较早峰裂峰,最终选择进样体积为1μl。3.5不同柱温考察取同一杜仲药材、盐杜仲药材供试品溶液,采用同一色谱柱和液相色谱仪,按照上述色谱条件,分别在不同柱温(30℃、35℃、40℃)下进样,记录色谱图。结果表明,用上述3种温度对样品进行检测时,不同柱温对特征图谱部分共有峰的相对峰面积有一定的影响,但对其相对保留无显著影响;结合分析实际情况,选择40℃柱温进行分析。3.6不同流速考察取杜仲药材、盐杜仲药材供试品溶液,按照上述色谱条件,分别用不同流速(0.2ml/min、0.3ml/min、0.4ml/min),进样测定,记录色谱图。结果表明,用上述3种流速对样品进行检测时,不同流速对各色谱峰的分离情况和相对峰面积有一定的影响,但对特征图谱各特征峰的相对保留无显著影响,因此固定流速为0.3ml/min。4.方法学考察4.1精密度实验取同一批号的杜仲药材、盐杜仲药材样品,按供试品溶液制备方法制备成杜仲药材、盐杜仲药材供试品溶液,进样6次,每次1μl,考察特征峰相对保留时间和相对峰面积的一致性。各特征峰的相对保留时间及相对峰面积的rsd均小于2%,结果表明,精密度良好。4.2重复性实验分别取同一批号杜仲药材、盐杜仲药材样品各6份,按供试品溶液制备方法制备成杜仲药材、盐杜仲药材供试品溶液,进样1μl分析,考察特征峰相对保留时间和相对峰面积的一致性。结果表明,该方法的重复性良好。4.3稳定性实验取同一批号杜仲药材、盐杜仲药材样品,按供试品溶液制备方法制备成杜仲药材、盐杜仲药材样品溶液,在0h、1h、2h、4h、8h、12h分别进样,共测定12小时,分别进样1μl,考察特征峰相对保留时间和相对峰面积的一致性。结果表明,供试液在12小时内稳定性良好。5.杜仲药材、盐杜仲药材特征图谱的测定5.1取杜仲药材、盐杜仲药材样品19批,每份1g,按照上述制备方法和色谱条件测定样品特征图谱,测定结果见表1、2和表3、4。表119批杜仲药材特征图谱(相对保留时间)序号药材批号峰1(京尼平苷酸)峰2(绿原酸)峰3s(松脂醇二葡萄糖苷)1g16111190.3280.4930.6931.0002g16111200.3250.4950.6931.0003g16111470.3250.4950.6931.0004g16111550.3260.4950.6921.0005g16111570.3250.4940.6941.0006g16112250.3280.4950.6951.0007g16112260.3280.4950.6961.0008g16112270.3300.4960.6941.0009g17040620.3240.4950.6941.00010g17040630.3250.4950.6931.00011g17051180.3240.4950.6941.00012g17051190.3270.4950.6941.00013g17051200.3260.4940.6931.00014g17051210.3280.4950.6941.00015g17051220.3250.4940.6931.00016g17051230.3230.4940.6931.00017yg17080370.3320.4980.6971.00018yg17080380.3320.4980.6971.00019yg17080390.3320.4980.6961.000均值0.3270.4950.6941.000rsd(%)0.860.280.210.00表219批杜仲饮片特征图谱(相对峰面积)序号药材批号峰1(京尼平苷酸)峰2(绿原酸)峰3s(松脂醇二葡萄糖苷)1g16111193.7521.7570.6051.0002g161112011.2863.4000.2971.0003g161114732.6590.5876.9091.0004g16111551.6171.2770.2021.0005g16111578.3814.5940.8851.0006g16112252.6331.3230.8331.0007g16112263.1376.0740.0001.0008g16112272.5263.9550.2891.0009g170406212.9581.8571.5271.00010g17040639.1265.8018.3791.00011g170511834.48410.36413.2651.00012g170511920.1937.43620.0631.00013g170512016.2888.6097.5551.00014g170512163.9861.9623.4931.00015g170512213.7513.6026.2051.00016g170512315.4274.9544.0561.00017yg17080373.88210.2830.0881.00018yg17080387.4633.9751.0251.00019yg17080395.35512.7970.0911.000均值14.1534.9793.9881.000rsd(%)108.3570.46135.30.00表319批盐杜仲饮片特征图谱(相对保留时间)表419批盐杜仲饮片特征图谱(相对峰面积)结果:19批杜仲药材样品中特征峰的保留时间rsd均小于0.9%,符合标准规定。各特征峰的相对峰面积差异较大,rsd值在70.46~135.30%之间,说明不同产地、批次样品所含各成分的相对峰面积比例差异较大,各特征峰的峰面积一定程度上反应不同杜仲药材样品的质量情况;19批杜盐仲药材样品中特征峰的保留时间rsd均小于1%,符合标准规定。各特征峰的相对峰面积差异较小,rsd值在5.080~17.204%之间,说明不同产地、批次样品所含各成分的相对峰面积比例差异不大。6.2杜仲药材、盐杜仲药材对照特征图谱的建立分别将19批杜仲药材、盐杜仲药材特征图谱采用《中药色谱指纹图谱相似度评价系统》,通过匹配,生成对照图谱,建立杜仲药材、盐杜仲药材对照特征图谱,如图1、2所示。确定杜仲药材的特征图谱中应有4个特征峰,其中峰4与参照物溶液对应;以峰4松脂醇二葡萄糖苷峰为s峰,各峰相对保留时间规定为:0.327(峰1)、0.495(峰2)、0.694(峰3);其相对保留时间应在规定值的±5%之内;盐杜仲药材的特征图谱中应有5个特征峰,其中峰5与参照物溶液对应;以峰5松脂醇二葡萄糖苷峰为s峰,各峰相对保留时间规定为:0.256(峰1)、0.322(峰2)、0.493(峰3)、0.695(峰4);其相对保留时间应在规定值的±5%之内。6.3杜仲药材、盐杜仲药材特征图谱特征峰的指认6.3.1仪器与试药仪器:uplc-ms-ms高分辨质谱仪qexactivefocus(赛默飞世尔科技有限公司,compounddiscoverer2.1数据库);同实施例1项下“仪器与试药”。6.3.2色谱条件和质谱条件色谱条件:固定相:acquityuplchsst3(1.7µm2.1x100mm);流动相:甲醇为流动相a,0.1%甲酸为流动相b,按下表规定的进行梯度洗脱;进样量:1µl;流速:0.4ml/min;柱温:30℃;时间流速a(甲醇)b(0.1%甲酸)00.45.095.09.000.49.091.022.000.422.078.040.000.433.067.045.000.433.067.0质谱条件:ms系统:watersxevotqd三重四极杆质谱;离子化模式:esi–&esi+;正离子模式下,msscan扫描,扫描时间40min,扫描范围150-800da,扫描时间:1s,锥孔电压:30v;负离子模式下,msscan扫描,扫描时间40min,扫描范围150-800da,扫描时间:1s,锥孔电压:30v;6.3.3参照物溶液的制备:同实施例项下“参照物溶液的制备”。6.3.4供试品溶液的制备:同实施例项下“供试品溶液的制备”。6.3.5测定法分别精密吸取对照品溶液与杜仲药材、盐杜仲药材供试品溶液各1μl,注入uplc-ms-ms高分辨质谱仪,测定,即得。6.3.6结果分析:根据一级和二级质谱及相关数据库分析以及文献检索结果,预测杜仲药材图谱的峰1为京尼平苷酸,峰2为绿原酸,峰4(s峰)为松脂醇二葡萄糖苷,峰4经对照品确认为松脂醇二葡萄糖苷;预测盐杜仲药材图谱的峰2为京尼平苷酸,峰3为绿原酸,峰5(s峰)为松脂醇二葡萄糖苷,峰5经对照品确认为松脂醇二葡萄糖苷。实施例2利用标准特征图谱鉴别杜仲药材的方法随机从市场上购买一批杜仲药材鉴别其真伪。首先按实施例1所述的特征图谱的建立方法,建立待检测杜仲药材的特征图谱;然后与按实施例1方法建立得到的杜仲药材和盐杜仲药材的标准特征图谱进行比较;通过国家药监局颁布的特征图谱相似度评价软件测得该批药材的特征图谱与杜仲药材的标准特征图谱一致,可以判定,该批药材为杜仲药材。实施例3利用标准特征图谱鉴别盐杜仲药材的方法随机从市场上购买一批杜仲药材鉴别其真伪。首先按实施例1所述的特征图谱的建立方法,建立待检测盐杜仲的特征图谱;然后与按实施例1方法建立得到的杜仲药材和盐杜仲药材的标准特征图谱进行比较;通过国家药监局颁布的特征图谱相似度评价软件测得该批药材的特征图谱与盐杜仲药材的标准特征图谱的一致,可以判定,该批药材为盐杜仲药材。以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1