流体样品分析系统的制作方法
本申请涉及流体样品分析系统。一些实施方案可以包括即时检测(poct)系统,该系统包括用于与流体样品盒相互作用的单元和用于调节流体样品相对于分析器的位置的聚焦组件。
背景
即时检测包括在患者护理现场处或在患者护理现场附近进行的医疗检测,例如在医生办公室或现场的患者检测实验室。即时检测的显著优点是可以快速且局部地执行检测(例如,血液检测等),以便可以在患者在现场时获得和评述检测结果。这种即时检测可以消除将样品送到非现场实验室的需要,将样品送到非现场实验室通常涉及延迟接收测试结果,这可能会延迟临床管理决策。
虽然poct系统可以在方便性和快速可用的测试结果方面提供显著的益处,为了提供有意义的信息,这些系统需要产生准确且可靠的检测结果。快速可用的现场检测结果可能很方便,但如果这些检测结果容易产生误差或者如果这些检测结果从测量到测量变化很大,则这些检测结果可能具有很小的临床价值。poct系统通常依赖于使用一次性元件来捕获和保持样品以进行分析。这样的一次性物品可能彼此变化并且可能将不精确度引入到系统中,这是因为每次新的测量可能会引入不同的一次性物品。因此,需要能够适应于引入到测量系统中的变化和通过与一次性元件相互作用进行的分析的poct单元。
一些poct系统可能涉及光学检测,并且可以包括可聚焦的光学器件,以便提高光学测量的信噪比。随着一次性单元的变化(例如,通过制造变化引入的变化,一次性物品在分析系统内的放置上的变化等),poct系统中的光学器件可能需要在每次将不同的一次性物品引入系统中时或甚至在某些类型的测量期间聚焦。在某些情况下,聚焦机构可能包括高度精确的步进系统或致动器系统(例如,基于压电的系统)。虽然这些系统可以提供所需的精度,但是它们可以向系统引入额外的费用和复杂性。
发明概述
1)本公开的一个方面可以包括流体分析系统,其可以包括台架,该台架配置成接收包括待分析的流体样品的样品保持器。流体分析系统还可以包括流体分析器,该流体分析器配置成监测待分析的流体样品的至少一个特性;和倾斜轨道;其中所述台架配置成沿着倾斜轨道移动以使样品保持器沿着流体分析器的分析轴线移动第一运动分量并且同时与流体分析器的分析轴线正交地移动第二运动分量,其中第一运动分量影响流体分析器相对于待分析的流体样品的至少一种成分的聚焦。
2)根据1)所述的流体分析系统,还包括激活单元,所述激活单元包括可旋转凸轮轴和与所述凸轮轴相关联的一个或更多个凸轮,其中所述一个或更多个凸轮配置成在所述凸轮轴旋转时引起与所述样品保持器相关联的流体的至少一些移动,其中所述激活单元机械地联接到所述台架并与所述台架一起沿着所述倾斜轨道移动。
3)根据2)所述的流体分析系统,还包括框架,其中所述马达、所述流体分析器和所述倾斜轨道机械地联接到所述框架。
4)根据2)所述的流体分析系统,还包括控制器,所述控制器被编程为控制所述激活单元的操作以制备用于分析的所述流体样品。
5)根据2)所述的流体分析系统,其中所述样品保持器包括具有至少两个可按压部分的盒,所述至少两个可按压部分与所述盒上的由流体导管连接的流体储器相关联,并且其中制备用于分析的所述流体样品包括使用所述一个或更多个凸轮交替地按压所述至少两个可按压部分,使得流体在所述流体储器之间来回流动。
6)根据1)所述的流体分析系统,其中所述流体分析器包括照相机,并且所述聚焦是光学聚焦。
7)根据1)所述的流体分析系统,还包括经由轴联接到所述台架的马达,其中所述马达的操作引起所述台架沿着所述倾斜轨道的移动。
8)根据1)所述的流体分析系统,还包括控制器,所述控制器被编程为使所述流体分析器相对于待分析的所述流体样品的所述至少一种成分自动聚焦。
9)根据8)所述的流体分析系统,其中所述控制器通过以下项进行自动聚焦:
自动使所述台架沿所述倾斜轨道移动到多个不同的位置;
确定在所述多个不同的位置中的每一个处的至少一个聚焦质量指示;和
基于所确定的在所述多个不同的位置处的聚焦质量指示,确定所述台架沿所述倾斜轨道的目标位置;和
使所述台架移动到所述目标位置。
10)根据1)所述的流体分析系统,其中待分析的所述流体样品的所述至少一种成分包括细胞。
11)根据10)所述的流体分析系统,其中所述细胞包括粘弹性地聚焦到与所述样品保持器相关联的微通道内的单个平面中的细胞。
12)根据1)所述的流体分析系统,其中所述一个或更多个凸轮配置成引起对与所述样品保持器相关联的至少一个流体导管的压力,以将所述至少一个流体导管夹紧关闭。
13)根据1)所述的流体分析系统,其中所述样品保持器包括微通道,并且其中在分析所述流体样品期间,使待分析的所述流体样品流过所述微通道。
14)根据1)所述的流体分析系统,其中所述流体分析器配置成当待分析的所述流体样品内的颗粒和所述流体样品在设置在所述样品保持器内的微通道内流动时,从相对于所述样品保持器的固定位置获取待分析的所述流体样品内的颗粒的图像。
15)根据14)所述的流体分析系统,其中所述颗粒是粘弹性地聚焦到所述微通道内的单个平面中的粘弹性地聚焦的颗粒。
16)本公开的另一方面可以包括用于分析流体样品的方法。该方法可以包括:将包括流体样品的样品保持器沿着倾斜轨道移动到沿着倾斜轨道的多个不同的位置,其中样品保持器的移动产生样品保持器沿着流体分析器的分析轴线的第一运动分量和样品保持器正交于分析轴线的第二运动分量,流体分析器配置成监测流体样品的至少一个特性;获取沿着倾斜轨道的多个不同的位置中的每一个处的图像;分析所获取的图像并自动确定在多个不同的位置中的每一个处的至少一个聚焦质量指示;根据所确定的在多个不同的位置处的聚焦质量指示,确定样品保持器沿着倾斜轨道的目标位置;使样品保持器移动到目标位置;以及分析目标位置处的流体样品。
17)根据16)所述的方法,还包括:
获取所述目标位置处的一个或更多个图像;和
基于对在所述目标位置处获取的所述一个或更多个图像的分析来确定所述流体样品中的细胞计数。
18)根据16)所述的方法,其中所述流体分析器包括照相机,并且所述分析轴线是所述照相机的光轴。
19)根据16)所述的方法,还包括:
将所述样品保持器保持在台架上,所述台架配置成在马达的影响下沿所述倾斜轨道移动;和
使用激活单元制备用于分析的所述流体样品,所述激活单元与所述台架一起沿着所述倾斜轨道行进。
20)根据19)所述的方法,其中所述激活单元包括可旋转凸轮轴和与所述凸轮轴相关联的一个或更多个凸轮,其中所述一个或更多个凸轮配置成在所述凸轮轴旋转时引起与所述样品保持器相关联的流体的至少一些移动。
21)根据20)所述的方法,还包括控制所述激活单元的操作以制备用于分析的所述流体样品。
22)根据21)所述的方法,其中所述样品保持器包括具有至少两个可按压部分的盒,所述至少两个可按压部分与所述盒上的由流体导管连接的流体储器相关联,并且其中制备用于分析的所述流体样品包括使用所述一个或更多个凸轮交替地按压所述至少两个可按压部分,使得流体在所述流体储器之间来回流动。
23)根据21)所述的方法,其中所述样品保持器包括具有至少两个可按压部分的盒,所述至少两个可按压部分与所述盒上的流体储器相关联,所述流体储器由流体导管连接并且与用易碎密封件密封的共同的流体出口相关联,并且其中制备用于分析的所述流体样品包括用所述一个或更多个凸轮同时按压所述至少两个可按压部分,使得引起对所述易碎密封件的压力,所述压力足以打开所述易碎密封件并使流体能够流过所述共同的流体出口。
24)根据16)所述的方法,其中分析所述目标位置处的所述流体样品包括基于所获取的粘弹性地聚焦到与所述样品保持器相关联的微通道内的单个平面中的细胞的图像来确定细胞计数。
25)本公开的另一方面可以包括流体分析系统。流体分析系统可以包括:台架,其配置成接收包括待分析的流体样品的样品保持器;以及激活单元,其包括可旋转凸轮轴和与凸轮轴相关联的一个或更多个凸轮。一个或更多个凸轮可以被配置成:在凸轮轴旋转时引起与样品保持器相关联的流体的至少一些移动;通过当凸轮轴旋转时交替地按压与在样品保持器上的两个流体储器相关联的可按压部分,使流体在样品保持器上的两个流体储器之间来回流动;和引起对与样品保持器相关联的至少一个流体导管的压力,以将该至少一个流体导管夹紧关闭。
附图说明
图1提供了根据示例性的公开的实施方案的分析系统的示意性表示。
图2提供了根据示例性的公开的实施方案的分析系统的框图表示。
图3提供了根据示例性的公开的实施方案的分析系统的所选内部部件的示意性侧视图表示。
图4提供了根据示例性的公开的实施方案的盒204的示意性表示。
图5提供了根据示例性的公开的实施方案的盒的一部分的示意图。
图6a和图6b描绘了根据示例性的公开的实施方案的密封件。
图7a和图7b描绘了根据示例性的公开的实施方案的密封件。
图8提供了根据示例性的公开的实施方案的盒的一部分的示意图。
图9提供了根据示例性公开的实施方案的盒的一部分的示意图。
图10a和10b示出了根据本公开的某些实施方案的两个制备单元构造。
图11示意性示出了根据示例性的公开的实施方案的分析隔室。
图12示意性示出了根据示例性的公开的实施方案的分析隔室。
图13示意性示出了根据示例性的公开的实施方案的分析隔室。
图14a和图14b示出了根据本示例性的公开的实施方案的包括制备隔室和分析隔室的盒。
图15a、图15b和图15c示例性描绘了根据目前描述的实施方案的采样器。
图16示出了根据示例性的公开的实施方案的包括刚性框架的盒的一部分。
图17a图示了根据示例性的公开的实施方案的盒。
图17b图示了根据示例性的公开的实施方案的盒。
图17c图示了根据示例性的公开的实施方案的盒。
图18提供了根据示例性的公开的实施方案的分析系统的所选内部部件的示意性透视图表示。
图19提供了根据示例性的公开的实施方案的激活单元的示意性表示。
图20提供了根据示例性的公开的实施方案的多凸角凸轮的示意性表示。
图21提供了根据示例性的公开的实施方案的与凸轮的旋转相对应的定性压力图。
详细描述
所公开的实施方案可以包括分析系统,该分析系统可以接收用于对容纳在盒中或以其他方式包括在盒上的流体样品进行测试的一次性盒/样品保持器。盒可以包括一种或更多种液体试剂,这些试剂可以储存在单独的隔室中。在测试过程中,分析系统可以控制试剂的流动(例如,在盒的不同区域之间)和试剂的混合(例如,将不同类型的试剂彼此混合和/或将试剂与用于分析的诸如样品流体的一种或更多种样品混合)。在一些实施方案中,混合和流动控制可以在不与试剂或样品物理接触的情况下实现。在样品已经与适当的试剂混合并准备进行测量后,分析系统可以使制备的样品(例如悬浮在流体中的细胞)流入分析室,比如透明测量室,在该室中可以进行样品分析。在一些情况下,分析可以包括对所制备的样品流体中的细胞或其他类型的颗粒进行显微成像。为了进行成像,分析系统可以调节分析室相对于成像单元的光学器件的位置,使得悬浮在制备的样品流体中的细胞或颗粒处于光学焦点上。
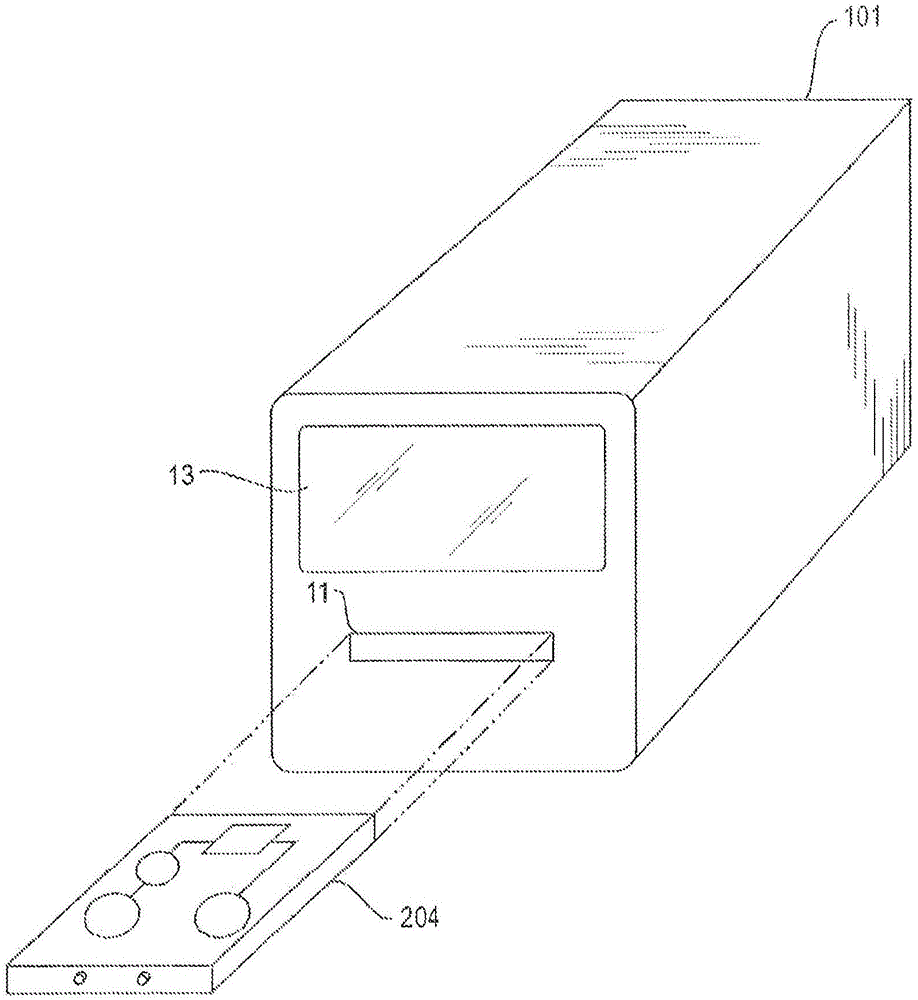
图1提供了根据示例性的公开的实施方案的分析系统101的示意性表示。在一些实施方案中,分析系统101可以是用于分析流体样品的poct单元。要分析的样品可以被收集并引入盒204,盒204可以在分析过程之前插入到分析系统101中的接收器11中。可以在显示器13上提供分析结果。分析系统101的操作者可以经由一个或更多个输入设备与系统交互,这可以包括显示器13包括触敏设备的实例。诸如键盘、定点设备(pointdevice)、语音识别单元等的其它输入/输出设备可用来向操作员提供与分析系统101交互并向分析系统101提供命令的能力。
图2提供了根据示例性的公开的实施方案的可以包括在分析系统101中的部件的框图表示。例如,分析系统101可以包括直接或间接地连接到分析系统101的各部件的控制器20。控制器20可以访问存储器21并且可以在显示器13上呈现文本和/或图像。在一些情况下,在显示器13包括触敏设备的情况下,控制器20可以经由与显示器13相关联的触敏设备接收用户命令。控制器20可以经由输入-输出(i/o)设备14接收用户输入并且提供各种类型的输出,如所指出的,输入-输出(i/o)设备14可以包括各种键盘、定点设备、语音识别单元等。控制器20还可以例如通过数据总线15连接到流体分析器22、盒激活单元24和盒定位单元26。
存储器21可以包括任何合适类型的数据存储设备,并且可以包括相同类型或不同类型的一个或更多个数据存储设备。在一些情况下,存储器21可以包括易失性或非易失性存储单元。存储器21可以包括例如ram、rom、sram、dram、prom、eprom、eeprom、磁性计算机可读介质、光学计算机可读介质、闪速存储器、fpga等的任何组合。
存储器21可以包括可访问控制器20的各种类型的数据和指令。为了本公开的目的,对被配置为或被编程为执行某些任务或功能的控制器的引用表示存储器21已经填充了特定数据和/或机器可执行指令,使得控制器20可以通过访问数据和/或指令并执行包括在存储器21中的一个或更多个指令来执行某些任务或功能。在一些情况下,存储器21可以包括与控制器20分开的设备。在其他实例中,存储器21可以与控制器20集成在一起。
控制器20可以包括能够执行一个或更多个指令的任何合适的基于逻辑的设备。例如,控制器20可以包括一个或更多个数字信号处理器、微控制器、cpu等。控制器20可以执行基于x86或arm的指令或来自任何其他合适的架构的指令。控制器20可以仅包括单个集成电路或处理单元,或者可以包括多个集成电路或处理单元。例如,控制器20可以包括一个或更多个应用处理器、触摸处理器、运动控制单元、视频处理器等。
控制器20可以具有在系统101内的各种功能。例如,在一些实施方案中,控制器20可以包括用于操作系统101的各种部件(包括马达、照明单元、传感器)或与其相互作用的电子器件和逻辑。在某些实施方案中,这样的部件可以包括用于帮助流体移动到样品保持器的不同部分的泵、压力计、光电二极管传感器、用于照亮样品流体的led、照相机或用于捕获样品流体的图像的其他类型的图像采集设备。在一些实施方案中,控制器20还可以与诸如触摸屏或键盘的部件进行交互或对其进行控制,并且可以运行用于实现与系统101相关联的过程或功能的各种算法,该过程或功能包括例如:自动聚焦过程、图像采集、对获得的样品流体图像进行处理、细胞计数、细胞分类、样品流体在样品保持器中的制备、样品保持器移动到系统101内的适当分析位置、流体在样品保持器内的移动以及其他过程和功能。
图3提供了分析系统101的所选内部部件的示意性侧视图。例如,盒204可经由接收器11引入分析系统101中。在一些实施方案中,在将盒204插入系统101中时,盒保持器31可以将盒204保持并以其他方式固定在分析系统101内的期望位置。为了制备包括在盒204上的样品,激活单元24可以与盒204的一个或更多个区段相互作用,以便制备用于分析的流体样品。在一些实施方案中,盒激活单元24可以包括并入在旋转凸轮轴33上的一个或更多个凸轮32,以便按压(直接通过接触盒的各区段或间接地通过与接触盒的一个或更多个活塞(或任何其它合适的结构)相互作用)盒的各区段,以对用于分析的样品进行制备、混合、移动、分配等。
定位单元26可以包括用于控制制备的样品(例如,在盒204上)相对于包括在流体分析器22中的分析部件的位置的各种部件。例如,在一些实施方案中,定位单元26可以包括经由轴36连接到台架35的马达34。当被插入到分析系统101中时,盒204可以由台架35直接或间接地支撑。例如,盒保持器31可以包括一个或更多个元件以在盒204上施加力,以便将盒204固定在台架35上的适当位置。马达34可以用于使轴36旋转或以其它方式移动以便移动台架35。在一些情况下,台架35可以安装在倾斜轨道37上。在这样的实施方案中,马达34的控制可能导致台架35以及联接到台架的任何部件(例如,所保持的盒)例如沿倾斜轨道37移动。由于沿轨道37的移动,台架35可以同时相对于流体分析器22沿x方向和z方向移动。
流体分析器22可以安装到框架组件38,马达34和倾斜轨道37也可以安装到框架组件38。流体分析器22可以包括用于分析容纳在盒204内或包括在盒204上的流体样品的一个或更多个设备。在一些情况下,流体分析器22可以包括用于基于激光散射、荧光、阻抗测量等进行流式细胞术的部件。可替代地或另外,流体分析器22可以包括光学成像器,光学成像器包括例如透镜、图像传感器和适于获取样品的光学图像的其他部件。例如,在一些实施方案中,流体分析器22可以包括光学传感器(例如ccd、cmos或光电倍增器)。可以提供一个或更多个激励源(未示出),以用于用具有适于所选的分析类型的波长的辐射来照射待分析的样品流体。在一些实施方案中,光学传感器可以包括照相机,照相机获取在盒204的检查区域内流动的细胞或颗粒的图像。获取的图像然后可以由控制器20使用合适的软件和/或硬件来处理,以便确定例如存在于样品流体中的一种或更多种细胞类型(例如,中性粒细胞、淋巴细胞,红细胞等)的细胞计数。作为分析过程的一部分确定或得到的所获取的图像、图像流、分析结果、获取或计算的数据等可以被存储在例如存储器21中。流体分析器22、激活单元24和定位单元26中的每一个的详细描述以及每个在执行流体样品分析中的作用包括在下面的部分中。
盒
如所指出的,所公开的实施方案可包括用于制备用于分析的样品流体的盒204。样品流体可以包含感兴趣的颗粒,例如细胞。样品流体可以包括体液,包括例如:血液、脑脊髓液(csf)、心包液、胸膜液或可能包含细胞的任何其它流体。可以分析任何类型的细胞(或其他颗粒)。在某些情况下,要分析的细胞可包括原核细胞(例如,细菌);真核细胞(例如,红细胞);白细胞(白血球);上皮细胞;循环肿瘤细胞;细胞碎片(例如,血小板);或其他。
在一些实施方案中,盒204可用于制备用于光学分析以提供全血计数(cbc)的血液样品。然而,应当注意的是本公开不限于cbc。根据本公开的一次性盒可用于需要细胞分析的多种应用中,例如:hiv监控(如,使用cd4/cd8比率);f-血红蛋白、疟疾抗原或其它血液寄生虫、阵发性睡眠性血红蛋白尿(pnh)的检测;使用肠肌内膜自身抗体(ema)的腹腔疾病、阿尔茨海默氏病的诊断;或与基于细胞的诊断可能相关的任何其他应用。
图4示意性地示出了根据本公开的某些实施方案的盒204。可以用于将样品流体引入到盒中的采样器202可以例如从一侧插入盒204中。样品流体可以由制备隔室201来接收,在制备隔室201中可以相对于样品流体执行一个或更多个过程以制备用于分析的样品流体。分析隔室203可以联接到制备隔室201。分析隔室可以从制备隔室201中接收所制备的样品流体,并且可以实现样品流体的一个或更多个方面的分析。在一些实施方案中,制备隔室201和分析隔室203可以单独形成并通过一个或更多个流动路径联接在一起。在一些实施方案中,盒制备隔室201和分析隔室203可以一起制造,并在制造期间或紧接在制造后联接,或者它们可以分开制造,并且在该盒销售至其终端用户前被联接,或甚至仅在使用它们之前被联接,甚至有可能由执行检测的人联接或在系统101内自动地联接。泵(未示出)可用于产生驱动样品流体在盒的各个区段内和盒的各个区段之间流动的压力梯度,例如真空。
在一些实施方案中,制备隔室201和分析隔室203可以包括联接在一起的两个单独的隔室。然而,在其他实施方案中,制备隔室201和分析隔室203可以包括盒204的一体部分。例如,在一些实施方案中,制备隔室201和分析隔室203可以相对于共同的基体一体地形成。另外,采样器和分析隔室可以根据特定应用的要求以任何合适的定向或布局布置关于盒204定位。
在一些实施方案中,采样器202可以形成为盒204的一体部分。然而,在其它实施方案中,采样器202可以形成为与盒204分离的部件。然而,在任一情况下,采样器202可包括用于保持样品流体的运载体(carrier)。运载体可以包括例如可用于收集流体样品的一个或更多个毛细管。根据某些实施方案,系统101可以自动地将采样器202联接到盒204,以便把样品流体引入盒204中。
图5提供了根据某些实施方案的盒204的截面的示意图。在盒204中,第一开口301可位于盒的侧面中的一个中,并可以配置成接收运载样品流体的运载体。第一通道302联接到第一开口301和储器303。储器303配置成接收样品流体和执行影响样品流体的程序,从而形成输出流体。然后,储器配置成将输出流体释放到第二通道304中,并且经由第二开口305从其中离开盒。配置成防止经由第一开口从储器流动的在前密封件306可以联接到第一通道302,并且配置成防止经由第二开口从储器流动的在后密封件307可以联接到第二通道304。
术语“输出流体”可以包括来源于影响样品流体的程序的流体。在影响的程序之前,进入储器中的流体可以称为“输入流体”。在一些情况下,例如输入流体可以对应于引入到储器303中的样品流体。
在诸如储器303的储器内进行的影响样品流体的程序可以包括可以提供样品流体的或容纳在样品流体内的细胞的物理或化学状态的变化(或至少一种性质或特性的变化)的任何程序。可能的影响程序的例子可以包括加热、混合、稀释、染色、透化、裂解等。
在本公开的某些实施方案中,储器303可以预装载有物质。预装载的物质可以是液体物质、固体物质或其组合。该物质可以由单一试剂组成,或由几种不同的试剂组成。由几种试剂组成的液体物质的示例是pbs(磷酸盐缓冲盐水),而固体物质的示例包括冻干的抗体、可溶解在例如水或乙醇中的不同种类的粉末状染色剂、包衣微丸等。物质可以自由地放置在储器的底部上或可以附接到储器的内表面。可选地,物质可以附接到填充储器的空间的诸如海绵或微纤维的结构或部件。这样的结构或部件可以增加暴露于样品流体的表面区域的量。
此外,一些可能的程序,比如加热,可能不需要在储器中具有预装载的物质。因此,在某些实施方案中,储器未预先装载有物质,然而可能的是,储器代替地(或除了预装载的物质之外)保持诸如加热机构的机构或其一部分。此外,应理解,预装载物质可以在制造盒期间或在引入样品流体之前的任何时间进行,可以理解的是,根据可选择的实施方案,物质可以与样品流体一起引入到储器中,或在引入样品流体之后引入到储器中。在其它情况下,其中该物质包括成分的组合,或其中该物质是多于一种成分之间的化学反应的结果,可能的是,至少一种成分是预装载的,而至少另一种成分与样品流体一起引入或在引入样品流体之后引入。
在储器303装载有物质的情况下,不管该物质被预装载或与样品流体一起被装载还是在引入样品流体之后被装载,影响该样品流体的程序可以包括将样品流体与物质混合。在一些情况下,样品流体和物质可以彻底混合,虽然非均质性可能影响随后的分析。根据本公开的某些实施方案,为了能够进行混合,储器的表面的至少一部分(部分)可以包括由弹性聚合物(例如聚氨酯或硅树脂)或不同的弹性材料制成的可按压部分(pressableportion)。由于受到按压和/或释放可按压部分的影响引起的储器的变形(例如收缩),容纳在储器内的流体可以在储器内形成射流,射流是可以增强混合的一种流动形式。因此,根据本公开的实施方案,通过交替按压和释放储器的可按压部分实现混合是可能的。当可按压部分被按压时,流体可以从受压区域流走,而当其被释放时,流体可以流回来,使得流体来回流动。
在本公开的某些实施方案中,可按压部分可以构成储器的表面(例如储器的上表面)的一部分或其表面的一定百分比。在本公开的其它实施方案中,整个储器可以是可按压的。为了本公开的目的,术语“可按压”是指材料响应于施加到材料的压力而至少部分地变形的能力。在一些实施方案中,可按压材料的变形可导致至少部分地由可按压材料包含的区中的容积的变化。
除了混合之外或除混合外,储器中执行的影响样品流体的程序可以包括可以在物质和样品流体之间发生的反应。该反应可以包括化学反应,例如氧化/还原,或生物化学反应,例如抗体与配体的结合。该程序可以导致样品流体或样品流体中包含的细胞的物理状态和/或化学状态的变化。例如,该程序可以影响样品流体的粘弹性性质或ph的变化。样品流体中包含的细胞的浓度可以因稀释而降低。细胞膜可能变得可渗透,使包含在物质内的着色剂或抗体结合到细胞组分,比如细胞质颗粒。可能发生不同细胞组分的氧化或还原,比如包含在红细胞中的血红蛋白氧化成高铁血红蛋白等。
在完成该程序(或至少部分地完成)之后,所得到的输出流体可以从储器中释放。这种释放可能受正压或“推动”流体离开储器的影响。例如,流体可通过按压被推动离开储器。另外地或可选地,该流体可能会受到负压的影响,例如如果通过“拉”其出来的诸如重力的物理力或由于施加诸如真空的外力将流体从储器中驱出。在本公开的某些实施方案中,由联接至分析隔室的真空泵所产生的抽吸力可以导致输出流体经由第二开口从储器流动进入分析隔室中,如图1所示。
储器303可封闭在两个密封件之间,其中在前密封件306防止流体经由第一开口301流出储器,并且在后密封件307防止流体经由第二开口流出储器。在将样品流体引入到储器303中之前,两个密封件306和307可以防止物质从储器释放。这些密封件还可以防止在影响程序期间物质和/或样品流体的释放。并且,该密封件可以防止输出流体的无意的释放。
关于密封件307,密封件307的破坏或破裂可允许输出流体朝着第二开口流出储器。在一些实施方案中,在密封件破裂之后,密封件可以保持是打开的。在一些实施方案中,第二密封件307可以构成可破裂的或“易碎的密封件”。可能的是,由例如配置成通过施加超过某一阈值的压力而破坏的粘合剂来形成密封件。在储器的可按压部分上施加压力可在密封件的位置处产生超过密封的破坏阈值的压力,这导致密封件断裂。然后,输出流体可以释放到第二通道304中、经过第二开口305并进入分析隔室中。换言之,输出流体可以经由第二通道304和第二开口305传输到分析隔室。
通过间歇地按压储器的可按压部分来混合样品流体和物质可能不会在密封件的位置处产生超阈值的压力。因此,在混合期间,密封件307可以保持完整。在一些实施方案中,可以在密封件307前的流动路径中形成结构或障碍物以保护该密封件免受混合期间可能引起的任何超阈值压力的影响。例如,可以在储器和密封件之间的通道上施加压力,从而获得防止储器中产生的压力到达密封件的物理障碍物。在其它实施方案中,可以允许超阈值压力到达密封件并使密封件破裂,然而,位于通道上的物理障碍物可以防止流体流动直到障碍物被移除。
返回参照在前密封件306,该密封件可以具有两个不同的作用。在第一个作用中,密封件306可以防止在引入样品流体之前物质从储器释放。然而,当引入样品流体时,为了允许这样的引入,在前密封件必须被破坏。在一些实施方案中,为了允许使用提供到储器的可按压部分的压力进行混合,储器可以从两侧密封。因此,在前密封件306在引入样品流体之后也可以是可再密封的。密封件306的再密封可以允许混合,同时避免输出流体例如经由通道302从储器的无意地释放。
如所指出的,样品流体可以使用运载体经由第一开口引入。在运载体在引入样品流体之后留在盒中的实施方案中,再密封可以防止流体经由存在于运载体和第一通道的内表面之间的任何间隙而通过。
图6a和图6b描绘了根据本公开的某些实施方案的在前密封件306。图6a和图6b中所示的实施方案可适合于在输送或引入样品流体后保持在第一通道内的运载体。
根据所示出的实施方案,所描绘的在前密封306可以包括两个单独的密封件,即第一密封件401和第二密封件402。图6a描绘了在使用运载体403引入样品流体之前的在前密封件,而图6b描绘了当运载体穿透在前密封件306插入时的密封件。在一些实施方案中,运载体403可以包括与采样器202相关联的毛细管。
第一密封件401配置成防止在引入样品流体之前经由第一开口从储器流动(上面所提到的第一个作用)。因此,与在后密封件类似,第一密封件401可以是由粘合剂或塞子形成的易碎密封件。在运载体403经由第一开口插入到储器中时,运载体403破坏密封件401,如图6b中所示。
第二密封件402可以操作以在运载体插入后再密封储器。第二密封件配置成防止通过运载体(更准确地说,运载体的外表面)和通道的内表面之间的交界部泄漏。根据某些实施方案,密封件402可以包括安装在通道内的柔性环(例如,o形环)。该环的内径比运载体的直径小。因此,尽管密封件402允许运载体通过,但是其可以围绕运载体紧紧封闭以防止泄漏。根据可选择的实施方案,第一密封件401和第二密封件402可以交换,即密封件402可以在第一密封件401之前出现。
运载体403可以是中空的。因此,在将其插入之后,可能会发生从储器出来的流动或泄漏进入或经过运载体的中空内部空间。这种泄漏可以通过位于运载体内的疏水膜来防止。
图7a和图7b描述了根据本公开的某些实施方案的另一在前密封件。如图7a和图7b中所示的密封件包括单个构件,该构件的功能类似于组合的密封件401和密封件402的功能。例如,在图7a中,具有居中的肩部的阻塞件(stopper)501被模制在第一通道302内。阻塞件501防止在引入样品流体之前经由第一开口301从储器流动。当插入运载体403时,如图7b所图示的,阻塞件501的中心破裂,同时阻塞件的肩部堵塞了运载体的外表面和通道的内表面之间的交界部,从而防止进一步泄漏到样品流体引入。根据某些实施方案,阻塞件501可以由软的粘合剂弹性体形成。然而,阻塞件501也可以使用其它材料形成。
某些实施方案可以包括制备用于分析的样品流体的过程,例如通过激活单元24与盒204的相互作用(将在下文更详细地描述)。例如,样品流体的运载体403可以经由第一开口301插入第一通道302中。运载体使联接到第一通道的在前密封件306破裂并将样品流体输送到储器303中(图6a)。在储器内,可以相对于样品流体执行程序,例如将输送的样品流体与预装载到储器中的物质混合从而获得输出流体。可以通过在储器的可按压部分上施加间歇压力来实现混合。当完成该程序时,可以通过以在在后密封件的位置处产生超阈值压力的方式按压储器而使在后密封件307(图5)破坏。超阈值压力可以导致密封件307的打开和所获得的输出流体从储器的释放。释放的输出流体然后可以经由第二通道304和第二开口305流入分析隔室203中,输出流体可以在该分析隔室203中进行分析。
图8示出了根据本公开的某些实施方案的包括包含两个隔室的储器的盒的截面。两个隔室701(任一个或这两个可以预装载有物质)通过流动路径702互相连接。第一隔室经由第一通道302连接到第一开口301,而第二隔室经由第二通道304连接第二开口305,两个隔室中的任一个或两个可以包括可按压部分。
在两个隔室都包括可按压部分的情况下,通过交替地施加到两个可按压部分(例如一个隔室然后是另一个)的压力实现混合可以是可能的。隔室701之间的流动路径702可导致射流发生,射流可以增强混合。例如通过同时按压两个隔室和/或通过施加比用于混合所施加的压力更强的压力,可以引起在后的密封件307的破坏。
在仅有一个可按压部分的情况下,在隔室中的一个上,通过间歇地按压该部分实现混合可以是可能的。通过在可按压部分上施加超阈值压力可导致在后密封件307破坏。
图9示出了根据本公开的某些实施方案的包括由两个储器构成的制备单元的盒的截面。联接到第一开口301的第一储器801可以包括可按压的储器,而联接到第二开口305的第二储器802可以包括可按压或者不可按压的储器。这两个储器可以通过连接通道803连接,连接通道803又可以由密封件804密封。两个储器可定位在密封件306和307之间,第一储器801之前是密封件306,而第二储器802之后是密封件307。
尽管每个储器可以与相应的输入流体和相应的输出流体关联,但是第一储器801的输入流体(经由第一开口引入至第一储器801)可以包括样品流体。在第一储器内可以执行影响流体的程序。该程序可称为“第一程序”。通过在密封件804上作用适当的压力(例如与密封件804相关联的超阈值的压力),可以使密封件804破裂,从而导致输出流体从第一储器801释放,使得输出流体传送到第二储器802。第一储器的输出流体可以用作第二储器的输入流体。
在密封件804是易碎密封件的情况下,一旦密封件被破裂,储器801和802之间的通道803可保持打开,并且在储器801和802之间在两个方向上(即从801到802和从802到801)的流体流动可以是可能的。在密封件804包括易碎密封件的情况下,一旦密封件被破裂,两个储器实际上可以形成单个储器的两个隔室。因此,在连接通道803中具有易碎密封件的实施方案中,在该密封件破裂之后,第一储器801的输出流体可以在两个前述储器之间来回流动,并且当流体存在于这些隔室中时,可能受到与储器801或储器802相关联的任何程序影响。此外,在使易碎密封件804破裂以有效地形成具有两个隔室的单个储器之后,连接单个储器的两个隔室的通道803可以被称为“隔室”801与“隔室”802以及因此与开口305的联接部。
在其它实施方案中,例如,密封件804是可再密封的,在将储器801的输出流体传送到储器802之后,密封件804可被再密封,使得流体可被阻止行进回到储器801。可再密封的密封件的示例可包括阀。可选择地或另外地,某些实施方案可包括可再密封的连接通道803,在该连接通道803中可以进行再密封,例如通过将压力重新引入到连接通道803以物理地堵塞通道803的开口并防止流体流过通道803。
在第二储器802内,可进行“第二程序”。通过在密封件307上产生适当的压力水平,可以使该密封件破裂,因此导致从第二储器802朝向第二开口305释放输出流体。第二储器的输出流体可以构成基于储器801和802形成的制备单元的输出流体。该制备单元的输出流体可以经由第二开口305流入分析隔室(比如图4的分析隔室203),在该分析隔室中对输出流体进行分析。
在制备单元中的每个储器可以配置成执行特定程序或以其它方式与特定程序相关联。例如,如果第一储器获得样品流体,则与第一储器相关联的过程可以影响该样品流体,得到该样品流体的衍生物。衍生物可包括在样品流体的任一种中或两种中的或在包含在样品流体内的细胞或组分中所发生的变化。该变化可以包括化学变化、生物化学变化、物理变化等。化学变化的示例可以包括在ph方面的变化、细胞组分的氧化/还原或化学剂(比如染料)铰合(hinge)至其;生物化学变化的示例可以包括抗体结合至配体;且物理变化的示例可以包括在粘弹性性质方面、在温度方面或在稀释剂的浓度方面的变化。在一些实施方案中,样品流体可以被认为是其自身的衍生物,即样品流体的衍生物。因此,程序可以获得作为输入的样品流体衍生物,并且产生输出,该输出是该衍生物的衍生物。在这样的实施方案中,储器的输入可称为样品流体的第一衍生物,而储器的输出可称为样品流体的第二衍生物。相同的参考方案可用于指代在制备单元中的所有储器:每个储器可以得到输入流体,该输入流体是样品流体的衍生物。在样品流体上进行的第一过程可以提供样品流体的第一衍生物,对样品流体的第一衍生物执行的第二过程可以为与制备单元的储器相关联的每个过程提供样品流体的第二衍生物等等。
由于储器可连续布置,因此这些程序也可连续发生。例如,某个储器中的一系列程序可以产生样品流体的第二衍生物,该第二衍生物成为该储器的输出。下一个储器可以获得作为从在前的储器输入的第二衍生物,并提供样品流体的第三衍生物。这种链可以持续,直到最后的储器朝向最终开口传送其相应的样品流体衍生物。在某些情况下,储器的输出不只是顺序地传输到下一个储器。而是,在某些情况下,两个储器之间的诸如易碎密封件的密封件可以被打开,并且两个储器中的任何流体可以混合以产生样品流体的新的衍生物。然而,值得注意的是,新的衍生物可跨越两个储器中的两者被共用(例如,通过来回混合过程),使得新的衍生物流体中的至少一些存在于两个储器中。
连续程序的示例可以包括细胞的免疫标记:使用一级抗体标记可以在第一储器中进行,接下来使用二级抗体连续标记在第二储器中进行。另一示例可以包括用两种染色试剂(这两种试剂在储存期间必须是分离的)进行的血液样品的白细胞的鉴别染色。用第一试剂染色的程序在第一储器中执行,随后用第二试剂的染色可在连续的、可能地最后一个储器中进行。
但是应理解的是,根据本公开的实施方案,该程序可以在储器内执行,其中在输出流体的制备中每个储器增加了一个阶段,一起产生累积的连续的过程。此过程可导致流体和试剂有效且完全地混合。
图10a和图10b示出了根据本公开的某些实施方案的两种制备单元构造。如图10a和图10b中所示,制备单元中的一个包括包含两个互连隔室701的单个储器。这种制备单元已在上面参考图8进行描述。图10a和图10b中所示的另一个制备单元包括两个储器801和储器802,储器801和储器802由通道803连接并且由密封件804密封。这种制备单元已在上面参考图9进行描述。每个制备单元具有相应的第一开口301和相应的第二开口305。两个制备单元的第一开口可以构成盒的第一开口。
通过图10a和图10b所描绘的盒的两种构造关于作为制备单元的组合的出口提供的第二开口是不同的。例如,在一个实施方案中,图10a所描绘的盒可以包括单个盒第二开口901,该单个盒第二开口901与相应制备单元的第二开口305流体连通。在另一个实施方案中,图10b所描绘的盒可以包括与每个制备单元相关联的第二开口305,其中第二开口305中的每一个还构成制备隔室201的出口。
在所描述的实施方案中,盒的每个制备单元可以配置成从相应的运载体中接收样品流体。然而,在其它实施方案中,可以构造单个运载体,使得单个运载体可以将样品流体引入到盒的多个制备单元中。样品流体可以同时地或不同时地引入到盒的制备单元中。
每个制备单元的输出流体可以在不同时间流入分析隔室中。此外,每个制备单元的输出流体可以经历单独的分析过程。
包括两个并行的制备单元的实施方案可使能够进行与样品流体有关的两个单独的独立程序。例如,在某些实施方案中,该盒可以配置成执行全血计数。在这样的实施方案中,该盒可以包括两个并行的制备单元,其中一个制备单元配置成制备用于分析的红细胞,且另一个制备单元配置成制备用于分析的白细胞。
虽然图10a和图10b所描绘的盒包括两个制备单元,但是也可以根据特定应用的要求使用其它构造。包括在盒中的制备单元的数量以及包括在每个制备单元中的储器的数量和包含多于一个隔室的储器的数量可以不同,因为该盒的构造可以适合执行所需的程序和/或用于制备用于某些分析程序的样品流体的目的。
图11示意性地图示了根据本公开的某些实施方案的分析隔室203。分析隔室203可包括分析器皿1002,分析器皿1002配置成接收由一个制备单元或多个制备单元传送的输出流体,并配置成以允许分析输出流体的方式提供输出流体。第三通道1004可联接到分析器皿1002,并且可以配置成从其排空一次性输出流体。在一些实施方案中,分析器皿和第三通道一起可以包括分析单元。配置成储存一次性输出流体的废物容器1005可以经由第三通道1004联接到分析单元。废物容器1005还可以经由第四通道1006和开口1007联接到真空泵。
输出流体可以从制备单元经由第三开口1001流入到分析单元203中。在分析器皿1002内,输出流体可以提供到分析系统101。经过分析后,输出流体可以经由第三通道1004进入废物容器1005中被处置并储存在其中。
输出流体在分析单元内的流动可以通过由真空泵产生的抽吸力驱动,真空泵可以作为分析系统101的一部分被包括。真空泵通过开口1007、第四通道1006、开口1008和废物容器1005可联接到分析单元。尽管抽吸力可以施加到废物容器1005,但是所储存的输出流体可能不会从其流出。反而,废物容器可以设计为集液器。开口1008可以位于容器1005中所储存的输出流体的液面上方,以提供集液器。
在一些实施方案中,分析器皿1002可以是微通道1003,其配置成使包含在输出流体中的细胞对准成便于分析的图案。例如,在一些实施方案中,微通道1003可以使在输出流体中流动的细胞对准到单个的平面中,这可以便于通过照相机获取流动细胞的图像。在其它的实施方案中,这样的细胞可以通过例如血细胞计数器中的聚焦光束/激光束来探测。可以通过称为粘弹性聚焦的方法来进行细胞的对准。粘弹性聚焦在题为“systemsandmethodsforfocusingparticles”的pct公布第wo2008/149365号中描述,而配置成用于粘弹性聚焦的微通道在题为“microfluidicsystemandmethodformanufacturingthesame”的pct公布第wo2010/013238号中进一步描述,这两个pct公布通过引用并入本文。然后可以通过微通道1003的透明或半透明表面(例如,可视区域)光学地分析对准的细胞。
图12示意性地图示了根据本公开的某些实施方案的另一分析隔室203。图12的分析隔室203可以配置成确定血液血红蛋白的水平。这个隔室可包括分析器皿1002,该分析器皿1002可以包括联接到第三通道1103的分析储器1101。通道1103可以包括例如相对于分析储器1101的小的横截面和长的长度。
分析储器1101可容纳粉末状氧化剂和/或裂解剂。该剂可以是十二烷基硫酸钠(sds)、tritonx或另外的合适的氧化剂/裂解剂。当储器1101填充有输出流体(该输出流体可以包括血液样品的衍生物)时,氧化剂可以被溶解。溶解的氧化剂裂解血液样品的衍生物的红细胞,这可以导致血红蛋白的释放。然后,所释放的血红蛋白可被氧化剂氧化以形成高铁血红蛋白(高铁血红蛋白是不可以释放结合的氧的血红蛋白的形式)。然后,可以使用光谱仪通过测量一个或更多个波长的吸收来确定高铁血红蛋白的浓度。因此,在一些实施方案中,在该实施方案中的流体分析器22可包括光谱仪。
根据某些实施方案,粉剂可以自由地存在于储器1101内。可选地,粉剂可以涂覆储器1101的内表面。为了扩大该剂和血液试样品的衍生物之间的接触面积,根据某些实施方案,储器的内表面可以包含涂覆有该剂的凸起,比如柱状物、挡板或其它结构。可选地或另外地,粉末状的氧化剂可以附着到运载体,比如存在于储器中(例如填充储器)的海绵。除了粉剂,例如可使用其它剂,例如凝胶。
血红蛋白氧化和吸收测量可能各自需要一定的时间量。因此,血液样品的衍生物可以保留在分析储器内一段合适的时间。在一些实施方案中,可能的是,通过将阻力施加至流动,因而使流动减缓来实现样品流体在分析储器中停留。一种用于施加这种阻力的方法可以借助于联接到分析储器1101的具有小横截面的长的第三通道1103。当通道是空的时,可提供流动的零阻力或低的阻力。在这样的条件下,血液样品的衍生物可以经由第三开口1001自由地流到分析器皿1002和分析储器1101中。然而,用血液样品的衍生物填充第三通道可能会导致阻力增大,这可能减缓或停止在分析储器1101中的流动。
图13示意性地图示了根据本公开的某些实施方案的包括两个分析单元的分析隔室203。分析单元中的一个包括微通道1003,类似于图11中所描绘的分析单元。其它分析单元包括分析储器1101,类似于图12中所描绘的分析单元。在一些实施方案中,为了从一个或更多个制备单元中获得输出流体,两个分析单元可在一侧上联接到第三开口1001。分析单元可以在另一侧上联接到废物容器1005,在废物容器1005中可以处置一次性流体。在一些实施方案中,两个分析单元可以并行地构造,如图13中所示。
应当注意,分析隔室内的这种并行布置的分析单元可以使能够并行地进行输出流体的两种不同类型的分析。例如,使用通过图13描绘的分析隔室,可以进行细胞计数和血液样品衍生物的血红蛋白水平的测量。两种类型的分析可以使用包括在流体分析器22中的不同的分析模块(例如,照相机、光谱仪等)进行。
图14a和图14b示出了根据本公开的某些实施方案的包括制备隔室201和分析隔室203的盒。盒204的制备隔室201已经在上面参考图10a和图10b进行了描述。在图14a和图14b中提供的示例中,制备隔室可包括两个制备单元,第一单元和第二单元。可包括包含两个互连隔室701的单个储器的第一制备单元在上面已经关于图8进行了描述。包括储器801和储器802的第二制备单元在上面已经参考图9进行了详细描述。
图14a和14b的分析隔室203可以容纳两个分析单元。分析单元中的包括微通道1003的一个分析单元可以配置成使包含在输出流体中的细胞对准到单个平面中,从而允许使用照相机拍摄流动的细胞的图像,或者如在血细胞计数器中所进行的通过聚焦光束/激光束来探测流动的细胞。包括联接到长的小横截面的第三通道1004的分析储器1101的另一个分析单元可以配置成例如使用光谱仪确定血红蛋白水平。
为了允许制备的用于分析的输出流体从制备隔室201流动到分析隔室203,两个隔室可通过制备隔室的联接到分析隔室的开口1001的开口901相互连接。
根据某些实施方案,盒204可以构造成接收血液样品并且可以使能够执行血细胞计数。通过盒204执行的血细胞计数可以包括确定样品中存在的红细胞、白细胞(总数)和血小板的数量,以及确定每种白细胞类型的数目(分类计数)。白细胞类型可以是中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞和单核细胞或其一部分,白细胞的其他类型和子类型也可以被计数。此外,所公开的实施方案可以适用于在血液中循环的任何类型的细胞,包括例如循环的肿瘤细胞、血小板聚集等等。
在所描述的实施方案中,细胞计数可以通过由照相机获取流动细胞的图像的方式或通过如在细胞仪计数器中进行的聚焦光束/激光束探测来进行。为了允许可靠的计数,细胞可以被引入到分析光学器件的焦距位置。因此,细胞将例如通过粘弹性聚焦在单个平面中对准。因此,该方法基于具有某些粘弹性性质的聚焦介质中的悬浮细胞,该聚焦介质如果在一定几何形状的微通道(例如具有大于100微米的长度和小于100微米例如在5微米和100微米之间的至少一个横截面尺寸)中流动的话引起悬浮于其中的细胞对准到单个的平面中。在盒204的制备隔室201中进行的用于计数的样品流体的制备可包括将聚焦介质添加到样品流体,从而产生样品流体的衍生物。
第一制备单元可以配置成制备用于确定红细胞、白细胞(总数)和存在于其中的血小板的数量的血液样品。容纳在储器701中的物质包括具有添加了表面活性剂的聚焦介质。聚焦介质可以包括包含例如可溶性高分子量聚合物的缓冲液。缓冲液可以包括适合于管理活细胞的任何等渗缓冲液,包括,例如磷酸盐缓冲盐水(pbs)。适合于提供具有粘弹性性质的血液样品的可溶性聚合物的示例包括聚丙烯酰胺(paa)、聚乙二醇(peg)、丙二醇等。添加到聚焦介质的表面活性剂可以作为球化剂,该球化剂可引起红细胞的形状从双凹圆蝶形变成球形,这可以有助于获得细胞的更高质量的图像。表面活性剂的示例包括sds(十二烷基硫酸钠)和ddaps(十二烷基二甲基铵丙磺酸盐)。例如在题为“systemsandmethodsforfocusingparticles”的pct公布第wo2008/149365号中公开了聚焦介质的组合物,该pct公布通过引用并入本文。
通过储器701进行的程序可以包括将所输送的血液样品与聚焦介质混合。混合完成之后,可通过压力使在后密封件307破裂,从而允许所产生的输出流体流入到分析隔室203中。
第二制备单元可以配置成制备用于白细胞类型的分类计数的血液样品。在某些实施方案中,该制备可包括细胞的化学染色,其中两个连续的染色程序可以在制备单元的储器801和储器802中进行。
容纳在储器801中的物质可包括溶解在聚焦介质中的细胞染色试剂。细胞染色试剂的实例包括荧光桃红b(phloxineb)、比布列西猩红(biebrichscarlet)和基本橙色21(basicorange21)。由于在一些情况下可能需要细胞的固定,因此也可包括固定试剂,包括例如福尔马林或甲醛。在将血液样品与物质混合后,可以进行培养,从而允许染色。在预定的培养时间结束时,将储器801与储器802分离的密封件804可通过压力破裂,导致所生成的输出流体向储器802释放。
容纳在储器802中的物质可包括溶解在聚焦介质中的其它细胞染色试剂。包括在储器802中的细胞染色试剂的例子可包括甲基绿、亚甲基蓝和barrel'sblue。在将输入流体(其构成储器801的输出流体)与物质混合之后,可以进行第二次培养,允许发生第二染色过程。在第二预定培养时间结束时,第二制备单元的密封件307可以通过压力破裂,允许所产生的输出流体流入分析隔室203中。
在一些实施方案中,用于分析的细胞的制备可以包括细胞的基于免疫的染色。在这些实施方案中,制备单元的一个或两个储器可容纳适合于免疫染色的试剂,其中该试剂和聚焦介质可以容纳在单个储器内或在不同的储器内。适于免疫染色的试剂的示例包括不同的颜色的抗体涂覆的微珠,如染剂的组合和cd14/cd15。
从两个制备单元的第二开口305流出的输出流体可以传送到联接到两个分析单元的分析器皿的单个通道。输出流体的分析可以顺序地或同时地进行。顺序分析可以通过暂时地分离两种输出流体的流动而成为可能,这种分离可以在制备隔室中来控制。如上面所描述的,由第一制备单元所进行的制备过程可包括在单个储器中混合而没有培养,而由第二制备单元所进行的制备过程除了可包括在两个不同的储器中混合之外还可包括可能需要培养时间的两个染色程序。因此,在第二制备单元的输出流体准备好流入分析隔室中之前,第一制备单元的输出流体可以准备好流入分析隔室中。
当流入分析隔室203中时,第一制备单元的输出流体可以在两个图示的分析单元之间分开。流体的一部分可以进入微通道1003,在该微通道1003中,输出流体内的细胞可以经由例如粘弹性聚焦而对准到单个的平面中。然后,对准的细胞可以通过与微通道1003相关联的透明或半透明的表面或窗口进行光学分析。然后,输出流体流入废物容器1005中,输出流体可以储存在其中。输出流体的另一部分可以进入分析储器1101,在分析储器1101中,输出流体内的细胞被裂解并且其血红蛋白含量以参照图12所描述的方式被量化。
在使第二制备单元的密封件307破裂之前,可以中止第一制备单元的输出流体流入分析隔室中,以便最小化或阻止输出流体的混合,输出流体的混合可能阻碍分析。这由于第一制备单元的第二通道304是可再密封的而成为可能。例如,可以通过将压力施加到在后密封件或第一制备单元的第二通道304的另一个区域来进行通道的再密封。
如上所描述,联接到储器1101的第三通道1103的长度和横截面形状可以为储器中的流动提供阻力,特别是在某些条件下。因此,当使第二制备单元的密封件307破裂时,大体上所有的输出流体可以流入分析隔室203中,并且可以传送到微通道1003,而不是在两个分析单元之间分流。在微通道1003内,第二制备单元的输出流体内的细胞可对准到单个平面中,从而允许光学分析。然后,输出流体可以流入废物容器1005中,输出流体被储存在其中。
图15a、图15b和图15c示意性地描绘了根据当前描述的实施方案的采样器。采样器1400可配置成对流体进行采样并且例如以精确的量将流体引入到盒204中。图15a所描绘的采样器可以包括附接到手柄1402的运载体1401。在一些实施方案中,运载体可包括毛细管。在毛细管内,可以形成密封件/塞子,并且该密封件或塞子可以包括允许至少一些空气流动但阻止液体流动的任何类型的材料或构造。例如,在一些实施方案中,疏水膜1404可以附连在距毛细管出口的预定距离处。毛细管1401可包括任何类型的具有疏水膜附连在里面并且适合于特定应用的毛细管。例如,通过drummondaqua-captm微型分配器制造的毛细管可以在当前公开的实施方案中使用。
流体采样可通过将毛细管1401的出口浸没在流体中来进行。样品流体可以由毛细管力驱动到毛细管中。附连在毛细管1401内的疏水膜1404可促进这个过程,因为它允许被样品流体取代的空气流出。流体填充毛细管,直到到达疏水膜。应该理解的是,由于膜1404的疏水性质,流体不会与膜接触。因此,在膜内可能没有样品流体吸收,或者换句话说,膜没有发生流体体积的损失。因此,采样流体的最终体积可以基于疏水膜1404距毛细管出口的距离和通过毛细管的内径来确定。
一旦流体已被取样,它可通过将毛细管1401穿过盒204的第一开口301插入而被输送或引入到盒204中。在此阶段,可能发生样品流体从毛细管到储器303中的仅有限的泄漏,因为该流体可通过毛细管力保持在内部。柱塞1405可以用于将样品流体推出毛细管使样品流体进入到储器303中。图15b中所描绘的柱塞1405可以包括附接到保持构件1407的插入构件1406。插入构件1406可以配置成穿过位于手柄1402中的毛细管入口1403插入到毛细管1401中。柱塞推动疏水膜1404直到疏水膜1404到达毛细管出口,任选地导致全部样品流体输送到储器303中。应该考虑的是,如果插入构件1406不足够长以到达毛细管出口,则某些剂量的流体可能保留在毛细管中。因此,输送到储器中的样品流体的体积可以取决于相对于毛细管1401的长度的插入构件1406的长度。可以预先知道毛细管的直径与毛细管的长度以及柱塞的长度。因此,由采样器可转移的流体体积可以是预先确定的。
如上所描述的取样和推入可以使固定体积的样品流体能够输送到储器中。输送固定体积的流体的能力可能是重要的,因为因样品而不同的输送体积的偏差可能影响顺序的分析的可靠性。可能不需要将血液从采样器(在这种情况下为毛细管)中冲洗出来,因为疏水膜可以有助于确保所有样品流体例如血液被分配到第一储器中。
参考某些实施方案,柱塞1405可以作为分析系统101的一部分被包括,使得柱塞在当盒204放置到分析系统101的盒保持单元内时被插入到盒204中。然而,在不同的实施方案中,柱塞可构成单独的设备,而将柱塞插入到盒中可以在将盒放置到盒保持单元中之前进行。
如图15c所图示的,采样器可以包括两个运载体1401,其中,通过运载体进行的流体采样同时地或顺序地进行。包括两个运载体的图15c的采样器可以用于例如对血液进行采样并将血液输送到配置成允许进行血液计数的盒中。在一些实施方案中,采样器的两个运载体可以包括具有疏水膜的、抗凝剂涂覆的毛细管。涂覆毛细管的抗凝剂可用于防止采样血液的凝固。抗凝剂的示例包括edta(乙二胺四乙酸)。
由采样器1400的每个运载体1401采样的并且输送到盒204中的流体体积可以是小到20μl或甚至更少。因此,使用采样器1400进行血细胞计数,盒204和分析系统101可能需要从个体获得尽可能少的单滴血。这样的小体积的血液可能通过以例如通过家庭血糖监测装置进行的方式刺指尖或前臂来获得,从而免去从静脉抽血,从静脉抽血对患者、特别是儿童是不方便的。
在一些实施方案中,盒204可包括大体上刚性的框架,该框架至少部分地容纳具有一个或更多个制备单元的储器。图16示出了包括刚性框架1501的盒1500的一部分。刚性框架1501可包括任何刚性或半刚性材料。例如,在一些实施方案中,刚性框架1501可以由pmma、cop(环烯烃共聚物)、聚乙烯(polyethylene)、聚碳酸酯、聚丙烯、聚乙烯(polythene)等或其组合中的任一种制成。
刚性框架1501可以制成为包括与上述所描述的制备单元相关联一个或更多个的结构。例如,在一些实施方案中,刚性框架1501可以通过注射成型制成,并且可包括各种流动路径、入口、出口和/或储器元件(例如,形成在刚性框架的表面中的凹部,该凹部在用帽或覆盖层覆盖时提供储器)。刚性框架1501可以被提供为大体上单片的基底,例如,如图16中所示的。可选择地,刚性框架1501可以包括与盒204/1500相关联并且为盒204/1500的一个或更多个元件提供支撑的一个或更多个结构部件。
在一些实施方案中,刚性框架1501可包括分别通向流动通道1516和流动通道1517的开口1506和开口1507。开口1506和/或开口1507可依尺寸制作成接受含一定量样品流体的采样器。例如,开口1506和开口1507中的任一个或两个可依尺寸制作成接受与采样器1400相关联的毛细管1401。在一些实施方案中,开口1506和开口1507之间的间距可设置成与如图15c中所示的设置在双毛细管采样器上的毛细管1401之间的间距相匹配。
形成于刚性框架中或以其它方式与刚性框架关联的另外的通道1516和/或通道1517可配置成对准并稳定采样器的毛细管。这种构造可有利于将毛细管1401对准并插入到盒1500中。此外,这些通道可以帮助将毛细管引导到刚性框架或盒204内的期望位置,并且当插入到刚性框架1501中时可以防止毛细管损坏。
在一些实施方案中,开口1506和开口1507以及通道1516和通道1517可以为与盒1500相关联的一个或更多个储器提供流体流动路径。例如,如图16中所示,通道1516可以通向储器1504,并且通道1517可以通向储器1505。因此,提供到通道1516的样品流体可以流到储器1504,并且提供到通道1517的样品流体可以流到储器1505。应当理解,尽管图16示出了在大体上刚性的框架中的两个开口,但是大体上刚性的框架可以包括任何数量的开口而不脱离本公开的范围。在大体上刚性的框架中的开口中的一个或更多个可以配置成对准和稳定毛细管。
储器1504和储器1505可以作为盒1500的制备单元的一部分(如上所描述的)被包括。例如,储器1504可经由通道1520和密封件1507联接到另一储器1502。同样,储器1505可经由通道1521和密封件1508联接至另一储器1503。
在一些实施方案中,盒1500及其相关联的制备单元可以基于两部分式构造(two-partconstruction)来形成。例如,盒1500的第一部分可以包括刚性框架1501,该刚性框架1501包括用于提供与盒1500的制备单元相关联的结构的至少一部分的模制部件。盒的第二部分可包括设置在刚性框架1501上的薄膜1530。在刚性框架1501上设置薄膜1530可以完成制备单元的结构或部件的至少一部分。例如,储器1504(和图16中所示的其它储器)可以包括第一部分,该第一部分包括形成于刚性框架1501中的凹部。当薄膜1530放置在刚性框架之上时,薄膜的一部分将覆盖与储器1504相关联的凹部。此外,由弹性材料形成薄膜1530还可以使与盒1500关联的储器中的一个或更多个能够是可按压的,如上面所描述的。
薄膜1530可以由任何合适的材料形成。在一些实施方案中,薄膜1530可以由pvc、聚丙烯、聚乙烯、聚氨酯以及包含铝和pe的层压板,或者其组合来形成。
在一些实施方案中,刚性框架1501和薄膜1530中的一个或更多个由当暴露于热时可以结合在一起的材料形成。在构造如图16所示的盒1500的两部分式结构期间,可施加不同程度的热以实现期望的结果。例如,在施加高温(例如,140℃-180℃)的情况下,可以使薄膜1530永久地焊接到刚性框架1501的材料。在其中施加很少施加热量或不施加热量的其它区域中,薄膜1530可以保持未结合到下面的刚性框架。并且,在热量以低于材料的焊接阈值的水平(例如,100℃-130℃)被提供的区域中,薄膜1530的材料可与刚性框架1501的材料结合在一起,但这种结合可能是非永久的。也就是说,在这些区域中,所结合材料以后可以相互拉开。在一些实施方案中,可以例如使用具有多层结构的薄膜1530实现上面所描述的选择性结合。多层结构的第一子薄膜(例如,首先接触刚性框架1501的最下层)可包括与刚性框架1501的材料形成相对较弱的结合的材料。因此,在第一子薄膜已经结合到刚性框架1501的区域上的随后的力可以导致子薄膜的分离(例如,剥离),并且因此导致整个薄膜1530远离刚性框架1501。
在一些实施方案中,薄膜1530的多层结构可以包括设置在第一子薄膜上方的第二子薄膜。第二子薄膜可以通过施加较高的温度与刚性框架1501的材料形成更持久的结合。例如,在一些实施方案中,较高的温度可以引起第一子薄膜熔化,并从结合区域流走,这可以使第二子薄膜能够直接结合至刚性框架材料(永久地或半永久地)。
这种类型的结合可以促进构造与盒1500的制备单元相关联的部件。例如,在远离制备单元的结构的诸如区1531的区域中,可以施加高的温度以将薄膜1530的材料永久地焊接到刚性框架1501。在与储器1502、1503、1504、1505相关联并与通道1520和通道1521相关联的区域中,可以避免施加热以使得薄膜1530在这些区中保持与刚性框架1501脱离。在与密封件1507和密封件1508相关联的区中,可使用次级焊接加热水平使得薄膜1530被附加到或暂时结合到刚性框架1501。这些密封件可称为“剥离密封件(peelseal)”,当例如通过储器1504内的流体按压密封件1507来将压力施加在密封件上时,可导致薄膜1530从框架1501剥离。在这些情况下,流体可被允许流经密封件。虽然这些剥离密封件可能是易碎的,但是流经破坏的密封件1507或密封件1508的流体可通过例如在这些密封件的区域中将压力施加到薄膜1530而停止,以便在密封处关闭流体通路。
盒1500还可以包括分别设置在通道1516和通道1517内的密封件1518和密封件1519。密封件1518和密封件1519可以例如防止流体或预先装载到储器1504和储器1505的其它材料从盒逸出或被周围环境污染。
图17a图示了根据示例性的公开的实施方案的盒1700。如图17a中所示,该盒1700包括第一入口或开口1701、第一储器1702、第二储器1703、第二入口或开口1704、第三储器1705和第四储器1706。入口1701与第一储器1702相关联,并且入口1704与第三储器1705相关联。示例性盒还包括第一密封件1707、第二密封件1708以及第三密封件1709。密封件中的任一个或全部可以制造成如上描述的“剥离密封件”。如图17a中所示,第一流动路径跨越第一储器1702和第二储器1703、流体通道1720以及第一密封件1707形成。第二流动路径跨越第三储器1705和第四储器1706、流体通道1721、第二密封件1708和第三密封件1709形成。
第一流动路径可以配置成将血液或流体样品与第一试剂混合,而第二流动路径可以配置成将血液或流体样品与第二试剂混合。该试剂可以被预装载并且密封在储器中。可选地,该试剂可以经由盒中的入口注入储器中。该试剂可包括白细胞染剂(例如酸性染剂和碱性染剂)、裂解剂、生物标记和流体形式的至少一种高分子量聚合物中的至少一种。当按压储器中的一个或更多个时,可引起对应的密封间打开以使在储器中的任何流体沿相应的流动路径流动。
盒1700还可以包括缓冲剂隔室1710。缓冲剂隔室1710可包括在样品流体制备储器(例如储器1702和储器1703)和通向分析区段的流体出口1712之间的流动路径内。在一些实施方案中,管1711可以设置在出口1712处以将样品流体或其衍生物运送到一个或更多个分析区段。在一些实施方案中,在盒1700投入使用之前,缓冲剂隔室1710可以保持安全没有流体。当将样品流体接收到盒1700中(例如,经由入口1701和/或入口1704)时,样品流体可以提供到包括储器1702和储器1703的制备单元,并且根据上面描述的任何制备过程进行制备以用于分析。
在一些实施方案中,一旦样品流体(或者其衍生物)制备成并准备好用于分析,在分析之前样品流体/样品流体衍生物可以被提供到缓冲剂隔室1710。缓冲剂隔室1710可包括储器并且可以在分析流体之前用作盒1700内的临时保持位置。在一些实施方案中,由于进入缓冲剂隔室1710中的流速可能超过从缓冲剂隔室1710出来的流速,所以流体聚集在缓冲剂隔室1710中。在其它实施方案中,缓冲剂隔室1710可作为流体的传递室,其中从缓冲室出来的流体流速等于或在某些情况下超过进入缓冲剂隔室1710的流速。
提供给缓冲剂隔室1710的流体的量可以通过任何合适的技术来控制。在一些实施方案中,来自储器1702/1703的制备的样品流体可以通过打开密封件1707(例如,经由施加到密封件的超阈值压力、释放或去除与密封件1707相关联的物理障碍物来打开,或通过任何其它打开技术)而提供到缓冲剂隔室1710并将所需量的制备流体计量到缓冲剂隔室1710中。可以使用一个或更多个步进电动机,例如,以按预定量和/或以预定的速率按下储器1702和/或1703的部分,以便向缓冲剂隔室1710提供预定量的制备流体。
提供到缓冲剂隔室1710的流体可从缓冲剂隔室1710抽出以使用任何合适的技术来分析。例如,在一些实施方案中,真空可以经由管1711施加到出口1712,以便使流体从缓冲剂隔室1710流动。计量技术(例如包括步进马达、柱塞、流动控制密封件等)可以用于从缓冲剂隔室1710抽出预定量的流体以用于分析。
缓冲剂隔室1710可以根据特定构造的结构或基于特定的操作方案提供某些性能特性。例如,在操作期间,缓冲剂隔室1710可以用作电容器的流体模拟并且可在分析流体之前缓冲流体流动。缓冲剂隔室1710可以帮助减少存在于待分析的流体中的气泡的量。在一些实施方案中,从缓冲剂隔室1710抽取的用于分析的流体可以从缓冲剂隔室1710的存在于在缓冲剂隔室1710中的流体水平线下方的区域中抽取。提供到缓冲剂隔室1710的流体中的气泡(例如源自制备的流体穿过制备单元的一个或更多个部件的流动)可能倾向于积聚在缓冲剂隔室1710中的流体的表面上。通过从流体水平线下方抽取隔室1710中的流体,这种气泡可以保留在缓冲剂隔室1710中,并且从缓冲剂隔室1710抽出的用于分析的流体可以是无气泡的或可以至少包括比在缓冲剂隔室1710中存在的全部流体少的每单位体积气泡。另外,缓冲剂隔室1710可避免与控制密封件1707的操作特性有关的复杂性,以便提供用于分析的所需的流体流动。在一些实施方案中,提供到缓冲剂隔室1710的流体的量可以超过流体的量。
图17b和图17c提供了根据示例性的公开的实施方案的盒1900的透视图。图17b示出了盒1900的组装图,而图17c示出了盒1900的分解图。盒1900可以包括制备部分1901以及分析部分1902。如图17c中所示,盒1900可包括刚性框架或刚性部分1910。刚性部分1910可以制造成(例如通过模制或任何其它合适的技术)两部分式结构。如图所示,刚性框架1910可包括配置成与底部部分1912配合并附接到底部部分1912的顶部部分1911。
在一些实施方案中,刚性部分1910可以包括一个或更多个入口1920,该一个或多个入口1920可各自配置成接收、支撑和/或对准流体采样器,例如含一定量样品流体的毛细管。可以将各种流动路径制造到刚性部分1910中或制造到刚性部分1910上,以在盒1900内建立流体流动路径。例如,上面关于图17a的盒所描述的流动路径中的任一个或全部也可以包括在图17c的两部分式刚性框架1910中。
盒1900可以不仅制造成具有如图17c中所示的两部分式刚性框架1910而且还制造成具有两个或更多个柔性材料片。例如,盒1900可以包括第一片1970和第二片1980。在一些实施方案中,片层1970和片层1980可以包括柔性材料(例如聚合物或任何其它合适的弹性材料),并且可以在制造盒1900期间结合在一起。可以使用用于将柔性材料结合在一起的任何合适的技术。在一些实施方案中,层1970和层1980的不同区域可用不同的结合强度结合在一起。这样的构造对于例如永久或半永久地将特定的区域结合在一起以及更暂时地将其它区域结合在一起可能是有用的。例如,在一些区中,可通过在层1970和层1980之间形成暂时结合来形成易碎密封件,层1970和层1980可剥离开以打开密封件。
多种机构可以用于将层1970和层1980结合在一起。例如,可以使用粘合剂。在一些区中,比如区1984,在该区域中需要永久或半永久地结合,合适的粘合剂可用于在这些区中将层1970和层1980永久或半永久地结合在一起。同样,例如那些仅提供临时的、可剥离的结合的其它粘合剂也可以用于其它区中,例如其中可能需要临时结合以便产生易碎密封件的区1985。
这种结合还可以通过焊接来实现。例如,在一些实施方案中,电极可用于在层1970和层1980之间产生点焊。在这种实施方案中,两个层之间的结合强度可取决于在特定区域中的点焊的密度和/或形状。因此,区(比如区1984)可能需要高结合强度,可以使用与可使用较低点焊密度以提供临时可剥离的结合的区(比如区1985)相比较高的点焊密度。
层1970和层1980也可以经由其它机构结合在一起。例如,每个层1970和层1980可以包括两个子薄膜,比如与具有较高的熔融温度或结合温度的第二子薄膜相比具有较低熔融温度或结合温度的第一子薄膜。可以形成层1970和层1980,使得在结合期间,它们被定向成使得来自于层1970的第一子薄膜与层1980的第一子薄膜形成交界部,而层1970和层1980中的每个的第二子薄膜不相互接触。为了在特定的区(比如区域1985)中在易碎密封件位置处形成临时可剥离的结合,可施加低的温度(例如,在约100℃至约130℃的范围内),使得第一子薄膜结合在一起。随后可通过所结合的第一子薄膜的分离或通过撕裂由所结合的第一子薄膜形成的结构来剥离开在这个区域中结合的结构。为了例如在区1984中产生永久性或半永久性结合,可施加较高的温度(例如,在约140℃至约180℃的范围内)。这样的温度可引起第一子薄膜熔融和/或从待结合的区流走,从而使层1970和层1980的第二子薄膜能够接触并形成永久性或半永久性结合。包括粘合剂、点焊和/或多层的温度依赖性结合的结构的这样的结合技术也可以结合本文所描述的盒中的任一个来使用。
层1970和层1980可预制成或形成为包括各种结构,该各种结构当层1970和层1980结合在一起时用于提供流动路径、储器、密封件等。例如,层1970和层1980一旦结合在一起,可形成储器1940。这些储器可以是柔性的,并且因此,响应于按压是可变形的(即“可按压的”)。同样,层1970和层1980一起可以形成例如在储器、隔室等之间的流动路径中的易碎密封件。这种易碎密封件可包括如图17c中所示的区1985中的密封件。结合的层1970和层1980可以形成其它结构,例如缓冲剂隔室1960。激活单元
激活单元
图18提供了根据示例性公开的实施方案的分析系统的所选内部部件的示意性透视图表示。如先前关于图3所指出的,并且如图18进一步所示,为了制备包括在盒204上的样品,激活单元24可以与盒204的一个或更多个区段相互作用,以便制备用于分析的流体样品。在一些实施方案中,盒激活单元24可以包括并入在由马达1801、皮带1802和齿轮1803转动的旋转凸轮轴33上的一个或更多个凸轮32,以便按压(直接通过接触盒的区段或间接地通过与接触盒的一个或更多个活塞1804相互作用)盒的区段,进而制备、混合、移动、分配等用于分析的流体样品。激活单元24可以包括比所描述的凸轮、凸轮轴、马达、皮带、活塞和齿轮更多或更少的部件。
凸轮32和/或活塞1804可以被配置为与盒204的任何合适的部分相互作用以制备用于分析的流体样品、在盒204的一些部分内输送流体、打开密封件等。例如,凸轮和/或活塞1804可以与上述关于盒204的各个实施方案中的任何一个所描述的可按压部分、储器、缓冲剂室、隔室、流体通道等中的任一项相互作用。例如,如图18所示,凸轮轴33的旋转可引起凸轮32旋转。借助于凸轮32的各种形状的轮廓(例如包括围绕凸轮轴33径向分布的不同形状的凸角),凸轮32可以按压活塞1804以在各个不同的时间按下活塞1804。凸轮凸角可以布置成例如使活塞交替地按压邻近的流体储器,如上所述,以便反复地将流体从一个储器转移到另一个储器。
以下讨论提供关于包括凸轮32、凸轮轴33、活塞1804的激活单元24的各个构造的另外的细节以及激活单元24如何与盒204的各个区段相互作用。为了公开的目的,凸轮32不限于任何特定的结构或构造。凸轮32可以包括整体元件或者可以包括组装在一起的多个单独的部件。凸轮32可以具有任何合适的厚度和任何合适的凸角构造。此外,可以使用任何数量的凸轮轴33(例如,一个轴、两个、三个或更多个)。此外,马达1801(或用于激活单元24的任何其他驱动器)可以直接连接到凸轮轴33,或者可以通过齿轮、皮带等间接附接到凸轮轴33(如图18所示)。激活单元驱动机构(例如,马达1801)可以包括适于引起期望的激活运动(例如,使轴旋转)的任何驱动机构。驱动机构可以被配置为以固定或可变的速度驱动旋转机构,并且可以在操作期间改变速度和/或旋转方向。控制器20可以使马达1801根据适合于特定盒构造的预定模式来旋转凸轮轴33。
参照图19,根据结合某个盒204(该盒204包括可按压元件(例如,覆盖或自身构成储器801和802(图9)的全部或一部分的元件))的预定模式来驱动凸轮轴33,导致响应于凸轮32的移动而定时地按压和释放可按压元件。例如,如图19所示,凸轮32a具有接触活塞1804a的凸角(或节点),从而使活塞1804a部分地按下与储器801相关联的可按压元件。凸轮32b具有与凸轮32a相似的轮廓,但具有不同的旋转位置。因此,凸轮32b的长凸角尚未与活塞1804b接触。当凸轮轴33充分地旋转以使凸轮32b接触活塞1804b时(这将使活塞1804b向下移动并按压与储器802相关联的可按压元件),凸轮32a将会旋转成使得凸轮32a不再接触活塞1804a。因此,凸轮轴33连续不断地旋转将导致对与储器801和802相关联的可按压元件周期地且顺序地按压,使得随着凸轮32a和32b通过重复循环旋转,流体可以在储器801和802之间来回流动。当然,图19所示的布置只是一个示例。可以包括更多或更少的凸轮。可以包括更多或更少的活塞(或没有活塞),并且激活单元24可以配置成按下与盒204相关联的任何数量的不同结构或与其相互作用。另外,凸轮32可以具有任何合适的轮廓。在一些实施方案中,如图19所示,凸轮32中的任一个包括单个凸角(节点)。然而,在其他实施方案中,凸轮32中的任一个可以包括定位在不同径向位置处的多个凸角(节点),如图20所示。激活单元24内的多个凸轮32可以配置有相同或相似的宽度。在其他实施方案中,凸轮32可以包括不同的宽度。
除了将压力施加到与储器801和802相关联的可按压元件之外,凸轮32a和32b可以构造成引起对盒204的其他区域的压力。例如,在一些实施方案中,凸轮可以导致将压力施加到与盒204相关联的一个或更多个流体导管。在该压力下,这些流体导管可夹紧封闭(pinchshut),以便减少或防止流体在盒204的两个或更多个区之间流动。
压力图可基于凸轮的节点的构造与凸轮相关联。这样的图可以反映当凸轮旋转时由凸轮的节点赋予可按压元件的压力变化。这种定性压力图在图21中示出,其提供了在一个完整的旋转周期(360度)上由凸轮32赋予可按压元件上的压力的示意性定性表示。图21的压力图包括由凸轮32的旋转引起的三个压力阶段:升压阶段2101、保压阶段2102和减压阶段2103。上升阶段的斜率的绝对值不一定与减小阶段的斜率的绝对值相似,并且取决于凸轮32的凸角2105的轮廓。如上面所指出的,包括在激活单元24中的任一凸轮32可以被构造成具有任何期望的凸轮轮廓(例如,凸角形状、凸角数、凸角幅度、凸轮宽度等),以在盒204的一个或更多个特定位置处(例如,在与储器801和801相关联的可按压构件处)提供期望的压力分布。
除了将凸轮32旋转完整的360度周期以便向盒204的可按压元件施加压力之外,凸轮轴33可以在更有限的角度范围内旋转。例如,在一些实施方案中,可以通过在整个360度范围的一部分内(例如,在±10度范围内;±20度范围内;或者更大或更小的范围内)来回旋转凸轮轴33以及因此来回旋转凸轮32来获得期望的压力分布。
定位单元
如上所述并返回参考图3,系统101还可以包括定位单元26。定位单元26可以包括用于控制制备的样品(例如,在盒204上)相对于包括在流体分析器22中的分析部件的位置的各种部件。例如,在一些实施方案中,定位单元26可以包括经由轴36连接到台架35的马达34(或其他合适类型的致动器)。马达34可以用于旋转或以其它方式移动轴36以便移动台架35,盒204可以在分析期间保持在台架35上。台架35可以安装在倾斜轨道37上,使得轴36(其可以平行于倾斜轨道37延伸)的移动可以将台架35沿倾斜轨道37向上拉动或将台架35沿倾斜轨道37向下推动。由于沿轨道37的移动,台架35可以同时相对于流体分析器22沿x方向和z方向移动。如图3所示,x轴在与流体分析器22的分析轴线27大体上正交的方向上延伸,且z轴在与流体分析器22的分析轴线大体上平行的方向上延伸。在某些情况下,例如在流体分析器22包括诸如照相机的成像设备的情况下,分析轴线27可对应于成像设备的光轴。定位单元26可以包括比本文所描述的用于移动台架35的马达和轴更多或更少的部件。
台架35沿倾斜轨道37的移动可引起驻留在台架35上或保持抵靠着台架35的盒204的对应的移动。在一些实施方案中,台架35可以构造成具有大体上垂直于流体分析器22的分析轴线27(和z方向)并且大体上平行于x方向的顶表面(或样品支撑表面)(见图3)。因此,在一些实施方案中,当盒204被放置在台架35上时,盒204可以被布置成使得盒204的分析区(例如,微通道1003)沿着x方向并且垂直于分析轴线27延伸。
如图3所示,倾斜轨道37可以相对于x方向被包括。因此,台架35沿倾斜轨道37的移动可使盒204相对于分析单元22在x和z方向上平移。换句话说,台架35沿倾斜轨道37的移动可产生台架35/盒204在x方向上(垂直于分析轴线27)的第一运动分量和台架35/盒204在z方向上(平行于分析轴线27)的第二运动分量。由于在平行于分析轴线27的z方向上的运动,盒204上的制备样品的至少一部分可以相对于流体分析器22的分析部件进行聚焦。在流体分析器22包括一个或更多个成像器的实施方案中,这样的聚焦可以包括光学聚焦。
可以在定位单元26中采用任何合适类型的移动机构,以使台架35沿着倾斜轨道37移动。在一些实施方案中,定位单元26可包括马达34。在一些情况下,马达34可以包括步进马达,其可以提供精确性和可重复性的益处。可以使用其它类型的移动设备,例如伺服马达、直流马达编码器等。如所指出的,马达34可以联接到轴36(直接地或间接地通过一个或更多个联接部件),轴36又可以联接到台架35(直接地或间接地通过一个或更多个联接部件)。在一些实施方案中,轴36可以例如通过螺纹或螺纹部件与台架35接合。在这样的实施方案中,马达34可以使轴36转过所需的旋转角度,以便使台架35沿着倾斜轨道37平移期望的量(例如,通过轴36上的螺纹与包括在台架35中的或包括在与台架35相关联的部件中的对应的螺纹相互作用)。
这样的布置可以提供对样品聚焦进行精确控制而不需要同样精确的马达的益处。例如,在马达或其他类型的致动器使样品直接沿着成像器的光轴移动以使样品相对于成像器聚焦的实施方案中,聚焦调节的精度可取决于由马达或致动器提供的精度。并且,在可能需要微米或亚微米分辨率的应用中,提供所需精度水平的马达或致动器可能是昂贵的。
然而,在目前公开的实施方案中,可以用马达或致动器实现微米或亚微米分辨率,如果该马达或致动器配置成直接沿着分析单元22的光轴或分析轴线移动样品则该马达或致动器将不能提供这种分辨率。例如,使用所公开的倾斜轨道布置,使台架35沿倾斜轨道37平移足够引起rmm的水平移动(沿着x方向,如图3所示)将在z方向(图3)上引起rxsmm的移动(其中,s是与倾斜轨道相关的斜率比)。例如,在线性轨道37构造成具有1/10的斜率比(s)的情况下,台架35沿着倾斜轨道37平移足够在x方向上产生6微米的水平移动(r)将在z方向上产生0.6微米的移动。因此,通过利用倾斜轨道的倾斜,有效的竖直聚焦精度可以明显地增加,超出马达或其它致动器的精度(例如,2倍、5倍、10倍或甚至更高)。
虽然所公开的系统除了沿z轴移动以用于聚焦之外,还可能产生沿着x轴的移动,然而对于范围广泛的应用而言这种水平平移可能是无关紧要的。例如,在一些实施方案中,盒204上的流体检查区域可以包括微通道1003(如图11、13、14a或14b所示)。使用上述粘弹性聚焦技术,悬浮在粘弹介质中并流过微通道1003(例如,具有大于100微米的长度和小于100微米例如介于5微米和100微米之间的至少一个横截面尺寸)的细胞或颗粒可以变得物理地聚焦到或对准到单个平面中。例如,将流动的细胞布置到单个平面中可以有助于例如通过与分析单元22相关联的照相机来获取流动细胞的图像。可以分析这些图像以进行细胞计数。
使待分析的颗粒或细胞沿着微通道流动还可以有助于上述聚焦布置的使用。例如,因为流动的细胞可以物理地聚焦在沿着微通道1003延伸的平面中,所以可以在沿着适当布置着流动细胞的微通道长度的任何位置处对细胞进行分析。例如,在一些实施方案中,微通道可以是约1mm宽、40微米深和20mm长(当然,可以使用任何其它合适的尺寸,特别是如果它们允许粘弹性聚焦效果的话)。在进入微通道1003之后,细胞或颗粒可以在进入微通道的短距离内对准(例如,通过粘弹性聚焦)。例如,在一些实施方案中,细胞或颗粒的物理聚焦可以在从入口至微通道5mm或更小或者3mm或更小的范围内发生,并且当细胞或颗粒流过微通道的剩余长度时细胞或颗粒可以保持聚焦。聚焦的细胞可以在微通道1003的底部以上大约20微米的平面中对准,其中微通道具有40微米的深度。为了检查细胞或颗粒,分析单元22可以定位在沿着检查区的任何位置,例如微通道,在该微通道中待分析的细胞或颗粒表现出适于分析的布置。在所述的粘弹性聚焦示例中,包括例如照相机或其他类型的成像器的分析单元22可以定位在沿着微通道1003的任何位置,使得照相机或成像器的视野与其中待分析的细胞或颗粒被粘弹性地聚焦到单个平面中的区域重叠。例如,假设视野为约0.3mm×0.3mm,粘弹性聚焦的细胞或颗粒的图像可以沿着微通道在细胞或微粒被聚焦的任何位置获得。这可以包括在通道的1mm宽度内的任何位置以及从通道入口往下游到通道出口的约3mm的任何位置的区域,在上述示例中,该区域距入口约20mm。因为细胞或颗粒可能在流动,所以在沿着微通道的不同位置处收集图像可能是无关紧要的,因为从图像到图像捕获的细胞不管怎样都将因流动而改变。
这种定位合适的分析点的灵活性与上述聚焦系统兼容,这可以包括至少一些水平(x方向)平移以及用于在竖直方向(z)上聚焦的移动。在一些情况下,台架35沿倾斜轨道37的水平行进方向可以与包括在盒204上的微通道或其他检查区域对准。因此,当台架35沿倾斜轨道37平移时,分析单元22可以跟随微通道或其他检查区域的路径。在具体的示例中,当台架35和盒204相对于分析单元22沿着倾斜轨道37移动时,0.3mm×0.3mm视野的图像可以在具有1mm宽度的微通道1003的5mm的长度内拍摄。假设倾斜轨道37的斜率因子比为1/10,沿着微通道1003的5mm图像捕获区可以允许多达500微米的z移动,这足可以实现在整个微通道深度(例如,约30-40微米的深度)内的任何位置处进行光学聚焦或者大体上超出了实现该光学聚焦所需的z移动。
本公开的实施方案还可以包括自动聚焦功能。例如,在分析器单元22包括照相机或成像器的情况下,定位单元26可以由控制器20控制,以作为自动聚焦处理的一部分自动移动台架35,以用于将与分析器单元22相关联的成像部件光学聚焦在待分析流体的感兴趣的区域上。在一些实施方案中,控制器20可以使分析器单元22的成像部件实现与微通道1003内的细胞的粘弹性聚焦区域的位置一致的光学焦点。
自动聚焦过程可以根据用于实现相对于待分析的细胞或颗粒的期望聚焦水平的任何合适的过程来继续进行。在一些实施方案中,自动聚焦过程可以通过在沿z轴的一系列位置处(通过沿倾斜轨道37平移台架35)使用分析器单元22收集图像来继续进行。例如,台架35可以沿着倾斜轨道37平移,使得台架在z方向上在100微米的范围内移动(或移动任何其它合适的距离)。图像可以在z方向上每隔2微米(或以沿着轨道的任何预定距离间隔或以任何其它合适的间隔)来获取。可以分析在各个z位置处收集的图像(例如,使用控制器20)以确定关于感兴趣的细胞或颗粒的聚焦水平或质量。在一些实施方案中,分析可以包括可以表示特定z位置处的聚焦质量的数学评价标准(例如,空间频率分析)。在一些实施方案中,较高的空间频率可以表示较高的聚焦质量,而较低的空间频率可以表示较低的聚焦质量基于对各种z位置/轨道位置的扫描和对在其处捕获的图像的分析,可以确定对应于最高质量观察焦点的位置(例如,目标位置)。为了进行所需的流体分析(例如,细胞计数等),控制器20可以使台架35重新定位在确定为对应于最高观察聚焦质量的目标位置处。
另外,不是简单地将台架移动到最初被确定为具有最高观察聚焦质量的目标位置且然后在该位置执行流体分析,而是可以执行一个或更多个后续扫描。例如,在各个z方向上进行第一次扫描之后,可以对例如围绕先前确定的最高聚焦质量的目标位置在z方向上进行的越来越精细的移动进行一次或更多次附加扫描,以便改善对感兴趣的细胞或颗粒的聚焦水平。每次后续扫描可导致确定的新的目标位置。这样的后续扫描可以包括例如1.5微米、1微米、0.5微米或更小的z方向步长。
除了这种涉及在各个z位置上进行的多次扫描的迭代自动聚焦方法外或作为这种迭代自动聚焦方法的替代方案,控制器20还可以基于z位置的单次扫描来计算期望提供最高聚焦质量的z位置。例如,在该过程中,自动聚焦过程可以通过在沿z轴的一系列位置处(通过使台架35沿倾斜轨道37平移)使用分析器单元22收集图像来继续进行。在各个z位置/轨道位置处收集的图像可以被分析(例如,利用控制器20)以确定关于感兴趣的细胞或颗粒的聚焦水平或聚焦质量。各个z位置/轨道位置处的聚焦质量水平可用于预测最高聚焦质量的z位置/位置。例如,控制器20可以基于观察到的聚焦质量值推断出最高聚焦质量z位置/轨道位置(例如,目标位置),可以使用曲线拟合技术或任何其他合适类型的计算来预测预期提供最高聚焦质量的z位置。一旦确定了该目标位置,则控制器20可以使台架35沿着倾斜轨道37重新定位,使得该台架定位在计算出的目标位置。
应注意,所确定的提供最高聚焦质量的z位置(无论是观察所得或还是计算所得的)可以对应于或可以不对应于分析器单元22与盒204、台架35或要分析的细胞之间的任何特定距离。而是,在一些情况下,所确定的提供最高聚焦质量的z位置可以仅对应于控制器20相对于定位系统26的操作跟踪的值。换句话说,控制器26可以不对分析器单元的任何部分与盒的任何部分或盒中容纳的流体之间的任何实际竖直距离z进行确定。相反,控制器20可以跟踪电马达34的位置,并将其用作跟踪观察到的聚焦质量值的基础。然而,由于每个唯一的马达位置可以对应于盒204的唯一的z位置,例如,本公开中对所跟踪的z位置、所确定的z位置等的所有引用应理解为跟踪、确定等马达位置或控制器20可以用于指引(index)台架35沿倾斜轨道37的移动的任何其他量的同义词。例如,马达34的运动可能导致台架35沿倾斜轨道37的对应的运动l,使得马达位置可以使能够确定台架35沿倾斜轨道37的位置。台架35(以及因此盒204)因沿倾斜轨道37的平移l而产生的在z方向上的移动可以表示为z=l*sin(a)。在较小的倾斜角度下,正切近似等于sin,且因此,在小的角度下,倾斜率s近似为sin(a)。因此,在较小的倾斜角度下,在平行于分析轴线27的z方向上的z(台架/盒的运动分量)近似等于沿着倾斜轨道的平移l乘以倾斜率s。
在一些实施方案中,分析可以包括可以指示特定z位置处的聚焦质量的合适的数学标准的评估(例如,空间频率分析)。在一些实施方案中,较高的空间频率可以指示较高的聚焦质量,且较低的空间频率可以指示较低的聚焦质量。基于对各个z位置的扫描和对其处所捕获的图像的分析,可以确定最高质量聚焦的位置。为了进行所需的流体分析(例如,细胞计数等),控制器20可以使台架35重新定位在确定为对应于最高观察聚焦质量的位置处。
所公开的系统还可以包括自动聚焦验证步骤。例如,如上所指出的,基于在各个z位置/轨道位置处观察到的聚焦质量值,可以计算出目标位置。所计算的目标位置可以对应于期望提供最高质量聚焦的z位置/轨道位置。为了验证计算结果,控制器20可以将台架35定位在期望的z位置/轨道位置,通过分析单元22收集图像,分析所收集的图像,并且确定聚焦质量是否如预期的那样。
在所公开的系统中,某些系统可以彼此关联以提供至少某种水平的机械隔离。例如,如图3和图18所示,分析器单元22可以被安装或联接到框架38,马达34和倾斜轨道37也联接到框架38。然而,台架35和激活单元24不联接到框架38。而是,例如,在马达34和轴36的影响下,台架35和激活单元24都沿着倾斜轨道37一起自由地滑动。
由于这种构造,由激活单元24中的各个部件的运动对流体分析产生的潜在影响可以被减小或消除。例如,通过将台架35和激活单元24机械联接在一起,凸轮32和/或活塞1804的运动可以操作以在盒204上施加向下的力,该力可以平移到台架35。然而,由于激活单元(包括凸轮32和活塞1804)与台架35安装在一起,来自凸轮32和/或活塞1804的运动的力不会传递到线性轨道37。这可能是有益的,因为施加在轨道上的任何力可能潜在地损坏轨道或阻碍台架35沿轨道的运动。而且,任何不保持在盒/台架/激活单元系统内部的力可能导致盒与分析器单元22之间的相对运动,且因此影响或改变分析器单元22相对于盒204内的流体的聚焦,这可能妨碍到流体分析。
但对于本领域的技术人员显然的是,可在所公开的流体分析系统中作出各种修改和变化而不脱离本公开的范围。考虑到本文公开的公开内容的说明书和实践,所公开系统的其他实施方案对于本领域的技术人员将是明显的。
- 还没有人留言评论。精彩留言会获得点赞!