液相色谱串联质谱测定维生素B12的方法及试剂盒与流程
本发明涉及维生素检测领域,特别涉及一种液相色谱串联质谱测定维生素b12的方法及试剂盒。
背景技术:
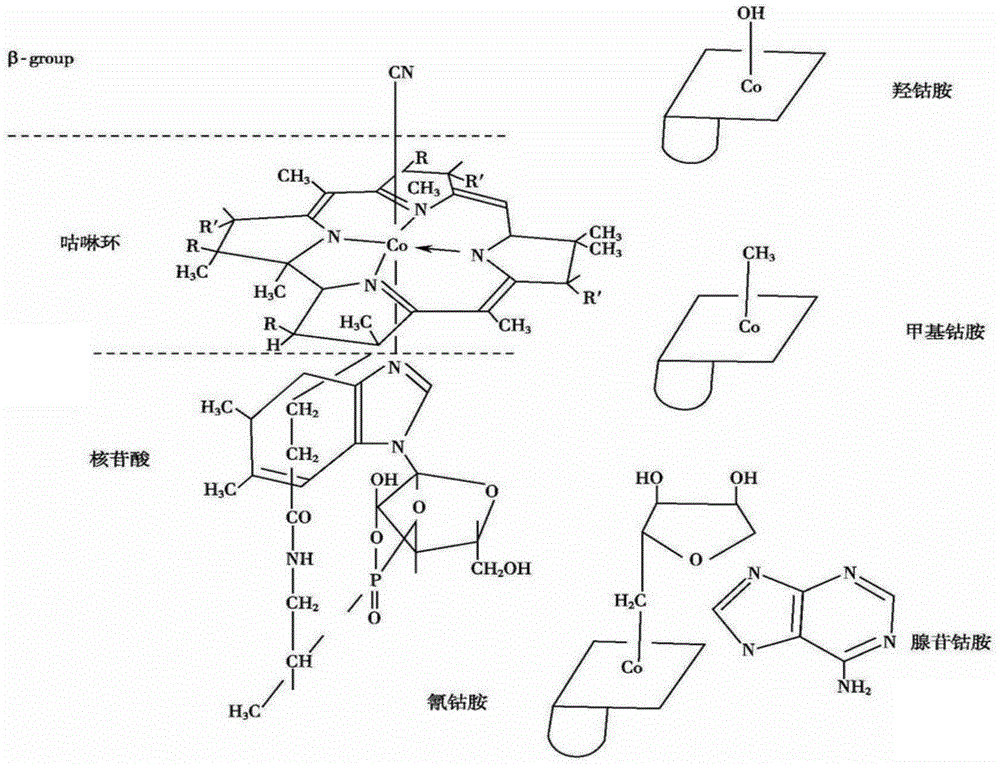
维生素b12是一类含有咕啉(corrin)环的类咕啉(corrinoids)化合物,维生素b12通俗名称又叫做“钴胺素(cobalamin)”,是唯一的一种含金属元素的维生素。然而人血清中大约1/3的维生素b12并非钴胺素,而是其他的类咕啉,它们在代谢上对人体是不具有生物学活性的。甲钴胺素和5′-脱氧腺苷钴胺素是维生素b12的活性型,也是血液中存在的主要形式。
人体不能合成维生素b12,主要依靠动物性食品提供,含量丰富者有肝肾组织、肉类、蛋类和乳类制品。维生素b12在人体代谢当中起到非常重要的作用,其可作为甲基丙二酸单酰辅酶a异构酶的辅酶,参与甲基丙二酸单酰辅酶a转变为琥珀酸单酰辅酶a的反应,该反应在奇数碳原子脂肪酸的代谢中起重要作用。维生素b12亦可作为β-甲基天门冬氨酸变构酶的辅酶,参与β-甲基天门冬氨酸向谷氨酸转化的过程。此外,维生素b12与叶酸协同参与甲基转移作用,影响体内的多种代谢过程。维生素b12缺乏时,可导致dna合成障碍和巨幼细胞贫血,影响神经髓鞘形成,从而出现神经系统症状。
另外,人类血浆中存在3种维生素b12的结合蛋白,即tcⅰ、tcⅱ、tcⅲ(transcobalaminⅰ、ⅱ、ⅲ),正常情况下,约80%以上的血清维生素b12会与tcⅰ和tcⅲ结合,称为血清全结合咕啉,仅20%与tcⅱ相结合,形成holotcⅱ。全结合咕啉的半衰期约为240小时,holotcⅱ的半衰期仅为6分钟。因此总血清维生素b12含量可作为一类主要的生物标志物用于体现机体维生素b12水平。
目前,维生素b12的检测方法有多种,包括化学发光免疫法、微生物法和同位素放射免疫方法等,然而免疫检测方法和微生物方法有很多的弊端,如下:
第一、免疫反应对反应条件的要求比较严苛,必须保证适宜的ph、电解质环境和排除交叉反应;
第二,不同厂商检测试剂盒检测结果存在显著差异,即免疫反应的检测准确度得不到保障;
第三,特异性差,不能有效区分钴胺素和类咕啉,不能给出准确的维生素b12含量;
第四,放射性免疫法存在放射线辐射和污染等问题。
技术实现要素:
本发明的目的在于针对目前检测维生素b12存在的缺陷,提出一种液相色谱串联质谱测定维生素b12的方法及试剂盒,特异性强,灵敏度高,可满足临床检测的需求。
为了实现以上任一发明目的,本发明提供一液相色谱串联质谱测定维生素b12的方法,适用于测定血清或血浆中维生素b12,包括以下步骤:
(1)维生素b12的提取和稳定:
维生素b12的提取:将结合态维生素b12从钴胺素结合蛋白中游离出来;
维生素b12的稳定:提供氰基离子,转化钴胺素异构体(羟钴胺素、甲钴胺素和5-脫氧腺苷钴胺素等)为相对稳定的氰钴胺素;
(2)净化浓缩氰钴胺素;以及
(3)串联质谱检测;
其中色谱条件选择为:
色谱柱:
流动相a液:含有甲酸的乙酸铵水溶液;
流动相b液:含有甲酸的乙酸铵甲醇溶液:
流速:0.3-0.4ml/min;
进样量:20μl-40μl;
柱温:30-40℃;
其中质谱条件为:
离子源:电喷雾离子源;扫描方式:正离子模式;离子喷雾电压:4500-5500v;离子源温度(tem):400-500℃;气帘气(cur):20-35psi;碰撞气(cad):9psi;离子源雾化气(gs1):40-55psi;离子源加热辅助气(gs2):40-60psi;扫描模式:mrm。
对应维生素b12的检测离子对及其他条件如下表一,表一:
另外,在本发明中,采用甲氨喋呤作为内标定量,由于甲氨喋呤和维生素b12的色谱保留行为非常类似,故可被选为内标定量标准物,此时,对应甲氨喋呤的检测离子以及其他条件如表二,表二:
(4)定量检测:
采用维生素b12标准品制作标准曲线:
以标准溶液浓度为x轴,标准品和内标峰面积的比值为y轴,进行线性回归分析,经“i/x”权重得回归方程;
获取检测结果,代入回归方程得到血清或血浆中b12的含量。
在维生素b12的提取步骤当中,有以下几种可选的提取当值:
1、采用蛋白释放剂还原维生素b12结合蛋白中的二硫键,利用强碱破坏维生素b12和结合单元的氢键和组氨酸的配位键从而将维生素b12游离出来;
2、在缓冲液中利用高温条件控制蛋白质变性,从而将维生素b12从维生素b12结合蛋白中游离出来;
3、利用蛋白酶水解蛋白,将维生素b12从维生素b12结合蛋白中游离出来、
其中,第一种提取方式中,蛋白释放剂可选择dtt(二硫代苏糖醇)或tcep(三(2-羰基乙基)磷盐酸盐),强碱可选择氧化钠或氢氧化钾。
第二种提取方式中,缓冲剂可选择乙酸钠缓冲液或柠檬酸盐缓冲液,蛋白变性的条件选择为:水浴100℃加热或121℃高压灭菌器。
第三种提取方式中,蛋白酶可选择胰腺蛋白酶或木瓜蛋白酶。
在维生素b12的稳定步骤,采用氰基离子将钴胺素异构体(羟钴胺素、甲钴胺素和5-脫氧腺苷钴胺素等)转化为较稳定的氰钴胺素,稳定的原理如图2。与化学免疫方法的前处理步骤不同的是,在本发明的实施例中,只需要提供氰基离子而不需要提供显色离子,因为本发明检测原理是通过液相色谱质谱的方式进行检测,而不需要采用化学免疫法,故本发明的氰基离子可选择为:用氰化钾或氰化钠或含氰基的络合物溶液,降低样品前处理的难度和成本。
值得一提的是,维生素b12的提取和维生素b12的稳定步骤可同步进行,提高检测效率。
在净化浓缩氰钴胺素步骤当中,也可选择两种方式进行净化:
1、通过hlb固相萃取柱除盐、净化、浓缩。
2、选择维生素b12免疫亲和净化柱净化浓缩。
hlb指的是由亲脂性二乙烯苯和亲水性n-乙烯基吡咯烷酮两种单体按一定比例聚合成的大孔共聚物,选择的规格条件如下:1cc/30mg,厂家不限。活化平衡:500-1000μl甲醇活化,500-1000μl超纯水平衡。
维生素b12免疫亲和净化柱采用高特异性的单克隆抗体,抗体对维生素b12具有高亲和性,当样品提取液通过免疫亲和柱时,维生素b12与抗体结合,加水洗脱非键合成分,加甲醇将抗体吸附的维生素b12洗脱下来。
另外,本发明提供一种液相色谱串联质谱测定维生素b12的试剂盒,如表三:
相较现有技术,本发明具有以下的有益效果:
1、本发明提供的测定维生素b12的方法及试剂盒采用液相色谱串联质谱检测人体内维生素b12的含量,避免采用免疫方法进行检测,从而避免了免疫方法检测时产生的各种问题。
2、相较检测食品中维生素b12的试剂盒和方法,对氰钴胺素进行了净化浓缩,适用于检测血清和血浆中低浓度的维生素b12。
3、本试剂盒检测特异性高,在较短时间内即可获取准确的维生素b12的浓度,在生物检测领域中有极大的应用。
附图说明
图1是根据维生素b12的化学结构图。
图2是根据本发明的一实施例的液相色谱串联质谱测定维生素b12的方法及试剂盒的维生素b12检测原理图。
图3.是根据本发明的一实施例的液相色谱串联质谱测定维生素b12的方法及试剂盒的维生素b12定量标准工作曲线。
图4根据本发明的一实施例的液相色谱串联质谱测定维生素b12的方法及试剂盒的维生素b12标准品的色谱图。
图5根据本发明的一实施例的液相色谱串联质谱测定维生素b12的方法及试剂盒的维生素b12内标甲氨喋呤的色谱图。
图6根据本发明的一实施例的液相色谱串联质谱测定维生素b12的方法及试剂盒的人血清样品中维生素b12的色谱图。
图7根据本发明的另一实施例的液相色谱串联质谱测定维生素b12的方法及试剂盒的人血清样品中维生素b12的色谱图。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员所获得的所有其他实施例,都属于本发明保护的范围。
可以理解的是,术语“一”应理解为“至少一”或“一个或多个”,即在一个实施例中,一个元件的数量可以为一个,而在另外的实施例中,该元件的数量可以为多个,术语“一”不能理解为对数量的限制。
本发明提供具体实施例验证本发明的方法的可行性:
一、材料:
1.1方法学研究实验的样本:血清、血浆,来自于杭州度安医学检验实验室;
1.2仪器
氮吹机(md200,杭州奥盛仪器有限公司);96孔板(u型0.2ml,博纳艾杰尔);离心机(1-14k,sigma);离心管(1.5ml,axygen);色谱系统,质谱系统,(watersxevotqd/i-class三重四级杆质谱仪,waters公司);
1.3试剂耗材:
hlb固相萃取柱,1cc/30mg;色谱柱:polarc18;氰化钾溶液(1mg/ml,含2%氢氧化钠,百灵威);二硫苏糖醇(1mol/l,用ph5.2浓度为0.01mol/l的乙酸钠作为溶液自配制,阿拉丁);1%-2%冰醋酸溶液;5%甲醇;含有甲酸的乙酸铵水溶液;含有甲酸的乙酸铵甲醇溶液。
1.4标准品:维生素b12标准品,(氰钴胺素100mg,麦克林);
1.5内标物:0.1μg/ml甲氨喋呤,(0.2%氨水甲醇作为溶剂配制浓度为1mg/ml的甲氨喋呤储备液,用甲醇稀释至10μg/ml,然后用含有甲酸的乙酸铵水溶液稀释至0.1μg/ml,标准品购自百灵威);
1.6质控样品:(自配制);
二、样品前处理:
样品前处理后,用固相萃取法对试剂提取液中的维生素b12进行富集并除去杂质,高效液相色谱串联质谱测定,以甲氨喋呤为内标定量,该方法检测速度快,且可用于检测人血清或血浆中的维生素b12。
标准溶液的制备:配制1mg/ml的氰钴胺素甲醇储备液(含0.1%乙酸),用含0.1%乙酸的甲醇分别稀释至2ng/ml、4ng/ml、10ng/ml、20ng/ml、40ng/ml、100ng/ml、200ng/ml工作储备液,分别移取10μl上述工作储备液至1.5ml离心管中,分别加入190μlpbs缓冲液,混匀,制成浓度为0.1ng/ml、0.2ng/ml、0.5ng/ml、1ng/ml、2ng/ml、5ng/ml、10ng/ml的标准曲线。
质控样品的制备:用含0.1%乙酸的甲醇分别稀释1mg/ml的氰钴胺素甲醇储备液至4ng/ml、12ng/ml、24ng/ml,分别移取10μl上述工作储备液至1.5ml离心管中,分别加入190μlpbs缓冲液,混匀,制成浓度为0.2ng/ml、0.6ng/ml、1.2ng/ml的质控样品。
实施例1:
样品前处理:
精密量取标准溶液,质控样品,或人血清置于洁净离心管中;以10:1的体积比例加入内标(0.1μg/ml甲氨喋呤),加入2.5-4体积倍内标的氰化钾(1mg/ml,含2%氢氧化钠)溶液,加入0.5体积倍内标的二硫苏糖醇溶液,混匀3-5分钟,避光超声15-30分钟;
加入1%-2%冰醋酸溶液中和样品,混匀2分钟,12000rpm/min离心5分钟。取上清液上样至活化平衡好的hlb固相萃取柱,待样品流出后,5%甲醇水洗杂,干燥1-2min,用甲醇分两次洗脱,氮吹,复溶,涡旋混匀5min,移取至96孔板,离心5min,进样lc-ms-ms。
另外,如果是采用离心浓缩仪要换为50%甲醇水分两次洗脱,50%甲醇水洗脱要用离心浓缩仪浓缩至干后,复溶,涡旋混匀5min,移取至96孔板,离心5min,进样lc-ms-ms。
具体而言,精密量取标准溶液,质控样品,或人血清200μl置于洁净离心管中;加入内标(0.1μg/ml甲氨喋呤)20μl,加入50μl-200μl氰化钾(1mg/ml,含2%氢氧化钠)溶液或一定浓度的含氰根的络合物,加入10μl二硫苏糖醇溶液,混匀3-5分钟,避光超声15-30分钟。加入1%-2%冰醋酸溶液中和样品,混匀2分钟,12000rpm/min离心5分钟。取上清液上样至活化平衡好的hlb固相萃取柱,待样品流出后,分别加入1ml超纯水(也可省略此部),1ml5%甲醇水洗杂,干燥1-2min(注意将固相萃取柱上残留的水分清除干净,对后续氮吹的时间影响很大),600μl甲醇(如果有离心浓缩仪要换为50%甲醇水洗脱)分两次洗脱,氮吹(50%甲醇水洗脱要用离心浓缩仪浓缩至干),复溶,涡旋混匀5min,移取至96孔板,离心5min,进样lc-ms-ms。
实施例2:
样品前处理:精密量取标准溶液,质控样品,或人血浆置于洁净离心管中;以10:1的体积比例加入内标(0.1μg/ml甲氨喋呤),加入40-60体积倍内标的0.1m/lph4.0-4.6之间的乙酸钠缓冲液(含一定浓度氰化钠),混匀3-5分钟,100℃水浴30分钟,放于冰浴冷却,12000rpm/min离心5分钟。
取上清液上样至活化平衡好的hlb固相萃取柱,待样品流出后,分别加入超纯水(也可省略此步骤),5%甲醇水洗杂,干燥1-2min(注意将固相萃取柱上残留的水分清除干净,对后续氮吹的时间影响很大),用甲醇分两次洗脱,氮吹,复溶,涡旋混匀5min,移取至96孔板,离心5min,进样lc-ms-ms。
具体而言,精密量取标准溶液,质控样品,或人血清200μl置于洁净离心管中;加入内标(0.1μg/ml甲氨喋呤)20μl,加入800μl-1200μl0.1m/lph4.0-4.6之间的乙酸钠缓冲液(含一定浓度氰化钠),混匀3-5分钟,100℃水浴30分钟,放于冰浴冷却。12000rpm/min离心5分钟。取上清液上样至活化平衡好的hlb固相萃取柱,待样品流出后,分别加入1ml超纯水(也可省略此部),1ml5%甲醇水洗杂,干燥1-2min(注意将固相萃取柱上残留的水分清除干净,对后续氮吹的时间影响很大),600μl甲醇(如果有离心浓缩仪要换为50%甲醇水洗脱)分两次洗脱,氮吹(50%甲醇水洗脱要用离心浓缩仪浓缩至干),复溶,涡旋混匀5min,移取至96孔板,离心5min,进样lc-ms-ms。
三、液相色谱串联质谱检测:
色谱条件:
色谱柱:polarc18;流动相:a液:含有甲酸的乙酸铵水溶液,b液:含有甲酸的乙酸铵甲醇溶液;流速:0.4ml/min,柱温为35℃,进样20μl;等度洗脱。
质谱条件:
离子源:电喷雾离子源;扫描方式:正离子模式;离子喷雾电压:5500v;离子源温度(tem):500℃;气帘气(cur):20psi;碰撞气(cad):9psi;离子源雾化气(gs1):55psi;离子源加热辅助气(gs2):60psi;扫描模式:mrm。
维生素b12以及内标的mrm方法设置
四、数据处理:
4.1获取维生素标准品的色谱图
获取维生素b12标准品的色谱图如图4所示,作为标准曲线的定量下限。
4.2获取维生素b12内标内标甲氨喋呤的色谱图。
获取维生素b12内标甲氨喋呤的色谱图如图5所示,其色谱峰保留时间与维生素b12接近,可以很好的校准样品前处理过程中和色谱分离过程产生的波动,提高分析结果的准确度。
4.3获取维生素b12的定量标准工作曲线:
获取不同浓度的维生素b12标准曲线进行测定,得到检测数据,以标准溶液浓度为x轴,标准和内标峰面积的比值为y轴,进行线性回归分析,经“1/x”权重得回归方程:y=0.01672x+0.099974,其线性系数为0.99974,如图3所示,线性拟合方程,线性良好,满足定量要求。
五、检测结果:
5.1检测结果1:
以实施例1制备得到的样品进行检测,检测得到的色谱图如图6,由图6可知,色谱峰形较好,保留时间与维生素b12标准品对应,测定值为0.41ng/ml。
5.2检测结果2:
以实施例2制备得到的样品进行检测,检测得到的色谱图如图7,由图7可知,色谱峰形较好,保留时间与维生素b12标准品对应,测定值为0.59ng/ml。
六、该方法的可行性检测:
6.1、检出限:
配制0.03ng/ml的维生素b12标准溶液,上仪器进行测定,重复测定3次,计算信噪比均值,结果为4。该方法仪器检出限为0.03ng/ml。
6.2精密度:
0.2ng/ml、0.6ng/ml、1.2ng/ml浓度的批内批间精密度度均在15%以内,符合临床检测对精密度的要求。
6.3准确度:
0.2ng/ml、0.6ng/ml、1.2ng/ml浓度的批内批间准确度均在质控样品标示值的±15%以内,符合临床检测对准确度的要求。
七、液相色谱串联质谱测定维生素b12的试剂盒:
本发明不局限于上述最佳实施方式,任何人在本发明的启示下都可得出其他各种形式的产品,但不论在其形状或结构上作任何变化,凡是具有与本申请相同或相近似的技术方案,均落在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!