一种吖啶酯偶联抗体的方法及其应用与流程
1.本发明涉及免疫分析技术领域,具体而言,涉及一种吖啶酯偶联抗体的方法及其应用。
背景技术:
2.化学发光免疫分析(chemiluminescence immunoassay,clia),是将具有高灵敏度的化学发光测定技术与高特异性的免疫反应相结合,用于各种抗原、或抗体的检测分析技术。是继放免分析、酶免分析、荧光免疫分析和时间分辨荧光免疫分析之后发展起来的一项最新免疫测定技术。
3.吖啶酯是一类可用作化学发光标记物的化学物质,在碱性条件下,吖啶酯分子受到过氧化氢进攻可生成二氧乙烷,二氧乙烷不稳定而分解为co2和电子激发态的n-甲基吖啶酮,当其回到基态时发出波长为430nm的光子。
4.吖啶酯标记物在化学结构上有产生发光的特殊基团,在发光免疫分析过程中直接参与发光反应。通常这类物质没有本底发光,在反应中能用于检测低浓度或微量浓度的样品,是一类发光效率很高的发光剂。但是,吖啶酯标记化学发光检测经常会出现假阳性结果,检测的特异性有待改进。
5.鉴于此,特提出本发明。
技术实现要素:
6.本发明的目的在于提供一种吖啶酯偶联抗体的方法及其应用。
7.本发明是这样实现的:
8.第一方面,本发明实施例提供了一种吖啶酯偶联抗体的方法,其包括:在抗体偶联吖啶酯之前,将抗体与edta二钠混合反应。
9.第二方面,本发明实施例提供了edta二钠在制备用于提高吖啶酯标记化学发光免疫测定的检测特异性的试剂中的应用。
10.通过本发明可以提高抗体与吖啶酯偶联的反应活性,这种提高不限定于具体的抗体种类,针对不同抗原的抗体都有效果。不同的抗体区别最大的区域是cdr,但是与吖啶酯偶联是在抗体fc端。本发明人在多个项目中验证本发明是有效的,以下仅是举列说明。
11.本发明具有以下有益效果:
12.本发明提供了一种吖啶酯偶联抗体的方法及其应用,该方法先将edta二钠与抗体混合反应,再将混合反应后的抗体与吖啶酯进行偶联,与现有技术相比,对采用edta二钠处理后的抗体与吖啶酯偶联并进行检测,能有效地避免或减少化学发光免疫检测中出现的假阳性现象,提高检测的特异性。
附图说明
13.为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附
图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
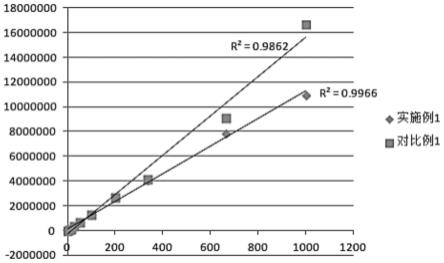
14.图1为本发明试验例1中对校准品的线性检测结果;
15.图2为本发明试验例2中对校准品的线性检测结果。
具体实施方式
16.为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
17.以下结合实施例对本发明的特征和性能作进一步的详细描述。
18.名词定义
19.本文中所述的“偶联”可以指:由两个有机化学单位进行某种化学反应而得到一个有机分子的过程,也可以称为结合。
20.本文中所述的“化学发光免疫检测”是将抗原与抗体特异性反应与灵敏度的化学发光反应相结合而建立的一种免疫检测技术。从反应原理上,化学发光免疫技术主要分为直接化学发光和酶促反应化学发光。在直接化学发光中,化学发光剂在发光免疫分析过程中不需酶的催化作用,直接参与发光反应,它们在化学结构上有产生发光的特有基团,可直接标记抗原或抗体。代表性的发光剂包括吖啶酯。
21.本文中所述的“吖啶酯”是三环有机化合物,在碱性条件下被h2o2氧化时,发出波长为470nm的光,具有很高的发光效率,其激发态产物n-甲基吖啶酮是该发光反应体系的发光体。
22.本发明实施例提供了一种吖啶酯偶联抗体的方法,其包括:在抗体偶联吖啶酯之前,将抗体与edta二钠混合反应。
23.发明人经一系列创造性劳动发现,将抗体与吖啶酯混合偶联前,先采用edta二钠对抗体进行预处理,对预处理后的抗体与吖啶酯偶联物进行检测,能够有效避免或减少化学发光免疫检测中出现的假阳性现象,有效特高检测的特异性。
24.在一些实施例中,edta二钠与抗体混合时的工作浓度为1~10mm。具体地,edta二钠的工作浓度可以为1mm、1.5mm、2mm、2.5mm、3mm、3.5mm、4mm、4.5mm、5mm、5.5mm、6mm、6.5mm、7mm、7.5mm、8mm、8.5mm、9mm、9.5mm、10mm中的任意浓度。
25.优选地,edta二钠与抗体混合时的工作浓度为2~5mm。当edta二钠处于该浓度范围内时,能更有效地减少或避免检测的特异性。
26.优选地,edta二钠与抗体的混合时间为5~40min。在一些实施方式中,edta二钠与抗体的混合时间可以为5min、10min、15min、20min、25min、30min、35min和40min中的任意时间。
27.优选地,edta二钠与抗体的混合温度为15~25℃。在一些实施方式中,混合温度可以为15℃、16℃、17℃、18℃、19℃、20℃、21℃、22℃、23℃、24℃、25℃中的任意温度。
28.优选地,edta二钠与抗体混合时,抗体溶液的浓度为1~3mg/ml。在一些实施方式
中,抗体溶液的浓度可以为1mg/ml、1.5mg/ml、2mg/ml、2.5mg/ml、3mg/ml中的任意浓度。
29.在一些实施例中,吖啶酯与抗体溶液的混合方式为:混匀后,室温避光反应。具体可以为:在小型旋涡振荡器中立即旋涡震荡混匀10s;小型离心机中稍离心后,室温避光反应40~80分钟,然后采用甘氨酸溶液进行封闭。
30.在一些实施方式中,吖啶酯与抗体混合偶联后,所述方法还包括对该混合物或偶联物进行纯化步骤。
31.优选地,纯化步骤包括:将偶联好的偶联物加入0.5ml 7k脱盐柱中,在高速离心机中1500
ⅹ
g离心2min,收集脱盐后的标记物,使用pbs(20mm pb和150mm nacl,ph 7.4)溶液将脱盐纯化后的偶联物定至一定浓度,加入等体积高压甘油混匀,-20℃保存。
32.本发明对抗体不作具体限定,可选自能被吖啶酯标记的任意抗体类型。可以为基因工程抗体、多克隆抗体和单克隆抗体中的一种或两种。按照来源分类,可以为鼠源抗体、兔源抗体、羊源抗体以及羊驼抗体中的一种或多种。
33.所述抗体偶联吖啶酯时,吖啶酯溶液的浓度为0.05~2mm,具体可以为0.05mm、0.10mm、0.15mm、0.2mm中的任意浓度;抗体的加入量为50~1000μg,具体可以为50μg、100μg、150μg、200μg、250μg、300μg、400μg、500μg、600μg、700μg、800μg、900μg、1000μg中的任意数值。
34.优选地,所述抗体偶联吖啶酯的条件为:于15~25℃,避光混合10~60min,加入牛血清蛋白bsa溶液后,避光混合10~60min。避光混合的混合方式优选为震荡,时间可以为10min、20min、30min、40min、50min、60min中的任意时间。
35.优选地,抗体偶联吖啶酯时,采用的偶联缓冲液为碳酸盐cbs缓冲液;
36.优选地,所述cbs缓冲液中包括:15~20mm cb和130~170mm nacl,ph 9~10。
37.此外,本发明实施例还提供了edta二钠在制备用于提高吖啶酯标记化学发光免疫测定的检测特异性的试剂中的应用。
38.除非特殊说明,本发明实施例所用的化学试剂,均为分析纯,购自sigma-aldrich公司。所用的化学发光检测仪为中国北京滨松光子技术股份有限公司滨松bhp9507化学发光检测仪。
39.实施例1
40.一种吖啶酯偶联抗体的方法,其包括以下步骤:
41.(1)抗体处理:
42.取一定量的待标记抗体,用脱盐置换纯化至碳酸盐cbs(20mm cb和150mm nacl ph 9.5)缓冲溶液中,将置换纯化后的抗体平均分成两份,取其中一份抗体溶液加入edta二钠,使用cbs溶液将抗体浓度定至为2mg/ml,edta二钠的工作浓度为5mm,抗体与edta二钠充分混匀后室温反应半小时;另一份抗体溶液直接使用cbs溶液定至相同的浓度2mg/ml备用。
43.(2)抗体与吖啶酯偶联:
44.2.1、量取12mlcbs(20mm cb和150mm nacl ph 9.5)缓冲溶液于离心管中;
45.2.2、加入待标记抗体1mg,充分混匀;
46.2.3、加入吖啶酯溶液(1mg/ml)400μl,充分混匀,室温避光震荡1小时;
47.2.4、加入10%的bsa溶液1.4ml,混匀,室温避光振荡反应30分钟;
48.2.5、上述产物加入30ml g25脱盐柱中,在高速离心机中1500
ⅹ
g离心2min,收集脱
盐后的标记物,使用pbs(20mm pb和150mm nacl,ph 7.4)溶液将脱盐纯化后的偶联物定至一定浓度,加入等体积甘油混匀,-20℃保存。
49.实施例2
50.一种吖啶酯偶联抗体的方法,大致与实施例1相同,区别在于,edta二钠的工作浓度的不同,区别如下:
51.edta二钠的工作浓度为4mm。
52.实施例3
53.一种吖啶酯偶联抗体的方法,大致与实施例1相同,区别在于,edta二钠的工作浓度的不同,区别如下:
54.edta二钠的工作浓度为3mm。
55.实施例4
56.一种吖啶酯偶联抗体的方法,大致与实施例1相同,区别在于,edta二钠的工作浓度的不同,区别如下:
57.edta二钠的工作浓度为2mm。
58.实施例5
59.一种吖啶酯偶联抗体的方法,大致与实施例1相同,区别在于,edta二钠的工作浓度的不同,区别如下:
60.edta二钠的工作浓度为1mm。
61.实施例6
62.一种吖啶酯偶联抗体的方法,大致与实施例1相同,区别在于,edta二钠的工作浓度的不同,区别如下:
63.edta二钠的工作浓度为8mm。
64.实施例7
65.一种吖啶酯偶联抗体的方法,大致与实施例1相同,区别在于,edta二钠的工作浓度的不同,区别如下:
66.edta二钠的工作浓度为10mm。
67.对比例1
68.一种吖啶酯偶联抗体的方法,大致与实施例1相同,区别在于,未加入edta二钠。
69.对比例2
70.一种吖啶酯偶联抗体的方法,大致与实施例1相同,区别在于,edta二钠的加入时机不同,在本对比例中,edta二钠的加入时机为:在吖啶酯与抗体混合后,作为缓冲液加入。
71.需要说明的是,在本对比例1中,edta二钠的工作浓度为5mm。
72.试验例1
73.实验方法
74.分别采用实施例1和对比例1提供的吖啶酯偶联抗体的方法,偶联ca153抗体(待标记抗体)和吖啶酯溶液,采用偶联后的抗体对校准品和临床样本进行检测。
75.校准品的检测结果如表1所示。
76.表1校准品检测结果
[0077][0078]
由表1和图1可知,采用edta二钠对抗体进行预处理,能够得到更好的线性值r2=0.99,且校准品线性范围上线可以达到1000u/ml。
[0079]
临床样本检测结果如表2所示。
[0080]
表2临床样本检测结果
[0081]
临床样本(u/ml)实施例1(u/ml)对比例1(u/ml)样本1:19.620.118100.1669样本2:22.721.227740.0903样本3:24.823.152328.6699样本4:26.827.101628.6209样本5:85.484.413479.5694样本6:137.9132.0966153.8142
[0082]
由表2可知,采用edta二钠对抗体进行预处理,能够提高检测的准确度,提高抗血清基质的影响。对比例1在临床样本1和2都检测出假阳性结果,而采用本发明的方法检测的值与临床值相符合。
[0083]
试验例2
[0084]
实验方法
[0085]
分别采用实施例1和对比例2提供的吖啶酯偶联抗体的方法,偶联ca153抗体和吖啶酯溶液,采用偶联后的抗体对校准品和临床样本进行检测。
[0086]
校准品的检测结果如表3所示。
[0087]
表3校准品的检测结果
edta二钠预处理的实施例与临床值偏差不超过5%。
[0101]
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1