一种人源MOB1蛋白的应用的制作方法
本发明涉及生物医药技术领域,尤其涉及一种人源mob1蛋白的应用。
背景技术:
肝癌是最常见的恶性肿瘤之一,包括肝细胞癌(hepatocellularcarcinoma,hcc)、肝胆管癌等多种类型,其中肝细胞癌是最主要的肝癌类型。根据globocan2018的资料显示,2018年全球共有841,080例新发肝癌病例,其中男性596,574例,女性244,506例。肝癌已成为全球第六大常见肿瘤,也是全球癌症死亡的第四大原因。
肝细胞癌具有起病隐匿、进展快、复发早、预后差等临床特点,患者在出现明显症状而就诊时,大多已经进展到中晚期,且由于中国大部分患者有乙型肝炎病毒感染,肝功能常受损严重且全身状态较差,失去了手术治疗机会。由于肝癌细胞的多药耐药性,化疗并不作为肝细胞癌的常规治疗方式,靶向药物在晚期肝细胞癌的系统治疗中常作为一线药物使用。2007年,具有划时代意义的多靶点酪氨酸激酶抑制剂索拉非尼上市,成为肝细胞癌治疗的一线药物,但使用索拉非尼后肝细胞癌患者的中位存活时间只有1年左右。2018年,新一代靶向药物仑伐替尼在中国上市,被批准用于不可以进行手术的肝细胞癌患者的一线治疗。与索拉非尼相比,仑伐替尼的中位生存时间延长4.8个月(15.0个月vs10.2个月),客观缓解率提高28.2%(40.6%vs12.4%),无进展生存期提高3.7个月(7.4个月vs3.6个月)。但总体来说,肝细胞癌的耐药强、进展快及复发率高的问题并未解决,治疗依然存在巨大缺口。
靶向药物因其良好的特异性、高效性及耐受性而备受关注。从索拉非尼到仑伐替尼,针对肝细胞癌的靶向药物治疗展现出巨大的潜力。分子靶向治疗是目前肝细胞癌的研究热点,也对药物研发提出了更高的要求,需要从分子水平探索肝细胞癌的具体发病机制,寻找影响肝细胞癌发生发展的关键靶点,并探索关键靶点的干预手段。
传统观点认为mob1(mpsonebinder1)蛋白具有抑癌作用。mob1蛋白最初在芽殖酵母中被发现,mob1与磷酸化的蛋白激酶dbf2结合,作为效应器介导有丝分裂退出途径(mitoticexitnetwork,men),抑制细胞的增殖过程。在黑腹果蝇中,进一步发现mob1蛋白属于经典的hippo信号通路,通过抑制下游效应蛋白yap及其旁系同源蛋白taz的磷酸化及入核水平,在调节器官大小、抑制组织增生及抑制肿瘤发生的过程中发挥重要作用。在哺乳动物细胞中,多个研究也报导了mob1蛋白通过yap蛋白介导的抑癌作用。例如,在结肠癌中,mob1的表达水平显著降低,其低表达与远端及淋巴转移密切相关,且与病人的生存率降低相关。进一步的机理研究也证明,mob1能够影响yap蛋白的磷酸化和入核,抑制肿瘤细胞的增殖和迁移能力。
近年来,越来越多的研究指出同一蛋白质在不同的细胞中可能发挥的作用不同。例如,hippo信号通路的关键蛋白mst1/2的功能缺失不会引起免疫细胞的过度增殖,而是引起免疫系统的功能紊乱。相对于hippo信号通路的其他成员来说,mob1蛋白的研究相对较少,而mob1蛋白对肿瘤细胞的作用在学术界并未达成一致,研究者在不同的肿瘤中发现mob1蛋白可能发挥着不同的作用。例如,在51.2%的肺癌样本中(共计205例)mob1的蛋白水平高表达,且高表达的mob1与肿瘤内的血管侵袭及病人的低存活率密切相关。此外,还发现mob1过表达能促进人肺癌细胞系h1299和pc9的侵袭,而敲低mob1能显著抑制上述两个细胞系的侵袭。值得注意的是,mob1蛋白在肝癌中的作用尚无报道。
技术实现要素:
本发明的目的是针对现有技术中的不足,提供一种人源mob1蛋白的应用。
为实现上述目的,本发明采取的技术方案是:
本发明的第一方面是提供一种检测mob1蛋白的制剂在制备诊断或/和预后肝细胞癌试剂盒中的应用。
本发明的第二方面是提供一种mob1蛋白的抑制剂在制备预防或/和治疗肝细胞癌药物中的应用。
优选地,所述mob1蛋白为人源mob1蛋白,包括高度同源的mob1a蛋白,pubmedgeneid:55233和mob1b蛋白,pubmedgeneid:92597。
优选地,所述肝细胞癌为原发性肝细胞癌或其复发或其转移。
本发明采用以上技术方案,与现有技术相比,具有如下技术效果:
本发明基于现有技术现状,提出mob1蛋白在肝细胞癌中的促进作用,及其作为靶点在肝细胞癌诊断、治疗及预后中的用途。本发明通过挖掘tcga数据库,发现mob1基因表达在肝细胞癌样本中显著上升,且与病人的低生存率显著相关。在自建肿瘤样本库中,对比肝癌样本及癌旁组织后发现,mob1蛋白在肝细胞癌组织样本中显著高表达,但在其他肝癌类型癌组织中无明显变化。利用mob1蛋白敲低及过表达的细胞系发现,mob1蛋白能够显著促进多株肝癌细胞系的增殖,且即使在仑伐替尼存在的情况下,mob1蛋白依然能够促进肝癌细胞的增殖。
附图说明
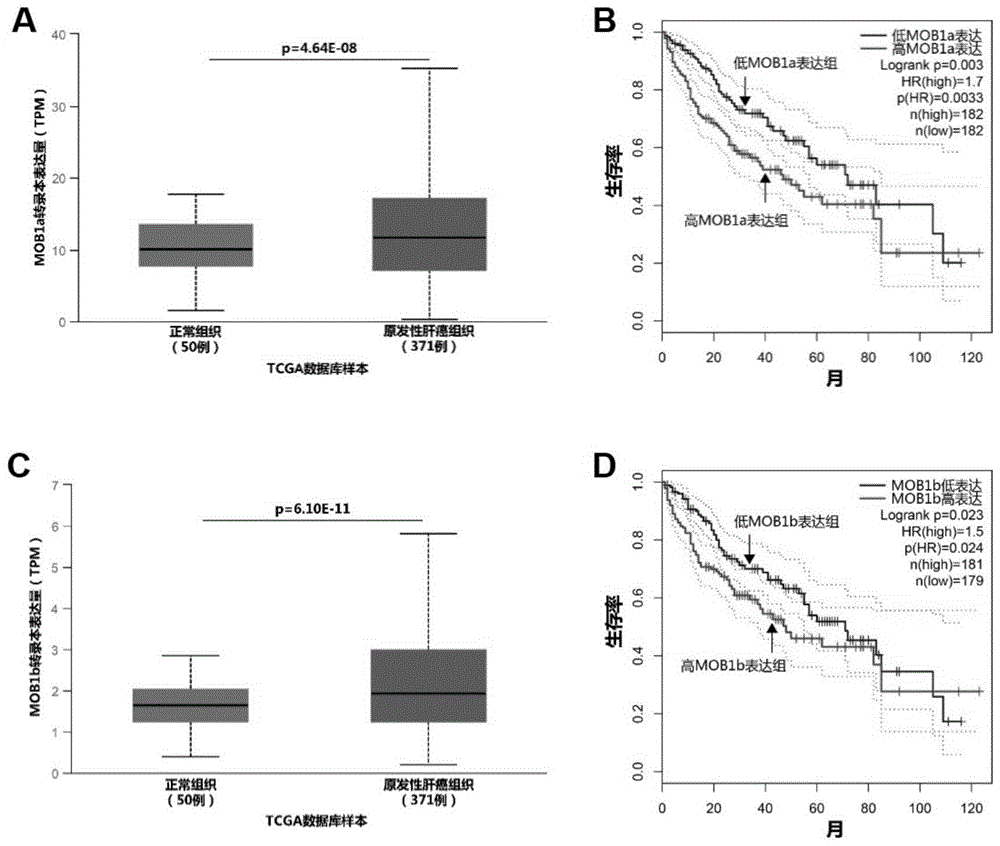
图1为tcga数据库挖掘mob1蛋白与肝细胞癌的关系;其中,(a,b)为正常组织及肝细胞癌组织中mob1a和mob1b基因表达水平;(c,d)为mob1a和mob1b基因表达水平与病人存活率的关系;
图2为自建样本库肝癌组织中mob1的表达水平;其中,(a)为肝细胞癌病人癌组织及癌旁组织中mob1的蛋白表达水平;(b)为肝胆管癌病人癌组织及癌旁组织中mob1的蛋白表达水平;(c)为肝血管癌病人癌组织及癌旁组织中mob1的蛋白表达水平;(d)为肝细胞腺癌病人癌组织及癌旁组织中mob1的蛋白表达水平;(e)为纤维性肝癌病人癌组织及癌旁组织中mob1的蛋白表达水平;(f)为直肠癌和乳腺癌肝转移后肝癌组织及癌旁组织中mob1的蛋白表达水平;(g)为肝细胞癌病人癌组织及癌旁组织中mob1的蛋白表达量;(h)为其他肝癌病人癌组织及癌旁组织中mob1的蛋白表达量;
图3为mob1敲低对肝癌细胞系的增殖的影响;其中,(a)为westernblot检测mob1在hepg2细胞中的敲低效果;(b)为mob1敲低对hepg2细胞增殖的影响;(c)为westernblot检测mob1在huh-7细胞中的敲低效果;(d)为mob1敲低对huh-7细胞增殖的影响;
图4为mob1过表达对肝癌细胞系增殖的影响;其中,(a)为westernblot检测mob1在hepg2细胞中的过表达效果;(b)为mob1过表达对hepg2细胞增殖的影响;(c)为在仑伐替尼存在情况下,mob1过表达对hepg2细胞增殖的影响;(d)为westernblot检测mob1在huh7细胞中的过表达效果;(e)为mob1过表达对huh7细胞增殖的影响;(f)为在仑伐替尼存在情况下,mob1过表达对huh7细胞增殖的影响。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动的前提下所获得的所有其他实施例,都属于本发明保护的范围。
需要说明的是,下述实施例中的实验方法,如无特殊说明,均为常规方法;下述实施例中所用的材料、试剂等,如无特殊说明,均可从公开商业途径获得;在不冲突的情况下,本发明中的实施例及实施例中的特征可以相互组合。
下面结合附图和具体实施例对本发明作进一步说明,但不作为本发明的限定。
实施例:探索新靶点mob1蛋白对肝细胞癌增殖的作用。
①实验方法
1)tcga数据库挖掘
人源mob1包括高度同源的mob1a蛋白(pubmedgeneid:55233)和mob1b蛋白(pubmedgeneid:92597)。从tcga数据库中获取50例正常肝组织及371例肝细胞癌组织的rna测序信息及生存率信息,统计正常组织及肝细胞癌组织中mob1a和mob1b的转录本表达量(transcriptpermillion,tpm),并分析不同mob1a和mob1b表达量肝细胞癌病人的生存率。
2)自建肝癌样本库
28例肝癌组织及癌旁组织来自深圳市人民医院收集自2020年01月至2020年12月手术切除标本,其中包括15例肝细胞癌、5例胆管癌、3例肝血管癌、1例肝细胞腺癌、2例纤维性肝癌、1例直肠癌肝转移、1例乳腺癌肝转移样本,所有样本均有明确的病理诊断报告。将每个病人的癌旁组织与癌组织进行配对研究。样本取得后,立即切成小块分装,并储存于液氮中,直至使用。取50mg左右的组织,加入含蛋白酶抑制剂和蛋白磷酸酶抑制剂的ripabuffer,在冰上进行高速研磨裂解后,12000g离心15分钟,取上清进行蛋白定量,并加入loadingbuffer煮沸15分钟后储存于-80℃。
3)westernblot检测肝癌组织的mob1蛋白表达水平
取等量蛋白样品进行sds-page电泳,随后利用湿转的方法将蛋白转移至0.45μm的pvdf膜上,用5%的脱脂牛奶封闭1小时。随后加入mob1抗体或β-actin抗体在室温孵育1小时或在4℃孵育过夜,用tbst洗膜3次。加入hrp标记的二抗,继续在室温孵育1小时,用tbst洗膜3次,然后用ecl化学发光试剂盒进行显影。蛋白定量的结果采用imagej软件分析条带的灰度值。
4)细胞培养及细胞系构建
所有细胞的培养基均为含有10%fbs和1%青霉素/链霉素的dmem培养基,培养于37℃,含5%co2的细胞培养箱中。
利用慢病毒介导的crispr/cas9技术构建敲低细胞系。根据mob1的序列分别设计sgrna(mob1bsgrnaforward:caccggaccaaagaagaacattccag,mob1bsgrnareverse:aaacctggaatgttcttctttggtcc),并分别连接到lenticrisprv2载体上,测序确定序列正确性。将pspax2和pmd2.g及目的质粒共转染至293t细胞中进行病毒包装,于48小时和72小时收集含病毒液上清,并用0.45μm的滤膜过滤。将病毒液加入至目的细胞中,转染48小时后用puromycin进行筛选,至未转染的对照细胞全部死亡,建立稳定转染细胞系。用lenticrisprv2载体(cas9)转染的细胞作为对照。利用westernblot的方法鉴定mob1的敲低效果。
利用慢病毒介导的过表达质粒plvx-3flag-puro构建稳定过表达的细胞系。将全长的mob1a的编码序列克隆至plvx-3flag-puro质粒中,测序确定序列正确性。慢病毒包装及稳定细胞系构建的方法同上所述。用plvx-3flag-puro载体(plvx)转染的细胞作为对照。利用westernblot的方法鉴定flag-mob1a的过表达效果。
5)细胞生长曲线
将分别将细胞接种到96孔板中进行培养,其中,hepg2细胞的密度均为5×103每孔,huh7的密度为5×103每孔。培养12、24、48、72后,加入总体积10%的cck-8溶液,继续孵育3小时后,测定450nm处测量吸光度。
②实验结果
1)tcga数据库中挖掘mob1与肝细胞癌的关系
人源mob1a和mob1b是mob1的两个同源蛋白,两者具有95%的氨基酸同源性。本发明首先在tcga肿瘤数据库中进行数据挖掘,通过对50例正常组织及371例肝细胞癌组织进行对比,我们发现mob1a和mob1b两个基因在肝细胞癌组织中均存在显著上调(图1a和1b)。将肝细胞癌病人分为mob1的高表达组和低表达组,发现mob1a和mob1b高表达组病人的生存率均显著下降(图1c和1d)。以上结果说明,mob1蛋白可能具有促进肝细胞癌发生发展的作用。
2)自建肝癌样本库中验证mob1与肝癌的关系
自建肝癌样本库中包含的28例病人的基本信息见表1所示。利用westernblot的方法,检测自建肝癌样本库中28例肝癌样本及配对癌旁组织中mob1的蛋白表达水平,结果如图2所示,发现在15例肝细胞癌样本中,有13例样本的mob1蛋白水平高表达(86.7%),而在13例其他类型肝癌样本中,仅有6例样本的mob1蛋白水平高表达(46.2%)。进行卡方检验分析后,证明相比于其他类型肝癌,在肝细胞癌中mob1的蛋白水平存在显著高表达(p<0.05)(表2)。通过imagej软件对各样本的表达量进行定量统计,发现mob1的蛋白量在肝细胞癌样本中显著升高,而在其他肝癌样本中无明显变化(图2g和2h)。
表1自建样本库中28例肝癌(肝细胞癌及其他肝癌)病人的信息概述。
表2mob1蛋白在28例肝癌病人肿瘤样本中表达情况的统计;
3)mob1促进肝癌细胞系的增殖作用
利用肝癌细胞系huh7和hepg2进一步验证mob1对肝癌细胞的影响,发现用crispr/cas9技术敲低mob1蛋白后,相比于空载质粒对照,两株mob1敲低细胞系的增殖速度均明显降低(图3)。而过表达flag-mob1a蛋白后,huh7和hepg2细胞的增殖速度显著增强(图4a,4b,4d和4e),且在仑伐替尼存在的情况下,mob1依然能够促进huh7和hepg2细胞的增殖速度(图4c和4f)。
综上所述,本专利发现了mob1对肝细胞癌增殖的促进作用。鉴于肝细胞癌靶向治疗的重要性,本专利提出以mob1为靶点的肝细胞癌治疗新策略,并提出靶向mob1的化学(如小分子抑制剂)和生物(如抗体、crispr/cas9、shrna、sirna等)抑制剂在肝细胞癌治疗中的新用途。
以上所述仅为本发明较佳的实施例,并非因此限制本发明的实施方式及保护范围,对于本领域技术人员而言,应当能够意识到凡运用本发明说明书及图示内容所作出的等同替换和显而易见的变化所得到的方案,均应当包含在本发明的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!