一种总钴胺素和氰钴胺的检测方法及其检测试剂盒和应用
本发明涉及分析检测技术领域,具体涉及一种总钴胺素和氰钴胺的检测方法及其检测试剂盒和应用。
背景技术:
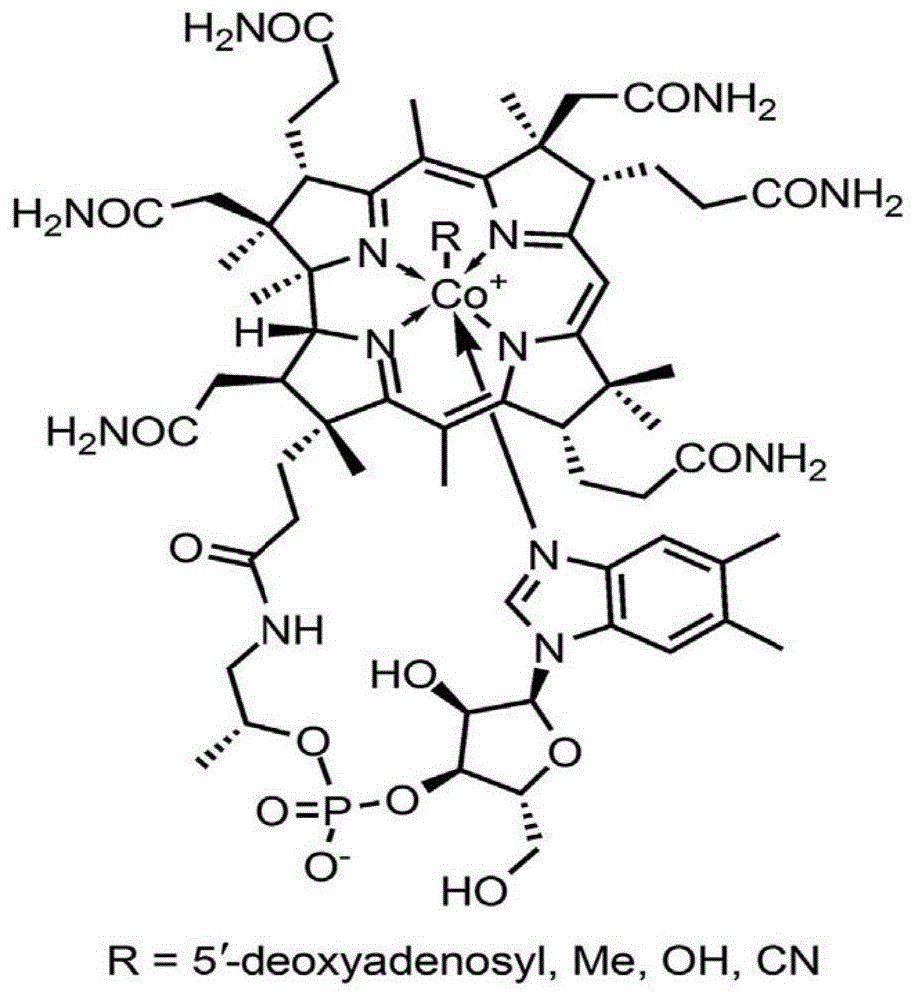
维生素b12(vitaminb12)又称钴胺素(cobalamin)、氰钴胺素,其分子结构(图1)是以钴离子为中心的咕啉环和5,6-二甲基苯并咪唑为碱基组成的多环化合物。因中央钴分子上结合的基团(图1中的“r”:5-脱氧腺苷、甲基、羟基、氰根离子)不同,维生素b12有多种活性形式,包括腺苷钴胺、甲钴胺、羟钴胺、氰钴胺。在人体内,腺苷钴胺和甲钴胺可作为人体中酶的辅因子,腺苷钴胺是甲基丙二酰辅酶a的辅酶,参与甲基丙二酸辅酶a向琥珀酰辅酶a的转化。甲钴胺是甲硫氨酸合成酶的辅酶,参与甲硫氨酸与同型半胱氨酸的代谢。在体外血中腺苷钴胺和甲钴胺含量很低,主要存在于细胞内,羟钴胺和氰钴胺则可存在于离心后血清或血浆中。
目前已有的检测样品中维生素b12的方法大部分基于免疫学方法(同位素放射免疫法,电化学发光免疫法,化学发光免疫法,荧光免疫分析法等)等。在临床最为常用的方法是采用化学发光原理的免疫学方法,其检测方便、快速、通量较高,然而,基于抗原抗体反应原理的免疫学方法可能存在着潜在的交叉干扰,譬如内因子抗体阳性时,可能干扰维生素b12的测定,使得维生素b12假性升高。
lc-ms/ms方法作为小分子代谢物的参考方法可为维生素b12的准确测定提供潜在的有力工具,然而目前lc-ms/ms方法对维生素b12营养的评估多为测定其代谢物-甲基丙二酸来间接反映维生素b12营养水平。另外,已报道的lc-ms/ms测定维生素b12多为测定钴胺素中的一种,如氰钴胺(d'ulivol,etal.determinationofcyanocobalaminbyisotopedilutionlc-ms/ms.analchimacta.2017oct16;990:103-109.),无法真实反映维生素b12的总含量。
技术实现要素:
本发明的目的是提供一种总钴胺素和氰钴胺的检测方法,该方法可检测样品中的总钴胺素含量,还可检测样品中的氰钴胺含量,并根据两者确定其他维生素b12的活性形式的含量。本发明还提供基于该检测方法的检测试剂盒及其应用。
本发明的检测方法为基于液相色谱串联质谱检测技术建立,通过衍生化前处理方法,定量血液等样本中不同形式钴胺素(维生素b12)的总含量(总钴胺素)以及氰钴胺的含量。其中,总钴胺素的测定方法为基于以下构思建立:根据不同钴胺素的结构差异,采用衍生化方法,使不同形式的钴胺素均衍生为其最稳定的氰钴胺形式,而后进行样本提取,再在液相色谱质谱仪器上结合氰钴胺的分子量,其在质谱中产生特异的质量/电荷比(质荷比)以及在色谱中的极性,采用同位素内标法实现对总钴胺素的定量。氰钴胺的测定方法为基于以下构思建立:氰钴胺在体外较为稳定,因此不经过衍生,在液相色谱质谱仪器上结合氰钴胺的分子量,其在质谱中产生特异的质量/电荷比(质荷比)以及在色谱中的极性,采用同位素内标法实现对氰钴胺的定量。
具体地,本发明提供以下技术方案:
第一方面,本发明提供一种总钴胺素和氰钴胺的检测方法,该方法包括总钴胺素的检测和氰钴胺的检测,所述总钴胺素的检测包括:将待测样品进行衍生处理,再采用液相色谱串联质谱法进行检测,
所述衍生处理采用的衍生剂包括第一衍生剂和第二衍生剂,
所述第一衍生剂为含有1-5g/l氰化钠或氰化钾以及10-100g/l氢氧化钠的水溶液;所述第二衍生剂为1-10g/l的二硫代苏糖醇水溶液,ph为2-9。
优选地,所述衍生剂还包括第三衍生剂,所述第三衍生剂为含有0.1%-10%甲酸的水溶液。
进一步优选地,所述第一衍生剂为含有1-3g/l氰化钠或氰化钾以及30-50g/l氢氧化钠的水溶液;所述第二衍生剂为0.8-1.5g/l的二硫代苏糖醇水溶液,ph为4-6;所述第三衍生剂为含有0.5%-2%甲酸的水溶液。
本发明发现,采用上述衍生剂能够显著提高样品中各种形式钴胺素的衍生化效率,使得样品中不同形式的钴胺素最大程度地衍生为稳定的氰钴胺形式,提高总钴胺素检测的准确度和精密度。
具体地,总钴胺素检测的衍生化处理方法如下:将所述待处理样品与样品制备液混合后分离上清液,将所述上清液干燥后,与所述第一衍生剂和所述第二衍生剂混合,反应5-15分钟后,再将反应体系与所述第三衍生剂混合,得到衍生化的样品。
上述衍生化处理中,第一衍生剂和第二衍生剂处理的时间优选为8-12分钟。
优选地,所述样品制备液为含有同位素标记氰钴胺的甲醇溶液。
在衍生化处理后,将所述衍生化的样品经萃取、干燥、复溶后再进行液相色谱分离。
具体地,氰钴胺检测的样品前处理方法包括:将所述待处理样品与所述样品制备液混合后分离上清液,将所述上清液干燥后,与所述第三衍生剂混合,经萃取、干燥、复溶后,再采用液相色谱串联质谱法进行检测。
本发明所述的所述萃取可为固相萃取或液液萃取,其中,固相萃取可采用固相萃取板进行(例如:prime-hlb固相萃取板等)。所述干燥可采用氮气吹干等常规干燥方法。
作为本发明的优选实施方式,总钴胺素检测的样品前处理方法如下:取20-200μl血样或校准溶液,加入50-500μl样本制备液,混合震荡,离心后取上清,氮气吹干,分别加入10-50μl第一衍生剂、10-50μl第二衍生剂,反应8-12分钟后加入100-1000μl第三衍生剂;之后将样本加入活化后的固相萃取板,正压洗脱,加入水洗脱,再加入10-100μl固相萃取液(10-80%乙腈溶液),正压洗脱,收集此步洗脱液,氮气吹干,用20-200μl样本复溶液进行复溶,然后进行液相色谱串联质谱检测。
作为本发明的优选实施方式,氰钴胺检测的样品前处理方法如下:取20-200μl血样或校准溶液,加入50-500μl样本制备液,混合震荡,离心后取上清,氮气吹干,加入100-1000μl第三衍生剂;之后将样本加入活化后的固相萃取板,正压洗脱,加入水洗脱,再加入10-100μl固相萃取液(10-80%乙腈溶液),正压洗脱,收集此步洗脱液,氮气吹干,用20-200μl样本复溶液进行复溶,然后进行液相色谱串联质谱检测。
以上所述的方法中,样本复溶可采用0.1-5%的甲酸水溶液。
本发明所述的总钴胺素和氰钴胺的检测方法中,液相色谱的流动相包括流动相a和流动相b,所述流动相a为含有0.01-0.5%甲酸的水溶液,所述流动相b为甲醇。
优选地,所述流动相a为含有0.05-0.2%甲酸的水溶液,所述流动相b为甲醇。
优选地,所述流动相按照以下梯度进行梯度洗脱:0-0.5min,流动相a95%,0.5-3.0min,流动相a95-50%,3.0-4.0min,流动相a50%,4.0-4.01min,流动相a50-2%,4.01-4.5min,流动相a2%,4.5-5.0min,流动相a2-95%。
本发明发现,采用上述流动相体系和洗脱程序有利于提高总钴胺素和氰钴胺检测的准确度和精密度。
优选地,所述流动相的流速为0.3-0.5ml/min。
液相色谱分离优选采用c18或氟苯基柱。进样体积优选为1~10μl。
本发明所述的总钴胺素和氰钴胺的检测方法中,质谱检测条件如下:多离子监测反应模式,正离子模式,电喷雾电离,离子源温度400~600℃,同时监测氰钴胺和氰钴胺内标的离子对:氰钴胺(定量):m/z678.3→147.1;氰钴胺(定性)m/z678.3→997.6;氰钴胺同位素内标:m/z681.7→154.02。
本发明中,所述待测样品可为血清、血浆、全血。
本发明的检测方法可用于总钴胺素和氰钴胺的定性检测或定量检测。在进行定量检测时,利用不同浓度的标准品制作标准曲线,以标准溶液浓度为x轴,标准和内标峰面积的比值为y轴,进行线性回归分析,经“1/x”权重得回归方程。将样品中待测成分与其内标峰面积比代入标准曲线方程,计算样品中总钴胺素和氰钴胺的浓度。样本检测信号强度与同位素内标的比值与样本中待测成分的浓度呈正比。本发明发现,采用本发明的检测方法进行检测,标准曲线的相关系数高,能够满足定量检测的要求。
第二方面,本发明提供用于总钴胺素的液相色谱串联质谱检测的衍生剂,所述衍生剂包括第一衍生剂和第二衍生剂,所述第一衍生剂为含有1-5g/l氰化钠或氰化钾以及10-100g/l氢氧化钠的水溶液;所述第二衍生剂为1-10g/l的二硫代苏糖醇水溶液,ph为2-9。
优选地,所述衍生剂还包括第三衍生剂,所述第三衍生剂为含有0.1%-10%甲酸的水溶液。
进一步优选地,所述第一衍生剂为含有1-3g/l氰化钠或氰化钾以及30-50g/l氢氧化钠的水溶液;所述第二衍生剂为0.8-1.5g/l的二硫代苏糖醇水溶液,ph为4-6;所述第三衍生剂为含有0.5%-2%甲酸的水溶液。
第三方面,本发明提供所述衍生剂在制备总钴胺素和氰钴胺的检测试剂盒中的应用。
第四方面,本发明提供一种总钴胺素和氰钴胺的检测试剂盒,包括:
试剂i:含有1-5g/l氰化钠或氰化钾以及10-100g/l氢氧化钠的水溶液,用于样品衍生化处理;
试剂ii:1-10g/l的二硫代苏糖醇溶液,用于样品衍生化处理;
试剂iii:含有0.1%-10%甲酸的水溶液,用于样品衍生化处理;
试剂iv:含有0.01-0.5%甲酸的水溶液,用于作为液相色谱分离的流动相a;
试剂v:甲醇,用于作为液相色谱分离的流动相b。
可选地,所述试剂盒还包括:
试剂vi:氰钴胺的同位素内标,浓度为50-1000nmol/l;
试剂vii:氰钴胺标准品。
上述氰钴胺标准品可用于配制5nmol/l-4000nmol/l的校准溶液。
上述试剂盒可采用本发明所述的总钴胺素和氰钴胺的检测方法进行使用。
第五方面,本发明提供所述衍生剂或所述试剂盒在总钴胺素和氰钴胺检测中的应用。
本发明的有益效果在于:本发明基于液相色谱串联质谱技术建立了不受内因子抗体等非特异性交叉干扰的lc-ms/ms测定总钴胺素和氰钴胺的方法,该方法用样量少,检测速度快,且具有较高的准确度和精密度,可显著提高总钴胺素和氰钴胺检测的准确性和有效性。该方法可测定样品中总钴胺素和氰钴胺的含量,并可通过两者差值来间接计算其他钴胺素的含量,为各种钴胺素的含量测定提供了有效的技术手段。
附图说明
图1为本发明背景技术中维生素b12的分子结构图。
图2为本发明实施例1中氰钴胺检测的代表性液相色谱图,其中上图为未经衍生化测定的氰钴胺色谱图,下图为氰钴胺同位素内标色谱图。
图3为本发明实施例1中总钴胺素检测的代表性液相色谱图,其中上图为经衍生化后样本中的氰钴胺(其他钴胺素均转化为氰钴胺)色谱图,下图为氰钴胺同位素内标色谱图。
图4为本发明实施例2中氰钴胺检测的代表性液相色谱图,其中上图为经衍生化后样本中的氰钴胺色谱图,下图为氰钴胺同位素内标色谱图。
图5为本发明对比例1中氰钴胺检测的液相色谱图。
图6为本发明实验例3中利用实施例1的方法检测氰钴胺的标准曲线。
图7为本发明实验例3中利用实施例2的方法检测氰钴胺的标准曲线。
图8为本发明实验例4中检测方法的检出限(a)和定量限(b)的评价结果。
具体实施方式
以下实施例用于说明本发明,但不用来限制本发明的范围。
实施例1
本实施例提供一种总钴胺素和氰钴胺的检测方法,该方法采用液相色谱串联质谱法进行检测,具体如下:
1、样品衍生化处理
总钴胺素检测:取100μl血样或校准溶液至2ml塑料管或玻璃管,加入300μl样本制备液,混合震荡,离心后取上清至新管中,氮气吹干,分别加入20μl第一衍生剂、40μl第二衍生剂,10分钟后加入600μl第三衍生剂;之后将衍生后的样本加入活化后的prime-hlb固相萃取板,正压洗脱,加入200μl水洗脱,再加入50μl固相萃取液,正压洗脱,收集此步洗脱液,氮气吹干,用50μl样本复溶液进行复溶,等待上机进行液相色谱串联质谱测试,进样体积:5μl。
氰钴胺素检测:取100μl血样或校准溶液至2ml塑料管或玻璃管,加入200μl样本制备液,混合震荡,离心后取上清至新管中,氮气吹干,加入600μl第三衍生剂;之后将经上述处理的样本加入活化后的oasisprimehlpuelution固相萃取板,正压洗脱,加入200μl水洗脱,再加入50μl固相萃取液,正压洗脱,收集此步洗脱液,氮气吹干,用50μl样本复溶液进行复溶,等待上机进行液相色谱串联质谱测试,进样体积:5μl。
上述使用的试剂配方如下:
样品制备液:含200nmol/l同位素标记氰钴胺的甲醇溶液;
第一衍生剂:含有2g/l氰化钠和40g/l氢氧化钠的水溶液;
第二衍生剂:1g/l的二硫代苏糖醇溶液,ph5.5;
第三衍生剂:含1%甲酸的水溶液;
固相萃取液1:50%乙腈溶液;
样本复溶液:1%甲酸水溶液;
校准溶液:准确称量氰钴胺至定容瓶,使用水配制成母液,之后使用水进行一系列稀释制备成浓度分别为20、50、100、200、500、1000、2000nmol/l的工作校准液。
2、液相色谱检测
流动相:流动相a:含有0.1%甲酸的水溶液;
流动相b:甲醇溶液。
洗脱程序:梯度洗脱程序如表1所示。
表1液相梯度
液相色谱柱:色谱分离采用acquityuplccshfluoro-phenyl1.7μm氟苯基柱。
3、质谱检测
质谱选择多离子监测反应模式,正离子模式,电喷雾电离,离子源温度400~600℃,同时监测氰钴胺和氰钴胺内标的离子对:氰钴胺(定量):678.3→147.1;氰钴胺(定性)678.3→997.6;氰钴胺同位素内标:681.7→154.0
利用上述方法进行血清样本中氰钴胺和总钴胺素检测的代表性色谱图如图2和图3所示。
实施例2
本实施例提供一种总钴胺素和氰钴胺的检测方法,该方法采用液相色谱串联质谱法进行检测,其与实施例1的区别仅在于第一衍生剂:含有2g/l氰化钾和40g/l氢氧化钠的水溶液。利用上述方法进行血清样本中氰钴胺检测的代表性色谱图如图4所示。
对比例1
本对比例提供一种总钴胺素和氰钴胺的检测方法,该方法采用液相色谱串联质谱法进行检测,其与实施例1的区别仅在于不使用第二衍生剂。利用上述方法进行血清样本中氰钴胺检测的色谱图如图5所示。
实验例1检测方法的精密度评价
采用实施例1的方法进行血清样本中总钴胺素和氰钴胺的检测,对检测方法的精密度进行评价,具体方法如下:三个水平血清样本,分三批次测定,每次测定5个平行样,得到批内及总不精密度,评价结果如表2所示,结果表明,本发明的检测方法的精密度良好。
表2lc-ms/ms方法测定总维生素b12不精密度
实验例2检测方法的回收率和准确度评价
氰钴胺和羟钴胺是体液样本中两种主要的钴胺素存在形式。采用分别添加氰钴胺和羟钴胺标准品的加标供试品溶液进行添加回收试验,共设置两个水平的加标供试品溶液。结果如表3所示。
表3回收率和准确度
实验例3定量检测的线性相关性分析
分别配置浓度为20、50、100、200、500、1000、2000nmol/l的氰钴胺标准品溶液。分别采用实施例1和实施例2的检测方法进行检测,以浓度为横坐标,以峰面积为纵坐标,进行线性回归处理,计算回归方程及相关系数。根据测定结果可知,实施例1的检测方法中,氰钴胺在20-2000nmol/l范围内,回归方程为y=0.00045336x-0.00158,相关系数r=0.998,线性关系良好(图6)。实施例2的检测方法中,回归方程为y=0.00039878x-0.00030,相关系数r=0.997,线性关系良好(图7)。
实验例4检测方法的灵敏度评价
利用氰钴胺的标准品溶液检测实施例1的方法对氰钴胺的检测限(lod)和定量限(loq)。结果显示(图8),检出限lod:5nmol/l;信噪比:12.72;定量限loq:10nmol/l;信噪比:37.36。
虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
- 还没有人留言评论。精彩留言会获得点赞!