血液学系统和方法与流程
血液学系统和方法
1.本技术是申请日为2014年03月18日、申请号为201480015388.0(国际申请号为pct/us2014/030942)、名称为“血液学系统和方法”的发明专利申请的分案申请。
2.相关专利申请的交叉引用
3.本技术要求提交于2013年3月15日的美国临时专利申请no.61/799,152以及美国专利申请no.14/215,834、14/216,533、14/216,339、14/216,811和14/217,034的优先权权益,它们的内容以引用的方式并入本文。本技术还涉及提交于2014年3月17日的多份国际专利申请no.pct/us2014/030902、pct/us2014/030928、pct/us2014/030850以及2014年3月18日提交的pct/us2014/030939。这些提交文档中的每一者的内容均以引用方式并入本文。
背景技术:
4.本发明涉及用于粒子分析的装置、系统、组合物和方法的领域,所述粒子分析包括使用全部或部分自动化的设备使流体样品中的粒子成像以区分和定量样品中的粒子诸如血细胞。本发明还涉及可用于分析来自受试者的样品中的粒子的粒子和/或细胞内细胞器配向液(pioal)、用于制备所述液体的方法、以及使用所述液体检测和分析粒子的方法。还公开了可用于进行基于图像的生物流体样品分析的组合物、系统、设备和方法。本发明的组合物、系统、设备和方法也可用于检测、计数和表征生物流体中的粒子诸如红血细胞、网织红细胞、有核红血细胞、血小板,并且可用于基于图像和形态的白血细胞分类计数、分类、子分类、表征和/或分析。
5.血细胞分析是最常执行的用以提供患者健康状态概况的医学测试之一。可从患者身体抽取血样并保存在含有防止凝血的抗凝血剂的试管中。全血样通常包含三种主要类别的血细胞,包括红血细胞(红血球)、白血细胞(白血球)和血小板(凝血细胞)。每一类别可进一步划分成多个成员的亚类别。例如,五种主要类型或亚类别的白血细胞(wbc)具有不同形状和功能。白血细胞可包括中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞和嗜碱性粒细胞。还有红血细胞类型的亚类别。样品中的粒子的外观可根据病理条件、细胞成熟度和其他原因而有所差异。红血细胞亚类别可包括网织红细胞和有核红血细胞。
6.可手动地或使用自动分析仪进行血细胞计数来估计rbc、wbc或血小板浓度。当手动地进行血细胞计数时,将一滴血在显微镜载片上涂成薄层涂片。传统上,使用显微镜载片上的干燥染色血涂片的手动检查来确定五种类型的白血细胞的数量或相对量。使用组织学染料和染液对细胞或细胞结构进行染色。例如,瑞氏染液是用于对血涂片染色以在光学显微镜下检查的组织学染液。可使用自动化分析仪获得全血细胞计数(cbc),其中一种类型的自动化分析仪是基于粒子或细胞沿着小管穿过感测区时的阻抗或动态光散射,对血样中的不同粒子或细胞的数量进行计数。自动化cbc可采用仪器或方法来区分包括rbc、wbc和血小板(plt)的不同类型的细胞,这些细胞可单独地进行计数。例如,要求最小粒度或体积的计数技术可用于仅对大细胞计数。血液中的某些细胞诸如异常细胞可能不能被正确地计数或识别。彼此附着的小细胞可能被错误地计数为大细胞。当怀疑存在错误计数时,可能需要对仪器的结果进行人工复核以验证并识别细胞。
7.自动化血细胞计数技术可涉及流式细胞术。流式细胞术涉及提供窄流路,并且对单个血细胞的通过进行感测和计数。已使用流式细胞方法来检测悬浮于流体中的粒子,诸如血样中的细胞,并且针对粒子类型、尺度和体积分布来分析粒子以便推断血样中的各自粒子类型或粒子体积的浓度。用于分析悬浮于流体中的粒子的合适方法的例子包括沉降、显微表征、基于阻抗和动态光散射的计数。这些工具易出现测试误差。另一方面,粒子类型和浓度的准确表征在诸如医学诊断的应用中可能是关键的。
8.在基于成像的计数技术中,使用耦合到数码相机的显微镜物镜镜头捕获可穿过观察区的制备样品的像素数据图像。像素图像数据可使用数据处理技术进行分析,并且也显示于监视器上。
9.具有流通池的自动化诊断系统的各方面公开于授予turner等人的美国专利no.6,825,926、以及均授予kasdan等人的美国专利no.6,184,978、6,424,415、和6,590,646,所述专利据此以引用方式并入如同在本文完全地阐述。
10.已使用利用动态光散射或阻抗的自动化系统来获得全血细胞计数(cbc):总白血细胞计数(wbc)、红血细胞的总细胞体积(rbc分布)、血红蛋白hgb(血液中的血红蛋白的量);平均细胞体积(mcv)(红细胞的平均体积);mpv(平均plt体积);血细胞比容(hct);mch(hgb/rbc)(每个红血细胞的血红蛋白的平均量);以及mchc(hgb/hct)(细胞中的血红蛋白的平均浓度)。已使用自动化或部分自动化方法来帮助白血细胞五部分分类计数和血样分析。
11.虽然此类当前已知的粒子分析系统和方法以及相关医学诊断技术可为医生、临床医生和患者提供实际益处,但还需要进一步改进。例如,对于在使用自动化系统执行基于图像的样品分析时可用于粒子和/或细胞内细胞器配向的改进方法和组合物有着持续的需求。本发明的实施例对这些尚未解决的需求中的至少一些提供了解决方案。
技术实现要素:
12.本发明的实施例涉及用于分析含有粒子的制备样品的装置、系统、组合物和方法。在一些方面,系统包括可为视觉分析仪的分析仪。在一些方面,装置包含视觉分析仪和处理器。在一个方面,本发明涉及自动化粒子成像系统,其中使含有所关注粒子的液体样品流过具有观察口的流通池,高光学分辨率成像设备通过该观察口来捕获图像。在一些方面,高光学分辨率成像设备包括相机诸如数码相机。在一个方面,高光学分辨率成像设备包括物镜镜头。
13.流通池耦合到样品流体源诸如制备样品,并且耦合到粒子和/或细胞内细胞器配向液(pioal)源。系统允许捕获流动的样品中的粒子的聚焦图像。在一些实施例中,图像可用于自动化、高通量方法以对粒子进行分类和子分类。示例性视觉分析仪可包括处理器以帮助图像的自动化分析。在一些情况下,视觉分析仪可用于本发明的方法以提供自动化的基于图像的wbc分类计数或其他血样粒子分析方案。在一些情况下,本发明的方法涉及自动化识别形态异常以便对受试者是健康还是具有疾病、病症、异常和/或感染进行确定、诊断、预后、预测和/或支持诊断,并且监测受试者是对治疗响应还是无响应。
14.pioal使非球形粒子配向于基本上平行于流动方向的平面中,以致图像优化。pioal还帮助球形细胞将细胞内结构、细胞器或裂片(lobe)定位、重定位和/或更好定位成
基本上平行于流动方向。在一些实施例中,将血小板、网织红细胞、有核rbc和wbc(包括中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞、嗜碱性粒细胞)以及未成熟wbc(包括母细胞、早幼粒细胞、中幼粒细胞或晚幼粒细胞)作为粒子进行计数和分析。
15.本发明的实施例提供可用于用粒子造影剂组合物处理过的细胞中的粒子和/或细胞内细胞器配向的系统、方法和鞘液组合物。此类技术克服了与用于流式细胞术的常规鞘液相关的某些难题,常规鞘液可能存在维持细胞形态和/或不能捕获允许测定一种或多种血液组分的优化图像的缺点。
16.在某些实施例中,在带形样品料流与鞘液之间的粘度差和/或速度差和/或带形样品料流的厚度例如与变窄流路过渡区所提供的几何聚焦作用相结合可引入剪切力而作用在流动中的粒子上,从而导致粒子在视觉分析仪中的整个成像过程中配向或保持配向。在一些实施例中,样品将为造影剂增强的。在一些实施例中,鞘液可包含最多至100%的粘度剂。在另一个实施例中,鞘液具有最多至60%v/v的粘度剂。取决于所用的粘度剂的类型,在一些实施例中,鞘液可包含约5%至7%或更具体地讲6.5%(w/v)的浓度的粘度剂,该粘度剂可以干燥形式商购获得。
17.在其他实施例中,本发明涉及可用于对样品中的粒子(诸如细胞)以及其他生物流体(诸如与特定病症相关的脑脊髓液和积液)中的其他粒子特征进行基于图像的分析的鞘液。如所述用于血样的细胞类目和/或亚类目计数在本发明中作为可以分析的该类样品的非限制性实例。在一些实施例中,存在于样品中的细胞也可包括细菌或真菌细胞以及白血细胞、红血细胞或血小板。在一些实施例中,可分析从组织或抽吸物获得的粒子悬浮液。
18.在一些实施例中,可将样品流体的料流注射穿过具有平坦开口的插管以建立具有相当大的宽度的流路。鞘液可被引入流通池并与样品流体一起输运穿过成像区,然后朝排放口输运。鞘液具有与样品流体不同的粘度,例如更高的粘度,并且任选地,在向带形样品料流注射时的不同流速导致样品流体变平成薄带形状。样品流体的薄带与鞘液一起被输运穿过变窄流路过渡区,以在观察口的前方通过,在观察口处布置高光学分辨率成像设备和光源以观察带形样品料流。
19.在一个实施例中,鞘液的粘度可高于样品的粘度。对鞘液的粘度、样品材料的粘度、鞘液的流速和样品材料的流速进行调整,例如与变窄过渡区所提供的带压缩效应相结合,从而以具有预定尺度特性(诸如有利的带形样品料流厚度)的带形样品料流提供流动。保持有利的带形样品料流厚度提供了例如高百分比的焦点内细胞或焦点内细胞组分。
20.本发明的实施例至少部分地基于以下发现:在鞘液中添加适量的粘度剂明显改善流通池中(例如具有变窄过渡区的流通池中)的粒子/细胞配向,并增加焦点内的细胞的细胞内内容物,从而与使用非粘度改性的用于流式细胞术的常规鞘液相比产生更高质量的流动中的细胞的图像。添加粘度剂增加对细长或非球形粒子或细胞如红血细胞(rbc)的剪切力,然后使细胞在基本上平行于流动方向的平面中配向,以致图像优化。对于如白血细胞(wbc)的细胞,这还导致细胞内结构、细胞器或裂片定位、重定位和/或更好地定位成基本上平行于流动方向。例如,白血细胞可响应于粘度剂或粘度差所赋予的剪切力而压缩或变形,从而导致粒子在剪切下伸长或压缩和配向。
21.直径比流动料流小的粒子的配向可通过增大鞘液的粘度而获得。这使得那些粒子在基本上平行于流动方向的平面中具有改善的配向。
22.带形样品料流厚度可受样品流体和鞘液的相对粘度和流速的影响,例如与流通池的变窄过渡区的几何形状相结合。样品的进料源和/或鞘液的进料源(例如包括精密排量泵)可被配置成以稳定的流速提供样品和/或鞘液以优化带形样品料流的尺度,即作为至少与成像设备的视野一样宽的薄带。
23.示例性鞘液实施例用于在流通池中进行粒子分析。样品被包裹在鞘液的料流中并穿过分析设备的流通池。然后,采集穿过检测区时得自样品的信息,从而使得分析仪能够分析样品中所含的粒子/细胞。在这样的分析仪上使用鞘液允许对样品中所含的细胞和/或粒子进行准确的分类和子分类及计数。
24.如本文所用,鞘液可用于获得与以下细胞和/或其相关粒子有关的信息:包括例如中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞、嗜碱性粒细胞、血小板、网织红细胞、有核rbc、母细胞、早幼粒细胞、中幼粒细胞和/或晚幼粒细胞。
25.本发明提供用于进行粒子分析的新型组合物及其使用方法。具体地讲,本发明涉及用在分析仪中以分析样品中的粒子的粒子和/或细胞内细胞器配向液(pioal)。术语鞘液和pioal在此整个公开内容中可互换使用。本发明还提供用于产生pioal的方法以及使用pioal分析粒子的方法。本发明的pioal可例如用于样品中粒子的自动化分类及子分类方法。
26.在一个方面,本发明的实施例涵盖使用粒子分析系统使多个粒子成像的方法。该系统可被配置用于组合式粘度和几何流体聚焦。粒子可包含在具有样品流体粘度的血液流体样品中。示例性方法可包括使鞘液沿着流通池的流路流动,而鞘液可具有与样品流体粘度相差一个处于预定粘度差范围内的粘度差的鞘液粘度。方法还可以包括将血液流体样品注射到流通池内的流动鞘液中以便提供被鞘液包裹的样品流体料流。另外,方法可包括使样品流体料流和鞘液穿过流路尺寸的缩减段流向成像位点,使得与粘度差相关的鞘液和样品流体料流之间的相互作用所引起的粘度流体聚焦作用连同与流路尺寸的缩减段相关的鞘液和样品流体料流之间的相互作用所引起的几何流体聚焦作用有效地在成像位点在多个粒子的至少一些中提供靶标成像状态,同时鞘液中的粘度剂保持样品流体料流中细胞的活力,使得细胞从样品流体料流延伸到流动鞘液中时细胞的结构和内容物完好无损。而且,方法可包括在成像位点使多个粒子成像。在一些情况下,鞘液的折射率n=1.3330。在一些情况下,鞘液的折射率与水的折射率相同。在一些情况下,与流路尺寸的缩减段相关的鞘液和样品流体料流之间的相互作用通过对多个粒子产生剪切力而有助于提供靶标成像状态。在一些情况下,靶标成像状态包括流动中的一个或多个靶标粒子相对于在成像位点用来采集图像的成像设备的焦平面的靶标取向。
27.根据一些实施例,在成像位点的流路限定基本上平行于焦平面的平面。在一些情况下,靶标取向对应于相对于成像位点处的焦平面的靶标配向。在一些情况下,靶标配向对应于相对于成像位点处的焦平面的靶标粒子配向。在一些情况下,靶标配向对应于相对于成像位点处的焦平面的靶标粒子内结构配向。在一些情况下,靶标取向对应于相对于成像位点处的焦平面的靶标位置。在一些情况下,靶标位置对应于相对于成像位点处的焦平面的靶标粒子位置。在一些情况下,靶标位置对应于相对于成像位点处的焦平面的靶标粒子内结构位置。在一些情况下,靶标位置在焦平面内。在一些情况下,靶标位置与焦平面有一定距离,该距离对应于位置公差。在一些情况下,靶标取向对应于相对于焦平面的靶标配向
和相对于焦平面的靶标位置。在一些情况下,靶标成像状态对应于流动中的一个或多个靶标粒子内结构相对于在成像位点用来采集图像的成像设备的焦平面的靶标取向。在一些情况下,在成像位点的流路限定基本上平行于焦平面的平面。在一些情况下,靶标取向对应于相对于成像位点处的焦平面的靶标配向。在一些情况下,靶标配向对应于相对于成像位点处的焦平面的靶标粒子配向。在一些情况下,靶标配向对应于相对于成像位点处的焦平面的靶标粒子内结构配向。在一些情况下,靶标取向对应于相对于成像位点处的焦平面的靶标位置。在一些情况下,靶标位置对应于相对于成像位点处的焦平面的靶标粒子位置。在一些情况下,靶标位置对应于相对于成像位点处的焦平面的靶标粒子内结构位置。在一些情况下,靶标位置在焦平面内。在一些情况下,靶标位置与焦平面有一定距离,该距离对应于位置公差。在一些情况下,靶标取向对应于相对于焦平面的靶标配向和相对于焦平面的靶标位置。在一些情况下,靶标成像状态对应于一个或多个靶标粒子或一个或多个靶标粒子内结构的靶标变形。
28.根据一些实施例,注射血液流体样品的过程通过将血液流体样品的料流以样品流体速度引导通过样品注射管而进行。注射管可在流路内具有端口。该端口可限定宽度、厚度以及沿着流路延伸的流动轴线。该宽度可大于厚度以使得样品料流具有横向于成像位点附近的成像路径的相对主表面。在一些情况下,沿着流通池的流路流动的鞘液沿着样品料流的主表面延伸,并具有不同于样品流体速度的鞘液速度。在一些情况下,与不同速度相关的鞘液和样品流体之间的相互作用连同与不同粘度相关的鞘液和样品流体之间的相互作用提供靶标成像状态。根据一些实施例,所述多个粒子可包括红血细胞、白血细胞和/或血小板。根据一些实施例,所述多个粒子可包括具有粒子内结构的细胞。在一些情况下,粒子内结构可以为细胞内结构、细胞器或裂片。
29.在一些实施例中,鞘液具有1与10厘泊(cp)之间的粘度。在一些情况下,预定粘度差具有约0.1至约10厘泊(cp)范围内的绝对值。在一些情况下,预定粘度差具有约1.0至约9.0厘泊(cp)范围内的绝对值。在一些情况下,预定粘度差具有约1.0至约5.0厘泊(cp)范围内的绝对值。在一些情况下,预定粘度差具有约3.0厘泊(cp)的绝对值。在一些情况下,鞘液的粘度剂包含甘油、甘油衍生物、乙二醇、丙二醇(二羟基丙烷)、聚乙二醇、聚乙烯吡咯烷酮(pvp)、羧甲基纤维素(cmc)、水溶性聚合物和/或葡聚糖。在一些情况下,鞘液的粘度剂包含约1至约50%(v/v)之间的浓度的甘油。在一些情况下,鞘液的粘度剂包含甘油和聚乙烯吡咯烷酮(pvp)。在一些情况下,鞘液的粘度剂包含5%(v/v)浓度的甘油以及1%(w/v)浓度的甘油和聚乙烯吡咯烷酮(pvp)。在一些情况下,鞘液的粘度剂包含在操作条件下以约3%至约30%(v/v)之间的最终浓度存在的甘油。在一些情况下,鞘液的粘度剂包含在操作条件下以约30%(v/v)的最终浓度存在的甘油。在一些情况下,鞘液的粘度剂包含在操作条件下以约6.5%v/v的最终浓度存在的甘油。在一些情况下,鞘液的粘度剂包含在操作条件下以约5%(v/v)的最终浓度存在的甘油以及以约1%(w/v)的浓度存在的聚乙烯吡咯烷酮(pvp)。
30.根据一些实施例,在成像位点的血液流体样品具有20至200mm/s范围内的线速度。在一些情况下,在成像位点的血液流体样品具有50至150mm/s范围内的线速度。在一些情况下,血液流体样品在成像位点具有最多7μm的样品料流厚度和500至3000μm范围内的样品料流宽度。在一些情况下,血液流体样品在成像位点具有2至4μm范围内的样品料流厚度和1000至2000μm范围内的样品料流宽度。在一些情况下,所述多个粒子包含一组非球形粒子,
所述血液流体样品在成像位点具有流动方向,并且所述一组非球形粒子中的75%以上基本上在平行于所述流动方向的平面内配向,使得各配向的非球形粒子的主表面与平行于所述流动方向的平面平行。在一些情况下,所述多个粒子包含一组非球形粒子,所述血液流体样品在成像位点具有流动方向,并且所述一组非球形粒子中的至少90%在基本上平行于所述流动方向的平面的20度内配向。在一些情况下,所述多个粒子包含粒子内结构,所述血液流体样品在成像位点具有流动方向,并且所述粒子内结构的至少92%基本上平行于所述流动方向。
31.在另一方面,本发明的实施例涵盖用于使具有样品流体粘度的血液流体样品中的多个粒子成像的系统。该系统可被配置成与鞘液一起使用,所述鞘液具有与样品流体粘度相差一个处于预定粘度差范围内的粘度差的鞘液粘度。示例性系统可包括:具有流路和样品流体注射管的流通池,所述流路具有流路尺寸的缩减段;与流通池的流路流体连通以便沿着流通池的流路传递鞘液流的鞘液输入口;以及与流通池的注射管流体连通以便将血液流体样品流注射到流通池内的流动鞘液中的血液流体样品输入口,以使得当鞘液和样品流体穿过流路尺寸的缩减段流向成像位点时,与粘度差相关的鞘液和样品流体之间的相互作用所引起的粘度流体聚焦作用连同与流路尺寸的缩减段相关的鞘液和样品流体之间的相互作用所引起的几何流体聚焦作用在成像位点在所述多个粒子的至少一些中提供靶标成像状态,同时鞘液中的粘度剂保持样品流体料流中细胞的活力,使得细胞从样品流体料流延伸到流动鞘液中时细胞的结构和内容物完好无损。系统还可以包括在成像位点使所述多个粒子成像的成像设备。
32.根据一些实施例,靶标成像状态对应于流动中的一个或多个靶标粒子相对于在成像位点用来采集图像的成像设备的焦平面的靶标取向。在一些情况下,所述多个粒子包括选自红血细胞、白血细胞和血小板的成员。在一些情况下,所述多个粒子包括具有粒子内结构的细胞。细胞内结构可以为细胞内结构、细胞器或裂片。在一些情况下,预定粘度差具有约0.1至约10厘泊(cp)范围内的绝对值。在一些情况下,鞘液的粘度剂包含甘油、甘油衍生物、乙二醇、丙二醇(二羟基丙烷)、聚乙二醇、聚乙烯吡咯烷酮(pvp)、羧甲基纤维素(cmc)、水溶性聚合物和/或葡聚糖。在一些情况下,鞘液的粘度剂包含约1至约50%(v/v)之间的浓度的甘油。在一些情况下,鞘液的粘度剂包含甘油和聚乙烯吡咯烷酮(pvp)。在一些情况下,鞘液的粘度剂包含5%(v/v)浓度的甘油以及1%(w/v)浓度的甘油和聚乙烯吡咯烷酮(pvp)。
33.根据一些实施例,所述多个粒子包含一组非球形粒子,所述血液流体样品在成像位点具有流动方向,并且所述一组非球形粒子中的至少90%在基本上平行于所述流动方向的平面的20度内配向。在一些情况下,靶标取向对应于相对于成像位点处的焦平面的靶标粒子取向。粒子在一些实施例中可以是红血细胞、白血细胞或血小板。在一些情况下,靶标取向对应于相对于成像位点处的焦平面的靶标粒子内结构取向。(例如,粒子内结构可以为细胞内结构、细胞器或裂片)。在一些情况下,在成像位点的流路限定基本上平行于焦平面的平面。在一些情况下,靶标取向对应于相对于成像位点处的焦平面的靶标配向。在一些情况下,靶标配向对应于相对于成像位点处的焦平面的靶标粒子配向。在一些情况下,靶标配向对应于相对于成像位点处的焦平面的靶标粒子内结构配向。在一些情况下,靶标取向对应于相对于成像位点处的焦平面的靶标位置。在一些情况下,靶标位置对应于相对于成像
位点处的焦平面的靶标粒子位置。在一些情况下,靶标位置对应于相对于成像位点处的焦平面的靶标粒子内结构位置。在一些情况下,靶标位置在焦平面内。在一些情况下,靶标位置与焦平面有一定距离,该距离对应于位置公差。在一些情况下,靶标取向对应于相对于焦平面的靶标配向和相对于焦平面的靶标位置。在一些情况下,靶标成像状态对应于成像位点的靶标变形。
34.根据一些实施例,血液流体样品源可被配置成为血液流体样品提供进入流动鞘液中的样品流体速度,以使得鞘液具有与样品流体速度不同的鞘液速度。在一些情况下,与不同速度相关的鞘液和样品流体之间的相互作用连同与不同粘度相关的鞘液和样品流体之间的相互作用提供靶标成像状态。
35.根据一些实施例,流通池的流路包括具有流路尺寸变化的区,并且与流路尺寸变化相关的鞘液和样品流体之间的相互作用连同与不同粘度相关的鞘液和样品流体之间的相互作用提供靶标成像状态。在一些情况下,与流路尺寸变化相关的鞘液和样品流体之间的相互作用通过产生侧向流体压缩力而有助于提供靶标成像状态。在一些情况下,所述多个粒子包括红血细胞、白血细胞和/或血小板。在一些情况下,所述多个粒子包括具有粒子内结构的细胞,并且所述结构可以是细胞内结构、细胞器或裂片。
36.根据一些实施例,预定粘度差具有约0.1至约10厘泊(cp)范围内的绝对值。在一些情况下,预定粘度差具有约1.0至约9.0厘泊(cp)范围内的绝对值。在一些情况下,预定粘度差具有约1.0至约5.0厘泊(cp)范围内的绝对值。在一些情况下,预定粘度差具有约3.0厘泊(cp)的绝对值。在一些情况下,鞘液包含粘度剂,所述粘度剂可包括甘油、甘油衍生物、乙二醇、丙二醇(二羟基丙烷)、聚乙二醇、聚乙烯吡咯烷酮(pvp)、羧甲基纤维素(cmc)、水溶性聚合物和/或葡聚糖。在一些情况下,鞘液包含约1至约50%(v/v)之间的浓度的甘油。
37.根据一些实施例,在成像位点的血液流体样品具有20至200mm/s范围内的线速度。在一些情况下,在成像位点的血液流体样品具有50至150mm/s范围内的线速度。在一些情况下,血液流体样品在成像位点具有最多至7μm的样品料流厚度和超过500μm的样品料流宽度。在一些情况下,血液流体样品在成像位点具有2至4μm范围内的样品料流厚度和1000至2000μm范围内的样品料流宽度。在一些情况下,所述多个粒子包含一组非球形粒子,所述血液流体样品在成像位点具有流动方向,并且所述一组非球形粒子中的至少90%基本上在平行于所述流动方向的平面中配向和/或定位。在一些情况下,所述多个粒子包含一组非球形粒子,所述血液流体样品在成像位点具有流动方向,并且所述一组非球形粒子中的至少95%在基本上平行于所述流动方向的平面的20度内配向。在一些情况下,所述多个粒子包含粒子内结构,所述血液流体样品在成像位点具有流动方向,并且所述粒子内结构的至少92%基本上平行于所述流动方向。
38.在另一方面,本发明的实施例涵盖用于组合式粘度和几何流体聚焦分析仪的粒子和细胞内细胞器配向液(pioal)。pioal可引导被注射到视觉分析仪的变窄流通池过渡区中的给定粘度的血样流体的流动,以便产生被pioal包裹的样品流体料流。pioal可包含粘度比血样流体的粘度更高的流体。与粘度差相关的pioal流体和样品流体之间的相互作用所引起的粘度流体聚焦作用连同与变窄流通池过渡区相关的pioal流体和样品流体之间的相互作用所引起的几何流体聚焦作用有效地在视觉分析仪的成像位点在多个粒子的至少一些中提供靶标成像状态,同时pioal中的粘度剂保持样品流体料流中细胞的活力,使得细胞
从样品流体料流延伸到流动鞘液中时细胞的结构和内容物完好无损。在一些情况下,鞘液的粘度剂包含甘油、甘油衍生物、乙二醇、丙二醇(二羟基丙烷)、聚乙二醇、聚乙烯吡咯烷酮(pvp)、羧甲基纤维素(cmc)、水溶性聚合物和/或葡聚糖。在一些情况下,鞘液的粘度剂包含约1至约50%(v/v)之间的浓度的甘油。在一些情况下,鞘液的粘度剂包含聚乙烯吡咯烷酮(pvp)。在一些情况下,聚乙烯吡咯烷酮(pvp)的浓度为1%(w/v)。在一些情况下,鞘液的粘度剂还包含甘油。在一些情况下,鞘液的粘度剂包含5%(v/v)浓度的甘油以及1%(w/v)浓度的甘油和聚乙烯吡咯烷酮(pvp)。在一些情况下,pioal具有约1
‑
10cp的粘度。
39.在又一个方面,本发明的实施例涵盖用于被配置成引导给定粘度的样品在流路中流动的视觉分析仪的粒子和细胞内细胞器配向液(pioal)。pioal可包含粘度比样品的粘度更高的流体。pioal可有效支持样品的流动以及使粒子配向并增大在流路中流动的粒子和细胞的细胞内细胞器的焦点内内容物,于是可以使配向的粒子和细胞的细胞内细胞器成像。在一些情况下,pioal还包含粘度剂。在一些情况下,pioal还包含缓冲剂、ph调节剂、抗微生物剂、离子强度改性剂、表面活性剂和/或螯合剂。在一些情况下,粒子和细胞内细胞器配向液为等渗的。在一些情况下,粒子和细胞内细胞器配向液包含氯化钠。在一些情况下,其中氯化钠以约0.9%的浓度存在。在一些情况下,pioal样品的ph在操作条件下在约6.0至约8.0之间。在一些情况下,pioal样品混合物的ph在操作条件下在约6.5至约7.5之间。在一些情况下,pioal包含用于将操作条件下的ph调到约6.8至约7.2的ph调节剂。在一些情况下,pioal液体在操作条件下具有约1
‑
10厘泊之间的靶标粘度。
40.在再一个方面,本发明的实施例涵盖浓缩的pioal的储备液。在一些情况下,浓缩的储备液可稀释以达到靶标粘度。在一些情况下,储备液的浓度在操作条件下以pioal的至少约1.1x至至少约100x浓度存在。在一些情况下,
41.139。根据权利要求127所述的pioal,其中所述粘度剂选自如下的至少一者:甘油、甘油衍生物;pvp、cmc、乙二醇;丙二醇(二羟基丙烷);聚乙二醇;水溶性聚合物和葡聚糖。在一些情况下,粘度剂包含甘油。在一些情况下,粘度剂包含甘油和聚乙烯吡咯烷酮(pvp)。在一些情况下,粘度剂包含甘油和羧甲基纤维素(cmc)。在一些情况下,粘度剂包含甘油和硫酸葡聚糖。在一些情况下,粘度剂包含甘油衍生物。在一些情况下,粘度剂包含pvp。在一些情况下,粘度剂包含丙二醇(二羟基丙烷)。在一些情况下,粘度剂包含聚乙二醇。在一些情况下,粘度剂包含水溶性葡聚糖。在一些情况下,甘油在操作条件下以约1至约50%(v/v)之间的最终浓度存在。在一些情况下,所述甘油在操作条件下以约3至约30%(v/v)之间的最终浓度存在。在一些情况下,所述甘油在操作条件下以约30%(v/v)的最终浓度存在。在一些情况下,所述甘油在操作条件下以约6.5%v/v的最终浓度存在。在一些情况下,在操作条件下所述甘油以约5%v/v的最终浓度存在而pvp以约1%w/v的浓度存在。在一些情况下,所述pvp在操作条件下以约1%w/v的最终浓度存在。在一些情况下,本发明的实施例涵盖包含如本文所述的pioal的试剂盒。
42.在另一方面,本发明的实施例涵盖用于分析具有样品流体粘度的血液流体样品中的多个细胞的方法,所述细胞具有相对的主表面。示例性方法可包括使鞘液沿着流通池的流路流动。鞘液可具有比样品流体粘度更高的鞘液粘度。方法还可以包括将血液流体样品注射到流通池内的流动鞘液中。所述多个细胞可包括第一亚组,其具有横向于成像路径的取向而取向的主表面。方法还可以包括在所述多个细胞包括具有横向于成像路径而取向的
主表面的第二亚组时沿着成像位点的成像路径使粒子成像,第二亚组的数量比第一亚组更多。方法还可以包括引导流体血样和鞘液穿过流路尺寸的缩减段,使得与不同粘度相关的鞘液和样品流体之间的相互作用使所述多个细胞中的至少一些重新取向,使得第二亚组的数量比第一亚组更多。
43.在另一方面,本发明的实施例涵盖用于使具有样品流体粘度的血液流体样品中的多个细胞成像的系统。系统可被配置成与具有比样品流体粘度更高的鞘液粘度的鞘液一起使用,所述细胞具有相对的主表面。示例性系统可包括具有流路和样品流体注射管的流通池,与流通池的流路流体连通以便沿着流通池的流路传递鞘液流的鞘液输入口,以及与流通池的注射管流体连通以便将血液流体样品流注射到流通池内的流动鞘液中的血液流体样品输入口,使得多个注射的细胞包括第一亚组,其具有横向于成像路径的取向而配向的主表面。在一些情况下,流通池的流路可具有流路尺寸发生变化的区,其被配置成使得与不同粘度相关的鞘液与血样流体之间的相互作用使粒子中的至少一些重新取向。系统还可以包括成像设备,在所述多个细胞的第二亚组的主表面横向于成像路径取向时,该成像设备沿着成像位点的成像路径使所述多个粒子成像。
44.在一个方面,本发明涉及使粒子成像的方法,其包括:使用本发明的粒子造影剂组合物对样品中的粒子进行处理;在包括流通池和自动对焦装置的视觉分析仪中用光照射染色的粒子;获得包裹在粒子和/或细胞内细胞器配向液(pioal)中的粒子的数字化图像;以及基于图像信息分析样品中的粒子。在一些实施例中,粒子选自以下至少一者:中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞、嗜碱性粒细胞、血小板、网织红细胞、有核红血细胞(rbc)、母细胞、早幼粒细胞、中幼粒细胞、晚幼粒细胞、红血细胞(rbc)、血小板、细胞、细菌、颗粒物、细胞团块或细胞碎片或组分。例如,在一些实施例中,所述装置可用于自动化的基于图像的白血细胞(wbc)分类计数,以及形态异常的自动化识别,其可用于对受试者是健康还是具有疾病、病症或感染和/或对治疗有响应还是无响应进行确定、诊断、预后、预测和/或支持诊断。
45.在一个方面,本发明的实施例涵盖使用被配置用于组合式粘度和几何流体聚焦的粒子分析系统使粒子成像的方法。粒子可包含在血液流体样品的第一和第二样品流体内。示例性方法可包括使鞘液沿着粒子分析仪的流通池的流路流动,并且鞘液可具有与血液流体样品的粘度不同的粘度。在一些情况下,鞘液具有与样品流体粘度相差粘度差的鞘液粘度,并且粘度差具有预定的粘度差范围内的值。方法还可包括将第一样品流体从样品流体注射管注射到流通池内的流动鞘液中以便提供具有邻近注射管的第一厚度的样品流体料流。流通池的流路可具有流路尺寸的缩减段使得样品流体料流的厚度从初始厚度降低到邻近图像捕获位点的第二厚度。方法还可包括在流通池的图像捕获位点使来自第一样品流体的第一多个粒子成像,以及通过终止向流动鞘液中注射第一样品流体并向流动鞘液中注射第二样品流体而引发样品流体瞬变。而且,方法可包括在流通池的图像捕获位点使来自第二样品流体的第二多个粒子成像。使第二多个粒子成像可基本上在样品流体瞬变之后和在使第一多个粒子成像的4秒内进行。在一些情况下,流路尺寸的缩减段由具有近侧厚度的近侧流路部分和具有小于近侧厚度的远侧厚度的远侧流路部分限定。样品流体注射管的下游端可定位在近侧流路部分的远侧。鞘液与血液流体样品之间的粘度差连同流路尺寸的缩减段可有效地在图像捕获位点流体聚焦第一和第二样品流体,同时鞘液中的粘度剂保持第一
和第二样品流体中的细胞的活力,使细胞从样品流体料流延伸到流动鞘液中时细胞的结构和内容物完好无损。
46.在一些方法中,注射管可包括内部体积,其基于注射管的流动区横截面与流通池的流动区横截面的比率、注射管的流动区横截面与流通池的外径的比率、或注射管的流动区横截面与样品料流的流动区横截面的比率。在一些情况下,流路尺寸的缩减段可由流路的相对壁限定,所述相对壁沿着流路径向地向内成角度,总体上关于横向平面对称,所述横向平面平分样品流体料流第一和第二厚度。在一些情况下,流路尺寸的缩减段的对称性能有效地将血液流体样品中的红血细胞成像取向失准限制到小于约20%。在一些情况下,血液流体样品包括球形粒子,并且样品流体与鞘液之间的粘度差能有效地在流通池的图像捕获位点将球形粒子的细胞内细胞器配向在焦平面内。在一些情况下,样品流体注射管的远侧部分定位在离图像捕获位点的轴向分隔距离,并且轴向分隔距离具有约16mm至约26mm范围内的值。在一些情况下,注射管具有小于约30μl的内部体积。
47.在一些方法中,注射管含有具有第一流动横截面积的近侧部分和具有第二流动横截面积的远侧部分,并且近侧部分的流动横截面积大于远侧部分的流动横截面积的1.5倍。在一些方法中,注射管具有设置在近侧部分与远侧部分之间的中心部分,所述中心部分具有第三流动横截面,并且第三流动横截面大于第一和第二流动横截面。
48.在一些方法中,样品流体注射管的远侧部分包括具有高度和宽度的出口,并且所述高度可小于所述宽度。在一些情况下,高度为约150μm并且宽度为约1350μm。在一些情况下,高度具有约50μm至约250μm范围内的值并且宽度具有约500μm至约3000μm范围内的值。
49.在一些方法中,鞘液流速与样品流体流速的比率为约70。在一些情况下,鞘液流速与样品流体流速的比率为约200。在一些情况下,鞘液具有约35μl/s的流速并且样品流体具有约0.5μl/s的流速。在一些情况下,在图像捕获位点处样品流体具有约20与200mm/s之间的速度。在一些情况下,在邻近注射管管出口的流路位置处鞘液速度和流体样品速度可不同,并且在图像捕获位点处鞘液速度和流体样品速度可相同。在一些情况下,样品流体料流的第一厚度为约150μm,例如在样品流体离开注射管的情况下。在一些情况下,样品流体料流的第二厚度在约2μm至约10μm的范围内,例如在样品流体料流流过图像捕获位点的情况下。在一些情况下,样品流体料流的第二厚度在约2μm至约4μm的范围内。在一些情况下,样品流体料流的第一厚度与样品流体料流的第二厚度的比率具有约20:1至约70:1范围内的值。在一些情况下,样品流体料流的第一厚度与样品流体料流的第二厚度的比率具有约5:1至约200:1范围内的值。在一些情况下,近侧流路部分的近侧厚度与远侧流路部分的远侧厚度的比率具有选自10:1、15:1、20:1、25:1、30:1、35:1、40:1、45:1、50:1、55:1、60:1、65:1、70:1、75:1、80:1、85:1、90:1、95:1、100:1、105:1、110:1、115:1、125:1、130:1、140:1、150:1、160:1、170:1、180:1、190:1和200:1的几何变薄值。在一些情况下,流通池具有约50:1的最小压缩比和约125:1的最大压缩比。
50.在一些方法中,流通池被取向成使得流通池内流动的样品流体和鞘液克服重力流动。在一些情况下,流通池被取向成使得流通池内流动的样品流体和鞘液在重力作用下流动。示例性方法还可包括从流动样品流体中移除气泡。在一些情况下,在将第一样品流体从样品流体注射管注射到流动鞘液中后约1至3秒内,第一样品流体达到稳定状态。在一些情况下,在将第一样品流体从样品流体注射管注射到流动鞘液中后小于1秒内,第一样品流体
达到稳定状态。在一些情况下,在将第一样品流体从样品流体注射管注射到流动鞘液中后约1.8秒内,第一样品流体达到稳定状态。在一些情况下,样品流体具有约2至4秒范围内流过流通池的通过时间。在一些情况下,图像捕获位点具有约150μm
×
150μm与400μm
×
400μm之间的视野。在一些情况下,第一样品流体具有约50至约150μl范围内的体积。在一些情况下,注射管的近侧部分耦合到样品入口配件的样品口。
51.在另一个方面,本发明的实施例涵盖执行组合式粘度和几何流体聚焦以便使血液流体样品中的粒子成像的粒子分析系统。粒子可包含在第一和第二样品流体内。示例性系统可包括具有被配置用于传递鞘液流的流路的流通池。鞘液可具有与血液流体样品的粘度不同的粘度。在一些情况下,鞘液粘度大于血液流体样品粘度。在一些情况下,鞘液具有与样品流体粘度相差粘度差的鞘液粘度,并且粘度差具有预定的粘度差范围内的值。系统还可包括与流路流体连通的样品流体注射系统。样品流体注射系统可被配置用于将样品流体注射到流通池内的流动鞘液中以便提供具有邻近注射管的第一厚度的样品流体料流。流通池的流路可具有流路尺寸的缩减段使得样品流体料流的厚度从初始厚度降低到邻近图像捕获位点的第二厚度。此外,系统可包括与图像捕获位点配向的图像捕获设备以便在流通池的图像捕获位点处使来自第一样品流体的第一多个粒子成像。而且,系统可包括与样品流体注射器系统和图像捕获设备耦合的处理器。处理器可被配置成终止向流动鞘液中注射第一样品流体并向流动鞘液中注射第二样品流体使得样品流体瞬变被引发,以及在样品流体瞬变后和在使第一多个粒子成像的4秒内,在流通池的图像捕获位点处使来自第二样品流体的第二多个粒子成像。在示例性系统中,鞘液与血液流体样品之间的粘度差连同流路尺寸的缩减段能有效地在流通池的图像捕获位点处流体聚焦第一和第二样品流体,同时鞘液中的粘度剂保持第一和第二样品流体中的细胞的活力,使细胞从样品流体料流延伸到流动鞘液中时细胞的结构和内容物完好无损。
52.在一些系统中,注射管包括内部体积,其基于注射管的流动区横截面与流通池的流动区横截面的比率、注射管的流动区横截面与流通池的外径的比率、或注射管的流动区横截面与样品料流的流动区横截面的比率。在一些情况下,流路尺寸的缩减段由流路的相对壁限定,所述相对壁沿着流路径向地向内成角度,总体上关于横向平面对称,所述横向平面平分样品流体料流第一和第二厚度。在一些情况下,流路尺寸的缩减段的对称性能有效地将血液流体样品中的红血细胞成像取向失准限制到小于约20%。在一些情况下,样品流体注射管的远侧部分定位在离图像捕获位点的轴向分隔距离,并且轴向分隔距离具有约16mm至约26mm范围内的值。在一些情况下,注射管包括具有第一流动横截面积的近侧部分和具有第二流动横截面积的远侧部分,并且近侧部分的流动横截面积大于远侧部分的流动横截面积的1.5倍。在一些情况下,样品流体具有约2至4秒范围内流过流通池的通过时间。在一些情况下,流通池被配置成在第一流动方向上在流路中接收来自鞘液源的鞘液,所述第一流动方向垂直于沿着成像位点处的流路的鞘液的第二流动方向。在一些情况下,流通池包括图像捕获设备的自动对焦靶标。
53.本发明的实施例涵盖使用示例性动态或检测范围扩展技术定量存在于血液流体样品中的细胞或粒子的系统和方法。
54.例如,示例性实施例涵盖用于基于参数诸如粒子体积来校正与至少一个检测范围相关的不准确粒子计数的技术。通过操作如本发明中所述的装置,可准确地检测和测量浓
度和/或体积在检测范围之外的粒子。
55.如本文所用,与本发明提及的粒子计数器相关的术语“检测限值”或“检测范围之外”应当理解为涵盖这样的范围,在该范围内粒子计数更准确和/或在该范围之外粒子计数较不准确或甚至不可操作。检测范围可包括检测上限和/或检测下限,通常表示为最大或最小浓度,但也可以表示为在给定精度公差内对粒子进行计数的最大或最小频率。因此,本发明的实施例涵盖用于血液流体样品的并行流通池和阻抗分析以定量稀少和/或大量物质计数的系统和方法。
56.检测范围可基于浓度(可包括局部浓度)和/或其他规定的一种或多种标准。例如,比正常plt更小的粒子诸如血细胞或碎片(即,具有小于2μm的直径)可能难以在粒子计数器中准确地检测和计数。比正常白细胞更大的异常细胞(即,具有高于15μm的直径)可能难以在粒子计数器中准确地检测和计数。此外,在高浓度时,rbc和plt可能难以准确地计数。即使在稀释后,rbc和plt也可能聚集形成团块,导致使用粒子计数器得到的粒子计数的读数错误。此外,难以提供以低浓度存在于样品中的一些未成熟或异常血细胞的准确计数。
57.例如,通过使用本文所述的装置,测量的检测范围、wbc的检测上限在一些实施例中可扩展最多至每单位体积300,000、400,000、500,000、600,000、700,000、800,000、900,000或1,000,000。plt的检测下限在一些实施例中可扩展到低于每μl 20,000、19,000、18,000,17,000、16,000、15,000、14,000、13,000、12,000、11,000、10,000、9,500、9,000、8,500、8,000、7,500、7,000、6,500、6,000、5,500、5,000、4,500、4,000、3,500、3,000、2,500、2,000、1,500或1,000、或500。
58.相关地,示例性实施例涵盖用于通过区分在一个通道中检测到的不同类别(包括每种类别的成员)的粒子来校正粒子计数器中获得的不准确结果的技术。如本文所述,一些粒子具有类似体积或形态并且可在一个通道中检测到。例如,在被设计成检测wbc的一个通道中,“巨大”plt、plt聚集体或团块和有核rbc可被计数为“wbc”。此外,其他物质诸如未裂解细胞、冷球蛋白、海因茨小体和疟原虫可被计数为“wbc”,从而得出的wbc计数高于实际存在于样品中的wbc计数。相似地,高浓度的wbc和巨大plt可被计数为“rbc”并导致rbc计数高于实际值。小细胞性红细胞、红细胞内含物、白细胞碎片、尘粒、溶血/裂细胞和甚至电子/电噪声的存在可导致plt的计数高于实际值。另一方面,相同类别内的凝集和涂抹细胞或一种类别的细胞与另一种类别的混淆可导致粒子计数器上对应类别的细胞的计数不准确且偏低。
59.在本发明方法的一些方面,第一类目和/或亚类目的粒子以高于适用于第一类目和/或亚类目的粒子的检测范围的浓度存在于样品中;并且第二类目和/或亚类目的粒子在适用于第二类目和/或亚类目的粒子的检测范围内存在于样品中。在本发明方法的其他方面,第一类目和/或亚类目的粒子以低于适用于第一类目和/或亚类目的粒子的检测范围的浓度存在于样品中,并且第二类目和/或亚类目的粒子在适用于第二类目和/或亚类目的粒子的检测范围内存在于样品中。在其他方面,第一类目和/或亚类目的粒子包括异常血细胞、未成熟血细胞、成团血细胞、具有大于15微米的直径的血细胞、以及具有小于2微米的直径的血细胞中的至少一种类型;并且第二类目和/或亚类目的粒子包括白血细胞。
60.通过操作如本发明中所述的装置,在粒子计数器的一个通道中被错误计数为另一种类型的粒子的那些粒子可被单独并准确地测量。示例性方法也可用于测定不能在粒子计
数器上准确地检测的粒子的粒子计数或浓度。这些粒子包括但不限于在正常体积范围之外的粒子和/或以在粒子计数器上可检测的浓度的高端或低端附近或之外的浓度存在的粒子。相关地,通过操作如所述的系统装置(特别包括粒子计数器和图像分析仪)连同如本发明中所述的示例性粒子造影剂组合物和pioal,在粒子计数器的一个通道中可能被错误计数为另一种类型的粒子的一些粒子可被单独并准确地测量。本发明的方法也可在一些情况下用于测定不能在粒子计数器上准确地检测的粒子的粒子计数或浓度。这些粒子包括但不限于在检测范围之外的粒子和/或以在粒子计数器上可检测的浓度的高端或低端附近或之外的浓度存在的粒子。这通过应用得自图像分析仪的信息来进行。
61.总而言之,通过操作如本文所公开的装置,例如使用示例性粒子造影剂组合物和pioal鞘液,可在粒子计数器的标称检测范围之外的检测范围内进行包含粒子诸如血细胞或其他碎片的样品的分析。相关地,使用如本文所述的系统和组合物时,可在基于参数诸如浓度或粒子体积的扩展检测范围内进行血液流体样品的分析。扩展检测范围可在粒子计数器的检测范围之外。
62.在一些实施例中,系统或装置可包括粒子计数器。在其他实施例中,该粒子计数器具有至少一个检测范围。在某些方面,分析仪和处理器可被配置成提供另外的信息以校正与粒子计数器相关的测试误差,并且还测定样品中不同类目和/或亚类目的粒子的准确粒子计数或浓度。如果可从粒子计数器和分析仪获得关于在粒子的至少两个类目和/或亚类目内的计数、一个或多个比率和/或分布的信息,则可校正来自粒子计数器的计数、分类和/或子分类的误差,并且可得到最初未被粒子计数器报告的计数、类目和/或亚类目。
63.本发明的实施例涵盖某些聚焦技术,其允许血液学系统和方法产生存在于流体血样中的粒子的高质量图像。此类高质量图像提供实现可用于准确地对细胞分类的高区分水平的基础,允许使用具有高放大倍率和高数值孔径的物镜的光学系统。示例性光学配向或聚焦技术有利于产生具有高分辨率水平的图像,且具有与输运粒子的流体样品的薄带相对应的短视野深度。
64.在一些情况下,可定期地重新聚焦血液学系统以针对局部温度和其他因素的变化进行调整。例如,如本文所述的自动对焦技术可补偿存在于血液学分析仪中的热膨胀或其他因素,它们会改变成像物镜与流通池之间的距离,从而例如通过产生偏离焦点的图像而对成像结果造成负面影响。本发明的实施例还涵盖用于血液学仪器的自动对焦系统和方法,其涉及使成像系统自动地聚焦而无需聚焦液体或溶液或其他用户干预。例如,示例性自动对焦技术可涉及获得对相对于流通池固定的靶标的初始聚焦,而非使用基于使出现于图像中的主题自身的对比度最大化的技术。
65.本发明的某些实施例至少部分地基于这样的观察:流通池内的料流位置不会响应于温度波动而变化,并且可涉及使靶标聚焦在流通池的某处,然后使用固定偏移量实现对样品料流的良好聚焦。此类方法可在不使用流过流通池的聚焦溶液的情况下具体实施,并且可自动地且对用户完全透明化地执行。
66.根据一些实施例,本发明涉及用于使包含悬浮于液体中的粒子的样品成像的视觉分析仪,其中装置包括耦合到样品源和耦合到pioal源的流通池,其中流通池限定内部流路,流通池被配置成将被pioal包裹的带形样品料流的流引导穿过流通池中的观察区。与高光学分辨率成像设备相关的物镜镜头设置在与带形样品料流相交的光轴上。物镜和流通池
之间的相对距离可通过耦合到控制器的电机驱动器的操作来改变,以便在光敏元件阵列上分辨和采集数字化图像。自动对焦光栅或成像靶标设置在相对于流通池固定的位置处,自动对焦光栅位于离制备的带形样品料流的平面的预定距离处。光源照明带形样品料流和自动对焦光栅。至少一个数字处理器与耦合的控制器相连以操作电机驱动器。处理器还被布置用于分析数字化图像。处理器测定自动对焦光栅的位置以生成聚焦图像,然后使物镜和流通池在离聚焦位置的预定距离(例如,位移距离)内相对地位移,以将高光学分辨率成像设备聚焦于带形样品料流。
67.在一个方面,本发明的实施例涵盖使用粒子分析系统使血液流体样品中的粒子成像的方法。粒子分析系统可被配置用于几何流体聚焦。在一些情况下,该系统可被配置用于组合式粘度和几何流体聚焦。在一些情况下,粒子可包含在具有样品流体粘度的血液流体样品中。示例性方法可包括使鞘液沿着粒子分析系统的流通池的流路流动。在一些情况下,鞘液可具有与样品流体粘度相差一个处于预定粘度差范围内的粘度差的鞘液粘度。方法还可包括将血液流体样品注射到流通池内的流动鞘液以使得血液流体样品流体以流动料流宽度大于流动料流厚度的样品流动料流流动,样品流动料流流过流路尺寸的缩减段并横穿成像轴。此外,方法可包括通过使具有相对于流通池固定的位置的成像靶标成像来使图像捕获设备聚焦。而且,方法可包括使用图像捕获设备在流动料流内采集适用于粒子表征和计数的粒子的聚焦图像,其中使用位移距离使图像捕获设备聚焦于样品流动料流。根据一些实施例,鞘液与血液流体样品之间的粘度差连同流路尺寸的缩减段能有效地在成像轴处流体聚焦样品流动料流,同时鞘液中的粘度剂保持样品流动料流中的细胞的活力,使细胞从样品流动料流延伸到流动鞘液中时细胞的结构和内容物完好无损。在一些情况下,样品流动料流在成像轴处具有约2μm至约10μm范围内的厚度。在一些情况下,流路在成像轴处具有约150μm的厚度。在一些情况下,成像靶标位于观察口窗口上,所述观察口窗口设置在样品流动料流与图像捕获设备之间。在一些情况下,成像靶标位于照明窗口上,并且样品流动料流设置在照明窗口与图像捕获设备之间。在一些情况下,位移距离为零。在一些情况下,成像靶标位于照明窗口与观察口窗口之间。在一些情况下,在采集步骤中,通过基于位移距离调节图像捕获设备的焦距而使图像捕获设备聚焦于样品流动料流。
68.根据一些实施例,采集聚焦图像的方法包括使用位移距离调节图像捕获设备与流通池之间的距离。在一些情况下,调节图像捕获设备与流通池之间的距离包括移动图像捕获设备的部件。图像捕获设备的部件可为图像捕获设备的变焦镜头、反射镜、或包括图像捕获设备的组件。在一些情况下,调节图像捕获设备与流通池之间的距离包括移动流通池。在一些情况下,调节图像捕获设备与流通池之间的距离包括移动图像捕获设备的至少光学元件和流通池。在一些情况下,位移距离为沿着成像轴在成像靶标与样品流动料流之间的距离。在一些情况下,位移距离为图像捕获设备与靶标之间的第一焦距和图像捕获设备与样品流动料流之间的第二焦距之间的距离差。在一些情况下,方法包括自动对焦步骤,所述自动对焦步骤涉及将测试流体样品注射到鞘液中以形成流通池内的测试样品流动料流;使用图像捕获设备获得成像靶标的第一聚焦图像,使得聚焦的成像靶标和图像捕获设备限定第一焦距;使用图像捕获设备获得测试样品流动料流的第二聚焦图像,使得聚焦的测试样品流动料流和图像捕获设备限定第二焦距;以及通过计算第一焦距与第二焦距之间的差值获得位移距离。在一些情况下,测试流体样品是相同的血液流体样品并且测试样品流动料流
与样品流动料流相同。在一些情况下,自动对焦步骤建立与图像捕获设备相关的焦平面,并且焦平面相对于图像捕获设备保持静止。在一些情况下,使用温度诸如样品流体温度、鞘液温度、流通池温度或图像捕获设备温度,使图像捕获设备聚焦于样品流动料流。在一些情况下,可使用温度诸如成像位点处的流通池温度、成像位点上游位置处的流通池温度和成像位点下游位置处的流通池温度,使图像捕获设备聚焦于样品流动料流。在一些情况下,可使用温度变化率诸如样品流体温度变化率、鞘液温度变化率、流通池温度变化率或图像捕获设备温度变化率,使图像捕获设备聚焦于样品流动料流。
69.根据一些实施例,方法可包括检测自动对焦再引发信号,以及响应于自动对焦再引发信号而重复自动对焦和图像采集步骤。在一些情况下,自动对焦再引发信号包括或基于温度的变化、聚焦质量的降低、流逝的时间间隔、或用户输入。在一些情况下,图像捕获设备对样品流动料流的聚焦独立于图像捕获设备的温度进行。在一些情况下,成像靶标包括用于将图像捕获设备的成像轴相对于样品流动料流定位的刻度。在一些情况下,成像靶标包括相对于成像轴配向的光圈,使得成像粒子设置在由光圈限定的孔内,并且在自动对焦期间使光圈的一个或多个边缘部分成像。在一些情况下,通过如下方式使图像捕获设备聚焦于样品流动料流:实施图像捕获设备围绕成像轴进行的轴向旋转、流通池围绕沿着成像轴延伸且在成像设备的视野内的轴线进行的轴向旋转、图像捕获设备围绕沿着流路延伸的轴线进行的顶端旋转、流通池围绕沿着流路且在流路内的轴线进行的顶端旋转、图像捕获设备围绕横穿流路和成像轴的轴线进行的倾斜旋转、和/或流通池围绕横穿流路和成像轴且在图像捕获设备的视野内的轴线进行的倾斜旋转。在一些情况下,通过实施流通池的旋转(该旋转以图像捕获设备的视野为中心)而使图像捕获设备聚焦于样品流动料流。在一些情况下,图像捕获设备的自动对焦包括从多个焦点位置中确定最佳焦点位置。
70.在另一方面,本发明的实施例涵盖使血液流体样品中的粒子成像的方法。示例性方法可包括使鞘液沿着流通池的流路流动,以及将血液流体样品注射到流通池内的流动鞘液以使得血液流体样品以流动料流宽度大于流动料流厚度的样品流动料流流动。流通池可具有相关的温度。方法还可包括在与流通池相关的温度处于第一温度时,使图像捕获设备沿着成像轴聚焦于流动料流达到第一焦点状态,以及使用处于第一焦点状态的图像捕获设备采集流动料流内的第一亚组粒子的第一聚焦图像。方法还可包括确定与流通池相关的温度已经历从第一温度到第二温度的变化,以及响应于温度的变化及流通池温度与所需焦点之间的已知关系而自动地将图像捕获设备的焦点从第一焦点状态调节到第二焦点状态。此外,方法可包括使用图像捕获设备在第二焦点状态下采集流动料流内的第二亚组的粒子的第二聚焦图像。在一些情况下,调节图像捕获设备的焦点涉及使用温度的变化及流通池温度与所需焦点之间的已知关系来调节图像捕获设备与流通池之间的距离。在一些情况下,调节图像捕获设备的焦点涉及使用温度的变化及流通池温度与所需焦点之间的已知关系来调节图像捕获设备的焦距。在一些情况下,调节图像捕获设备的焦点涉及实施图像捕获设备围绕成像轴进行的轴向旋转、流通池围绕沿着成像轴延伸且在成像设备的视野内的轴线进行的轴向旋转、图像捕获设备围绕沿着流路延伸的轴线进行的顶端旋转、流通池围绕沿着流路且在流路内的轴线进行的顶端旋转、图像捕获设备围绕横穿流路和成像轴的轴线进行的倾斜旋转、和/或流通池围绕横穿流路和成像轴且在图像捕获设备的视野内的轴线进行的倾斜旋转。在一些情况下,通过实施流通池的旋转(该旋转以图像捕获设备的视野为
中心)而使图像捕获设备聚焦于样品流动料流。
71.在另一方面,本发明的实施例涵盖执行几何流体聚焦或在一些情况下执行组合式粘度和几何流体聚焦以便使血液流体样品中的粒子成像的粒子分析系统。示例性系统可包括具有带有注射管的流路以及具有带有从中穿过的成像轴的成像窗口的流通池。流通池的流路可具有流路尺寸的缩减段。系统还可包括与流路流体连通的鞘液输入口。此外,系统可包括与注射管流体连通的血液流体输入口。血液流体输入口可被配置用于将血液流体样品注射到流通池内的流动鞘液中以使得血液流体样品以流动料流宽度大于流动料流厚度的样品流动料流流动。在一些情况下,鞘液可具有大于血液流体样品的粘度的粘度。而且,系统可包括图像捕获设备、被配置成设定图像捕获设备相对于流通池的焦点状态的聚焦机构、以及具有相对于流通池固定的位置的成像靶标。在一些情况下,成像靶标和样品流动料流可沿着成像轴限定位移距离。此外,系统可包括处理器和聚焦模块,所述聚焦模块具有体现机器可读代码的有形介质,所述机器可读代码在处理器上执行以便操作聚焦机构使用位移距离设定适于粒子表征和计数的图像捕获设备的焦点状态。在一些情况下,鞘液与血液流体样品之间的粘度差连同流路尺寸的缩减段能有效地在成像轴处流体聚焦样品流动料流,同时鞘液中的粘度剂保持样品流动料流中的细胞的活力,使细胞从样品流动料流延伸到流动鞘液中时细胞的结构和内容物完好无损。在一些情况下,聚焦机构可包括被配置成调节图像捕获设备与流通池之间的距离的驱动电机。在一些情况下,成像靶标位于观察口窗口上,所述观察口窗口设置在样品流动料流与图像捕获设备之间。在一些情况下,成像靶标位于照明窗口上,并且样品流动料流设置在照明窗口与图像捕获设备之间。在一些情况下,系统被配置成执行采集步骤,所述采集步骤包括通过基于位移距离调节图像捕获设备的焦距而使图像捕获设备聚焦于样品流动料流。在一些情况下,系统被配置成执行采集步骤以便通过使用位移距离调节图像捕获设备与流通池之间的距离来获得聚焦图像。在一些情况下,系统被配置成通过移动流通池来调节图像捕获设备与流通池之间的距离。在一些情况下,系统被配置成执行自动对焦步骤,所述自动对焦步骤包括将测试流体样品注射到鞘液中以形成流通池内的测试样品流动料流;使用图像捕获设备获得成像靶标的第一聚焦图像,使得聚焦的成像靶标和图像捕获设备限定第一焦距;使用图像捕获设备获得测试样品流动料流的第二聚焦图像,使得聚焦的测试样品流动料流和图像捕获设备限定第二焦距;以及通过计算第一焦距与第二焦距之间的差值获得位移距离。在一些情况下,系统被配置成使用温度诸如样品流体温度、鞘液温度、流通池温度或图像捕获设备温度,使图像捕获设备聚焦于样品流动料流。在一些情况下,系统被配置成检测自动对焦再引发信号,以及响应于自动对焦再引发信号而重复自动对焦和图像采集步骤。
72.在另一方面,本发明的实施例涵盖使血液流体样品中的粒子成像的系统。示例性系统可包括具有带有注射管的流路以及具有带有从中穿过的成像轴的成像窗口的流通池、与流路流体连通的鞘液输入口、以及与注射管流体连通的血液流体输入口。血液流体输入口可被配置用于将血液流体样品注射到流通池内的流动鞘液中以使得血液流体样品以流动料流宽度大于流动料流厚度的样品流动料流流动。系统还可包括图像捕获设备、被配置成设定图像捕获设备相对于流通池的焦点状态的聚焦机构、热耦合到流通池的温度传感器、处理器以及聚焦模块。聚焦模块可包括体现机器可读代码的有形介质,所述机器可读代码在处理器上执行以便操作聚焦机构响应于温度传感器所感测到的温度变化和温度与所
需焦点之间的已知关系,而设定适于粒子表征和计数的图像捕获设备的焦点状态。在一些情况下,聚焦机构包括被配置成调节图像捕获设备与流通池之间的距离的驱动电机。
73.在另一方面,本发明的实施例涵盖用于血液流体样品中的细胞的分析的方法。示例性方法可包括使鞘液沿着流通池的流路流动,以及将血液流体样品注射到流通池内的流动鞘液以使得血液流体样品以流动料流宽度宽于流动料流厚度的样品流动料流流动。样品流动料流可沿着成像轴与流通池的成像窗口偏移第一距离。方法还可包括通过使附连到流通池的成像靶标成像来使图像捕获设备自动对焦。成像靶标可沿着成像轴定位在离成像窗口的第二距离。此外,方法可包括使用图像捕获设备采集流动料流内适于细胞表征和计数的细胞的聚焦图像。在一些情况下,可使用自动对焦步骤和第一距离与第二距离之间的已知关系而使图像捕获设备聚焦于样品流动料流。
74.在另一方面,本发明的实施例涵盖用于血液流体样品中的细胞的分析的系统。示例性系统可包括具有带有注射管的流路以及具有带有从中穿过的成像轴的成像窗口的流通池。系统还可包括与流路流体连通的鞘液输入口以及与注射管流体连通的血液流体输入口。血液流体输入口可被配置用于将血液流体样品注射到流通池内的流动鞘液中以使得血液流体样品以流动料流宽度大于流动料流厚度的样品流动料流流动。样品流动料流可沿着成像轴与流通池的成像窗口偏移第一距离。系统还可包括可沿着成像轴取向的图像捕获设备。图像捕获设备可包括聚焦机构。此外,系统可包括附连到流通池上的成像靶标。成像靶标可沿着成像轴位于离成像窗口表面的第二距离。而且,系统可包括耦合到聚焦机构的处理器。处理器可被配置成通过使图像捕获设备聚焦于靶标并且通过使用第一距离与第二距离之间的已知关系,采集足以对细胞进行表征和计数的流动料流内的粒子的聚焦图像。
75.在又一方面,本发明的实施例涵盖用于血液流体样品中的细胞的分析的系统。示例性系统可包括具有带有注射管的流路以及具有带有从中穿过的成像轴的成像窗口的流通池。此外,系统可包括与流路流体连通的鞘液输入口以及与注射管流体连通的血液流体样品输入口。样品流体输入口可被配置用于将血液流体样品注射到流通池内的流动鞘液中以使得血液流体样品以流动料流宽度大于流动料流厚度的样品流动料流流动。此外,系统可包括可沿着成像轴取向的图像捕获设备,并且图像捕获设备可包括聚焦机构。系统还可包括热耦合到流通池的温度传感器以及耦合到温度传感器和聚焦机构的处理器。在一些情况下,处理器被配置成响应于温度的变化以及温度与所需焦点之间的已知关系而调节图像捕获设备的焦点,以足以对细胞进行表征和计数。
76.根据一些实施例,视觉分析仪可包括耦合到样品源和鞘液源的流通池。流通池可限定内部流路,并且可被配置成引导被鞘液包裹的样品流穿过流通池中的观察区。分析仪还可包括在与带形样品料流相交的光轴上具有物镜的高光学分辨率成像设备,并且物镜与流通池之间的相对距离可通过电机驱动器的操作来改变,以便在光敏元件阵列上分辨和采集数字化图像。分析仪还可包括具有相对于流通池固定的位置的自动对焦光栅,自动对焦光栅位于离带形样品料流的平面的位移距离处。位移距离可为预定的。分析仪还可包括被配置成照明带形样品料流和自动对焦光栅的光源。此外,分析仪可包括耦合的至少一个数字处理器以操作电机驱动器并分析数字化图像。处理器可被配置成测定自动对焦光栅的焦点位置并且使高光学分辨率成像设备和流通池在离聚焦位置的位移距离内相对地位移,从而使高光学分辨率成像设备聚焦于带形样品料流。根据一些实施例,自动对焦光栅包括具
有有限尺寸的形式并且位移距离是足够的使得当聚焦于带形样品料流时所述形式在数字化图像中基本上不可见。在一些情况下,光轴基本上垂直于带形样品料流。
77.在另一方面,本发明的实施例涵盖使视觉分析仪聚焦以便进行样品分析的方法。示例性方法可包括使高光学分辨率成像设备聚焦于相对于流通池固定的自动对焦光栅,自动对焦光栅位于离带形样品料流的预定的位移距离,高光学分辨率成像设备在与带形样品料流相交的光轴上具有物镜,高光学分辨率成像设备与流通池之间的相对距离可通过电机驱动器的操作来改变,高光学分辨率成像设备被配置成分辨和采集光敏元件阵列上的数字化图像。此外,方法可包括使电机驱动器在位移距离内操作以使高光学分辨率成像设备聚焦于带形样品料流。
78.在另一方面,本发明的实施例涵盖使样品中的粒子成像的方法。示例性方法可包括为包含悬浮于液体中的粒子的样品提供视觉分析仪,在视觉分析仪中建立具有粘度更高和更低的层状截面的流。分析仪可包括耦合到样品源和耦合到具有比样品粘度更高的粘度的pioal的源的流通池。流通池可限定内部流路,并且可引导被pioal包裹的样品流穿过流通池中的观察区。分析仪还可包括在与带形样品料流相交的光轴上具有物镜的高光学分辨率成像设备,并且高光学分辨率成像设备与流通池之间的相对距离可通过电机驱动器的操作来改变,以便在光敏元件阵列上分辨和采集数字化图像。分析仪还可包括具有相对于流通池固定的位置的自动对焦光栅,自动对焦光栅位于已预定的离带形样品料流的平面的位移距离;被配置成照明带形样品料流和自动对焦光栅的光源;耦合以操作电机驱动器并分析数字化图像的至少一个数字处理器,其中处理器被配置成测定自动对焦光栅的焦点位置并且使高光学分辨率成像设备和流通池在离聚焦位置的位移距离内相对地位移,从而使高光学分辨率成像设备聚焦于带形样品料流。在一些情况下,分析仪可包括耦合到样品源和pioal源的流通池,其中流通池限定内部流路并且被配置成引导被pioal包裹的样品流穿过流通池中的观察区;与带形样品料流相交的光轴上具有物镜的高光学分辨率成像设备,物镜与流通池之间的相对距离可通过电机驱动器的操作来改变,以便在光敏元件阵列上分辨和采集数字化图像;具有相对于流通池固定的位置的自动对焦光栅,自动对焦光栅位于已预定的离带形样品料流的平面的位移距离;被配置成照明带形样品料流和自动对焦光栅的光源;耦合以操作电机驱动器并分析数字化图像的至少一个数字处理器,其中处理器被配置成测定自动对焦光栅的焦点位置并且使高光学分辨率成像设备和流通池在离聚焦位置的位移距离内相对地位移,从而使高光学分辨率成像设备聚焦于带形样品料流。
79.粒子造影剂组合物被公开用于对在自动化粒子分析系统中成像的血液流体样品进行染色。粒子造影剂组合物可包括选自结晶紫、新亚甲蓝、甲基绿、伊红y和番红o的至少一种粒子造影剂。粒子造影剂组合物还可包括选自表面活性剂、皂草苷、季铵盐、非离子表面活性剂、清洁剂和两性离子表面活性剂的透化剂。粒子造影剂组合物还可包括选自戊二醛和甲醛的固定剂。
80.在一个实施例中,透化剂可为皂草苷,其存在的量足以产生染色条件下的约50mg/l与约750mg/l之间的浓度。固定剂可为戊二醛,其存在的量足以产生染色条件下的等于或低于0.1%的浓度。
81.在一个实施例中,所述至少一种粒子造影剂可包括结晶紫、新亚甲蓝和伊红
‑
y。结晶紫与新亚甲蓝的比率可为染色条件下的约1:90至约1:110之间。伊红
‑
y存在的量可足以
产生染色条件下的约3μm至约300μm的浓度。
82.在一个实施例中,结晶紫存在的量可足以产生染色条件下的约6μm至约10μm的浓度。新亚甲蓝存在的量可足以产生染色条件下的约70μm至约2.4mm的浓度。伊红
‑
y存在的量可足以产生染色条件下的约10μm至约50μm的浓度。
83.在一些实施例中,结晶紫为大约90%纯或更纯。新亚甲蓝可为大约70%纯或更纯。伊红
‑
y可为大约80%纯或更纯。
84.在一些实施例中,结晶紫存在的量足以产生染色条件下的约7.8μm的浓度。新亚甲蓝存在的量足以产生染色条件下的约735μm的浓度。伊红
‑
y存在的量可足以产生染色条件下的约27μm的浓度。在一些实施例中,粒子造影剂组合物可另外包括缓冲组分。
85.公开了一种对将使用自动化粒子分析系统使其成像的血液流体样品的粒子进行处理的方法。所述方法可包括将血液流体样品与粒子造影剂组合物组合而获得样品混合物,以及将样品混合物在约37℃与约60℃之间的温度下温育少于90秒。粒子造影剂组合物包括选自结晶紫、新亚甲蓝、甲基绿、伊红y和番红o的至少一种粒子造影剂;选自表面活性剂、皂草苷、季铵盐、非离子表面活性剂、清洁剂和两性离子表面活性剂的透化剂;以及选自戊二醛和甲醛的固定剂。
86.在一些实施例中,粒子造影剂的结晶紫、新亚甲蓝的含量可足以产生染色条件下的约1:1至约1:500之间的结晶紫与新亚甲蓝的比率。皂草苷的含量可足以产生染色条件下的约50mg/l与约750mg/l之间的浓度。戊二醛的含量可足以产生染色条件下的等于或低于0.1%的浓度。所述方法可包括将样品混合物温育少于60秒。
87.在一些实施例中,粒子造影剂组合物可包含结晶紫,其存在的量足以产生染色条件下的约6μm至约10μm的浓度。新亚甲蓝存在的量可足以产生染色条件下的约70μm至约2.4mm的浓度。伊红
‑
y存在的量可足以产生染色条件下的约10μm至约50μm的浓度。可以约1:2至约1:10的血液流体样品与粒子造影剂组合物的比率,将血液流体样品与粒子造影剂组合物组合。
88.在一些实施例中,所述方法可包括将样品混合物加热到46℃与约49℃之间持续40至50秒。
89.在某个实施例中,结晶紫可为大约90%纯或更纯。新亚甲蓝可为大约70%纯或更纯。伊红
‑
y可为大约80%纯或更纯。
90.在一些实施例中,粒子造影剂可包含结晶紫,其存在的量足以产生染色条件下的约7.8μm的浓度;新亚甲蓝,其存在的量足以产生染色条件下的约735μm的浓度;以及伊红
‑
y,其存在的量足以产生染色条件下的约27μm的浓度。粒子造影剂组合物还可包含缓冲组分。可以约1:3至约1:4的血液流体样品与粒子造影剂组合物的比率,将血液流体样品与粒子造影剂组合物组合。可将样品混合物加热至约47℃持续约45秒。
91.当结合附图来考虑时通过参考下文的具体实施方式,本发明实施例的上述特征和许多其他特征以及伴随的优点将会变得显而易见并得到进一步地理解。
附图说明
92.图1是根据本发明实施例的以部分横截面表示的且未按比例绘制的示意图,示出了用于使用数字图像处理进行样品图像分析的示例性流通池、和自动对焦系统及高光学分
辨率成像设备的各操作方面。
93.图1a和1b示出了根据本发明实施例的光具座布置方式。
94.图1c是根据本发明实施例的血液学分析仪的框图。
95.图1d示出了根据本发明实施例的方法的流程图。
96.图1e是根据本发明实施例的示例性模块系统的简化框图。
97.图2示出了根据本发明实施例的流通池的各部件。
98.图3、3a和3b示出了根据本发明实施例的流通池的各方面。
99.图4示出了根据本发明实施例的分析仪系统的各方面。
100.图4a示出了根据本发明实施例的流通池。
101.图4b
‑
1和4b
‑
2示出了根据本发明实施例的流通池流路的各方面。
102.图4a
‑
1和4a
‑
2示出了根据本发明实施例的样品料流尺度的变化。
103.图4c描绘了根据本发明实施例的示例性插管或样品进料管的特征
104.图4d描绘了根据本发明实施例的插管的纵截面。
105.图4e示出了根据本发明实施例的远侧平坦区段的横截面。
106.图4f示出了根据本发明实施例的中心渐缩区段的横截面。
107.图4g示出了根据本发明实施例的近侧区段的横截面。
108.图4c
‑
1示出了根据本发明实施例的示例性插管或样品进料管。
109.图4d
‑
1示出了根据本发明实施例的示例性插管或样品进料管。
110.图4h示出了根据本发明实施例的插管的一部分。
111.图4i和4j描绘了根据本发明实施例的流通池。
112.图4k和4l示出了根据本发明实施例的流过流通池的图像捕获位点的样品料流。
113.图4k
‑
1、4k
‑
2和4k
‑
3示出了根据本发明实施例的靶标成像位点。
114.图4l
‑
1示出了根据本发明实施例的抛物线流动剖面。
115.图4m和4n示出了根据本发明实施例的细胞内粒子配向的各方面。
116.图4o示出了根据本发明实施例的使用pioal获得的图像与使用非pioal鞘液获得的图像的比较。
117.图4p和4q示出了根据本发明实施例的使用标准鞘液和示例性pioal流体获得的图像的比较。
118.图4r示出了根据本发明实施例的对称与不对称流通池相比时在pioal中使用0%
‑
30%甘油获得的未配向细胞的百分比的图表。
119.图5描绘了根据本发明实施例的与流通池中一种或多种样品流体的注射相对应的时间表。
120.图5a、5b、5c和5d描绘了根据本发明实施例的使用某些处理技术获得的结果。
121.图5e描绘了根据本发明实施例的与流通池技术相比的基于传统显微镜湿法封片技术的图像捕获结果。
122.图6描绘了根据本发明实施例的使用被配置用于组合式粘度和几何流体聚焦的粒子分析系统使多个粒子成像的示例性方法的各方面。
123.图6a和6b描绘了根据本发明实施例的示例性流动料流特性。
124.图6c描绘了根据本发明实施例的用于使血液流体样品中的粒子成像的示例性方
法的各方面。
125.图7和8描绘了根据本发明实施例的流动料流应变速率的各方面。
126.图9a描绘了根据本发明实施例的示例性自动对焦靶标。
127.图9b示出了根据本发明实施例的包括自动对焦靶标多部分的捕获图像。
128.图10和11描绘了根据本发明实施例的示例性自动对焦靶标。
129.图12a描绘了根据本发明实施例的示例性自动对焦靶标。
130.图12b示出了根据本发明实施例的自动对焦靶标的中心部分的近距离视图。
131.图13a、13b和13c描绘了根据本发明实施例的流通池温度传感器的视图。
132.图13d描绘了根据本发明实施例的流通池气泡移除技术的各方面。
133.图14是根据本发明实施例的框图,示出了用于实现在血样中进行粒子分析的动态或检测范围扩展的系统和方法的另外方面。
134.图15示出了根据本发明实施例的用于分析样品的示例性装置。
135.图15a描绘了根据本发明实施例的示例性计数器或计数模块的各方面。
136.图16描绘了根据本发明实施例的用于测量血液流体样品中的第一细胞类型的数量的系统和方法的各方面。
137.图17示出了根据本发明实施例的用于分析包含粒子的样品的方法。
138.图18示出了根据本发明实施例的测定两个亚类目的粒子的浓度的示例性方法。
139.图19a、19b、19c和19d示出了根据本发明实施例的多个类目的粒子的检测。
140.图20a和20b提供了根据本发明实施例的截面侧视图,其示出了成像系统和方法的各方面。
141.图20c描绘了根据本发明实施例的流通池的截面端视图。
142.图20d示出了根据本发明实施例的图像捕获设备的焦距。
143.图21描绘了根据本发明实施例的正视图,示出了自动对焦光栅的实施例。
144.图22a和22b示出了根据本发明实施例的焦点配置。
145.图23描绘了根据本发明实施例的样品处理技术的各方面。
146.图a1是根据一个实施例的粒子造影剂组合物的制备的示意图。
147.图a2是根据一个实施例的快速一步染色方法的流程图。
148.图a3是根据一个实施例的根据快速一步染色方法染色的所选白血细胞的代表性图示。
149.图a4是根据一个实施例的来自用粒子造影剂组合物染色的样品的所选白血细胞的代表性图示。
150.图a5是根据之前实例1的染色细胞的代表性图示。
151.图a6是根据之前实例2的染色细胞的代表性图示。
152.图a7是根据之前实例3的染色细胞的代表性图示。
153.图a8是根据之前实例4的染色细胞的代表性图示。
154.图a9是根据之前实例的染色细胞的代表性图示。
155.图a10是根据之前实例5的染色细胞的代表性图示。
156.图a11是根据之前实例6的染色细胞的代表性图示。
具体实施方式
157.本发明涉及用于分析包含粒子的样品的装置、系统、组合物和方法。在一个实施例中,本发明涉及包括分析仪(可以为例如视觉分析仪)的自动化粒子成像系统。在一些实施例中,视觉分析仪还可以包括便于图像的自动化分析的处理器。
158.根据本发明,提供了包括视觉分析仪的系统以获得包含悬浮在液体中的粒子的样品的图像。该系统可用于例如表征生物流体中的粒子,诸如检测和定量红血球、网织红细胞、有核红血细胞、血小板和白血细胞,包括白血细胞分类计数、分类及子分类和分析。本发明的实施例也涵盖其他类似的用途,诸如表征其他流体中的血细胞。通常,将血液流体样品引入流动鞘液中,并将合并的鞘液和样品流体通过变窄的流路过渡区压缩,所述过渡区降低样品带形流体流的厚度。因此,诸如细胞的粒子可在血液流体样品内通过周围的粘性鞘液例如连同变窄过渡区所提供的几何聚焦作用而取向和/或压缩。相似地,血液细胞的内部特征可因样品流体与鞘液之间的粘度差例如连同变窄过渡区所提供的几何聚焦作用而取向配向。
159.为了提高对诸如细胞的粒子进行分类和/或子分类的能力、速度和有效性,提供清晰的高质量血细胞图像以通过数据处理系统进行自动化分析是有利的。根据本发明,将制备好的样品料流以在流通池的相对壁之间具有稳定位置的薄带形式布置。样品料流的定位及其变平成薄带形状可通过引入流通池的pioal的层之间的流动而实现,所述pioal与样品流体的粘度不同并流过流动通道的对称变窄过渡区。
160.血液学
‑
粒子分析系统
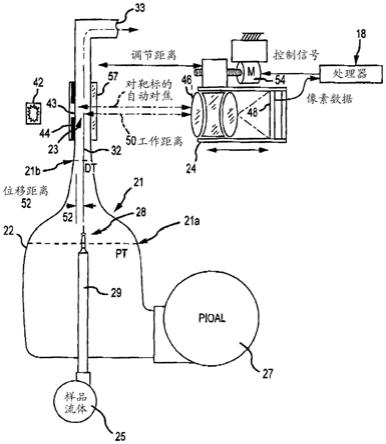
161.现在转到附图,图1示意性地示出了示例性流通池22,所述流通池用于将样品流体传送经过高光学分辨率成像设备24的观察区23,所述高光学分辨率成像设备被配置用于使用数字图像处理使样品流动料流32中的微观粒子成像。流通池22耦合到可接受处理(诸如与粒子造影剂组合物接触并加热)的样品流体源25。流通池22还耦合到一个或多个粒子和/或细胞内细胞器配向液(pioal)源27,诸如粘度大于样品流体的粘度的透明甘油溶液。
162.样品流体被注射通过样品进料管29的远端28的平坦开口,并在一定的点进入流通池22的内部,在所述点已基本上建立了pioal流,从而在带形样品料流的上方和下方(或在其相对侧上)产生稳定和对称的pioal层流。样品和pioal料流可由精密计量泵提供,该泵使pioal与注射的样品流体一起沿着大幅变窄的流路移动。pioal在流路变窄的区21中包裹并压缩样品流体。因此,在区21的流路厚度降低可有助于样品料流32的几何聚焦。样品流体带32被包裹并与pioal一起被输运到变窄区21的下游,从而在高光学分辨率成像设备24的前方经过或以其他方式穿过高光学分辨率成像设备24的观察区23,在所述成像设备中例如使用ccd 48采集图像。处理器18可接收来自ccd 48的像素数据作为输入。样品流体带与pioal一起流向排放口33。
163.如此处所示,变窄区21可具有近侧流路部分21a和远侧流路部分21b,近侧流路部分具有近侧厚度pt而远侧流路部分具有远侧厚度dt,使得远侧厚度dt小于近侧厚度pt。样品流体可因此在位于近侧部分21a远侧和远侧部分21b近侧的位置注射通过样品管29的远端28。因此,当pioal料流被区21压缩时,样品流体可进入pioal包层,其中样品流体注射管具有远侧出口,样品流体穿过该远侧出口注射到流动鞘液中,该远侧出口由流通池的流路尺寸的缩减段界定。
164.具有物镜镜头46的数字高光学分辨率成像设备24沿着与带形样品料流32相交的光轴而定向。物镜46和流通池33之间的相对距离可通过电机驱动器54的操作来改变,以便在光敏元件阵列上分辨和采集聚焦的数字化图像。
165.根据一些实施例,系统可以操作以对样品流体带32进行流体聚焦。术语流体聚焦可指受鞘液与样品流体之间的粘度差、流通池的几何变窄过渡区以及鞘液与样品流体之间的速度差影响的聚焦作用。流体动力流因样品流体料流与鞘液料流之间的速度差而产生,其影响流带厚度和形状。
166.本发明提供自动实现高光学分辨率成像设备24的正确工作位置以对带形样品料流32聚焦的技术。流通池结构22可被配置成使得带形样品料流32在限定样品流体的流路的流通池内具有固定且可靠的位置,以pioal层之间的薄带形式穿过流通池22中的观察区23。在某些流通池实施例中,pioal的流路的横截面在一定点处对称变窄,在该点处将样品插入穿过平坦孔口诸如在孔口具有矩形内腔的管29、或插管。变窄流路(例如,以20:1的比率或以20:1至70:1之间的比率在横截面积上几何变窄)连同pioal与样品流体之间的粘度差以及任选地与样品流相比的pioal的线速度差配合使样品横截面以约20:1至70:1的比率压缩。在一些实施例中,该横截面厚度比率可为40:1。
167.在一个方面,流通池22的对称性质以及样品流体与pioal的注射方式为两层pioal之间的带形样品料流32提供流通池22内的可重复位置。因此,方法变量(诸如样品和pioal的特定线速度)不会倾向于使带形样品料流从其流动位置发生位移。相对于流通池22的结构,带形样品料流32位置是稳定且可重复的。
168.然而,流通池22与光学系统的高光学分辨率成像设备24的相对位置可发生改变并且可受益于不时的位置调节以保持高光学分辨率成像设备24与带形样品料流32之间的最佳或所需距离,从而提供带形样品料流32中的被包裹粒子的高质量聚焦图像。根据一些实施例,高光学分辨率成像设备24与带形样品料流32之间可存在获得被包裹粒子的聚焦图像的最佳或所需距离。可首先通过自动对焦或其他技术使高光学分辨率成像设备24位于离具有相对于流通池22的固定位置的自动对焦靶标44的最佳或所需距离处,从而将光学器件相对于流通池22准确地定位。例如由于初始校准步骤,精确地知道自动对焦靶标44与带形样品料流32之间的位移距离。在对自动对焦靶标44自动对焦后,然后使流通池22和/或高光学分辨率成像设备24在自动对焦靶标44与带形样品料流32之间的已知位移距离内位移。因此,高光学分辨率成像设备44的物镜镜头精确聚焦于包含被包裹粒子的带形样品料流32。
169.本发明的示例性实施例涉及对聚焦或成像靶标44自动对焦,成像靶标44是限定沿着高光学分辨率成像设备或数字图像捕获设备24的光轴的已知位置的高对比度图形。靶标44可具有相对于带形样品料流32的位置的已知位移距离。对比度测量算法可特别地用于靶标特征。在一个例子中,高光学分辨率成像设备24的位置可沿着平行于高光学分辨率成像设备或数字图像捕获设备的光轴的线改变,以找到这样的深度或距离,在该深度或距离处,在沿着图像中已知与对比图形的边缘交叉的像素的线出现的各像素亮度值中可发现一个或多个最大差分幅度。在一些情况下,自动对焦光栅沿着平行于光轴的线没有变化,该线也是这样的线:机动化控制器沿着该线操作以调节高光学分辨率成像设备24的位置,从而提供记录的位移距离。
170.这样,可能不必要自动对焦或依靠于可在不同图像之间变化、就对比度而言不太
高度受限定、或可能位于一系列位置的某处的图像内容方面,作为确定供参考的距离位置的基础。由于发现了对于自动对焦靶标44的最佳或所需焦点的位置,高光学分辨率成像设备物镜24与流通池22的相对位置可移动记录的位移距离从而为带形样品料流32中的粒子提供最佳或所需焦点位置。
171.根据一些实施例,高光学分辨率成像设备24可分辨如由穿过照明开口(窗口)43施加的光源42所背光照明的带形样品料流32的图像。在图1中所示的实施例中,照明开口43的周边形成自动对焦靶标44。然而,目标是通过光敏元件阵列上的高光学分辨率成像设备光学器件46,诸如集成电荷耦合设备,来采集带形样品料流32的精确聚焦图像。
172.高光学分辨率成像设备24及其光学器件46被配置成分辨在距离50处位于焦点内的带形样品料流32中的粒子的图像,所述距离可以是光学系统的尺度、镜头的形状、以及其材料的折射率的结果。在一些情况下,高光学分辨率成像设备24与带形样品料流32之间的最佳或所需距离并未变化。在其他情况下,可改变流通池22与高光学分辨率成像设备及其光学器件46之间的距离。高光学分辨率成像设备24和/或流通池22相对于彼此移动得更靠近或进一步分开(例如,通过调节成像设备24与流通池22之间的距离51)使聚焦点的位置移动到相对于流通池的距离50的末端。
173.根据本发明的实施例,聚焦靶标44可位于离带形样品料流32的一定距离处,在这种情况下在来自照明源42的光所用的开口43的边缘处直接固定于流通池22。聚焦靶标44位于离带形样品料流32的恒定位移距离52处。通常,位移距离52是恒定的,因为带形样品料流32在流通池中的位置保持恒定。
174.示例性自动对焦工序涉及使用电机54调节高光学分辨率成像设备24与流通池22的相对位置以达到适当的焦距,从而使高光学分辨率成像设备24聚焦于自动对焦靶标44。在该例子中,自动对焦靶标44位于流通池中的带形样品料流32的后面。然后使高光学分辨率成像设备24朝向或远离流通池22移动直到自动对焦工序确定光敏元件上分辨的图像是自动对焦靶标44的精确聚焦图像。然后操作电机54以使高光学分辨率成像设备24与流通池22的相对位置位移,使得高光学分辨率成像设备聚焦于带形样品料流32,也就是通过使高光学分辨率成像设备24远离流通池22移动精确的位移距离52的跨度来进行。在该示例性实施例中,成像设备24被示出为通过电机54来移动以到达焦点位置。在其他实施例中,通过类似装置移动流通池22或移动流通池22和成像设备24两者而获得聚焦图像。
175.如果聚焦靶标44位于与后照明窗口43对置的前观察口窗口上,则这些移动方向当然会反向。在这种情况下,位移距离将是前观察口(未示出)处带形样品料流32与靶标44之间的跨度。
176.位移距离52等于沿着高光学分辨率成像设备24的光轴的带形样品料流32与自动对焦靶标44之间的距离,其可在工厂校准步骤中确定或由用户确定。通常,一旦确定,位移距离52就不会变化。热膨胀变化和振动可导致高光学分辨率成像设备24和流通池22的精确位置相对于彼此改变,从而需要自动对焦过程的再引发。但对靶标44的自动对焦提供相对于流通池22固定从而相对于带形样品料流32固定的位置参照。同样,位移距离是恒定的。因此,通过对靶标44自动对焦并使高光学分辨率成像设备24和流通池22位移所述位移距离的跨度,结果是高光学分辨率成像设备聚焦于带形样品料流32。
177.根据一些实施例,聚焦靶标被提供为围绕照明开口43印刷或施加的高对比度圆
形。可选的聚焦靶标构形在本文别处讨论。当在靶标44的焦点中采集方形或矩形图像时,照明中心周围出现高对比度边界。在开口的内部边缘处搜寻获得图像中的最高对比度的位置使高光学分辨率成像设备自动对焦于靶标44的工作位置。根据一些实施例,术语“工作距离”可指物镜与其焦平面之间的距离并且术语“工作位置”可指成像设备的焦平面。图像的最高对比度量度是处于这样的位置处:最亮白色和最暗黑色测量像素沿着穿过内部边缘的一条线彼此相邻。最高对比度量度可用于评估成像设备的焦平面是否处于相对于靶标44的所需位置中。也可使用其他自动对焦技术,诸如边缘检测技术、图像分割、以及对相邻像素之间的幅度差值进行积分及寻找差值的最高总和。在一种技术中,在涵盖靶标44的任一侧上的工作位置的三个距离处计算差值总和并将所得值与特征曲线匹配,其中最佳距离位于曲线上的峰值处。相关地,示例性自动对焦技术可涉及在不同位置采集流通池靶标的图像并分析图像以使用在靶标的图像最清晰时最大的度量来找到最佳焦点位置。在第一步骤(粗调)期间,自动对焦技术可操作以从在2.5μm间隔采集的一组图像找到初步最佳位置。从该位置处自动对焦技术可随后涉及在0.5μm间隔采集第二组图像(细调)并计算靶标上的最终最佳焦点位置。
178.在一些情况下,聚焦靶标(自动对焦光栅)可位于将出现样品的视区的周边。还可能的是,聚焦靶标可由位于视野中的对比形状(如图15中所描绘)限定。通常,自动对焦靶标安装在流通池上或者牢牢附接在相对于流通池的固定位置中。在由对自动对焦靶标的图像的对比度最大化作出响应的检测器所控制的定位电机的作用下,装置自动对焦于靶标而非带形样品料流。然后通过使流通池和/或高光学分辨率成像设备相对于彼此位移所述位移距离(已知为自动对焦靶标与带形样品料流之间的距离),使高光学分辨率成像设备的工作位置或焦平面从自动对焦靶标位移到带形样品料流。因此,带形样品料流出现在采集的数字图像中的焦点中。
179.为了通过数据处理技术区分粒子类型,诸如红和白血细胞的类目和亚类目,记录具有足够分辨率和清晰度以展示将一种类目或亚类目与其他区分开的方面的微观像素图像是有利的。本发明的一个目标是方便如所述的自动对焦技术。
180.在实际的实施例中,装置可基于如图1a所示并如图1b中放大的光具座布置方式,其具有照射到安装在万向载体或流通池载体55中的流通池22上的照明源42,对由高光学分辨率成像设备24获得的图像中的流通池22的内容物进行背光照明。载体55安装在电机驱动器上以便可精确地朝向和远离高光学分辨率成像设备24移动。载体55也允许流通池相对于高光学分辨率成像设备或数字图像捕获设备的光学观察轴的精确配向,以使得带形样品料流在正交于带形样品料流成像的区中的观察轴的平面中流动,也就是在如图1中所描绘的照明开口43与观察口57之间流动。聚焦靶标44可有助于载体55的调节,例如以建立正交于高光学分辨率成像设备或数字图像捕获设备的光轴的带形样品料流的平面。
181.因此,载体55提供流通池22例如相对于图像捕获设备24或图像捕获设备物镜的位置和取向的非常精确的线性和角度调节。如此处所示,载体55包括两个枢轴点55a、55b以方便载体和流通池相对于图像捕获设备的角度调节。角度调节枢轴点55a、55b位于相同平面中并且以流通池通道(例如,在图像捕获位点)为中心。这允许在不引起流通池位置的任何线性平移的情况下调节角度。载体55可围绕枢轴点55a的轴线或围绕枢轴点55b的轴线或围绕这两条轴线旋转。此类旋转可由处理器和流通池移动控制机构控制,诸如由图4中所描绘
的处理器440和流通池控制机构442控制。
182.返回参照图1b,可以看出图像捕获设备24和载体55(连同流通池22)中的任一者或两者可沿着三维中的各条轴线(例如,x、y、z)旋转或平移。因此,用于调节图像捕获设备的焦点的示例性技术可包括实施图像捕获设备24围绕成像轴的轴向旋转,例如使设备24围绕轴线x旋转。还可通过流通池22和/或载体55围绕沿着成像轴延伸的轴线,例如围绕轴线x,并在成像设备的视野内的轴向旋转来实现焦点调节。在一些情况下,焦点调节可包括图像捕获设备的顶端旋转(例如,围绕轴线y的旋转)。在一些情况下,焦点调节可包括流通池的顶端旋转(例如,围绕轴线y或围绕枢轴点55a的旋转)。如此处所描绘,枢轴点55a对应于沿着流通池的流路并在流通池的流路内延伸的y轴。在一些情况下,焦点调节可包括图像捕获设备的倾斜旋转(例如,围绕轴线z的旋转)。在一些情况下,焦点调节可包括流通池的倾斜旋转(例如,围绕轴线z或围绕枢轴点55b的旋转)。如此处所描绘,枢轴点55b对应于横穿流路和成像轴的z轴。在一些情况下,可通过实施流通池的旋转(例如围绕轴线x)使得该旋转以图像捕获设备的视野为中心而使图像捕获设备聚焦于样品流动料流。可实施本文所述的三维旋转调节以便考虑分析仪系统的一个或多个部件中的位置漂移。在一些情况下,可实施三维旋转调节以便考虑分析仪系统的一个或多个部件中的温度波动。在一些情况下,分析仪系统的调节可包括使成像设备24沿着轴线x平移。在一些情况下,分析仪系统的调节可包括使载体55或流通池22沿着轴线x平移。
183.根据一些实施例,用于获得包含悬浮于液体中的粒子的样品的图像的视觉分析仪包括流通池22,其耦合到样品源25并耦合到pioal材料源27,如图1中所描绘。如图3的剖面图中可以看出,流通池22限定在流动方向(图3中从右到左或者图1中从底部到顶部)对称地变窄的内部流路。流通池22被配置成引导被pioal包裹的样品流32穿过流通池中的观察区,即在观察口57后面。
184.再次参照图1,具有物镜镜头46的数字高光学分辨率成像设备24沿着与带形样品料流32相交的光轴而定向。物镜46和流通池33之间的相对距离可通过电机驱动器54的操作来改变,以便在光敏元件阵列上分辨和采集聚焦的数字化图像。
185.自动对焦光栅44具有相对于流通池22固定的位置,位于离带形样品料流32的平面的位移距离52。在所示实施例中,自动对焦光栅(靶标44)在高光学分辨率成像设备24采集的图像中可见的位置直接施加到流通池22。在另一个实施例中,靶标如果未以一体化方式直接施加到流通池的主体,则可承载于相对于流通池22和其中的带形样品料流32牢牢固定在适当位置的部件上。
186.光源42可为稳定源或可为在操作高光学分辨率成像设备光敏元件时闪光的频闪灯,所述光源被配置成照明带形样品料流32并且还有助于靶标44的对比度。在所描绘的实施例中,照明来自背光照明。
187.图1c提供了框图,示出了示例性血液学分析仪的另外方面。如此处所示,分析仪100c包括耦合的至少一个数字处理器18以操作电机驱动器54并分析如在相对于靶标自动对焦光栅44的不同焦点位置处采集的来自光敏元件阵列的数字化图像。处理器18被配置成测定自动对焦光栅44的焦点位置,即自动对焦于靶标自动对焦光栅44并且从而确定高光学分辨率成像设备24与自动对焦光栅44之间的最佳距离。这可通过图像处理步骤来实现,诸如施加算法以评估第一距离处图像中的对比度水平,该算法可施加到整个图像或至少自动
对焦光栅44的边缘。处理器使电机54移动到另一个位置并评估该位置或边缘处的对比度,并且在两次或更多次迭代后测定使自动对焦光栅44上的焦点的精确度最大化(或如果已移动到该位置,则将优化焦点的精确度)的最佳距离。处理器依赖于自动对焦靶标自动对焦光栅44与带形样品料流之间的固定间距,处理器18然后控制电机54将高光学分辨率成像设备24移动到正确距离以聚焦于带形样品料流32。更具体地讲,处理器操作电机以使高光学分辨率成像设备与带形样品料流32之间的距离位移所述位移距离52(例如如图1所描绘),带形样品料流从靶标自动对焦光栅44位移所述位移距离52。这样,高光学分辨率成像设备聚焦于带形样品料流。
188.电机54可包括精度略微小于高光学分辨率成像设备或数字图像捕获设备所成像的区别性特征(特别是血细胞的各方面)的齿轮步进电机。如果调节高光学分辨率成像设备24的位置以将光学物镜的位置定位于带形样品料流的宽度内,则带形样品料流中的细胞/粒子的视图在焦点内。自动对焦光栅44可位于高光学分辨率成像设备或数字图像捕获设备的视野的边缘处,并且因此不会干扰观察。
189.此外,当高光学分辨率成像设备在位移距离内移动并且自动对焦光栅偏离焦点时,出现在焦点内的特征是血细胞而非自动对焦光栅。在图21的实施例中,例如,自动对焦光栅由视野中的形状限定。所述形状为有限尺寸的相对薄的离散形式,并且因此在移动位移距离之后,当聚焦于带形样品料流时所述形式在数字化图像中基本上不可见。在尺度适合血液学(血细胞)成像应用的流通池中,典型的位移距离可为例如50至100μm。在一些实施例中,自动对焦特征保持高光学分辨率成像设备处于最佳焦点距离的1μm内。
190.可调节流通池内部轮廓以及pioal和样品流速以使得样品形成带形料流。料流可与包裹在带形样品料流中的粒子大约一样薄或甚至更薄。白血细胞可具有例如约10μm的直径。通过提供厚度小于10μm的带形样品料流,可在带形样品料流被鞘液或pioal伸展时使细胞取向。带形样品料流沿着变窄流路在粘度与带形样品料流不同(诸如更高粘度)的pioal层内的出奇伸展有利地趋于使非球形粒子在基本上平行于流动方向的平面中配向,并对细胞施加力,从而提高细胞的细胞内结构的焦点内内容物。高光学分辨率成像设备24的光轴基本上正交(垂直)于带形样品料流的平面。带形样品料流在成像时的线速度可为例如20
‑
200mm/s。在一些实施例中,带形样品料流的线速度可为例如50
‑
150mm/s。
191.带形样品料流厚度可受样品流体和pioal的相对粘度和流速的影响。返回参照图1,样品源25和/或pioal源27(例如,包括精密排量泵)可被配置成以可控的流速提供样品和/或pioal用来优化带形样品料流32的尺度,即作为至少与高光学分辨率成像设备24的视野一样宽的薄带。
192.在一个实施例中,pioal源27被配置成以预定的粘度提供pioal。该粘度可与样品的粘度不同,并且可以高于样品的粘度。对pioal的粘度和密度、样品材料的粘度、pioal的流速和样品材料的流速进行调整以在离自动对焦光栅的位移距离处保持带形样品料流,并具有预定的尺度特性,诸如有利的带形样品料流厚度。
193.在实际的实施例中,pioal具有比样品更高的线速度和比样品更高的粘度,从而将样品伸展成平带。在一些情况下,pioal粘度可为最多至10厘泊。
194.在图1c中所示的实施例中,用于分析从光敏元件阵列获得的像素数字图像的相同数字处理器18也用于控制自动对焦电机54。然而,通常高光学分辨率成像设备24并不会对
每张捕获的图像自动对焦。自动对焦过程可周期性地(在当天开始时或在轮班开始时)或例如在适当传感器检测到温度或其他工艺变化时或在图像分析发现可能需要重聚焦时完成。在一些情况下,自动化自动对焦过程可在约10秒的持续时间内进行。在一些情况下,自动对焦工序可在处理一个齿条的样品(例如,每个齿条10个样品)之前进行。在其他实施例中还可以使血液学图像分析由一个处理器完成,并且使单独的处理器,任选地连同其自身光敏元件阵列,被布置用于处理自动对焦于固定靶标44的步骤。
195.数字处理器18可被配置成在程序化时间或在程序化条件下或根据用户需求自动对焦,并且还被配置成执行基于图像的粒子的分类和子分类。示例性粒子包括细胞、白血细胞、红血细胞等等。
196.在一个实施例中,图1或图1c的数字处理器18被配置成检测自动对焦再引发信号。自动对焦再引发信号可由检测到的温度变化、如由像素图像日期的参数所识别的聚焦质量的降低、时间的流逝或用户输入而触发。有利的是,从测量图1中所描绘的位移距离52以重新校准的意义上说,不必要重新校准。任选地,自动对焦可程序化从而在运行之间以特定频率/间隔重新校准以便进行质量控制和/或保持聚焦。
197.位移距离52在一个流通池与另一个流通池之间略有差异,但对于给定流通池而言保持恒定。作为拟合图像分析仪与流通池时的安装过程,首先估计位移距离,然后在其中执行自动对焦和成像方面的校准步骤期间,测定流通池的准确位移距离并作为常数输入处理器18的程序设计中。
198.因此,如图1d中的流程图所示,并且参照图1和/或图1c的血液学分析仪,根据所公开的方法和装置进行的过程可涉及校准一次或很少校准。校准可包括聚焦于对比度靶标44、聚焦于带形样品料流32以及记录沿着光轴在这两个位置之间的位移,如步骤110d中所指示。该位移可作为常数记录。然后通过控制电机54并分析来自光敏元件阵列的图像数据,处理器18自动对焦于靶标44并且使高光学分辨率成像设备24和/或流通池22相对于彼此位移所记录的位移距离,如步骤120d中所指示。带形样品料流32进而在焦点内并且可每隔一定间隔,特别是在足以采集在观察口57处穿过观察区的带形样品料流的部分的基本上不重叠的相邻视图的间隔处,采集(如步骤130d中指示)和处理(如步骤140d中指示)其图像。当自行监测(如步骤150d中指示)揭示数据异常或温度变化(可能因热膨胀的差异而改变高光学分辨率成像设备24与流通池22的相对位置)时,则引发自动对焦(如步骤160d中指示),此后恢复常规操作。因此,自动对焦过程可包括检测自动对焦再引发信号,以及响应于自动对焦再引发信号而重复自动对焦和图像采集步骤。在一些实施例中,自动对焦再引发信号可包括或基于温度的变化、聚焦质量的降低、流逝的时间间隔、或用户输入。
199.带形样品料流的线速度可被充分限制以防止在光敏元件阵列的图像曝光时间时数字化图像出现运动模糊。光源可任选地为频闪灯,该频闪灯闪光而在短暂时间内施加高入射振幅。由于自动对焦光栅44和图像处于相同视野,光源被配置成同时照明带形样品料流和自动对焦光栅。然而,在其他实施例中,用于成像和用于自动对焦的视野可不同,例如单独地照明和/或成像。
200.所讨论的开发具有方法以及装置方面。使视觉分析仪聚焦的方法包括使高光学分辨率成像设备24聚焦在相对于流通池22固定的自动对焦光栅44上,所述高光学分辨率成像设备24可为数字高光学分辨率成像设备或数字图像捕获设备,其中自动对焦光栅44位于离
带形样品料流32的位移距离52。数字高光学分辨率成像设备24具有物镜,其光轴与带形样品料流32相交。物镜与流通池22之间的相对距离通过操作电机驱动器54而改变,而沿着光轴的在高光学分辨率成像设备与最佳焦点之间的距离是已知的。数字高光学分辨率成像设备被配置成分辨和采集光敏元件阵列上的数字化图像。在自动对焦过程中操作电机驱动器以聚焦于自动对焦光栅上。然后在位移距离内操作电机驱动器,从而使高光学分辨率成像设备聚焦于带形样品料流上。
201.可以使用对靶标的自动对焦和位移所述位移距离来获得适于对带形样品料流聚焦的距离。然而,有利的是,每次图像捕获不需要或不重复自动对焦。然而,在某些条件下开始自动对焦。可检测或生成自动对焦再引发信号,从而引起如下步骤:重聚焦于自动对焦光栅,在位移距离内操作电机驱动器,以及使高光学分辨率成像设备重聚焦于带形样品料流。自动对焦再引发信号可由例如温度的变化、聚焦质量的降低、时间的流逝、其他工艺参数或用户输入的检测而引起。
202.图1e为示例性模块系统的简化框图,该框图广义地例示了可如何以分离方式或更集成化的方式实施模块系统100e的个体系统元件。模块系统100e可以是根据本发明实施例的用于使血样流体中的粒子成像的粒子分析系统的一部分或与该粒子分析系统相连。模块系统100e非常适于生成与聚焦和成像技术相关的数据或指令、接收与聚焦和成像技术相关的输入、和/或处理与聚焦和成像技术相关的信息或数据,如本文别处所述。在一些情况下,模块系统100e包括经由总线子系统102e电耦合的硬件元件,包括一个或多个处理器104e、一个或多个输入设备106e(诸如用户界面输入设备)、和/或一个或多个输出设备108e(诸如用户界面输出设备)。在一些情况下,系统100e包括网络接口110e和/或成像系统接口140e,该成像系统接口可从成像系统142e接收信号以及/或者将信号传送到成像系统142e。在一些情况下,系统100e包括软件元件,所述软件元件例如在此处被显示为当前正位于存储器114e的工作存储器112e内,为操作系统116e和/或其他代码118e(诸如被配置为实施本文所公开技术的一个或多个方面的程序)。
203.在一些实施例中,模块系统100e可以包括存储子系统120e,该存储子系统可以存储提供本文所公开的各种技术的功能的基础编程和数据构造。例如,实现如本文所述方法各方面的功能的软件模块可以存储于存储子系统120e中。这些软件模块可由一个或多个处理器104e执行。在分布式环境中,所述软件模块可存储在多个计算机系统上并由所述多个计算机系统的处理器执行。存储子系统120e可以包括存储器子系统122e和文件存储子系统128e。存储器子系统122e可包括多个存储器,包括用于在程序执行期间存储指令和数据的主随机存取存储器(ram)126e,以及其中存储固定指令的只读存储器(rom)124e。文件存储子系统128e可为程序和数据文件提供永久性(非易失性)存储,并且可以包括有形存储介质,该有形存储介质可以任选地收录样品、患者、治疗、评估数据,或其他数据。文件存储子系统128e可以包括硬盘驱动器、连同相关联的可移动介质的软盘驱动器、紧凑型数字只读存储器(cd
‑
rom)驱动器、光盘驱动器、dvd、cd
‑
r、cd rw、固态可移动存储器、其他可移动的介质盒或盘,等等。所述驱动器中的一个或多个可位于在其他位点处耦合到模块系统100e的其他连接计算机上的远程位置处。在一些情况下,系统可以包括存储一个或多个指令序列的计算机可读存储介质或其他有形存储介质,所述一个或多个指令序列在被一个或多个处理器执行时,可导致所述一个或多个处理器执行本文所公开的技术或方法的任何方面。
实现本文所公开技术的功能的一个或多个模块可由文件存储子系统128e存储。在一些实施例中,所述软件或代码将提供允许模块系统100e与通信网络130e进行通信的协议。任选地,此类通信可以包括拨号连接通信或互联网连接通信。
204.应当理解,系统100e可被配置成实施本发明方法的各方面。例如,处理器部件或模块104e可以是微处理器控制模块,该微处理器控制模块被配置成从传感器输入设备或模块132e、从用户界面输入设备或模块106e、和/或从成像系统142e,任选地经由成像系统接口140e和/或网络接口110e以及通信网络130e接收温度参数信号和/或流通池操作参数。在一些情况下,传感器输入设备可包括粒子分析系统或为粒子分析系统的一部分,所述粒子分析系统被装配为获得血液流体样品的图像。在一些情况下,用户界面输入设备106e和/或网络接口110e可被配置成接收由粒子分析系统生成的图像参数信号,所述粒子分析系统被装配为获得图像参数。在一些情况下,成像系统142e可包括粒子分析系统或为粒子分析系统的一部分,所述粒子分析系统被装配为获得与血液流体样品相关的图像参数。
205.处理器部件或模块104e还可以被配置成将任选地根据本文所公开技术的任何一种处理的粒子分析参数信号或图像参数信号传送到传感器输出设备或模块136e、到用户界面输出设备或模块108e、到网络接口设备或模块110e、到成像系统接口140e、或到它们的任何组合。根据本发明实施例的设备或模块中的每一个可以包括位于被处理器处理的计算机可读介质上的一个或多个软件模块,或硬件模块,或它们的任何组合。可使用多种常用平台(诸如windows、macintosh和unix)中的任何一种,连同多种常用编程语言中的任何一种,来实现本发明的实施例。
206.用户界面输入设备106e可以包括(例如)触摸板、键盘、指示设备(诸如鼠标)、轨迹球、图形输入板、扫描器、操纵杆、结合到显示器中的触摸屏、音频输入设备(诸如语音识别系统)、麦克风、以及其他类型的输入设备。用户输入设备106e还可以从有形存储介质或从通信网络130e下载计算机可执行代码,该代码具体化为本文所公开方法或其各方面中的任何一者。应当理解,终端软件可以时常更新,并且在适当的情况下被下载到终端。一般来讲,使用术语“输入设备”旨在包括用于将信息输入模块系统100e中的多种传统和专属的设备和方法。
207.用户界面输出设备106e可以包括(例如)显示子系统、打印机、传真机、或非视觉显示器(诸如音频输出设备)。显示子系统可以是阴极射线管(crt)、平板设备(诸如液晶显示器(lcd))、投影设备等等。显示子系统还可以诸如经由音频输出设备提供非视觉显示。一般来讲,使用术语“输出设备”旨在包括用于从模块系统600向用户输出信息的多种传统和专属的设备和方法。
208.总线子系统102e提供用于使模块系统100e的各种部件和子系统彼此按预期的方式或根据需要进行通信的机制。模块系统100e的各种子系统和部件无需处于相同的物理位置,而是可以分布在分布式网络内的各个位置处。尽管总线子系统102e被示意性地显示为单根总线,但是总线子系统的另选实施例可以利用多根总线。
209.网络接口110e可提供通向外部网络130e或其他设备的接口。外部通信网络130e可被配置成根据需要或期望实现与其他方的通信。该外部通信网络由此可以接收来自模块系统100e的电子数据包,并且根据需要或期望将任何信息传输回模块系统100e。如此处所描绘,通信网络130e和/或成像系统接口142e可向成像系统142e传输信息或接收来自成像系
统142e的信息,该成像系统被装配为获得对应于血液流体样品的多个图像或图像参数。
210.除了提供系统内部的此类基础结构通信链接之外,通信网络系统130e还可以为诸如互联网之类的其他网络提供连接,并且可以包括有线、无线、调制、和/或其他类型的接口连接。
211.对技术人员显而易见的是,可以根据具体要求来使用大量的变型。例如,也可以使用定制的硬件并且/或者可以在硬件、软件(包括便携式软件,诸如小应用程序)或这两者中实现特定的元件。此外,可以采用至其他计算设备(诸如网络输入/输出设备)的连接。模块终端系统100e本身可以是包括计算机终端、个人计算机、便携式计算机、工作站、网络计算机、或任何其他数据处理系统的不同类型的模块终端系统。由于计算机和网络的不断变化的性质,因此图1e中描绘的模块系统100e的描述仅旨在作为出于举例说明本发明的一个或多个实施例的目的的具体例子。模块系统100e的比图1e中所描绘的模块系统具有更多或更少部件的许多其他配置是可能的。模块系统100e的模块或部件中的任何一个或此类模块或部件的任何组合可以与本文所公开的粒子分析和/或成像系统实施例中的任何一个耦合、或集成到其中、或以其他方式被配置成与其建立连接。相关地,以上论述的硬件和软件部件中的任何一个可以与在其他位置处使用的其他医疗评估或治疗系统集成在一起或被配置成与所述系统接合。
212.在一些实施例中,模块系统100e可以被配置成接收输入模块处的血液流体样品的一种或多种图像参数。可将图像参数数据传输到评估模块,在评估模块处,可基于图像数据的分析来预测或确定诊断或其他结果。图像或诊断数据可以经由输出模块输出至系统用户。在一些情况下,模块系统100e可例如通过使用诊断模块来确定血液流体样品的诊断结果。诊断信息可以经由输出模块输出至系统用户。任选地,该诊断的某些方面可以由输出设备确定,并且传输至诊断系统或诊断系统的子设备。可将与血液流体样品或从其获得样品的患者相关的多个数据中的任何一个输入到模块系统中,包括年龄、体重、性别、治疗史、病史,等等。可以基于这种数据来确定治疗方案或诊断评价的参数。
213.相关地,在某些情况下,系统包括被配置成接收图像数据作为输入的处理器。任选地,处理器、存储介质或这两者可以结合在血液学或粒子分析机器内。在一些情况下,血液学机器可以生成用于输入到处理器中的图像数据或其他信息。在一些情况下,处理器、存储介质或这两者可以结合在计算机内,并且该计算机可以与血液学机器进行通信。在一些情况下,处理器、存储介质或这两者可以结合在计算机内,并且该计算机可以经由网络与血液学机器进行远程通信。
214.流通池
215.流通池22的实际实施例进一步在图2和3中描绘。如此处所示,流通池22可与样品源25耦合并且还耦合到pioal材料的源27。经由插管29,例如通过插管29的远侧出口31,将样品流体注射到流通池22中。通常,pioal鞘液从源27朝观察区23行进通过流通池中的弯曲通道区段41时,其不处于层流状态。然而,流通池22可被配置成使得pioal鞘液在流过样品流体被引入流动鞘液中的远侧出口31时,pioal鞘液为层流式或变为层流式,或呈现平坦速度剖面。样品流体和pioal可在总体上由箭头a指示的方向上沿着流通池22流动,然后经由排放口33流出流通池22。流通池22限定在流动方向a上对称地变窄(例如,在过渡区21)的内部流路20。流路的对称性有助于样品料流的稳固且居中的流动。流通池22被配置成将被
pioal包裹的样品的流动32导向通过流通池中的观察区23,即观察口57之后。与观察口57相连的是自动对焦光栅44。流通池22还具有圆形或凹陷底座58,其被配置成接受或接收显微镜物镜(未示出)。
216.根据一些实施例,自动对焦光栅44可具有相对于流通池22固定并且位于离带形样品料流32的平面一定位移距离的位置。在此处所示的实施例中,在通过高光学分辨率成像设备(未示出)穿过观察口57采集的图像中可见的位置处,将自动对焦光栅(靶标44)直接应用于流通池22。流通池22可由单件材料构造。或者,流通池22可由第一或上区段或层22a和第二或下区段或层22b构造。如此处所示,玻璃或透明窗格60附接到第一区段22a或与第一区段22a一体化。窗格60可限定流通池内的样品流路的至少一部分。来自光源42的光可行进通过自动对焦光栅44的孔或通路以照明在流动料流32内流动的样品粒子。
217.在一些情况下,窗格60的厚度可具有约150μm至约170μm范围内的值。如上指出的,窗格60可限定或形成流路或鞘液(例如,pioal)通道的一部分。通过使用薄窗格60,可以将显微镜物镜放置在非常靠近样品流体带的位置,因此获得沿着流路流动的粒子的高度放大图像。
218.图3a描绘了流通池实施例的各方面,其中成像轴355与远侧过渡区部分316之间的距离为约8.24mm。远侧过渡区部分316与插管出口331之间的距离为约12.54mm。插管出口331与鞘液入口301之间的距离为约12.7mm。插管出口331与近侧过渡区部分318之间的距离为约0.73mm。图3b描绘了流通池实施例的各方面,其中插管出口已被移动到相对于过渡区更远侧的位置,如相比于图3a实施例。如此处所示,插管远端被推进到流通池的变窄过渡区中,并且成像轴355与远侧过渡区部分316之间的距离在约16mm至约26mm的范围内。在某种情况下,成像轴355与远侧过渡区部分316之间的距离为约21mm。
219.返回参照图1,流通池内部轮廓(例如,在过渡区21)以及pioal和样品流速可被调整成使得样品形成为带形料流32。料流可与包裹在带形样品料流中的粒子大约一样薄或甚至更薄。白血细胞可具有例如约10μm的直径。通过提供厚度小于10μm的带形样品料流,可在带形样品料流被鞘液或pioal伸展时使细胞取向。带形样品料流沿着变窄流路在与带形样品料流不同的粘度诸如更高粘度的pioal层内的出奇伸展,有利地趋于使非球形粒子配向在基本上平行于流动方向的平面中,并对细胞施加力,从而提高了细胞的细胞内结构的焦点内内容物。高光学分辨率成像设备24的光轴基本上正交(垂直)于带形样品料流的平面。带形样品料流在成像时的线速度可为例如20
‑
200mm/s。在一些实施例中,带形样品料流的线速度可为例如50
‑
150mm/s。
220.带形样品料流厚度可受样品流体和pioal的相对粘度和流速的影响。样品源25和/或pioal源27(例如,包括精密排量泵)可被配置成以可控的流速提供样品和/或pioal以优化带形样品料流32的尺度,即作为至少与高光学分辨率成像设备24的视野一样宽的薄带。
221.在一个实施例中,pioal源27被配置成以预定的粘度提供pioal。该粘度可与样品的粘度不同,并且可以高于样品的粘度。对pioal的粘度和密度、样品材料的粘度、pioal的流速和样品材料的流速进行调整以在离自动对焦光栅的位移距离处保持带形样品料流,并具有预定的尺度特性,诸如有利的带形样品料流厚度。
222.在实际实施例中,pioal具有比样品更高的线速度和比样品更高的粘度,从而将样品伸展成平带。pioal粘度可最多至10厘泊。
223.还参照图2和3,流通池的内部流路在带形样品料流向pioal中注射的点的下游变窄,以产生带形样品料流厚度,例如最多至7μm,和/或内部流路产生500
‑
3,000μm的带形样品料流宽度。在示例性实施例中,如图1中所描绘,流通池的内部流路在样品料流向pioal中注射的点的上游开始出现变窄过渡区。
224.在另一个实施例中,内部流路变窄以产生厚度为2
‑
4μm的带形样品料流厚度,和/或内部流路产生宽度为2000μm的带形样品料流。这些尺度特别适用于血液学。在这种情况下料流的厚度小于一些粒子诸如处于其松弛状态的红血细胞的直径。因此,这些粒子可被重新取向以将其较宽的尺度面向成像轴,这有助于展现有区别的特性。
225.带形样品料流的线速度可被充分限制以防止在光敏元件阵列的图像曝光时间时数字化图像出现运动模糊。光源可任选地为频闪灯,该频闪灯闪光而在短暂时间内施加高入射振幅。由于自动对焦光栅44和图像处于相同视野,光源被配置成同时照明带形样品料流和自动对焦光栅。然而,在其他实施例中,用于成像和用于自动对焦的视野可不同,例如单独地照明和/或成像。
226.所讨论的开发具有方法以及装置方面。使视觉分析仪聚焦的方法包括使高光学分辨率成像设备24聚焦在相对于流通池22固定的自动对焦光栅44上,所述高光学分辨率成像设备24可为数字高光学分辨率成像设备或数字图像捕获设备,其中自动对焦光栅44位于离带形样品料流32的位移距离52。数字高光学分辨率成像设备24具有物镜,其光轴与带形样品料流32相交。物镜与流通池22之间的相对距离通过操作电机驱动器54而改变,而沿着光轴的在高光学分辨率成像设备与最佳焦点之间的距离是已知的。数字高光学分辨率成像设备被配置成分辨和采集光敏元件阵列上的数字化图像。在自动对焦过程中操作电机驱动器以聚焦于自动对焦光栅上。然后在位移距离内操作电机驱动器,从而使高光学分辨率成像设备聚焦于带形样品料流上。
227.该方法还可包括使带形样品料流形成为带形。呈现带形使得高光学分辨率成像设备的光轴基本上垂直于带形样品料流,即正交于带形料流的平面。
228.图4描绘了用于使血液流体样品中的粒子成像的系统400的各方面。如此处所示,系统400包括样品流体注射系统410、流通池420和图像捕获设备430、以及处理器440。流通池420提供流路422,该流路传递鞘液流,任选地结合样品流体一起传递。根据一些实施例,样品流体注射系统410可包括插管或管412或与插管或管412耦合。样品流体注射系统410可与流路422(例如,经由样品流体入口402)流体连通并且可操作以将样品流体424注射通过插管412的远侧出口413并进入流通池420内的流动鞘液426以便提供样品流体料流428。例如,处理器440可包括存储介质或与存储介质操作性地相连,所述存储介质具有计算机应用程序,所述计算机应用程序被配置成在被处理器执行时导致样品流体注射系统410将样品流体424注射到流动鞘液426中。如此处所示,鞘液426可通过鞘液注射系统450(例如,经由鞘液入口401)引入流通池420中例如,处理器440可包括存储介质或与存储介质操作性地相连,所述存储介质具有计算机应用程序,所述计算机应用程序被配置成在被处理器执行时导致鞘液注射系统450将鞘液426注射到流通池420中。如图4中所描绘,插管412的远侧出口413可定位在沿着变窄过渡区419的长度的中心位置。在一些情况下,远侧出口可定位在更靠近过渡区419的开始处(近侧部分)。在一些情况下,远侧出口可定位在更靠近过渡区419的末端处(远侧部分)。在一些情况下,远侧出口413可完全定位在过渡区419之外,例如如图
3a中所描绘(其中远侧出口331设置在变窄过渡区的近侧)。
229.样品流体料流428具有邻近注射管412的第一厚度t1。流通池的流路422具有流路尺寸的缩减段使得样品流体料流428的厚度从初始厚度t1降低到邻近图像捕获位点432的第二厚度t2。图像捕获设备430与图像捕获位点432配向以便在流通池420的图像捕获位点432处使来自第一样品流体的第一多个粒子成像。
230.处理器440与样品流体注射器系统410、图像捕获设备430和任选的鞘液注射系统450耦合。处理器440被配置成终止向流动鞘液426中注射第一样品流体并开始向流动鞘液426中注射第二样品流体使得样品流体瞬变被引发。例如,处理器440可包括存储介质或与存储介质操作性地相连,所述存储介质具有计算机应用程序,所述计算机应用程序被配置成在被处理器执行时导致样品流体注射系统410将第二样品流体注射到流动鞘液426中使得样品流体瞬变被引发。
231.此外,处理器440被配置成在样品流体瞬变后和在使第一多个粒子成像的4秒内,引发在流通池420的图像捕获位点432处捕获来自第二样品流体的第二多个粒子的图像。例如,处理器440可包括存储介质或与存储介质操作性地相连,所述存储介质具有计算机应用程序,所述计算机应用程序被配置成在被处理器执行时导致图像捕获设备430在样品流体瞬变后和在使第一多个粒子成像的四秒内,引发在流通池420的图像捕获位点432处捕获来自第二样品流体的第二多个粒子的图像。
232.在一些实施例中,处理器440可包括存储介质或与存储介质操作性地相连,所述存储介质具有计算机应用程序,所述计算机应用程序被配置成在被处理器执行时导致流通池移动控制机构442调节流通池420例如相对于图像捕获设备430的位置。在一些实施例中,处理器440可包括存储介质或与存储介质操作性地相连,所述存储介质具有计算机应用程序,所述计算机应用程序被配置成在被处理器执行时导致图像捕获设备移动控制机构444调节图像捕获设备430例如相对于流通池420的位置。移动控制机构442、444可包括分别促进和产生流通池和图像捕获设备中的移动的电机、万向接头以及其他机械特征。在一些情况下,流通池控制机构442和/或图像捕获设备控制机构444可包括高精度步进电机控制器,其提供图像捕获设备相对于流通池的机动化和自动化聚焦。如图1中所描绘,处理器可控制图像捕获设备24的移动。相似地,如图1b中所描绘,处理器可控制流通池载体55的移动。
233.因此,本发明的实施例涵盖执行组合式粘度和几何流体聚焦以便使血液流体样品中的粒子成像的粒子分析系统。示例性系统可包括具有带有注射管的流路以及具有带有从中穿过的成像轴的成像窗口的流通池。流通池的流路可具有流路尺寸的缩减段。此外,分析仪系统可包括与流路流体连通的鞘液输入口以及与注射管流体连通的血液流体输入口。血液流体输入口可被配置用于将血液流体样品注射到流通池内的流动鞘液中以使得血液流体样品以流动料流宽度大于流动料流厚度的样品流动料流流动。鞘液可具有大于血液流体样品的粘度的粘度。而且,分析仪系统可包括图像捕获设备和聚焦机构,所述聚焦机构设定图像捕获设备相对于流通池的焦点状态。此外,系统可包括具有相对于流通池固定的位置的成像靶标,其中成像靶标和样品流动料流限定沿着成像轴的位移距离。系统还可包括处理器和聚焦模块,所述聚焦模块具有体现机器可读代码的有形介质,所述机器可读代码在处理器上执行以便操作聚焦机构使用位移距离设定适于粒子表征和计数的图像捕获设备的焦点状态。鞘液与血液流体样品之间的粘度差连同流路尺寸的缩减段可有效地在成像轴
处流体聚焦第一和第二样品流体,同时保持血液流体样品中的细胞的活力。在一些情况下,聚焦机构可包括被配置成调节图像捕获设备与流通池之间的距离的驱动电机。
234.在一些情况下,分析仪系统400可包括与流通池420热耦合的温度或热传感器448,如图4中所描绘。聚焦模块可与处理器操作性地相连,可包括收录机器可读代码的有形介质,所述机器可读代码在处理器上执行以便操作聚焦机构(例如,流通池控制机构442或图像捕获设备控制机构444),从而响应于温度传感器所感测到的温度变化和温度与所需焦点之间的已知关系,而设定适于粒子表征和计数的图像捕获设备的焦点状态或焦平面。
235.因此,本发明的实施例涵盖用于使具有样品流体粘度的血液流体样品424中的多个粒子成像的系统400。系统400可与鞘液426一起使用,该鞘液具有与样品流体粘度相差一个处于预定粘度差范围内的粘度差的鞘液粘度。系统400可包括具有流路422的流通池420和样品流体注射管412。流路422可具有流路尺寸的缩减段或变窄过渡区。此外,系统400可包括与流通池420的流路422流体连通的鞘液输入口401,以便沿着流通池420的流路422传递鞘液流。系统400还可以包括与流通池420的注射管412流体连通的血液流体样品输入口402,以便将血液流体样品的流或料流428注射到流通池420内的流动鞘液428中。例如,样品流体424可离开插管412的远侧出口423并进入流动鞘液426的包层中以在其中形成样品带428。
236.当鞘液426与样品流体424所形成的样品流体带428一起穿过流路尺寸的缩减段419流向成像位点432时,与粘度差相关的鞘液426和样品流体424之间的相互作用所引起的粘度流体聚焦作用连同与流路尺寸的缩减段相关的鞘液426和样品流体424之间的相互作用所引起的几何流体聚焦作用在成像位点432在多个粒子的至少一些中提供靶标成像状态。如这里所示,系统400还包括在成像位点432对多个粒子成像的成像设备430。
237.如图4a中所描绘的流通池实施例中所示,流路尺寸的缩减段(例如,在过渡区419a)可由流路422a的相对壁421a、423a限定。相对壁421a、423a可沿着流路422a径向地向内成角度,总体上关于横向平面451a对称,所述横向平面平分样品流体料流428a。平面451a可平分样品料流428a,其中在样品料流428a离开插管或样品注射管412a的远侧部分427a的位置处,样品料流具有第一厚度t1。相似地,平面451a可平分样品料流428a,其中在样品料流428a通过图像捕获位点432a的位置处,样品料流具有第二厚度t2。根据一些实施例,第一厚度t1具有约150μm的值并且第二厚度t2具有约2μm的值。在此类情况下,样品带料流的压缩比为75:1。根据一些实施例,第一厚度t1具有约50μm至约250μm范围内的值并且第二厚度t2具有约2μm至约10μm范围内的值。当样品料流流体流过流通池时,随着其加速和伸展,带变薄。流通池的两个特征可有助于样品流体带的变薄。第一,鞘液包层与样品流体带之间的速度差可起到降低带的厚度的作用。第二,过渡区的渐缩几何形状可起到降低带的厚度的作用。如图4a中所描绘,插管412a的远侧出口413a可定位在沿着变窄过渡区419a的长度的中心位置。在一些情况下,远侧出口可定位在更靠近过渡区419a的开始处(近侧部分415a)。在一些情况下,远侧出口可定位在更靠近过渡区419a的末端处(远侧部分416a)。在一些情况下,远侧出口413a可完全定位在过渡区419a之外,例如如图3a中所描绘(其中远侧出口331设置在变窄过渡区的近侧)。
238.如图4a(以及图4和4b
‑
1中)所描绘,过渡区419a可由近侧(415a)和远侧(416a)部分处的成角过渡段限定。还应当理解,过渡区419a可相反在近侧(415a)和远侧(416a)部分
处呈现平滑或弯曲过渡段,类似于如图1、3、3a、3b和4b
‑
2中所描绘的平滑或弯曲过渡段。
239.通常,第一厚度t1远大于样品粒子的尺寸,因此粒子完全包含于样品带料流内。然而,第二厚度t2可小于某些样品粒子的尺寸,因此这些粒子可延伸出样品流体并进入周围的鞘液。如图4a中所示,样品带料流可总体上沿着与其离开插管并朝图像捕获位点行进的相同平面流动。
240.流通池还可以在远侧插管部分427a与图像捕获位点432a之间提供间隔距离430a。根据一些实施例,样品流体注射管412a的远侧部分427a可定位在离图像捕获位点432a的轴向间隔距离430a处,其中轴向间隔距离432a具有约21mm的值。在一些情况下,轴向间隔距离430a具有约16mm至约26mm范围内的值。
241.插管出口与图像捕获位点之间的轴向间隔距离430a可影响样品流体从出口向图像捕获位点行进时流体的过渡时间。例如,相对更短的轴向间隔距离430a可有助于更短的过渡时间,而相对更长的轴向间隔距离430a可有助于更长的过渡时间。
242.插管远侧部分427a处的出口相对于流路过渡区419a或相对于流路过渡区419a的近侧部分415a的位置也可推断出样品流体从出口向图像捕获位点行进时流体的过渡时间。例如,鞘液可在近侧部分415a具有相对更慢的速度,而在近侧部分415a与远侧部分416a之间的位置具有相对更快的速度。因此,如果将远侧部分427a处的插管出口定位在近侧部分415a,则样品流体到达图像捕获位点将花费更长的时间,这不仅因为行进距离更长,还因为样品流体的初始速度在其离开插管远侧端口后更慢(由于鞘液速度更慢)。换句话说,样品流体存在于流通池的较厚部分(例如,靠近近侧部分415a)的时间越长,则样品到达图像捕获位点所花的时间越长。反之,如果将远侧部分427a的插管出口定位在近侧部分415a的远侧(例如,在近侧部分415a与远侧部分416a之间的中心位置,如图4a中所描绘),则样品流体到达图像捕获位点所花的时间将更短,这不仅是因为行进距离更短,还因为样品流体在离开插管远侧端口后的初始速度更快(由于更快的鞘液速度)。如本文别处所讨论,鞘液在穿过过渡区419a流动时因区419a的变窄横截面积而被加速。
243.根据一些实施例,过渡时间越短,图像捕获位点处采集图像可用的时间越多。例如,当从插管远侧顶端到成像区域的过渡持续时间缩短时,可以在特定的时长内处理更多的样品,并相关地可以在特定的时长内获得更多的图像(例如,每分钟的图像数)。
244.虽然存在与将插管远侧部分427a的出口定位在更靠近图像捕获位点432a的位置相关的优点,但在所述出口与捕获位点之间保持一定的距离也是可取的。例如,如图3中所描绘,成像设备的光学物镜或前透镜可定位在流通池22的底座58中。如果插管的出口31太靠近底座58,则样品流体在被注射到鞘液中后可能不够稳定,而不能在图像捕获位点提供所需的成像性质。相似地,可能有利的是在离观察区23一定的距离处保持渐缩过渡区21,以使得渐缩区不干扰接收图像捕获设备物镜的底座58的定位。
245.继续参照图4a,样品流体注射管412a的下游端427a可定位在流路过渡区419a的近侧部分415a的远侧。相关地,样品流体注射管412a的下游端427a可定位在流路过渡区419a的远侧部分416a的近侧。因此,根据一些实施例,样品流体可从注射插管412a在过渡区419a内的某一位置注射到流通池中。
246.根据一些实施例,流路尺寸的缩减段的对称性(例如,在流路过渡区419a)起到限制血液流体样品中的粒子失准的作用。例如,这种对称性可有效将血液流体样品中的红血
细胞成像取向失准限制到小于约20%。
247.根据一些实施例,本文所公开的方法可起到使血细胞计数分析期间的标记率低于样品的30%、29%、28%、27%、26%、25%、24%、23%、22%、21%、20%、19%、18%、17%、16%、15%、14%、13%、12%、11%、10%、9%、8%、7%、6%或5%的作用。
248.根据一些实施例,图像捕获位点432a具有约150μm
×
150μm与400μm
×
400μm之间的视野433a。在一些情况下,图像捕获位点432a具有约275μm
×
275μm的视野433a。在一些情况下,视野可根据长度乘以宽度加以限定。如果表示为表面积,则275μm
×
275μm视野具有75,625μm2的面积。根据一些实施例,视野可由成像设备物镜及其放大倍数确定。在一些情况下,视野可对应于由采集光学元件(例如,物镜、镜筒透镜和相机)成像的场(区域)范围。在一些情况下,视野远小于图像捕获位点处的透明区的观察口。
249.图4a
‑
1和图4a
‑
2示出了当样品料流从插管出口向图像捕获位点行进时流体聚焦对样品料流的影响。如图4a
‑
1中所示,样品料流可具有约150μm的高度h(s)和约1350μm的宽度w(s)。另外,pioal鞘液料流可具有约6000μm的高度h(p)和约4000μm的宽度w(p)。在流体聚焦之后,如图4a
‑
2中所示,样品料流可具有约2μm的高度h(s)和约1350μm的宽度w(s)。另外,pioal鞘液料流可具有约150μm的高度h(p)和约4000μm的宽度w(p)。在一个实施例中,pioal鞘液料流在插管出口处的横截面积是图像捕获位点附近的横截面积的40倍。
250.根据一些实施例,其可用于确定图像捕获位点处的流通池通道的横截面。这可对应于如图4a
‑
2中所描绘的约150μm的pioal鞘液料流高度h(p)和约4000μm的宽度w(p)。其还可用于确定在图像捕获位点处流过流通池的合并样品和鞘液的体积流速。当已知横截面积和流速时,可以确定图像捕获位点处的合并样品和鞘液的速度。
251.根据一些实施例,样品和鞘液穿过流通池的流动可用平行板轮廓模型估算。相关地,样品流体料流的中心的流速(例如,如图4a
‑
2中所描绘)可为合并样品和鞘液料流的平均流速的约1.5倍。
252.根据一些实施例,在插管出口处的样品流的横截面积(例如,图4a
‑
1中的w(s)
×
h(s))为成像位点处的样品流的横截面积(例如,图4a
‑
2中的w(s)
×
h(s))的40倍。在成像区域处的鞘液的体积流速可为约45μl/s。在成像区域处的样品流体的体积流速可为约0.232μl/s。在一些情况下,在成像位点处的合并的鞘液和样品料流的横截面积为600,000μm2。在一些情况下,在成像位点处的平均流动料流速度为75mm/s。
253.流速或速度可作为产生清晰和聚焦的细胞图像的速率而确定。示例性流速和速度基于据观察在成像位点实现一定样品流动料流带形或特性的两个样品的流速而发现。例如,在约75mm/s(或20
‑
200mm/s范围内)的流速下,细胞不会流动得过慢以使得在连续图像中存在细胞的重叠,并且细胞也不会流动得过快以使得形成幻影效应(模糊的图像)。相关地,通过避免过高的流速,可以节省更多的试剂和样品。根据一些实施例,最佳的或所需的线速度可通过改变体积流量(泵速)或插管形状而实现。
254.穿过图像捕获区的样品料流的流动速度也可与图像捕获设备相对于流通池功能的性能相关。例如,如果样品料流流动得过快,则可能难以获得样品中所含的粒子的清晰图像(例如,图像捕获设备的快门速度可能过慢,从而产生模糊的图像)。相似地,如果样品料流流动得过慢,则图像捕获设备可能获得同一粒子的连续图像(例如,同一粒子在两次图像捕获过程中保持在捕获帧中)。在一些实施例中,样品带的速度可相对于图像捕获速率进行
调节(例如,通过调整多个流通池操作参数中的任何一个),以使得在帧捕获之间存在最少的流动,并因此对高百分比的样品成像。
255.根据一些实施例,粒子分析系统和相关部件可被配置成使得当鞘液和流体样品流过流通池时,鞘液可以45μl/s的鞘液体积速度流动,而流体样品可以0.232μl/s(或在0.2至0.35μl/s的范围内)的流体样品体积流速流动。在一些情况下,鞘液流速与样品流体流速的比率为约200。在一些情况下,鞘液流速与样品流体流速的比率具有约70至200范围内的值。在一些情况下,鞘液流速与样品流体流速的比率为约193。在一些情况下,鞘液流速与样品流体流速的比率为约70。在一些情况下,在流通池内流动的鞘液体积与流体样品体积的比率可在25:1至250:1的范围内。
256.根据一些实施例,所述系统和相关部件可被配置成使得当鞘液和流体样品流过流通池420时,鞘液可以75mm/s的鞘液速度在成像区域前流动,而流体样品可以130mm/s的流体样品速度在成像区域前流动。在一些情况下,在流通池内流动的鞘液体积与流体样品体积的比率可在100:1至200:1的范围内。
257.在一些情况下,流通池可具有约50:1的最小压缩比和约125:1的最大压缩比。在一些情况下,最小压缩比可为约30:1或20:1。该压缩比是指当将图4a
‑
1与图4a
‑
2相比时的流动料流厚度h(s):h(s)的比率。该压缩比可受几何压缩(例如,当将图4a
‑
1与图4a
‑
2比较时,鞘液厚度h(p):h(p)的比率,其也可总体上对应于图4a中所示的流通池变窄渐缩过渡区419a的尺度)和流体动力压缩(例如,也对应于速度差)的组合的影响。根据一些实施例,几何压缩比为约40:1。
258.对应于过渡区的流路尺寸的缩减段可由近侧流路部分和远侧流路部分限定,近侧流路部分具有近侧厚度或高度,而远侧流路部分具有比近侧厚度或高度小的远侧厚度或高度。例如,如图4b
‑
1和4b
‑
2的局部视图所示,流路的过渡区419b可在近侧部分415b与远侧部分416b之间具有长度l,其中近侧部分415b具有近侧高度417b,而远侧部分416b具有远侧高度418b。如图4b
‑
2中所描绘,并如本文别处所述,过渡区的形状或轮廓可以为弯曲的或平滑的,并例如可以s形曲线、蛇形曲线或正切曲线的形状提供。根据一些实施例,近侧高度417b具有约6000μm的值。在一些情况下,近侧高度417b具有约3000μm至约8000μm范围内的值。根据一些实施例,远侧高度418b具有约150μm的值。在一些情况下,远侧高度418b具有约50μm至约400μm范围内的值。
259.过渡区419a的几何形状可提供在第一流路边界403b与平分横向平面451b之间的第一角度α1,和在第二流路边界404b与平分横向平面451b之间的第二角度α2。在一些情况下,角度α1为约45度而角度α2为约45度。在一些情况下,角度α1具有约10度至约60度范围内的值。在一些情况下,角度α2具有约10度至约60度范围内的值。根据一些实施例,角度α1和α2具有相同的值。可对角度α1和α2进行选择以便在样品流体从近侧部分415b向远侧部分416b行进时保持样品流体的层流或最大程度降低样品流体的湍流,继而可增强样品内的粒子沿着横向平面451b的配向。如上文参照图4a所述,过渡区的远侧和近侧边界或部分可以为弯曲的或平滑的,而不是成角度的。
260.图4c描绘了根据本发明实施例的示例性插管或样品进料管400c的特征,其中插管具有长度l。图4d描绘了插管400d的纵向横截面。如此处所示,插管400d包括远侧平坦区段410d、中心渐缩区段420d和近侧管状部分430d。如图4c
‑
1中所描绘,示例性插管或样品进料
管400c
‑
1可具有远侧部分410c
‑
1和近侧部分430c
‑
1。在一些情况下,远侧部分410c
‑
1具有约1.359mm的长度和约1.43mm的宽度。在一些情况下,远端的出口具有约1.359mm的出口宽度w(e)。根据一些实施例,插管可具有与图4c和4d中所描绘的不同的内部流路几何形状。例如,如图4d
‑
1中所示,插管400d
‑
1不包括具有扩展流动区横截面的渐缩中心区段。如图4d
‑
1中所描绘,插管400d
‑
1具有远侧区段410d
‑
1、内径渐缩的中心渐缩区段420d
‑
1以及近侧区段430d
‑
1。对应于中心区段420d
‑
1的渐缩内径,410d
‑
1的内部横截面积小于430d
‑
1的内部横截面积。
261.根据本发明实施例的血液学系统可处理体积为约150μl的血样。抽出的血液体积可为约120
‑
150μl。在一些情况下,样品管中的最低可用血液体积对于自动采样模式为约500μl,而对于人工采样模式为约250μl。图4d中所示的插管或注射管400d具有约13μl的内部体积。根据一些实施例,插管或注射管具有小于约30μl的内部体积。
262.图4e示出了远侧平坦区段410e的横截面。如此处所示,远侧区段410e具有内部宽度w(i)和内部高度h(i),样品料流从中流动。此外,远侧区段410e具有外部宽度w(o)和外部高度h(o)。如图4d和4e合在一起所描绘,样品流体注射管的远侧部分410e具有出口p,其具有高度h(i)和宽度w(i),其中高度h(i)小于宽度w(i)。根据一些实施例,远侧部分410e的出口p的高度h(i)(或远侧部分410d的内部高度)可具有约150μm的值。在一些情况下,高度h(i)可在约50μm至约250μm的范围内。根据一些实施例,远侧部分410e的出口p的宽度w(i)(或远侧部分410d的内部宽度)可具有约1350μm的值。在一些情况下,宽度为约1194μm。在一些情况下,宽度w(i)可具有约500μm至约3000μm范围内的值。在一些情况下,远侧平坦区段410d可通过向管或导管施加夹持力而制成。
263.图4f示出了中心渐缩区段420f的横截面。如此处所示,中心渐缩区段420f具有内径d(i),样品料流从中流动。另外,中心渐缩区段420f具有外径d(o)。图4g示出了近侧区段430g的横截面。如此处所示,近侧区段430g具有内径d(i),样品料流从中流动。此外,远侧区段430g具有外径d(o)。
264.如图4d中所描绘,注射管或插管400d可具有近侧部分430d、远侧部分410d和设置在近侧部分430d与远侧部分410d之间的第三部分420d,近侧部分具有第一流动横截面积(例如,图4g中所示的π*(d/2)2),远侧部分具有比第一流动横截面积小的第二流动横截面积(例如,图4e中所示的w(i)*h(i))。第三部分420d可具有大于第一和第二流动横截面积的第三流动横截面积(例如,图4f中所示的π*(d/2)2)。在一些情况下,近侧部分430g的外径d(o)为约1067μm,而近侧部分430g的内径d(i)为约813μm。
265.根据一些实施例,注射管的近侧部分可与样品入口配件的样品口耦合。例如,如图4h中所示,插管400h的近侧部分405h可在样品入口配件420h的出口处直接耦合到样品口410h。
266.用于使血液流体样品中的粒子成像的系统的流通池可以相对于重力方向的任何所需角度或方向取向。例如,流通池可在向上方向上取向,以使得流通池内流动的流体(例如,鞘液,任选地与样品流体相结合)可克服重力在向上方向上行进。同样,流通池可在向下方向上取向,以使得流通池内流动的流体(例如,鞘液,任选地与样品流体相结合)可在重力作用下在向下方向上行进。图4i描绘了在向上方向上取向的流通池420i,以使得流通池420i内流动的样品流体424i和鞘液426i克服重力g流动。图4j描绘了在向下方向上取向的
流通池420j,以使得流通池420j内流动的样品流体424j和鞘液426j不是克服重力g流动,而是在重力g作用下流动。
267.如图4k中所示,穿过流通池420k的图像捕获位点432k流动的样品料流带r可具有约2μm的厚度t。在一些情况下,样品料流带r的厚度t可最多为约3μm。通常,小于样品料流厚度的细胞或粒子将被包含在带内。示例性红血细胞(rbc)可呈现为双面凹陷的圆盘并可具有约6.2μm与约8.2μm之间的直径d。此外,示例性红血细胞可具有约2μm与约2.5μm之间的最大厚度t1和约0.8μm与约1μm之间的最小厚度t2。在一些情况下,红血细胞可具有最多至约3μm的厚度。示例性人血小板的尺寸可以变化,并也可具有约2μm的厚度或直径。虽然此处未按比例示出,但是流通池可在图像捕获位点处限定值为约150μm的流路厚度f。在一些情况下,流路厚度f具有50μm与400μm之间的值。该流路厚度f还可对应于图4b
‑
1和图4b
‑
2中所描绘的远侧部分461b的远侧高度418b。
268.如图4k中所示,样品流体料流的厚度t与粒子(红血细胞)的厚度的比率为约1:1。根据一些实施例,在图像捕获位点处的样品流体料流的厚度t与粒子之一的尺寸的比率在0.25至25的范围内。在一些情况下,厚度t可具有0.5μm至5μm范围内的值。可对鞘液与样品流体之间的粘度差进行选择以便实现带状样品料流在流通池内的所需定位。
269.样品带r的流体与鞘液之间的粘度差可起到沿着流动方向配向样品料流中的粒子(例如红血细胞)或使其取向的作用。当如此配向时,如图4k中所示,成像设备或相机可获取红血细胞的图像使得它们看起来为圆的,因为该血细胞的主表面面向相机。这样,红血细胞呈现的配向展示出相对于流动的低阻力。因此,鞘液和样品流体的相对粘度特性可有助于高百分比或数量的红血细胞面向相机,从而增强粒子分析系统的评估能力。
270.根据一些实施例,鞘液的粘度特性起到限制血液流体样品中的粒子失准的作用。例如,粘度差可有效地将血液流体样品中的红血细胞成像取向失准限制到小于约10%。也就是说,样品中的100个红血细胞中的90个或更多个红血细胞可配向以使得其主表面面向成像设备。对称的变窄过渡区可提供20%的值。如本文别处所述,例如参照图4r,可以将从涉及具有对称变窄流通池过渡区的流通池的分析仪构形获得的配向结果与从涉及具有对称变窄流通池过渡区的流通池而不使用粘性鞘液的分析仪构形获得的配向结果进行比较。使用粘性鞘液可降低失准细胞的百分比。根据一些实施例,鞘液具有类似于水的折射率(即n=1.3330)。在一些情况下,鞘液具有约89%的水含量。除了因粘度差而观察到的配向作用外,还因双侧渐缩过渡区观察到了配向作用。在一些情况下,据观察,双侧(即,对称)渐缩过渡区在配向粒子方面的有效性是不对称渐缩过渡区设计的两倍。
271.红血细胞的有效配向可有助于改善诊断。在一些情况下,可将成像的红血细胞的形状用于确定从其获取样品的患者是否具有特定的生理病症或疾病。例如,具有镰状细胞病的患者展示出形状异常(即,镰刀形状)的血细胞。因此,通过获得配向红血细胞的高质量图像,可以确保准确的诊断。红血细胞的其他形状变化,例如具有薄周边区域和大平坦中心区域的红血细胞(因此红血细胞看起来具有自行车轮胎轮廓),可用本发明的配向技术有效地成像。相似地,可出于诊断目的对具有小中心部分和厚周边区域的红血细胞(因此红血细胞看起来具有卡车轮胎轮廓)成像。本文所公开的改进的成像技术还可用于评估其他红血细胞特性,诸如血红蛋白含量、铁含量等等。
272.不受任何特定理论的束缚,据信,鞘液的粘度与样品流体的粘度之间的粘度差产
生改变的抛物线剖面,其中该剖面总体上为抛物线的,并具有对应于加速度增大的流动中心区域的中心隆起,并且该中心隆起有助于样品粒子或粒子内细胞器的配向。根据一些实施例,鞘液与样品带之间的速度差和粘度差生成剪切力以增加细胞器或细胞内粒子的配向。鞘液抛物线剖面的示例性方面在共同待审的美国专利申请no.________中有所讨论,该专利申请的内容以引用方式并入本文。
273.白血细胞通常大于红血细胞和血小板。例如,示例性中性粒细胞和嗜酸性粒细胞可具有约10μm与约12μm之间的直径。示例性嗜碱性粒细胞可具有约12μm与约15μm之间的直径。示例性淋巴细胞(小)可具有约7μm与约8μm之间的直径,而示例性淋巴细胞(大)可具有约12μm与约15μm之间的直径。示例性单核细胞可具有约12μm与约20μm之间的直径。粒子分析系统的构形(包括鞘液和流体样品带在穿过流通池时它们之间的相互作用)可在白血细胞穿过图像捕获位点432l行进时起到压缩白血细胞的作用,如图4l中所指示。因此,例如,白血细胞(wbc)的中心部分可定位于样品流体带r内,而白血细胞的周边部分可定位于鞘液内。因此,当白血细胞通过样品带而穿过流通池传输时,白血细胞的侧面可延伸到鞘液中。如上文关于图4k所讨论的样品料流带r的厚度t和流路的厚度f的数值或范围相似地适用于图4l。
274.根据一些实施例,鞘液与样品流体之间的粘度差可起到配向存在于诸如白血细胞的细胞内的细胞器或其他细胞内特征的作用。不受任何特定理论的束缚,据信,与鞘液和样品流体之间的粘度差相关的剪切力可作用于白血细胞而配向细胞内特征。在一些情况下,与鞘液和样品流体之间的速度差相关的剪切力可有助于这种配向。这些配向作用可受粒子之间的尺寸差异以及样品流体带的影响。例如,如果粒子的部分延伸到样品流体带之外并进入周围的鞘液中,则与粘度差相关的剪切力可对细胞内特征配向具有明显的影响。
275.如图4l中所描绘,细胞(诸如白血细胞)的部分可延伸到鞘液中。本发明的实施例涵盖鞘液组合物,该鞘液组合物在将细胞暴露于鞘液时不裂解或破碎细胞或者说是影响外部细胞膜的完整性。该鞘液中的粘度剂可起到保持样品流体料流中的细胞的活力的作用,从而在细胞膜或细胞壁横穿样品流体带与鞘液包层之间的界面时或者说是从样品流体料流延伸到流动鞘液中时使细胞的结构(例如,形状)和内容物(例如,细胞核)保持完整。
276.通常,当细胞或粒子沿着流通池在样品流体带内流动时存在作用于细胞或粒子的压缩力。因此,当细胞因变窄过渡区而处于压缩状态或者说是经受压缩力时细胞可与鞘液接触。鞘液的粘度剂至少在细胞到达图像捕获位点之前,可保护被压缩的细胞在从薄样品流体带出现并变为暴露于粘性鞘液时免遭破碎或毁坏。因此,鞘液的粘度剂组合物可起到细胞保护剂的作用,同时还增强粒子或粒子内内容物的配向。
277.参照图4k和图4l,在一些情况下,细胞或粒子的部分可延伸到薄样品流体带r之外并进入周围的鞘液中。如在共同待审的美国专利申请no.____中所讨论,鞘液可包含抑制或防止鞘液破坏或裂解细胞或粒子的细胞保护剂。例如,鞘液可包含当将细胞暴露于鞘液的化学环境时保持细胞壁的结构完整性的细胞保护剂。相似地,细胞保护剂也可在细胞经历由流通池几何形状和样品流体与鞘液之间的速度和/或粘度差所引起的任何剪切力时起到保持细胞壁的结构完整性的作用。相关地,保护剂可使细胞或粒子免受样品流体与鞘液之间的速度差所引起的力的影响。这样,细胞在到达图像捕获位点时保持其活力。
278.剪切力在样品流体带与鞘液包层之间的界面处可能是显著的。根据一些实施例,
流通池流路内的流动可由抛物线流动剖面表征。图4l
‑
1描绘了抛物线流动剖面400l
‑
1a和400l
‑
1b的示例性方面。上图中的抛物线剖面400l
‑
1a是存在于本发明的某些流通池实施例内的流动中的典型速度剖面(例如,其中在被包裹在鞘液流动料流内的样品流体流动料流之间存在很小的粘度差或不存在粘度差)。可以看出,在流体料流的中间观察到了最高的线速度,并在流通池壁附近观察到了较慢的线速度。剖面400l
‑
1a也可在鞘液与样品流体之间具有轻微粘度差的流体料流中观察到。在鞘液与流体料流之间存在高粘度差的情况下,观察到了如剖面400l
‑
1b中所示的中心隆起,其中存在具有放大的线速度的局部中心区域。根据一些实施例,尺寸足够大的粒子将经受一定量的剪切力,甚至在此类粒子被完全包含在单一流体相内时(即,在鞘液包层内或者在样品流体带内)。
279.在一些情况下,鞘液的速度可与样品流体的速度不同。例如,鞘液可以80mm/s行进而样品流体可以60mm/s行进。因此,在一些情况下,样品流体以慢于周围包层的鞘液速度的样品流体速度离开远侧插管端口。因此,鞘液可起到沿着插管的流路拖动样品流体的作用,从而加速样品流体并降低样品流体带的厚度。样品流体带保持总体体积和质量不变,因此当其行进得越快时变得越薄。根据一些实施例,鞘液和样品流体在图像捕获位点处具有约20与200mm/s之间的速度。
280.通常,当样品流体从插管出口向图像捕获位点行进时,样品流体的速度增加。在一些情况下,在图像捕获位点处样品流体的速度是样品流体离开插管远侧部分的插管端口时的速度的40倍。根据一些实施例,样品带的横截面积的减小与速度的增加呈线性关系。根据一些实施例,如果在插管出口处的鞘液速度高于样品带速度,则这也将增大成像区域处的最终样品带速度。
281.鞘液可起到对样品流体带和样品流体带内的粒子施加显著的剪切力的作用。一些力平行于流动方向,而粒子也可能遇到垂直于流动方向的力。通常,当鞘液和样品流体接近图像捕获位点或区时,鞘液和样品流体以相同的速度或接近相同的速度行进。因此,当鞘液和样品流体通过图像捕获位点时在其之间的边界或界面可呈现出与远侧插管出口处或渐缩过渡区处的边界或界面相比更低的剪切力。例如,在渐缩过渡区处,鞘液包层与样品流体带之间的边界或界面可处于过渡中,以使得最初较慢较厚的样品带变得更快更薄,并且样品流体中的粒子变得更配向。换句话说,剪切力在渐缩过渡区可能是突出的,并可向图像捕获位点耗散。在图像捕获位点处的剪切力可由抛物线剖面表示,并可远低于渐缩过渡区处的剪切力。因此,细胞或粒子可在通过过渡区时经受更高的剪切力,并在通过图像捕获位点时经受更低的剪切力。根据一些实施例,鞘液与样品流体之间的粘度差可使红血细胞配向并因而聚焦。根据一些实施例,鞘液与样品流体之间的粘度差可使白血细胞配向并因而聚焦。相关地,可得到因料流的几何变窄和鞘液与样品流体之间的速度差而配向并聚焦的细胞和细胞器组分的增强的成像结果。
282.如本文别处所述,并参照图4k和4l,当鞘液和样品流体r流过流通池的流路尺寸缩减段或过渡区并流向成像位点432k或432l时,与鞘液粘度和样品流体粘度之间的粘度差相关的鞘液和样品流体r之间的相互作用所引起的粘度流体聚焦作用连同与流路尺寸缩减段或过渡区相关的鞘液和样品流体r之间的相互作用所引起的几何流体聚焦作用在成像位点432k或432l处在多个粒子的至少一些中提供靶标成像状态。
283.在一些情况下,靶标成像状态是相对于成像位点处的焦平面f的靶标取向。例如,
如图4k
‑
1中所描绘,粒子(rbc)可从焦平面f位移一定的距离。在一些情况下,靶标取向涉及相对于成像位点432k
‑
1的焦平面f的靶标粒子取向。粒子可以是血细胞,诸如红血细胞、白血细胞或血小板。如这里所示,成像位点432k
‑
1处的流路可限定基本上与焦平面f平行或共平面的p平面。在一些情况下,粒子的一部分可沿着焦平面f定位,而粒子的中心部分则可从焦平面f偏移。在一些情况下,靶标取向涉及相对于成像位点432k
‑
1的焦平面f的靶标位置。例如,靶标位置可涉及对粒子进行定位以使得粒子的至少一部分沿着焦平面f设置。在一些情况下,靶标位置可涉及对粒子进行定位以使得粒子与焦平面f之间的距离不超过某一阈值。在一些情况下,靶标位置涉及相对于成像位点432k
‑
1的焦平面f的靶标粒子位置。在一些情况下,靶标位置与焦平面f相隔距离d或不到距离d,其中距离d对应于位置公差。可对鞘液与样品流体之间的粘度差进行选择以便在流通池内实现带状样品料流的所需定位(例如,相对于流路平面p和/或焦平面f)。在一些情况下,可对粘度差进行选择以便实现处于位置公差d或不到位置公差d的靶标粒子位置。
284.在一些情况下,焦平面f具有如图4k
‑
2中所指示的视野厚度或深度,而粒子(rbc)具有相对于焦平面厚度的靶标成像状态。例如,粒子的靶标位置可在焦平面f内或至少部分地在焦平面f内。在一些情况下,高光学分辨率成像设备或相机可具有约7μm的视野深度或焦平面厚度。在一些情况下,视野深度或焦平面厚度具有约2μm至约10μm范围内的值。在一些情况下,相机的视野深度类似于或等于图像捕获位点处的样品带厚度。
285.在一些情况下,靶标取向可涉及相对于成像位点处的焦平面f的靶标配向。例如,靶标配向可指示由粒子限定的平面与焦平面f配向,不超过如图4k
‑
3所示的相对于图像捕获位点432k
‑
3的焦平面f的特定角度α。在一些情况下,靶标成像状态可涉及对样品中的未配向粒子的数量或百分比的限制。例如,鞘液与样品流体r之间的粘度差可将血液流体样品中的红血细胞成像取向未配向有效限制到低于约10%。也就是说,样品中的100个红血细胞中的90个或更多个红血细胞可配向以使得其主表面面向成像设备(如图4k
‑
1和4k
‑
2中所描绘)或使得那90个或更多个rbc的配向在基本上平行于流动方向的平面的20度内(例如,rbc配向角度α为20度或更小)。如本文其他地方所讨论,在一些情况下,至少92%的非球形粒子(诸如rbc)可在基本上平行于流动方向的平面中配向。在一些情况下,至少75%与95%之间的非球形粒子(诸如rbc)可基本上配向,即,在基本上平行于流动方向的平面的20度内(例如,配向角度α为20度或更小)。根据一些实施例,90%或更多的某些粒子(例如,红血细胞和/或血小板)可横向于成像设备的成像轴取向。
286.在一些情况下,本发明的实施例包括与如本文所述的血液学系统一起使用的组合物,诸如鞘液或粒子和细胞内细胞器配向液(pioal)。此类鞘液或pioal适用于组合式粘度和几何流体聚焦视觉分析仪。pioal可起到引导或促进给定粘度的血样流体流过视觉分析仪的变窄流通池过渡区的作用。pioal可包含粘度比样品的粘度更高的流体。与粘度差相关的pioal流体和样品流体之间的相互作用所引起的粘度流体聚焦作用连同与变窄流通池过渡区相关的pioal流体和样品流体之间的相互作用所引起的几何流体聚焦作用可有效地在视觉分析仪的成像位点在多个粒子的至少一些中提供靶标成像状态,同时维持血样流体中的细胞的活力。
287.图4m描绘了具有内部细胞器(诸如裂片410m)的示例性中性粒细胞400m(一种类型的白血细胞)。因样品流体与鞘液之间的粘度差,内部细胞器可在细胞内配向,如图4n所指
示。因此,细胞内细胞器可通过图像捕获设备430m有效地成像,而细胞器不彼此重叠。也就是说,不同于如图4m中所描绘的裂片彼此堆叠,当从图像捕获设备的成像轴或光轴观察时,裂片配向和并排,如图4n中所描绘。因此,可在捕获的图像中更有效地看见裂片。内部细胞器配向是样品流体与鞘液之间的粘度差的出奇且意外的结果。因此,使用粘度差、流体动力流和几何压缩特征实现了对应于细胞配向和处于焦点内的增强的成像结果。
288.如本文别处所述,并参照图4m和4n,当鞘液和样品流体r流过流通池的流路尺寸缩减段或过渡区并流向图像捕获设备430m或430n的成像位点时,与鞘液粘度和样品流体粘度之间的粘度差相关的鞘液和样品流体r之间的相互作用所引起的粘度流体聚焦作用连同与流路尺寸缩减段或过渡区相关的鞘液和样品流体r之间的相互作用所引起的几何流体聚焦作用在成像位点处在多个粒子的至少一些中提供靶标成像状态。根据一些实施例,靶标成像状态可对应于成像状态的分布。
289.在一些情况下,靶标成像状态可涉及相对于成像位点处的焦平面的靶标粒子内结构取向(例如,配向和/或位置)。例如,如图4n中所描绘,内部结构410m(例如,细胞内结构、细胞器、裂片等)可相对于焦平面f取向。在一些情况下,靶标配向涉及相对于成像位点处的焦平面f的靶标粒子内结构配向,类似于图4k
‑
3中所描绘的粒子配向关系。在一些情况下,靶标位置涉及相对于成像位点处的焦平面的靶标粒子内结构位置,类似于图4k
‑
1中所描绘的粒子位置关系。在一些情况下,粒子内结构的靶标取向既可包括相对于焦平面的靶标配向也可包括相对于焦平面的靶标位置。在一些情况下,靶标成像状态可涉及成像位点处的靶标变形。例如,如图4n中所描绘,粒子400m具有与图4m中所描绘的粒子形状相比压缩的形状。因此,可以看出的是,流通池的运行可对粒子形状产生侧向压缩作用。相关地,粒子内特征可在粒子本身的形状被压缩时在位置或方向上取向(例如,相对于焦平面f和/或带状流平面配向)。根据一些实施例,鞘液与样品流体之间的速度差可在流动料流内产生摩擦,而鞘液与样品流体之间的粘度差可放大该流体动力摩擦。
290.实例
291.可使用流过流通池的样品流体的图像执行多种血液学或血液粒子分析技术中的任一种。通常,图像分析可涉及确定某些细胞或粒子参数,或测量、检测或评价某些细胞或粒子特征。例如,图像分析可涉及评价细胞或粒子尺寸、细胞核特征、细胞质特征、细胞内细胞器特征等等。相关地,分析技术可涵盖某些计数或分类方法或诊断测试,包括白血细胞(wbc)分类。在一些情况下,使用流通池得到的图像可支持5分法wbc分类测试。在一些情况下,使用流通池得到的图像可支持9分法wbc分类测试。相关地,参照图4,处理器440可包括存储介质或与存储介质操作性地相连,所述存储介质具有计算机应用程序,所述计算机应用程序被配置成在被处理器执行时导致系统400基于得自图像捕获设备的图像区分不同类型的细胞。例如,诊断或测试技术可用于区分各种细胞(例如,中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞、嗜碱性粒细胞、晚幼粒细胞、中幼粒细胞、早幼粒细胞和母细胞)。
292.本文提供的实例仅用于举例说明的目的,并且本发明不限于这些实例,而是涵盖因本文所提供的教导而显而易见的所有变型形式。
293.在本文所述的实验之前,还没有公开的方案允许包括如本文所公开的用于配向粒子和重定位细胞内内容物的pioal的开发和使用方法。这可用于体液(例如,血液)样品中的粒子的基于图像的分析和分类及子分类。本文所公开的方法和组合物可任选地以适于实现
白细胞染色、网织红细胞染色和血小板染色的方式对粒子染色和/或使粒子裂解,类似于在全血涂片上所见的瑞氏染液染色细胞。
294.本文所述的示例性组合物允许在相对低的血液与试剂稀释度下发生染色,并且染色可快速地发生(例如,在30秒内)。如果需要,示例性方法可采用表面活性剂并加热来实现红细胞裂解。可对示例性制剂进行修改以保持rbc完整性,并仍实现wbc、网织红细胞和血小板染色功效。
295.本发明的多个方面和实施例基于以下出奇且意外的发现:某些pioal组合物在用于执行基于图像的粒子/细胞分析时具有意外的配向细胞和重定位细胞内结构的性质。
296.以举例的方式,开发了若干示例性pioal制剂及其使用方法。以下是具有所需性质的pioal制剂的一些示例。
297.图4o显示了使用pioal得到的图像与使用非pioal鞘液得到的图像的比较。使用pioal产生了更多的焦点内细胞内容物,诸如裂片、细胞质和/或颗粒。在该实例中,将包含粘度剂(约30%甘油)的pioal用于处理样品。将ph调节到约6.8至7.2的ph,并通过0.9%氯化钠使样品混合物为等渗的。此处所示的结果证实了用在图像分析仪上的示例性pioal配向细胞和细胞内细胞器的功效。
298.图4p和4q示出了使用标准鞘液得到的图像(图p上图和下图)与使用示例性pioal流体得到的图像(图4q上图和下图)的比较。如这里所示,使用pioal导致了改善的rbc配向,例如通过使红血细胞的主表面取向从而面向相机或成像设备。使用仪器聚焦方案(对如图1中所描绘的示例性靶标44)分析样品,并通过视觉分析仪使靶标聚焦。然后使聚焦系统偏移位移距离52,从而使带形样品料流中的粒子处于焦点内。血样已用样品稀释剂进行了稀释。样品流过插管并沿着流通池的流路流动,从而产生在两层pioal或标准鞘液(在对照中)之间的带形样品料流(例如,2微米厚)。视觉分析仪然后生成将用于分析的带形样品料流中的粒子的聚焦图像(例如,以每秒约60帧)。血样得自受试者并进行处理以通过血液分析仪进行分析。在使用标准鞘液或pioal处理样品的同时,捕获流通池中rbc的图像。基于成像数据(例如,4p和4q),相对百分比展示了配向rbc的数量的显著提高。结果证实了:使用如本文所述的聚焦仪器/方案,pioal有效地增加了带形样品料流中处于流动中的rbc的配向百分比。
299.另据观察,基于在对称和不对称流通池中使用浓度渐增的甘油(gly),pioal的具体实施导致了改善的配向。
300.图4r中的图表显示了对称与不对称流通池相比时在pioal中使用0%
‑
30%甘油得到的未配向细胞的百分比。在pioal中使用30%甘油并使用对称流通池使失准细胞的百分比降低到仅8%。注意,在pioal中没有甘油并使用不对称池时,失准细胞的百分比增至87%。因此,该图表证实了甘油百分比和流通池几何形状对粒子(例如,rbc)配向的作用。在使用对称或不对称流通池几何形状时,添加甘油降低了失准rbc细胞的百分比。未配向rbc的百分比在不对称池中从87%降至15%,在对称池中从46%降至8%。因此,该图表提供了以下两种失准结果的比较:得自涉及具有对称变窄流通池过渡区的流通池和粘性鞘液的分析仪构形的失准结果(8%),和得自涉及具有对称变窄流通池过渡区的流通池而不使用粘性鞘液的分析仪构形的失准结果(46%)。
301.这些结果为以下出奇且意外的发现提供了证据:某些pioal组合物在用于执行基于图像的粒子/细胞分析时具有意外的配向细胞和重定位细胞内结构的性质。
302.以举例的方式,开发了若干示例性pioal制剂及其使用方法。以下是具有所需性质的pioal制剂的一些示例。pioal包含稀释剂和至少一种粘度改性剂。
303.示例性pioal制剂a包含具有300ml甘油的30%(v/v)甘油溶液,并用稀释剂适量定量到1l(足够的或使最终体积定容至1l的量),所述稀释剂包含9.84g硫酸钠、4.07g氯化钠、0.11g盐酸普鲁卡因、0.68g磷酸二氢钾、0.71g磷酸氢二钠和1.86g乙二胺四乙酸二钠。然后将初始混合物用去离子水适量定量到1l,同时用氢氧化钠将ph调至7.2。
304.示例性pioal制剂b包含具有65ml甘油的6.5%(v/v)甘油溶液,并用合适的示例性稀释剂适量定量到1l,所述稀释剂包含9.84g硫酸钠、4.07g氯化钠、0.11g盐酸普鲁卡因、0.68g磷酸二氢钾、0.71g磷酸氢二钠和1.86g乙二胺四乙酸二钠。然后将初始混合物用去离子水适量定量到1l,同时用氢氧化钠将ph调至7.2。
305.示例性pioal制剂c包含在缓冲液中具有1%pvp(w/v)的5%甘油(v/v)溶液,其具有50ml甘油、10g pvp(分子量:360,000)、1包sigma pbs粉末,ph为7.4(0.01m磷酸盐缓冲盐水;0.138m氯化钠;0.0027m氯化钾),并用去离子水适量定量到1l。
306.示例性pioal制剂d包含1.6%pvp(w/v)溶液,其具有16g pvp(分子量:360,000)和1包sigma pbs粉末,ph为7.4(0.01m磷酸盐缓冲盐水;0.138m氯化钠;0.0027m氯化钾),并用去离子水适量定量到1l。
307.通量
308.图5描绘了与流通池中一种或多种样品流体的注射相对应的时间表500。如此处所示,可引发第一样品流体向流通池中的注射,如步骤510所指示。随后,可在流通池中使来自第一样品流体的粒子成像,如步骤515所指示。根据一些实施例,第一样品流体可具有约5μl至约150μl范围内的体积。在一些情况下,在成像区域处的流速为0.232μl/s(或在0.2μl/s至0.35μl/s的范围内)。对于20秒的成像,流量值可在5μl至15μl的范围内。可终止第一样品流体的注射,如步骤520所指示,并且可引发第二样品流体向流通池中的注射,如步骤530所指示。由于第一样品流体注射的终止和第二样品流体注射的引发,可引发样品流体瞬变,如步骤535所指示。随后,流通池中的样品流体瞬变可耗散,如步骤445所指示。可在流通池中使来自第二样品流体的粒子成像,如步骤550所指示。可终止第二样品流体的注射,如步骤560所指示。在一些情况下,在约18℃至约40℃范围内的温度下执行注射和流动程序。
309.通常,在注射样品时并且在终止注射时,鞘液的料流保持流动于流通池内。因此,根据一些实施例,在样品流体脉冲式注射到流动鞘液的同时保持鞘液的连续流。当样品流体沿着流通池流动时,鞘液的连续流可有助于保持样品流体中的带形。
310.根据一些实施例,可在与步骤515相关的图像捕获的四秒内执行与步骤550相关的图像捕获。根据一些实施例,第一与第二样品流体注射之间(例如,步骤510与530之间)的时间为约30秒。相关地,根据一些实施例,第一与第二样品流体的成像的引发之间(例如,步骤515的引发与步骤550的引发之间)的时间为约30秒。这样,可以每小时处理120个样品流体。在一些情况下,图像捕获设备以180帧/秒(fps)的帧速率操作,从而以高频率或高速率产生多个独特的连续图像或帧。如此处所示,成像步骤(例如515或550)的持续时间可为15秒,从而每个样品流体产生2,700张图像。
311.在一些情况下,在将第一样品流体从样品流体注射管注射到流动鞘液中(例如,步骤510)后约1至3秒内,第一样品流体达到稳定状态。在一些情况下,在将第一样品流体从样
品流体注射管注射到流动鞘液中(例如,步骤510)后小于1秒内,第一样品流体达到稳定状态。样品向流通池中的注射可为两步过程。根据该实施例,第一步为将所有稀释剂从插管清除的高速推进,并且在初始推进后,样品的流速显著下降。过渡时间可被定义为样品(例如细胞)在成像流动条件(较慢样品流速)下从插管出口行进到成像区域花费的时间。在一些情况下,在将第一样品流体从样品流体注射管注射到流动鞘液中(例如,步骤510)后约1.8秒内,第一样品流体达到稳定状态。在一些情况下,样品流体具有约2至4秒范围内流过流通池(例如,从插管出口到图像捕获位点)的通过时间。
312.根据一些实施例,流体稳定或从插管的远侧出口行进到成像区域要花费约5秒。在一些情况下,图像捕获持续时间段可为约20秒。
313.根据本发明实施例的血液学系统可处理体积为约150μl的血样。抽出的血液体积可为约120
‑
150μl。在一些情况下,样品管中的最低可用血液体积对于自动采样模式为约500μl,而对于人工采样模式为约250μl。图4d中所示的插管或注射管400d具有约13μl的内部体积。根据一些实施例,插管或注射管具有小于约30μl的内部体积。在开始图像采集之前血样的体积能有效地注满插管,因此可避免延长的样品流不稳定的时间段。例如,具有约13μl的内部体积的插管的使用可对应于约2至3秒的样品流不稳定时间段。根据一些实施例,插管内部体积可能不会影响样品流稳定性。根据一些实施例,如果初始高速样品推进不足以置换插管内的所有稀释剂,插管内部体积可能会影响样品带自身中的细胞浓度稳定性。相关地,可使用少量稀释剂在短时长内在样品之间清洗插管。这样,可以实现有利于捕获高质量图像的稳定样品流,并且同时实现高通量,且具有低残留。根据一些实施例,具有高内部体积的插管可需要样品的高体积初始高速推进以清除管线和插管中的所有稀释剂。本发明的实施例涵盖较低内部插管体积的具体实施,所述较低内部插管体积适用于这样的血液学应用,其中可用样品体积较低,并且其中可在较短时长内完成较低体积推进。
314.根据一些实施例,血液学系统可被配置成限制瞬变和顺序样品的交叉污染从而加速从血液流体样品的图像采集。
315.细胞结构、内容物和配向
316.根据一些实施例,为实现白血细胞的染色和可视化,裂解样品中的红血细胞并渗透白血细胞以便允许染剂掺入白血细胞内是有帮助的。通常希望在细胞形态很少改变或不改变的情况下获得白血细胞的染色。另外,通常希望获得类似于瑞氏染液的染色性质。此外,通常希望获得高红细胞配向(例如,靶标>90%)。
317.图5a示出了使用不含戊二醛的染液制剂得到的结果。据观察,细胞因流通池中遇到的剪切力而破碎。虽然实现了细胞核的良好染色,但细胞核本身看起来发生了变形,并且细胞膜看起来发生了损坏。总之,当成像时,细胞看起来因细胞内容物和结构的破坏而毁坏。
318.图5b示出了使用含有戊二醛的染液制剂得到的wbc结果。如这里所示,细胞膜是完整的,且细胞为圆的。因此,据观察,未使用戊二醛的染液的版本(例如,图5a中所示)导致了弱化的wbc。虽然wbc比图5b更完整,但细胞核部分受到损坏。
319.用于获得图5b图像的鞘液(pioal)包含30%甘油。相比之下,用于获得图5c图像的鞘液(pioal)包含6.5%甘油。较低浓度的甘油产生了更好的形态,其中细胞核大部分无变化。因此,据观察,图5c中的细胞膜甚至比图5b中的细胞膜更完整。图5c中的较低甘油浓度
可起到降低粘度差的作用,从而减小剪切力。如果存在过大的剪切力,则该力可破坏细胞膜。甘油可具有某些与细胞不相容的性质,因此较高的甘油浓度也可破坏细胞膜。因此,可以得出结论:图5a中所描绘的细胞核损坏可能是鞘液中30%甘油的结果。
320.然而,当甘油浓度降低到如图5c中所描绘的6.5%时,观察到样品流体中红血细胞配向的减弱。
321.尝试了将各种替代pioal制剂用于获得改善的红血细胞配向,但是这些替代制剂并未提供令人满意的结果。例如,尝试了若干不同的粘度增强剂,但其中许多表现出与较高的30%甘油制剂相似的行为,以致于细胞内容物受到损坏。
322.据观察,通过使用聚乙烯吡咯烷酮(pvp)和5%甘油作为粘度剂组分,有可能在不产生破坏细胞核的负面作用的情况下得到粘度与30%甘油制剂的粘度相匹配的鞘液(并因此实现改善的配向结果)。图5d描绘了使用具有5%甘油和1%pvp的pioal得到的结果。因此,可以看出,鞘液中的粘度剂保持了样品流体料流中细胞的活力,从而使细胞的结构和内容物完整,例如,当细胞流过流通池并暴露于流动鞘液时。根据一些实施例,甘油的浓度百分比以(v/v)表示,而pvp的浓度百分比以(w/v)表示。
323.图5e描绘了与根据本发明实施例的流通池技术(右列)相比的基于传统显微镜湿法封片技术(左列)的图像捕获结果。湿法封片程序可被视为图像清晰度和质量的目标标准。据观察,涉及如本文所公开而设计的鞘液和流通池的技术有效实现了与湿法封片程序相当的图像清晰度和质量。
324.根据一些实施例,当样品流体与鞘液之间的粘度差超过某一阈值时,流动料流带可发生分离。根据一些实施例,当使用包含60%的甘油的鞘液时,观察到了流动料流带分离。
325.方法
326.图6描绘了根据本发明实施例使用被配置用于组合式粘度和几何流体聚焦的粒子分析系统使多个粒子成像的示例性方法600的各方面。粒子可包含在具有样品流体粘度的血液流体样品610中。如这里所示,该方法可包括如步骤630所指示使鞘液620沿着流通池的流路流动。鞘液620可具有与样品流体粘度相差一个处于预定粘度差范围内的粘度差的鞘液粘度。该方法还可以包括如步骤630所指示将血液流体样品610注射到流通池内的流动鞘液中,以便提供被鞘液包裹的样品流体料流。另外,该方法可包括如步骤640所指示使样品流体料流和鞘液流过流路尺寸缩减段流向成像位点。当样品料流和鞘液穿过流路尺寸的缩减段或变窄过渡区时,与粘度差相关的鞘液和样品流体料流之间的相互作用所引起的粘度流体聚焦作用(如步骤650中所描绘)连同与流路尺寸的缩减段相关的鞘液和样品流体料流之间的相互作用所引起的几何流体聚焦作用(如步骤660中所描绘)有效地在成像位点在多个粒子的至少一些中提供靶标成像状态,同时鞘液中的粘度剂保持样品流体料流中细胞的活力,使得细胞从样品流体料流延伸到流动鞘液中时细胞的结构和内容物完好无损(如步骤670中所描绘)。方法还可以包括在成像位点对多个粒子成像,如步骤680中所描绘。
327.图6a和6b描绘了与剪切力、侧向压缩、取向、差异粘度、鞘液与样品流体之间的相对运动等相关的示例性流动料流特性。
328.图6c描绘了根据本发明实施例的用于使血液流体样品中的粒子成像的示例性方法6000的各方面。如此处所示,血样6010包含粒子,并且可分成一个或多个样品流体,诸如
包含粒子的第一样品流体6012和包含粒子的第二样品流体6014。该方法可包括如步骤6020所指示使鞘液沿着流通池的流路流动。此外,该方法可包括将第一样品流体6012从样品流体注射管注射到流通池内的流动鞘液中,如步骤6030所指示,以便提供具有邻近注射管的第一厚度的样品流体料流。流通池的流路可具有流路尺寸的缩减段,使得样品流体料流的厚度从初始厚度降低到邻近图像捕获位点的第二厚度。方法6000还可包括在流通池的图像捕获位点处使来自第一样品流体的第一多个粒子成像,如步骤6040所指示。
329.方法6000还可包括引发样品流体瞬变。例如,通过如下方式引发样品流体瞬变:终止向流动鞘液中注射第一样品流体,以及将第二样品流体注射到流动鞘液中,如步骤6050所指示。此外,方法6000可包括在流通池的图像捕获位点处使来自第二样品流体的第二多个粒子成像,如步骤6060所指示。根据一些实施例,使第二多个粒子成像可基本上在样品流体瞬变之后和在使第一多个粒子成像的4秒内进行。
330.剪切应变速率
331.图7和8描绘了根据本发明实施例的对于流通池中某些流动条件的剪切应变速率值的各方面。在这些附图的每一个中,使用30%甘油鞘液。在一些情况下,粘度可具有2.45
×
10
‑3的值。剪切应变值可等于粘度值乘以应变速率值得到的乘积。参照图7,样品可具有0.3μl/s的流速,而鞘液可具有21μl/s的流速。参照图8,样品可具有1μl/s的流速,而鞘液可具有70μl/s的流速。在这些图的每一个中,可以看出,流动展示出朝向中心(c)的更低的应变值和朝向周边(p)的更高的应变值。此类应变值在一些实施例中可对应于不对称流通池构造。
332.如图7中所描绘,根据一些实施例,朝向流动料流的中心(c)部分的更低的应变速率可具有约500(1/s)或更低的值,而朝向流动料流的周边(p)的更高的应变速率可具有约3000(1/s)或更高的值。如图8中所描绘,根据一些实施例,朝向流动料流的中心(c)部分的更低的应变速率可具有约1000(1/s)或更低的值,而朝向流动料流的周边(p)的更高的应变速率可具有约9000(1/s)或更高的值。
333.因此,可以看出,更低的样品和鞘液速率(例如,图7)对应于更低的应变速率,而更高的样品和鞘液速率(例如,图8)对应于更高的应变速率。应当理解,本发明的实施例涵盖使用对应于各种粘度值、各种应变速率值和/或各种剪切应力值的样品和/或鞘液。
334.自动对焦靶标
335.pioal可被引入流通池并将样品输运穿过成像区,然后朝排放口输运。可将样品流体的料流注射穿过具有平坦开口的插管以建立具有相当大的宽度的流路。例如,pioal可具有比样品流体相对更高的粘度、合适的密度,并且在样品注射时的流速使得样品流体变平为薄带形状。样品流体的带与pioal一起被输运,以在观察口的前方通过,在观察口中布置高光学分辨率成像设备和光源以观察带形样品料流。
336.带形样品料流与pioal一起被输运,以在观察口的前方通过,在观察口中布置高光学分辨率成像设备和光源(例如,紫外、可见或红外)以观察带形样品料流。高光学分辨率成像设备和光源可设置在流通池的相对侧以便获得粒子诸如血细胞的背光图像。高光学分辨率成像设备通过流通池中的观察口捕获样品的像素数据图像。例如,高光学分辨率成像设备以与样品流动速度一致的重复率捕获图像,使得带形样品料流的截面在无大量空隙或重叠的情况下成像。
337.本发明的实施例提供在用于采集流过流通池的带形样品料流的图像的系统的设计和操作中实施的多种独特结构和功能特征。示例性实施例被配置成获得粒子的充分聚焦图像,所述图像具有足够的清晰度和分辨率以揭示各种粒子诸如血细胞的不同特征,所述不同特征允许粒子和/或细胞类型彼此区分开。
338.为了使带形样品料流聚焦,可设定高光学分辨率成像设备与带形样品料流之间的距离,使得带形样品料流位于沿着光轴离高光学分辨率成像设备的所需距离(例如,聚焦距离)。
339.聚焦距离是用于分辨光敏元件阵列上的图像的高光学分辨率成像设备的镜头的特性,其由镜头元件的材料、形状和尺度以及其配置和沿着光轴的设置限定。成像的样品的区域的尺度以及样品中焦点内的视野深度由镜头配置决定。
340.孔调节和变焦调节是可行的,但出于简明目的,本发明中的某些实施例使得高光学分辨率成像设备聚焦于带形样品料流中的粒子仅仅需要在正确距离,即分辨带形样品料流中的粒子在光敏元件阵列(例如,电荷耦合设备阵列)上的聚焦图像的距离,使高光学分辨率成像设备与流通池中的带形样品料流相对定位。高光学分辨率成像设备可包括记录或传送用于显示和/或处理和/或传输的静态图像或视频图像的相机。
341.在一个方面,流通池的对称性质以及样品流体与pioal的注射方式为pioal中的带形样品料流提供流通池内的可重复位置。然而,流通池与高光学分辨率成像设备的相对位置可发生改变并且需要不时的位置调节以保持高光学分辨率成像设备与带形样品料流之间的最佳距离,从而提供高质量聚焦图像。
342.本发明的实施例涵盖用于血液和/或其他生物流体的自动化视觉分析仪系统和方法,其结合自动对焦设备/装置以通过非常精确地设定带形样品料流与高光学分辨率成像设备之间的距离来提供样品的可靠聚焦的图像。在一个方面,本文所公开的自动对焦系统实施例可非常精确地设定带形样品料流与高光学分辨率成像设备之间的距离并且捕获样品的可靠聚焦的图像。在一些实施例中,使用算法确定实现良好聚焦结果的距离。
343.一个目标是采用为包裹在pioal流中的带形样品料流提供稳定且高度可重复的位置的流通池,同时结合高光学分辨率成像设备及保持高光学分辨率成像设备和带形样品料流之间的最佳距离的自动对焦设备/装置,从而提供高质量聚焦图像。
344.此类装置和方法在本文中公开并要求保护。提供了对称流通池,已发现其产生流通池内的可重复带形样品料流位置。聚焦涉及设定高光学分辨率图像设备相对于带形样品料流的完全正确相对位置,以便保持聚焦于带形样品料流。
345.有利的是,可使用自动对焦光栅诸如高对比度光栅或类似聚焦靶标,优选具有尖锐对比的特征诸如边缘的平坦靶标,在自动对焦过程中使流通池和/或高光学分辨率图像设备相对于彼此移动,所述自动对焦光栅固定在相对于流通池的适当位置并且用作聚焦对象代替样品自身。带形样品料流是沿着平行于高光学分辨率成像设备的光轴的线离自动对焦光栅的固定距离处的薄带。自动对焦光栅与带形样品料流位置之间的位移距离为恒定距离,该距离被初始测定并且编程到自动对焦工序中。其后的示例性技术是自动对焦于自动对焦光栅,然后使高光学分辨率图像设备和/或流通池相对于彼此位移已知且恒定的预定距离,于是高光学分辨率图像设备与带形样品料流位置之间的距离是提供带形样品料流的高质量聚焦图像的最佳距离。例如,首先,自动对焦算法使高光学分辨率成像设备的位置聚
焦于位于离带形样品料流的固定距离处的自动对焦光栅。聚焦于自动对焦光栅后,处理器在固定距离内操作电机驱动器,从而使带形样品料流处于高光学分辨率成像设备的焦点内。
346.示例性高光学分辨率图像设备包括物镜镜头和相关的像素图像传感器,所述像素图像传感器能够捕获图像,所述图像以足够的放大倍数和分辨率揭示粒子以提供分辨粒子的视觉特征的足够细节。在某些实施例中,与传统血液学分析仪相比,放大倍数要高至少2x(因此拍摄的每张图像提供2x图像面积),从而生成每个粒子的更详细信息。
347.pioal流路可对称地布置成使得带形样品料流上方和下方流过等量的pioal,pioal使带形样品料流伸展为薄带并定位于沿着平行于高光学分辨率成像设备的光轴的线离自动对焦光栅的固定距离处。在一个实施例中,自动对焦光栅包括在允许来自后照明源的光透过的开口周围的不透明边界,并且自动对焦光栅的距离能容易且明确地通过自动对焦对照物来定位。然后,通过使高光学分辨率成像设备在预定且恒定的位移距离内相对于流通池位移,而使带形样品料流处于焦点中。没有必要直接自动对焦于样品的图像内容,尽管进一步自动对焦是可以想到的。
348.自动化聚焦配置包括电机驱动器,所述电机驱动器响应于来自评估一系列距离内的聚焦质量的一个或多个量度并寻找最佳距离的处理器的控制信号,而调节沿着光轴的流通池与高光学分辨率成像设备的相对位置。例如,处理器可评估对比度的量度并操作电机驱动器以便自动对焦。在正常操作中,处理器操作电机驱动器以自动对焦于靶标,然后将高光学分辨率成像设备与流通池之间的距离调节所记录的离靶标的位移,以使带形样品料流处于焦点内。只要设备继续以相同方式移动带形样品料流并且不发生热膨胀或类似混杂因素,带形样品料流的图像就将保持在焦点内。
349.可使用初步的设置或校准过程测定并记录靶标与流通池中的带形样品料流位置之间的位移距离。准确位移距离(不同流通池可能略微不同)通过初步测试来确定,诸如通过交替地对靶标和测试带形样品料流自动对焦若干次,并记录平均结果作为与流通池相关的常数。
350.因此,将待成像的样品诸如制备的血样或另一种类型的样品沿着限定的流路引导穿过流通池中的观察区。pioal流路优选地是对称的并且样品被注射到pioal流的中心,其中样品被pioal流包裹。样品和鞘液材料诸如pioal的流速和粘度及密度特性与流通池的轮廓一起配合,以便使带形样品料流形成为一致地在可重复位置处流过观察区的平带。
351.样品可通过高光学分辨率成像设备的相机部件成像,并且采集的数字图像将通过至少部分自动化的图像分析过程(包括如本文所述的自动对焦过程)进行分析。
352.一个目标是区分、分类、子分类和/或计数血样以及本文所述的其他生物样品中的可能与特定病症相关的粒子诸如血细胞。在一个方面,本发明的粒子造影剂组合物可与视觉分析仪诸如本文所述的分析仪在方法中结合以提供流动细胞的出奇高质量的聚焦图像。可自动捕获并处理细胞。
353.图像允许自动化的基于图像的wbc分类计数,以及形态异常的自动化识别,其可用于对受试者是健康还是具有疾病、病症、异常和/或感染进行确定、诊断、预后、预测和/或支持诊断,和/或确定或监测受试者对治疗有响应还是无响应。血样中的细胞类目和/或亚类目计数在本发明中用作可以分析的该类流体的非限制性例子。
354.在一个方面,与本发明组合物一起使用的图像分析仪可通过非常精确地设定带形样品料流与光学系统的高光学分辨率成像设备之间的距离来捕获样品的可靠聚焦的图像。在一些实施例中,视觉分析仪可与本发明的组合物和算法联合使用以确定可实现良好聚焦结果的所述距离。样品被布置在流通池中并且被照明以允许通过观察口进行观察。单独的细胞或粒子清楚地出现在捕获的像素数据图像中,且具有揭示属性的足够特征细节,然后将所述属性与已知将细胞的各类目和亚类目彼此区分开的参数进行比较和对比。
355.一个目标是采用流通池,同时结合本文所述的示例性粒子造影剂组合物以及示例性pioal,从而提供对于粒子识别具有最佳质量和细节的图像。另外,pioal和装置为包裹在pioal流中的带形样品料流提供稳定且高度可重复的位置。这与高光学分辨率成像设备及保持高光学分辨率成像设备到带形样品料流的最佳距离的自动对焦设备/装置相结合,提供高质量聚焦图像。
356.自动对焦靶标
357.返回参照图1,粒子成像系统可包括相对于流通池22固定的自动对焦光栅或靶标44。自动对焦靶标44可用于获得流过流通池的血液流体粒子的聚焦图像。
358.图9a描绘了根据本发明实施例的示例性自动对焦靶标900。如此处所示,靶标900包括不透明环形带910和透明中心或孔920。在操作中,成像设备聚焦于带910并通过孔捕获图像。如本文别处和共同待审的美国专利申请no.____中所讨论,图像捕获方法可涉及首先聚焦(或自动对焦)于带910,然后在通过孔920获得图像之前调节图像捕获设备与样品流体料流之间的距离。因此,带910可提供图像捕获设备的自动对焦系统可对其检测和聚焦的靶标,并且靶标的某些部分(例如,边缘或段)可包括在图像中。在一些情况下,靶标可以具有中心孔的铬圆盘的形式提供。示例性靶标可设置有胶粘或固定到流通池的直径为约0.5mm的中心针孔。中心针孔或孔920的尺寸可被选择为使得捕获的图像940中可见不透明环形带910的仅四个边缘部分930,如图9b中所示。因此,环形带910不干扰细胞图像的捕获(例如,光可穿过孔920以照明样品粒子,并且视野基本上不受环形带妨碍)。这样,带910仅在图像的拐角中显现。
359.图10描绘了根据本发明实施例的示例性自动对焦靶标1000。靶标1000包括带或边界1010和中心孔1020。图11示出了根据本发明实施例的另一个示例性自动对焦靶标1100。靶标1100包括带或边界1110和中心孔1120。根据一些实施例,自动对焦靶标1100提供顶部和底部上具有50黑色像素的图像。在一些情况下,自动对焦靶标1100提供约65.3μm的流通池聚焦偏移量(fcfo)。fcfo的各方面在共同待审的美国专利申请no._____中进一步讨论,该专利申请的内容以引用方式并入本文。
360.图12a描绘了根据本发明实施例的示例性自动对焦靶标1200。靶标1200呈现为信箱设计,并且包括第一或上边界1210和第二或下边界1220。靶标1200还包括第一与第二边界之间的孔或透明通路1230。根据一些实施例,靶标具有约4mm的直径,并且信箱的高度为265μm。在一些情况下,上边界和下边界可呈现为半圆,并且可用沉积金属诸如氧化铬或一些其他不透明材料制备。
361.图12b示出了自动对焦靶标1200的中心部分的近距离视图。如此处所示,第一边界1210包括负/正数值刻度和居中的零值。第二边界1220包括类似的刻度。在一些情况下,刻度增量为100μm。根据一些实施例,刻度可用于有利于流通池的定位使得成像设备或相机的
视野可集中于样品料流。如此处所示,样品料流1240在垂直于第一和第二边界的刻度的方向上流动。作为聚焦方案的一部分,图像捕获设备可操作以聚焦于存在于边界1210、1220上的数字或其他字符或可成像对象。
362.本发明的实施例涵盖用于解决与使用粒子分析系统相关的热漂移的技术,由于所述热漂移,此类热效应可损害用成像设备获得的图像的质量。图13a描绘了具有热传感器1370、反射器1380和自动对焦靶标1344的流通池1320的局部侧视图。在粒子分析系统的操作期间,热效应可导致样品料流缓慢漂移偏离成像设备的焦点。例如,热效应可由来自灯的辐射热使流通池热膨胀所引起。此外,热效应可由传导性和辐射性加热使流通池和光具座组件(oba)组件热膨胀所引起。在一些实施例中,oba的某些部件可膨胀,这可导致聚焦误差。例如,此类部件可包括将相机24保持在一起的金属板、保持或连接到流通池的金属板、或将流通池和相机24保持在一起的金属板。图13b描绘了具有热传感器1370和自动对焦靶标1344的流通池1320的局部透视图。此外,图13c描绘了具有热传感器1370、反射器1380和自动对焦靶标1344的流通池1320的另一个透视图。
363.图13b描绘了具有热传感器1370和自动对焦或成像靶标1344的流通池1320的局部透视图。根据本发明的一些实施例,可使用与分析仪相关的热传感器所感测的温度,使图像捕获设备聚焦于样品流动料流。例如,温度可对应于样品流体温度、鞘液温度、流通池温度或图像捕获设备温度。在一些情况下,温度为流通池的成像位点处的温度。在一些情况下,温度为成像位点下游位置处的温度。在一些情况下,温度为成像位点上游位置处的温度。根据本发明的一些实施例,可使用与分析仪相关的温度变化率,使图像捕获设备聚焦于样品流动料流。例如,温度变化率对应于样品流体温度变化率、鞘液温度变化率、流通池温度变化率或图像捕获设备温度变化率。
364.图13c描绘了具有热传感器1370、反射器1380和自动对焦或成像靶标1344的流通池1320的另一个透视图。反射器1380可操作以减少或限制被流通池1320吸收的热的量。例如,反射器1380可阻断由闪光灯1342辐射的热,如图13a中所指示。因此,反射器1380可使灯的热冲击最小化。反射器1342也可减少灯所产生的炫光和光散射,从而得到改善的图像质量。热传感器1370定位在流体流通道附近并与图像捕获位点相邻,以使得可获得准确的温度读数。来自温度传感器的信息可用于使图像捕获设备聚焦于样品流体带料流。本文所公开的示例性自动对焦技术可基于出现于分析仪某些元件内的温度波动。
365.如图13d中所描绘,流通池1320d可包括具有气泡1302d可通过其释放或移除的端口或排放口1301d的流路1322d。如此处所描绘,可通过其施加真空的管1303d可与端口1301d接触以便从流动料流抽出气泡1302d。此类气泡移除机构适用于从流通池内的流动流体移除气泡,并且可操作以防止气泡或微气泡驻留或滞留在流通池的内部。
366.根据一些实施例,用于使血液流体样品中的粒子成像的方法可包括使鞘液沿着流通池的流路流动,以及将血液流体样品注射到流通池内的流动鞘液中从而血液流体样品以流动料流宽度大于流动料流厚度的样品流动料流流动,使得流通池具有相关温度。此外,方法可包括在与流通池相关的温度处于第一温度时,使图像捕获设备沿着成像轴聚焦于流动料流达到第一焦点状态,以及使用处于第一焦点状态的图像捕获设备采集流动料流内的第一亚组粒子的第一聚焦图像。而且,方法还可包括确定与流通池相关的温度已经历从第一温度到第二温度的变化,以及响应于温度的变化及流通池温度与所需焦点之间的已知关系
而自动地将图像捕获设备的焦点从第一焦点状态调节到第二焦点状态。此外,方法可包括使用图像捕获设备在第二焦点状态下采集流动料流内的第二亚组的粒子的第二聚焦图像。
367.在一些情况下,调节图像捕获设备的焦点的过程包括使用温度的变化及流通池温度与所需焦点之间的已知关系来调节图像捕获设备与流通池之间的距离。在一些情况下,调节图像捕获设备的焦点的过程包括使用温度的变化及流通池温度与所需焦点之间的已知关系来调节图像捕获设备的焦距。
368.动态范围扩展
369.图14是根据本发明实施例的框图,示出了用于实现在血样中进行粒子分析的动态或检测范围扩展的系统和方法的另外方面。如此处所描绘,耦合至少一个数字处理器18以操作电机驱动器54并分析如在相对于靶标自动对焦光栅44的不同焦点位置处采集的来自光敏元件阵列的数字化图像。处理器18被配置成测定自动对焦光栅44的焦点位置,即自动对焦于靶标自动对焦光栅44并且从而确定高光学分辨率成像设备24与自动对焦光栅44之间的最佳距离。这可通过图像处理步骤来实现,诸如施加算法以评估第一距离处图像中的对比度水平,该算法可施加到整个图像或至少自动对焦光栅44的边缘。处理器使电机54移动到另一个位置并评估该位置或边缘处的对比度,并且在两次或更多次迭代后测定使自动对焦光栅44上的焦点的精确度最大化(或如果已移动到该位置,则将优化焦点的精确度)的最佳距离。处理器依赖于自动对焦靶标自动对焦光栅44与带形样品料流之间的固定间距,处理器18然后控制电机54将高光学分辨率成像设备24移动到正确距离以聚焦于带形样品料流32。更具体地讲,处理器操作电机以使高光学分辨率成像设备与带形样品料流32之间的距离位移所述位移距离52(参见图1),带形样品料流从靶标自动对焦光栅44位移所述位移距离52。这样,高光学分辨率成像设备聚焦于带形样品料流。
370.根据一些实施例,视觉分析仪17为图1的示例性分析仪17。视觉分析仪17可包括至少一个流通池22和至少一个成像设备24诸如具有成像传感器如数字相机的高光学分辨率成像设备。视觉分析仪17还可包括样品注射器29。样品注射器29被配置成向所述至少一个流通池22中提供样品12。流通池22限定内部pioal流路,所述流路例如在流动方向对称地变窄。流通池22被配置成引导样品流32穿过流通池22中的观察区。
371.图14示出了如所述的数字成像的自动对焦和其他方面。此类技术可结合血细胞装置一起使用,其不基于成像或可能与所述实施例相比较少与图像相关,诸如库尔特血细胞计数器,也称为流式细胞仪。此类计数器已知用于检测和计数流体中的血细胞和粒子,但通常不通过成像来进行。在这种类型的计数器中,流通池被布置成输运包裹在流体中的粒子流。流通池变窄而迫使流路中的粒子成单行。横跨流路的一对电极或其他检测器通过在细胞穿过时检测电阻抗的脉冲式变化或光源与光检测器之间的光路的遮挡来产生计数。
372.流式细胞仪是有利的,因为可对大量细胞或其他粒子进行计数,远大于可实际上在视觉计数器中成像的细胞的数量。但流式细胞仪在如下方面不那么有效:按类型区分细胞,或实现正常与异常细胞之间的区别,或将成群细胞诸如血小板团块与离散血细胞区分开。通过在统计上显著数量的带形样品料流的图像帧中操作分析仪,例如如所述的视觉分析仪,可测量血细胞类型的分布或成比例比率。由视觉分析仪测定的成比例比率或其函数应用于血细胞计数,并且更大数量的血细胞由流式细胞仪计数,但就细胞类型而言较少区分或未区分,从而提供利用这两种类型的分析仪的特殊优点的准确总血细胞计数。
373.根据一些实施例,可通过应用算法,例如基于粒子计数的成比例比率的算法,来推断粒子计数。图14示出了适于血液分析的示例性装置。在一些实施例中,粒子计数器15和视觉分析仪17可串联而非并联。粒子计数器15可为例如库尔特血细胞计数器,其检测并计数流体中的血细胞和粒子。在这种类型的计数器中,流路(未示出)被布置成输运包裹在流体中的粒子流。流路变窄而迫使流路中的粒子成单行。横跨流路的一对电极或其他检测器通过在细胞穿过时检测电阻抗的脉冲式变化或光源与光检测器之间的光路的遮挡来产生计数。粒子计数器15被配置成对大量细胞或其他粒子进行计数。但粒子计数器15可能不能区分各亚类目细胞的各成员和/或区分正常与异常细胞,或将成群细胞诸如血小板团块与离散血细胞区分开。
374.视觉分析仪17还可包括至少一个接触室25,所述接触室被配置成提供能有效产生用于粒子分类和/或子分类的视觉区别的至少一种化学品,所述化学品包括稀释剂、透化剂、造影剂中的至少一者。例如,如参照图1和14所示,通过样品注射器29将接触的样品引入流通池中,并且从注射器27引入鞘液或细胞内细胞器配向试剂。可使用稀释剂将样品稀释到合适的浓度。使用造影剂和/或透化剂产生用于分类和/或子分类粒子的视觉区别。使用pioal使特定类型的细胞或细胞结构在更好成像的方向上配向。在一些实施例中,可施加所述至少一种化学品以首先接触样品,然后将所处理的样品提供于视觉分析仪17上。通过至少添加至少一种化学品对样品的处理可在室温下进行。在一些实施例中,此类处理可在诸如10、15、20、25、30、35、36、37、38、38、39、40、45、46、47、48、49或50℃的温度下进行。在所选温度下的处理可在培养箱中进行,所述培养箱与视觉分析仪17分隔开或在视觉分析仪17上,并且是温度受控的。
375.在一些实施例中,视觉分析仪可具有造影剂注射器以用于使样品与造影剂和/或透化剂或表面活性剂接触。在其他实施例中,可在注射到视觉分析仪中之前,使样品与造影剂、透化剂接触。在其他实施例中,视觉分析仪包含加热元件以用于在与造影剂和/或透化剂接触时将样品在受控温度下加热受控时间。视觉分析仪还可具有冷却元件以用于在加热步骤之后冷却样品混合物。可用于处理血液流体样品的示例性造影剂组合物和方法在共同待审的美国专利申请号________中有所公开,所述专利的内容以引用方式并入本文中。
376.通过在统计上显著数量的带形样品料流的图像帧中操作如所述的视觉分析仪17,可通过处理器18测定各细胞类目和/或亚类目中的细胞的成比例比率。由视觉分析仪17测定的成比例比率应用于血细胞计数,并且更大数量的血细胞由粒子计数器15计数,但就细胞类目和/或亚类目内的成员而言较少区分或未区分,从而提供利用粒子计数器15和视觉分析仪17两者的特殊优点的准确总血细胞计数。
377.除了提供准确结果之外,包括粒子计数器15和视觉分析仪17的装置还提供改善分析速度方面的显著优点。在图14中,计数不同血细胞的准确结果可通过显示器63输出。在分析过程期间,操作人员可通过终端65与处理器18进行交互。之前,至多约25%至30%的结果由操作人员在显微镜下检查通过造影剂制备的载片来人工复核。相比之下,使用本发明的装置的示例性方法包括粒子计数器上的cbc以及根据一些实施例分类和/或子分类血细胞。通过操作如本发明中所述的装置,可在视觉分析仪上检查图像并且样品将需要更少频率的人工复核。
378.电机54可包括精度略微小于高光学分辨率成像设备或数字图像捕获设备所成像
的区别性特征(特别是血细胞的各方面)的齿轮步进电机。如果调节高光学分辨率成像设备24的位置以将光学物镜的位置定位于带形样品料流的宽度内,则带形样品料流中的细胞/粒子的视图在焦点内。自动对焦光栅可位于高光学分辨率成像设备或数字图像捕获设备的视野的边缘处,从而不会干扰观察。
379.此外,当高光学分辨率成像设备在位移距离内移动并且自动对焦光栅偏离焦点时,出现在焦点内的特征是血细胞而非自动对焦光栅。根据一些实施例,自动对焦光栅可由视野中的形状限定。所述形状为有限尺寸的相对薄的离散形式,并且因此在移动位移距离之后,当聚焦于带形样品料流时所述形式在数字化图像中基本上不可见。在尺度适合血液学(血细胞)成像应用的流通池中,典型的位移距离可为例如50至100μm。在一些实施例中,自动对焦特征保持高光学分辨率成像设备处于最佳焦点距离的1μm内。
380.可调节流通池内部轮廓以及pioal和样品流速以使得样品形成带形料流。料流可与包裹在带形样品料流中的粒子大约一样薄或甚至更薄。白血细胞可具有例如约10μm的直径。通过提供厚度小于10μm的带形样品料流,可在带形样品料流被鞘液或pioal伸展时使细胞取向。带形样品料流沿着变窄流路在粘度与带形样品料流不同(诸如更高粘度)的pioal层内的出奇伸展有利地趋于使非球形粒子在基本上平行于流动方向的平面中配向,并对细胞施加力,从而提高细胞的细胞内结构的焦点内内容物。高光学分辨率成像设备24的光轴基本上正交(垂直)于带形样品料流的平面。带形样品料流在成像时的线速度可为例如20
‑
200mm/s。在一些实施例中,带形样品料流的线速度可为例如50
‑
150mm/s。
381.带形样品料流厚度可受样品流体和pioal的相对粘度和流速的影响。样品源25和/或pioal源27(例如,包括精密排量泵)可被配置成以可控的流速提供样品和/或pioal以优化带形样品料流32的尺度,即作为至少与高光学分辨率成像设备24的视野一样宽的薄带。
382.在一个实施例中,pioal源27被配置成以预定的粘度提供pioal。该粘度可与样品的粘度不同,并且可以高于样品的粘度。对pioal的粘度和密度、样品材料的粘度、pioal的流速和样品材料的流速进行调整以在离自动对焦光栅的位移距离处保持带形样品料流,并具有预定的尺度特性,诸如有利的带形样品料流厚度。
383.在实践实施例中,pioal具有比样品更高的线速度和比样品更高的粘度,从而将样品伸展成平带。pioal粘度可最多至10厘泊。
384.在图14中所示的实施例中,用于分析从光敏元件阵列获得的像素数字图像的相同数字处理器18也用于控制自动对焦电机54。然而,高光学分辨率成像设备24并不会对每张捕获的图像自动对焦。自动对焦过程可周期性地或例如在适当传感器检测到温度或其他工艺变化时或在图像分析发现可能需要重聚焦时完成。在其他实施例中还可以使血液学图像分析由一个处理器完成,并且使单独的处理器,任选地连同其自身光敏元件阵列,被布置用于处理自动对焦于固定靶标44的步骤。
385.在图14中,至少一个所述数字处理器18被配置成在程序化时间或在程序化条件下或根据用户需求自动对焦,并且还被配置成执行基于图像的粒子的分类和子分类。示例性粒子包括细胞、白血细胞、红血细胞等等。
386.在一个实施例中,至少一个所述数字处理器18被配置成检测自动对焦再引发信号。自动对焦再引发信号可由检测到的温度变化、如由像素图像日期的参数所识别的聚焦质量的降低、时间的流逝或用户输入而触发。有利的是,从测量位移距离52以重新校准的意
义上说,不必要重新校准。任选地,自动对焦可程序化以在运行之间以特定频率/间隔重新校准以便进行质量控制和/或保持聚焦。
387.位移距离52在一个流通池与另一个流通池之间略有差异,但对于给定流通池而言保持恒定。作为装配图像分析仪与流通池时的安装过程,首先估计位移距离,然后在其中执行自动对焦和成像方面的校准步骤期间,测定流通池的准确位移距离并作为常数输入处理器18的程序设计中。
388.参照图15,根据一些实施例用于分析包含粒子的样品12的示例性装置10包括具有至少一个检测范围的粒子计数器15、分析仪17和处理器18。图15的框图是出于举例说明的目的。粒子计数器15、分析仪17和处理器18可以彼此连接或可以不彼此连接。在一些实施例中,处理器可耦合到分析仪和/或粒子计数器。在其他实施例中,处理器可为分析仪和/或粒子计数器的部件。
389.粒子计数器15包括至少一个通道,并且被配置成为至少一种类目和/或亚类目的粒子提供粒子计数。在一些实施例中,粒子计数器15包括用于不同类目和/或亚类目的粒子的至少两个通道。在一些实施例中,通过感测样品的电阻抗或光散射来对粒子进行计数。适用的粒子计数器15的例子包括但不限于流式细胞仪。在一些实施例中,检测可能响应于不同物理性质而同时或顺序地在多个通道中的每一个中进行。
390.分析仪17被配置成区分不同类目和/或亚类目以及每种类目和/或亚类目的粒子的对应成员。适用的分析仪17的例子包括但不限于视觉分析仪、数字相机或可捕获像素数据的任何其他像素数据分析仪,并且被程序化以区分像素文件中代表的属性。处理器18和分析仪17被配置成应用算法,诸如测定两种类目或两种对应亚类目的粒子的计数的成比例比率,以及将此成比例比率应用于在粒子计数器15的至少一个通道中获得的至少一种类目和/或亚类目的粒子的粒子计数。在数据分析之后,处理器18在输出20处提供样品12中的每种类目和每种对应亚类目的粒子的浓度的准确量度。
391.在一些实施例中,在样品12中,至少第一类目和/或亚类目的粒子可以适用于第一类目和/或亚类目的粒子的检测范围之外的浓度存在,而至少第二类目和/或亚类目的粒子以适用于第二类目和/或亚类目的粒子的检测范围之内的浓度存在。在粒子计数器15上测定第二类目和/或亚类目的粒子的浓度。在分析仪17上测定第一类目和/或亚类目与第二类目和/或亚类目的粒子的成比例比率。至少部分地通过如下方式在处理器18上计算第一类目和/或亚类目中的粒子的浓度:将此成比例比率应用于第二类目和/或亚类目的粒子的浓度。
392.在一些实施例中,粒子计数器15的所述至少一个通道中检测到的一类目和/或亚类目的粒子可包括至少两种类别的粒子。并且每种类别的粒子可包括多种亚类别。粒子计数器15被配置成检测符合例如基于预定尺寸范围的一项或多项选择标准的多个粒子并提供其粒子计数。选择标准涵盖至少两种类别的粒子的成员。分析仪17和处理器18被程序化以区分所述至少两种类目和/或亚类目的粒子的成员。在处理器18上测定每个成员在至少两种类目和/或亚类目内的分布。处理器18使用此分布校正粒子计数器15上获得的所述至少两个类目和/或亚类目中至少一者的成员的粒子计数。
393.更具体地讲,装置10可用于识别和定量样品中的不同血细胞,包括rbc、wbc、plt和其他血细胞、胎儿细胞、或细菌细胞、病毒粒子、寄生生物、囊肿(包括寄生虫性囊肿)、晶体
或其碎片或其他细胞碎片。
394.图15a描绘了根据本发明实施例的示例性计数器或计数模块1500a的各方面。此类计数器可以操作从而控制或实施针对wbc、rbc和plt细胞计数和血红蛋白测量的各种机械功能以及电子和光度测量功能。示例性计数器可用于制备cbc分析用样品,以及经由孔浴槽组件(例如,wbc浴槽1510a和rbc浴槽1520a)生成cbc参数测量值。根据一些实施例,图15的计数器15可由图15a的计数器1500a表示。相似地,根据一些实施例,图14的计数器15可由图15a的计数器1500a表示。根据一些实施例,图16的计数器722可由图15a的计数器1500a表示。
395.可使用电阻抗方法对血液的细胞成分(例如,红血球、白血球和血小板)进行计数。例如,可将抽吸的全血样品分成两个等分试样,并与等渗稀释剂混合。可将第一稀释液递送到rbc孔浴槽1520a,并可将第二稀释液递送到wbc孔浴槽1510a。在rbc室中,可通过细胞穿过感测孔时的电阻抗对rbc和血小板两者进行计数和区分。例如,可将介于2fl和20fl之间的颗粒计作血小板,且可将大于36fl的那些颗粒计作rbc。对于wbc室处理而言,可将rbc裂解试剂添加到wbc稀释液等分试样,用于裂解rbc和释放血红蛋白,然后可在wbc浴槽的感测孔中通过阻抗对wbc进行计数。在一些情况下,所述浴槽可包括多个孔。因此,例如,可使用rbc三孔浴槽来获得血细胞计数技术中所使用的血细胞计数。
396.示例性cbc样品制备技术可包括两个过程,即样品采集和样品递送。样品采集可在抽吸165μl患者样品并将该样品导向至血液采样阀(bsv)时进行。bsv可操作以将特定体积的患者样品与处理试剂一起导向,以递送到两个三孔浴槽。患者样品和处理试剂能够以一定角度递送到孔浴槽的底部,该孔浴槽由于具有圆形设计,允许样品和试剂充分混合而不会混合气泡。然后可以制备供测量和分析用的样品。根据一些实施例,在wbc浴槽中,6.0ml(
±
1.0%)稀释剂和28μl样品可以与1.08ml(
±
1.0%)dxh细胞裂解物混合,达到1:251的最终稀释度。根据一些实施例,在rbc浴槽中,10ml(
±
1.0%)稀释剂和1.6μl样品可进行混合,达到1:6250的最终稀释度。在患者样品和试剂进行混合之后,可对孔施加真空和孔电流,以测量细胞计数和细胞体积。rbc和plt计数还可包括施用扫流技术,以防止细胞在孔附近发生再循环。在某些实施例中,针对rbc和plt的数据采集可持续最多20秒,且针对wbc的数据采集可持续最多10秒。在某些实施例中,可通过前置放大器卡放大由孔组件生成的所有模拟脉冲,然后将所述模拟脉冲发送到cbc信号调节分析器卡以进行模拟
‑
数字转换和参数提取。根据一些实施例,可以使用系统测量针对每个细胞事件的多种参数,并且可以使用数字参数提取方法提供数字测量值,诸如时间、体积(脉冲属性,包括振幅和脉冲宽度)、计数和计数率、以及等待时间。可使用此类测量值进行脉冲编辑、重叠校正、计数投票,生成wbc、rbc和plt的直方图,进行直方图投票、模式分析、以及干扰校正,等等。
397.图16描绘了根据本发明实施例用于测量血液流体样品中的第一细胞类型的数量的系统和方法的各方面,其中样品还包含第二细胞类型。如此处所示,方法700可包括从血液流体样品710获得样品的第一体积720和样品的第二体积730。如步骤724所指示,方法可包括通过使第一体积流过血液学细胞计数器722来测定样品的第一体积720中的第二细胞类型的群体。通常,细胞计数器722适用于在样品中有足够量的电可区分类型的细胞时且不在细胞类型的量超过特定限值或阈值时准确地对细胞进行计数。细胞计数器可用于在较短时长内对血样中的红血细胞或其他组分(例如,大组分)的总数进行计数。在一些情况下,当
区分血液中的白血细胞和其他组分(例如,大组分)或可能存在若干不同物质但每种物质数量相对较少时,细胞计数器可能会有难度。
398.此外,方法700可包括如步骤732所指示通过将样品的第二体积730注射到流通池内流动的鞘液中以便提供具有厚度和大于厚度的宽度的样品料流,从而采集第一数量的第一类型细胞和第二数量的第二细胞类型的图像,所采集的图像是沿着横穿样品料流的厚度的图像路径采集的。在一些情况下,使用如图14和/或图15中所描绘的分析仪17进行图像采集732。在一些情况下,分析仪可有效地区分血液流体样品中的白血细胞、巨大血小板和其他大组分。然而,当使用此类分析仪获得样品中的全粒子计数时,可能存在挑战。此外,在一些情况下,可能不期望使用分析仪获得某些计数(例如,所有红血细胞的计数),因为除获得计数之外,此类计数工序还可涉及进行粒子的表征。根据一些实施例,分析仪用于获得通过分析仪处理的仅一定百分比或一部分的样品的图像。
399.如图16中所描绘,方法700可包括如步骤738所指示使用所采集的图像测定第一数量的第一细胞类型734与第二数量的第二细胞类型736的比率。方法还包括如步骤740所指示使用比率738和第二细胞类型724的群体计算样品中的第一细胞类型的细胞数量量度。
400.根据一些实施例,步骤740处计算的细胞数量量度为血液流体样品710中的第一细胞类型的细胞浓度。在一些情况下,步骤740处计算的细胞数量量度为血液流体样品710中的第一细胞类型的细胞计数。在一些情况下,细胞计数器722具有与对第一细胞类型计数相关的第一精确度和与对第二细胞类型计数相关的第二精确度,其中第二精确度优于或高于第一精确度。在一些情况下,(参见例如图19a和19b)血液学细胞计数器722具有所需精确度范围,并且所需精确度范围在第一体积720中的细胞的最小群体与第一体积720中的细胞的最大群体之间延伸,其中在步骤724处测定的体积的第二细胞类型的群体在所需精确度范围之内,并且其中在步骤740处计算的样品的第一细胞类型的细胞数量量度在所需精确度范围之外。
401.如图16中进一步描绘(且继续参照图19a和19b),方法可任选地包括由于第一体积流过血液学细胞计数器722而测定样品的第一体积中的第一细胞类型726的群体。第一体积中的第一细胞类型726的所测定群体可高于或低于第一细胞类型的所需精确度范围,并且也可不同于如步骤740中所计算的第一细胞类型的细胞数量量度。在一些情况下,(例如,图19a),第一细胞类型726的所测定群体为零。在一些情况下,(例如,图19b),第一细胞类型726的所测定群体大于零。
402.根据本发明的一些实施例,血液学细胞计数器722可包括响应于第二类型细胞流过细胞计数器而检测电阻抗的变化的传感器机构。根据一些实施例,血液学细胞计数器722包括响应于第二类型细胞流过细胞计数器而检测光路的遮挡的传感器机构。
403.在一些情况下,血液学细胞计数器722具有第一细胞类型的最小可检测浓度限值和最大可检测浓度限值,以及第二细胞类型的最小可检测浓度限值和最大可检测浓度限值。第二细胞类型724的所测定群体可基于高于第二细胞类型最小限值并低于最大限值的第二细胞类型的所检测浓度参数。第一细胞类型可以低于第一细胞类型最小限值或高于最大限值的浓度存在。
404.在一些情况下,血液学细胞计数器722具有第一细胞类型的最小可检测体积限值和最大可检测体积限值,以及第二细胞类型的最小可检测体积限值和最大可检测体积限
值。第二细胞类型724的所测定群体可基于高于第二细胞类型最小限值并低于最大限值的第二细胞类型的所检测体积参数。第一细胞类型可以低于第一细胞类型最小限值或高于最大限值的体积参数存在。
405.在一些情况下,血液学细胞计数器722具有第一细胞类型的最小可检测尺寸限值和最大可检测尺寸限值,以及第二细胞类型的最小可检测尺寸限值和最大可检测体积尺寸。第二细胞类型724的所测定群体可基于高于第二细胞类型最小限值并低于最大限值的第二细胞类型的所检测尺寸参数。第一细胞类型可以低于第一细胞类型最小限值或高于最大限值的尺寸参数存在。
406.根据本发明的一些实施例,(参照图13b、c),样品第一体积中的第二细胞类型724的群体的测定包括将第一细胞类型的细胞和第二细胞类型的细胞分组在一起。在一些情况下,方法还可包括使用比率和第二细胞类型的群体计算样品中的第二细胞类型的细胞数量量度。在一些情况下(例如,如图19d中所描绘),样品第一体积中的第二细胞类型724的群体的测定包括将第一细胞类型的细胞和第二细胞类型的细胞分组在一起,以及由于第一体积流过血液学细胞计数器722而测定样品的第一体积中的第一细胞类型726的群体。如步骤740中计算的样品中的第一细胞类型的细胞数量量度可使用比率738、第二细胞类型724的群体和第一细胞类型726的群体。
407.在其他方面,例如如图17和/或图19a和19b中所描绘,提供了用于分析包含粒子的样品的方法。在此方法中,将样品提供于具有检测限值的粒子计数器上,如图17的方法70中的步骤72所指示。至少第一类目和/或亚类目的粒子可以适用于第一类目和/或亚类目的粒子的检测范围之外的浓度存在于样品中,并且至少第二类目和/或亚类目的粒子在适用于第二类目和/或亚类目的粒子的检测范围内存在于样品中。在粒子计数器上测定样品中第二类目和/或亚类目的粒子的浓度,如步骤74所指示。还将样品提供于分析仪上以测定第一类目和/或亚类目的粒子与第二类目和/或亚类目的粒子的成比例比率,如步骤76所指示。至少部分地通过如下方式计算第一类目和/或亚类目中的粒子的浓度:将成比例比率应用于第二类目和/或亚类目的粒子的浓度,如步骤78所指示。图19a示出了低于检测范围的样品中的粒子的检测,并且图19b示出了高于检测范围的样品中存在的粒子的检测。
408.图17因此示出了根据一些实施例的测定第一类目的粒子的浓度的示例性方法70,所述第一类目的粒子以粒子计数器的检测范围之外的浓度存在于样品中。在步骤72中,还参照图15和17,将样品12提供于具有至少一个检测范围的粒子计数器15上。样品12包含可分散于流体中的粒子。在一些实施例中,第一类目的粒子以高于适用于第一类目的粒子的检测范围的上限的浓度存在于样品中。第二类目的粒子在适用于第二类目的粒子的检测范围内存在于样品中。例如,第一类目和/或亚类目的粒子可包括wbc。第二类目的粒子可包括血小板。
409.在一些实施例中,第一类目的粒子以低于适用于第一类目的粒子的可检测范围的下限的浓度存在于样品中。第二类目的粒子在适用于第二类目的粒子的检测范围内存在于样品中。例如,第一类目的粒子包括血小板。第二类目的粒子包括白血细胞。
410.在图17的步骤74中,在粒子计数器15上测定样品12中的第二类目的粒子的浓度。粒子计数器可包括至少一个通道。在一些实施例中在通道之一中测量第二类目的粒子。在一些实施例中粒子计数器可包括至少两个通道。如果浓度在适用于第一类目的粒子的检测
范围内,则第一类目的粒子可在另一个通道中进行计数。
411.在图17的步骤76中,将样品12提供于分析仪诸如视觉分析仪17(例如,如图14或15中所描绘)上以测定第一类目的粒子与第二类目的粒子的成比例比率。在一些实施例中,视觉分析仪17包括如上所述连接到成像设备的流通池22。可根据本文所述的方法测定第一类目的粒子与第二类目的粒子的成比例比率。例如,可将包括稀释剂、透化剂和造影剂中至少一者的至少一种化学品引入样品中。可用于处理血液流体样品的示例性化学品、组合物、造影剂和相关组合物在共同待审的美国专利申请no.____中有所讨论,所述专利的内容以引用方式并入本文中。造影剂可有效地产生能区分第一类目和/或亚类目和第二类目和/或亚类目的粒子的视觉区别。在一些实施例中可将图14中所描绘的所制备样品12b施加到所述至少一个流通池22。捕获所制备样品12b的粒子的图像。通过分析仪进行图像分析,所述分析仪可为视觉分析仪17和/或处理器18。然后通过分析带形样品料流的多个图像,测定第一类目的粒子与第二类目的粒子的成比例比率。
412.在图17的步骤78中,然后可通过处理器18(例如,如图15中所描绘)至少部分地通过将成比例比率应用于第二类目的粒子的浓度来计算第一类目中的粒子的浓度。
413.本发明还提供用于分析包含粒子的样品的方法。图18示出了根据一些实施例测定两种亚类目的粒子的浓度的示例性方法80,所述粒子不能被粒子计数器区分开。在步骤82中,将样品(例如,图15的样品12)提供于粒子计数器(例如,图15的粒子计数器15)上,所述粒子计数器具有希望区分开的至少两种类目或亚类目的粒子所符合的检测标准。来自粒子计数器的结果涵盖图18的步骤84中单个计数内的这些类目或亚类目。
414.在步骤86中,将样品提供于分析仪(诸如视觉分析仪)上以测定第一类目或亚类目的粒子与第二类目或亚类目的粒子的成比例比率。在一些实施例中,例如如图14和/或15中所描绘,视觉分析仪17包括连接到成像设备的流通池22。
415.可根据本文所述的方法测定第一类目或亚类目的粒子与第二类目或亚类目的粒子的成比例比率。将包括稀释剂、透化剂和造影剂中至少一者的至少一种化学品引入样品中。造影剂能有效地产生用于将第一类目或亚类目与第二类目或亚类目的粒子区分开的粒子分类和子分类的视觉区别。如图14中所描绘,在一些实施例中可将所制备样品12b施加到所述至少一个流通池22。捕获所制备样品12b的粒子的图像。通过视觉分析仪和/或处理器18进行图像分析。然后通过分析多个图像,测定所述至少第一类目的粒子与第二类目的粒子的成比例比率。
416.在图18的步骤88中,然后可通过处理器18,如图14或15中所描绘,至少部分地通过将成比例比率应用于从粒子计数器获得的单个计数(例如,图18的步骤84)来计算第一类目或亚类目中的粒子的浓度。
417.在一些实施例中,第一类目和/或亚类目的粒子以高于适用于第一类目和/或亚类目的粒子的检测范围的上限的浓度存在于样品中。第二类目和/或亚类目的粒子在适用于第二类目和/或亚类目的粒子的检测范围内存在于样品中。例如,第一类目的粒子包括白血细胞。第二类目的粒子包括血小板。如图19b所示,来自本发明分析仪的粒子计数可用于校正与粒子计数器所用的至少一个检测范围诸如粒子浓度、体积和/或尺寸相关的不准确粒子计数。通过操作如本发明中所述的装置,可准确地检测和测量以高于检测范围的上限的量存在的粒子。
418.在一些实施例中,第一类目和/或亚类目的粒子以低于适用于第一类目和/或亚类目的粒子的某种参数例如浓度的可检测范围的下限存在于样品中,如图19a所示。第二类目和/或亚类目的粒子在适用于第二类目和/或亚类目的粒子的检测范围内存在于样品中。如图19a所示,来自本发明分析仪的两种类目和/或亚类目中的粒子计数的成比例比率可用于校正来自粒子计数器的至少一种类目和/或亚类目的不准确计数。通过操作如本发明中所述的装置,可准确地测量不能通过粒子计数器检测的以低于检测范围限值存在的粒子。
419.如图19a所示,粒子计数器提供类目2的粒子计数。分析仪提供类目1和2的粒子计数的成比例比率。通过将成比例比率乘以类目2的粒子计数,该过程得到类目1的粒子计数。第一类目和/或亚类目的粒子可包括例如血小板。第二类目和/或亚类目的粒子包括白血细胞。根据一些实施例,当样品中所含的血小板数量较低时,本文所公开的动态或检测范围扩展系统和方法可用于获得准确的血小板计数。
420.在一些实施例中,分析仪包括成像设备和连接到成像设备的流通池以测定第一类目和/或亚类目的粒子与第二类目和/或亚类目的粒子的成比例比率。将稀释剂、透化剂、造影剂中的至少一者引入样品中。所述至少一种化学品能有效地产生能区分第一和第二类目和/或亚类目的粒子的视觉区别。在测定此成比例比率的步骤中,将样品施加到存在于一些实施例中的所述至少一个流通池中。捕获样品的粒子的多个图像以提供计数或成比例比率的统计上显著的估计。然后通过对第一和第二类目和/或亚类目的粒子每者中的粒子进行计数,测定所述至少第一类目和/或亚类目的粒子与第二类目和/或亚类目的粒子的成比例比率。
421.在另一方面,如图18和/或图19d中所描绘,提供了用于分析包含粒子的样品的方法80以校正粒子计数器上获得的粒子计数。例如,本发明的来自分析仪的结果例如相对计数可用于获得粒子计数器单独所用的一种或多种检测标准无法区分开的各类目和/或亚类目的粒子的准确粒子计数。
422.在图19c中所示的另一个实施例中,计数器可为多种粒子提供基本上准确的计数。所述多种粒子涵盖至少两种亚类目的成员,但计数无法在亚类目之间区分。可在分析仪上测定所述至少两种亚类目的成员每者的分布。亚类目的分布是各自亚类目的计数与总计数的成比例比率。处理器被程序化以区分所述至少两种亚类目的成员。通过使用来自分析仪的分布和来自粒子计数器的总粒子计数,例如如图19c中所描绘,然后可由处理器通过使用所述成员每者的分布测定所述至少两种亚类目中的至少一者的成员的粒子计数。
423.根据一些实施例,如图19d中所描绘,样品可具有存在的两种类目的粒子。在该上下文中,类目可理解为包括多个类目和/或多个亚类目的可能性。通过操作如本发明中所述的装置,可对粒子的计数进行校正,其中来自至少一种另外类目的粒子的至少一些成员被粒子计数器错误分类或子分类为第一类目的粒子的成员。在此方法中,可使用预定范围例如尺寸和/或体积范围在粒子计数器上提供其粒子计数,从而测定多种粒子的计数。在粒子计数中所述预定范围将第一类目的粒子的成员和至少第二类目的粒子的至少一些成员分组在一起。可使用被配置成区分样品中的粒子在第一类目的粒子和所述至少第二类目的粒子内的分布的分析仪,单独且准确地测量在装置的一个通道中被错误计数为另一种类目的粒子的一种或多种类目或亚类目中的那些粒子。类目和/或亚类目的分布是各自类目和/或亚类目的计数与总计数的成比例比率。处理器然后使用该分布计算第一类目和所述至少第
二类目和/或亚类目的粒子的成员的粒子计数。在该实施例中,如图19d所示,可校正本发明的装置和方法及每种类目和/或亚类目中的粒子的计数。
424.如图19d所示,粒子计数器可提供包含两种类目的基本上准确的总计数。该计数可包括类目1和2的假定计数。然而,该假定计数不准确,因为粒子计数器将类目2的至少一个成员错误分类为类目1。分析仪为类目1和2提供基于比粒子计数器中所用更小的样品的粒子计数的分布,但分析仪产生准确的分布。处理器使用该信息得到这两种类目的准确计数。该相同方法可用于包含不止两种类目和/或亚类目的粒子的样品。
425.例如,具有类似尺寸或形态的不同粒子类目或亚类目的成员可能不能被粒子计数器准确地分类或子分类。例如,“巨大”plt、plt聚集体、团块、多个血小板和有核rbc可能被错误计数为wbc,导致wbc计数高于样品中实际存在的计数。又如,小细胞性红细胞、细胞碎片、伪影和甚至电子噪声可能被错误计数为血小板,导致plt的不准确高计数。
426.在一些实施例中,分析仪是包括成像设备和流通池的视觉分析仪。例如,将包括稀释剂、透化剂、造影剂中至少一者的至少一种化学品引入样品中。所述至少一种化学品能有效地产生能区分第一类目和/或亚类目和第二类目和/或亚类目的粒子的视觉区别。在测定此分布的步骤中,将样品施加到存在于一些实施例中的所述至少一个流通池中。
427.在测定至少两种类目和/或亚类目的粒子的成员每者的分布的步骤中,将样品的至少一部分施加到所述至少一个流通池中。所述至少一种化学品能有效地产生能区分各类目和/或亚类目的粒子的成员的视觉区别。捕获样品的粒子的多个图像。捕获样品的粒子的多个图像以提供计数或成比例比率的统计上显著的估计。然后通过对第一和第二类目和/或亚类目的粒子每者中的粒子进行计数,测定所述至少第一类目和/或亚类目的粒子与第二类目和/或亚类目的粒子的成比例比率。
428.可基于样品的粒子的多个图像来测定两种或更多种亚类目的粒子每者的成员在一种类目和/或亚类目的粒子内的成比例比率、和/或第一类目和/或亚类目的粒子的成员与至少一种其他类目和/或亚类目的粒子的成员的成比例比率。然后可计算、估计、推测和/或导出每种类目和/或亚类目的粒子的计数或浓度值。例如,可基于来自分析仪的每种类目的粒子的成比例比率以及来自粒子计数器的该类目中的粒子的总数的计数,来测定各亚类目的粒子的浓度。在一些实施例中,所述至少两种亚类目的成员包括选自以下亚类目的至少一种类型的粒子:白血细胞、血小板和红血细胞。
429.因此,在一些实施例中,所述方法还包括基于来自分析仪和/或处理器的样品的粒子的多个图像,测定以适用于粒子计数器的一种类目的粒子的检测范围之外的浓度存在的所述一种类目和/或亚类目的粒子中的粒子的计数与在适用于第二类目和/或亚类目的粒子的检测范围内的第二类目和/或亚类目的粒子中的粒子的计数的成比例比率。然后可通过将成比例比率应用于粒子计数器上获得的粒子计数,测定在粒子计数器的检测范围之外的所述类目和/或亚类目的粒子在样品中的浓度。例如,在一些实施例中,第一类目和/或亚类目的粒子以高于适用于第一类目和/或亚类目的粒子的检测范围限值的上限的浓度存在于样品中。第二类目和/或亚类目的粒子在适用于第二类目和/或亚类目的粒子的粒子计数器的检测范围内(低于检测范围的上限并高于检测范围的下限)存在于样品中。又如,当粒子计数器所用的一种或多种检测标准通过将第一类目和/或亚类目的粒子与至少第二类目和/或亚类目的粒子分组在一起而错误分类粒子时,可由根据来自视觉分析仪和/或处理器
的样品的粒子的多个图像所测定的粒子的成比例比率来校正第一和第二类目和/或亚类目的粒子计数。
430.测量值的检测范围在图15中单独的粒子计数器15上可能受到限制。例如,wbc的检测上限在粒子计数器15上可能小于100,000至200,000个/μl。plt的检测下限可能高于10,000个/μl。通过使用本文所述的装置,可扩展测量值的有效检测范围,例如在一些实施例中wbc的检测上限可扩展最多至约300,000、350,000、400,000、410,000、420,000、430,000、440,000、450,000、460,000、470,000、480,000、490,000、500,000、510,000、520,000、530,000、540,000、550,000、560,000、570,000、580,000、590,000、600,000、610,000、620,000、630,000、640,000、650,000、660,000、670,000、680,000、690,000、700,000、710,000、720,000、730,000、740,000、750,000、760,000、770,000、780,000、790,000、800,000、810,000、820,000、830,000、840,000、850,000、860,000、870,000、880,000、890,000、900,000、910,000、920,000、930,000、940,000、950,000、960,000、970,000、980,000、990,000、或1,000,000、1,000,000、1,010,000、1,020,000、1,030,000、1,040,000、1,050,000、1,060,000、1,070,000、1,080,000、1,090,000、1,100,000、1,110,000、1,120,000、1,130,000、1,140,000、1,150,000、1,160,000、1,170,000、1,180,000或约1,190,000个细胞/μl、或这些值中任何两者之间的任何范围。在一些实施例中plt的检测下限可扩展低至10,000、9,500、9,000、8,500、8,000、7,500、7,000、6,500、6,000、5,500、5,000、4,500、4,000、3,500、3,000、2,500、2,000、1,500或1,000、或500、400、300、200、或100个细胞/μl。
431.分析仪优选地包括视觉分析仪17,所述视觉分析仪可操作以测定第一类目和/或亚类目的粒子与第二类目和/或亚类目的粒子的成比例比率。在该实施例中,可通过分析视觉分析仪17上拍摄的样品中的粒子的多个图像来测定如上所述的成比例比率。
432.视觉分析仪17可被配置成向样品中引入包括稀释剂、透化剂和/或造影剂中至少一者的至少一种化学品以产生用于粒子分类和/或子分类的视觉区别。此类视觉区别将所述至少两种类目的成员区分开。捕获样品的粒子的图像。视觉分析仪17和处理器18被配置成通过区分样品的粒子的图像来测定每种类目或亚类目的粒子的成比例比率。然后计算每种类目或亚类目的粒子的浓度。例如,可测定wbc、巨大plt和nrbc的准确结果。在粒子计数器上,由于类似的尺寸或形态,巨大plt和nrbc被计数为wbc。通过操作如所述的装置,可准确地报告巨大plt和nrbc的粒子计数或浓度。
433.在一些实施例中,样品可包含尺寸在粒子计数器15的检测尺寸范围之外的粒子。视觉分析仪17和处理器18被配置成检测粒子并且基于样品的粒子的图像来测定粒子计数器15的检测尺寸范围之外的粒子与检测尺寸范围之内的粒子的成比例比率。然后可计算在粒子计数器15的检测尺寸范围之外的该类目和亚类目的粒子的浓度。
434.一般来讲,提供了用于分析包含粒子的样品的方法以校正粒子计数器上获得的粒子计数。示例性方法可用于区分不同类目的粒子,包括属于粒子计数器15上的相同类目和/或亚类目的粒子的对应亚类目,例如如图14和15中所描绘。所述方法可用于校正粒子计数器15中获得的粒子计数。在一些实施例中,例如,第一类目和/或亚类目的粒子包括异常血细胞、未成熟血细胞、成团血细胞或异常尺寸的血细胞中的一种或多种类型。第二类目和/或亚类目的粒子包括白血细胞。通过操作如本文所述的装置,可通过分析仪区分各亚类目中的粒子,并且可校正由粒子计数器获得的各类目和/或亚类目的粒子的计数。
435.将样品或其部分提供于粒子计数器15上以检测粒子并且基于可涵盖至少两种类目的粒子的亚类目的一种或多种选择标准提供粒子计数。例如,来自粒子计数器的所声称wbc类目也可包含少量巨大plt和nrbc。来自粒子计数器的该类目还可包含不能被粒子计数器区分的各亚类目的白血细胞。如下所述也可在视觉分析仪上分析样品的另一部分以分辨这些错误分类和/或对未经区分的wbc亚类目进行子分类。
436.可在如图14中所描绘的分析仪17上测定所述至少两种亚类目或类目每者的分布。此分布可以数值比率、成比例比率和/或相对计数的其他函数呈现。在一些实施例中,可根据本文所公开的方法在包括流通池22和成像设备24的视觉分析仪17上测定此分布。如所述,可将样品12a(可为样品的一部分)施加到所述至少一个流通池22。将包括稀释剂、透化剂和造影剂中至少一者的至少一种化学品引入样品12a中。包括稀释剂、透化剂和造影剂中至少一者的所述至少一种化学品能有效地产生能区分所述至少两种类目的粒子并区分所述至少一种类目的粒子的所述至少两种亚类目的视觉区别。捕获样品12b的粒子的多个图像。在视觉分析仪17和/或处理器18上进行图像分析。
437.在一些实施例中,处理器18被程序化以区分所述至少两种类目和/或亚类目的成员。可基于样品的粒子的多个图像,测定所述至少两种亚类目或类目的粒子每者中的粒子的计数的成比例比率。然后可在处理器18上通过使用亚类目每者的分布来校正由粒子计数器15获得的所述至少两种类目中至少一者的亚类目的粒子计数。可基于每种亚类目的粒子的成比例比率以及由粒子计数器获得的该类目粒子的粒子计数,在处理器18上计算每种亚类目的粒子的浓度。
438.根据一些实施例,本文所公开的方法还可用于区分在粒子计数器15的检测范围之外的一种或多种类型的粒子。例如,这些粒子可为血细胞或其他碎片,对于在粒子计数器15上检测而言它们不是太大就是太小。在视觉分析仪17上,可基于样品的粒子的多个图像,测定在粒子计数器的检测范围之外的一种类型的粒子与在粒子计数器的检测范围之内的另一种类型的粒子的计数的成比例比率。然后可通过至少部分地将成比例比率应用于粒子计数器15上获得的粒子计数,测定样品中在检测范围之外的该类型粒子的浓度。
439.聚焦图像
440.图20a和20b提供了根据本发明实施例的截面侧视图,其示出了成像系统和方法的各方面。参照图20a,粒子分析系统1400a诸如血液学分析仪可被配置用于组合式粘度和几何流体聚焦,例如使用流通池和粘性鞘液技术诸如共同待审的美国专利申请_____中所述的那些,所述专利的内容以引用方式并入本文中。使用粒子分析系统使血液流体样品中的粒子成像的示例性方法可包括使鞘液1410a沿着粒子分析系统的流通池1430a的流路1420a流动。流路1420a可至少部分地由流通池的相对流通池壁1422a、1424a限定。鞘液1410a可具有与血液流体样品的粘度不同的粘度。成像方法还可包括将血液流体样品注射到流通池1430a内的流动鞘液1410a中,以使得血液流体样品流体在样品流动料流1440a中流动。样品流动料流1440a可具有大于流动料流厚度的流动料流宽度。样品流动料流1440a也可流过流路尺寸的缩减段并横穿成像轴1450a。在图20a图示中,流动的方向为从左到右。
441.另外,通过使具有相对于流通池1430a固定的位置的成像靶标1470a成像来使图像捕获设备1460a聚焦。例如,如此处所描绘,成像靶标1470a可具有相对于流通池的照明窗口1480a固定的位置。在一些情况下,成像靶标1470a可嵌入窗口1480a内或固定在窗口1480a
上。方法也可包括用图像捕获设备1460a采集样品流体的粒子(例如,至少部分地设置在流动料流1440a内的粒子1490a)的聚焦图像。聚焦图像适用于粒子表征和计数。
442.可使用位移距离使图像捕获设备1460a聚焦于样品流动料流1440a。例如,位移距离可对应于样品流动料流1440a与成像靶标1470a之间的距离d。鞘液1410a与血液流体样品之间的粘度差连同流路尺寸的缩减段能有效地在成像轴1450a处流体聚焦样品流动料流1440a中的样品流体,同时保持血液流体样品中的细胞的活力。例如,与粘度差相关的鞘液1410a和样品流体料流1440a之间的相互作用所引起的粘度流体聚焦作用连同与流路尺寸的缩减段相关的鞘液1410a和样品流体料流1440a之间的相互作用所引起的几何流体聚焦作用可有效地在成像轴1450a处在流体样品粒子的至少一些中提供靶标成像状态,同时鞘液1410a中的粘度剂保持样品流体料流1440a中细胞的活力,使得细胞从样品流体料流1440a延伸到流动鞘液1410a中时细胞的结构和内容物完好无损。
443.当使用位移距离使图像捕获设备1460a聚焦于样品流动料流1440a时,图像捕获设备1460a可在成像轴1450a处或在与成像轴1450a相关的图像捕获位点处获得样品流动料流1440a内的粒子或细胞的图像。在一些情况下,可用照明源或灯1426a照明粒子。可在粒子接近成像轴1450a时,在粒子横越成像轴1450a时和/或在粒子远离成像轴1450a流动时,获得样品流动料流1440a的图像。
444.图20b描绘了替代流通池构形的各方面,其中成像靶标1470b具有相对于流通池1430b的观察口窗口1482b固定的位置。例如,成像靶标1470b可嵌入窗口1482b内或固定在窗口1482b上。如此处所示,成像方法可包括通过使具有相对于流通池1430b固定的位置的成像靶标1470b成像来使图像捕获设备1460b聚焦。此外,可使用位移距离使图像捕获设备1460b聚焦于样品流动料流1440b。例如,位移距离可对应于样品流动料流1440b与成像靶标1470b之间的距离d。
445.图20c描绘了流通池1430c的截面端视图,示出了自动对焦或成像靶标的各自替代设置位置。例如,成像靶标1472c可位于流通池1430c的观察口窗口1482c。任选地,成像靶标1474c可位于流通池1430c的照明窗口1480c。还任选地,成像靶标1476c可位于侧向流通池壁(例如,1432c和/或1434c)中。可使用位移距离使图像捕获设备1460c聚焦于样品流动料流1440c,所述样品流动料流包围在鞘液1410c内。在一些实施例中,位移距离可对应于沿着成像轴1450c在样品流动料流1440c(或由流动料流1440c限定的中心平面1441c)与观察口窗口成像靶标1472c之间的距离d1或由该距离限定。在一些实施例中,位移距离可对应于沿着成像轴在样品流动料流1440a(或中心平面1441c)与照明窗口成像靶标1476c之间的距离d2或由该距离限定。在一些实施例中,位移距离可对应于沿着成像轴在样品流动料流1440a(或中心平面1441c)与流通池侧壁成像靶标1474c之间的距离d3或由该距离限定。在一些情况下,距离d3具有大于零的值。在一些情况下,距离d3具有零的值;即,样品流动料流1440a(或中心平面1441c)与成像靶标1474c共面的情形。在一些情况下,可以限定不基于距离d1、距离d2或距离d3计算的位移距离。例如,位移距离可为由流通池或血液学分析仪制造商提供的预定数或值。
446.根据一些实施例,样品流动料流1440c在成像轴处可具有约2μm至约10μm范围内的厚度t1。在一些情况下,流路或鞘液1410c在成像轴处可具有约150μm的厚度t2。如此处所示,成像靶标1472c可位于观察口窗口1482c上,所述观察口窗口设置在样品流动料流1440c
与图像捕获设备1460c之间。在一些情况下,成像靶标(例如,1474c)可位于照明窗口1480c与观察口窗口1482c之间。如本文别处所讨论,采集聚焦图像的方法可包括使用位移距离调节图像捕获设备1460c与流通池1430c之间的距离。在一些情况下,如本文别处所讨论,采集聚焦图像的方法可包括使用位移距离调节图像捕获设备1460c的焦距。在一些情况下,采集聚焦图像的方法可包括调节图像捕获设备1460c与流通池1430c之间的距离,并且调节距离的方法包括将流通池1430c移动到例如更靠近图像捕获设备1460c的位置,或离图像捕获设备1460c更远的位置。
447.如图20d中所描绘,图像捕获设备1460d的第一焦距可对应于图像捕获设备1460d与成像靶标1470d之间的距离d1(例如,沿着成像轴1450d),并且图像捕获设备1460d的第二焦距可对应于图像捕获设备1460d与样品流动料流1440d(或由样品流动料流限定的中心平面)之间的距离d2(例如,沿着成像轴1450d)。在一些情况下,成像靶标可位于流通池中的另一个位置,例如如图20c中所描绘。根据一些实施例,位移距离可对应于第一焦距(或距离d1)与第二焦距(或距离d2)之间的距离差。可使用该位移距离(例如,d1与d2之间的差值)使图像捕获设备1460d聚焦于样品流动料流1440d。
448.图21描绘了正视图,示出了自动对焦光栅(或成像靶标)的实施例,所述自动对焦光栅(或成像靶标)例如可位于照明孔口或窗口上、观察口或窗口上,或位于另一流通池位置。随着高光学分辨率成像设备的距离或位置相对于带形样品料流移动,靶标可逐渐变弱。如图9
‑
12b中所描绘,成像或聚焦靶标(自动对焦光栅)可位于将出现样品的视区的周边。返回参照图21,可以看出还可能的是,聚焦靶标可由位于视野中的对比形状限定。
449.当成像设备聚焦于自动对焦光栅(靶标)(图21中的图b)时,如由设备成像的形状被明确限定并且可用于如本文所述的自动对焦,即寻找靶标与成像设备之间的距离,在该距离处,在沿着与所述形状交叉的线(诸如如箭头所示的线)定位的相邻像素之间所述形状产生幅度上的最高对比度。图b中所描绘的焦点配置对应于图22a中所描绘的类似焦点配置。如图22a所示,图像捕获设备的焦平面与自动对焦靶标配向,并且因此图像捕获设备处于适当位置以获得自动对焦靶标的清晰图像。
450.返回参照图21,当例如通过调节物镜的工作距离或物镜与其焦平面之间的距离使工作位置(例如,成像设备的焦平面)远离自动对焦光栅(在图21中的自动对焦光栅的左侧和右侧所示的图a和c中示出)移动时,聚焦靶标形状当前偏离焦点,并且在高光学分辨率成像设备聚焦于带形样品料流的位置处,聚焦靶标形状完全不再能分辨(参见图21中的图d)。图d中所描绘的焦点配置可对应于图22b中所描绘的类似焦点配置。如图22b所示,图像捕获设备的焦平面与样品流体料流配向,并且因此图像捕获设备处于适当位置以获得样品流动料流中的粒子的清晰图像。图22a的焦平面与图22b的焦平面间隔距离d。如图22b所示,通过将图像捕获设备移动距离d,可以也将焦平面移动距离d,并且因此将焦平面从自动对焦靶标移动到样品流动料流。在一些情况下,可通过内部调节图像捕获设备的焦距同时保持图像捕获设备处于相对于流通池的固定位置,使焦平面从自动对焦靶标移动到样品流动料流。在一些情况下,可通过内部调节图像捕获设备的焦距同时调节图像捕获设备相对于流通池的位置,使焦平面从自动对焦靶标移动到样品流动料流。自动对焦形状可提供于视野内且相对于流通池固定的任何位置处,诸如在照明开口或窗口上、或在穿过其引导高光学分辨率成像设备的观察口或窗口的前方或后方、或在附接到光电管以保持靶标处于待成像
的位置的夹具处。
451.根据一些实施例,当高光学分辨率成像设备在位移距离内移动并且自动对焦光栅偏离焦点时,出现在焦点内的特征是血细胞而非自动对焦光栅。在图21的实施例中,自动对焦光栅由视野中的形状限定。所述形状为有限尺寸的相对薄的离散形式,并且因此在移动位移距离之后,当聚焦于带形样品料流时所述形式在数字化图像中基本上不可见。在尺度适合血液学(血细胞)成像应用的流通池中,典型的位移距离可为例如50至100μm。在一些实施例中,自动对焦特征保持高光学分辨率成像设备处于最佳焦点距离的1μm内。
452.因此,图21中所述的特征提供用于测定位移距离的示例性技术。例如,测定位移距离的方法可包括自动对焦过程,所述自动对焦过程涉及将测试流体样品注射到鞘液中以形成流通池内的测试样品流动料流,以及使用图像捕获设备获得成像靶标的第一聚焦图像。第一聚焦图像可对应于图21中的图b,其中聚焦成像靶标和图像捕获设备限定第一焦距。如此处所描绘,图像捕获设备的焦平面或工作距离/位置定位在成像靶标处。自动对焦过程也可包括使用图像捕获设备获得测试样品流动料流的第二聚焦图像。第二聚焦图像可对应于图21的图d,其中聚焦测试样品流动料流和图像捕获设备限定第二焦距。如此处所描绘,图像捕获设备的焦平面或工作距离/位置定位在成像靶标处。自动对焦过程还可包括通过计算第一焦距与第二焦距之间的差值来获得位移距离。在一些情况下,测试流体样品与血液流体样品相同并且测试样品流动料流与样品流动料流相同。在一些情况下,自动对焦过程建立与图像捕获设备相关的焦平面,并且焦平面相对于图像捕获设备保持静止。在一些情况下,自动对焦图像捕获设备的过程包括从多个焦点位置中确定最佳焦点位置。
453.根据一些实施例,可在不使用温度数据的情况下使图像捕获设备聚焦于样品流动料流。例如,图像捕获设备聚焦于样品流动料流的过程可独立于图像捕获设备的温度进行。在一些情况下,成像靶标可包括用于将图像捕获设备的成像轴相对于样品流动料流定位的刻度(例如,如图12b中所描绘)。在一些情况下,成像靶标可包括相对于成像轴配向的光圈,使得成像粒子设置在由光圈限定的孔内,并且在自动对焦期间使光圈的一个或多个边缘部分成像。
454.在示例性实施例中,自动对焦技术可将流通池定位在离样品料流的最佳焦点位置的
±
1μm内。在一些情况下,实施例涵盖这样的自动对焦技术,其可自动地使成像系统聚焦而不需要单独的聚焦液体或溶液或任何用户干预。示例性自动对焦技术也可考虑次优聚焦性能的机械原因,诸如漂移或热膨胀,其可造成成像设备物镜与流通池之间的距离的波动。在一些情况下,据观察样品流在流通池内的位置可以非常稳定并且与温度无关。因此,示例性成像技术可涉及聚焦于流通池中的成像靶标,以及使用固定偏移量实现对样品料流的最佳聚焦。
455.根据一些实施例,成像系统上使用的显微镜物镜具有0.75的数值孔径,产生
±
0.5μm的理论视野深度(dof)。在某些实验性尝试中,据观察可在离最佳焦点
±
1.25μm处获得良好图像质量。还据观察,实际或实验视野深度可与理论视野深度不同。例如,在某些实验性尝试中,据观察,视野深度为约2.5至3μm。根据某些实验研究,已确定用于将流通池定位在
±
1.25μm内的自动对焦性能可确保良好图像质量。在一些实施例中,自动对焦系统可操作以将流通池定位在离样品料流的最佳焦点位置的
±
1μm内。在某些实验性尝试中,据观察如本文所公开的自动对焦技术可重复地定位流通池中的靶标,且标准偏差小于0.3μm。在一些
情况下,试验自动对焦系统运行证实了出色的可重复性(标准偏差≤0.23μm)并且能够确定样品料流的焦点位置在离优化度量位置<0.6μm内,所述优化度量位置在
±
1μm位置公差内。在各种温度条件下的另外自动对焦试验运行也表现出出色的定位性能(例如,流通池定位在最佳焦点位置的所需
±
1μm公差内)。自动化分析仪系统的该准确程度非常适于一致地且可靠地从如本文别处所公开的薄带流动料流中流动的血液流体样品在对应于标准实验条件的操作温度范围内获得粒子的高质量图像。
456.图23描绘了根据本发明实施例的样品处理方法2300的各方面。如此处所示,样品处理方法可包括将样品抽吸到剪切阀门中,如步骤2305所指示。该步骤可由cbc模块执行。方法也可包括将样品和试剂分配到反应室中,如步骤2310中所描绘。该步骤可由cbc模块和第一射流系统(例如,bbl1射流)执行。此外,方法可包括将反应混合物在所需温度下温育所需持续时间(例如,在47.5℃下温育40秒),如步骤2315所指示。方法也可包括将猝灭试剂分配到反应室中,如步骤2320所指示;将反应混合物抽吸到成像准备区段中,如步骤2325所指示;以及切断空气/液体界面并且将样品推动到流通池中,如步骤2330所指示。根据一些实施例,步骤2315、2320、2325和2330可由射流系统(例如,bbl射流)执行。根据一些实施例,方法可包括采集图像,如步骤2335中所指示。例如,成像采集过程可包括采集5000
‑
7000个帧,并且可将图像保存在视频文件中。在一些情况下,步骤2335可由视频系统(例如,bbl视频)执行。而且,方法可包括执行每个帧的面片提取,从而产生图像的集合,如步骤2340所指示;产生5部分分类或其他诊断结果文件,如步骤2345所指示;以及对每个面片/细胞分类,如步骤2350所指示。在一些情况下,可使用血液学自动化粒子识别(apr)软件通过离线处理来执行步骤2340、2345和2350。
457.pioal具有合适的粘度和密度,并且在样品引入流通池时的流速使得样品流体变平为薄带。带形样品料流与pioal一起被输运,以在观察口的前方通过,其中物镜镜头和光源被布置成允许观察带形样品料流。将样品流体引入,例如,在pioal的流路对称变窄的点处注射。因此,样品流体料流变平并伸展成薄带。本发明的pioal可作为鞘液与本发明的任何视觉分析仪一起使用。在一个实施例中,可将pioal引入流通池的末端以沿着样品流体向排放口输运。
458.观察区中的带形样品料流的尺度受pioal流路的几何变薄以及样品流体和pioal的差异线速度(导致带形样品料流的变薄和伸展)的影响。样品与pioal的初始差异线速度可在0.5:1至5:1的范围内。pioal流路横截面可通过降低深度而变薄约10:1、15:1、20:1、25:1、30:1、35:1、40:1、45:1、50:1、55:1、60:1、65:1、70:1、75:1、80:1、85:1、90:1、95:1、100:1、105:1、110:1、115:1、125:1、130:1、140:1、150:1、160:1、170:1、180:1、190:1或200:1的因子。在一个实施例中,几何变薄为40:1。在一个实施例中,几何变薄为30:1。所考虑的因素为流过流通池的通过时间,所需的样品通量率,实现与粒子尺寸相当的带形样品料流厚度,获得粒子和细胞器的配向,实现粒子的焦点内内容物,在操作限值内平衡压力、流动和粘度,优化带形样品料流厚度,获得所需的线速度,可制造性考量,以及所需的样品和pioal体积。
459.可对插管的长度和体积以及横截面变平进行选择以缩短样品流动不稳定的时期,从而增大通量。在一些实施例中,流动不稳定的时期可短于约3、2.75、2.5、2.25、2、1.75、1.5、1.25或短于约1秒。较小的插管体积也可缩短所述时间并减小在样品运行之间清洗插
管所需的稀释剂的体积。在一些实施例中,流过流通池的通过时间为1、2、3或4秒,或那些时间中任何两个之间的任何范围。在一些实施例中,该通过时间可短于4、3或2秒。
460.样品流体和pioal的粘度和流速以及流通池的轮廓被布置成使得pioal流变平并将样品流伸展成平带,所述平带在对应于图像捕获位点的可靠位置一致地穿过观察区。样品流体料流可被压缩成约2至3μm的流体流厚度。若干血细胞类型都具有大于料流厚度的直径。在平行于流动方向的方向上的剪切力导致在成像条件下在高光学分辨率成像设备的焦平面中粒子的图像投影增加和/或导致粒子内结构(例如,细胞内结构、细胞器或裂片)定位、重定位和/或更好地定位成基本上平行于流动方向。高光学分辨率成像设备视野深度为最多7μm,例如1
‑
4μm。
461.与带形样品料流一起输运的pioal的流动横截面始终穿过观察口(物镜镜头被引导穿过其中)前方的观察区。物镜镜头可以是高光学分辨率成像设备或数字图像捕获设备的物镜组件。带形样品料流在流通池内的已知且可重复的位置处(例如,在离流通池的两个壁的已知且可重复的距离处)顺着横跨观察区的路径流动,并在下游排放。
462.当带形样品料流被输运穿过观察口前方的观察区时,来自样品中的粒子的光学信息通过分析仪中的检测段检测,从而生成样品中所含粒子/细胞的数据。使用该分析仪允许对样品中所含的细胞和/或粒子进行捕获、处理、分类及子分类和计数。pioal液体可通过添加粘度改性剂、缓冲剂、ph调节剂、抗微生物剂、离子强度改性剂、表面活性剂和/或螯合剂而制备。本发明中的分析仪的示例性功能组件和/或特征可包括例如采集和/或处理来自图像分析的数据、样品染色处理、图像处理和/或粒子图像鉴定、计数和/或分类及子分类的能力。
463.在一个实施例中,本发明基于以下出奇且意外的发现:在pioal中添加适量的粘度剂明显改善流通池中的粒子/细胞配向,从而使配向细胞或处于焦点内的细胞组分的百分比更高,以及使流动中的细胞和/或粒子的图像的质量更高。粘度差连同变窄过渡区的几何聚焦作用可实现增强的配向和聚焦结果。添加粘度剂增加对细胞(如rbc)的剪切力,这改善在基本上平行于流动方向的平面中的细胞配向,从而导致图像优化。这还导致粒子内结构(诸如细胞内结构、细胞器或裂片)基本上平行于流动方向而定位、重定位和/或更好地定位,从而导致图像优化。粘度剂还减少细胞的失准,所述细胞通常为但不限于直径比流动料流小的细胞。
464.直径比流动料流小的细胞(例如,红血细胞)的配向可通过例如增大pioal的粘度或通过增大流速比而获得。这导致rbc平行于流动方向并平行于焦平面fp配向(例如,如图4k中所描绘)。在一些实施例中,rbc失准的减少和/或rbc配向的增加通过增大pioal的粘度而实现。
465.带形样品料流厚度可受样品流体和pioal的相对粘度和流速的影响。样品源和/或pioal源(例如,包括精密排量泵)可被配置成以受控的流速提供样品和/或pioal以优化带形样品料流的尺度,即作为至少与高光学分辨率成像设备或数字图像捕获设备的视野一样宽的薄带。
466.与带形样品料流一起输运的pioal的流动横截面始终穿过观察口(高光学分辨率成像设备被引导穿过其中)前方的观察区。带形样品料流在离流通池前壁和后壁任一者的已知且可重复的距离处顺着横跨观察区的路径流动,并在其下游排放。
467.本发明提供自动实现高光学分辨率成像设备的正确工作位置以对带形样品料流聚焦的技术。流通池结构被配置成使得带形样品料流在限定样品流体的流路的流通池壁之间具有固定且可重复的位置,以pioal层之间的薄带形式穿过流通池中的观察区。在例如图1
‑
4g中所公开的流通池实施例中,pioal的流路的横截面可在过渡区对称变窄,并且样品可插入平坦的孔口,诸如在孔口具有矩形内腔的管。变窄流路(例如,以20:1至40:1的比率在横截面积上几何变窄)并且还由于与样品流相比任选地更大的pioal线速度配合使样品横截面以约20:1至70:1的比率变平。根据一些实施例,该比率可在10:1至100:1的范围内,在50:1至100:1的范围内,在70:1至80:1的范围内。根据一些实施例,该比率为75:1。有效地,由于流速、粘度和几何形状的组合,样品形成薄带。变窄流路(例如,以40:1的比率或以20:1至70:1的比率在横截面积上几何变窄)以及与样品流相比的pioal的线速度差配合使样品横截面以约20:1至70:1的比率压缩。在一些实施例中,该横截面厚度比率可为40:1。在一些实施例中,该横截面厚度比率可为30:1。
468.因此,方法变量(诸如样品和pioal的特定线速度)不会倾向于使带形样品料流从其流动位置发生位移。相对于流通池的结构,带形样品料流位置是稳定且可重复的。
469.在另一方面,本发明涉及包括本发明的粒子造影剂组合物的试剂盒。该试剂盒还可以包括根据本文所述的任何方法的粒子造影剂组合物的使用说明。该试剂盒还可以包括粒子和/或细胞内细胞器配向液(pioal)。该试剂盒还可以包括可编程的存储介质和用于诸如以下粒子的基于图像的鉴定的相关软件:中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞、嗜碱性粒细胞、血小板、网织红细胞、有核rbc、母细胞、早幼粒细胞、中幼粒细胞、晚幼粒细胞、细菌、真菌、原生生物、原生动物或寄生生物。该试剂盒还可以包括一种或多种缓冲剂,其可以包括等渗缓冲剂和/或稀释剂。该试剂盒和/或缓冲剂还可以包括表面活性剂、ph调节剂和/或抗微生物剂。在其他实施例中,该试剂盒还可以包括清洗溶液或冲洗溶液。该试剂盒还可以包括阳性和阴性对照的标准品。在一些实施例中,该标准品可以包括标准染色细胞试剂。该试剂盒还可以包括一次性用品,诸如用于转移试剂盒组分的一次性微量移液器、移液头或试管。该试剂盒可以包括这些试剂盒组分中的任一种,或两种或更多种的任何组合。
470.区分血样中的血细胞是本发明实施例尤其适合的示例性应用。样品通过自动化技术制备并作为薄带形样品料流呈递给高光学分辨率成像设备,以在带形样品料流流经视野的同时周期性地成像。粒子(诸如血细胞)的图像可用像素图像数据编程的处理技术完全自动地或以有限的人工辅助而彼此区分、分类、子分类和计数,以识别和计数细胞或粒子。除了可以存储并使得就粒子的不寻常或关键特征而言可用的细胞图像之外,输出数据还包括在所记录的样品图像中区分的各特定分类和/或子分类的细胞或粒子的出现次数。
471.存在于各图像中的不同粒子的计数可进一步处理,例如用于作为一个整体而累积样品中各区分分类和/或子分类的细胞的准确且统计上显著的比率。用于视觉辨别的样品可进行稀释,但在稀释的样品中各分类和/或子分类中的细胞的比例依旧,特别是在处理多个图像之后。
472.本文所公开的设备、组合物和方法可用于基于视觉区别而辨别和定量样品中的细胞。样品可以为生物样品,例如包含白血细胞的体液样品,包括但不限于血液、血浆、骨髓、灌洗液、积液、渗出液、脑脊髓液、胸膜液、腹膜液和羊水。在一些实施例中,样品可以为实体
组织样品,例如,已进行了处理而产生细胞悬液的活检样品。样品也可以为通过处理粪便样品而得到的悬液。样品也可以为包含粒子的实验室或生产线样品,诸如细胞培养样品。术语样品可用于指代得自患者或实验室或其任何级分、部分或等分试样的样品。样品可进行稀释、分成多个部分或在一些过程中进行染色。
473.在一个方面,本发明的系统、组合物和方法提供流动中的细胞的出奇高质量的图像。在一个方面,视觉分析仪可用于本发明的方法以提供自动化的基于图像的wbc分类计数。在某些实施例中,本发明的方法涉及视觉区别(包括形态特征和/或异常)的自动化识别,以用于确定、诊断、预后、预测和/或支持对受试者是健康还是具有疾病、病症、异常和/或感染和/或对治疗有响应还是无响应的诊断。该系统在一些实施例中还可以包括粒子计数器。应用包括分类和/或子分类,以及对流体样品(诸如血样)中的细胞计数。也设想了用于对另外类型的粒子和/或其他流体样品中的粒子计数的其他类似的用途。本发明的系统、组合物和方法可用于采用任何合适的自动化粒子识别算法进行实时分类及子分类以及图像观察。可存储各样品的捕获图像以日后观察。
474.在另一方面,本发明的设备、组合物和方法提供出奇更准确的基于图像的细胞分类及子分类和标记,与使用目前的自动分析仪时的人工复核率相比,所述标记降低人工复核率。所述系统、组合物和方法降低人工复核率并允许在仪器上进行人工复核。此外,本发明的系统、组合物和方法还降低在自动分析期间标记的需要人工复核的样品的百分比。
475.本发明还涉及用于将全血细胞计数(cbc)计数器与分析仪(诸如视觉分析仪)相结合的系统、方法和组合物,以便得到cbc以及基于图像的扩展白血细胞分类计数和基于图像的扩展血小板计数,从而延伸血小板计数的有效检测范围。
476.因此,在一些实施例中,本发明提供用于分析包含粒子(例如,血细胞)的样品的设备和方法。根据本发明,提供视觉分析仪以获得包含悬浮在液体中的粒子的样品的图像。在一些实施例中,视觉分析仪包括流通池和自动对焦部件,其中使包含所关注粒子的液体样品流过具有观察口的流通池,而耦合到物镜镜头的相机通过所述观察口捕获粒子的数字图像。可使用本发明的实施例实施的示例性自动对焦技术在共同待审的美国专利申请no.____中有所公开,该专利申请的内容以引用方式并入本文。流通池耦合到样品流体源,诸如经稀释和/或处理的血样或如本文所述的其他体液样品,并耦合到透明鞘液或粒子和/或细胞内细胞器配向液(pioal)源。
477.在一个实施例中,所述设备还包括具有至少一个检测范围的粒子计数器,以及分析仪和处理器。所述分析仪和处理器被配置成提供另外的信息以纠正与粒子计数器相关的计数、分类和子分类误差,并且还确定样品中不同分类和/或子分类的粒子的准确粒子计数或浓度。
478.本发明在进行基于图像的样品分析中提供可用于粒子和/或细胞内细胞器配向的方法和组合物。在一些实施例中,本发明涉及用于组合式计数和成像系统的方法和组合物,该系统能够执行全血细胞计数(wbc)和基于图像的扩展白血细胞(wbc)分类,而能够鉴定细胞类型并进行计数,诸如wbc、rbc和/或血小板,包括例如中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞、嗜碱性粒细胞、网织红细胞、有核rbc、母细胞、早幼粒细胞、中幼粒细胞或晚幼粒细胞,并提供wbc计数和形态、红血细胞(rbc)计数和形态以及血小板(plt)计数和形态的基于图像的信息。
479.在其他实施例中,本发明涉及可用于如本文所述的基于图像的粒子分析的pioal。血样中的细胞分类和/或子分类计数在本发明中用作可以分析的样品的分类的非限制性例子。在一些实施例中,存在于样品中的细胞还可以包括细菌或真菌细胞以及白血细胞、红血细胞和/或血小板。在一些实施例中,可分析从组织或抽吸物获得的粒子悬浮液。
480.辨别血样中的血细胞是主题特别适合的示例性应用。将样品通过自动化技术制备并以带形样品料流形式呈递给高光学分辨率成像设备以在样品流过视野时使其周期性地成像。可使用像素图像数据程序化处理技术仅仅自动地或在有限人工辅助的情况下将粒子(诸如血细胞)的图像彼此区分开、分类、子分类和/或计数,以识别和计数细胞或粒子。除了细胞图像(其可在异常或关键特征的情况下存储和供使用)之外,输出数据包括所记录样品图像中区分开的每种特别类目和/或亚类目的细胞或粒子的事件的计数。可进一步处理存在于每个图像中的不同粒子的计数,例如用于积累整体样品中每种区分开的类目和/或亚类目的细胞的准确且统计上显著的成比例比率或其函数。也可高度稀释用于视觉区别的样品,但在稀释样品的分布中每种类目和/或亚类目中的细胞的比例依旧,特别是在已处理多个图像后。
481.在一些方面,样品以自动方式呈递、成像和分析。就血样而言,可用合适的稀释剂或盐水溶液充分稀释样品,所述稀释剂或盐水溶液降低了未稀释或稀释度较低的样品中一些细胞的视线可能被其他细胞遮挡的程度。可用增强一些细胞方面的对比度的试剂来处理细胞,例如使用透化剂使细胞膜具有透性以及使用组织学染液粘附于结构中并显示结构,诸如颗粒和细胞核。在一些实施例中,可能有利的是,对样品的等分试样进行染色以用于对包括网织红细胞、有核红血细胞和血小板的粒子进行计数和表征,以及用于白血细胞分类、表征和分析。在其他实施例中,包含红血细胞的样品可在引入流通池并成像之前进行稀释。
482.根据一些实施例,用于样品稀释、透化和组织学染色的样品制备装置和方法的详情一般使用由一个或多个可编程控制器操作的精密泵和阀门来实现,并且不是本发明的重点。例子可见于转让给国际遥感成像系统公司(international remote imaging systems,inc.)的专利,诸如关于可编程控件的us 7,319,907。同样,用于按照其属性诸如相对尺寸和颜色区分某些细胞类目和/或亚类目的技术可见于与白血细胞有关的us 5,436,978。这些专利的公开内容据此以引用方式并入。根据一些实施例,样品制备技术可包括染色、裂解、透化和其他处理模式,诸如在共同待审的美国专利申请no.____中所述的那些,这些专利的内容以引用方式并入本文。
483.术语高光学分辨率成像设备可包括能够获得粒子图像的设备,所述图像具有充分的视觉区别以区分形态特征和/或变化。示例性高光学分辨率成像设备可包括光学分辨率为1μm或更低(包括例如0.4至0.5μm,诸如0.46μm)的设备。
484.在一些实施例中,在本发明的任何组合物和/或方法中得到的图像可以为数字化图像。在一些实施例中,所得的图像为显微镜图像。在某些实施例中,所述图像可以手动方式获得。在其他实施例中,获得图像的工序的至少一部分为自动化的。在一些实施例中,使用包括流通池、高光学分辨率成像设备或数字图像捕获设备(任选地具有自动对焦特征)的视觉分析仪获得图像。
485.在一个实施例中,图像提供与细胞的细胞质、细胞核和/或细胞核组分相关的信息。在一个实施例中,图像提供与细胞的颗粒组分和/或其他形态特征相关的信息。在一个
实施例中,图像提供与细胞的细胞质、细胞核和/或颗粒组分相关的信息。颗粒和/或细胞核图像和/或特征独立地或彼此相结合地为细胞分类及子分类决定性的。
486.在本发明方法的一个方面,与粒子造影剂组合物接触和/或成像的细胞为有核红血细胞。在又一个方面,本发明的方法涉及用于执行基于图像的红血细胞分类及子分类的方法,其包括:a)对红血细胞的一部分成像;以及b)确定所成像的红血细胞的形态。如本文所用,红血细胞(rbc)可包括例如正常或异常的红血细胞、网织红细胞、有核红血细胞和/或疟疾感染的细胞。在一些实施例中,使用本发明的装置(诸如包括粒子计数器、视觉分析仪和处理器的装置)进行成像。
487.如本文所用,示例性全血细胞计数(cbc)可包括医生或其他医学专业人员通常要求的检验组合,从而提供与患者血样中的粒子和/或细胞相关的信息。在血流中循环的示例性细胞一般可分成三类:包括但不限于例如白血细胞(例如,白血球)、红血细胞(例如,红血球)和血小板(例如,凝血细胞)。
488.如本文所用,异常高或低的计数可指示存在疾病、失调和/或病症。因此,cbc是在医学中常常进行的血液检验中的一种,因为其可提供患者一般健康状态的概况。因此,cbc通常在年度体检期间进行。
489.如本文所用,通常采血师从受试者采集血样,而血液一般被抽入通常容纳有抗凝剂(例如edta,有时为柠檬酸盐)以防止其凝结的试管。然后将样品送往实验室。有时使用巴斯德吸管从手指针刺处吸走样品,以便立即通过自动化计数器处理。在一个实施例中,在粒子被包裹在鞘液或pioal中时采集粒子图像。在某些实施例中,可在显微镜下在用患者血液的样品制作的载片(血膜或外周涂片)上观察血样。在某些实施例中,通过自动化分析仪进行全血细胞计数。
490.如本文所用,一般来讲,血液分析仪可通过窄管路抽吸非常少量的样本。传感器可检测通过管路的细胞的计数和/或数量,并且可识别细胞的类型。示例性传感器可包括光(例如,可见、uv或ir)和/或电阻抗的检测器。示例性检测参数可包括尺寸、体积和/或细胞特征。在某些实施例中,传感器可检测约200nm至约10000nm范围内的波长谱中的可见和不可见光。在某些实施例中,传感器可检测约380nm与约760nm之间的波长。
491.如本文所用,血细胞计数的数据/参数包括例如总红血细胞;血红蛋白
‑
血液中血红蛋白的量;血细胞比容或红细胞压积(pcv);平均红细胞体积(mcv)
‑
红细胞的平均体积(基于该值是高于还是低于预期正常范围而将贫血分类成小红细胞性或大红细胞性贫血。可影响mcv的其他病症包括地中海贫血、网状细胞过多症和酒精中毒);平均红细胞血红蛋白(mch)
‑
每个红血细胞的血红蛋白的平均量,单位为皮克;平均红细胞血红蛋白浓度(mchc)
‑
细胞中的血红蛋白的平均浓度;红血细胞分布宽度(rdw)
‑
rbc群体的细胞体积的变化;总白血细胞;中性粒细胞(可指示细菌感染,通常在急性病毒感染中增加)。由于细胞核的分段式外观,中性粒细胞有时称为“seg”。不太成熟的中性粒细胞的细胞核不分段,但具有带式或细长形状。不太成熟的中性粒细胞(最近从骨髓释放到血流中的那些)称为“band”。血细胞计数的其他数据/参数也可包括例如淋巴细胞(例如,在一些病毒感染诸如腺热的情况下以及在慢性淋巴细胞白血病(cll)中增加,或因hiv感染而减少);单核细胞(可在细菌感染、肺结核、疟疾、落基山斑疹热、单核细胞性白血病、慢性溃疡性结肠炎和局限性回肠炎中增加);嗜酸性粒细胞(例如,在寄生虫感染、哮喘或变态反应中增加);嗜碱性
粒细胞(例如,在骨髓相关病症诸如白血病或淋巴瘤中增加)。
492.如本文所用,血细胞计数的数据/参数还可以包括例如与血小板相关的数据,包括血小板数、其在血液中的尺寸和尺寸范围的相关信息;平均血小板体积(mpv)
‑
血小板平均尺寸的量度。
493.在本发明的方法的另一个方面,与粒子造影剂组合物接触和/或成像的细胞为异常细胞,诸如疟疾感染的细胞、非典型淋巴细胞。在本发明的一些方面,细胞是可用于对病症、疾病、感染和/或综合征进行识别、预测、诊断、预后或支持诊断的异常细胞。
494.在本发明的方法的另一方面,细胞为血小板。
495.除非另外明确指明,否则本发明中提及的“粒子”应当理解为涵盖分散于流体中的任何离散或有形对象。如本文所用,“粒子”可包括生物流体中的所有可测量且可检测(例如,通过图像和/或其他可测量参数)的组分。粒子具有任何材料、任何形状和任何尺寸。在某些实施例中,粒子可包括细胞。粒子的例子包括但不限于细胞,包括血细胞、胎儿细胞、上皮细胞、干细胞、肿瘤细胞,或细菌、寄生生物或任何前述物质的碎片或生物流体中的其他碎片。血细胞可以为任何血细胞,包括可能存在于生物流体中的任何正常或异常、成熟或未成熟的细胞,例如红血细胞(rbc)、白血细胞(wbc)、血小板(plt)和其他细胞。成员也包括未成熟的或异常的细胞。未成熟的wbc可包括晚幼粒细胞、中幼粒细胞、早幼粒细胞和母细胞。除了成熟的rbc之外,rbc的成员还可以包括有核rbc(nrbc)和网织红细胞。plt可包括“巨大”plt和plt团块。血细胞和有形成分在本发明的别处进一步描述。
496.示例性粒子可包括生物流体样品中的有形成分,包括例如球形和非球形粒子。在某些实施例中,粒子可包括非球形组分。非球形组分的图像投影可在高光学分辨率成像设备的焦平面中最大化。在某些实施例中,非球形粒子在高光学分辨率成像设备的焦平面中配向(在基本上平行于流动方向的平面中配向)。在一些实施例中,作为粒子对血小板、网织红细胞、有核rbc和wbc(包括中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞、嗜碱性粒细胞)以及未成熟wbc(包括母细胞、早幼粒细胞、中幼粒细胞或晚幼粒细胞)计数和分析。
497.如本文所用,可检测和可测量的粒子参数可包括例如尺寸、形状、对称性、轮廓和/或其他特性的基于视觉和/或非图像的指标。
498.在另一个实施例中,本发明涉及在包括例如以下步骤的方法中使用例如本发明的试剂盒对粒子进行成像的方法:1)在视觉分析仪中用光照射粒子;2)获得包裹在pioal中的样品粒子的数字化图像;以及3)基于图像信息分析包含粒子的样品。在其他实施例中,该方法还可以包括在照射经处理的样品之前将包含粒子的样品与粒子造影剂组合物接触。
499.在一个实施例中,所分析的粒子包括球形粒子、非球形粒子中的至少一种,或这两种。在另一个实施例中,粒子包括至少一个球形粒子。在又一个实施例中,粒子包括至少一个非球形粒子。在另一个实施例中,非球形粒子或具有非球形组分的粒子的图像投影在基本上平行于流动方向的平面中最大化。粒子可以为例如wbc、rbc和/或血小板。在一个实施例中,至少50%的非球形粒子在基本上平行于流动方向的平面中配向。在另一方面,在流通池中使用本发明的pioal允许至少90%的非球形粒子在基本上平行于流动方向的平面中配向。
500.小于包裹在pioal中的带形样品料流的厚度的细胞的流动导致那些细胞平行于流动方向配向。在本发明的一个实施例中,至少92%的非球形粒子在基本上平行于流动方向
的平面中配向。在又一个实施例中,至少90%的非球形粒子在基本上平行于流动方向的平面中配向。在另一个实施例中,至少75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%或至少95%的粒子基本上配向,即在基本上平行于流动方向的平面的20度内。在另一个实施例中,在基本上平行于流动方向的平面中配向的非球形和/或球形粒子的百分比可为所列百分比中的任何两个之间的任何范围,例如至少75
‑
85%、75
‑
80%,和其他范围,诸如75
‑
92%。
501.因包裹在pioal中的样品中的较大细胞(诸如wbc)的流动而在平行于流动方向的方向中产生的剪切力导致细胞核结构、细胞质结构或颗粒或其他细胞内组分或结构更靠近平行于流动方向的平面而定位、重定位和/或更好地定位。
502.在一个实施例中,非球形粒子包括红血细胞。在本发明的另一方面,球形粒子包括白血细胞或有核红血细胞。
503.在本发明的方法的一个实施例中,粒子为非球形粒子。在一个实施例中,所分析的粒子包括球形粒子、非球形粒子中的至少一种,或这两种。在另一个实施例中,粒子包括至少一个球形粒子。在又一个实施例中,粒子包括至少一个非球形粒子。在另一个实施例中,非球形粒子或具有非球形组分的粒子的图像投影在基本上平行于流动方向的平面中最大化。粒子可以为例如rbc(包括网织红细胞和有核rbc)、血小板和/或wbc(包括中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞、嗜碱性粒细胞)或未成熟的wbc(包括母细胞、早幼粒细胞、中幼粒细胞或晚幼粒细胞)。在一个实施例中,至少50%的非球形粒子在基本上平行于流动方向的平面中配向。在另一方面,在流通池中使用本发明的pioal允许至少90%的非球形粒子在基本上平行于流动方向的平面中配向。
504.在本发明的一个实施例中,图像横截面包括在wbc(包括中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞、嗜碱性粒细胞)或未成熟的wbc(包括母细胞、早幼粒细胞、中幼粒细胞或晚幼粒细胞)中差异染色的细胞核结构、差异染色的细胞质结构或差异染色的颗粒中的至少一种。在另一个实施例中,至少50%、55%、60%、65%、70%、75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%或至少95%的球形和/或非球形粒子在高光学分辨率成像设备的焦平面或视野深度中具有细胞核结构、细胞质结构或颗粒。
505.在本发明的方法的一些实施例中,图像信息是粒子的图像横截面。在一些方面,图像横截面包括在wbc(包括中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞、嗜碱性粒细胞)或未成熟的wbc(包括母细胞、早幼粒细胞、中幼粒细胞或晚幼粒细胞)中差异染色的细胞核结构、差异染色的细胞质结构或差异染色的颗粒中的至少一种。
506.在一个实施例中,本发明的方法提供出奇高质量的细胞图像,其中流动中的高百分比的粒子和粒子内容物处于焦点内,这可用于获得自动化的、基于图像的wbc分类,以及自动化识别形态异常,其可用于对受试者是健康还是具有疾病、病症、异常或感染和/或对治疗有响应还是无响应进行确定、诊断、预后、预测或支持诊断。
507.在另一方面,本发明的组合物和方法提供更准确的基于图像的细胞分类及子分类和标记,与目前的分析仪相比,所述标记大大降低人工复核率。
508.如本文所用,示例性白血细胞(wbc)可包括例如中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞、嗜碱性粒细胞、未成熟的粒细胞(包括晚幼粒细胞、中幼粒细胞、早幼粒细胞和母细胞)以及异常的白血细胞。如本文所用,红血细胞(rbc)可包括例如正常或异常的红
血细胞、网织红细胞和有核红血细胞。
509.如本文所用,粘度剂可包括粘度剂或粘度改性剂。示例性粘度剂/改性剂具有与样品的粘度不同的特性粘度,使得当混合pioal和粘度剂时,pioal的粘度发生改变和/或增加以便最大程度提高粒子的配向。在某些实施例中,带形样品料流与pioal之间的粘度差和/或速度差可引入剪切力而作用在处于流动中的粒子上,从而减少失准和/或使粒子配向。
510.如本文所用,粒子造影剂组合物可适于与粒子和/或细胞内细胞器配向液(pioal)组合用于视觉分析仪以分析得自受试者的样品中的粒子。示例性pioal可用于例如得自受试者的样品中的不同类型的粒子的自动化识别方法。
511.在另一方面,在获得图像时细胞可被包围在pioal中。本文描述了合适的示例性细胞内细胞器配向液。
512.在一个实施例中,本发明涉及用于视觉分析仪的pioal。在某些实施例中,pioal可包含以下至少一者:缓冲剂;ph调节剂;缓冲剂;粘度剂/改性剂;离子强度改性剂、表面活性剂、螯合剂和/或抗微生物剂。
513.在一个方面,pioal可包含两种或更多种粘度剂/改性剂。
514.在一个方面,本发明的pioal可具有约1至约10厘泊之间的粘度。在一个实施例中,本发明的pioal可包含粘度剂/改性剂。在一个实施例中,pioal包含最多100%的粘度剂。
515.如本文所用,粘度剂和/或粘度改性剂可包括适于实现约1至约10厘泊的粘度而光学特性(包括光学清晰度)适用于成像系统的任何物质。一般来讲,粘度剂或改性剂是无毒的、生物相容的并使细胞结构和内容物基本上完整。粘度剂和/或粘度改性剂可包含以下至少一者:甘油;甘油衍生物;乙二醇;丙二醇(二羟基丙烷);聚乙二醇;水溶性聚合物和/或葡聚糖。在一个方面,pioal中的粘度剂/改性剂可以为甘油。例如,在一个方面,pioal中的粘度剂/改性剂可以为甘油衍生物。例如,在一个方面,pioal中的粘度剂/改性剂可以为聚乙烯吡咯烷酮(pvp)。又如,pioal中的粘度剂/改性剂可以为乙二醇。又如,pioal中的粘度剂/改性剂可以为丙二醇(二羟基丙烷)。又如,pioal中的粘度剂/改性剂可以为聚乙二醇。又如,pioal中的粘度剂/改性剂可以为水溶性聚合物或葡聚糖。在其他方面,pioal中的粘度剂/改性剂可包含以下一者或更多者:甘油、甘油衍生物;乙二醇;丙二醇(二羟基丙烷);聚乙烯吡咯烷酮(pvp);聚乙二醇;水溶性聚合物或葡聚糖。粘度剂/改性剂可包括适于提供约1至约10厘泊的粘度而光学特性(包括光学清晰度)适用于成像系统的任何试剂。
516.如本文所用,其他示例性粘度剂/改性剂可包括例如天然水解胶体(及衍生物),诸如阿拉伯树胶、黄蓍胶、藻酸、角叉菜胶、刺槐豆胶、瓜耳胶、黄原胶、阿拉伯树胶、瓜耳胶、明胶、纤维素、海藻酸盐、淀粉、糖类、葡聚糖;明胶;糖类(及衍生物),诸如右旋糖、果糖;聚右旋糖;葡聚糖;多聚葡聚糖;糖类;和多糖;半合成水解胶体(及衍生物),诸如甘油、甲基纤维素、羟乙基淀粉(hetastarch)、羧甲基纤维素钠、羟乙基纤维素、羟丙基甲基纤维素、聚乙烯吡咯烷酮(pvp);合成水解胶体(及衍生物),诸如聚乙烯醇(pva)和/或也考虑了其他细胞相容性粘度剂/改性剂可用于该目的。
517.在另一方面,pioal中的粘度剂/改性剂可以为以pioal的约1至约50%(v/v)的浓度存在的甘油。例如,在一个实施例中,粘度剂/改性剂可以约5.0%至约8.0%(v/v)的浓度存在于pioal中。在另一方面,粘度剂/改性剂可以约6.5%(v/v)的浓度存在。在一个实施例中,粘度剂/改性剂是以约6.5%(v/v)的浓度存在的甘油。
518.在又一个实施例中,pioal可包含以约30%(v/v)的浓度存在的甘油粘度剂/改性剂。
519.在另一方面,pioal中的粘度剂/改性剂可以为以约0.5至约2.5%(w/v)的浓度存在的pvp。例如,在一个实施例中,粘度剂/改性剂pvp可以约1.0至约1.6%(w/v)的浓度存在于pioal中。在一个实施例中,pvp以约1.0%(w/v)的浓度存在。
520.在另一方面,pioal中的粘度剂/改性剂可以为pvp和甘油。例如,在一个实施例中,甘油可以约5%(v/v)的浓度与约1%(w/v)的pvp相结合存在于pioal中。
521.在一个实施例中,本发明的pioal可用于视觉分析仪以对粒子进行成像。在一个方面,视觉分析仪包括具有对称流路的流通池,和自动对焦部件。
522.粘度剂和/或粘度改性/调节剂(诸如甘油)可包含在pioal中。粘度剂或粘度改性剂在引入时可适当地将pioal的粘度调节到所需的范围。可以使用足以增加pioal的粘度的任何合适的粘度剂,其具有允许对流动中的细胞进行高质量成像的合适的光学特性。pioal将具有合适的粘度以将细胞和/或细胞结构配向到基本上与流动方向平行的单个平面中,从而部分地增加粒子的焦点内内容物。
523.pioal可与本发明的任何分析仪一起使用。
524.如本文所用,术语“甘油”涵盖甘油和甘油的衍生物(下文称为甘油衍生物)。甘油衍生物的例子包括硫甘油、聚甘油等。聚甘油的可用例子可包括双甘油、polyglycerin#310(坂本药品工业株式会社(sakamoto yakuhin kogyo co.,ltd.))、polyglycerin#750(坂本药品工业株式会社)、polyglycerin#500(坂本药品工业株式会社)等。
525.在另一个实施例中,本发明的pioal还包含ph调节剂。在一个方面,pioal和/或样品的最终ph在约6.0至约8.0之间。在另一方面,pioal和/或样品的最终ph在约6.6至约7.4之间。在一个方面,pioal的最终ph可与制备的样品12b的ph相同(参照图8)。
526.示例性ph调节剂可包括例如酸(示例包括有机酸和矿物酸)、碱(示例包括有机碱以及碱金属和碱土金属氢氧化物)。示例性有机酸可包括乙酸、乳酸、甲酸、柠檬酸、草酸和尿酸。示例性矿物酸可包括例如盐酸、硝酸、磷酸、硫酸、硼酸、氢氟酸、氢溴酸和过氯酸。示例性有机碱可包括例如吡啶、甲胺、咪唑、苯并咪唑、组氨酸、磷腈和阳离子氢氧化物。示例性碱金属和碱土金属氢氧化物可包括例如氢氧化钾(koh)、氢氧化钡(ba(oh)2)、氢氧化铯(csoh)、氢氧化钠(naoh)、氢氧化锶(sr(oh)2)、氢氧化钙(ca(oh)2)、氢氧化锂(lioh)和氢氧化铷(rboh)。
527.在一些实施例中,使用缓冲剂,优选地将pioal的ph维持在约6.0至约8.5,更优选地约7.0至约8.0。在一些实施例中,优选的是向pioal添加缓冲剂以便调节pioal的ph。可以使用一种或多种任何合适的缓冲剂,只要所述缓冲剂能够将pioal调节到适当的范围即可。这样的缓冲剂的例子包括可以单独使用或组合使用的pbs、good's缓冲液(具体地讲,tris缓冲液、mes、bis
‑
tris、ada、pipes、aces、mopso、bes、mops、tes、hepes、dipso、tapso、popso、heppso、epps、tricine、bicine、taps等)、磷酸氢二钠、磷酸二氢钠、磷酸二氢钾、巴比土钠盐酸盐(veronal sodium
‑
hcl)、可力丁盐酸盐(collidine
‑
hcl)、三(羟甲基)氨基甲烷
‑
马来酸、三(羟甲基)氨基甲烷
‑
hcl。
528.在另一个实施例中,本发明的pioal包含离子强度改性剂以调节所得制剂的离子强度。示例性离子强度改性剂可包括li
+
、na
+
、k
+
、mg
++
、ca
++
、cl
‑
、br
‑
、hco
‑3、硫酸盐、焦硫酸
盐、磷酸盐、焦磷酸盐(例如焦磷酸钾)、柠檬酸盐、卡可基酸盐或其他合适的盐。在一个实施例中,pioal可以为等渗的。
529.可将表面活性剂加入pioal中。表面活性剂的种类无特别限制,只要它们与pioal的其他组分相容且与带形样品料流和样品中的粒子相容即可。表面活性剂可包括例如阳离子、阴离子、非离子和两性表面活性剂。示例性表面活性剂可包括聚氧乙烯烷基醚型表面活性剂、聚氧乙烯烷基苯基醚型表面性活性剂(例如,nissan nonion ns
‑
240(日本油脂株式会社(nof corporation),注册商标))、聚氧乙烯山梨糖醇烷基酯型表面活性剂(例如,rheodol tw
‑
0120(花王株式会社(kao corporation),注册商标))、多元醇共聚物(例如,pluronic f
‑
127、f
‑
123、f
‑
109、f
‑
87、f
‑
86、f
‑
68、t
‑
1107、t
‑
1102(巴斯夫公司(basf corporation),注册商标))、mega
‑
8、蔗糖单癸酸酯、脱氧
‑
bigchap、正辛基
‑
β
‑
d
‑
硫代葡糖苷、正壬基
‑
β
‑
d
‑
硫代麦芽糖苷、正庚基
‑
β
‑
d
‑
硫代葡糖苷、正辛基
‑
β
‑
d
‑
硫代葡糖苷、chaps、chapso等。其他表面活性剂可包括处于样品和带形样品料流相容性浓度的triton
‑
x
‑
100和tween 20。
530.表面活性剂在pioal中的浓度优选地为样品中的粒子(诸如细胞)不受影响和/或保持基本上完整的浓度水平。具体地讲,该浓度优选地为5至5000mg/l,更优选地为100至3000mg/l。
531.当用分析仪分析样品中所含的粒子时,诸如磷酸铵、磷酸镁、碳酸钙的无定形盐可在样品中沉淀。可将螯合剂加入pioal中以便溶解这些无定形盐。添加螯合剂使得不仅能够溶解无定形盐,还能够抑制pioal的氧化。螯合剂的可用例子包括edta盐、cydta、dheg、dpta
‑
oh、edda、eddp、gedta、hdta、hida、甲基
‑
edta、nta、ntp、ntpo、eddpo等。螯合剂在pioal中的浓度优选地在0.05至5g/l的范围内。
532.在另一个实施例中,pioal还可以包含一种或多种抗微生物剂。在一些方面,抗微生物剂可以为例如具有杀真菌活性的物质(杀真菌剂)和/或具有杀菌活性的物质(杀菌剂)。在某些实施例中,合适的抗微生物剂可包括例如对羟基苯甲酸酯、异噻唑啉酮、酚类物质、酸性防腐剂、卤化化合物、quarternia和醇。示例性对羟基苯甲酸酯可包括对羟基苯甲酸酯和对羟基苯甲酸酯盐。示例性异噻唑啉酮可包括甲基氯异噻唑啉酮、甲基异噻唑啉酮、苯异噻唑啉酮、proclin 150、proclin 200、proclin 300和proclin 950。示例性酚类可包括苯氧基乙醇、苄醇和苯乙醇。示例性酸性防腐剂可包括脱氢乙酸、苯甲酸、山梨酸、水杨酸、甲酸、丙酸。示例性卤化化合物可包括2
‑
溴
‑2‑
硝基丙烷
‑
1,3
‑
二醇、氯乙酰胺、氯代丁醇、氯二甲苯酚、氯苯甘油醚、二氯苄醇、丁基氨基甲酸碘代丙炔酯、甲基二溴戊二腈。示例性quaternia可包括苯扎氯铵、苄索氯铵、氯己定、己脒定二羟乙基磺酸盐和聚氨丙基双胍。示例性醇可包括乙醇和异丙醇。其例子包括三嗪抗微生物剂、噻唑杀菌剂(例如,苯并异噻唑啉酮)、吡啶硫酮、吡啶杀菌剂(例如,1
‑
羟基吡啶
‑2‑
硫钠等)、2
‑
苯氧基乙醇等。具体地讲,可以使用proxel gxl(奥维斯公司(avecia))、tomicide s(api公司(api corporation))等。杀菌剂和/或杀真菌剂有助于改善pioal的稳定性。
533.在一个实施例中,抗微生物剂的浓度可以为0.01%至0.5%(w/v)。该浓度可以为0.03至0.05%(w/v)。
534.在实施例中接受使用具有pioal的分析仪的分析的样品无特别限制。通常使用得自活体的样品(生物样品)。或者,那些样品可用造影剂等进行稀释、纯化、接触以供使用。具
体地讲,这样的样品的例子可包括血液、精液、脑脊髓液等。样品还可以包括源自组织样品的粒子悬液。在分析粒子(红血细胞、白血细胞、细菌等)时,该实施例中的pioal是适用的。
535.本发明的pioal可用于对粒子进行成像的视觉分析仪。在一个方面,视觉分析仪包括能够以预定的尺度特性(诸如有利的带形样品料流厚度)维持带形样品料流的流动的流通池。在一些实施例中,流通池可具有对称流路,并与自动对焦部件结合使用。
536.本发明涉及对粒子进行成像的方法,其包括:1)将样品与粒子造影剂组合物接触;2)照明制备的粒子;3)获得包裹在pioal中的带形样品料流中的粒子的数字化图像;以及4)分析图像信息以对粒子分类或子分类。在一些实施例中,粒子可以为wbc、rbc和/或血小板(包括例如中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞、嗜碱性粒细胞、网织红细胞、有核rbc、母细胞、早幼粒细胞、中幼粒细胞或晚幼粒细胞)、细胞、细菌、寄生生物、颗粒物、细胞团、细胞组分和未成熟粒细胞中的至少一种。在一些实施例中,基于粒子图像信息对血小板、网织红细胞、有核rbc以及wbc(包括中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞、嗜碱性粒细胞)和未成熟的wbc(包括母细胞、早幼粒细胞、中幼粒细胞或晚幼粒细胞)计数和分析。
537.在一些实施例中,视觉分析仪包括具有对称或不对称流路的流通池,和自动对焦部件。
538.在一般的方面,当与存在于研究和/或医学实验室中的自动化分析仪结合使用时,所述示例性pioal及其使用方法是有用的。示例性自动化分析仪为被设计成以最少的人工辅助快速地测量多种生物样品(包括例如人类体液样品)中的不同有形成分和/或其他特性的仪器。示例性自动化分析仪可包括例如血液学分析仪和/或细胞计数器,其可执行例如全血细胞计数(cbc)测定。示例性分析仪可逐一地、分批地或连续地处理样品。
539.在一个方面,示例性分析仪/系统包括被配置成检测符合一项或多项选择标准的多个粒子并提供其粒子计数的自动化粒子计数器,其中所述选择标准涵盖所述粒子中至少两种类目的成员。可包括处理器(可包括计数器的部件)的分析仪被程序化以区分所述至少两种类目的粒子。各粒子的分布使用该分析仪进行测定。该处理器使用所述分布来校正所述至少两种类目和/或亚类目中至少一者的成员的粒子计数。在一些实施例中,粒子计数器包括至少一个通道,所述通道被配置成基于体积、尺寸、形状和/或其他标准的预定范围提供所述至少一种类目和/或亚类目的粒子计数。例如,所述至少一种类目和/或亚类目的成员包括选自以下亚类目的至少一种类型的粒子:白血细胞(wbc)、红血细胞(rbc)、巨大血小板(plt)和有核红血细胞(nrbc)。在粒子计数器上,由于相似的尺寸或其他测得的特性,诸如巨大plt和nrbc的细胞可作为wbc计数。通过操作如本文所述的装置,可准确地测量巨大plt和nrbc的粒子计数或浓度。
540.样品可为分离和/或制备的生物样品,包括例如体液样品、血液、血清、脑脊髓液、胸膜液、腹膜液、唾液、精液、泪液、汗液、母乳、羊膜液、灌洗液、骨髓穿刺液、渗漏液、渗出液、或从受试者获得的其他样品(例如,经处理产生细胞悬液的活检样品、或包含粒子的实验室或生产线样品)。在一些实施例中,样品可以为实体组织样品,例如,已进行了处理而产生细胞悬液的活检样品。样品也可以为通过处理粪便样品而得到的悬液。样品也可为包含粒子的实验室、化学、工业或生产线样品,诸如细胞培养样品。术语样品可用于指代得自患者或实验室或其任何级分、部分或等分试样的样品。在一些方法中可将样品稀释、分成多个
部分、或用造影剂处理。
541.本文所公开的方法适用于来自广泛生物体的样品,所述生物体包括哺乳动物,例如人类、非人灵长类(例如,猴)、马、牛或其他牲畜、狗、猫或其他作为宠物饲养的哺乳动物、大鼠、小鼠或其他实验室动物;禽类,例如鸡;爬行动物,例如短吻鳄;鱼类,例如鲑鱼或其他养殖品种;以及两栖动物。
542.可通过任何常规方法,例如排泄、抽取、收获、抽吸或活检,来获得样品。样品可来自被认为健康的受试者,例如作为日常体检的一部分而采集的样品。样品也可来自具有失调、有失调风险或疑似具有失调的受试者。失调可由疾病、遗传异常、感染、损伤或未知原因引起。作为另外一种选择或除此之外,方法可用于在治疗失调的过程期间监测受试者。如果存在对治疗和/或疗法的非响应性的迹象,临床医生可选择替代或辅助药剂。根据受试者的病症和具体失调(如果有的话),可每日、每周、每月或每年采集一次(或两次、三次等等)样品。
543.粒子可根据样品而有所差异。粒子可为生物细胞,例如,血细胞、胎儿细胞、干细胞、肿瘤细胞或其碎片。在一些实施例中,粒子可为感染因子,例如病毒或细菌。
544.本发明中提及的“血细胞”应当理解为涵盖可能存在于生物流体中的任何正常或异常、成熟或未成熟细胞,例如,红血细胞(rbc)、白血细胞(wbc)、血小板(plt)和其他细胞。一般来讲,正常rbc、plt和wbc分别具有6
‑
8μm、2
‑
3μm和8
‑
15μm范围内的粒径。正常rbc、plt和wbc分别以3.9
‑
5.7
×
1012个细胞/l、1.4
‑
4.5
×
1011个细胞/l、3.5
‑
11
×
109个细胞/l的近似浓度范围存在于来自正常患者的全血样中。参见barbara j.bain,blood cells,a practical guide,4th ed.,blackwell publishing,2007,34
‑
36(barbara j.bain,《血细胞,实用指南》,第4版,布莱克威尔出版公司,2007年,第34
‑
36页)。
545.提及的“有形成分”应当理解为涵盖存在于生物流体样品中的非流体成分。有形成分包括例如基于科学分类或生理功能的血细胞的类别,包括红血球(rbc)、白血球(wbc)和血小板(plt)、wbc团块、白血球的亚类别,所述白血球的亚类别包括成熟淋巴细胞和未成熟白血球诸如单核细胞、中性粒细胞、嗜酸性粒细胞、嗜碱性粒细胞。可用于本文的“有形成分”也将包括粒子诸如微生物、细菌、真菌、寄生生物或其碎片或其他细胞碎片。wbc的主要成员包括但不限于中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞和嗜碱性粒细胞。成员也包括未成熟的或异常的细胞。例如,未成熟wbc可包括晚幼粒细胞、中幼粒细胞、早幼粒细胞。除了成熟的rbc之外,rbc的成员还可以包括有核rbc(nrbc)和网织红细胞。plt可包括正常plt和“巨大”plt,“巨大”plt的尺寸接近正常wbc的尺寸。本发明中提及的一类目和/或亚类目粒子的“成员”应当理解为涵盖一类目或亚类目粒子内的单独粒子。
546.除非另外明确指明,本发明中提及的一“类目”粒子应当理解为涵盖使用至少一种测量的、检测的或推导的检测标准诸如尺寸、形状、质构或颜色所检测的一群粒子。在一些实施例中,通过本发明的装置计数的至少一种类目和/或亚类目的粒子的成员将为有形成分的相同类型。
547.此类粒子可在“通道”中检测。本发明中提及的“通道”应当理解为涵盖粒子计数器的一部分,该部分包括耦合到信号源的检测器,从而提供随符合至少一个通道检测标准的粒子的较强或较弱检测而变化的输出。例如,通道检测标准可基于粒子的尺寸或体积。在一些实施例中,粒子计数器中的通道数量为一个。在一些其他实施例中,粒子计数器中的通道
数量为两个或更多个。
548.粒子计数器的一个通道中检测到的一种类目和/或亚类目的粒子可包括不同类别和亚类别的粒子以及两种或更多种亚类别的粒子的成群成员。本发明中提及的一“类目”粒子应当理解为涵盖与测量的、检测的或推导的标准诸如尺寸、形状、质构或颜色相对应的一群粒子。在一些实施例中,通过本发明的装置计数的至少一种类目和/或亚类目的粒子的成员将为有形成分的相同类型。
549.如本文所用,“配向”可部分通过球形和/或非球形粒子的配向来表征。例如,粒子诸如非球形粒子可配向在基本上平行于流动方向的平面中。在某些实施例中,非球形粒子的配向通过这样的粒子取向来表征,该取向增大了非球形粒子在成像条件下在高光学分辨率成像设备的焦平面中的图像投影。粒子诸如球形粒子可具有增加量的粒子和细胞的焦点内粒子内内容物,从而能有效地产生用于粒子分类和子分类的视觉区别。粒子诸如球形粒子的粒子内结构可定位、重定位和/或更好定位成基本上平行于流动方向。例如,细胞内结构、细胞器或裂片也可定位、重定位和/或更好定位成基本上平行于流动方向。
550.本发明中提及的一“类别”粒子应当理解为涵盖基于科学分类的一群粒子。例如,三种主要类别的血细胞存在于全血样中,包括rbc、wbc和plt。
551.本发明中提及的粒子的“成员”应当理解为涵盖一类目或亚类目粒子中的粒子。例如,每种类目的血细胞可进一步分成亚类目或成员。wbc的主要成员包括但不限于中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞和嗜碱性粒细胞。成员也包括未成熟的或异常的细胞。例如,未成熟wbc可包括晚幼粒细胞、中幼粒细胞和早幼粒细胞。除了成熟的rbc之外,rbc的成员还可以包括有核rbc(nrbc)和网织红细胞。plt可包括正常plt和“巨大”plt,“巨大”plt的尺寸接近正常wbc的尺寸。
552.提及的“未成熟细胞”应当理解为涵盖某些发育阶段中,例如骨髓内部或从骨髓释放不久之后但在完全发育成成熟细胞之前的细胞。
553.提及的“异常细胞”应当理解为涵盖具有异常形态特性的细胞或与某些疾病或病症相关的细胞、或者可能在某些情况下与某些疾病或病症相关的异常。特定疾病的例子包括但不限于红细胞增多症、多血症、贫血症、幼红细胞减少症、白细胞增多症、白细胞减少症、淋巴细胞增多症、淋巴细胞减少症、粒细胞增多症、粒细胞减少症或粒细胞缺乏症、中性粒细胞增多症、中性粒细胞减少症、嗜酸性粒细胞增多症、嗜酸性粒细胞减少症、嗜碱性粒细胞增多症、嗜碱性粒细胞减少症、血小板增多症、血小板减少症和全血细胞减少症。一种类别的细胞在血流中可增多或减少。在一些条件下,比正常白细胞大得多的异常细胞以小浓度存在于血样中。尺寸、形状、颜色和/或细胞内结构的变化可与某些疾病或病症相关。
554.本发明中提及的粒子的“计数”或“粒子计数”应当理解为涵盖从粒子计数器的一个通道获得的粒子的数量。本发明中提及的粒子的某类别或成员的“浓度”应当理解为意指每单位体积(例如每升)或已知体积的每个样品的粒子的数量。例如,粒子计数器可为各类目的粒子提供计数或浓度或其他基于计数的函数,同时视觉分析仪可为每种类目或亚类目的粒子提供计数、浓度、比率或其他基于浓度的参数。
555.本发明中提及的“比率”应当理解为涵盖粒子的两种类目/亚类目、类别或成员的任何定量的和/或成比例的比率。此类比率的例子包括但不限于按浓度、重量和/或按粒子数量的比率。通常比率涉及一种类目、类别或成员的计数相对于另一种这样的类目、类别或
成员的计数的数字分数。在一些实施例中,也可使用加权的计数或加权的和/或成比例的比率进行确定。
556.因此,本发明的实施例涵盖混合系统和方法,例如其结合了电子细胞计数和摄影细胞成像技术,例如以分析可能难以在电学上区分的细胞,或分析以使得获得其准确电子计数变得困难的量存在的细胞。
557.本发明还涉及用于快速产生样品中的视觉区别的出奇且意外的粒子造影剂组合物。粒子造影剂组合物尤其可用于自动化流式细胞术系统。粒子造影剂组合物由粒子造影剂、透化剂和固定剂的组合构成。在一个实施例中,粒子造影剂组合物为结晶紫、新亚甲蓝、皂草苷和戊二醛的混合物。在出奇有效的实施例中,在染色条件下,结晶紫以足以得到约7.8μm的浓度的量存在,新亚甲蓝以足以得到约735μm的浓度的量存在,皂草苷以足以得到约50mg/l与约750mg/l之间的浓度的量存在,组合物还包含以足以得到约27μm的浓度的量存在的伊红
‑
y,并且戊二醛以足以得到等于或低于0.1%的浓度的量存在。
558.给出这些示例性例子的目的是向读者介绍此处所讨论的一般主题,并非旨在限制所公开的概念的范围。以下部分将参照附图(其中类似的数字指示类似的元件)描述各种另外的特征和例子,并且指向性描述用于描述示例性实施例,但是与示例性实施例一样,不应当用于限制本发明。本文图示中包括的元件可能未按比例绘制。
559.本发明的粒子造影剂组合物在施加到血液流体样品时导致此类样品中的细胞的染色类似于用标准血涂片染液处理的血涂片的染色,并且具体地讲类似于用瑞氏染液处理的血涂片染色。瑞氏染液是有利于区分血细胞类型(例如,wbc)的组织学染液。其主要用于对在光学显微镜下检查的外周血涂片和骨髓穿刺液进行染色。在细胞遗传学中,其用于对染色体染色以有利于综合征和疾病的诊断。存在称为含缓冲液的瑞氏染液、瑞氏
‑
姬姆萨染液以及含缓冲液的瑞氏
‑
姬姆萨染液的相关染液。因为瑞氏染液方法涉及醇溶剂,这种染色工序会破坏活细胞并且不能得到基本上完整的细胞。产生更强烈着色的梅格二氏染液也要花更长的时间进行。
560.本发明的各方面和实施例基于这样的出奇且意外的发现:当用于执行自动化、基于图像的样品分析诸如血液分析时,某些粒子造影剂组合物(包括例如染液/染料组合物和/或它们的组合)具有意外的性质和功效。
561.本文所公开的组合物和方法可与许多不同类型的血液学成像系统一起使用。具体地讲,本文所述的组合物和方法可与基于图像的样品分析诸如流通池分析一起使用。此流通池分析的例子可包括流式细胞术的传统、已知方法。另外,本文所述的组合物和方法可有利地与下文简要描述及如下共同提交的申请中进一步描述的流通池分析系统和方法一起使用:2014年3月17日提交的名称为“flowcell systems and methods for particle analysis in blood samples”(用于血样中的粒子分析的流通池系统和方法)的申请no.__/___,___和2014年3月17日提交的名称为“hematology systems and methods”(血液学系统和方法)的申请no.pct________,这两份申请据此以引用方式并入。
562.粒子造影剂组合物
563.图a1是根据一个实施例的粒子造影剂组合物的制备的示意图。在方框208处,将粒子造影剂202、透化剂204和固定剂206组合以形成粒子造影剂组合物210。在一个实施例中,将粒子造影剂202、透化剂204和固定剂206同时组合。在其他实施例中,按照任何顺序,将粒
子造影剂202、透化剂204和固定剂206中的一种与粒子造影剂202、透化剂204和固定剂206中的另一种组合,然后与粒子造影剂202、透化剂204和固定剂206中的最后一种组合。可按照任何顺序和任何合适的方式执行方框208处的组合。
564.在替代实施例中,透化剂204和固定剂206中的一种不包含在粒子造影剂组合物210中。在另外的实施例中,在方框208处将另外的材料作为粒子造影剂组合物210的一部分组合,如下文更详细描述。
565.粒子造影剂组合物210可作为试剂盒的一部分提供。粒子造影剂组合物210可作为已制备的方式或作为必须组合的一种或多种组分提供。
566.粒子造影剂
567.粒子造影剂202可为能够产生可见区别(诸如类似于瑞氏染液的那些可见区别)的任何造影剂。此类造影剂的例子包括阿利新蓝和阿利新蓝86(pas中性和酸性粘液物质);茜素红s;诱惑红ac(偶氮染料红色染料#40);苯胺蓝(用草酸加强纤毛);金胺o;天青b;天青c;俾斯麦棕;亮蓝fcf(考马斯蓝);亮甲酚蓝;亮绿;carmium(由胭脂红酸和钾明矾构成的红色细胞核染料);刚果红;氯唑黑e(细胞核黑色,细胞质灰色,糖原粉色);醋酸甲酚紫;达罗红;带蓝伊红;赤藓红b(红色染料#3);乙基伊红;固绿fcf(绿色染料#3);碱性品红
‑
(细胞核和鞭毛);荧光素
‑
(红汞);姬姆萨
‑
外周血涂片;哈里斯氏苏木精
‑
退行性细胞核染液;靛蓝胭脂红(蓝色染料#2);詹纳斯绿b(线粒体);詹纳尔染液
‑
(外周血涂片);亮绿sf淡黄;麦克尼尔
‑
(四铬血液染液);孔雀石绿;甲基橙;马休黄;迈尔氏苏木精
‑
退行性细胞核染液;甲基紫2b;乌洛托品银
‑
过碘酸;亚甲紫;迈格林华
‑
血液学染液;mtt
‑
甲臜染液;粘蛋白胭脂红
‑
原发性肿瘤染液;中性红;苯胺黑;尼罗蓝a;核固红c.i.60760;萘酚酯酶;氮蓝四唑
‑
不褪色甲臜染料;橙g;橙ii;地衣红;巴氏染液eas
‑
细胞质亮染;碱性副品红;副品红;过碘酸希夫氏染液
‑
(pas,特异性碳水化合物染液);焰红b;蛋白银s;派洛宁b;派洛宁y;刃天青;罗曼诺斯基
‑
姬姆萨;孟加拉玫瑰红;番红o;苏丹黑b;苏丹红iii
‑
(含α
‑
萘酚,对髓性粒细胞染色);苏丹红iv
‑
对甘油三脂染色;酒石黄
‑
(偶氮染料黄#5);硫堇
‑
对异染色质染色;三苯基四唑;ttc
‑
甲臜红色染料;甲苯胺蓝o;瑞氏染液
‑
(用于常规血涂片的固定剂、缓冲剂和染液);以及瑞氏
‑
姬姆萨。
568.通过有意义的尝试和实验,已经发现使用包含结晶紫、新亚甲蓝、番红o、伊红y和甲基绿中至少一者的粒子造影剂202可在粒子造影剂组合物210中实现出奇有效的结果,如本文更详细描述。以有效地对活细胞和/或基本上完整的细胞进行染色的量加入粒子造影剂202以用于基于图像的分类和子分类。粒子造影剂202可为上述粒子造影剂中两者或更多者的任何组合。可对粒子造影剂202进行选择以有效地获得活性细胞和/或基本上完整的细胞的“类似瑞氏”染色的图像。
569.在一个实施例中,粒子造影剂202包含结晶紫。结晶紫存在的量可足以实现染色条件下的约1μm至约100μm。如本文所用,术语“染色条件”是指组分与样品混合的时候。结晶紫存在的量可足以实现染色条件下的约6μm至约10μm。结晶紫存在的量可足以实现染色条件下的约7.8μm。结晶紫存在的量可足以实现染色条件下非常接近7.8μm。可将结晶紫纯化到至少90%纯。可将结晶紫纯化到至少91%、92%、93%、94%、95%、96%、97%或98%纯。可将结晶紫纯化到至少99%纯。粒子造影剂202可仅仅为结晶紫,或可为与一种或多种另外的粒子造影剂组合的结晶紫。
570.在一个实施例中,粒子造影剂202包含新亚甲蓝。新亚甲蓝存在的量可足以实现染色条件下的约70μm至约2.4mm。新亚甲蓝存在的量可足以实现染色条件下的约500μm至约950μm。新亚甲蓝存在的量可足以实现染色条件下的约735μm。新亚甲蓝存在的量可足以实现染色条件下非常接近735μm。可将新亚甲蓝纯化到至少70%纯。可将新亚甲蓝纯化到至少71%、72%、73%、74%、75%、76%、77%、78%、79%、80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%纯。可将新亚甲蓝纯化到至少100%纯。
571.在一些实施例中,当粒子造影剂202包含结晶紫和新亚甲蓝两者时,能实现出奇有效的结果。结晶紫与新亚甲蓝的比率可介于约1:1至约1:500(摩尔/摩尔)之间。结晶紫与新亚甲蓝的比率可介于约1:50至约1:160(摩尔/摩尔)之间。结晶紫与新亚甲蓝的比率可介于约1:90至约1:110(摩尔/摩尔)之间。
572.在一个实施例中,粒子造影剂202包含伊红y。伊红y存在的量可足以实现染色条件下的约3μm至约300μm。伊红y存在的量可足以实现染色条件下的约10μm至约50μm。伊红y存在的量可足以实现染色条件下的约27μm。伊红y存在的量可足以实现染色条件下非常接近27μm。可将伊红y纯化到至少80%纯。可将伊红y纯化到至少81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%纯。可将伊红y纯化到至少100%纯。
573.在一些实施例中,当粒子造影剂202为结晶紫、新亚甲蓝和伊红y的组合且各自具有如上所述的浓度和纯度的任何组合时,能实现出奇有效的结果。在一些实施例中,粒子造影剂202具体地是以足以实现约7.8μm的量存在的结晶紫、以足以实现约735μm的量存在的新亚甲蓝以及以足以实现约27μm的量存在的伊红y。在一些实施例中,粒子造影剂202具体地是以足以实现约7.8μm的量存在的至少99%纯结晶紫、以足以实现约735μm的量存在的至少99%纯新亚甲蓝以及以足以实现约27μm的量存在的至少99%纯伊红y。
574.在一个实施例中,粒子造影剂202包含番红o。番红o存在的量可足以实现染色条件下的约1μm至约100μm。番红o存在的量可足以实现染色条件下的约3μm至约30μm。番红o存在的量可足以实现染色条件下的约9μm。番红o存在的量可足以实现染色条件下非常接近9μm。可将番红o纯化到至少80%纯。可将番红o纯化到至少81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%纯。可将番红o纯化到至少100%纯。
575.在一个实施例中,粒子造影剂202包含甲基绿。甲基绿存在的量可足以实现染色条件下的约0.1g/l。甲基绿存在的量可足以实现染色条件下非常接近0.1g/l。可将甲基绿纯化到至少80%纯。可将甲基绿纯化到至少81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%纯。可将甲基绿纯化到至少100%纯。
576.在一些实施例中,粒子造影剂202包含一定量的结晶紫、新亚甲蓝、番红o、伊红y和甲基绿中的一者或多者,所述量能有效地例如通过增强呈递进行成像时的样品中的粒子的细胞内内容物特征而产生粒子中的视觉区别。粒子造影剂202存在的量可足以增强和/或染色中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞和嗜碱性粒细胞以及网织红细胞、有核红血细胞、血小板、母细胞、早幼粒细胞、中幼粒细胞、晚幼粒细胞或细胞碎片的亚细胞结
构。可视化区别或视觉区别可包括可使用任何光源(例如,uv、可见、ir)可视化或以其他方式可检测的任何粒子或粒子内特征。
577.在粒子造影剂组合物210包含两种或更多种粒子造影剂202的实施例中,可根据粒子造影剂202是否对用于粒子分类和子分类的视觉区别的产生具有独立、竞争性和/或增强性作用,适当地调节粒子造影剂202每者的量。
578.透化剂
579.在一些实施例中,透化剂204可包含表面活性剂。在一些实施例中,透化剂204可包含皂草苷。在替代实施例中,透化剂204可包含季铵盐、非离子表面活性剂和两性离子表面活性剂中的至少一者。透化剂可改变细胞的渗透性以增强粒子造影剂202对细胞内内容物的可及性。可对透化剂进行选择并且其含量足以允许快速一步染色工序。
580.非离子表面活性剂的例子可包括(1)聚氧乙烯烷基或芳基醚(聚乙氧基化物),包括与聚乙二醇或聚氧乙烯乙醇醚化的直链脂族疏水物,例如35;(2)与聚乙二醇醚化的支链脂族/芳族(例如,辛基酚)疏水物,例如triton
‑
100;(3)与聚乙二醇醚化的直链脂族/芳族(例如,正壬基酚)疏水物,例如c0897;以及(4)与聚乙二醇酯化的直链脂族(例如,羧酸)疏水物,例如53及其他。非离子聚氧乙烯烷基或芳基醚(聚乙氧基化物)表面活性剂的例子可包括聚氧乙烯(4)月桂醚(30);聚氧乙烯(23)月桂醚(35);聚氧乙烯(2)十六烷基醚(52);聚氧乙烯(20)十六烷基醚(58);聚氧乙烯(2)硬脂醚(72);聚氧乙烯(10)硬脂醚(76);聚氧乙烯(20)硬脂醚(78);聚氧乙烯(2)油基醚(92);聚氧乙烯(10)油基醚(96);聚氧乙烯(20)油基醚(98);聚氧乙烯(21)硬脂醚(721);聚氧乙烯(100)硬脂醚(700);及其他。非离子表面活性剂的另外例子可包括triton
‑
100(非还原和还原)、x
‑
114(非还原和还原)、triton
‑
165和triton
‑
305(非还原和还原)及其他。
581.在一个实施例中,透化剂204可包含35,其量足以产生染色条件下的约0.10g/l至约0.20g/l的浓度。35存在的量可足以产生染色条件下的约0.10g/l至约0.16g/l的浓度。35存在的量可足以产生约.012g/l至约0.14g/l的浓度。
582.两性离子表面活性剂的例子可包括tdaps(十四烷基二甲基铵基丙磺酸盐)、chapso(3
‑
[(3
‑
胆酰胺丙基)二甲氨基]
‑2‑
羟基
‑1‑
丙磺酸盐)、具有约12至约16个碳原子的烷基n,n
‑
二甲基n
‑
氧化物、月桂基二甲基胺n
‑
氧化物(lo)、ddaps(n
‑
十二烷基
‑
n,n
‑
二甲基
‑3‑
铵基
‑1‑
丙磺酸盐)及其他。
[0583]
在一些实施例中,透化剂204包含足以裂解红血细胞的试剂。在一些实施例中,透化剂204包含足以裂解红血细胞而非网织红细胞或有核红血细胞的试剂。在一些实施例中,透化剂204包含足以裂解红血细胞同时白血细胞、网织红细胞、有核红血细胞、血小板和其他细胞保持基本上完整的试剂。在一些实施例中,透化剂204使白血细胞、网织红细胞、有核红血细胞和/或血小板的成员和/或核膜更具渗透性和/或多孔以有利于粒子造影剂202进
入。
[0584]
在一些实施例中,可对透化剂204进行选择以能够快速形成允许粒子造影剂202进入样品的细胞所需的孔或开口。
[0585]
通过有意义的尝试和实验,已经发现使用包含得自位于佛罗里达州劳德代尔堡(ft.lauderdale,florida)的临床诊断解决方案公司(clinical diagnostic solutions(cds))的5pd
‑
裂解剂的透化剂204,可在粒子造影剂组合物210的一些实施例中实现出奇有效的结果。5pd
‑
裂解剂包含皂草苷。5pd
‑
裂解剂总体在以引用方式并入本文的美国专利6,632,676中描述。
[0586]
通过有意义的尝试和实验,已经发现使用包含皂草苷的透化剂204可在粒子造影剂组合物210的一些实施例中实现出奇有效的结果,所述皂草苷存在的量足以产生染色条件下的约10mg/l至约1000mg/l的浓度。在一些实施例中,皂草苷存在的量足以产生约50mg/l至约750mg/l的浓度。在一些实施例中,皂草苷可为季铵取代的皂草苷醚。
[0587]
固定剂
[0588]
在一些实施例中,可对固定剂206进行选择以确保白血细胞在染色和成像期间不会降解。在一些实施例中,固定剂206可确保其他细胞和细胞结构不会降解。固定剂的例子可包括戊二醛;甲醛;交联剂;等渗盐水中的苦味酸铵(例如,用于亚甲蓝染色);乙醇;甲醇(例如,在室温、
‑
20℃或
‑
70℃下);海登海因
‑
苏萨液
–
hgcl2、nacl三氯乙酸、福尔马林;布安液
–
苦味酸、福尔马林、乙酸;杜
‑
布氏液
–
含80%乙醇的布安液;卡诺氏液
–
乙醇、氯仿、乙酸;岑克尔氏液
–
hgc
l2
、k2cro7、naso4.h2o;醋酸洋红;gatensby氏液
–
铬酸、四氧化锇、nacl;贝克氏液
–
福尔马林、cacl2;史密斯氏液
–
k2cr2o7、福尔马林、乙酸;1%甲基绿、1%乙酸;苯酚、福尔马林、甘油、龙胆紫;肖氏液
–
hgcl2、乙醇、乙酸;尚皮氏液
–
铬酸、k2cro7、oso4;弗来明氏液
–
铬酸、oso4、乙酸;甲醛
‑
银
–
甲醛、agno3;斯特莱科组织固定剂
–
溴代硝基丙二醇、二偶氮烷基脲、znso
4.
7h2o、柠檬酸钠;pbs中的1%咪唑烷基脲;乙二醛:glyofix、prefer、safefix、histochoice;glydant
‑
乙内酰脲;二羟甲基脲;羟甲基甘氨酸钠;karnovsky氏液;氯化汞(b
‑
5);hollande氏液;及其他。另外,合适的示例性固定剂可包括单独或组合的任何下列物质。
[0589]
在一些实施例中,固定剂206可为氧化剂、汞化合物、苦味酸盐、羟乙基哌嗪乙磺酸
‑
谷氨酸缓冲剂介导的有机溶剂保护效应(hope)固定剂、或水溶性防腐剂。氧化剂的例子包括重铬酸钾、铬酸、高锰酸钾及其他。汞化合物的例子包括b
‑
5、岑克尔氏固定液及其他。水溶性防腐剂的例子包括对羟基苯甲酸甲酯、对羟基苯甲酸丙酯、二羟甲基脲、2
‑
吡啶硫醇
‑1‑
氧化物、山梨酸、山梨酸钾及其他。
[0590]
通过有意义的尝试和实验,已经发现使用包含戊二醛和甲醛中至少一者的固定剂206可在粒子造影剂组合物210的一些实施例中实现出奇有效的结果。
[0591]
在一些实施例中,可通过使用包含等于或低于0.1重量%的戊二醛的固定剂206实现出奇有效的结果。
[0592]
另外的组分
[0593]
在一些实施例中,可任选地在方框208处将任选的另外组分212组合到粒子造影剂组合物210中。另外组分212的例子可包括缓冲组分、粘度改性剂、抗微生物剂、渗透调节剂、离子强度改性剂、表面活性剂、螯合剂及其他。在一些实施例中,当粒子造影剂组合物210包
含磷酸盐缓冲盐水时,可实现出奇有效的结果。
[0594]
示例性粘度改性剂包括天然水解胶体(及衍生物),诸如角叉菜胶、刺槐豆胶、瓜耳胶和明胶;糖类(及衍生物),诸如右旋糖、果糖;聚右旋糖;葡聚糖;多聚葡聚糖;糖类;和多糖;半合成水解胶体(及衍生物),诸如甲基纤维素、羧甲基纤维素;合成水解胶体(及衍生物),诸如以及粘土(及衍生物),诸如膨润土和
[0595]
快速一步染色方法
[0596]
图a2是根据一个实施例的快速一步染色方法300的流程图。虽然快速一步染色方法300可包含若干子步骤,但术语“一步”用来标识在染色工序期间不需要将样品引入多种不同溶液中。在方框302处制备粒子造影剂组合物210,如上文参照图a1所述。任选地,在一些实施例中,可在方框306处纯化组分,诸如任何粒子造影剂202。纯化粒子造影剂202可减少在与样品接触时形成的沉淀物的水平,从而减少背景并且改善基于图像的血样分析的结果,且降低了进一步检查图像或载片或者手动准备显微镜检的需要。
[0597]
在方框308处,将粒子造影剂组合物210与样品组合。可以任何合适的方式将粒子造影剂组合物210与样品组合,包括混合在一起。在方框308处的组合可包括用特定量的粒子造影剂组合物210稀释样品。可用粒子造影剂组合物210稀释样品。可对稀释的量进行选择以提供基于图像的分析期间每帧的最佳数量的细胞。可对稀释的量进行选择以提供基于图像的分析期间每帧的最佳数量的白血细胞。可另外对稀释的量进行选择以为任何其他非基于图像的分析提供最佳体积。
[0598]
通过有意义的尝试和实验,已经发现使用介于约2:1至约20:1之间的粒子造影剂组合物210与样品的比率可在粒子造影剂组合物210的一些实施例中实现出奇有效的结果。粒子造影剂组合物210与样品的比率可介于约3:1至约10:1之间。粒子造影剂组合物210与样品的比率可介于约3:1至约4:1之间。粒子造影剂组合物210与样品的比率可介于约3:1或约4:1之间。在一些实施例中,使用非常接近3:1或非常接近4:1的粒子造影剂组合物210与样品的比率可实现出奇有效的结果。
[0599]
可通过使用含40ml的5pd
‑
裂解剂和50ml的磷酸盐缓冲盐水的粒子造影剂以及10:1粒子造影剂组合物210与样品的稀释比率,实现出奇有效的结果。可通过使用含40ml的5pd
‑
裂解剂、额外皂草苷和40ml的磷酸盐缓冲盐水的粒子造影剂以及5:1粒子造影剂组合物210与样品的稀释比率,实现出奇有效的结果。可通过使用含40ml的5pd
‑
裂解剂、额外皂草苷和36ml的磷酸盐缓冲盐水的粒子造影剂以及4:1粒子造影剂组合物210与样品的稀释比率,实现出奇有效的结果。
[0600]
在一些实施例中,在高温下,诸如下文结合温育所述的任何温度,将样品与粒子造影剂组合物210组合。
[0601]
如本文所用,组合的样品和粒子造影剂组合物210称为样品混合物。
[0602]
在方框310处,将样品混合物在特定温度下温育特定时长。温育可增强细胞或其内部结构的渗透性,允许粒子造影剂202更好地渗入细胞或细胞结构。可对温育的时间和温度进行选择以使粒子造影剂组合物210能够适当地渗透、固定和染色样品。可对温育的时间和温度进行选择以确保红血细胞的裂解同时保持白血细胞、血小板和有核红血细胞基本上完整。
[0603]
通过有意义的尝试和实验,已经发现样品混合物在约37℃与约60℃之间的温度下
温育约1至60秒的情况下可在粒子造影剂组合物210的一些实施例中实现出奇有效的结果。可将样品混合物加热至约46℃与约49℃之间的温度。可将样品混合物温育40至50秒。可将样品混合物温育最多至一小时。在一些实施例中,可通过将样品混合物在约48℃下温育约45秒,实现出奇有效的结果。在一些实施例中,可通过将样品混合物在约47℃下温育约45秒,实现出奇有效的结果。
[0604]
在一些实施例中,在方框308处的组合和在方框310处的温育以与在成像设备中处理样品混合物所花的时间和冲洗和/或清洗成像设备的管路所花的时间大约相同的时长或较之更短的时长完成。这样,可在组合和温育第二样品混合物的同时使第一样品混合物成像。一旦第一样品混合物已成像并且成像设备已清洗,第二样品混合物就可立即成像。
[0605]
在替代实施例中,在方框308处的组合和在方框310处的温育以比在成像设备中处理样品混合物所花的时间和冲洗和/或清洗成像设备的管路所花的时间少两倍的时间完成。这样,当第一样品混合物正成像时,第二样品混合物可准备好成像,并且第三样品混合物和第四样品混合物可正处于组合和温育的过程中。一旦第一样品混合物已成像并且成像设备已清洗,第二样品混合物就可立即成像。第三样品混合物可正完成其组合和温育并且第四样品混合物可仍然在组合和温育。一旦第二样品混合物已成像并且成像设备已清洗,第三样品混合物就可立即成像,同时第四样品混合物开始完成组合和温育并且第五样品混合物开始组合和温育。该过程可无限期地继续以使样品混合物连续地成像。
[0606]
通过有意义的尝试和实验,已经发现通过粒子造影剂组合物210的某些实施例、将粒子造影剂组合物210与样品组合的某些方式、以及温育样品混合物的某些方式的组合,可实现出奇有效的结果。
[0607]
具体而言,可通过使用包含如下的粒子造影剂组合物210实现出奇有效的结果:染色条件下约7.8μm的90%纯或更纯的结晶紫、染色条件下约735μm的70%纯或更纯的新亚甲蓝、染色条件下约27μm的80%纯或更纯的伊红
‑
y、染色条件下约50mg/l至约750mg/l的预处理皂草苷、以及染色条件下约0.1%或更小的戊二醛;其中以约3:1与约4:1之间的粒子造影剂210与样品的比率将粒子造影剂210与样品组合;并且其中将所得样品混合物在约48℃下温育约45秒。
[0608]
某些有效粒子造影剂组合物210和染色工序由于使用非基于醇的溶剂体系中的染料使得利用自动化视觉分析仪能够有效地获得活细胞和/或基本上完整的细胞的“类似瑞氏”染色的图像。某些有效粒子造影剂组合物210和染色工序能够对样品进行快速染色使得各种细胞组分、核裂片和粒状结构清晰可辨。某些有效粒子造影剂组合物210和染色工序适用于离体活体染色。某些有效粒子造影剂组合物210和染色工序产生用于粒子分类和子分类的视觉区别。某些有效粒子造影剂组合物210和染色工序能有效地增强血清、脑脊髓液、胸膜液、滑膜液、精液、腹膜液、羊膜液、灌洗液、骨髓穿刺液、渗漏液、渗出液或血样中的粒子的细胞内内容物特征。某些有效粒子造影剂组合物210和染色工序能有效地对中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞、嗜碱性粒细胞、血小板、网织红细胞、有核红血细胞、母细胞、早幼粒细胞、中幼粒细胞、晚幼粒细胞、管型、细菌、上皮细胞和/或寄生生物进行染色。某些有效粒子造影剂组合物210和染色工序能有效地产生用于粒子分类和子分类的视觉区别,例如通过提供细胞中的主要和次要颗粒的差异染色,诸如以便基于主要和次要颗粒的差异染色或增强来帮助未成熟粒细胞的子分类及其年龄测定。某些有效粒子造影
剂组合物210和染色工序能有效地产生用于计数和表征红血细胞、网织红细胞、有核红血细胞和血小板以及用于白血细胞分类计数及白血细胞表征和分析的视觉区别。某些有效粒子造影剂组合物210和染色工序能有效地在具有保持基本上完整的结构的一种和/或多种活性细胞和/或活细胞中产生视觉区别。某些有效粒子造影剂组合物210和染色工序能有效地对中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞和嗜碱性粒细胞以及网织红细胞、有核红血细胞、血小板、母细胞、早幼粒细胞、中幼粒细胞、晚幼粒细胞或细胞碎片的亚细胞结构进行染色。
[0609]
由本文所述的某些有效粒子造影剂组合物210和染色工序所实现的快速染色可与手动或半自动化成像和/或分析工序一起使用。
[0610]
通过有意义的尝试和实验,已经发现可用包含非基于醇的溶剂体系中的粒子造影剂的粒子造影剂组合物210的某些实施例来实现出奇有效的结果,据本发明人所知,所述粒子造影剂首次产生活细胞和/或基本上完整的细胞的“类似瑞氏”染色的图像,所述图像可揭示各种细胞组分、核裂片和粒状结构并使这些粒子和/或细胞特征在视觉上不同。
[0611]
通过有意义的尝试和实验,已经发现当使用如表a1中所列组成的粒子造影剂组合物210时可实现出奇有效的结果,其中通过将40ml的新甲基蓝与5ml的结晶紫混合来制备工作染色试剂。
[0612]
表a1
[0613]
50ml磷酸盐缓冲盐水40ml工作染色试剂40mlcds 5pd
‑
裂解剂中的0.09%新甲基蓝5mlcds 5pd
‑
裂解剂中的0.009%结晶紫10ml0.5%皂草苷足以实现染色条件下的0.1%的量戊二醛
[0614]
图a3是用表a1中所示粒子造影剂组合物210染色并使用上述快速一步染色工序染色的样品中的所选白血细胞的代表性图示。白血细胞完好无损并且显示出瑞氏染液的染色特性。各种类型的白血细胞(例如,中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞、嗜碱性粒细胞等等)是视觉上可辨的。
[0615]
在一些实施例中,由本发明的粒子造影剂组合物所染色的细胞的特征记录于表a2中。
[0616]
表a2
[0617]
[0618][0619]
在某些实施例中,染液/染料组合物被配制成具有稳定性、易于贮存、处理和/或有限的毒性。
[0620]
图a4是用根据一个实施例的粒子造影剂组合物210染色的样品中的所选白血细胞的代表性图示,包括通过手动、湿法封片成像和自动流动成像所成像的细胞。
[0621]
早期实验
[0622]
如参照以下实例所述,测试并修改了多种染色组合物和方法以便得到上文所公开的实施例。
[0623]
在早期实例1中,存在两步染色方法,其中将样品和粒子造影剂组合物的早期实施例组合并在47.5℃下温育40秒,然后将猝灭试剂施加到样品混合物中。粒子造影剂组合物包含coulter lh系列稀释剂、coulter lyse s iii diff裂解试剂、coulter lh系列pak试剂盒以及coulter lh系列retic pak试剂盒。结果示于图a5。
[0624]
在实例1之后的早期实例2中,将实例1的两步染色方法替换为一步染色方法。与实例1的结果相比嗜碱性粒细胞的改善结果示于图a6。
[0625]
在早期实例3中,不含戊二醛的粒子造影剂组合物会产生变弱的白血细胞,这些白血细胞会由于流通池中的剪切力而碎裂。图a7中示出了显示膜受损的实例3的结果的图像。
[0626]
在实例3之后的早期实例4中,将戊二醛加入粒子造影剂组合物中。白血细胞膜在实例4中更为完整,但核膜仍然受损。在调整适应于pioal以降低甘油含量之后,白血细胞的形态在成像期间大部分未变化,如图a8所示。
[0627]
在使用新亚甲蓝和结晶紫的粒子造影剂组合物时具有双染料染色剂的早期实例中,大多数细胞类型是区别明显的,例外的是嗜酸性粒细胞,其在一定程度上不一致并且不总是易于与中性粒细胞区分开,如图a9所示。在后续的实例5和6中,将第三粒子造影剂加入粒子造影剂组合物中。
[0628]
在实例5中,将甲基绿加入粒子造影剂组合物中。甲基绿有助于对嗜酸性粒细胞更好地染色,但细胞的核不再能染上所需的紫色,而是蓝色。图a10描绘了实例5中性粒细胞的
图像,其中核被染成蓝色,但损失了粒状细节。
[0629]
在实例6中,使用伊红
‑
y代替甲基绿作为粒子造影剂组合物中的第三粒子造影剂。伊红
‑
y保留细胞核的紫色染色,并且颗粒一致地染上略微橙色光泽,如图a11所示。
[0630]
通过上述实验和另外的实验,已确定所公开的实施例和要求保护的实施例能提供优选的结果。
[0631]
可使用计算机或具有硬件、软件和/或固件的其他处理器来执行本文描述的计算或操作中的每一个。各个方法步骤可通过模块执行,并且所述模块可包括被布置用于执行本文所述的方法步骤的多种多样的数字和/或模拟数据处理硬件和/或软件中的任何一种。所述模块任选地包括数据处理硬件,该数据处理硬件由于具有与其相关联的适当机器编程代码而适于执行这些步骤中的一个或多个,用于两个或更多个步骤(或两个或更多个步骤的部分)的模块被集成到单个处理器板中或采用多种多样的集成式和/或分布式处理架构中的任何一种被分成不同的处理器板。这些方法和系统通常将采用有形介质,该有形介质收录有用于执行上述方法步骤的指令的机器可读代码。合适的有形介质可包括存储器(包括易失性存储器和/或非易失性存储器)、存储介质(诸如软盘、硬盘、磁带等上的磁记录;光学存储器诸如cd、cd
‑
r/w、cd
‑
rom、dvd等上的磁记录;或任何其他数字或模拟存储介质),等等。
[0632]
本发明中所论述的所有专利、专利公布、专利申请、期刊论文、书籍、技术参考手册等全文以引用方式并入本文中以用于所有目的。
[0633]
在附图中描绘或上文所述的组件的不同布置,以及未示出或描述的组件和步骤也是可行的。相似地,一些特征结构和子组合是可用的,且它们可以在与其他特征结构和子组合无关的情况下被采用。出于例示性和非限制性的目的描述了本发明的实施例,但可供选择的实施例对于本专利的读者而言将是显而易见的。在某些情况下,方法步骤或操作可按不同的顺序执行或实施,或者可对操作进行添加、删除或修改。应当理解,在本发明的某些方面,可用多个部件来替换单个部件,并且可用单个部件来替换多个部件,以提供元件或结构或者执行给定的一种或多种功能。除了这种替换将不能有效实践本发明的某些实施例的情况之外,这种替换被视为在本发明的范围之内。因此,本发明不限于上文所述或在附图中描绘的实施例,并且可以在不脱离以下权利要求的范围的前提下,创造各种实施例和进行各种修改。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1