一种HER2生物制剂的抗体检测试剂盒及制备方法与流程
一种her2生物制剂的抗体检测试剂盒及制备方法
技术领域
1.本发明涉及抗体检测技术领域,具体而言,涉及一种her2生物制剂的抗体检测试剂盒及制备方法。
背景技术:
2.her2(人表皮生长因子受体2)是具有酪氨酸激酶活性的表皮生长因子受体家族的一个成员。受体的聚合作用会导致受体酪氨酸残基的磷酸化,并启动多种信号通路导致细胞增殖和肿瘤发生。大约15%~30%乳腺癌和10%~30%的胃癌会发生her2基因扩增或过度表达。her2基因的过度表达不仅与肿瘤的发生发展关系密切,也是临床预后的重要指标。
3.以her2为靶点而设计的单抗药物包括曲妥珠单抗(trastuzumab)和帕妥珠单抗 (pertuzumab)_被fda批准用于治疗乳腺癌、转移性乳腺癌或转移性胃癌等疾病。
4.尽管临床实践证明此类生物制剂在治疗上述疾病时获得良好的疗效,但不是所有的患者均有效,有些患者一开始就无效(原发性无效),更多的患者表现为开始时有效,但在使用多次后产生耐药而无效(继发无效)。进一步的研发发现,继发无效者跟体内产生抗生物制剂药物的抗体有关,因此,检测血液中抗生物制剂的抗体是一项重要的伴随诊断。
5.鉴于此,特提出本发明。
技术实现要素:
6.本发明的目的在于提供一种her2生物制剂的抗体检测试剂盒及制备方法以解决上述技术问题。
7.现有的抗her2的抗体检测方法存在假阳性和假阴性的问题。经发明人研究发现,假阴性的问题根源在于:双抗原夹心方法在捕获样本中的抗her2的抗体后,存在与后续的检测抗体元件结合效率的问题,导致本来是阳性样本而无法检测出,导致假阴性。
8.假阳性的问题根源在于:受样本中大量的无关抗体干扰,导致假阳性等检测失真。
9.本发明是这样实现的:本发明提供了一种her2生物制剂的抗体检测试剂盒,其包括抗体捕获器件和抗体检测器件,抗体捕获器件包括固相载体,抗体检测器件为纤维素膜或带有可被检测的标记物的功能性片段;且在固相载体上包被有her2生物制剂,在纤维素膜上固定有不带标记物的功能性片段;功能性片段为her2生物制剂的可变区、重链可变区或互补决定区。
10.发明人发现:用her2生物制剂作为捕获抗原,由于空间接触面大,更容易捕获到样本中的抗抗体,具有捕获效率高的优点。而借助双抗原夹心的方法实现抗抗体的检测,可以极大程度上规避大量的无关抗体干扰,提高检测准确度,避免假阳性的发生。
11.捕获后形成的抗原-抗体复合物本身具有较大的位阻,如果抗体检测器件的分子量较大(比如生物制剂),则较难与复合物中抗抗体的另一个fab结合。发明人发现小分子量的her2生物制剂的可变区、重链可变区或互补决定区具有位阻小,更易于被抗抗体fab结合的优势,以其作为抗体检测器件,可以提高抗原-抗体复合物与检测抗体元件结合效率,提
高检测的灵敏度,避免假阴性的发生。达到her2生物制剂药物的伴随诊断目的。
12.在一种可选的实施方式中,上述功能性片段通常具有与其来源抗体相同的结合特异性。上述可变区(fv)的检测抗原为:由重链可变区和轻链可变区通过连接肽或二硫键连接以保持fv的稳定性的fv(可变区)。互补决定区包含重链互补决定区中的cdr1、cdr2及cdr3和轻链互补决定区中的cdr1、cdr2及cdr3。本领域技术人员根据本发明记载的内容易理解到,上述抗体的功能性片段可以通过比如酶消化的方法(包括胃蛋白酶或木瓜蛋白酶)和/或通过化学还原分裂二硫键的方法获得。在本发明公开了完整抗体的结构基础上,本领域技术人员容易获得上述的功能性片段。
13.上述抗体的功能性片段还可以通过本领域技术人员所知的重组遗传学技术(如基因重组的方法重组表达)或通过例如自动肽合成仪,比如applied biosystems等销售的自动肽合成仪合成获得。
14.在本发明应用较佳的实施方式中,上述her2生物制剂选自her2的单抗药物。
15.在一种可选的实施方式中,her2的单抗药物包括不限于曲妥珠单抗(trastuzumab)、帕妥珠单抗 (pertuzumab)_。
16.在一种可选的实施方式中,固相载体选自荧光微球、乳胶微球、树脂微球、磁性微球、胶体金颗粒、量子点、微孔板或微孔膜。上述胶体金即四氯金酸经还原剂还原后得到的胶体溶液。在其他实施方式中,上述胶体金也可以是其他的胶体物质,例如胶体碳、胶体银或胶体硒。
17.在一种可选的实施方式中,上述量子点为核壳型量子点,如zns/cdse或zns/cdte形成的量子点。此外,在其他实施方式中,根据需要,上述量子点可以调整为单一化合物形成的量子点,如硒化镉(cdse)、硫化锌(zns)、碲化镉(cdte)、硫化镉(cds)、硒化锌(znse)、磷化铟(inp)或砷化铟(inas),或是cdse核上包裹一层zns或cds组成的纳米晶或半导体纳米晶等物质中的一种。
18.在一种可选的实施方式中,固相载体上包被的her2生物制剂上修饰有亲和素或生物素,修饰亲和素或生物素有利于进一步提高检测信号的放大,提高检测的灵敏度。需要说明的是,在一种可选的实施方式中,也可以根据需要在her2生物制剂上选择不修饰亲和素或生物素。
19.在一种可选的实施方式中,固相载体上包被有her2物制剂全长。用her2生物制剂全长作为捕获抗原,由于空间接触面大,更容易捕获到样本中的抗her2生物制剂的抗体(即抗抗体),具有捕获效率高的优点。通过在捕获器件上包被her2生物制剂全长,可以更好地避免假阳性的发生。
20.在一种可选的实施方式中,荧光微球选自时间分辨荧光微球或含荧光素的荧光微球,磁性微球选自磁珠。在一种可选的实施方式中,上述含荧光素的荧光微球的荧光激发波长为300~520nm,发射波长为340~630nm,微球直径范围为100nm~1000nm。
21.含荧光素的荧光微球包括不限于:蓝色荧光微球、绿色荧光微球、红色荧光微球或绿色与红色干荧光微球。
22.时间分辨荧光物质为镧系元素、镧系元素与乳胶的结合物、镧系元素的螯合物中的一种;镧系元素可以为铕,铽,钐或镝中的任意一种。
23.可被检测的标记物是指具有能够被肉眼直接观察或被仪器检测或探测到的特性
例如发光、显色、放射性等特性的一类物质,通过该特性可以实现对相应目标物的定性或定量检测。
24.在一种可选的实施方式中,可被检测的标记物包括不限于荧光染料、催化底物显色的酶、放射性同位素、化学发光试剂或纳米颗粒类标记物。
25.在一种可选的实施方式中,荧光染料包括但不限于荧光素类染料及其衍生物(例如包括但不限于异硫氰酸荧光素(fitc)羟基光素(fam)、四氯光素(tet)等或其类似物)、罗丹明类染料及其衍生物(例如包括但不限于红色罗丹明(rbitc)、四甲基罗丹明(tamra)、罗丹明b(tritc)等或其类似物)、cy系列染料及其衍生物(例如包括但不限于cy2、cy3、cy3b、cy3.5、cy5、cy5.5、cy3等或其类似物)、alexa系列染料及其衍生物(例如包括但不限于alexafluor350、405、430、488、532、546、555、568、594、610、33、647、680、700、750等或其类似物)和蛋白类染料及其衍生物(例如包括但不限于藻红蛋白(pe)、藻蓝蛋白(pc)、别藻蓝蛋白(apc)、多甲藻黄素-叶绿素蛋白(precp)等)。
26.在一种可选的实施方式中,催化底物显色的酶包括不限于辣根过氧化物酶、碱性磷酸酶、β-半乳糖苷酶、葡萄糖氧化酶、碳酸酐酶、乙酰胆碱酯酶以及6-磷酸葡萄糖脱氧酶。
27.在一种可选的实施方式中,放射性同位素选自
212
bi、
131
i、
111
in、
90
y、
186
re、
211
at、
125
i、
188
re、
153
sm、
213
bi、
32
p、
94
mtc、
99
mtc、
203
pb、
67
ga、
68
ga、
43
sc、
47
sc、
110
min、
97
ru、
62
cu、
64
cu、
67
cu、
68
cu、
86
y、
88
y、
121
sn、
161
tb、
166
ho、
105
rh、
177
lu、
172
lu和
18
f;在一种可选的实施方式中,化学发光试剂包括不限于鲁米诺及其衍生物、光泽精、甲壳动物荧光素及其衍生物、联吡啶钌及其衍生物、吖啶酯及其衍生物、二氧环乙烷及其衍生物、洛粉碱及其衍生物或过氧草酸盐及其衍生物。
28.在一种可选的实施方式中,纳米颗粒类标记物选自纳米颗粒和胶体。
29.在一种可选的实施方式中,胶体选自胶体金属、分散型染料、染料标记的微球和乳胶;在一种可选的实施方式中,胶体金属包括不限于胶体金、胶体银、胶体碳或胶体硒。
30.在一种可选的实施方式中,纳米颗粒选自有机纳米颗粒、磁性纳米颗粒、量子点纳米颗粒或稀土络合物纳米颗粒。
31.在一种可选的实施方式中,纤维素膜上还固定有质控抗体作为质控t线,且功能性片段与质控抗体分别间隔设置;在一种可选的实施方式中,纤维素膜选自醋酸纤维素膜或硝酸纤维素膜。
32.在一种可选的实施方式中,可变区(fv)包含通过二硫键或连接肽连接的重链可变区和轻链可变区。曲妥珠单抗的重链可变区和轻链可变区分别如seq id no.1-2所示:seq id no.1:evqlvesggglvqpggslrlscaasgfnikdtyihwvrqapgkglewvariyptngytryadsvkgrftisadtskntaylqmnslraedtavyycsrwggdgfyamdywgqgtlvtvss;seq id no.2:diqmtqspsslsasvgdrvtitcrasqdvntavawyqqkpgkapklliysasflysgvpsrfsgsrsgtdftltisslqpedfatyycqq hyttpptfgqgtkveikrtv。
33.曲妥珠单抗的互补决定区包括通过二硫键或连接肽连接的cdr1-vh1、cdr2
ꢀ–
vh2、cdr3
–
vh3、cdr1-vl1、cdr2
ꢀ–
vl2和cdr3
–
vl3:
cdr1-vh1:dtyih;cdr2-vh2:riyptngytryadsvkg;cdr3-vh3:wggdgfyamdy;cdr1-vl1:rasqdvntava;cdr2-vl2:sasflys;cdr3-vl3:qqhyttppt。
34.帕妥珠单抗的重链可变区和轻链可变区分别如seq id no.3-4所示:seq id no.3:evqlvesggglvqpggslrlscaasgftftdytmdwvrqapgkglewvadvnpnsggsiynqrfkgrftlsvdrskntlylqmnslraedtavyycarnlgpsfyfdywgqgtlvtvss。
35.seq id no.4:diqmtqspsslsasvgdrvtitckasqdvsigvawyqqkpgkapklliysasyrytgvpsrfsgsgsgtdftltisslqpedfatyycqqyyiypytfgqgtkveikrtv。
36.帕妥珠单抗的互补决定区包括通过二硫键或连接肽连接的cdr1-vh1、cdr2
ꢀ–
vh2、cdr3
–
vh3、cdr1-vl1、cdr2
ꢀ–
vl2和cdr3
–
vl3:cdr1-vh1:dytmd;cdr2-vh2:dvnpnsggsiynqrfkg;cdr3-vh3:nlgpsfyfdy;cdr1-vl1:kasqdvsigva;cdr2-vl2:sasyryt;cdr3-vl3:qqyyiypyt。
37.需要说明的是,在其他的实施例中,本发明提供的her2生物制剂的可变区、重链可变区或互补决定区的氨基酸序列可以与上述对应可变区、重链可变区或互补决定区可以具有至少80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同源性。
38.在一种可选的实施方式中,her2生物制剂的抗体检测试剂盒为定量检测试剂盒或定性检测试剂盒。
39.在一种可选的实施方式中,her2生物制剂的抗体检测试剂盒为荧光免疫层析检测试剂盒、胶体金免疫层析检测试剂盒、量子点荧光免疫层析检测试剂盒、酶联免疫检测试剂盒或化学发光检测试剂盒;在一种可选的实施方式中,荧光免疫层析检测试剂盒为时间分辨荧光免疫层析检测试剂盒。
40.本发明还提供了一种her2生物制剂的抗体检测试剂盒的制备方法,其包括:将her2生物制剂全长固定在固相载体上作为抗体捕获器件,将不带标记物的功能性片段结合或固定在纤维素膜上或者对功能性片段进行标记物标记作为抗体检测器件。
41.在一种可选的实施方式中,当固相载体选自微孔板时,在将her2生物制剂全长固定在微孔板前,还包括将链霉亲和素包被在微孔板上,然后将修饰有生物素的her2生物制剂全长与包被有链霉亲和素的微孔板进行孵育。
42.本发明具有以下有益效果:
本发明用her2生物制剂作为捕获抗原,由于空间接触面大,更容易捕获到样本中的抗抗体,具有捕获效率高的优点。而借助双抗原夹心的方法实现抗抗体的检测,可以极大程度上规避大量的无关抗体干扰,提高检测准确度,避免假阳性的发生。
43.捕获后形成的抗原-抗体复合物本身具有较大的位阻,发明人发现小分子量的her2生物制剂的可变区、重链可变区或互补决定区具有位阻小,更易于被抗抗体fab结合的优势,以其作为抗体检测器件,可以提高抗原-抗体复合物与检测抗体元件结合效率,提高检测的灵敏度,避免假阴性的发生。达到her2生物制剂药物的伴随诊断目的。
44.附图说明
45.为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
46.图1是本发明抗曲妥珠单抗抗体时间分辨荧光免疫层析试纸的装置图;图2是本发明抗帕妥珠单抗抗体酶联免疫测定试剂盒检测原理图;图3是本发明抗曲妥珠单抗抗体化学发光测定试剂盒检测原理图;图4是本发明抗曲妥珠单抗抗体时间分辨荧光免疫层析试剂盒校准曲线回归图;图5是本发明抗帕妥珠单抗抗体酶联免疫测定试剂盒校准曲线回归图;图6是本发明抗曲妥珠单抗抗体化学发光测定试剂盒校准曲线回归图;附图标记:1-样品垫;2-结合垫;3-硝酸纤维素膜;4-检测线;5-质控线;6-吸水膜;7-背衬底板。
47.具体实施方式
48.为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
49.以下结合实施例对本发明的特征和性能作进一步的详细描述。
50.本发明提供的试剂盒的工作原理如下,1)用her2生物制剂的固定固相载体,用于捕获待检样本中的抗抗体,由于her2生物制剂的分子空间作用面大,能高效捕获样本中的抗抗体,形成抗原-抗体复合物;2)用her2生物制剂的可变区、重链可变区或互补决定区作为检测抗原,由于分子量较小,能有效克服位阻,与抗原-抗体复合物中抗体的另一个fab结合,形成抗原-抗体-抗原复合物,该复合物用周知的显色方法进行定量或定性检测。
51.实施例1本实施例提供了一种抗曲妥珠单抗抗体时间分辨荧光免疫层析定量检测试剂盒及其制备方法。
52.参照图1 所示,该试纸是在背衬底板7上设置有硝酸纤维素膜3、样品垫1、结合垫2
和吸水膜6,样品垫1叠压在结合垫2一端,结合垫2另一端和吸水膜6分别叠压在硝酸纤维素膜3的两端上;该结合垫2上包被有时间分辨荧光微球标记的曲妥珠单抗和时间分辨荧光微球标记的羊抗鸡igy抗体2;该硝酸纤维素膜3上设有检测线4(t线)和质控线5(c线),检测线4(t线)包被有曲妥珠单抗的可变区fv,质控线5(c线)包被有鸡igy抗体。
53.曲妥珠单抗的可变区(fv)包含通过二硫键连接的曲妥珠单抗重链可变区和曲妥珠单抗轻链可变区,其中曲妥珠单抗重链可变区序列如下:seq id no.1:evqlvesggglvqpggslrlscaasgfnikdtyihwvrqapgkglewvariyptngytryadsvkgrftisadtskntaylqmnslraedtavyycsrwggdgfyamdywgqgtlvtvss;曲妥珠单抗轻链可变区序列如下:seq id no.2:diqmtqspsslsasvgdrvtitcrasqdvntavawyqqkpgkapklliysasflysgvpsrfsgsrsgtdftltisslqpedfatyycqq hyttpptfgqgtkveikrtv。
54.制备方法如下:1)时间分辨荧光微球的标记取时间分辨荧光微球500μl(300nm)(1%原液),13000rpm,4℃离心10min,弃上清。加入10mg/ml 的edc,反应15min;离心,弃上清,加硼酸盐缓冲液(20mm,ph8.0)1000μl,超声10秒混匀;加入标记抗体(乌司奴单抗或羊抗鸡igy) 100μg(标记浓度100μg /ml),室温反应2h;离心,弃上清,加入封闭液,反应1h;离心,弃上清,加入1000μl硼酸盐缓冲液,超声混匀,做好标签,4℃保存待用。
55.2)样品垫、结合垫的处理聚酯膜用含有表面活性剂的缓冲液( 配方:20mm ph 8.0 bb,其中含有2%bsa、0.5%s9和2%海藻糖 )浸泡进行预封闭,37℃干燥过夜,制备得到结合垫;取制备好的结合垫,以金标hm3035喷金划膜仪,将标记有时间分辨荧光微球的曲妥珠单抗和羊抗鸡igy抗体混合后,以3μl/cm喷至预处理过宽为1cm的结合垫上,37℃干燥,干燥时间3h,制备得到特异性结合垫。
56.玻璃纤维素膜用含有表面活性剂的缓冲液( 配方:100mm ph 7.4 pb,其中含有2%bsa、0.5%s9 )浸泡进行预封闭后,37℃干燥过夜,裁切为30*1.5cm制备得到样品垫。
57.3)硝酸纤维素膜(nc膜)的包被氨基酸合成方法合成曲妥珠单抗的可变区,经验证,用该合成多肽包被酶标板,能与抗曲妥珠单抗抗体反应。
58.将nc膜贴至背衬底板的指定位置,用50mm的ph 7.4磷酸盐缓冲液将曲妥珠单抗的重链可变区稀释至1.5mg/ml,用于制备t线;50mm的ph7.4磷酸盐缓冲液将鸡igy抗体稀释至0.5mg/ml,用于制备c线;按1μl/cm划液量,通过金标hm3035喷金划膜仪将上述两种稀释后的抗体均匀的划至nc膜上制备t线和c线;将划好的nc膜放置于37℃干燥箱中干燥过夜。
59.4)组装将步骤2)结合垫叠压在步骤3)得到的硝酸纤维素膜的一端,并将吸水膜固定叠压在硝酸纤维素膜的另一端,最后将步骤2)得到的样品垫叠压在结合垫另一端,用裁膜仪按每条4mm的宽度进行裁剪,并装入层析条壳体中,即得成品。
60.5)检测将血清稀释10倍,取90μl加入加样孔,反应10min后置于荧光读数仪检测。与标准
品或参考品的数值比较,判断待检样本中抗抗体的含量。
61.本实施例之中,时间分辨荧光物质乳胶微球为含铕乳胶微球,即时间分辨荧光物质为镧系元素铕与乳胶的结合物;根据需要,时间分辨荧光物质可以调整为镧系元素、镧系元素与乳胶的结合物、镧系元素的螯合物中的一种;镧系元素可以为铕,铽,钐或镝中的一种。
62.实施例2本实施例提供了一种抗帕妥珠单抗抗体酶联免疫测定试剂盒制备方法。检测原理图参照图2所示。
63.试剂盒包括包括酶标板、生物素化帕妥珠单抗,抗帕妥珠单抗抗体校准品、抗帕妥珠单抗抗体质控品、酶结合物、清洗液、终止液。所述酶结合物为辣根过氧化物酶(hrp)标记的帕妥珠单抗互补决定区(cdrs)。该酶标板包被有链霉亲和素。
64.帕妥珠单抗的互补决定区(cdrs)包括通过连接肽连接的cdr1-vh1、cdr2
ꢀ–
vh2、cdr3
–
vh3、cdr1-vl1、cdr2
ꢀ–
vl2和cdr3
–
vl3:cdr1-vh1:dytmd;cdr2-vh2:dvnpnsggsiynqrfkg;cdr3-vh3:nlgpsfyfdy;cdr1-vl1:kasqdvsigva;cdr2-vl2:sasyryt;cdr3-vl3:qqyyiypyt。
65.连接肽选自ggggsggggsggggs。
66.制备方法如下:1)帕妥珠单抗的生物素化取1mg帕妥珠单抗置于5 ml离心管中,加入50μl 10mg/ml的活化生物素 (sulfo-nhs-lc-bintin),,室温反应1h,将反应液取出,以0.02m pbs透析过夜。将生物素化帕妥珠单抗取出,加入0.03% proclin300 防腐,4度备用。
67.2)hrp标记帕妥珠单抗互补决定区(cdrs)氨基酸合成方法合成帕妥珠单抗互补决定区(cdrs),经验证,该合成多肽包能与抗帕妥珠单抗抗体反应。
68.称取5mg hrp置于5 ml离心管中,加入1ml纯水溶解,加入1ml naio4溶液(10mg/ml,现用现配),4度避光反应30min。加入0.02ml 乙二醇,室温反应15min。将上述溶液透析后取出。将1mg帕妥珠单抗互补决定区(cdrs)加入上述活化好的溶液中,室温避光反应2小时,加0.2ml nabh4溶液(5mg/ml,现用现配),混匀,以0.05m cb透析过夜。将标记好的酶标抗体取出,加入等体积甘油,置于-20℃保存备用。
69.3)包被酶标板将cb缓冲液稀释链霉亲和素至1μg/ml,每孔100μl包被微孔板,37℃ 2h。吸去包被液,用含2%bsa的封闭缓冲液每孔200μl,37℃孵育2小时,拍去封闭液,37度烘干备用。
70.4)包被生物素化帕妥珠单抗用中性磷酸盐缓冲液稀释生物素化帕妥珠单抗至1μg/ml,每孔100μl,37℃ 2h。洗板3次,用含2%bsa的封闭缓冲液每孔200μl,37℃孵育2小时,拍去封闭液,37度烘干备用。
71.5)把待检血清样本稀释100倍,每孔100μl加入微孔板,37度孵育2小时,洗板4次。
72.6)加入hrp标记帕妥珠单抗互补决定区(cdrs),孵育1小时,洗板4次7)微孔板中加入hrp酶的底物tmb,孵育15分钟,加入终止液hcl溶液终止显色反应,用450nm波长检测od值,与标准品或参考品的od值比较,判断待检样本中抗抗体的含量。
73.实施例3本实施例提供了一种曲妥珠单抗抗体化学发光测定试剂盒及制备方法。
74.抗曲妥珠单抗抗体化学发光检测试剂盒包括:生物素化曲妥珠单抗、抗曲妥珠单抗抗体校准品、抗曲妥珠单抗抗体质控品、吖啶酯标记的曲妥珠单抗重链可变区(hv)、磁微粒试剂、激发液和清洗液。
75.曲妥珠单抗重链可变区序列见实施例1所示。
76.制备方法如下:1)曲妥珠单抗的生物素化取1mg曲妥珠单抗置于5 ml离心管中,加入50μl 10mg/ml的活化生物素 (sulfo-nhs-lc-bintin),室温反应1h,将反应液取出,以0.02m pbs透析过夜。将生物素化曲妥珠单抗抗体取出,加入0.03% proclin300 防腐,4度备用。
77.2)吖啶酯标记曲妥珠单抗重链可变区(hv)氨基酸合成方法合成曲妥珠单抗重链可变区(hv),经验证,用该合成多肽包被酶标板,能与抗曲妥珠单抗抗体反应。
78.取2mg曲妥珠单抗重链可变区(hv),按抗体:吖啶酯=1:10~50摩尔比加入已活化的吖啶酯,室温反应30min。将反应液以0.05m cb溶液透析后取出,加入等体积甘油,置于-20℃保存备用。
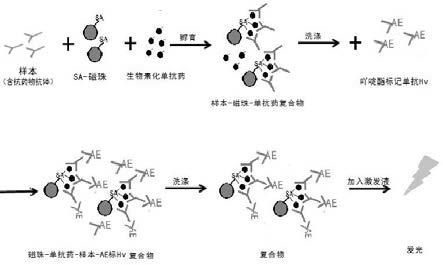
79.3)检测步骤本实施例利用吖啶酯化学发光免疫分析技术-结合生物素-亲和素磁颗粒分离技术实现抗抗体检测。其检测原理如图3: 将样本(稀释20倍)和链霉亲和素磁微粒(1)及生物素化曲妥珠单抗(2)混合,得到链霉亲和素磁珠-生物素化曲妥珠单抗-样本复合物(3),洗涤后,加入吖啶酯标记的曲妥珠单抗重链可变区(hv)进行反应后,形成链霉亲和素磁珠-生物素化曲妥珠单抗-样本-吖啶酯标记曲妥珠单抗重链可变区(hv)复合物。加入发光激发液,测定发光强度,与标准品或参考品的数值比较,判断待检样本中抗抗体的含量。
80.实验例1本实验例对实施例1试剂盒进行定量检测。
81.1.1标准曲线制作1.1.1取抗曲妥珠单抗抗体校准品一套,具体值见表1.表11.1.2 检测方法取校准品90μl,直接加入层析条中样品窗口;10分钟之后,用时间分辨荧光定量分析仪定量检测信号值。
82.每个校准品检测2次,取t/c值的平均值。具体结果见表2。
83.表21.1.3 标准曲线制备根据上述检测结果,以浓度值为x轴,以t/c值为y轴,进行线性回归,得到线性方程:y = 0.0024x + 0.042,r2 = 0.9987。曲线见图4。
84.1.2精密度测试:1.2.1 取制备好的10张层析条,配置一个浓度(50ng/ml)的抗曲妥珠单抗抗体工作校准品;1.2.2 取90μl校准品,直接加入试剂条加样孔中;1.2.3 待校准品层析10min之后,用时间分辨荧光定量分析仪进行检测,根据上述线性方程测得10个试剂条的结果,结果如表3,说明本方法的抗曲妥珠单抗抗体时间分辨荧光免疫层析测定试剂盒精密度良好。
85.表31.3 与其他的方法相比:以曲妥珠单抗标记微球,以曲妥珠单抗包被nc膜为方法2;以曲妥珠单抗fab标记微球,以曲妥珠单抗fab包被nc膜为方法3。三种方法,除标记抗体和包被抗体不同,其他条件相同,三种结果对比如表4.表4实验例2本实验例对实施例2试剂盒进行定量检测。
86.2.1检测方法2.1.1取抗帕妥珠单抗抗体校准品一套,具体值见表5表52.1.2 检测步骤1)将校准品及质控品,每孔100μl加入微孔板,37度孵育2小时,洗板4次。
87.2)加入hrp标记帕妥珠单抗互补决定区,孵育1h,洗板4次。
88.3)微孔板中加入底物tmb,孵育15min,加入终止液终止显色反应,用450nm波长检测od值,判断试剂盒性能。具体结果见表6。
89.表62.1.3 标准曲线根据上述检测结果,以od值为x轴,以浓度值为y轴,进行曲线拟合,得到曲线方程: y = 0.0053x + 0.1398,r
²ꢀ
= 0.9961,曲线见图5.2.2精密度测试:根据检测的精密度质控品的od值,以曲线方程进行计算结果值,结果如表7,说明本方法的抗帕妥珠单抗抗体酶联免疫测定试剂盒精密度良好。
90.表72.3 与其他的方法相比:以帕妥珠单抗标记hrp,以生物素化帕妥珠单抗包被微孔板为方法2;以帕妥珠单抗fab标记hrp,以帕妥珠单抗fab包被微孔板为方法3。三种方法,除标记抗体和包被抗体不同,其他条件相同,三种结果对比如表8。
91.表8
实验例3本实验例对实施例3试剂盒进行定量检测。
92.3.1检测方法3.1.1取抗曲妥珠单抗抗体校准品一套,具体值见表9表9编号c0c1c2c3c4c5c6浓度(ng/ml)0510501002005002.1.2 检测步骤1)分别取20μl校准品、20μl链霉亲和素磁微粒、50μl 生物素化曲妥珠单抗加入微孔中混合,37度孵育15min,清洗3次。
93.2)加入吖啶酯标记曲妥珠单抗重链可变区(hv),37度孵育15min,清洗3次。
94.3)加入发光激发液,测定发光强度。具体结果见表10。
95.表10编号c0c1c2c3c4c5c6均值(发光值)15331246143457956881438662538666719503.1.3 标准曲线根据上述检测结果,以浓度值为x轴,以发光值为y轴,进行进行线性回归,得到线性方程:y = 1304.4x + 13507,r
²ꢀ
= 0.9963,曲线见图6.3.2精密度测试:取20μl精密度质控品、20μl链霉亲和素磁微粒、50μl 生物素化曲妥珠单抗加入微孔中混合,37度孵育15min,清洗3次;加入吖啶酯标记曲妥珠单抗重链可变区(hv),37度孵育15min,清洗3次;加入发光激发液,测定发光强度。根据上述曲线方程,计算结果值。本方法的抗曲妥珠单抗抗体化学发光免疫测定试剂盒精密度良好。具体结果见表11。
96.表11
编号12345678910均值sdcv浓度ng/ml48.247.550.349.849.750.451.548.752.250.649.91.452.90%
3.3 与其他的方法相比:以曲妥珠单抗标记吖啶酯,以曲妥珠单抗标记生物素为方法2;以曲妥珠单抗fab标记吖啶酯,以曲妥珠单抗fab标记生物素为方法3。三种方法,除标记吖啶酯的抗体和标记生物素的抗体不同,其他条件相同,三种结果对比如表12。
97.表12 本实施例方法2方法3检出限<5ng/ml<10ng/ml<20ng/ml检测范围5-500ng/ml10-200ng/ml20-500ng/ml
线性r20.99630.97440.9801精密度2.90%15.36%14.10%非特异背景干扰低高低综上,本发明提供的检测试剂盒具有捕获效率高、准确率高、灵敏度高的优势,可以有效避免假阳性和假阴性的发生。具有良好的应用前景。
98.以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1