大焦深的紫外光声显微成像系统及成像方法
1.本发明涉及光学显微成像的技术领域,尤其涉及一种大焦深的紫外光声显微成像系统及成像方法。
背景技术:
2.众所周知,组织病理检测是生物医学诊断的一项重要手段。常规的组织病理检测过程主要是:取一块病变组织,将其包埋在石蜡块里,切成薄片,再用苏木精-伊红(hematoxylin-eosin,h-e)染色,用显微镜观察,最后作出病理诊断。但是常规的组织病理检测时间较长,通常需要3-4天,不能够及时地作出诊断等。
3.光声显微成像是一门蓬勃发展的生物医学成像技术。光声成像可以通过检测由短脉冲激光照射生物组织、组织吸收脉冲光后热弹性膨胀引起的超声波,无损地观测生物组织。由于光声成像的诸多特性,使得其有潜力应用于组织病理成像,替代以往的用显微镜观察苏木精-伊红染色的组织切片。
4.基于生物组织丰富的成像对比机制,光声显微成像在揭示生物组织的病理过程方面具有重大的意义。光声成像相比组织病理切片具有诸多优势,首先在生物组织内,声学散射比光学散射低1000倍以上,从而使其突破光学散射的局限。同时,光声显微镜能够从不同维度成像高对比度的生物结构。并且,不同分子吸收不同的波长,能够揭示丰富的光学对比信息。
5.xueding wang等人通过光声显微镜,清晰地测量出小鼠大脑血管的分布情况,探测小鼠颅内小脑、海马体、侧室等构造,从而获得了小鼠大脑实质病损的图像信息。yating wang等人通过构建光声超声双模态显微镜,成像肿瘤相关的血管网络和测量黑色素瘤厚度,从而对黑色素瘤的活体检测进行诊断和评估。但是上述常规光声病理显微成像技术,焦深均较短,不适用于厚样本的组织病理检测,对于临床的医学检测提出了诸多挑战。
6.华中科技大学团队引入电控变焦透镜和成像光纤束等新型光学成像器件,通过建立分辨率连续可调的多尺度光声显微成像系统,实现了血液微循环网络的多尺度成像。利用贝塞尔光束的无衍射传输特性和自重建性质,研制了一套反射式大景深光学分辨光声显微成像系统。但是,这种大焦深的光声成像技术,无法工作于紫外光波段,所以该方法不能应用于组织病理检测。
7.为了提高光学聚焦长度,采用锥棱镜或者尼波尔-泽尔尼克光场调控技术等,可以将高斯型光束扩展成贝塞尔或者类贝塞尔光束,从而提高光学焦深,改善三维成像质量。虽然这一技术方法中采用数字微镜器件(digital micromirror devices,dmd)或者空间光调制器(spatial light modulator,slm)进行相位调制,也可以扩大光学焦深。但是,这些器件往往难以用于调制紫外波段的光声激发光束。
8.光学分辨率光声显微镜(optical-resolution photoacoustic microscopy,or-pam)能够测量生物组织内具有微米尺度横向分辨率的光学吸收特性。尽管光声显微镜技术已经取得了长足的发展,但是这一技术仍存在着诸多缺陷。传统的光声显微镜都采用的是
高斯型光束,成像焦深有限——只有几十微米,难以满足厚组织样本观测的需求。对于光声病理成像而言,在or-pam中通常使用的高斯光束由于焦深(depth of focus,dof)短,仅能在有限的深度范围内保持微米级横向分辨率,而在离焦区域,光声成像分辨率急剧恶化,导致图像质量严重降低,无法准确获得厚组织样本的三维微观形态结构特征,从而影响组织病理诊断的可靠性。因此,现有的光声显微成像技术在对样品进行成像时存在成像分辨率较低的问题。
技术实现要素:
9.本发明实施例提供了一种大焦深的紫外光声显微成像系统及成像方法,旨在解决现有的光声显微成像技术在对组织病理样品进行成像时所存在的成像分辨率较低的问题。
10.第一方面,本发明实施例提供了一种大焦深的紫外光声显微成像系统,所述系统包括信号采集装置及成像处理终端,所述信号采集装置包括:紫外脉冲激光器、偏振片、调光玻片、滤光片、光声透镜、移动平台、凹槽、介质、超声换能器、放大器及数据采集卡;所述偏振片设置于所述紫外脉冲激光器的下游,所述调光玻片设置于所述偏振片的下游,所述滤光片设置于所述调光玻片的下游,所述光声透镜设置于所述滤光片的下游;所述凹槽设置于所述移动平台上,以通过所述移动平台驱动所述凹槽进行二维平移;样品置于所述凹槽内,所述介质覆盖所述样品;所述光声透镜输出的光束聚焦并照射所述样品,以使所述样品因吸收光束而引发的体积膨胀激发光声波并经所述介质进行传导;所述光声透镜输出的光束为类贝塞尔光束;所述超声换能器与所述介质相接触,以通过所述超声换能器获取所述介质传导的光声波;所述超声换能器通过所述放大器与所述数据采集卡进行电连接,所述数据采集卡与所述成像处理终端进行电连接,以输出数字化光声信号至所述成像处理终端,所述成像处理终端对所述数据采集卡采集到的数字化光声进行处理得到所述样品的成像图像。
11.所述的大焦深的紫外光声显微成像系统,其中,所述调光玻片为带相位片的调光玻片。
12.所述的大焦深的紫外光声显微成像系统,其中,所述调光玻片与所述滤光片之间设置有共焦透镜,所述共焦透镜由共焦的第一透镜及第二透镜组成。
13.所述的大焦深的紫外光声显微成像系统,其中,所述介质为生理盐水、蒸馏水或去离子水。
14.所述的大焦深的紫外光声显微成像系统,其中,所述凹槽为透明凹槽。
15.所述的大焦深的紫外光声显微成像系统,其中,所述凹槽的深度为0.2-10cm。
16.所述的大焦深的紫外光声显微成像系统,其中,所述凹槽为树脂凹槽、玻璃凹槽或石英凹槽。
17.另一方面,本发明实施例还提供了一种大焦深的紫外光声显微成像方法,其中,所述大焦深的紫外光声显微成像方法应用于上述的大焦深的紫外光声显微成像系统,所述方法包括:
18.通过成像处理终端控制紫外脉冲激光器输出光声激发光;
19.所述光声激发光经偏振片调制为线偏振光,并经过调光玻片调制为圆偏振光;所述圆偏振光为左旋圆偏振光或右旋圆偏振光;
20.所述圆偏振光经过滤光片滤除紫外波段以外的光并调制光能量得到高斯光束;
21.所述高斯光束经过光声透镜进行扩展为类贝塞尔光束并聚焦照射与凹槽中放置的样品上;所述样品因吸收光束而引发的体积膨胀激发光声波并经介质进行传导;
22.通过超声换能器接收所述介质传导的光声波并输出至所述放大器进行放大得到放大信号;
23.所述放大信号经数据采集卡进行数字化得到数字化光声信号;
24.所述成像处理终端获取所述数字化光声信号并进行处理得到所述样品的成像图像。
25.所述的大焦深的紫外光声显微成像方法,其中,所述紫外脉冲激光器输出的光声激发光的脉宽为10纳秒~800纳秒。
26.所述的大焦深的紫外光声显微成像方法,其中,所述紫外脉冲激光器输出的光声激发光的波长为180纳米~350纳米。
27.本发明实施例提供了一种大焦深的紫外光声显微成像系统及成像方法,系统包括信号采集装置及成像处理终端,信号采集装置包括:紫外脉冲激光器、偏振片、调光玻片、滤光片、光声透镜、移动平台、凹槽、介质、超声换能器、放大器及数据采集卡。上述的大焦深的紫外光声显微成像系统,通过偏振片及调光玻片对光声激发光进行调制得到圆偏振光,通过光声透镜将高斯光束转换为类贝塞尔光束并聚焦照射样品,样品因吸收光束而引发的体积膨胀激发光声波并经介质进行传导,探测经介质传导的光声波并进行成像,从而大幅扩展了光学聚焦长度,使得光声激发光在更大的焦深范围内具有亚细胞级横向分辨率,大幅提高了对样品进行成像的分辨率,以此提高了成像质量。
附图说明
28.为了更清楚地说明本发明实施例技术方案,下面将对实施例描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
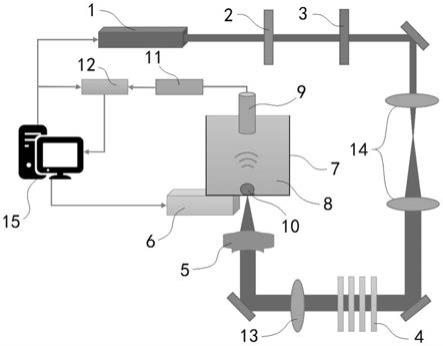
29.图1为本发明实施例提供的大焦深的紫外光声显微成像系统的结构示意图;
30.图2为本发明实施例提供的大焦深的紫外光声显微成像方法的流程示意图;
31.图3为本发明实施例提供的大焦深的紫外光声显微成像系统的效果示意图;
32.图4为本发明实施例提供的大焦深的紫外光声显微成像系统的效果示意图;
33.图5为本发明实施例提供的大焦深的紫外光声显微成像系统的效果示意图;
34.图6为本发明实施例提供的大焦深的紫外光声显微成像系统的效果示意图。
具体实施方式
35.下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
36.应当理解,当在本说明书和所附权利要求书中使用时,术语“包括”和“包含”指示所描述特征、整体、步骤、操作、元素和/或组件的存在,但并不排除一个或多个其它特征、整
体、步骤、操作、元素、组件和/或其集合的存在或添加。
37.还应当理解,在本发明说明书中所使用的术语仅仅是出于描述特定实施例的目的而并不意在限制本发明。如在本发明说明书和所附权利要求书中所使用的那样,除非上下文清楚地指明其它情况,否则单数形式的“一”、“一个”及“该”意在包括复数形式。
38.还应当进一步理解,在本发明说明书和所附权利要求书中使用的术语“和/或”是指相关联列出的项中的一个或多个的任何组合以及所有可能组合,并且包括这些组合。
39.在本实施例中,请参阅图1,图1为本发明实施例提供的大焦深的紫外光声显微成像系统的结构示意图。如图所示,本发明实施例提供了一种大焦深的紫外光声显微成像系统,所述系统包括信号采集装置及成像处理终端15,所述信号采集装置包括:紫外脉冲激光器1、偏振片2、调光玻片3、滤光片4、光声透镜5、移动平台6、凹槽7、介质8、超声换能器9、放大器11及数据采集卡12;所述偏振片2设置于所述紫外脉冲激光器1的下游,所述调光玻片3设置于所述偏振片2的下游,所述滤光片4设置于所述调光玻片3的下游,所述光声透镜5设置于所述滤光片4的下游;所述凹槽7设置于所述移动平台6上,以通过所述移动平台6驱动所述凹槽7进行二维平移;样品10置于所述凹槽7内,所述介质8覆盖所述样品10;所述光声透镜5输出的光束聚焦并照射所述样品10,以使所述样品10因吸收光束而引发的体积膨胀激发光声波并经所述介质8进行传导;所述光声透镜5输出的光束为类贝塞尔光束;所述超声换能器9与所述介质8相接触,以通过所述超声换能器9获取所述介质8传导的光声波;所述超声换能器9通过所述放大器11与所述数据采集卡12进行电连接,所述数据采集卡12与所述成像处理终端15进行电连接,以输出数字化光声信号至所述成像处理终端15,所述成像处理终端15对所述数字化光声信号进行处理得到所述样品的成像图像。
40.上述大焦深的紫外光声显微成像系统以紫外脉冲激光器1作为光源,输出紫外波段的光声激发光,之后光声激发光经过偏振片2调制为线偏振光,再经过调光玻片3调制为圆偏振光。其中调光玻片3为带相位片的调光玻片,可以是1/4玻片,经调光玻片3进行调制后可得到液晶工作所需的左旋圆偏振光或右旋圆偏振光。圆偏振光被反射镜反射后,通过滤光片4过滤掉紫外波段以外的光,并调制光的能量得到高斯光束。接着,通过透镜13进行准直后被反射镜反射并射入光声透镜5。光声透镜5为液晶相位板,则液晶相位板上设置有相应调制图案,可基于扩展的泽尔尼克算法设计液晶相位板上调制图案的光学相位分布。此外,相位片的材质不局限于液晶,也可使用其它能够进行相位调制的材料制作得到。光声透镜5可将入射的高斯光束扩展为类贝塞尔光束,并且光声透镜5可替代物镜将光束聚焦并照射到样品10上,样品被置于凹槽7内,凹槽7与移动平台6进行连接,可通过移动平台6驱动凹槽7进行二维平移,从而使聚焦后的类贝塞尔光束对样品10在x轴及y轴两个方向进行扫描。为实现对样品10进行二维扫描,还可使用振镜代替移动平台6,通过振镜可大幅提高对样品10进行扫描的速度。样品10吸收类贝塞尔光束的能量,引起热体积膨胀并发射出光声波。由样品10产生的光声波经介质8进行传导并被超声换能器9接收到,超声换能器9将接收到的光声波传输至放大器11进行放大得到放大信号,放大信号传输至数据采集卡12进行数字化并存储,数据采集卡12每次向成像处理终端15发出一个时钟信号,就采集一次超声数据。成像处理终端15接收到数字化的光声信号并进行处理,从而得到样品10的成像图像,从而准确获取样品组织的生理/病理信息。成像图像可以是基于数字化的光声信号重建的二维图像或三维图像。
41.本实施例中的技术方法,针对组织病理诊断面临的一系列挑战,提供了一种基于紫外光的显微成像系统,通过光声透镜实现大光学焦深的光声激发,进而构建新型紫外光声显微镜,实现厚组织样本三维微观形态结构的无标记快速病理观测。这一新技术具备大光学焦深、亚细胞横向分辨率、无标记观测等众多能力,可实现组织病理样本的“微尺度、免切片、无标记”观测,为临床医学检测提供了新型的技术支持。
42.与此同时,可将成像处理终端15与移动平台6及紫外脉冲激光器1进行电连接;从而通过成像处理终端15输入相应控制参数至紫外脉冲激光器1,以控制紫外脉冲激光器1产生特定波长及特定脉宽的光声激发光;同时,可通过成像处理终端输入相应移动参数至移动平台6,以通过移动平台6驱动凹槽7进行水平移动。所述成像处理终端15可以是台式电脑、笔记本电脑、平板电脑等可用于数据、图像处理的终端设备。
43.在更具体的实施例中,所述调光玻片3与所述滤光片4之间设置有共焦透镜14,所述共焦透镜14由共焦的第一透镜及第二透镜组成。为提高成像效果,还可在调光玻片3与所述滤光片4之间设置共焦透镜14,通过共焦透镜14构成的4f光学系统对调光玻片3射出的圆偏振光(左旋圆偏振光或右旋圆偏振光)进行扩束,扩束后的光束再传输至滤光片4进行滤光,扩束可使圆偏振光的光斑直径更大,从而提高滤光片4进行滤光处理的效果。具体的,调光玻片3输出的探测光束并不局限于左旋偏振光,在实际应用过程中,还可采用右旋圆偏振光,具体旋转方向可以以液晶的相应特性为准。
44.在更具体的实施例中,所述介质8为生理盐水、蒸馏水或去离子水,在实际使用过程中优选蒸馏水作为介质8进行使用,在最优实施例中选择去离子水作为介质8进行使用。
45.在更具体的实施例中,所述凹槽7为透明凹槽。具体的,所述凹槽7的深度为0.2-10cm。其中,所述凹槽7为树脂凹槽、玻璃凹槽或石英凹槽。具体的,可设置凹槽7为透明凹槽,从而增加凹槽7的透光率。还可根据实际使用情况合理设置凹槽7的深度,介质8的厚度应小于凹槽7的深度,根据实际情况进行调整。通过合理设置介质8的厚度,可提高超声换能器9接收光声波的效率。
46.和传统光声显微成像技术相比,上述大焦深的紫外光声显微成像系统中的信号采集装置具有以下特点:1、常规光声病理显微成像技术焦深短,而基于光声透镜的液晶相位调制可实现了大光学焦深的光声激发。2、其中的光声透镜在大深度范围内具有良好的横向分辨率(约为0.8微米),可以清晰观测细胞核等亚细胞结构。3、大焦深紫外光声显微成像技术,可以对厚样品进行组织病理检测,并具有集成化、小型化的优点,有利于其在临床医学诊断中的应用。
47.本发明实施例中对光声透镜中的类贝塞尔光束进行分析,图3、图4、图5及图6均为本发明实施例提供的大焦深的紫外光声显微成像系统的效果示意图,经分析后得到光声透镜中类贝塞尔光束的振幅、相位、强度分布情况如图3所示,图3中的(a)图为振幅分布情况,图3中的(b)图为相位分布情况,图3中的(c)图为强度分布情况;经分析后得到光声透镜中光场的分布情况如图4所示,经分析后得到光声透镜聚焦光场的横向分布(x轴方向)曲线如图5,经分析后得到光声透镜聚焦光场的轴向分布(z轴方向)曲线如图6。通过光声透镜的相位分布,我们可以计算出光束的光场分布,如图4所示。再对光场分布分别取横向、轴向截面,如图5及图6所示,通过图5及图6可以得知,光声透镜将光束拉伸成了一个类贝塞尔光束,横向分辨率为0.85μm,突破了衍射极限,轴向长度为300μm左右,是高斯型光束的5-6倍,
大大改善了光束的质量,从而可大幅提高成像分辨率。
48.请参阅图2,图2为本发明实施例提供的大焦深的紫外光声显微成像方法的方法流程示意图。本发明实施例还提供了一种大焦深的紫外光声显微成像方法,其中,所述大焦深的紫外光声显微成像方法应用于上述的大焦深的紫外光声显微成像系统,如图2所示,所述方法包括步骤s110-s170。
49.s110、通过成像处理终端控制紫外脉冲激光器输出光声激发光;
50.具体的,本实施例中可通过成像处理终端控制紫外脉冲激光器输出波长位于紫外光波段的光声激发光,其中光声激发光的波长为180纳米~350纳米。还可通过成像处理终端控制紫外脉冲激光器的脉冲宽度,如控制紫外脉冲激光器产生脉宽为纳秒级的光声激发光,如光声激发光的脉宽为10纳秒~800纳秒。对于不同组织样品可采用不同波长及不同脉宽的光声激发光进行成像,如对于某一特定组织样品可采用波长为266nm、脉冲宽度为200ns(纳秒)的光声激发光。对于不同的样品,波长可以改变,以样品的吸收系数最大、产生的光声信号最强为准。
51.s120、所述光声激发光经偏振片调制为线偏振光,并经过调光玻片调制为圆偏振光;所述圆偏振光为左旋圆偏振光或右旋圆偏振光。
52.经调光玻片调制输出的光束可以是左旋圆偏振光或右旋圆偏振光,具体应用过程中以调光玻片上配置的液晶相位板的液晶特性为准。
53.s130、所述圆偏振光经过滤光片滤除紫外波段以外的光并调制光能量得到高斯光束。
54.s140、所述高斯光束经过光声透镜进行扩展为类贝塞尔光束并聚焦照射与凹槽中放置的样品上;所述样品因吸收光束而引发的体积膨胀激发光声波并经介质进行传导。
55.具体的可选择介质为生理盐水、蒸馏水或去离子水中的任意一种。
56.s150、通过超声换能器接收所述介质传导的光声波并输出至所述放大器进行放大得到放大信号。
57.s160、所述放大信号经数据采集卡进行数字化得到数字化光声信号。
58.s170、所述成像处理终端获取所述数字化光声信号并进行处理得到所述样品的成像图像。
59.本实施例中的大焦深的紫外光声显微成像方法适用于紫外波段调制的光声透镜构建得到紫外光声显微成像系统,通过这一技术方法,克服了数字微镜器件(digital micromirror devices,dmd)或者空间光调制器(spatial light modulator,slm)无法在此波段工作的技术瓶颈。上述成像系统中的光声透镜将高斯型光束调制为类贝塞尔光束,实现了大光学焦深的聚焦,在更大的深度范围内具有亚细胞级横向分辨率,面向组织病理光声成像这一临床医学的重大需求,构建大焦深紫外光声显微镜,使得成像设备小型化、简约化,从而提供了一种适合厚组织样本“无标记、免切片”病理观测的新型技术手段。基于上述技术方法构建的大焦深紫外光声显微成像系统,适应于观测厚组织样本,可以在较大深度上激发组织的光声信号,同时保证亚细胞级别的横向分辨率,实现组织样本三维微观结构的“无标记、免切片”成像。
60.在本发明实施例所提供了一种大焦深的紫外光声显微成像系统及成像方法,系统包括信号采集装置及成像处理终端,信号采集装置包括:紫外脉冲激光器、偏振片、调光玻
片、滤光片、光声透镜、移动平台、凹槽、介质、超声换能器、放大器及数据采集卡。上述的大焦深的紫外光声显微成像系统,通过偏振片及调光玻片对光声激发光进行调制得到圆偏振光,通过光声透镜将高斯光束转换为类贝塞尔光束并聚焦照射样品,样品因吸收光束而引发的体积膨胀激发光声波并经介质进行传导,探测经介质传导的光声波并进行成像,从而大幅扩展了光学聚焦长度,使得光声激发光在更大的焦深范围内具有亚细胞级横向分辨率,大幅提高了对样品进行成像的分辨率,以此提高了成像质量。
61.以上所述,仅为本发明的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,可轻易想到各种等效的修改或替换,这些修改或替换都应涵盖在本发明的保护范围之内。因此,本发明的保护范围应以权利要求的保护范围为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1