检测免疫比浊试剂加液量是否异常的方法与流程
1.本发明涉及生化检测技术领域,尤其涉及检测免疫比浊试剂加液量是否异常的方法。
背景技术:
2.在体外诊断涉及血液的检测通常采用胶乳免疫比浊法进行。通常,检测试剂通常包括r1试剂和r2试剂。其中,所述r1试剂(也被记做reagent 1)中含有实现待测靶标检测试剂反应所需的缓冲液。所述r2试剂(也被记做reagent 2)中含有待测靶标浓度判定试剂主要组分以及待测靶标检测试剂的必需反应组分。所述待测靶标浓度判定试剂主要组分为包被有待测靶标抗体或抗原的胶乳颗粒。
3.根据实际检测需要,除r1试剂和r2试剂外,用于血液诊断的试剂还可以包括多种试剂。例如,除r1、r2试剂外,还包括1种、2种、3种、4种、5种、6种、7种、8种、9种或10种试剂。所述试剂为反应所需的缓冲液、金属离子溶液、盐离子溶液、包被抗原或抗体微球的悬液、保护剂溶液、酶溶液、表面活性剂溶液等。
4.全自动、半自动及手动测试过程中由于自动化仪器的加样模块偶发故障、人为操作失误或试剂存在气泡/粘稠度高等原因会出现加入试剂量异常(低于或高于目标量),会导致报告错误的测试结果,造成临床上的误诊,最终对病患可能造成严重的后果。
5.但目前,对于胶乳免疫比浊检测方法学,加入试剂量异常判断方法目前尚未见系统性解决方案。
技术实现要素:
6.有鉴于此,本发明要解决的技术问题在于提供检测免疫比浊试剂加液量是否异常的方法。
7.在所有的试剂混合前,致敏胶乳颗粒与待检测样本中的抗原/抗体不会接触,反应液呈均匀胶体状态,在选定入射光波长及选定胶乳颗粒粒径组合下,所能检测到的吸光度与反应液中胶乳颗粒的浓度呈正比。在单次测定中如果由于试剂量移取误差过大导致所加入胶乳颗粒浓度低于标准浓度(对应胶乳试剂加入量不足),则吸光度低于预设值范围;如果高于标准浓度(对应胶乳试剂加入量过多),则吸光度高于预设值范围。
8.因此,本发明提供了检测免疫比浊试剂加液量是否异常的方法,其包括:
9.将试剂混合后检测吸光度a0,a0值在预设值范围内则判断为加液量正常,a0值不在预设值范围内则判断为加液量异常。
10.本发明中,所述预设值范围为(a
标准
×
下浮指数)~(a
标准
×
上浮指数);
11.本发明中,所述a
标准
为标准加样条件下测得的吸光度。所述标准加样条件是指确定加样量无误的条件。a
标准
为多次标准加样后测得的平均值。
12.本发明中,所述下浮指数为80%~99%,所述上浮指数为101%~120%。实施例中,所述下浮指数为85%~97%,所述上浮指数为103%~115%。一些实施例中,所述下浮
指数为90%~95%,所述上浮指数为105%~110%。一些具体实施例中,所述下浮指数为90%、91%、92%、93%、94%或95%。一些具体实施例中,所述上浮指数为105%、106%、107%、108%、109%、110%。,本发明中,所述上浮指数和下浮指数可以根据不同检测的需要进行调整。本发明对此不做限定,在本发明实施例中,以a
标准
值
±
5%为可接受误差范围进行方法学验证,即上浮指数为105%,下浮指数为95%。
13.本发明中,所述试剂为免疫比浊法检测所需试剂,所述加液量异常为后添加的试剂加液量不足或过量。
14.以试剂数量为2为例,两试剂记为r1试剂和r2试剂,将r1试剂和r2试剂混合后,检测吸光度a0;a0值在预设值范围内则判断为加液量正常,a0值不在预设值范围内则判断为加液量异常。
15.以试剂数量为3为例,三个试剂分别被即为r1、r2和r3。将r1试剂和r2试剂混合后,检测吸光度a
0-1
,a
0-1
值不在预设值范围内则判断为加液量异常,需补加试剂,a
0-1
值在预设值范围内则判断为加液量正常,继续加入试剂r3,检测吸光度a
0-2,a0-2
值不在预设值范围内则判断为加液量异常,需补加试剂,a
0-2
值在预设值范围内则判断为加液量正常。
16.以试剂数量为4为例,四个试剂分别被即为r1、r2、r3和r4。将r1试剂和r2试剂混合后,检测吸光度a
0-1
,a
0-1
值不在预设值范围内则判断为加液量异常,需补加试剂,a
0-1
值在预设值范围内则判断为加液量正常,继续加入试剂r3,检测吸光度a
0-2,a0-2
值不在预设值范围内则判断为加液量异常,需补加试剂,a
0-2
值在预设值范围内则判断为加液量正常,继续加入试剂r4,检测吸光度a
0-3,a0-3
值不在预设值范围内则判断为加液量异常,需补加试剂,a
0-3
值在预设值范围内则判断为加液量正常。
17.依次类推,在添加多个试剂的情况下,每次添加完试剂都对吸光度进行检测,并与预设值范围进行比较,判断加液量是否异常,如异常则补加试剂,如正常则进行下一个检测步骤。
18.本发明还提供了一种样品的检测方法,其包括:将试剂混合后检测吸光度a0,
19.a0值在预设值范围内则判断为加液量正常,加入待测样本,检测吸光度a1,继续孵育后读取吸光度a2,采用标准曲线法根据吸光度变化计算样本中待测靶标的浓度;
20.a0值不在预设值范围内则判断为加液量异常,则检测停止。
21.本发明所述样品的检测方法中,加液量是否异常的判断方法与本发明所述的检测免疫比浊试剂加液量是否异常的方法一致。
22.以检测试剂数量为2为例,两试剂分别记做r1和r2。
23.所述r1试剂包括缓冲液a;所述r2试剂中包括包被有待测靶标抗体或抗原的胶乳颗粒和缓冲液b。
24.所述缓冲液a和缓冲液b独立的选自4-羟乙基哌嗪乙磺酸缓冲液、吗啉乙磺酸缓冲液、磷酸盐缓冲液、焦磷酸缓冲液、3-(n-吗啉代)丙磺酸缓冲液、1,4-哌嗪二乙磺酸缓冲液。
25.所述r1试剂中还包括钾盐、钠盐、氰基化合物或表面活性剂中至少一种或两者以上的组合;
26.所述r2试剂中还包括稳定剂,所述稳定剂选自海藻糖或蔗糖中至少一种或两者以上的组合。
27.在检测中,试剂的添加顺序包括:
28.i)、将r1预先添加在检测容器中,由设备将r2试剂加入r1试剂中。则r2加入r1后,检测a0,判断加样量是否正常。
29.ii)、将r1和r2分别向样本中添加,再进行混合,则混合后检测a0,判断是否异常。
30.iii)、将r2预先添加在检测容器中,由设备将r1试剂加入r2试剂中。则r1加入r2后,检测a0,判断加样量是否正常。
31.根据本领域试剂容错性的要求,通常判断加液量异常后,建议检测终止,但对于容错性较高的试剂,本发明所述判断为加液量异常后,可以通过补加试剂的方式继续检测。
32.在具体实施例中,所述a0值不在预设值范围内包括:
33.a0值≥a
标准
×
上浮指数,则检测终止,或者补充先加入的试剂;
34.a0值≤a
标准
×
下浮指数,则检测终止,或者补充后加入的试剂。
35.补充试剂后,再次检测吸光度a0’,
36.a0’值在所述预设值范围内,判断为加液量正常,校准试剂体积后继续检测;
37.a0’值不在预设值范围内则判断为加液量异常,检测终止。
38.因补充试剂后,r1试剂和r2试剂混合的体积与标准加样条件下的体积可能产生浮动(特别是r2加入量过高时),干扰加入样品后反应体系的体积,因此,在继续检测前,需校准试剂体积。
39.本发明中,所述采用标准曲线法根据吸光度变化计算样本中待测靶标的浓度包括在检测前建立吸光度变化值-靶标浓度的标准曲线。检测完成后,根据公式δa=a2-a1计算待测样本吸光度变化值,将δa代入待测靶标项目内置的校准曲线,即可获得该样本待测靶标浓度。
40.本发明中,所述样本包括全血、血浆、血清或尿液。
41.本发明中,所述待测靶标包括总胆红素、c反应蛋白、胆碱酯酶、β2-微球蛋白、胱抑素c或血清淀粉样蛋白a。
42.本发明中以含有抗体包被胶乳的r2试剂为例,验证本发明所述方法的可行性。所述r2试剂中,胶乳颗粒的质量分数为0.1%~0.5%。
43.以β2微球蛋白的检测为例,r1试剂与r2试剂的体积比为240:60,其中r2试剂的添加量为60μl,测得a0值为0.558~0.682判断为加液正常,测得a0值为<0.559或测得a0值>0.682判断为样本加样异常。
44.以c反应蛋白的检测为例,r1试剂与r2试剂的体积比为150:150,其中r2试剂的添加量为150μl,测得a0值为0.836~0.924判断为加液正常,测得a0值为<0.836或测得a0值>0.924判断为样本加样异常。
45.以肌红蛋白的检测为例,r1试剂与r2试剂的体积比为180:60,其中r2试剂的添加量为60μl,测得a0值为0.931~1.029判断为加液正常,测得a0值为<0.931或测得a0值>1.029判断为样本加样异常。
46.本发明提供的检测免疫比浊试剂加液量是否异常的方法中,在加入样本之前检测吸光度a0,将其与标准加样量下测得的标准值进行比较,判断样本加样量是否正常。实验表明,本发明提供的方法准确可靠,能够有效降低检测时误报结果的风险。
具体实施方式
47.本发明提供了检测免疫比浊试剂加液量是否异常的方法,本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明。本发明的方法及应用已经通过较佳实施例进行了描述,相关人员明显能在不脱离本发明内容、精神和范围内对本文的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。
48.本发明采用的试材皆为普通市售品,皆可于市场购得。下面结合实施例,进一步阐述本发明:
49.实施例1测量结果:
50.①
待测靶标项目:β2微球蛋白;
51.②
实验材料:待测样本为新鲜人尿液样本;
52.③
reagent1:4-羟乙基哌嗪乙磺酸缓冲液50mm~500mm,reagent 1预灌装于比色腔内;
53.④
reagent2:4-羟乙基哌嗪乙磺酸缓冲液50mm~500mm;β2微球蛋白抗体包被胶乳0.1%~0.5%;海藻糖1%~10%;
54.⑤
吸光度判定阈值:0.558~0.682;
55.⑥
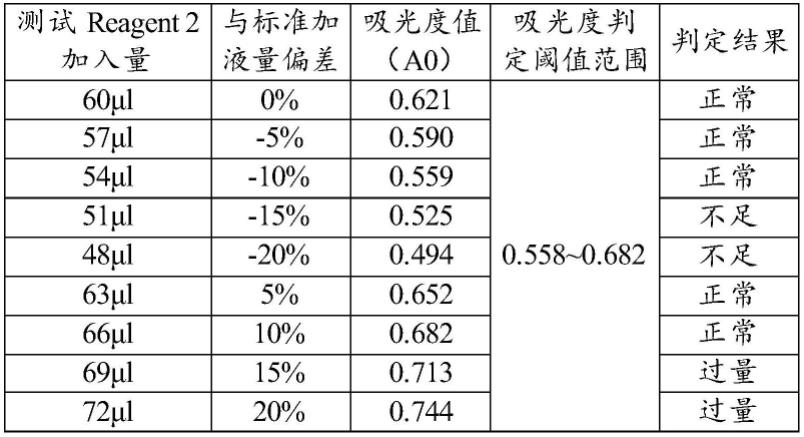
检测过程:将240μlreagent 1预灌装于反应腔中,测试时试剂/样本针将60μlreagent 2转移至前述反应腔中,充分混合均匀并读取吸光度a0。将a0与该项目设定阈值范围进行比较,高于0.682提示reagent2加入过量,低于0.558提示reagent 2加入量不足。试剂/样本针将10μl待测尿液样本转移至前述反应杯/腔中并混合均匀,读取吸光度a1,继续孵育3~5分钟,读取吸光度a2。根据公式δa=a2-a1计算待测样本吸光度变化值,将δa代入待测靶标项目内置的校准曲线,即可获得该样本待测靶标浓度。
56.表1实施例1测量结果:
[0057][0058]
实施例2
[0059]
①
待测靶标项目:c反应蛋白;
[0060]
②
实验材料:待测样本为新鲜人血清样本;
[0061]
③
reagent1:4-羟乙基哌嗪乙磺酸缓冲液50mm~500mm,nacl150mm~500mm;
reagent 1预灌装于比色腔内;
[0062]
④
reagent2:4-羟乙基哌嗪乙磺酸缓冲液50mm~500mm;c反应蛋白抗体包被胶乳0.1%~0.5%;蔗糖1%~10%;
[0063]
⑤
吸光度判定阈值:0.836~0.924;
[0064]
⑥
检测过程:将150μlreagent 1预灌装于反应腔中,测试时试剂/样本针将150μlreagent 2转移至前述反应腔中,充分混合均匀并读取吸光度a0。将a0与该项目设定阈值范围进行比较,高于0.924提示reagent 2加入过量,低于0.836提示reagent 2加入量不足。试剂/样本针将3μl待测血清样本转移至前述反应杯/腔中并混合均匀,读取吸光度a1,继续孵育3~5分钟,读取吸光度a2。根据公式δa=a2-a1计算待测样本吸光度变化值,将δa代入待测靶标项目内置的校准曲线,即可获得该样本待测靶标浓度。
[0065]
表2实施例2测量结果:
[0066][0067]
实施例3
[0068]
①
待测靶标项目:肌红蛋白;
[0069]
②
实验材料:待测样本为新鲜人血清样本;
[0070]
③
reagent1:4-羟乙基哌嗪乙磺酸缓冲液50mm~500mm,nacl150mm~500mm,聚乙二醇6000 1.0%~5.0%;reagent 1预灌装于比色腔内;
[0071]
④
reagent2:4-羟乙基哌嗪乙磺酸缓冲液50mm~500mm;肌红蛋白抗体包被胶乳0.1%~0.5%;蔗糖1%~10%;
[0072]
⑤
吸光度判定阈值:0.931~1.029;
[0073]
⑥
检测过程:将180μlreagent 1预灌装于反应腔中,测试时试剂/样本针将60μlreagent 2转移至前述反应腔中,充分混合均匀并读取吸光度a0。将a0与该项目设定阈值范围进行比较,高于1.029提示reagent 2加入过量,低于0.931提示reagent 2加入量不足。试剂/样本针将6μl待测血清样本转移至前述反应杯/腔中并混合均匀,读取吸光度a1,继续孵育3~5分钟,读取吸光度a2。根据公式δa=a2-a1计算待测样本吸光度变化值,将δa代入待测靶标项目内置的校准曲线,即可获得该样本待测靶标浓度。
[0074]
表3实施例3测量结果:
[0075][0076]
由上述结果可见,本发明所述方法在多种不同胶乳免疫比浊项目中均表现出预期效果,在加入reagent 2液量明显异常偏高或偏低时能准确识别,有效降低检测时误报结果的风险,且该检测不额外添加任何试剂,不会对检测结果产生影响。
[0077]
以上仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1