一种液质联用测定血浆中阿瑞匹坦浓度的方法与流程
1.本发明属于医药技术领域,具体涉及一种药物的测定方法,特别涉及一种液质联用测定血浆中阿瑞匹坦浓度的方法。
背景技术:
2.阿瑞匹坦别名醋胺硝唑,是一种灰白色至淡黄色水晶般的固体化学品,阿瑞匹坦是cyp3a4的底物、较轻至中度(剂量依赖性)抑制剂和诱导剂,也是cyp2c9诱导剂。联合使用阿瑞匹坦与可抑制cyp3a4活性的药物可导致阿瑞匹坦的血药浓度升高。临床上阿瑞匹坦主要用于预防高度致吐性抗肿瘤化疗的初次和重复治疗过程中出现的急性和迟发性恶心和呕吐。分子式:c
23h21
f7n4o3,分子量:534.43,其化学结构式为:
[0003][0004]
化疗引起的恶心和呕吐(cinv)是与抗癌治疗相关的一种常见不良事件,可显著影响患者的健康相关生活质量,并可能损害化疗的有效性。预防cinv的传统方案通常包括皮质类固醇和5-羟色胺(5ht3)受体拮抗剂的组合。近年来,随着p物质神经激肽1(nk1)受体拮抗剂(nk1类)阿瑞匹坦的使用,止吐治疗取得了很大进展。阿瑞匹坦具有独特的作用方式;它是人类p物质神经激肽1(nk1)受体的选择性高亲合力拮抗剂。关于阿瑞匹坦的临床前和人体正电子发射体层摄像术(pet)研究证明,它可以渗透至脑内,并占领脑nk1受体。临床前研究表明,阿瑞匹坦具有较长的中枢活性持续时间,可抑制顺铂诱导的急性期和延迟期呕吐,并增强5-ht3受体拮抗剂昂丹司琼和糖皮质激素地塞米松对顺铂诱导的呕吐的止吐活性。
[0005]
当与皮质类固醇(地塞米松)和血清素5-ht3受体拮抗剂(昂丹司琼)的标准方案联合使用时,口服阿瑞匹坦(第1天125mg,第2天和第3天80mg,每天一次)可有效预防与单周期或多周期高致吐化疗(hec)相关的急性和延迟化疗引起的恶心和呕吐(cinv)。这种阿瑞匹坦方案还可以有效预防接受单周期或多周期中度致吐化疗(mec)治疗的患者的cinv。在进行腹部手术的患者之前口服单剂量的阿瑞匹坦40mg也可有效预防术后恶心和呕吐(ponv)。阿瑞匹坦通常耐受性良好。阿瑞匹坦是治疗ponv的推荐方案,当与皮质类固醇和5-ht3受体拮抗剂联合使用时,是治疗cinv的推荐方案。
[0006]
阿瑞匹坦受体拮抗剂较5-ht3受体拮抗剂而言,普遍存在较好的耐受性,一般在前
期的临床应用中未见明显的毒副作用。目前临床中常用的nk-1受体拮抗剂阿瑞匹坦,据相关文献资料报道,其主要的临床不良反应的严重程度介于轻度和中度之间,常见的不良反应为困倦、打嗝、便秘、头痛、厌食以及肝指数谷丙转氨酶值升高等,此外还包括恶心、脱发及腹泻等。
[0007]
目前有一些报导基于lc-ms/ms检测阿瑞匹坦的方法,但是检测时间长,前处理相较于本专利复杂,不适合大批量检测样品的需求,因此,需要建立一个具有快速、准确、可靠,同时具有高灵敏度、高选择性的方法用于检测血浆中阿瑞匹坦浓度的方法。
技术实现要素:
[0008]
本发明的目的是提供一种液质联用测定血浆中阿瑞匹坦浓度的方法,解决上述现有技术问题中的一个或者多个。
[0009]
本发明提供的一种液质联用测定血浆中阿瑞匹坦浓度的方法,采用高效液相色谱-串联质谱检测预处理的血浆样品,利用内标法定量,检测样品中阿瑞匹坦和内标阿瑞匹坦-d4的色谱峰,进而得到所述血浆样品中的阿瑞匹坦浓度;
[0010]
其中:高效液相色谱的测试条件为:
[0011]
流动相a:h2o/fa=100/0.2(v/v);
[0012]
流动相b:acn/fa=100/0.2(v/v);
[0013]
洗液:meoh/h2o=50/50(v/v);
[0014]
采用梯度洗脱方式。
[0015]
在某些实施方案中,血浆样品预处理方法为:
[0016]
s1、以k2edta为抗凝剂,配制血浆样品后取100μl于96深孔板中;
[0017]
s2、添加5μl的1000ng/ml内标标准溶液至上述样品中并混匀;
[0018]
s3、添加1000μl acn于96深孔板中并涡旋混合1-5min后,于20℃下,进行离心操作;
[0019]
s4、转移1000μl上清液至装有1000μl acn/h2o/fa=55/45/0.2(v/v)的96深孔板中,涡旋混匀;
[0020]
s5、于20℃下,进行离心操作。
[0021]
其中:抗凝剂为:应用物理或化学方法,除掉或抑制血液中的某些凝血因子,阻止血液凝固的物质。能够阻止血液凝固的化学试剂或物质,称为抗凝剂或抗凝物质。
[0022]
在某些实施方案中,阿瑞匹坦标准溶液的配制方法为:称取阿瑞匹坦(分析物)5.032mg,加入meoh溶解至500000ng/ml,依次使用meoh/h2o=50/50(v/v)溶液稀释配制阿瑞匹坦标准溶液;
[0023]
阿瑞匹坦-d4内标标准溶液的配制方法为:精密称取阿瑞匹坦-d4(内标)1.107mg,加入meoh溶解至100000ng/ml,使用meoh/h2o(v/v)=50/50溶液稀释配制阿瑞匹坦标准溶液。
[0024]
在某些实施方案中,步骤s3中离心操作的离心转速为3000rpm,离心时间为10min;步骤s5中离心操作的离心转速为3000rpm,离心时间为5min。
[0025]
在某些实施方案中,高效液相色谱的测定条件为:
[0026]
色谱柱:agilent zorbax xdb-c18,5μm,柱规格为2.1
×
50mm;
[0027]
色谱柱温:40℃;
[0028]
进样温度:15℃;
[0029]
流速:0.4000ml/min;
[0030]
进样量:10μl;
[0031]
分析时间3min。
[0032]
在某些实施方案中,梯度洗脱的程序为:
[0033][0034][0035]
在某些实施方案中,质谱的测定包括阿瑞匹坦的测定和阿瑞匹坦-d4的测定;
[0036]
阿瑞匹坦的测定条件为:
[0037]
离子源采用电喷雾离子源,喷雾电压为5500v,雾化温度为500℃,喷雾气压力为30psi,辅助加热气压力为20psi,气帘气压力为30psi,碰撞气压力为8,去簇电压分别为30ev的阿瑞匹坦;碰撞室入口电压分别为8ev的阿瑞匹坦;碰撞电压分别为30ev的阿瑞匹坦;碰撞室出口电压分别为8ev的阿瑞匹坦;正离子方式检测;扫描方式为多重反应检测;
[0038]
阿瑞匹坦用于定量分析的离子对为:m/z535.1
→
m/z277.2;
[0039]
阿瑞匹坦-d4的测定条件为:
[0040]
离子源采用电喷雾离子源,喷雾电压为5500v,雾化温度为500℃,喷雾气压力为30psi,辅助加热气压力为20psi,气帘气压力为30psi,碰撞气压力为8,去簇电压分别为30ev的阿瑞匹坦;碰撞室入口电压分别为8ev的阿瑞匹坦-d4;碰撞电压分别为30ev的阿瑞匹坦-d4;碰撞室出口电压分别为8ev的阿瑞匹坦-d4;正离子方式检测;扫描方式为多重反应检测;
[0041]
阿瑞匹坦-d4用于定量分析的离子对为:m/z539.2
→
m/z281.3。
[0042]
在某些实施方案中,采用内标法,以阿瑞匹坦与内标阿瑞匹担-d4的峰面积比值代入标准曲线方程计算所述血浆样品中的阿瑞匹担的浓度。
[0043]
在某些实施方案中,所述标准曲线方程的建立包括以下步骤:
[0044]
取190μl空白血浆9份置于1.5ml离心管中,以储备液的形式添加10μl浓度分别为200ng/ml、400ng/ml、1000ng/ml、4000ng/ml、16000ng/ml、30000ng/ml、50000ng/ml、80000ng/ml、600ng/ml的阿瑞匹坦溶液至标样1、标样2、标样3、标样4、标样5、标样6、标样7、标样8、sst中;分别取标样1、标样2、标样3、标样4、标样5、标样6、标样7、标样8、sst、零浓度样品100μl于96深孔板中;然后添加5μl的1ng/μl内标标准溶液至样品中(db及残留样品加入5μl的meoh/h2o=50/50溶液)并混匀;添加1000μl acn于96深孔板中并涡旋混合1分钟。于20℃,3000rpm离心10分钟;然后转移30μl上清液至装有1000μl acn/h2o/fa=55/45/0.2
的96深孔板中,涡旋混匀;最后于20℃,3000rpm离心5分钟后作为测试样品待检测。
[0045]
在某些实施方案中,分别取10μl标准样品注入高效液相色谱-串联质谱仪中,检测样品中阿瑞匹坦及阿瑞匹坦-d4的色谱峰,并据此得到标准曲线,以用于计算所述血浆中的阿瑞匹坦的浓度。
[0046]
有益效果:与现有技术相比,本发明具有以下优点:
[0047]
(1)预处理方法简便,适用于常规测定;
[0048]
(2)专属性强:在本实验所采用的色谱条件下,阿瑞匹坦保留时间为1.051min左右,内标阿瑞匹坦-d4保留时间为1.040min左右;阿瑞匹坦及阿瑞匹坦-d4的峰型良好,无杂峰干扰测定,基线平稳;
[0049]
(3)灵敏度高:血浆最低定量限为10.0ng/ml,能准确测定血浆中阿瑞匹坦的浓度,灵敏度高,特异性强;
[0050]
(4)本发明方法快速、准确、灵敏度高、操作简便,为阿瑞匹坦的血药浓度测定提供依据;本方法的血浆标准曲线线性范围为10.0-4000ng/ml,批内和批间精密度rsd均在15.0%之内;本发明方法检测时间短归因于使用了分离更好、柱效更高的色谱柱,以及更合适的洗脱梯度。
[0051]
(5)该方法可以准确,快速测定人血浆中阿瑞匹坦的浓度,不仅可以用于仿制药一致性评价,加快进口药品国产替代的速度,降低患者的治疗成本,提高药品质量。
附图说明
[0052]
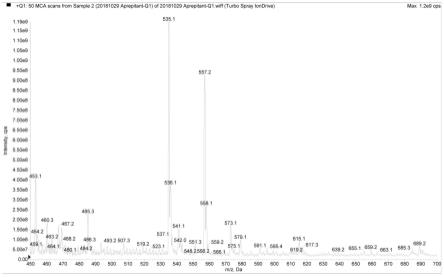
图1为分析物阿瑞匹坦和内标阿瑞匹坦-d4离子扫描图(a分析物阿瑞匹坦q1扫描图,b分析物阿瑞匹坦q3扫描图,c内标阿瑞匹坦-d4 q1扫描图,d内标阿瑞匹坦-d4 q3扫描图);
[0053]
图2为hplc-ms/ms法测得的阿瑞匹坦在人血浆中的标准曲线;
[0054]
图3为人空白血浆的hplc-ms/ms图;
[0055]
图4为人空白血浆加入阿瑞匹坦的hplc-ms/ms图。
具体实施方式
[0056]
下面通过实施方式对本发明进行进一步详细的说明。
[0057]
实施例1实验材料与分析设备
[0058]
阿瑞匹坦(分析物):u.s.pharmacopeial convention
[0059]
阿瑞匹坦-d4(内标):toronto research chemicals
[0060]
使用试剂见下表1:
[0061]
表1试剂明细
[0062]
试剂名称级别制造商乙腈(acn)hplcj.t.baker醋酸铵(ch3coonh4)hplcj.t.baker甲醇(meoh)hplcj.t.baker抗坏血酸(vc)acssigma-aldrich盐酸(hcl)argreagent
[0063]
注:亦可使用相同级别或更高级别的试剂
[0064]
使用分析设备见下表2:
[0065]
表2使用设备明细
[0066]
组件种类制造商binary pump(二元泵)ad pumpshimadzudegasser(脱气器)degassershimadzucolumn oven(恒温柱箱)ad column ovenshimadzuautosampler(自动取样器)ac autosamplershimadzusample rack(样品架)rack changershimadzumass spectrometer(质谱仪)triple quad 6500+sciexdata processor(数据处理器)analyst(software)sciex
[0067]
注:相同的lc-ms/ms系统亦可被使用。
[0068]
实施例2液相条件
[0069]
1、液相色谱条件:
[0070]
色谱柱:agilent zorbax xdb-c18,5μm,柱规格为2.1
×
50mm;色谱柱温:40℃;流动相a:h2o/fa=100/0.2(v/v);流动相b:acn/fa=100/0.2(v/v);洗液:meoh/h2o=50/50(v/v);自动进样器温度为15℃;梯度洗脱,流速为0.4000ml/min,进样量为10μl,分析时间为3.00min;
[0071]
表3梯度洗脱程序
[0072]
总时间(min)流速(ml/min)流动相a(%)流动相b(%)0.000.400045.055.00.600.400045.055.00.610.400020.080.01.200.400020.080.01.210.400045.055.03.000.400045.055.0
[0073]
2、质谱条件
[0074]
阿瑞匹坦条件为:
[0075]
离子源采用电喷雾离子源,喷雾电压为5500v,雾化温度为500℃,喷雾气压力为30psi,辅助加热气压力为20psi,气帘气压力为30psi,碰撞气压力为8,去簇电压分别为30ev的阿瑞匹坦;碰撞室入口电压分别为8ev的阿瑞匹坦;碰撞电压分别为30ev的阿瑞匹坦;碰撞室出口电压分别为8ev的阿瑞匹坦;正离子方式检测;扫描方式为多重反应检测;
[0076]
阿瑞匹坦用于定量分析的离子对为:m/z535.1
→
m/z277.2;
[0077]
阿瑞匹坦-d4条件为:
[0078]
离子源采用电喷雾离子源,喷雾电压为5500v,雾化温度为500℃,喷雾气压力为30psi,辅助加热气压力为20psi,气帘气压力为30psi,碰撞气压力为8,去簇电压分别为30ev的阿瑞匹坦;碰撞室入口电压分别为8ev的阿瑞匹坦-d4;碰撞电压分别为30ev的阿瑞匹坦-d4;碰撞室出口电压分别为8ev的阿瑞匹坦-d4;正离子方式检测;扫描方式为多重反应检测;阿瑞匹坦-d4用于定量分析的离子对为:m/z539.2
→
m/z281.3。
[0079]
实施例3试验过程
[0080]
1、阿瑞匹坦标准溶液的配制
[0081]
阿瑞匹坦标准溶液的配制:精密称取阿瑞匹坦(分析物)5.032mg,加入meoh溶解至500000ng/ml,依次使用meoh/h2o=50/50(v/v)溶液稀释配制阿瑞匹坦标准溶液,具体稀释浓度见下表4:
[0082]
表4阿瑞匹坦标准溶液配制浓度
[0083][0084][0085]
a:直接从阿瑞匹坦制备而成
[0086]
b:分析物的稀释溶液:meoh/h2o=50/50(v/v)
[0087]
阿瑞匹坦标准溶液不使用时储存于棕色玻璃容器及冰箱(-20℃)保存,体积可视需要依比例增加或减少。
[0088]
2、阿瑞匹坦-d4内标标准溶液的配制
[0089]
阿瑞匹坦-d4内标标准溶液的配制:精密称取阿瑞匹坦-d4(内标)1.107mg,加入meoh溶解至100000ng/ml,使用meoh/h2o=50/50(v/v)溶液稀释配制阿瑞匹坦标准溶液,具体稀释浓度见下表5:
[0090]
表5阿瑞匹坦-d4标准溶液配制浓度
[0091]
来源溶液(ng/ml)来源溶液体积(μl)最终体积(ml)最终浓度(ng/μl)100000b4001001000c[0092]
b:直接从阿瑞匹坦-d4(内标)制备而成
[0093]
c:用于样品制备步骤
[0094]
3、线性试验
[0095]
将空白血浆于室温环境放入水浴解冻;转移190μl的空白血浆10份至96深孔板中
(每一个标准曲线样品、db样品及空白样品),依下表6所列,分别精密加入不同浓度的阿瑞匹坦标准溶液10μl或稀释溶液配制每一个样品并混匀,配成不同浓度的含药血浆,按“血浆样品预处理”操作。以峰面积比y对血药浓度x作回归计算,结果见图2和表7及表8。以y对血药浓度x做回归计算,得回归方程y=0.0165x-0.00423,相关系数(r)为0.9993,拟合度(r2)为0.9986。权重系数w=1/x2,按该方法测得的阿瑞匹坦的血药浓度的最低定量限为:10.0ng/ml。
[0096]
表6阿瑞匹坦标准曲线配制浓度
[0097][0098]
a:分析物的稀释溶液:meoh/h2o=50/50
[0099]
表7hplc-ms/ms法测得的阿瑞匹坦在人血浆中的标准曲线(n=14)
[0100]
[0101][0102]
表8:标准曲线的回算浓度
[0103][0104]
a:超出接受标准,不纳入计算。
[0105]
4、准确度和精密度
[0106]
将空白血浆于室温环境解冻;转移190μl的空白血浆至适当的容器并添加阿瑞匹坦标准溶液制备5种不同浓度的含药血浆质控样品(lloq qc、lqc、gmqc、mqc、hqc)及一条随行标准曲线,按“血浆样品预处理”操作,质控样品制备如下表7所示。每天做一批及一条随行标准曲线,连续做3天,共3批,第一批、第二批分别做6份样品,第三批做16个样品,计算阿瑞匹坦和内标阿瑞匹坦-d4的峰面积比,代入当天的标准曲线中求得实测浓度,由实测浓度计算批内与批间精密度,实测浓度与理论浓度的比值即为准确度,结果见表10。阿瑞匹坦血浆样品批间、批内精密度、准确度在15.0%以内符合要求。
[0107]
表9质控样品配制浓度
[0108][0109]
依每一分析批所需,分装足够的体积至已标示的样品瓶中并储存于理论温度-20℃。体积可视需要依比例增加或减少。
[0110]
表10hplc-ms/ms法测定血浆中阿瑞匹坦的批内、批间精度和准确度
[0111]
[0112]
[0113][0114]
5、干扰性
[0115]
使用6个不同来源(每个来源一个)的空白血浆样品和3个不同来源(每个来源1个)的空白溶血血浆样品,将9个不同来源的空白血浆样品于同一分析批依样品制备步骤制备及分析,来评价不同空白血浆对阿瑞匹坦分析物及内标阿瑞匹坦-d4的干扰。
[0116]
9个不同来源的空白血浆样品制备分析后,在符合阿瑞匹坦保留时间处的干扰峰响应均低于该分析批的标准曲线中定量下限样品的阿瑞匹坦响应的20.0%,结果见表11。结果表明该分析方法对阿瑞匹坦的分析具有专属性。
[0117]
9个不同来源空白血浆样品制备分析后,在符合内标保留时间处的干扰峰响应均低于该分析批的标准曲线中定量下限样品的内标响应的5.0%,结果见表12。结果表明该分析方法对内标的分析具有选择性。
[0118]
表11 9个不同来源空白血浆对阿瑞匹坦分析物的干扰性数据对比表
[0119][0120][0121]
表12 9个不同来源空白血浆对内标的干扰性数据对比表
[0122][0123]
从表11和表12中可以看出,不同人体的空白血浆对阿瑞匹坦和内标阿瑞匹坦-d4的检测结果没有造成干扰。因此,该方法可以用于检测不同人体血浆中的阿瑞匹坦浓度。
[0124]
6、回收率
[0125]
将使用混合血浆配制的lqc、mqc和hqc来计算分析物的回收率。对于lqc、mqc和hqc的各3个平行样品和9个db进行提取。db提取后加入分析物和内标,使它们在提取后加入的db提取物中的浓度与提取的lqc、mqc和hqc样品相同。通过比较来自于qc的分析物和内标的峰面积与db提取后加入的分析物和内标的平均峰面积来计算提取回收率。从表13中可以看出,在分析物的每个浓度水平,分析物峰面积的%cv和总体%cv均在15.0%以内,回收率为89.7%,表明使用该前处理方法阿瑞匹坦的提取回收率高。从表14中可以看出,内标的全部提取样品的响应值%cv和全部未提取样品的响应值%cv均在15.0%以内,内标的平均提取回收率为95.1%。表明使用该前处理方法阿瑞匹坦-d4的提取回收率高。
[0126]
表13阿瑞匹坦分析物的提取回收率
[0127][0128]
表14内标的提取回收率
[0129]
[0130][0131]
7、基质效应
[0132]
7.1空白基质效应
[0133]
处理来自至少6个不同来源的空白基质样品。在提取db后加入分析物,确保它们在处理后db中的浓度(每个浓度每个来源1个样品)与处理后的lqc、mqc和hqc样品浓度相同;准备包含分析物的溶液,使最终浓度与处理后的lqc、mqc和hqc样品浓度相同,每个浓度6个平行,结果见表15,分析物峰面积比%cv均在15.0%以内,表明不存在空白基质效应问题。
[0134]
表15阿瑞匹坦分析物的空白基质效应
[0135][0136][0137]
7.2溶血基质效应
[0138]
为考察溶血基质中的基质效应,配制一份在溶血基质中lqc、mqc和hqc,每个浓度6个平行,结果见表16,分析物峰面积比%cv均在15.0%以内,表明不存在溶血基质效应问题。
[0139]
表16阿瑞匹坦分析物的溶血基质效应
[0140][0141]
7.3高脂基质效应
[0142]
为考察高脂基质中的基质效应,配制一份在高脂基质中lqc、mqc和hqc,每个浓度5个平行,结果见表17,分析物峰面积比%cv均在15.0%以内,表明不存在高脂基质效应问题。
[0143]
表17阿瑞匹坦分析物的高脂基质效应
[0144]
[0145][0146]
综上所述:本发明提供了一种预处理方法简便的血浆中阿瑞匹坦浓度的测定方法,采用蛋白质沉淀法,通过有机试剂沉淀蛋白,从样品中提取分析物。适用于常规测定;同时,在本实验所采用的色谱条件下,阿瑞匹坦保留时间为1.051min左右,内标阿瑞匹坦-d4保留时间为1.040min左右。阿瑞匹坦及阿瑞匹坦-d4的峰型良好,无杂峰干扰测定,基线平稳;本方法具有较高的特异性,能准确测定血浆中阿瑞匹坦的浓度,灵敏度较高,血浆最低定量限为10.0ng/ml;同时,本发明方法快速、准确、灵敏度高、操作简便,为阿瑞匹坦的血药浓度测定提供依据。本方法的血浆标准曲线线性范围10.0-4000ng/ml,批内和批间精密度rsd在
±
15.0%以内,分析物提取回收率高且不存在基质效应。
[0147]
以上表述仅为本发明的优选方式,应当指出,对本领域的普通技术人员来说,在不脱离本发明创造构思的前提下,还可以做出若干变形和改进,这些也应视为发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1