一种基于量子点标记的过敏原特异性IgE检测方法和用途与流程
本发明涉及过敏原特异性ige快速检测方法和用途,具体地说,本发明涉及一种基于量子点标记的过敏原特异性ige检测方法和用途。
背景技术:
1、过敏性疾病是临床常见病。据who统计,全球约22%人群受到过敏性疾病的干扰,且发病人数呈逐年上升趋势,给社会带来了沉重的经济负担。过敏原特异性ige是过敏主要的致病分子之一。当过敏原第一次进入机体,可导致机体形成过敏原特异性ige,后者与效应细胞嗜碱性粒细胞和肥大细胞表面的ige高亲和力受体fcεri结合,此为致敏过程;当过敏原再次进入机体,其可与效应细胞表面的特异性ige结合,导致相邻的fcεri交联,引起效应细胞激活。激活的效应细胞立刻释放胞浆内预先合成的颗粒,颗粒富含的释放炎症介质、细胞因子和趋化因子等,导致毛细血管扩张、血管通透性增加、平滑肌收缩、腺体分泌增加的活性因子,引起局部或全身过敏反应症状,包括过敏性鼻炎、哮喘、结膜炎、湿疹、食物过敏、药物过敏等。
2、目前临床上对于过敏性疾病的诊断,除了病史、体格检查外,实验室检查是重要辅助诊断手段。常用的实验室检查包括体内激发试验和体外过敏原特异性ige检测(sige)以及血清总ige检测。体内试验虽然准确性较高,但存在诱发严重过敏反应的风险、多种抗原过敏时的交叉反应结果难以判断,而且检测时患者尤其是儿童比较痛苦。体外试验中总ige水平受多种因素影响,特异性较低。目前,过敏原sige检测是过敏性疾病诊断应用最广泛的检测手段。临床常用的检测方法有荧光酶标法(unicap系统)和免疫印迹法(allergyscreen),这些检测法多为国外进口产品、试剂成本高,检测种类有限,操作步骤繁杂,耗时长。
3、与传统的临床实验室免疫诊断相比,近年来发展起来的免疫层析技术具有快速、高效、成本低、标本用量少等特点。胶体免疫层析技术是研究最早也是目前应用最广的快速免疫诊断方法。虽然具有检测结果肉眼可见、无需特殊检测设备等优点,但该方法检测灵敏度不够高,多为定性或半定量检测结果,无法满足疾病诊断中超微量检测的需求。随着纳米技术的不断发展,许多新型的纳米材料被不断制备,应用于免疫分析,给研发新一代诊断试剂盒带来了新的机遇。
4、量子点(qds),也称半导体纳米晶,作为一种新型荧光纳米粒子,具有:荧光尺寸效应、发射峰狭窄对称、激发波长范围广、量子产率高、荧光寿命长、化学和光稳定性好等特点。近年来量子点作为探针在快速免疫诊断领域有较多的研究报道。2008年,lin等首次报道以量子点为探针,采用免疫层析技术,结合荧光定量仪,实现对前列腺癌特异性抗原的快速、定量检测。所建立的量子点免疫层析检测方法具有灵敏度高(检测低限达0.02ng/ml)和重复性好(r.s.d.小于7%)的优点,检测时间仅需10分钟,与elisa检测方法的相关性好。随后,国内外学者也将该检测技术成功地应用于毒素小分子、血清甲胎蛋白、总ige快速定量检测。建立基于量子点标记的过敏原特异性ige免疫层析检测技术,可能实现对过敏性疾病的快速、准确、便捷的诊断。
5、然而,本领域目前的过敏原特异性ige检测技术无法在快速便捷诊断的同时保证较宽的检测范围。
6、因此,本领域需要开发一种检测范围更宽的量子点标记的过敏原特异性ige免疫层析检测技术。
技术实现思路
1、本发明的目的是提供基于量子点标记的过敏原特异性ige检测抗体偶联物、试剂盒及其用途。
2、本发明的目的之二是,提供基于量子点标记的过敏原特异性ige检测的方法。
3、在本发明的第一方面,提供了一种制备用于检测过敏原特异性ige的抗体偶联物的方法,所述方法包括步骤:
4、(s1)提供量子点微球和待标记的抗人ige抗体;和
5、(s2)将所述抗人ige抗体与量子点微球偶联,从而得到所述的抗体偶联物;
6、其中,所述的步骤(s2)中包括:
7、步骤(i)稀释所述待标记的抗人ige抗体至0.1-10mg/ml,从而得到稀释的抗体;
8、步骤(ii)在所述稀释的抗体中加入活化试剂,从而得到活化抗体,其中所述的活化试剂与所述抗体的摩尔比为1-100:1;和
9、步骤(iii)将所述量子点微球与步骤(ii)得到的活化抗体混合反应,以得到反应混合物,其中,所述活化抗体与量子点微球的摩尔比为0.1-10:1。
10、在另一优选例中,步骤(i)中待标记的抗人ige抗体优选地稀释至1-5mg/ml;进一步优选地稀释至2mg/ml。
11、在另一优选例中,步骤(ii)中所述的活化试剂与所述抗体的优选摩尔比为10-50:1;更优选地为20:1。
12、在另一优选例中,步骤(iii)中所述活化抗体与量子点微球的优选摩尔比为1-5:1;更优选地为2.7:1。
13、在另一优选例中,所述的步骤(iii)中,所述反应的温度优选为37℃,和/或所述反应的时间优选为12-24小时,更优选为14-20小时,进一步优选为16小时。
14、在另一优选例中,所述的步骤(s2)中包括步骤(iv)加入封闭液对所述反应混合物进行封闭反应,从而得到封闭的反应混合物,所述封闭反应温度优选为37℃,和/或所述封闭反应的时间优选为4小时。
15、在另一优选例中,所述的步骤(s2)中包括步骤(v)对所述反应混合物进行离心去除未标记的抗体,从而得到所述的抗体偶联物。
16、在另一优选例中,所述离心中,离心力优选为4000-12000g,更优选为6000-10000g,进一步优选为8000g;和/或离心时间为5-30分钟,优选为10-25分钟,进一步优选为20分钟。
17、在另一优选例中,所述的方法偶联效率>40%。
18、在另一优选例中,所述的抗人ige抗体选自羊抗人ige抗体。
19、在另一优选例中,所述方法制备得到的偶联物粒径为50-150nm,优选地为100-150nm,更优选地为140-150nm。
20、在另一优选例中,所述方法制备得到的偶联物zeta电位为-28~-15mv,优选地为为-25~-18mv,更优选地为为-22~-19mv。
21、在另一优选例中,所述方法制备得到的偶联物多分散指数pdi值为<0.5,优选地为<0.3,更优选地为<0.2。
22、在本发明的第二方面,提供了一种用于检测过敏原特异性ige的抗体偶联物,所述抗体偶联物为量子点微球和抗人ige抗体的偶联物,并且所述的抗体偶联物由如本发明第一方面所述的方法制备得到。
23、在另一优选例中,所述的偶联物粒径为50-150nm,优选地为100-150nm,更优选地为140-150nm。
24、在另一优选例中,所述的偶联物zeta电位为-28~-15mv,优选地为为-25~-18mv,更优选地为为-22~-19mv。
25、在另一优选例中,所述的偶联物多分散指数pdi值为<0.5,优选地为<0.3,更优选地为<0.2。
26、在本发明的第三方面,提供了一种检测过敏原特异性ige的试剂盒,所述试剂盒包括:
27、(a)如本发明第二方面所述的偶联物;
28、(b)试剂条,所述试剂条包括:底板、样品垫、结合垫、硝酸纤维素膜和吸水垫;
29、其中,所述硝酸纤维素膜上设置有检测线,所述检测线包被有过敏原。
30、在另一优选例中,所述包被的过敏原浓度为0.1-5mg/ml,优选地为0.5-1mg/ml。
31、在另一优选例中,所述的过敏原包括过敏原粗提物、天然提取的过敏原组分和重组过敏原组分。
32、在另一优选例中,所述的过敏原选自下组:户尘螨、粉尘螨、德国小蠊、艾蒿、烟曲霉、狗毛屑、猫皮屑、虾、小麦、花生、蟹、虾、鸡蛋、牛奶、芝麻、大豆、普通豚草、艾蒿、藜、苍耳、及其组分、及其组合。
33、在另一优选例中,若样本中存在过敏原特异性ige,过敏原特异性ige可与本发明第二方面所述的偶联物形成“抗体偶联物-过敏原特异性ige”复合物;所述检测线上的过敏原能够与所述“过敏原特异性ige-抗体偶联物”复合物再次结合形成“过敏原-过敏原特异性ige-抗体偶联物”三聚物。
34、在另一优选例中,所述的硝酸纤维素膜上,在检测线远端还设置有质控线,所述质控线包被有抗-抗人ige抗体的第二抗体,所述第二抗体能够与本发明第二方面所述的偶联物形成“抗体偶联物-第二抗体”复合物。
35、在另一优选例中,所述的第二抗体为兔抗羊igg抗体。
36、在另一优选例中,所述包被的抗体浓度为1mg/ml。
37、在另一优选例中,所述的试剂条的组装方法包括步骤:
38、(s1)将过敏原和第二抗体喷涂至硝酸纤维素膜上,分别作为检测线与质控线;
39、(s2)将喷涂后的硝酸纤维素膜干燥;
40、(s3)样品垫、喷涂后的硝酸纤维素膜、吸水垫依次连接组装;
41、(s4)用样本垫处理液浸润样本,取出后干燥。
42、在另一优选例中,所述的试剂条的组装方法包括步骤:
43、(s1)将0.5-1mg/ml过敏原蛋白和1mg/ml兔抗羊igg喷涂至硝酸纤维素膜上,分别作为检测线与质控线;
44、(s2)将喷涂后的硝酸纤维素膜37℃干燥16h;
45、(s3)样品垫、喷涂后的硝酸纤维素膜、吸水垫依次连接组装;
46、(s4)用样本垫处理液浸润样本30min,取出后37℃干燥24h。
47、在另一优选例中,所述的样本垫处理液为含1.0%bsa、0.5%tween-20ph8.4的0.1m磷酸盐缓冲液。
48、在另一优选例中,所述的检测为半定量检测。
49、在另一优选例中,所述的试剂盒包含说明书,所述说明书记载有使用试剂盒进行检测的方法,所述方法包括如下步骤:
50、(1)提供来自检测对象的待测样本;
51、(2)将待测样本、如本发明第二方面所述的偶联物和稀释液混合制备混合液;
52、(3)将所述混合液滴加在样本垫上;
53、(4)读取检测线值(t)和质控线值(c),计算比值(即t/c);
54、(5)根据t/c比值,参照标准曲线计算得到所述待测样本中的过敏原特异性ige浓度。
55、在另一优选例中,所述的样本优选为血清。
56、在另一优选例中,所述的待测样本、偶联物和稀释液的体积比为按体积比10-100:1-5:10-50。
57、在另一优选例中,所述的待测样本-稀释液-偶联物比例为30:2:20。
58、在另一优选例中,所述的说明书中记载有标准曲线的制作方法,其包括步骤:
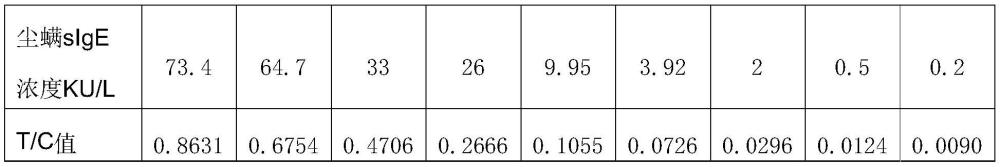
59、(1)提供已知浓度的过敏原特异性ige阳性血清作为标准品,和过敏原特异性ige阴性对象混合血清作为稀释血清,利用稀释血清将标准品稀释至梯度浓度;
60、(2)将稀释的标准品、如本发明第二方面所述的偶联物和稀释液按体积比30:2:20混合制备混合液;
61、(3)将所述混合液滴加在样本垫上;
62、(4)读取检测线值(t)和质控线值(c),计算比值(即t/c);
63、(5)以t/c比值为横坐标,过敏原特异性ige为纵坐标,制作标准曲线。
64、在另一优选例中,所述的说明书记载有标准曲线。
65、在另一优选例中,所述的稀释液含有:磷酸盐缓冲液(pbs)、0.1%tween20,2%bsa和3%蔗糖。
66、在另一优选例中,所述的试剂盒的检测范围为0.1-100ku/l,优选为0.2-80ku/l,更优选地为0.2-73.4ku/l。
67、在本发明的第四方面,提供了一种如本发明第二方面所述的偶联物的用途,用于制备试剂盒,所述试剂盒用于:
68、(a)检测样本中的过敏原特异性ige;和/或
69、(b)诊断过敏性疾病。
70、在另一优选例中,所述的过敏性疾病选自下组:过敏性哮喘、鼻炎、皮炎、或其组合。
71、在另一优选例中,所述的过敏原选自下组:户尘螨、粉尘螨、德国小蠊、艾蒿、烟曲霉、狗毛屑、猫皮屑、虾、小麦、花生、蟹、虾、鸡蛋、牛奶、芝麻、大豆、普通豚草、艾蒿、藜、苍耳、及其组分、及其组合。
72、在本发明的第五方面,提供了一种过敏原特异性ige检测方法,所述方法包括如下步骤:
73、(1)提供来自检测对象的待测样本;
74、(2)将待测样本、如本发明第二方面所述的偶联物和稀释液混合制备混合液;
75、(3)将所述混合液滴加在样本垫上;
76、(4)读取检测线值(t)和质控线值(c),计算比值(即t/c);
77、(5)根据t/c比值,参照标准曲线计算得到所述待测样本中的过敏原特异性ige浓度。
78、在另一优选例中,所述的过敏原选自下组:户尘螨、粉尘螨、德国小蠊、艾蒿、烟曲霉、狗毛屑、猫皮屑、虾、小麦、花生、蟹、虾、鸡蛋、牛奶、芝麻、大豆、普通豚草、艾蒿、藜、苍耳、及其组分、及其组合。
79、在另一优选例中,所述的检测方法使用如本发明第三方面所述的试剂盒进行检测。
80、在另一优选例中,所述的检测为半定量检测。
81、在另一优选例中,所述的方法为体外非诊断性检测方法。
82、应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
- 还没有人留言评论。精彩留言会获得点赞!